5 minute read
Angina Pectoris
Thomas F. Lüscher, Robert Manka , Felix Tanner und Oliver Gämperli
Klinische Präsentation
Advertisement
Die drei Charakteristika der Angina pectoris: 7 Retrosternaler Thoraxschmerz mit charakteristischer Qualität («druckartig», «würgend», «Enge») und Dauer (ca. 10 Min.), klassische Schmerzlokalisation und Ausstrahlung (Abb 1). 7 Getriggert durch körperliche Belastung oder emotionalen
Stress, verstärkt bei Kälte. 7 Rückläufig nach Ausruhen und/oder Einnahme von Nitraten (innerhalb von Minuten) • Typische Angina pectoris: erfüllt alle drei der folgenden
Kriterien. • Atypische Angina pectoris: erfüllt zwei der oben genannten
Kriterien. • Nichtanginöse Thoraxschmerzen: erfüllt keine oder nur eins der oben genannten Kriterien.
Angina pectoris und angiographisches Substrat
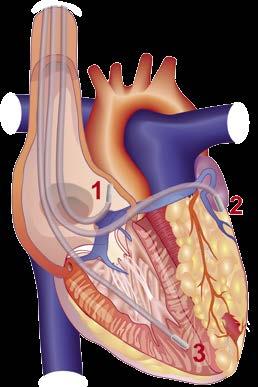
Abbildung 1: Links: Klassische Schmerzlokalisationen und Schmerzausstrahlung bei Angina pectoris Rechts: Zugrunde liegend koronare Veränderung mit Stenosis in Ramus interventricularis anterior
Step 1
Bestimmung der VortestWahrscheinlichkeit
Step 2
Wahl des besten Tests (nichtunvasiv oder invasiv) zur KHKDiagnose
Step 3
Risikostratifizierung im Hinblick auf Therapie
Abb. 2: Stufenschema zum Vorgehen bei Verdacht auf Angina pectoris
7 STEP 1: Entscheidend ist zunächst die klinische Beurteilung:
Ist es Angina pectoris? Sind die Beschwerden typisch? → Abschätzen der VortestWahrscheinlichkeit (Tabelle 1). 7 STEP 2: Danach ist abzuschätzen, ob der Patient weiter für eine koronare Herzkrankheit (KHK) abgeklärt werden soll, und falls ja, welcher KHKTest (Abbildung 3 und Tabelle 2+3): • FahrradErgometrie: Reproduzierbarkeit der Symptome,
BDAbfall bei Hauptstamstenose • Myokardszintigraphie/PositronenEmissionsTomographie:
Ischämiediagnostik • Stressechokardiographie: Wandbewegungsstörungen als
Ischämieäquivalent • PerfusionsMRI: Ischämiediagnostik (cave: Klaustrophobie,
Schrittmacher und ICD) • CTKoronarangiographie: Koronarstenosen und Verkalkungen, hoher negativ prädikiver Wert 7 STEP 3: Bei nachgewiesener KHK, Risikostratifizierung zum
Entscheid bzgl. Therapie (medikamentöskonservativ versus
Revaskularisation (mittels PCI [Percutaneous Coronary Intervention] oder ACBP [BypassOperation]) (s. Therapie bei
Angina pectoris).
Tabelle 1: Wahrscheinlichkeit für eine koronare Herzkrankheit aufgrund Anamnese und Belastungstest
Typische Angina Atypische Angina Nichtanginöse Thoraxbeschwerden Alter Männer Frauen Männer Frauen Männer Frauen 30–39 59.1 27.5 28.9 9.6 17.7 5.3 40–49 68.9 36.7 38.4 14.0 24.8 8.0 50–59 77.3 47.1 48.9 20.0 33.6 11.7 60–69 83.9 57.7 59.4 27.7 43.7 16.9 70–79 88.9 67.7 69.2 37.0 54.4 23.8 ≥80 92.5 76.3 77.5 47.4 64.6 32.3
Wahrscheinlichkeit für eine koronare Herzkrankheit aufgrund Anamnese, Geschlecht und Alter. Angegeben ist der Prozentsatz an Patienten mit signifikanten Koronarstenosen bei der Koronarangiographie (Genders TS, et al. Eur Heart J 2011;32:1316)
Auswahl des diagnostischen KHK Tests
Verdacht auf KHK
VTW <15% VTW 1585%
Patienten-Charakteristika/-Eignung? Lokale Verfügbarkeit und Expertise?
Bei unklaren Resultaten evt. 2. Test (Hybridbildgebung) oder direkt invasive Koro VTW >85%
VTW 15–50% CT-Koro VTW 15–65% Stress-EKG, falls verfügbar mit Imaging (SPECT, MRI, PET, Echo) VTW 30–65% Stress imaging (SPECT, MRI, PET, Echo)
KHK NEIN KHK JA
Alternative Diagnose? Risikostratifizierung und Therapie
Abbildung 3: Abkürzungen: VTW = Vortest-Wahrscheinlichkeit; KHK = Koronare Herzkrankheit; SPECT = Myokard-Szintigraphie; PET = Myokard-Positron-Emissions-Tomographie; CMR = Herz-Kernspintomographie; Echo = Stress-Echokardiographie
Tabelle 2: Möglichkeiten nicht-invasiver Bildgebungstests bei KHK
StressEcho Szintigraphie/ PET Computertomographie (CT) Magnetresonanz Imaging (MRI)
Struktur ++ + Klappen +++ Auswurffraktion ++ + Koronarien (+) Perfusion ++
Infarkt/Viabilität + + + (In Entwicklung) In Entwicklung +++ (late enhancement)
Tabelle 3: Welcher KHK-Test bei welchem Patienten?
Technik Vorteile Stress-EKG • Grösste Verfügbarkeit • Billig, einfaches Equipment Stress-Echo • Gute Verfügbarkeit • Tragbar • Keine Strahlen • Vergleichbar geringe Kosten SPECT • Gute Verfügbarkeit • Viele diagnostische und prognostische Daten PET • Flussquantifizierung • Viabilität Nachteile • Eingeschränkte diagnostische Treffsicherheit (v.a. tiefe Sensitivität) • Schlechte Schallfenster bei
Adipositas und Emphysem • Qualität abhängig von Operater
Skills • Strahlenbeslastung (5–10 mSv)
• Strahlenbeslastung (2–4 mSv) • Beschränkte Verfügbarkeit • Hohe Kosten MRI • Darstellung von Narbe/Fibrose • Kontraindikationen (Platzangst, • Ischämie und Viabilität Metalsplitter, alte Herzschrittmacher/ • Keine Strahlen Sonden) • Eingeschränkte Bildqualität bei Arrhythmie CT-Koro • Hoher negativer Prädiktivwert • Strahlenbelastung (1–2 mSv) • Eigeschränkte Bildqualität bei Verkalkungen, Stents, Arrhythmie, oder hoher Herzfrequenz >70/min
Die Therapie bei stabiler KHK richtet sich nach dem kardiovaskulären Gesamtrisiko: 7 Revaskularisation bei hohem Risiko (z.B. relevante myokardiale
Ischämie, eingeschränkte Auswurffraktion, Diabetes mellitus, eingeschränkte Leistungsfähigkeit, Angina pectoris bei leichter
Aktivität): perkutane koronarintervention (PCI) oder aortokoronare Bypassoperation (ACBP) 7 medikamentös-konservative Therapie bei niedrigem Risiko
Medikamente bei Angina Pectoris und Myokardischämie
Medikament Mechanismus Aspirin Thrombozytenhemmung Betablocker MVO2-Senkung Ca2+-Antagonisten2 Vasodilatation (Senkung Herzfrequenz)
ACE-Hemmer Vasodilatation Symptome Prognose – ++ ++ +1
++ Verapamil (bei Hypertonie und normaler LVEF) - ++ Ivabradin Herzfrequenzsenkung ++ ++ Molsidomin Preloadsenkung, Vasodilation ++ Fraglich Nicorandil Vasodilatation ++ ++ Nitrate Preloadsenkung, Vasodilatation ++ Fraglich (Toleranz)
Ranolazine Myokardstoffwechsel Hämodynamisch neutral
Statine LDL-Senkung
1 Betablocker wurden bei koronarer Herzkrankheit vor Einführung der Thrombolyse und
PCI untersucht; damals wurde der plötzliche Herztod und Re-Infarkt reduziert. Heute ist die prognostische Wirkung unklar. Nebivolol hat allerdings bei Patienten mit Herzinsuffizienz (siehe Kapitel «Chronische Herzinsuffizienz», Seite 184) im SENIORS Trial bei Patienten mit Herzinsuffizienz eine protektive Wirkung gezeigt (Primary Outcome:
Composite of all cause mortality or cardiovascular hospital admission; Eur Heart J. 2005
Feb;26(3):215–25). 2 Verapamil (2×80–160 mg/Tag) und Diltiazem (2×90 mg)senken die Herzfrequenz,
Dihydropyridine (Nifedipin CR 60–90 mg/Tag, Amlodipine 2.5–10 mg/Tag, Lercanidipin 10–20 mg/Tag) nicht. Verapamil verbessert nach Infarkt bei erhaltener LV Funktion (LVEF) die Prognose, Nifedipin und Amlodipine nur bei gleichzeitiger Hypertonie.
Vorgehen bei angiographisch nachgewiesener koronarer Herzkrankheit (mit nachgewiesener Ischämie oder FFR<=0.801)
Befund ACBP2 PCI3 Nur Medikamente4
Hauptstamm +++ +++ bei geeignete Anatomie 3-Asterkrankung +++ ++ geeignete Anatomie, KI: Diabetes 2-Asterkrankung ++ +++ 1-Asterkrankung6 + +++ + (diffuse Veränderungen, distaler Befall) – (nur in Ausnahmefällen5) – (nur in Ausnahmefällen5)
1 FFR = fractional flow reserve 2 ACBP = Aorto-Coronare Bypass Chirurgie 3 PCI = Perkutane Coronare Intervention (Ballon, Stent) 4 Medikamente wie Aspirin, Statine und ACE-Hemmer erhalten alle Patienten; hier geht es um antiischämische Therapie und Verbesserung der Prognose. 5 Die Courage-Studie hat zwar eine prognostische Gleichwertigkeit von PCI und Medikamenten ergeben, allerdings wurden <5% der Patienten in den beteiligten Zentren eingeschlossen und kaum das Ausmass der Ischämie bestimmt. Die Resultate entsprechen daher nicht der gegenwärtigen Praxis. Eine Metaanalyse kommt zum Schluss, dass eine
PCI mit second generation Drug-eluting Stents wahrscheinlich prognostisch einen Vorteil gegenüber Medikamenten alleine bietet (Brit. Med. J. 2014; 348: g3859). 6 Die kürzlich erschiene ORBITA-Studie mit weniger als 200 Patienten schloss, dass die
PCI einer medikamentösen Therapie der Angina pectoris nicht übelegen sei (Lancet 2018; 39: 31–40). Eine genaue Analyse zeigte jedoch, dass die Studie deutlich «underpowered» war und dass in der Tat die mit einer PCI versorgten Patienten eine bessere (wenn auch nicht signifikante) Belastungsfähigkeit zeigten und dass objektiv die Stressechokardiographie eine signifikante Verbesserung der linksventrikulären Funktion unter
Belastung ergab (Chaitman et al. Eur. Heart J. 2018; 2018; 39: 963–965).