Lesen Sie mehr auf seltenekrankheiten.de & gesunder-koerper.info


Lesen Sie mehr auf seltenekrankheiten.de & gesunder-koerper.info

„MAN WILL NICHT STÄNDIG
MIT ANGEZOGENER HANDBREMSE
LEBEN.“
Alexander Heise lebt mit einer seltenen Blutgerinnungsstörung. Im Interview spricht er mit uns über seinen Alltag und gibt wertvolle Tipps für den Umgang mit Hämophilie.
Polycythaemia Vera Der Weg bis zur Diagnose der seltenen Blutkrankheit war für Ilona Beyer lang. Wie man ihrer Erkrankung auf die Spur kam, teilt sie mit uns im Interview. 06
09
Sichelzellkrankheit Eine Gentherapie bietet neue und vielversprechende Behandlungsmöglichkeiten.
VERANTWORTLICH FÜR DEN INHALT DIESER AUSGABE JUNI 2025

Gulaim Steinrötter Wir möchten informieren, sensibilisieren und Mut machen. Tauchen Sie gemeinsam mit uns ein in die stille, faszinierende Welt des Blutes und entdecken Sie, welche Folgen es haben kann, wenn es aus dem Gleichgewicht gerät.
Bluthochdruck
Die unterschätzte Gefahr
Industry Development Managerin Healthcare: Gulaim Steinrötter Geschäftsführung: Johan Janing (CEO), Henriette Schröder (Managing Director), Philipp Colaço (Director Business Development), Lea Hartmann (Head of Design), Cover: Privat Mediaplanet-Kontakt: de.redaktion@mediaplanet.com
Alle Artikel, die mit “In Zusammenarbeit mit“ gekennzeichnet sind, sind keine neutrale Redaktion der Mediaplanet Verlag Deutschland GmbH. Aus Gründen der besseren Lesbarkeit wird auf die gleichzeitige Verwendung der Sprachformen männlich, weiblich und divers (m/w/d) verzichtet. Alle Personenbezeichnungengelten gleichermaßen für alle Geschlechter.
Etwa vier bis sechs Liter Blut fließen unaufhörlich durch unseren gesamten Körper, durch Adern, Kapillaren und Arterien. Es versorgt lebenswichtige Organe mit Sauerstoff, transportiert Nährstoffe, wehrt Krankheitserreger ab und ist maßgeblich an der Wundheilung beteiligt. Ein wahres Wunderwerk – solange alles reibungslos funktioniert. Doch was geschieht, wenn dieses ausgeklügelte System aus dem Gleichgewicht gerät?
Anlässlich des heutigen Welt-Sichelzell-Tags widmen wir diese Publikation den seltenen Bluterkrankungen. Diese sind kaum bekannt – auch die Betroffenen hören meist zum ersten Mal von ihnen, wenn die Diagnose gestellt wird.
Aufgrund dieser Seltenheit werden die Patienten manchmal selbst zu Experten ihrer Erkrankung: Sie informieren sich über neue Therapiemöglichkeiten, tauschen sich in Patientenverbänden aus und begegnen ihrem Arzt auf Augenhöhe. Genau diese starken Persönlichkeiten kommen in dieser Publikation zu Wort und erzählen offen über ihre Ängste und Hoffnungen. Dazu gehört auch Melanie Vanden-Brande. Sie hat den Austausch mit anderen Betroffenen der Paroxysmalen Nächtlichen Hämoglobinurie (PNH) als sehr wertvoll empfunden und eine Stiftung zur Bekämpfung dieser Erkrankung gegründet, bei der das Immunsystem die eigenen roten Blutkörperchen (oft unbemerkt) zerstört. Im Interview mit Alexander Heise werden Mythen rund um die Hämophilie, eine seltene Blutgerinnungsstörung, die auch

als „Bluterkrankheit“ bekannt ist, aufgeräumt. Gleichzeitig verrät er uns, wie wichtig Sport für die Gelenke ist, welche Sportarten er empfiehlt und von welchen er abrät. Weniger im öffentlichen Bewusstsein sind die myeloproliferativen Neoplasien (MPN) verankert. Dabei handelt es sich um eine Gruppe seltener, chronischer Erkrankungen der blutbildenden Zellen im Knochenmark, zu denen unter anderem die Polycythaemia Vera gehört.
Medizinischer Fortschritt, der sich den Herausforderungen der Zeit stellt und dabei die Lebensqualität der Betroffenen nicht aus den Augen verliert, ist wichtig.
Wie langwierig der Weg zur Diagnose sein kann, weshalb
Dieser Artikel ist in Zusammenarbeit mit der Vertex Pharmaceuticals (Deutschland) GmbH entstanden.
Selten, aber schwerwiegend: Die Sichelzellkrankheit beeinträchtigt das Leben der Betroffenen immens. Die Blutkrankheit gehört in Deutschland zu den sogenannten seltenen Erkrankungen. Wer an Sichelzellkrankheit leidet, hat mit starken Schmerzen und Organschäden zu kämpfen, zudem ist die Lebenserwartung verkürzt.
Text Dr. Christian Bruer
Die Sichelzellkrankheit ist genetisch bedingt –also angeboren – und begleitet die Betroffenen ein Leben lang. Der Name rührt daher, dass die Blutzellen sich unter bestimmten Umständen zu „Sicheln“ verformen. Ursache der Erkrankung ist eine Mutation in einem Gen, das für die Bildung des roten Blutfarbstoffs, des Hämoglobins, verantwortlich ist. Die Erkrankung beeinträchtigt das gesamte Leben der Betroffenen und ihrer Familien. Ein normaler Alltag oder eine geregelte Arbeit sind oft nicht möglich. Sichelzellkrankheit und Schmerzkrisen Rote Blutzellen sind dafür verantwortlich, Sauerstoff zu den Organen zu transportieren. Bei gesunden Menschen sehen diese aus wie runde, flache Scheiben. Bei der Sichelzellkrankheit (Sickle Cell Disease, kurz SCD) nehmen sie jedoch die Form von Sicheln an, sobald sie den Sauerstoff abgegeben haben. Diese Sichelzellen sind nicht mehr elastisch, und aufgrund ihrer Form können kleine Blutgefäße verstopfen. Dadurch kann das Blut schlecht fließen und lebenswichtige Organe werden nicht richtig versorgt. Die Folgen sind sehr starke Schmerzen, die überall im Körper auftreten können. Wer solch eine Schmerzkrise erleidet, muss schnell mit starken Schmerzmitteln behandelt werden – oftmals im Krankenhaus.
Herausforderungen eines Lebens mit Sichelzellkrankheit
Die Sichelzellkrankheit kann zu Komplikationen führen, wie dem lebensbedrohlichen akuten Thoraxsyndrom.
Dabei verstopfen rote Blutzellen die Blutgefäße der Lunge, was zu Atembeschwerden, Husten und starken Schmerzen führt. Weitere mögliche Folgeerscheinungen der SCD sind Schlaganfall, Lungenentzündung sowie Schäden am Herzen – bis hin zu Herzversagen. Die chronische Belastung durch die schwere Blutkrankheit führt bei vielen Betroffenen zu psychischen Beschwerden.
Sichelzellen sind nicht mehr elastisch, und aufgrund ihrer Form können kleine Blutgefäße verstopfen. Dadurch kann das Blut schlecht fließen und lebenswichtige Organe werden nicht richtig versorgt.
Bedarf an neuen Therapien Für solch schwere, seltene Erkrankungen wie SCD ist Forschung besonders wichtig, um den Betroffenen innovative Therapien zur Verfügung stellen zu können. Ziel ist dabei, nicht nur die Symptome zu behandeln, sondern Therapiemöglichkeiten anzubieten, die an der Ursache der Erkrankung ansetzen und diese dauerhaft heilen können.
das eigene Bauchgefühl nicht vernachlässigt werden sollte und dass eine Therapieumstellung nach Absprache mit dem Arzt auch wieder mehr Lebensqualität bedeuten kann, veranschaulicht Ilona Beyer in ihrem sehr ermutigenden Interview.
Medizinischer Fortschritt, der sich den Herausforderungen der Zeit stellt und dabei die Lebensqualität der Betroffenen nicht aus den Augen verliert, ist wichtig. Vor allem bei den seltenen, genetischen Bluterkrankungen hat die Gentherapie in den letzten Jahren einen Durchbruch erzielt. Dank ihr können Patienten mit Hämophilie A und B (über einen gewissen Zeitraum) komplett auf die herkömmliche, regelmäßige Infusion verzichten.
Prof. Roland Meisel erklärt uns am Beispiel der kürzlich zugelassenen Gentherapie für die transfusionsabhängige Beta-Thalassämie und die Sichelzellkrankheit, das Wirkprinzip von Gentherapien und weshalb sie sich besonders gut für erbliche Bluterkrankungen eignen.

„Realtalk!“:
Website mit hilfreichen Informationen
Auf unserer Website findest Du wertvolle Infos und praktische Tipps zu:
Ernährung und Bewegung Mentale Gesundheit Familienplanung Community und Austausch
Außerdem stehen Dir im Ressourcen Hub hilfreiche Materialien zum Download zur Verfügung! www.vrtx.com

Als Thrombosen bezeichnet man Blutgerinnsel, die die Venen verstopfen und sich durch ein geschwollenes, schmerzhaftes Bein äußern. Löst sich ein Gerinnsel und wandert mit dem Blutstrom in die Lungengefäße, entsteht eine Lungenembolie. Nicht jede Lungenembolie wird überlebt, daher ist schnelles Handeln wichtig.
Text Dr. Katja S. Mühlberg
Thrombosen entstehen aus verschiedenen Gründen: Immobilität, z. B. nach Beinbruch oder Operation, ist ein typischer Risikofaktor. Durch fehlende Bewegung stagniert der Blutfluss, das Blut gerinnt. Damit das nicht passiert, werden in solchen Situationen blutverdünnende Medikamente vorbeugend verabreicht, sodass Betroffene gut geschützt sind. Auch das rasche Wiederaufstehen und Laufen nach einer OP ist deshalb so wichtig. Kompressionsstrümpfe wirken dabei unterstützend. Liegt im Blut ein Ungleichgewicht von Gerinnungsfaktoren vor, kann auch dies die Blutgerinnung aktivieren. Solche Thrombophilien sind überwiegend angeboren und manchmal über mehrere Generationen in Familien nachweisbar. Menschen, in deren Familien eine Thromboseneigung besteht, können über einen Bluttest mit genetischer Analyse eine Thrombophilietestung vornehmen lassen. Dies sollte jedoch nie ohne konkreten Anlass erfolgen, da bei weitem nicht jede Thrombophilie gefährlich ist und zwangsläufig zu Thrombosen führt. Eine fachärztliche Beratung ist daher vor derartigen Tests Pflicht.
Thrombose ist keine Frage des Alters!
Dr. Katja S. Mühlberg
Fachärztin für Innere Medizin & Angiologie am Universitätsklinikum Leipzig und wissenschaftliche Leiterin des Aktionsbündnisses Thrombose, Deutsche Gesellschaft für Angiologie – Gesellschaft für Gefäßmedizin e.V.
östrogenhaltige Pillenpräparate sind häufige Trigger einer Thrombose. Bei der Wahl der Verhütung sollten daher stets eine familiäre Thromboseneigung erfragt werden und im Zweifel östrogenfreie Präparate oder hormonfreie Alternativen gewählt werden. Bei Kombinationspillen (Östrogen + Gestagen) sollten Pillen der ersten und zweiten Generation bevorzugt werden, da diese im Vergleich zu Pillen der dritten und vierten Generation niedrigere Thromboseraten aufweisen.
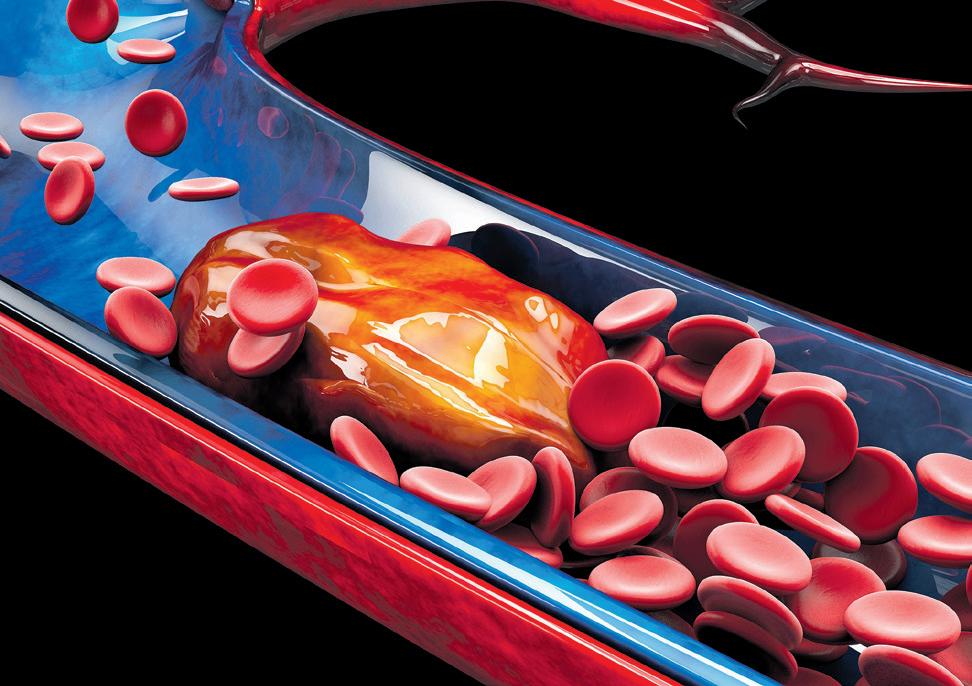
Lungenembolien werden rasch und sicher im CT (Computertomographie) diagnostiziert, können aber auch mittels Lungenszintigraphie und Herzultraschall unter Einbeziehung von Laborwerten erkannt werden. Behandelt werden sowohl Thrombosen als auch Lungenembolien mit Blutverdünnern, die mindestens drei bis sechs Monate, manchmal auch lebenslang, eingenommen werden müssen.

Verletzungen oder Schäden an der Venenwand, z. B. durch frühere Thrombosen oder auch Druck von außen auf die Gefäße können ebenfalls das Entstehen einer Thrombose begünstigen. Letzteres kann z. B. in der Schwangerschaft oder bei Tumoren vorkommen. Verschiedene anatomische Besonderheiten, aber auch Übergewicht und chronisch-entzündliche Erkrankungen können die Gerinnselbildung forcieren. Die Schwangerschaft selbst, die Zeit nach der Entbindung (Wochenbett), aber auch
Tumorerkrankungen gehen oft mit Thrombosen einher, weswegen Betroffene sorgfältig geschult werden sollten, damit die typischen Symptome rasch erkannt und behandelt werden können. Umgekehrt sind Thrombosen manchmal der erste Hinweis auf das Vorhandensein eines bis dato noch unbekannten Tumorleidens. Deshalb sollten alle Thrombosepatienten, bei denen keiner der genannten Risikofaktoren oder Trigger eruiert werden konnte, unbedingt auf das Vorliegen eines okkulten, also unbekannten Tumors untersucht werden. In der Regel genügen hierzu Blutanalysen, ein Röntgen des Brustkorbs, ein Bauchultraschall, eine Magen-/ Darmspiegelung sowie die Wahrnehmung der gynäkologischen bzw. urologischen und dermatologischen Vorsorgeuntersuchungen. Bei 15 Prozent aller Thrombosepatienten wird auf diese Weise ein bösartiger Tumor gefunden, der ohne dieses Screening vielleicht nicht mehr rechtzeitig behandelt worden wäre. Das Spektrum an Risikofaktoren und Triggern ist groß, aber überschaubar und anhand einer gewissenhaften Anamnese gut zu erfassen. Häufig treten mehrere Faktoren gemeinsam auf, in ca. 20 Prozent aller Thrombosen läßt sich jedoch keine Ursache finden. Bei Auftreten einer plötzlichen einseitigen Schwellung des Beins, egal ob mit oder ohne Schmerzen, sollte unverzüglich eine Thrombose mittels Gefäßultraschall ausgeschlossen werden. Plötzliche Luftnot, Herzrasen, aber auch eine kurze Bewusstlosigkeit (Synkope) oder Bluthusten sind typische Hinweise auf eine Lungenembolie und müssen sofort abgeklärt werden.
KOMPRESSIONSSOCKEN FÜR SPÜRBARE UNTERSTÜTZUNG BEI JEDEM SCHRITT
STOX Energy Socks verbindet medizinisches Know-how mit Funktionalität und Style – für mehr Komfort, bessere Regeneration und gezielte Unterstützung im Alltag, beim Reisen und beim Sport.
STOX Energy Socks mit Sitz in Amsterdam wurde 2015 gegründet und hat sich innerhalb kurzer Zeit als einer der führenden Hersteller im Bereich funktioneller Kompressionssocken in Europa etabliert. Was im medizinischen Bereich seinen Ursprung fand, entwickelte sich über die Jahre schnell zu einer erfolgreichen Performance-Brand im Lifestyleund Sportsegment. Neben Kompressionssocken im medizinischen Bereich, bietet das niederländische Unternehmen auch Recovery- und Kompressionssocken für Unterstützung beim Reisen sowie den Alltag an, die Schwellungen reduzieren und für einen produktiveren und bequemeren Tag sorgen. Zudem gehören Sportartspezifische Kompressionssocken zur wissenschaftlich bewiesenen körperlichen Leistungssteigerung beim Laufen, Wandern, Skifahren und ab Sommer 2025 auch fürs Fahrradfahren zum Produktportfolio der Marke.
Vorteile von Kompressionssocken für den Alltag, Reisen & Sport Kompression übt gezielten Druck auf Beine und Füße aus, wobei der Druck am Knöchel am stärksten ist und nach oben hin abnimmt. Dadurch wird die Blutzirkulation optimiert und die Muskeln besser mit Nährstoffen versorgt. Das beugt Muskelermüdung vor und ermöglicht dadurch eine Leistungssteigerung. Gleichzeitig unterstützt Kompression eine schnellere Erholung. Die Kompressionssocken von STOX Energy Socks sind alle mit der abgestuften Kompression der Klasse 2 (23-32 mmHg) ausgestattet, die eine mittlere bis starke Kompression bietet und damit sowohl ideal ist für den Einsatz im Alltag als auch für Hobbysportler:innen oder Athlet:innen, die von leistungssteigernder und schützender Kompression beim Wandern, Laufen oder Skifahren profitieren möchten. Das nahtlose Design der STOX Energy Socks sorgt zudem für eine faltenfreie, enganliegende Passform, die Druckstellen verhindert und maximalen Komfort bietet.
Qualität auf höchstem Niveau
Die Socken von STOX Energy Socks werden in Italien auf hochmodernen Rundstrickmaschinen gefertigt. Das Ergebnis ist ein passgenauer Halt um die Muskeln herum, der die Blutzirkulation steigert und Ermüdung und Verletzungen vorbeugt. Für noch mehr Leistung und Komfort verwendet STOX Energy Socks hochwertige Materialien wie Dryarn®, Merinowolle, Deocell® und Lycra®.
Genauso wichtig ist das Tragen von Kompressionsstrümpfen. Dabei sind Kniestrümpfe fast immer ausreichend. Wer die Kompression versäumt, läuft Gefahr, dass sich ein postthrombotisches Syndrom entwickelt. Dieses kann sich durch eine für immer fortbestehende Beinschwellung und schlimmstenfalls durch offene Beine (Geschwüre) äußern und tritt manchmal erst Jahre nach der Thrombose auf. Leiden Lungenemboliepatienten trotz sechs-monatiger Behandlung weiter an Luftnot, müssen weitere Untersuchungen einen chronischen Lungenhochdruck als Folgeerkrankung ausschließen. Grundsätzlich sind Bewegung und ein aktiver Lebensstil erlaubt und erwünscht. In einzelnen Fällen können sowohl Lungenembolien als auch Thrombosen minimalinvasiv mittels Kathetertechnik entfernt werden.
Das Aktionsbündnis Thrombose bietet auf seiner Homepage wertvolle Hinweise für Patientinnen und Patienten mit einem Online-Risiko-Check.
www.risiko-thrombose.de

Text Charlie Schröder
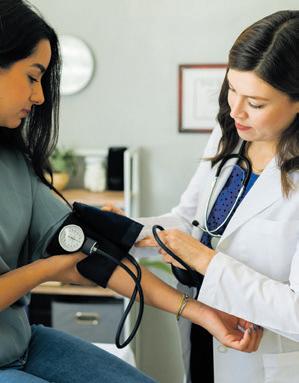
Bluthochdruck (Hypertonie) zählt zu den häufigsten Volkskrankheiten in Deutschland –und bleibt oft lange unbemerkt, da anfangs meist keine Beschwerden damit einhergehen, was sie besonders tückisch macht. Etwa jeder dritte Erwachsene ist betroffen, das sind rund 20 bis 25 Millionen Menschen in Deutschland. Unbehandelt kann Bluthochdruck zu schweren Folgeerkrankungen wie Herzinfarkt, Schlaganfall oder Nierenschäden führen. Umso wichtiger ist es, frühzeitig gegenzusteuern. Regelmäßiges Blutdruckmessen, gesunde Lebensweise und das Wissen um Warnzeichen können Leben retten.
Die Deutsche Herzstiftung sowie kardiologische Fachgesellschaften empfehlen allen Erwachsenen – entsprechend den aktuellen Leitlinien der Europäischen Gesellschaft für Kardiologie (ESC) – bei jedem Arztbesuch eine Blutdruckmessung durchführen zu lassen. Darüber hinaus gelten bestimmte Zeitintervalle für regelmäßige Blutdruckkontrollen: Bei Erwachsenen unter 40 Jahren sollte der Blutdruck mindestens alle drei Jahre überprüft werden, während ab dem 40. Lebensjahr eine jährliche Kontrolle empfohlen wird. Ziel ist es, dass der systolische Blutdruck idealerweise im Bereich von 120 bis 129 mmHg liegt. Optimalwerte für Erwachsene bewegen sich um 120/70 mmHg. Werden bei einer Messung erhöhte Werte festgestellt, ohne dass weitere Risikofaktoren (wie z. B. Übergewicht, Bewegungsmangel, Tabakkonsum oder eine familiäre Vorbelastung) vorliegen, die eine sofortige Behandlung erforderlich machen, sollte eine Langzeitblutdruckmessung erfolgen. Anschließend ist eine Nachkontrolle innerhalb eines Jahres vorgesehen, um den Blutdruck gezielt einzustellen. Zusätzlich kann es sinnvoll sein, eine sogenannte Messwoche pro Monat einzuplanen. Dabei messen Betroffene an sieben aufeinanderfolgenden Tagen jeweils morgens und abends ihren Blutdruck. Der Durchschnittswert aller Messungen dieser Woche gibt einen guten Überblick über den Blutdruckverlauf.
Ein gesunder Lebensstil trägt wesentlich zur Vorbeugung von Bluthochdruck bei. Dazu gehört eine ausgewogene Ernährung mit wenig Salz sowie einem hohen Anteil an
Obst und Gemüse. Ebenso wichtig ist regelmäßige körperliche Bewegung, idealerweise mindestens 150 Minuten pro Woche. Auch der bewusste Umgang mit Stress spielt eine große Rolle. Darüber hinaus ist es ratsam, auf Nikotin vollständig zu verzichten und den Alkoholkonsum möglichst gering zu halten.
Ein Blutdruckwert von über 140/90 mmHg wird als Bluthochdruck eingestuft. Kritisch wird es bei Werten über 180/110 mmHg – in diesem Fall spricht man von einer hypertensiven Krise, die ärztlich abgeklärt werden muss. Besonders alarmierend ist ein solcher Blutdruckanstieg, wenn gleichzeitig Symptome wie starke Kopfschmerzen, Schwindel, Sehstörungen, Brustschmerzen, Atemnot oder Verwirrtheit auftreten. In solchen Fällen sollte unverzüglich ärztliche Hilfe in Anspruch genommen oder der Notruf unter 112 verständigt werden, da ein medizinischer Notfall vorliegen kann.
Bei Erwachsenen unter 40 Jahren sollte der Blutdruck mindestens alle drei Jahre überprüft werden, während ab dem 40. Lebensjahr eine jährliche Kontrolle empfohlen wird.
Neben der Umstellung des Lebensstils können auch Medikamente notwendig sein – etwa ACE-Hemmer, Beta-Blocker oder Diuretika. Die Therapie wird individuell vom Arzt angepasst. Wichtig ist: Medikamente regelmäßig einzunehmen und nicht eigenständig abzusetzen. Auch pflanzliche Mittel (z. B. mit Knoblauch oder Hibiskus) können unterstützend wirken, ersetzen aber keine ärztliche Behandlung. Bei Übergewicht hilft oft schon eine moderate Gewichtsabnahme, um den Blutdruck deutlich zu senken.

Richtiger Zeitpunkt
Der Blutdruck sollte idealerweise morgens vor dem Frühstück und vor der Einnahme von Medikamenten sowie abends gemessen werden – möglichst immer zur gleichen Tageszeit, um vergleichbare Werte zu erhalten.
Körperliche Ruhe
Vor jeder Messung sollte man mindestens fünf Minuten ruhig sitzen und körperliche Anstrengung, Stress oder Aufregung vermeiden. Auch Kaffee, Nikotin oder Alkohol sollten in der Stunde vor der Messung nicht konsumiert werden.
Korrekte Körperhaltung
Während der Messung sollte man bequem sitzen, mit geradem Rücken und beiden Füßen flach auf dem Boden. Der Messarm (meist der linke) sollte locker auf Herzhöhe gelagert sein, z. B. auf dem Tisch.
Richtige Anwendung des Blutdruckmessgeräts
Die Manschette muss korrekt angelegt werden – nicht zu locker und nicht über der Kleidung. Bei Oberarmgeräten sollte die Manschette etwa zwei Finger breit oberhalb der Ellenbeuge sitzen. Bei Handgelenkgeräten ist es besonders wichtig, dass das Gerät während der Messung auf Herzhöhe gehalten wird.
Durchschnittswert bilden Es ist empfehlenswert, jeweils zwei Messungen im Abstand von ein bis zwei Minuten durchzuführen und den Durchschnittswert zu notieren. Einzelwerte können durch Stress oder Bewegungen verfälscht sein. Für eine noch bessere Aussagekraft kann eine sogenannte Messwoche durchgeführt werden, bei der täglich morgens und abends gemessen wird.
Schnell, präzise, komfortabel –smarte Blutdruckmessgeräte mit oder ohne App-Anbindung.
Jetzt 20% Rabatt auf die gesamte Blutdruck-Kategorie sichern!
Code: BLUTDRUCK20


Der Internist, Hämatologe und Onkologe Prof. Dr. med. Hermann Einsele war einer der Ersten in Deutschland, die die sogenannte CAR-T-Zelltherapie gegen Blutkrebs klinisch testeten. Hier erklärt der Klinikdirektor der Medizinischen Klinik II an der Uniklinik Würzburg, wie die Krebsimmuntherapie funktioniert und welches Potenzial sie birgt.
In den USA erhielt im Jahr 2012 erstmals weltweit ein Kind eine CAR-T-Zelltherapie. Die damals sechsjährige Emily Whitehead litt an akuter lymphatischer Leukämie, hatte 23 Monate Chemotherapie hinter sich und galt als austherapiert. 22 Tage nach der Behandlung war Emily krebsfrei und ist es bis heute.1
Mit dieser Beispielpatientin vor Augen und einem Mitarbeiter an der Seite, der die CAR-T-Zelltherapie in den USA mitentwickelt hatte, waren wir äußerst optimistisch.
Inzwischen sind deutschlandweit mehr als tausend Patientinnen und Patienten damit behandelt worden. Die Fakten sprechen für sich: Während sich normalerweise etwa 0,5 bis 1 Prozent der Immunzellen mit der Abwehr von Tumorzellen beschäftigen, sind es nach der CAR-T-Zelltherapie bis zu 95 Prozent. 25 bis 30 Prozent der von uns behandelten Patientinnen und Patienten mit einem Lymphknotenkrebs in weit fortgeschrittenem Stadium, für die es keine Therapie mehr gab, sind nach der einmaligen Infusion im Rahmen der CAR-T-Zelltherapie langfristig krebsfrei. Ein Teil der austherapierten Myelom-Betroffenen mit einer Aussicht auf nur noch vier bis fünf krankheitsfreie Monate ist nach einmaliger CAR-T-Zelltherapie fünf Jahre und länger krankheitsfrei. Wobei „krankheitsfrei“ für ein Leben in „gesunder Lebensqualität“ steht.
und Glioblastom sind in Vorbereitung. Zudem sind wir damit beschäftigt, die bislang überwiegend individuelle CAR-T-Zelltherapie universal zu machen. Derzeit entnimmt man einer Patientin oder einem Patienten T-Zellen, verändert sie genetisch und setzt ihr oder ihm diese wieder ein. Das Verändern dauert zwischen drei bis acht Wochen – eine Zeit, in der der Tumor in Schach gehalten werden muss.
Die Verwendung körpereigener T-Zellen mindert das Risiko, dass die CAR-T-Zellen später fälschlicherweise gesundes Gewebe angreifen oder vom Körper als feindlich angesehen und bekämpft werden (Autoimmunreaktion).
Forschungsziel ist es, auch CAR-T-Zellen, die von anderen Spendern generiert werden („fremd“), einzusetzen, die man vorrätig halten kann (sogenannte „Off-theShelf“-Lösung, auf Deutsch: „Aus-dem-Regal“-Lösung), um Zeit zu gewinnen: zum Behandeln und zum Leben.

Mit der CAR-T-Zelltherapie behandeln wir bislang erfolgreich Krebserkrankungen des blutbildenden Systems, zum Beispiel akute lymphatische Leukämien, Lymphknotenkrebs und multiple Myelome.
Prof. Dr. med. Hermann Einsele
Klinikdirektor Medizin II der Uniklinik Würzburg und Sprecher des Nationalen Centrums für Tumorerkrankungen NCT WERA
Herausforderungen der CAR-T-Zelltherapie Mit der CAR-T-Zelltherapie behandeln wir bislang erfolgreich Krebserkrankungen des blutbildenden Systems, zum Beispiel akute lymphatische Leukämien, Lymphknotenkrebs und multiple Myelome. Bei der Behandlung solider Tumore wie Brustkrebs, Nierenkrebs, Prostatakrebs und Lungenkrebs ist die große Herausforderung, die Krebszellen auf molekularer Ebene noch besser zu charakterisieren, sodass die spezifischen Oberflächenmarker von den CAR-T-Zellen noch zielsicherer erkannt und zerstört werden können. Zudem geht es hier darum, die CAR-T-Zellen in das Tumorgewebe einzuschleusen, wogegen sich diese wehren. In Würzburg werden mit neuen Konstrukten der CAR-TZellen Studien bei Patienten mit fortgeschrittenem Brustkrebs, Eierstockkrebs, Nierenzellkarzinom, Adenokortikalem Karzinom, Lungenkrebs durchgeführt und CAR-T-Zelltherapien bei Bauchspeicheldrüsenkrebs
5
Infusion der gentechnisch veränderten CAR-TZellen, die nun die Tumorzellen erkennen und bekämpfen können.
4
Bei jeder Zellteilung wird die neue, veränderte Erbinformation weitergegeben.
Fot o U n v e r s t ä t üWzr grub
Die Erfolge mit der CAR-T-Zelltherapie zeigen, dass Immuntherapien extrem wirken. Das rückte diese in den Fokus. Vielversprechend sind sie auch bei Autoimmunerkrankungen wie Lupus erythematodes, Myasthenia gravis, Multiple Sklerose und anderen Autoimmunerkrankungen, also Rheuma-ähnliche Erkrankungen, wo sie fehlgeleitete Immunzellen bekämpfen.
Auch bei Infektionserkrankungen wie Covid-Infektionen, Hepatitis-Infektionen und Pilzinfektionen kann die Immuntherapie zumindest im Modellsystem wirkungsvoll helfen. Sogar bei Herzerkrankungen laufen derzeit Untersuchungen CAR-T-Zellen einzusetzen, um die Gewebszerstörung im Herzmuskel zu reduzieren.
1 https://www.thedp.com/article/2024/03/enn-emily-whitehead-car-t-cell-therapy-carl-june
Eine Krebsgeschwulst (Tumor) entwickelt sich aus einer gesunden Körperzelle, deren Erbinformation beschädigt oder bei der Zellteilung fehlerhaft ausgelesen wird. Solche Erbgutfehler entstehen oft zufällig (Mutation). Sie verändern die Zellbiologie, sodass die Zelle unkontrolliert zu einem Tumor heranwächst.
Tückisch ist: Krebszellen können sich für die körpereigene Abwehr (Immunsystem) unsichtbar machen. Bei der CAR-T-Zelltherapie werden körpereigene Abwehrzellen (T-Zellen) genetisch so verändert, dass sie Tumorzellen erkennen und ausschalten – und das über viele Jahre hinweg.
Die CAR-T-Zelltherapie gegen Krebs
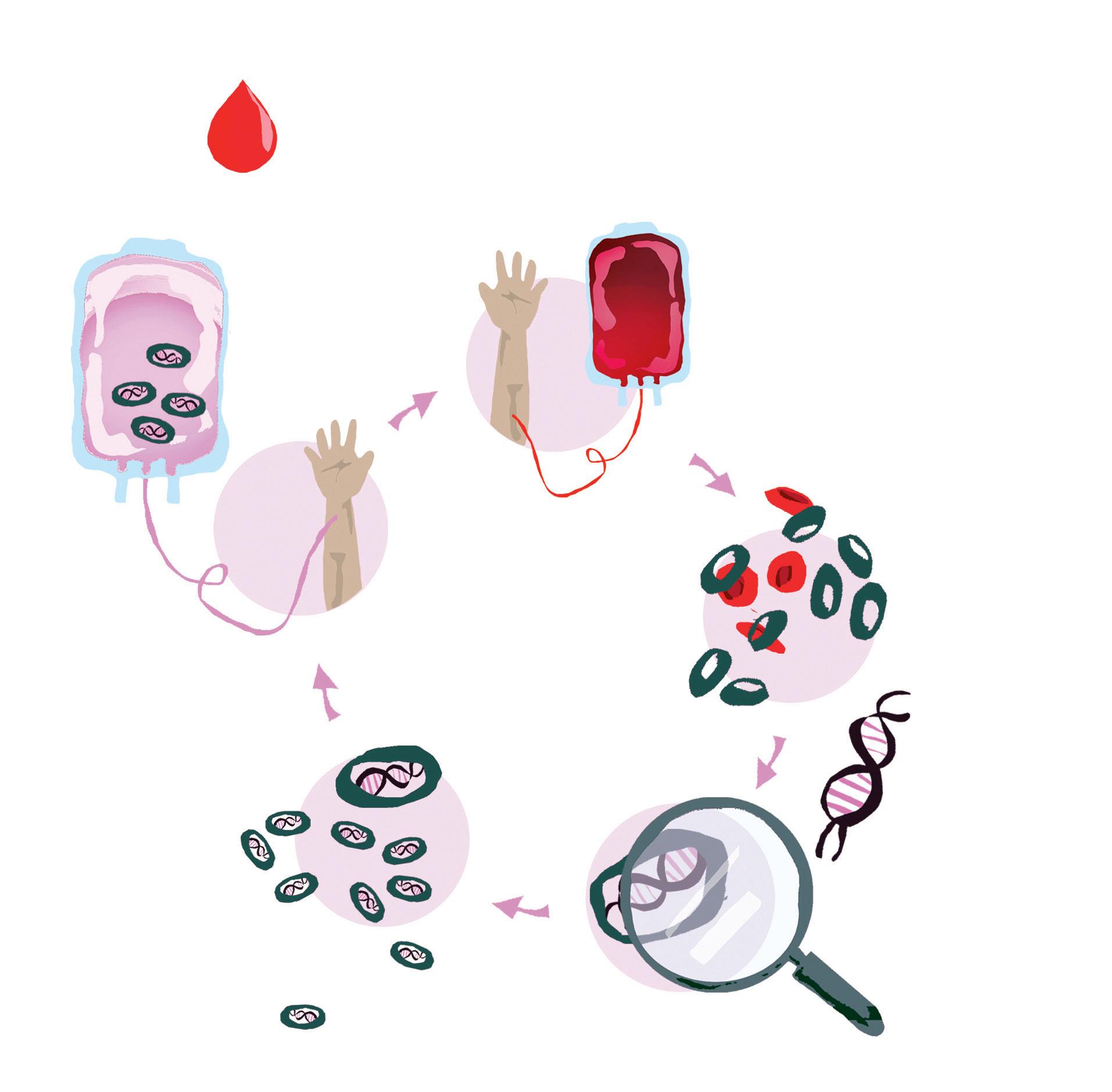
Herstellungsprozess
1
Patientinnen und Patienten werden weiße Blutkörperchen entnommen.
2
T-Zellen werden isoliert und aktiviert.
3
T-Zellen werden im Labor gentechnisch verändert; der Bauplan für den chimären Antigenrezeptor (chimeric antigen receptor, CAR) wird gezielt in die T-Zelle eingebracht und eingebaut.
„Ich lebe wieder ein ganz normales Leben und dafür bin ich sehr dankbar!“
Über lange Jahre blieb die seltene Bluterkrankung
Polycythaemia Vera (PV) bei Ilona Beyer unentdeckt, aber sie gab nicht auf. Wie man ihrer Erkrankung auf die Spur kam und wie sie heute damit lebt, erzählte sie uns im Interview.
Liebe Frau Beyer, wann haben Sie zum ersten Mal gemerkt, dass etwas nicht stimmt? Welche Symptome haben Sie aufhorchen lassen?
Zunächst hatte ich keine typischen PV-Symptome, aber ich hatte einen Bandscheibenvorfall und sollte operiert werden. Bei der Überprüfung der Blutwerte vorab waren die Thrombozyten zu hoch. Das war das erste Mal, dass ich hörte, dass meine Blutwerte nicht in Ordnung sind. Nicht lange darauf bekam ich Brustkrebs, den ich zum Glück besiegte. Nach der Behandlung wurde ich engmaschig überwacht, und es fiel immer wieder auf, dass die Thrombozyten zu hoch sind.
Es hat trotzdem noch Jahre gedauert, bis die Diagnose "Polycythaemia Vera" gestellt wurde – obwohl Ihr Hämatokritwert, der ein Anzeichen für PV sein kann, schon damals sehr hoch war. Können Sie uns sagen, woran es gelegen hat?
Meine Brustkrebs-Diagnose bekam ich 2006, meine PV-Diagnose tatsächlich erst 2013. Lange dachte man, dass der erhöhte Hämatokritwert mit meiner Krebsbehandlung zusammenhängen könnte, aber es wurde einfach nicht besser. Mein Gynäkologe, der mich auch nach meiner Krebsbehandlung intensiv betreute, überwies mich deswegen zu einem Leukämie-Spezialisten. Der sagte, dass ich nichts hätte, überwies mich aber zu einem Humangenetiker. Der wiederum verschrieb mir Blutverdünner, aber konnte auch nichts feststellen. Zurück bei meinem Hausarzt wurde mir bestätigt, dass meine Werte noch immer viel zu hoch wären und wir der Sache auf den Grund gehen müssten. Er überwies mich an einen Onkologen, der meine Blutprobe nach München schickte. Eine Woche später bekam ich meine Diagnose. Warum keiner die Puzzleteile früher richtig zusammengesetzt hat, frage ich mich bis heute.
Wie sah die anschließende Therapie aus? Waren Sie zuversichtlich?
Da ich mich direkt intensiv zur PV informierte, wusste ich: Es handelt sich um eine chronische Erkrankung, die man aber gut behandeln kann. Das gab mir Hoffnung, da die Symptome zu diesem Zeitpunkt sehr stark waren. Ich war bei Kleinigkeiten sofort auf 180, litt unter einer bleiernen Müdigkeit und meine Beine schmerzten. Meine Hände und mein Gesicht brannten und waren abends feuerrot.
Die Therapie bestand zunächst aus Aderlässen und der Gabe von Blutverdünnern; das verbesserte die Symptome deutlich. Aber die Wirkung hielt meist nicht lange an und es gab Nebenwirkungen, wie zum Beispiel einen permanenten Eisenmangel, der sich mit jedem Aderlass verstärkte. Müdigkeit wurde zu meinem ständigen Begleiter.

Von 2014 bis 2017 bekam ich daher ein weiteres Medikament, um diesen Kreislauf zu durchbrechen, aber litt dabei unter schlimmen Nebenwirkungen: Fatigue, Schmerzen, Magenprobleme, Nasenbluten. 2017 habe ich mit meinem behandelnden Arzt besprochen, dass es so für mich nicht weitergeht.
Man sollte nie locker lassen, wenn einem das eigene Bauchgefühl sagt, dass etwas nicht stimmt.
Was ist dann passiert?
Ich habe zu meinem Arzt eine sehr vertrauensvolle Beziehung auf Augenhöhe und habe ihm deutlich gesagt, dass ich keine Lebensqualität mehr habe. Er erzählte mir von anderen Behandlungsmöglichkeiten, wofür ich sehr offen war. Ich habe es nicht bereut, da sich meine Lebensqualität durch die Anpassung meiner Therapie enorm verbessert hat.
Wie geht es Ihnen denn heute?
Klar habe ich auch heute noch Tage, an denen es mir mal nicht so gut geht. Aber ich kann wieder alles machen, arbeite freiberuflich wieder als Eventmanagerin und kann mein Privatleben genießen. Ich kann mit meinen Enkelkindern aktiv Zeit verbringen und wir haben wieder einen Hund, der mich auf Trab hält.
Ich lebe wieder ein ganz normales Leben und dafür bin ich sehr dankbar! Die PV ist tatsächlich gerade meine kleinste Baustelle. Auch meine letzten Untersuchungswerte geben mir recht, denn da konnte man die PV kaum noch nachweisen. Daher behalten wir die Medikation weiter so bei, da ich damit wirklich gut fahre.
Was möchten Sie Betroffenen mit auf den Weg geben?
Man sollte nie locker lassen, wenn einem das eigene Bauchgefühl sagt, dass etwas nicht stimmt. Und wenn man sich ärztlich nicht gut aufgehoben fühlt oder keine zuverlässige Diagnose gestellt werden kann, sollte man sich nicht scheuen, zum nächsten Experten zu gehen oder sich an ein spezialisiertes Kompetenzzentrum zu wenden. Hat man die Diagnose erhalten, dann kann ich nur jedem raten, sich mit anderen Betroffenen auszutauschen und z. B. an Patientenveranstaltungen teilzunehmen, um so viel wie möglich über seine eigene Erkrankung zu lernen.
Was ist der Hämatokritwert?
Der Hämatokritwert gibt an, wieviel Prozent des Blutvolumens aus festen Bestandteilen besteht. Mit etwa 96 Prozent bestehen diese festen Bestandteile aus roten Blutkörperchen (Erythrozyten). Wenn der Flüssigkeitsanteil des Blutes sinkt, wird das Blut zu dick, zähflüssig und fließt in der Folge langsamer. Dadurch steigt der Hämatokritwert und mit ihm das Risiko für arterielle und venöse Thrombosen, Herzinfarkt und Schlaganfälle. Um dem entgegenzusteuern, sollte versucht werden, den Hämatokritwert unter 45 Prozent zu halten.
Ein zu hoher Wert kann auf Flüssigkeitsmangel oder Krankheiten wie Polycythaemia Vera hindeuten, ein zu niedriger auf Blut-verlust oder Anämie. Ein unauffälliger Hämatokritwert liegt bei Männern zwischen 42 und 50 Prozent, bei Frauen zwischen 37 und 45 Prozent.
Das forschende Pharmaunternehmen Novartis denkt Medizin neu, um besonders auch Menschen mit seltenen Erkrankungen mit innovativen Therapien und Informationsangeboten zu mehr Lebensqualität zu verhelfen.

Speziell für Menschen, die an einer Myeloproliferativen Neoplasie (MPN) wie der Myelofibrose, der Polycythaemia Vera oder der Chronischen Myeloischen Leukämie leiden, hat Novartis umfangreiche Informationsinitiativen ins Leben gerufen, die wissenschaftlich fundiertes Wissen zur Erkrankung und zum Umgang damit zur Verfügung stellen.
Symptome erkennen – und richtig in Zusammenhang bringen
Da die verschiedenen Symptome der MPN sehr vielschichtig sind und mit Fortschreiten der Erkrankung stärker werden können, sind fundierte Informationen zu den möglichen Beschwerden für Patient*innen und deren Angehörige sehr wichtig. Das macht das Beispiel der Polycythaemia Vera deutlich, denn Beschwerden wie chronische Müdigkeit, Schmerzen im linken Oberbauch, verstärktes nächtliches Schwitzen, Juckreiz besonders nach Kontakt mit Wasser und Appetitlosigkeit lassen oft nicht direkt auf eine schwere Erkrankung schließen. Gerade Frauen denken oftmals eher an die Wechseljahre und nicht an eine seltene Bluterkrankung. Auch Sehund Konzentrationsstörungen, Ohrensausen oder trockene Haut werden eher auf das Alter zurückgeführt und nicht in Kombination betrachtet. Die Folge: der Arztbesuch bleibt aus, die PV bleibt unentdeckt und somit auch unbehandelt, schwere Komplikationen können auftreten.
Zunehmende Beschwerden ernst nehmen
Aber auch wenn die Diagnose bereits gestellt wurde, sollten Betroffene die Symptome im Blick behalten und regelmäßige Kontrolluntersuchungen durchführen lassen. Wenn die Symptomlast zunimmt oder Nebenwirkungen auftreten, sollten Betroffene umgehend das Gespräch mit dem Behandlungsteam suchen, um krankheitsbedingte Beschwerden von therapiebedingten zu unterscheiden, denn manche Begleiterkrankungen oder Komplikationen können für Betroffene im schlimmsten Fall lebensbedrohlich werden. So sollten z. B. regelmäßig das Blut und die Milz untersucht werden. Zudem sollte einmal jährlich ein Hautscreening durchgeführt werden, um therapiebedingte Hautveränderungen früh zu erkennen, die sich möglicherweise zu schweren Hautveränderungen wie offenen Wunden oder gar Hautkrebs entwickeln könnten.
Wissen ist demnach für Betroffene der Schlüssel, um bei der Wahl und Durchführung der passenden Therapie intensiv mit einbezogen werden zu können. Die drei einzelnen Initiativen für das Leben mit Myelofibrose, Polycythaemia Vera und Chronischer Myeloischer Leukämie bieten auf der Internetseite www.leben-mit-blutkrankheiten.de viele Informationen, die über die Facetten der Erkrankungen informieren.
Bei Menschen mit hellem Hauttyp, die sich gerne in der Sonne aufhalten, besteht ein erhöhtes Risiko, eine Aktinische Keratose zu entwickeln, die sich in einem von zehn Fällen zu hellem Hautkrebs entwickeln kann. Dies gilt um so mehr für MPN-Patient*innen, da eine der medikamentösen Therapien dieses Risiko zusätzlich steigern kann. Deshalb sollten Betroffene Hautveränderungen in lichtexponierten Arealen ernst nehmen und sie einem Dermatologen zeigen. Diese Obacht gilt auch für Veränderungen an den Beinen. Streifige oder netzartige Rötungen und offene Stellen sollten möglichst frühzeitig einem Hautarzt oder den betreuenden Hämatoonkologen gezeigt werden, da das ein klares Indiz dafür sein könnte, die Therapie zu überdenken und entsprechend anzupassen.
Prof. Dr. Markus Braun-Falco
Facharzt für Dermatologie und Venerologie
Hier finden sich auch Patient*innen-Erfahrungsberichte und Expert*innenbeiträge zu verschiedenen krankheitsrelevanten Schwerpunkten. Zudem finden Patient*innen ausführliche Checklisten, die ihnen die Gespräche mit dem Behandlungsteam erleichtern können. Dazu kann auch eine Anpassung der Therapie gehören, wenn die bestehende Behandlung nicht den gewünschten Erfolg erzielt oder Nebenwirkungen auftreten, welche die Lebensqualität stark beeinträchtigen. Dabei kann auch der MPN-Tracker unter de.mpn.your-symptom-questionnaire.com helfen, der Patient*innen in Form eines Therapietagebuches bei der Dokumentation zur Entwicklung ihrer Erkrankung unterstützt.
Zusammen stärker
Auch der Austausch mit anderen Betroffenen, Selbsthilfeorganisationen und Fachärzt*innen stärkt Patient*innen und ihre Angehörigen im Umgang mit der Erkrankung. Seit 2016 können MPNBetroffene einen bundesweit etablierten Treffpunkt nutzen: die MPNPatient*innentage. Die Teilnahme an den MPN Veranstaltungen ist kostenlos.
Auf www.leben-mit-blutkrankheiten.de/mpn-patiententage findet man die Anmeldung für die nächsten Patient*innentage sowie weitere Informationen und einen kleinen Rückblick auf vergangene Veranstaltungen.


Wie meine Krankheit zur Gründung einer Stiftung führte
Ich war 21, als mein Körper mir zeigte, dass etwas nicht stimmte. Große blaue Flecken auf den Beinen – ohne Erinnerung an einen Stoß. Dann kleine, rote Pünktchen auf der Haut, wie Nadelstiche. Ich ging zum Hausarzt.
Die Blutwerte zeigten: Meine Blutplättchen waren auf ein Zehntel des Normalwertes gesunken. Plötzlich fiel ein erschreckendes Wort: Leukämie. Eine Knochenmarkpunktion folgte – das Warten auf das Ergebnis war zermürbend. Doch dann die erste Erleichterung: keine Leukämie. Stattdessen wurde ein Vitamin-B12-Mangel festgestellt. Endlich etwas, das behandelbar klang. Doch mein Zustand besserte sich nicht. Die bleierne Müdigkeit wurde stärker, das Studium rückte in weite Ferne.
Drei Monate später ergab eine spezielle Blutuntersuchung (Durchflusszytometrie) eine neue, unbekannte Diagnose: PNH – Paroxysmale Nächtliche Hämoglobinurie. Eine seltene Erkrankung, die auch mein Hausarzt kaum kannte. Es war, als wären wir im medizinischen Niemandsland.
Meine Familie recherchierte unermüdlich und fand einen Spezialisten in Aachen. Der Kontakt war sofort herzlich, aber die Informationen beunruhigend: PNH sei nicht nur selten, sondern auch lebensbedrohlich. Zudem gehe sie oft mit einer weiteren Krankheit einher: der Aplastischen Anämie (AA). In meinem Fall dominierte zunächst die PNH.
Besonders eindrücklich war ein Gespräch mit einer anderen Betroffenen. Sie lebte schon lange mit PNH und AA, beschrieb Symptome, die mir noch bevorstanden. Es machte mir Angst – und zugleich gab es mir Trost. Sie verstand mich. Dieses Gespräch war mehr als informativ: Es gab mir Verbindung, Verständnis, Hoffnung. Ich versuchte, meinen Alltag weiterzuleben. Doch nach einer einfachen Erkältung brach mein Blutbild zusammen. Nun waren alle drei Zelllinien betroffen – die Aplastische Anämie hatte übernommen. Die Notwendigkeit einer Therapie war unumgänglich. Zum Glück war mein Bruder ein passender Knochenmarkspender. Die Transplantation wurde geplant – und fiel auf meinen Geburtstag.
Es fühlte sich wie ein gutes Zeichen an. Die Zeit war hart, begleitet von Ängsten, Medikamenten, Nebenwirkungen –doch die Transplantation verlief so gut, wie man es sich nur wünschen konnte.

eindrücklich war ein Gespräch mit einer anderen Betroffenen. Sie lebte schon lange mit PNH und AA, beschrieb Symptome, die mir noch bevorstanden. Es machte mir Angst – und zugleich gab es mir Trost.
Melanie Vanden-Brande
Zwei Jahre später war ich zurück im Leben. Nicht im Überleben – im Leben. Die Krankenhausgänge, Blutabnahmen, Unsicherheiten – sie rückten in den Hintergrund. Wir waren voller Dankbarkeit. Ohne die Kompetenz und Empathie der Ärzt:innen hätten wir das nicht geschafft. Wir wollten etwas zurückgeben. Doch die Ärztinnen und Ärzte hatten eine größere Idee: eine Stiftung. Für Betroffene von PNH und AA – für Erkrankungen, die im Schatten stehen. Für Patientinnen und Patienten, die jahrelang auf eine Diagnose warten. Die kaum Ansprechpartner finden, oft unzureichend versorgt sind. Die Idee berührte uns. Etwas schaffen, das bleibt.
So entstand 2013 die Stiftung lichterzellen. Mein damaliger Arzt ist heute im Vorstand, die Patientin, mit der ich damals sprach, ist Geschäftsführerin. In den letzten zwölf Jahren wurden zahlreiche Projekte verwirklicht: Infomaterialien erstellt, Betroffene beraten, Forschung unterstützt. Heute gehen Erkrankte diesen Weg nicht mehr allein.
Ich bin stolz, was aus meinem Weg entstanden ist. Er war schwer – und wurde doch der Anfang von etwas Größerem. Die Stiftung lebt. Sie schenkt Hoffnung. Licht. Und wir machen weiter. Denn auch heute sterben Menschen an diesen Erkrankungen. Auch wenn sie selten sind – jeder Mensch zählt.

Die Gentherapie bietet neue und vielversprechende Behandlungsmöglichkeiten für Menschen mit Sichelzellkrankheit (SCD) und transfusionsabhängiger Beta-Thalassämie (TDT), zwei schweren, vererbten Bluterkrankungen. Wir sprachen mit Prof. Dr. Roland Meisel vom Universitätsklinikum Düsseldorf über die Chancen dieser neuen Behandlungsmöglichkeit.

Gentherapien werden von Experten als eine neue Ära der Medizin angesehen. Können Sie uns kurz erklären, was eine Gentherapie ist und was sie so besonders macht?
Das Wirkprinzip von Gentherapien ist eine Veränderung der Erbinformationen, die den Bauplan für unseren gesamten Körper darstellen und auch als Gene bezeichnet werden. Wenn – wie bei angeborenen Bluterkrankungen – ein Teil dieses Bauplans gestört ist, kann über die Gentherapie entweder eine korrigierte Version des betroffenen Gens eingeschleust oder die Erbinformation durch sogenannte Geneditierung zielgerichtet verändert werden. Gentherapien verfolgen das Ziel, durch eine einmalige Behandlung die wesentlichen Symptome der Erkrankungen erheblich zu mindern oder gar zu beseitigen – und das dauerhaft.
Seit einem Jahr ist die erste Gentherapie für Patienten mit schwerer Sichelzellkrankheit und transfusionsabhängiger Beta-Thalassämie in der EU zugelassen. Welche Hoffnungen sind damit verbunden? Bei beiden angeborenen Erkrankungen ist der Bauplan für den roten Blutfarbstoff Hämoglobin gestört. Bei der transfusionsabhängigen Beta-Thalassämie ist die Folge, dass kein reifes, sogenanntes „erwachsenes“ Hämoglobin gebildet wird. Bei der Sichelzellkrankheit wird dieses zwar gebildet, ist aber in seinen Eigenschaften stark verändert, was zu häufigen Verstopfungen von Blutgefäßen führt.
Patienten mit TDT sind dadurch in der Regel ab dem ersten oder zweiten Lebensjahr lebenslang auf regelmäßige Bluttransfusionen angewiesen. Patienten mit schwerer SCD erleiden häufig krisenhafte Schmerzattacken und Durchblutungsstörungen lebenswichtiger Organe. Die neu verfügbare Gentherapie zielt darauf ab, die Bildung des frühkindlichen, sogenannten fetalen Hämoglobins, das Babys im Mutterleib und Säuglinge perfekt mit Sauerstoff versorgt, zu reaktivieren.
Betroffenen möchte ich empfehlen, so früh wie möglich Experte ihrer eigenen Erkrankung zu werden.
Damit soll das fehlende erwachsene Hämoglobin beziehungsweise seine gestörte Funktion ersetzt und so die wesentlichen Symptome beider Erkrankungen minimiert oder eliminiert werden.
Wie wurden die beiden Erkrankungen bisher behandelt?
Die konventionelle Therapie bei der Beta-Thalassämie besteht aus Bluttransfusionen, die lebenslang alle drei bis vier Wochen erfolgen müssen. Zusätzlich müssen Medikamente eingenommen werden, um eine aus den Transfusionen resultierende Eisenüberladung mit schweren Organschäden zu vermeiden.
Bei der Sichelzellkrankheit fokussiert sich die Therapie auf die symptomatische Behandlung, zum Beispiel der schweren Schmerzkrisen mit Schmerzmitteln. Zudem kann ein Medikament verabreicht werden, das die Häufigkeit von Schmerzkrisen und Verstopfungen von Blutgefäßen reduzieren kann. Außerdem können – gerade im Notfall – Blutaustauschtransfusionen zum Einsatz kommen. All dies sind aber keine Maßnahmen, die den Patienten langfristig heilen, es geht primär um die Symptomkontrolle. Zudem muss deutlich gesagt werden: Auch Patienten, die diese konventionelle Therapie vorbildlich durchführen, haben eine gegenüber Gesunden verkürzte Lebenserwartung, da im Laufe der Zeit chronische Organschäden entstehen. Die bisher einzige Möglichkeit, die abgesehen von der Gentherapie auf eine Heilung abzielt, ist die Transplantation von blutbildenden Stammzellen eines gut passenden Spenders. Diese Behandlungsmöglichkeit ist aber durch die eingeschränkte Verfügbarkeit passender Spender sowie Risiken von Immunreaktionen zwischen Spender und Patient limitiert. Die Gentherapie hat den großen Vorteil, dass kein Spender notwendig ist und auch keine Risiken aus den oben genannten Immunreaktionen bestehen.
Wie wirkt sich eine erfolgreiche Gentherapie auf die Lebensqualität der Betroffenen aus?
Für einen Thalassämie-Patienten bedeutet es in erster Linie Freiheit in der täglichen Lebensplanung, da er nicht mehr alle drei bis vier Wochen zur Transfusion erscheinen muss. Auch die Medikamente zur Kontrolle der Eisenüberladung sind dann voraussichtlich nicht mehr nötig. Das ist ein riesiger Zugewinn an Unabhängigkeit und Lebensqualität und eröffnet völlig neue Perspektiven in der Lebensplanung und damit Selbstbestimmung.
Eine
erfolgreiche Gentherapie heißt also auch eine erhebliche Verbesserung der Lebensqualität und eine Planbarkeit, die sonst unmöglich wäre.
Prof. Dr. Roland Meisel Stellvertretender Klinikdirektor, Leiter des Bereichs Pädiatrische Stammzelltherapie, Universitätsklinikum Düsseldorf
Für Sichelzellpatienten heißt es, dass die plötzlich und völlig unerwartet auftretenden Schmerzkrisen, die Betroffene von jetzt auf gleich komplett aus dem Alltag reißen, deutlich reduziert oder eliminiert werden. Eine erfolgreiche Gentherapie heißt also auch für sie eine erhebliche Verbesserung der Lebensqualität und eine Planbarkeit, die sonst unmöglich wäre.
Was möchten Sie Betroffenen mit auf den Weg geben?
Betroffenen möchte ich empfehlen, so früh wie möglich Experte ihrer eigenen Erkrankung zu werden. Informieren Sie sich, mit welchen Maßnahmen man die Erkrankung möglichst von Beginn an optimal behandeln kann, wie die Stammzelltransplantation und die Gentherapie funktionieren, welche Chancen sie bieten und welche Limitationen sie haben.
Lassen Sie sich in einem spezialisierten Zentrum beraten, das viel Erfahrung in der Behandlung dieser Erkrankungen hat, und auch über die neuesten Behandlungsoptionen gut Bescheid weiß.



Was bedeutet es, mit Hämophilie frei zu leben?
Ein Leben mit Hämophilie bringt besondere Herausforderungen mit sich – körperlich wie emotional. Für viele bedeutet Freiheit vor allem eines: den Alltag selbstbestimmt gestalten zu können – mit mehr Sicherheit, weniger Blutungen und mehr Lebensqualität.
Moderne Therapien können dabei unterstützen. Neue Behandlungsansätze auf Basis von ‚natürlichem‘ Faktor VIII ersetzen gezielt den bei Hämophilie fehlenden Gerinnungsfaktor und tragen so zu einer normalisierten Blutgerinnung bei. Eine Therapie mit hohen Faktor VIII Spiegeln kann helfen, sichtbare und nicht sichtbare Blutungen in den Gelenken und Muskeln zu vermeiden –und damit auch Ängsten oder Unsicherheiten im Alltag entgegenwirken.
Freiheit heißt auch, eigene Grenzen zu erkennen – und neue Wege zu finden. Ob im Beruf, beim Sport oder auf Reisen: Menschen mit Hämophilie berichten, dass die passende Therapie ihnen dabei hilft, selbstbewusster zu leben und Herausforderungen besser zu meistern. Auf liberatelife.de finden Interessierte Informationen rund um moderne Hämophilie-Therapien sowie Artikel und Interviews zu Themen wie Gesundheit, Lebensqualität und Selbstbestimmung.

Liberate Life ist unser Verständnis, das Leben von Menschen mit Hämophilie zu verändern. Dein Leben ist einzigartig und mehr als Hämophilie. Mit unserem Engagement wollen wir neue Perspektiven eröffnen, Wissen vermitteln und deine Behandlung individuell verbessern.

Hämophilie ist eine seltene, genetisch bedingte Störung der Blutgerinnung, die über mehrere Generationen verborgen bleiben kann. Dies war in der Familie von Alexander Heise, Vorstandsmitglied der IGH e.V., der Fall: Erst eine anhaltende Blutung am Zahnfleisch des damals Eineinhalbjährigen führte zur Diagnose. Heute ist Alexander Mitte 20 und berichtet aus seinem Alltag mit Hämophilie A.
Text Miriam Rauh
Alexander, wie äußert sich die Blutgerinnungsstörung bei dir im Alltag?
Mittlerweile nicht viel mehr, als dass ich mir regelmäßig die Prophylaxe selbst spritze – für mich ein großer Freiheitsgewinn – und Kontrolltermine wahrnehme. Ich muss auf meine Gelenke besonders achten, weil ich als Kind und Jugendlicher mehrere Gelenkblutungen hatte. Erst mit 12 wurde ich an ein Hämophilie-Zentrum angebunden, wo ich Zugang zur Prophylaxe erhielt, die mir im Alltag einen höheren Schutz vor Blutungen bietet. Trotzdem gibt es natürlich Situationen, wo ich vorsichtiger bin als andere. Zum Beispiel beim Fahrradfahren – da achte ich sehr auf den Verkehr, fahre vorausschauend, halte lieber einmal mehr an. Über die Jahre habe ich ein gutes Gespür für mich entwickelt.
Wo ziehst du persönlich deine Grenzen?
Ich finde es sehr schwer, immer genau zu wissen, was noch vernünftig ist – und was vielleicht schon zu riskant. Man will ja auch nicht ständig mit angezogener Handbremse leben. Mir zum Beispiel wurde früher oft empfohlen, Nordic Walking zu machen – aber das ist für Jugendliche wenig attraktiv, auch wenn Sport an sich richtig gut ist. Stattdessen habe ich das Turniertanzen für mich entdeckt. Als ich mit 16 einen Tanzkurs machte, hat mich das Tanzen nicht mehr losgelassen. Ich war regelmäßig auf Tanzpartys und irgendwann kam auch die Möglichkeit, mit meiner damaligen Tanzpartnerin in den Turniertanz einzusteigen. Das war eine richtig tolle Zeit.
Und wie hat sich das auf deine Gesundheit ausgewirkt? Extrem positiv. Die Schmerzsituation hat sich massiv verbessert. Ich konnte plötzlich wieder lange Wanderungen machen – etwas, das ich mir vorher gar nicht vorstellen konnte. Das Tanzen hat mir eine ganz neue Welt eröffnet, für die ich sehr dankbar bin.
Gibt es Sportarten, die du generell nicht empfehlen würdest?
Kampfsportarten wie Boxen oder Kickboxen sind für Menschen mit Hämophilie sicher eher kritisch zu sehen. Aber auch da gibt es Alternativen: Man kann z. B. Boxtraining ohne Kontakt machen – mit dem Sandsack. Generell finde ich, dass man vieles ausprobieren kann, wenn es gut vorbereitet ist und natürlich in Absprache mit den behandelnden Ärzten und Ärztinnen. Man könnte z. B. sagen: „Probier es mal einen Monat aus, lass uns das eng begleiten.“ Wenn es gut läuft, super! Wenn es häufig zu Blutungen kommt, ist es vielleicht doch nicht der richtige Sport.

Es gibt viele Mythen und Vorurteile zu Hämophilie. Welche haben dich besonders genervt oder tun es immer noch? Ein Klassiker ist: „Wenn du dich mit einer Nadel stichst, blutest du sofort unendlich lange.“ Das stimmt so natürlich nicht. Viele glauben auch, dass mein Blut „dünner“ ist als bei anderen. Dabei fehlt bei mir einfach nur ein bestimmter Gerinnungsfaktor, und das wird erst dann ein Problem, wenn ich mich verletze. Das Blut selbst ist genauso „dick“ wie bei anderen Menschen. Was mich auch nervt: Dass viele automatisch denken, Hämophilie bedeutet, dass man total eingeschränkt leben muss. Klar, man muss vorsichtig sein –aber man kann mit der richtigen Therapie und Planung ein aktives Leben führen.
Und wie gehst du mit Ängsten um – etwa vor Verletzungen oder Operationen?
Die Angst ist definitiv ein Thema. Als ich 2021 meine Weisheitszähne rausbekam, wurde daraus zur Sicherheit ein mehrtägiger Klinikaufenthalt. Dass es zu längeren Blutungen kommen könnte, schwingt bei Eingriffen oder riskanten Situationen immer mit. Auch im Alltag merke ich, dass ich manches anders einschätze als andere – zum Beispiel, wenn meine Freunde irgendwo raufklettern. Da sage ich dann auch mal: „Nee, das ist mir zu heikel.“ Aber wenn ich es erkläre, verstehen sie es auch.
Was würdest du anderen Betroffenen gerne mit auf den Weg geben – besonders in Hinblick auf Sport? Findet eine Sportart, die euch wirklich Spaß macht! Es muss nicht Schwimmen oder Radfahren sein, nur weil das als „sicher“ gilt. Die Sportwelt ist riesig – probiert euch aus. Und: Seid offen. Ihr müsst eure Geschichte nicht jedem auf die Nase binden, aber ein gutes Gespräch mit Menschen, die euch nahestehen, kann viel verändern. Wir wachsen mit der Erkrankung auf – wir kennen uns gut aus. Aber andere wissen das nicht automatisch. Da hilft es, Dinge klar zu benennen.
Die Interessengemeinschaft Hämophiler e. V. ist ein bundesweit tätiger Patientenverband, der die Interessen der an einer angeborenen Blutungskrankheit leidenden Menschen und ihrer Angehörigen vertritt.
Weitere Informationen finden Sie unter: www.igh.info
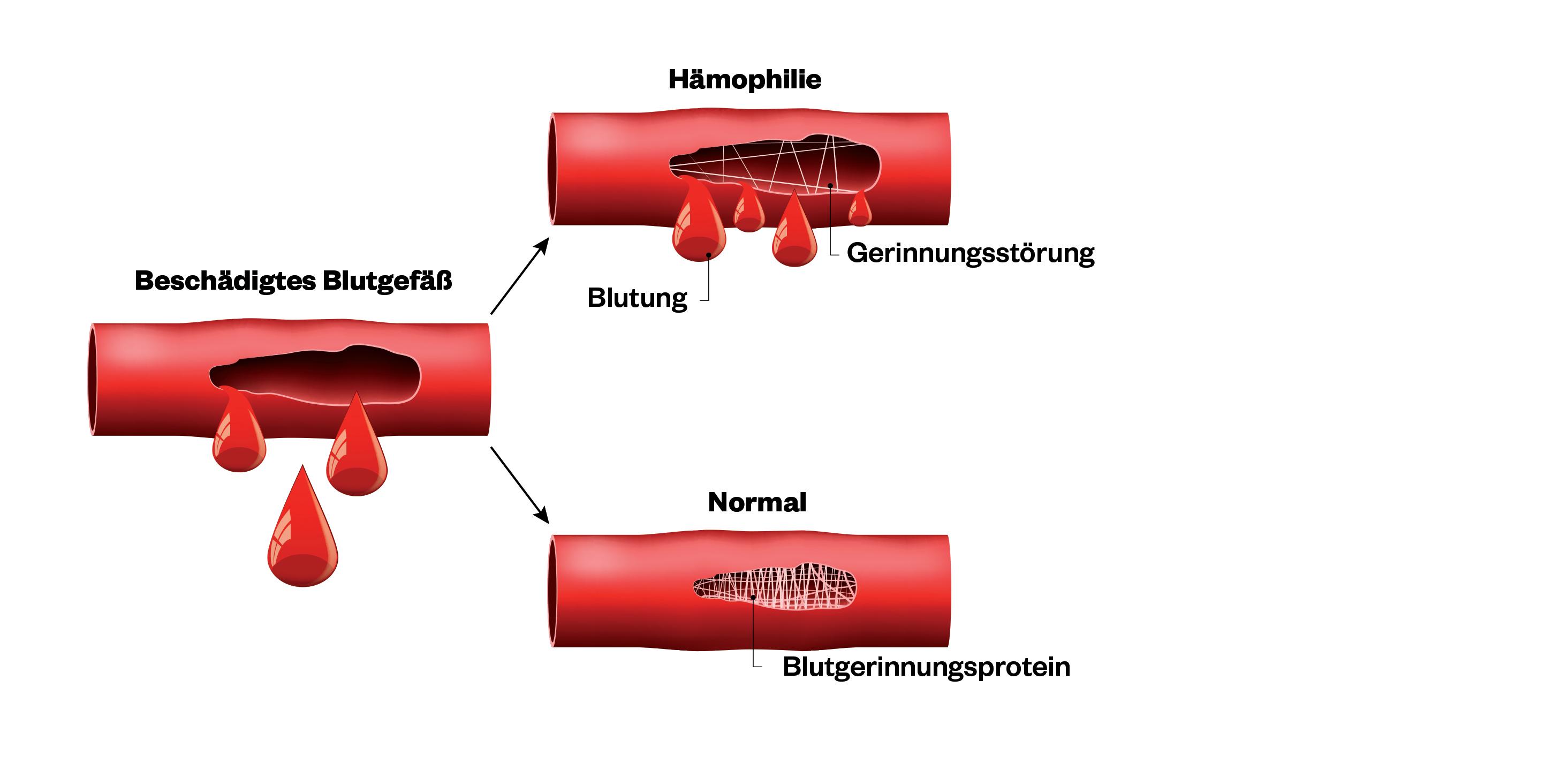

Die verschiedenen Gerinnungsfaktorenkurz auch Faktoren genannt - haben unterschiedliche Funktionen im Rahmen der Blutgerinnung. Durch ihr Zusammenspiel können Blutungen so schnell und dauerhaft gestillt werden.
Wenn ein bestimmter Faktor fehlt oder nur unzureichend vorhanden ist, kommt es zu einem Gerinnungsfaktormangel.
Daher spricht man bei Hämophilie A von einem Mangel an Faktor VIII, bei Hämophilie B von einem Mangel an Faktor IX.
Die einmal anzuwendende Gentherapie kann eine Alternative zu der üblichen kontinuierlichen Prophylaxe mit Faktor-IX oder Faktor-VIII bei Menschen mit Hämophilie sein. Sie kann dazu beitragen, die Lebensqualität der Betroffenen weiter zu verbessern.
Heute können Menschen mit Hämophilie ein nahezu normales Leben führen. Das war vor nur zwei Generationen noch ganz anders. Bei Menschen mit Hämophilie fehlt der Gerinnungsfaktor-VIII (Hämophilie A) oder Gerinnungsfaktor-IX (Hämophilie B) oder dieser wird nicht ausreichend produziert. Dank der kontinuierlichen Fortschritte der modernen Medizin haben sich die Behandlungsmöglichkeiten dieser erblich-bedingten Blutgerinnungsstörung über die Jahrzehnte enorm verbessert, sodass die Krankheit immer besser in den Griff zu bekommen ist. Regelmäßige Infusionen des fehlenden Gerinnungsfaktors ermöglichen den Betroffenen ein aktives Leben.
Die Symptome der Hämophilie bleiben jedoch lebenslang bestehen. Zu den wichtigsten Symptomen zählen starke, langanhaltende Blutungen, die zum Teil spontan, also ohne erkennbaren Grund, auftreten. Am häufigsten handelt es sich um Einblutungen in Gelenke und Muskeln, die mit der Zeit zu chronischen Schmerzen und Gelenkschäden führen können. Solche Blutungen können lebensbedrohlich sein und bleibende körperliche Beeinträchtigungen nach sich ziehen. Wie schwer die Symptome ausgeprägt sind, hängt insbesondere davon ab, wie viel Gerinnungsfaktor im Blut vorliegt – je weniger Gerinnungsfaktor, desto höher das Blutungsrisiko.
Therapieziel der Hämophilie
Das übergeordnete Ziel der Hämophilie-Therapie ist es, die Blutgerinnung und damit den Schutz vor Blutungen zu verbessern. Dies ist mit der Bedarfstherapie möglich, wenn akut eine Blutung auftritt, sowie mit der Prophylaxe, bei der regelmäßig, beispielsweise einmal wöchentlich, der fehlende Gerinnungsfaktor verabreicht wird, um Blutungen vorzubeugen.
Bei den meisten Betroffenen lässt sich die Hämophilie mit der Prophylaxe gut beherrschen. Trotz der bereits erzielten Fortschritte auf dem Gebiet der Hämophilie gibt es weiterhin Bedarf an neuen Behandlungsmöglichkeiten für Menschen, die mit Hämophilie leben. Denn selbst mit regelmäßiger Prophylaxe können noch Blutungen auftreten, die zu Schmerzen, Gelenkschäden und einer beeinträchtigten Lebensqualität führen können. Die regelmäßige Prophylaxe ist lebenslang mit dem Erfordernis von Infusionen verbunden. Für die Betroffenen und ihr Umfeld können die Symptome der Hämophilie sowie die regelmäßigen Infusionen in vielfacher Hinsicht eine Belastung sein: Fehlzeiten bei der Arbeit, in der Ausbildung oder in der Schule sind mögliche Folgen. Betroffene mit Hämophilie können ein höheres Verletzungsrisiko bei sportlichen Aktivitäten haben. All dies kann sich oft auf die Lebensgestaltung, Beziehungen und Partnerschaften auswirken. Ein gleichbleibend höherer FVIII- bzw. FIX-Spiegel würde einen besseren Schutz bedeuten.
Neuartiger Ansatz: Gentherapie
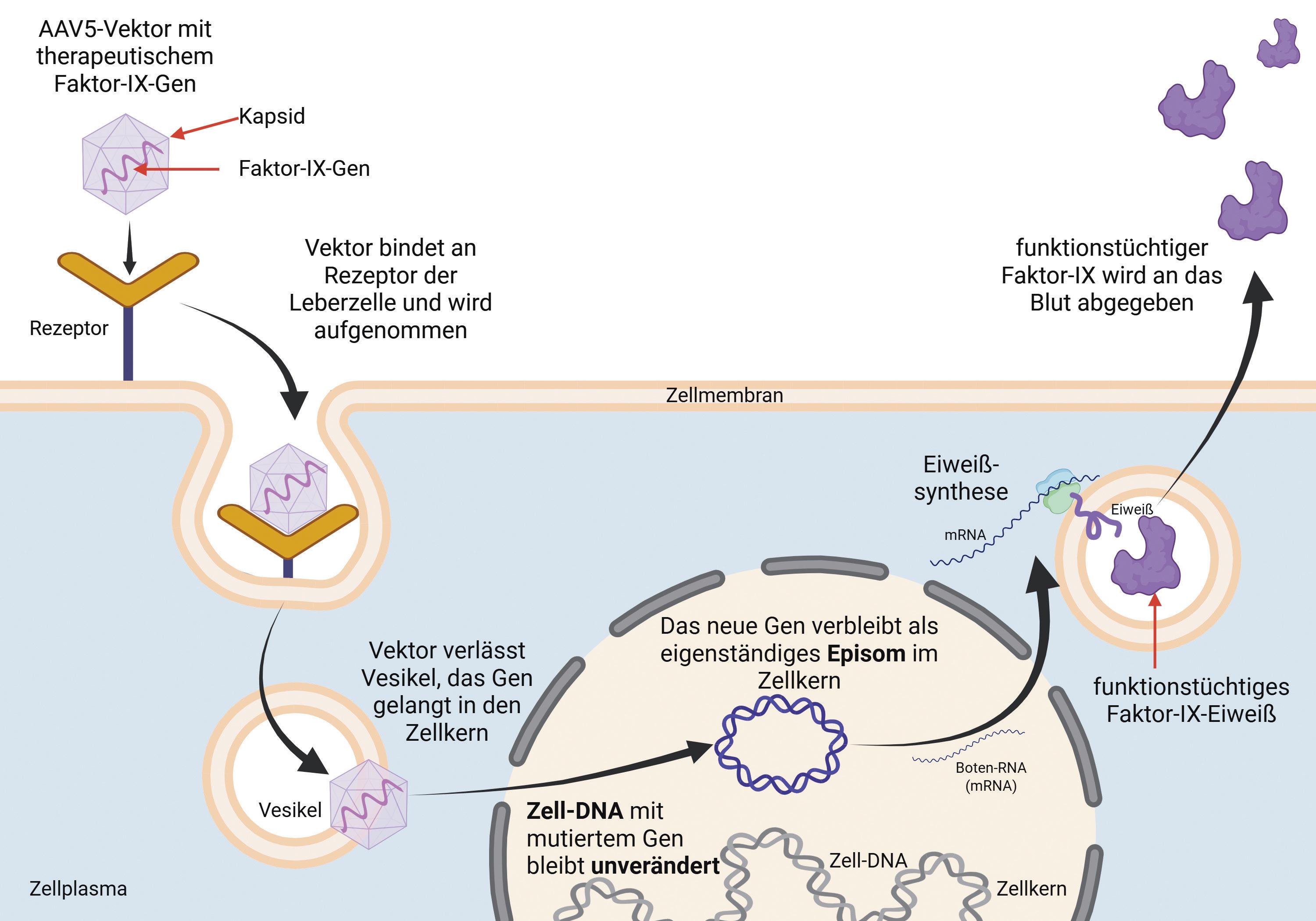
Die Gentherapie ist ein neuartiger Ansatz zur Behandlung genetischer Erkrankungen, die durch ein einzelnes defektes Gen verursacht werden – wie es bei der Hämophilie der Fall ist. Für die Durchführung wird ein funktionsfähiges Gen in den Körper eingeschleust, um das fehlerhafte Gen zu ersetzen. Hierfür wird ein Transportmittel benötigt: Das funktionsfähige Gen wird in sogenannte Vektoren verpackt, die das Gen auf der Reise in die Körperzellen schützen und zum Ziel leiten, den Leberzellen, da der Körper dort die Gerinnungsfaktoren bildet. Vektoren nutzen die biotechnologisch hergestellten "Verpackungen" von Viren, deren genetisches Material jedoch ersetzt wurde. Sie sind nicht mehr vermehrungfähig und lösen keine Infektionskrankheit mehr aus. Da die Leber der Ort der Bildung der
Gerinnungsfaktoren VIII und IX ist, erfolgt bei der Gentherapie der Hämophilie die Zufuhr als Injektion in eine Vene, um über das Blut die Leber zu erreichen. Nach der erfolgreichen Aufnahme des funktionsfähigen Gens in die Leberzelle kann diese den korrekten genetischen Bauplan für Faktor VIII oder Faktor IX nutzen, um selbst funktionsfähige Gerinnungsfaktor-Proteine zu bilden, wozu sie zuvor nicht in der Lage war.
Gentherapie – eine neue Behandlungsoption
Die speziellen Merkmale der Hämophilie machen die Behandlung und das Leben mit dieser Erkrankung zu einer Herausforderung. Gleichzeitig machen sie die Hämophilie aber auch zu einem idealen Ziel für die Gentherapie. Die einmalige Infusion der Gentherapie hat als Ziel:
1. Die Leber soll in die Lage versetzt werden, langfristig selbst den bisher unzureichend vorhandenen Gerinnungsfaktor herzustellen.
2. Der Gerinnungsfaktor-Spiegel soll weitgehend stabil bleiben, also möglichst ohne größere Schwankungen.
3. Spontane Blutungen sollen reduziert werden oder besser noch ganz ausbleiben.
Austausch mit den behandelnden Ärzten Wenn Sie Fragen zu Hämophilie haben, wenden Sie sich an Ihre behandelnden Ärzte bzw. an ein spezialisiertes Hämophilie-Zentrum.
Erfahren Sie mehr über die neuen Möglichkeiten! www.haemevolution.de