

www.medmag bg
Редакционна




www.medmag bg
Редакционна

ГАСТРОЕНТЕРОЛОГИЯ
12 ХРАНЕНЕ И ЗАХРАНВАНЕ НА КЪРМАЧЕТО. РОЛЯ НА ВИТАМИНИТЕ И МИКРОНУТРИЕНТИТЕ СПОРЕД ПРЕПОРЪКИТЕ НА СЗО З. Панделиева
18 КОНСЕНСУСНИ НАСОКИ ЗА ДИАГНОСТИКА, ЛЕЧЕНИЕ И ПРОСЛЕДЯВАНЕ ПРИ ИНФЕКЦИЯ С CLOSTRIDIOIDES DIFFICILE В
БОЛНИЧНА ПРАКТИКА В БЪЛГАРИЯ М. Лилова, Д. Райков, Р. Цонев, д.м., П. Карагьозов, д.м., FASGE
24 ХЕМОТРАНСФУЗИОННИ СТРАТЕГИИ
28 АНАЛИЗ НА АНАМНЕЗАТА И СЕРУМНИТЕ НИВА НА IGE ПРИ БРЕМЕННИ ЖЕНИ И ВРЪЗКАТА ИМ С РИСКА ОТ АЛЕРГИЧНИ ЗАБОЛЯВАНИЯ В. Карамишева, Д. Христова, М. Владимиров, Д. Колева, Б. Карамишев, А. Колев, Л. Колева, В. Спасова, Н. Христов, М. Перусанова
ПРЕПОРЪКИ ЗА УПРАВЛЕНИЕ НА ФРАКТУРНИЯ РИСК М. Недкова, Р. Каралилова, д.м.н., Ц. Петранова, д.м., С. Нейчева, д.м., З. Баталов, д.м. АЛЕРГОЛОГИЯ
42 АСТМА ПРИ ДЕЦА ОТ ПРЕДУЧИЛИЩНА ВЪЗРАСТ. ДИАГНОСТИЧНИ И ТЕРАПЕВТИЧНИ ПРОБЛЕМИ А. Кахтан ДЕРМАТОЛОГИЯ
52 АЛОПЕЦИЯ АРЕАТА: СЪВРЕМЕНЕН ПОГЛЕД ВЪРХУ ЕПИДЕМИОЛОГИЯ, ЕТИОЛОГИЯ, ПАТОГЕНЕЗА, КЛИНИЧНА
56









пушат. Те се нуждаят от повече фолат и витамин C, отколкото непушачите.
Многоплодна бременност: Жените, бременни с повече от едно бебе, очевидно се нуждаят от повече микроелементи, отколкото жените, които носят едно бебе. Следователно, те се нуждаят от добавки,


Ниските нива на витамин D през пър -
триместър на бременността са
свързани с по-високи нива на преждевременно раждане и намалена дължина на плода, според ново проучване, ръководено от изследователи от Департамента по хранителни науки на щата Пенсилвания. Това изследване предоставя доказателства, че ранната бременност или дори периодът преди зачеването може да представляват критични
от проучването са публикувани наскоро в The American Journal of Clinical Nutrition.
дователите сравняват резултатите за жени с недостатъчност на
nmol/L),
ста






































































Розмаринът има антиоксидантни и противовъзпалителни ефекти поради наличието на монотерпени, дитерпени и тритерпени. Освен това в състава му откриваме фенолни съе -
динения като розмаринова киселина, която има антиоксидантни, както и антимикробни свойства. Моно


седативни, антидепресантни и анксиолитични ефекти чрез активиране
на GABA рецепторите. За да се потвърди този
положителен ефект върху паметта, е прове -
дено проучване върху студенти. Някои студенти са консумирали капсули с розмарин от 500 мг два пъти дневно в продължение на
един месец, докато други са приемали капсули с плацебо. Резултатите от това проучване доказват, че консумацията
вдишването
ху тревожността
тестовете. Студентите заявяват, че розмаринът е повишил фокуса и концентрацията им по време на изпита. Инхалаторите и торбичките, напоени с етерично масло, са евтини и широко достъпни, така че представляват просто и безопасно решение за борба с тревожността от тестовете. Днес можем да намерим и гривни с дифузер за етерично масло, които
астежът през първите месе -
ци от живота протича с из -
ключително бързи темпо -
ве и играе критична роля
за правилното физическо и нервнопсихично развитие. Хране -
нето през този период е от жизнено -
важно значение за поддържане те -
глото и осигуряване на нормален растеж и развитие. В съответствие организмът на детето се нуждае от енергия и хранителни вещества, като потребностите в тази възраст са най-високи, отнесени към разме -
ефекти
нарушения в нервнопсихичното раз
витие, нарушени имунни функции, повишаване на заболеваемостта и смъртността.
ПРОТЕИНИ Протеините се използват за изграждане на тъкани, натрупване на телесна маса и растеж, участват в състава на ензими и хормони. Недостатъчният прием с храната е свързан с по
ние и са представени предимно от лакто -
за в количество - 7.4 (от 7.2 до 7.7) g/100 ml.
Съдържат се и галактоолигозахариди.
МАЗНИНИ
Мазнините са макронутриент с най-голяма енергийна плътност. Кърмата и млеката за кърмачета са основен източник на мазнини за кърмачето. Кърмата съдържа средно 3.6 (2.2 до 5.0) g/100 ml мазнини. Освен
енергия осигуряват на организма есенциални мастни киселини (алфа-линоленова и линолова), които играят важна функционална и структурна роля в клетъчния метаболизъм, както и абсорбция на мастноразтворими витамини. Тези процеси са от основно значение за нервното развитие и зрението. Дефицитът на есенциални мастни киселини се среща рядко и може да има разнородни прояви - обриви с десквамацация, алопеция, тромбоцитопения, нарушения в имунитета, в растежа. Тези мастни киселини са източник за образуването на дълговерижните ейкозапeнтaенова (ЕРА), докозахексаенова (DHA) и арахидонова (АRA) мастни киселини, характеризиращи се с разнородна структурна и функционална роля в клетката – мембранна пропускливост, генна експресия, модулиране на имунния отговор. Налични са в кърмата и често се добавят в млеката за кърмачета.
ЕНЕРГИЯ
Разходът на енергия в организма на детето има няколко компонента – основна обмяна, енергия, необходима за усвояване на храната, енергия за физическа активност и енергия за поддържане на растежа и развитието. Недостигът на енергия е свързан с нарушения в растежа, както и излишъкът крие риск от развитие на затлъстяване. Потребностите от енергия през първите 6 месеца са 570 kcal за момчета и 520 kcal за комичета, от 6 до 12 месеца съответно 740 kcal и 670 kcal. При реазграждането си макронутриентите освобождават енергия съответно: мазнините - 9 kcal/g, въглехидратите - 4 kcal/g
- 4 kcal/g. Кърмата
МИКРОНУТРИЕНТИ Микронутриентите включват витамини и минерали, есенциални за растежа и развитието на организма. Препоръките за прием на микронутриенти служат както за предотвратяване на дефицити, така и за осигуряване на добър здравен статус в бъдеще.
Кърмата осигурява оптимален прием на повечето микронутриенти, включително желязо и цинк. Независимо че са в малки количества, те са биодостъпни и задоволяват потребностите през първите 4-6 месеца, след което е необходимо внасянето им чрез храните, използвани за захранване на кърмачето. Потребностите от желязо са относително по-високи
установяваният
на цинк се проявява с
линеарния растеж, нарушения в имунния отговор и повишен риск от инфекции.
ВИТАМИНИ
Витамин Д има основна роля за усвояване на калция и отлагането му в костите, но и участва в разнообразни процеси в клетъчния метаболизъм. Кърмата е недостатъчен източник
на вит. Д, което налага прилагане на добавка от витамин Д за всички кърмачета за осигуряване на достатъчен прием – профилактична доза от 600 IU за всички здрави деца. Дефицит на витамин К може да бъде причина
лекули, които играят разнопосочни роли в
организма – защита срещу инфекции и въз -
паление, съзряване на имунната система, развитие на тъкани и органи, бактериална колонизация. Кърмата е динамична, биоак-
тивна течност, като съставът ѝ се променя от
коластра до зряло мляко и варира между отделните хранения. Съдържа специфични и
неспецифични имунни фактори, които под-
държат незрялата имунна система на новороденото. Към антибактериалните фактори в
кърмата се отнасят:
• Секреторни IgA – насочени към специфични антигени
• Лактоферин – имуномодулация, свързване на желязо, антимикробно и антиадхезивно действие, роля за интестиналния растеж
• К-Казеин – антиадхезивен ефект, роля за бактериалната флора
• Олигозахариди – предотвратяване на прикрепването на бактерии
• Цитокини – противовъзпалителен ефект, бариерна функция на епитела
Растежните фактори включват епидермален растежен фактор, трансформиращ растежен фактор, фактори, промотиращи нервния растеж. Нуклеотидите имат положителен ефект върху имунните функции.
Предимствата на кърменето се отнасят както за детето, така и за майката. Кърмата оси -
гурява необходимата енергия за растеж и
развитие през първите месеци от живота. Макронутриентите са в оптимално съдържа -
ние и балансирано съотношение, лесно ус -
воими са и в биодостъпна форма. Съдър -
жанието на протеини е относително ниско, осигурява 6-7% енергията, като това съответства на ензимната активност на храносмила -
телната система на детето и осигурява есенциални аминокиселини. Аминокиселините таурин и цистин са в по-високи концентрации и са есенциални
ниски нива на лактоза. След 4-6-ти ден се отделя преходното мляко, като образуването на зрялата кърма започва след втората седмица.
Препоръките на СЗО включват естестве

В редки случаи кърменето е проти -
вопоказано. Такива състояния включ -
ват инфекция с HIV, като препоръките
варират в различните страни, активна туберкулозна инфекция, инфекция с Варицела зостер или HSV, ако има риск от директен контакт със засегнатия кожен участък, химиотерапия, редки генетични заболявания при детето (фенилкетонурия, левциноза и др.).
Ако няма възможност на кърмачето да се осигури кърма, то се храни с млека за кърмачета. Напредването на индустрията, както и силната
конкуренция между отделните производители допринася за качест-
чете физиологичното съзряване
бъбречната
гастроинтестиналната функция, необходими за метаболизиране на немлечни продукти, за безопасно и ефективно усвояване на различни храни. Понастоящем се приема за препоръчително захранването да започне около 6-ти месец, но не по-рано 17-та седмица (навършени 4 месеца, начало на 5-ти месец) и не по-късно от 26-та седмица (навършени 6 месеца, начало на 7-ми месец). Лекарят или медицинският специалист препоръчва захранване на кърмачето с подходящи по състав и начин на приготвяне храни, различни от млякото, като се съобразява със състоянието на
хранени с млека за
кърмачета. Към много от млеката се
добавят ARA и DHA, които не се уста -
новяват в кравето мляко. Приготвя -
нето на млека за кърмачета изисква
спазване на отлична хигиена за ми -
нимализиране на риска от инфекции, внесени с храната. Необходимо е и стриктно спазване на указанията
на избутване на храната с език и да може да преглъща храната, както и да е напълно здраво. При деца, които се кърмят, кърменето продължава през целия период на въвеждане на храни, допълващи кърмата, за оптимален растеж и развитие на детето. Захранването се започва със зеленчуково пюре или обогатена с желязо каша, като постепенно се въвеждат различните групи храни.
1.Nelson’s Textbook of Pediatrics
2. Krause’s Food and Nutrition Therapy
3. World Health Organization, Infant and young child feeding, Feb.2018
4. World Health Organization, UNICEF, Global strategy of infant and young children feeding, Geneva, WHO, 2003.
5. Complementary Feeding - A Position Paper by the European Society for Paediatric Gastroenterology, Hepatology, and Nutrition (ESPGHAN) Committee on Nutrition
6. Review of Infant Feeding: Key Features of Breast Milk and Infant Formula /https://www.mdpi.com/2072-6643/8/5/279/htm/
7.Human Milk Composition: Nutrients and Bioactive Factors Olivia Ballard, JD, PhD (candidate) and Ardythe L. Morrow, PhD, MSc https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3586783/
8.

М. Лилова, Д. Райков, Р. Цонев, д.м., П. Карагьозов, д.м., FASGE
УМБАЛ „Аджибадем Сити Клиник Болница Токуда“ - София
Clostridioides difficile. Clostridioides
ПСЕВДОМЕМБРАНОЗЕН КОЛИТ
(ПМК)
Псевдомембранозният колит представлява тежко възпалително заболяване на дебелото черво, което се характеризира с наличието на фибринозно-гнойни налепи (псевдомембрани) върху увредената лигавица и се съпровожда от диария, абдоминална болка и общо влошаване на състоянието. Етиологичният причинител е Clostridioides difficile - анаеробна, грам-положителна, спорообразуваща пръчица, изолирана
за първи път през 1935 г., но чак през 1978 г. е утвърдена като причинител
на антибиотик-асоциирания колит[1]
тота, поради разпространението на хипервирулентни щамове и широкото използване
Честотата на колонизация
ция зависи от възрастта
инфек
състоянието на пациента. При здрави кърмачета се наблюдава носителство до 80%, докато при здрави възрастни то варира между
цията,
състояния[10,11]. Те се срещат при 20-25% от па
циентите
клинично рецидивиращата инфекция се определя като поява на симптоматична диария и/или коремна болка с положителен фекален тест в рамките на 56 дни от предишния епизод. Епизодите, възникнали след 56 дни, вероятно се дължат на реинфекция. За да се разграничи истинската рецидивираща инфекция от реинфекцията обаче, е необходим генотипен анализ. КЛИНИКО-ЛАБОРАТОРНА ДИАГНОЗА Clostridioides difficile може да предизвика широк спектър от клинични състояния – от асимптоматично носителство до лека или тежка диария, с фулминантен колит и токсичен мегаколон. Тежките форми се срещат при 3-5% от симптоматичните пациенти. Диагнозата клинично се поставя при наличие на три или повече течни изхождания (+/- слуз и/или кръв) за 24 часа в продължение на поне два последователни дни, в съчетание с положителен тест за токсини, болка в долната част на корема и допълнителни симптоми като гадене, липса на апетит и обща отпадналост
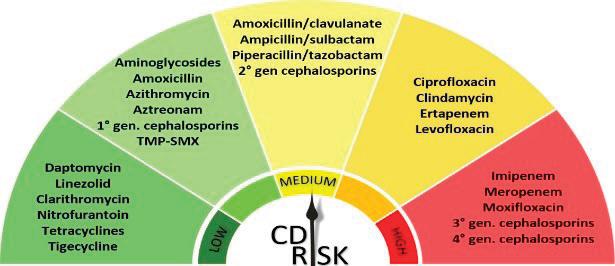
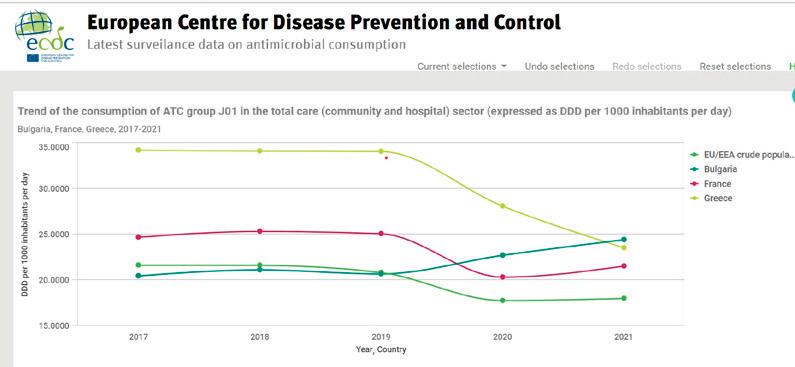
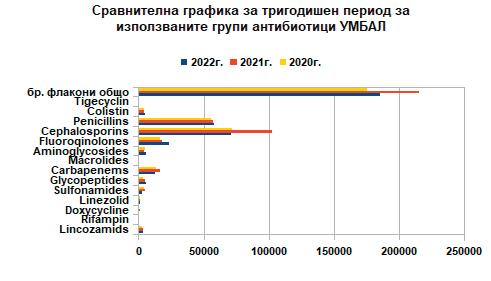
Infectious Diseases Society of America (IDSA)
Society for Healthcare Epidemiology of America (SHEA),
European Society of Clinical Microbiology and Infectious Diseases (ESCMID).
акцент върху клиничната приложи -
мост.
Съгласно критериите на IDSA/SHEA[27]
за тежка форма се приема левкоци -
тоза ≥15 000 клетки на микролитър
и/или повишение на серумния кре -
атинин с 1.5 пъти спрямо изходното ниво. Тежко усложнена инфекция се характеризира с наличие на хипото -
ния, сепсис, илеус, токсичен мегаколон, перфорация или летален изход, свързан с инфекцията. ESCMID подчертава важността на клиниката и образната диагностика.
Диагностичният алгоритъм включва комбинация от тестове за глута -
мат
дехидрогеназа (GDH) и токсин
A/B. При отрицателен резултат за
GDH и токсини, активна инфекция се
изключва. При положителен резул -
тат за GDH и отрицателен за токси -
ни се приема, че пациентът е коло -
низиран, без продукция на токсини
следователно не се препоръчва те -
рапия, освен ако няма клинични по -
дозрения[12]. При положителен резул -
тат за GDH и токсини се потвърждава
активна токсин-продуцираща инфек-
ция, изискваща терапевтично поведение (Фиг. 5).
ЛЕЧЕНИЕ
Различията в международните ръко -
водства, издадени от IDSA/SHEA, както и от ESCMID, поставят въпроса за създаването на единен подход в лечението при пациентите[20, 21]. С настоящият обзор имаме за цел да представим и сравним препоръките на IDSA/SHEA и ESCMID относно диагностиката, лечението и проследяването на Clostridioides difficile инфекция, като предложим практическа интерпретация на терапевтичните опции
алгоритми, базирана на предложените дози, продължителност на лечението и индикации за инвазивни интервенции (Фиг. 6).
При лек до умерен първи епизод, ESCMID препоръчва лечение с метронидазол[21], докато при IDSA/SHEA Фидаксомицин или Ванкомицин са предпочитани медикаменти[17,18,20]. И двете дружества признават Фидаксомицин като терапия от първи избор при налична възможност, поради доказано по-нисък риск от рецидив.
При тежък и тежко-усложнен епизод на първа линия се препоръчват Фидаксомицин и Ванкомицин и от двете ръководства[20,21]. От своя страна при фулминантен епизод стандартното лечение включва перорален Ванкомицин четири пъти дневно, в комбинация с венозен Метронидазол три пъти дневно[20]. При паралитичен илеус се обсъжда ректално
приложение на Ванкомицин[13,14,18].
ESCMID допуска използване на Фидаксомицин при противопоказания за приложение на Метронидазол[21]
И двете ръководства посочват ранна хирургична оценка при липса на подобрение до четиридесет и осем часа от началото на терапията[20]
При първи рецидив се прилага Фидаксомицин или Ванкомицин по схема[20,21]. При последващи рецидиви се разглежда терапия с Фидаксомицин, фекална микробиотна трансплантация или в крайните случаи –хирургична интервенция. Фекалната трансплантация
достъпа до оптимално лечение.
В ДОПЪЛНЕНИЕ КЪМ СПЕЦИФИЧНАТА АНТИБИОТИЧНА ТЕРАПИЯ СЕ ПРЕПОРЪЧВА:
• Прекъсване на налична не-CDI антибиотична терапия при възможност.
• Адекватно водно-електролитно заместване.
• Избягване на препарати за потискане на перисталтиката.
• Преоценка необходимостта от прилагане на инхибитори на протонната помпа.
ПРОСЛЕДЯВАНЕ
Clostridiodes
GDH (-) Toxin (-)
Първи епизод: лек до тежък (Т<38.50С, коремен дискомфорт, >3 дефекации/ден) (WBC ≤15 000 cells/µL, серумен Cr <1.5 mg/dL)
Първи епизод: тежък-усложнен (WBC ≥15 000 cells/µL, серумен Cr >1.5 mg/dL)
(Т>38.50С, коремна болка, кървава диария, хипоалбуминемия)
IDSA/SHEA 2021
Фидаксомицин 200 мг 2х1 т. за
10 дни
Или
Ванкомицин 125 мг 4х1 т. п.о. за 10 дни
Или
Метронидазол 500 мг 3х1 т. за 1014 дни
Фидаксомицин 200 мг 2х1 т. за 10
дни или 2х1 т. за 5 дни, след което х 1 т. за 20 дни
Или
Ванкомицин 125 мг 4х1 т. п.о. за 10 дни, 2х1 т. за 7 дни, х 1 т. за 7 дни, на всеки 2-3 дена за 2-8 сед. Или Bezlotoxumab 10 mg/kg i.v.
ESCMID 2021
Фидаксомицин 200 мг 2х1 т. за
10 дни Или
Ванкомицин 125 мг 4х1 т. п.о. за 10 дни
Или
Метронидазол 500 мг 3х1 т. за 8-10 дни
200 мг 2х1 т. за 10 дни Или
Ванкомицин 125 мг 4х1 т. п.о. за 10 дни Фулминантен (хипотония, шок, илеус или токсичен мегаколонм + ↑серумен лактат) Първи фулминантен повторен
на Clostridium difficile при възрастни
Първи епизод, лек до тежък
Първи епизод, тежко-усложнен
Първи епизод, фулминантен
Препоръчително лечение за България
Метронидазол 500 mg, 3 пъти дневно п.о., в продължение на 10-14 дни Или
Ванкомицин 125 mg, п.о., 4 пъти дневно, в продължение на 10-14 дни
Ванкомицин 125 mg, п.о., 4 пъти дневно, в продължение на 10-14 дни Или
Фидаксомицин 200 mg, п.о., 2 пъти дневно, в продължение на 10-14 дни
Ванкомицин 125 mg, п.о., 4 пъти дневно, в продължение на 14 дни И
Метронидазол 500 mg, 3 пъти дневно и.в., в продължение на 14 дни Или
Фидаксомицин 200 mg, п.о., 2 пъти дневно, в продължение на 14 дни
Ванкомицин 125 mg, перорално, 4 пъти дневно в продължение на 10-14 дни, след което 2 пъти дневно за 7 дни, веднъж дневно
Първи рецидив
отичен микс, съдържащ Lactobacillus spp., Bifidobacterium spp., Bacillus coagulans и Saccharomyces boulardii. Това рандомизирано, двойно-сляпо, плацебо-контролирано, фаза IV проучване, проведено в 63 амбулаторни практики в България, демонстрира значимо намаление на честотата на ААД при възрастни пациенти, приемащи широкоспектърни антибиотици – от 25.3% в плацебо групата до 9.2% в пробиотичната група. Относителният риск беше редуциран с 64%, а необходимият брой пациенти за лечение (NNT) за предотвратяване на един случай на ААД е едва шест.
Тези резултати подчертават потенциала на пробиотичната
Ефективното
затруднено поради ограничен достъп до основни терапевтични средства.
Настоящият консенсус подчертава необходимостта
1. Bartlett JG. Historical perspectives on studies of Clostridium difficile and C. difficile infection. Clin Infect Dis. 2008;46(S1):S4–S11.
2. Lessa FC, et al. Burden of Clostridium difficile infection in the United States. N Engl J Med. 2015;372(9):825–834.
3. Carter GP, et al. The role of TcdB in Clostridium difficile infection. Nat Microbiol. 2015;1:15009.
4. Gerding DN, et al. Clinical and microbiologic aspects of Clostridium difficile infection. Clin Microbiol Rev. 2014;27(4):529–550.
5. Buffie CG, Pamer EG. Microbiotamediated colonization resistance against intestinal pathogens. Nat Rev Immunol. 2013;13(11):790–801.
6. Kim KH, et al. Epidemiology and outcomes associated with community-acquired Clostridium difficile infection. JAMA. 2012;307(13):1399–1405.
7. Jump RLP, et al. Clostridium difficile in the long-term care facility: prevention and management. Curr Geriatr Rep. 2014;3(1):60–69.
8. McDonald LC, et al. Clinical practice guidelines for Clostridium difficile infection in adults and children: 2017 Update by IDSA and SHEA. Clin Infect Dis. 2018;66(7):987–994.
9. Leffler DA, Lamont JT. Clostridium difficile infection. N Engl J Med. 2015;372(16):1539–1548.
10. Johnson S. Recurrent Clostridium difficile infection: causality and therapeutic approaches. Int J Antimicrob Agents. 2009;33(S1):S33–S36.
11. Abou Chakra CN, et al. Risk factors for recurrence, complications and mortality in Clostridium difficile infection: a systematic review. PLoS One. 2014;9(6):e98400.
12. Crobach MJT, et al. European Society of Clinical Microbiology and Infectious Diseases: update of the diagnostic guidance document for Clostridium difficile infection. Clin Microbiol Infect. 2016;22:S63–S81.
13. Gerding DN, et al. Treatment of Clostridium difficile infection. Clin Infect Dis. 2008;46(S1):S32–S42.
14. Kelly CR, et al. Fecal microbiota transplantation for recurrent Clostridium
difficile infection in clinical practice. Clin Gastroenterol Hepatol. 2012;10(11):1185–1192.
15. McFarland LV. Surprising results for vancomycin in the treatment of Clostridium difficile infection: meta-analysis. Am J Gastroenterol. 2007;102(8):1789–1797.
16. Weber DJ, et al. Role of the environment in the transmission of Clostridium difficile in health care facilities. Am J Infect Control. 2010;38(1):S25–S33.
17. Wilcox MH, et al. Bezlotoxumab for prevention of recurrent Clostridium difficile infection. N Engl J Med. 2017;376(4):305–317.
18. McDonald LC, Gerding DN, Johnson S, et al. Clinical Practice Guidelines for Clostridioides difficile Infection in Adults and Children: 2021 Update by the IDSA and SHEA. Clin Infect Dis. 2021;73(5):e1029–e1044.
19. Kelly CP, LaMont JT. Clostridium difficile — more difficult than ever. N Engl J Med. 2008;359:1932–1940.
20. Johnson S, Lavergne V, Skinner AM, Gonzales-Luna AJ, Garey KW, Kelly CP, et al. Clinical Practice Guideline by the Infectious Diseases Society of America and Society for
Healthcare Epidemiology of America: 2021 Focused Update Guidelines on Management of Clostridioides difficile Infection in Adults. Clinical Infectious Diseases. 2021;73(5):e1029–e1044
21. Debast SB, Bauer MP, Kuijper EJ. European Society of Clinical Microbiology and Infectious Diseases: Update of the Treatment Guidance Document for Clostridium difficile Infection. Clinical Microbiology and Infection. 2021;27(Suppl 2):S1–S21
22. Cammarota G, Ianiro G, Kelly CR, et al. International Consensus Conference on Stool Banking for Fecal Microbiota Transplantation in Clinical Practice. Gut. 2019;68(12):2111–2121
23. Bartlett JG. Clinical practice. Antibioticassociated diarrhea. N Engl J Med. 2002;346(5):334–9.
24. Baur D, Gladstone BP, Burkert F, et al. Effect of antibiotic stewardship on the incidence of infection and colonisation with antibioticresistant bacteria and Clostridium difficile: a systematic review and meta-analysis. Lancet Infect Dis. 2017;17(9):990–1001.
25. Siegel JD, Rhinehart E, Jackson M, Chiarello L. Management of multidrug-resistant organisms in healthcare settings, 2006. Am J Infect Control. 2007;35(10 Suppl 2):S165–93.
26. Gerding DN, Johnson S, Peterson LR, et al. Clostridium difficile-associated diarrhea and colitis. Infect Control Hosp Epidemiol. 1995;16(8):459–77.
27. Bishop EJ, Tiruvoipati R. Management of Clostridioides difficile infection in adults and challenges in clinical practice: review and comparison of current IDSA/SHEA, ESCMID and ASID guidelines. Therap Adv Infect Dis. 2019.
28. Vladimir Hodzhev, Karen Dzhambazov, Nikolay Sapundziev, Milena Encheva, Spiridon Todorov, Vania Youroukova, Rumen Benchev,Rosen Nikolov, Boris Bogov, Georgi Momekov, and Veselin Hadjiev. Highdose Probiotic Mix of Lactobacillus spp., Bifidobacterium spp., Bacillus coagulans, and Saccharomyces boulardii to Prevent Antibiotic-associated Diarrhea in Adults: A Multicenter, Randomized, Double-blind, Placebo-controlled Trial (SPAADA). 2024.
В. Жеков, П. Карагьозов, д.м., FASGE
УМБАЛ „Аджибадем
Сити Клиник Болница Токуда“ - София
ОКГГИГ в зависимост от интензитета
на кръвозагубата може да варира от
безсимптомно състояние до хиповолемичен шок и смърт. Развитието на
анемия поставя в риск здравословното състояние на пациентите, пора -
ди намаляването на капацитета на
кръвта да пренася кислород към периферните тъкани. В резултат на това
те могат да изпаднат в хипоксия. Тъй като при нормални обстоятелства
кислорода в циркулиращата кръв е свързан предимно с хемоглобина (Хб), основен подход за коригиране на настъпилите
което доминира в продължение на десетилетия в хемотрансфузионната терапия. Според него кръвопреливането трябва да започне, когато хемоглобинът на пациента спадне под 100 g/L Хб и/или хематокритът се понижи под 30[1] . През последните няколко десетилетия, обаче, тази ясна и лесна
между 100-120 g/L. Получените резултати по -
казват не само, че рестриктивната стратегия за кръвопреливане е безопасна за пациенти в интензивно отделение, а и че либералната трансфузионна стратегия повишава риска от смърт.
Посоченото по-горе изследване дава начало на дебат, който продължава и до днес, относно ефективността и безопасността на двете стратегии като цяло и специфично за различните нозологични единици.
Тъй като ОКГГИТ е една от честите причини, налагащи кръвопреливане, постепенно за -
До края на първото десетилетие на XXI век са налице само малки обсервационни или контролирани проучвания, които предполагат, че хемотрансфузията може да оказва неблагоприятни въздействия при пациенти с хиповолемична анемия в резултат на ОКГГИТ[3,16]
През 2013 г. Villanueva еt al.[15] провежда първото добре структурирано и широко цитирано рандомизирано проучване, касаещо проблемите на кръвопреливането при ОКГГИТ. То включва 921 участници, разпределени на случаен принцип в две групи. Пациентите, кръвопреливани според рестрик -

нивото му след трансфузия
от 90 до 110 g/L. Получените резултати сочат, че при пациенти с ОКГГИТ е безопасно и ефективно да се пристъпи към кръвопре -
ливане едва когато стойностите на хемоглобина спаднат под 70 g/L.
Последващи проучвания на Jairath еt al.
2015[9] и Kola et al. от 2021 г.[10] не откриват ка -
тегорични доказателства в подкрепа на изводите от изследването на Villanueva еt al.
Мета-анализите на натрупаните данни по този проблем също не успяват да изяснят
това противоречие.
През 2017 г. Odutayo et al.[13] публикуват проучването, включващо четири публикувани
едно непубликувано рандомизирано контролирано проучване с общо 1965 участници. Из -
водът от него е, че рестриктивната трансфузионна стратегия при пациенти с
торното кървене. Уточнява се, че при паци -
енти с ИБС или тежък кръвоизлив, рестриктивната стратегия не трябва да се прилага по
подразбиране, а решенията за кръвопрели -
ване трябва да се основават на клинична преценка и индивидуален риск.
През 2023 г. Teutsch et al.[14] публикуват друг мета-анализ, резултатите от който в голяма
степен влизат в противоречие с по-горе цитираното изследване. То включва седем рандо
1. Adam RC LJ. Anesthesia in cases of poor risk. Some suggestions for decreasing the risk. Surg Gynecol Obstet. 1942: 74: 1011–1101.
2. Antunes C CIE. Upper Gastrointestinal Bleeding. [Updated 2023 Apr 7]. 2024.
3. Blair SD JSMCGR. Effect of early blood transfusion on gastrointestinal haemorrhage.. Br J Surg. 1986:73(10):783785.
4. Сonference. C. Perioperative red blood cell transfusion. Paper presented at: JAMA, 1988; 260(18):2700-2703.
7. Gralnek IM SAMAea. Endoscopic diagnosis and management of nonvariceal upper gastrointestinal hemorrhage (NVUGIH): European Society of Gastrointestinal Endoscopy (ESGE) Guideline - Update 2021. Endoscopy. 2012:53(3):300-332.
8. Hébert PC WGBMea. A multicenter, randomized, controlled clinical trial of transfusion requirements in critical care.
5. Gralnek IM CDMGPJea. Endoscopic diagnosis and management of esophagogastric variceal hemorrhage: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy. 2022:54(11):1094-1120. 6. Gralnek IM,NZ&SLL. Acute lower gastrointestinal bleeding. N. Engl. J. Med. 2017: 376,1054–1063.
Transfusion Requirements in Critical Care Investigators, Canadian Critical Care Trials Group. N Engl J Med. 1999:340(6):409-417.
9. Jairath V KBGAea. Restrictive versus liberal blood transfusion for acute upper gastrointestinal bleeding (TRIGGER): a pragmatic, open-label, cluster randomised feasibility trial.. Lancet. 2015:386(9989):137-144..
10. Kola G SSMSSGKV. Restrictive versus liberal transfusion strategy in upper gastrointestinal bleeding: A randomized controlled trial. Saudi J Gastroenterol. 2021:27(1):13-19.
11. Laine L. Upper gastrointestinal bleeding due to a peptic ulcer. N. Engl. J. Med.
2016:374, 2367–2376.
12. Laine L BASJMMLG. ACG Clinical Guideline: Upper Gastrointestinal and Ulcer Bleeding. Am J Gastroenterol. 2021:116(5):899-917.
13. Odutayo A DMTMea. Restrictive versus liberal blood transfusion for gastrointestinal bleeding: a systematic review and meta-analysis of randomised controlled trials. Lancet Gastroenterol Hepatol. 2017:2(5):354-360.
14. Teutsch B VDPDSOHMBEB. Potential benefits of restrictive transfusion in upper gastrointestinal bleeding: a systematic review and meta-analysis of randomised controlled trials. Sci Rep.. 2023:13(1):17301.
15. Villanueva C CABAea. Transfusion strategies for acute upper gastrointestinal bleeding. N Engl J Med. 2013:368(1):11-21.
16. Villarejo F RMLEDGAGAC. Anemia aguda en la hemorragia digestiva alta. Márgenes de seguridad para su manejo sin transfusiones de glóbulos rojos [Acute anemia in high digestive hemorrhage. Margins of security for their handling without transfusion of red globules]. Acta Gastroenterol Latinoam. 1999:29(4):261270.
17. Wang JK KH. Red blood cell transfusion in the treatment and management of anaemia: the search for the elusive transfusion trigger. Vox Sang. 2010:98(1):2-11.
¹Втора гинекологична клиника, СБАЛАГ „Майчин дом“ - София
²НЦЗПБ - София
³Медицински факултет, МУ - София
⁴Клиника по оперативна гинекология, УМБАЛСП „Пирогов“ - София ⁵Катедра по Медицинска генетика, МУ - София ⁶Клиника по нервни болести, УМБАЛСП „Пирогов“ - София
7Медицински факултет, СУ - София
ВЪВЕДЕНИЕ Атопичните заболявания са сред во -
дещите хронични патологии с нача -
ло в детска възраст. Имуноглобулин Е (IgE) играе централна роля в па -
тогенезата на атопичните реакции, участвайки в активацията на мастоцити и базофили. Данни показват, че
предразположението към алергии може да се формира още по време на вътреутробното развитие, а майчиният IgE профил може да окаже
влияние върху имунната система на плода[1-3]
ЛИТЕРАТУРЕН ОБЗОР Атопичните заболявания се увеличават значително през последните десетилетия, като склонността към повишена продукция на IgE – ключов медиатор в алергичния процес – често се проявява още
стойност за оценка на риска от атопия при новороденото[1,8]. Деца, родени от майки с повишен IgE, показват по-високи нива на еозинофилия, дерматит и положителни кожни проби още през първата година от живота си[6,10]
Дълго време се е приемало, че IgE – поради молекулното си тегло – не преминава плацентарната бариера. Съвременните данни обаче посочват, че FcRn рецепторът, отговорен за трансфера на IgG, може да пренесе имунни комплекси от IgG и IgE, което създава възможност
от развитие на атопичен дерматит при новородените [14]. Този риск допълнително се засилва от психо-социални фактори, като стрес, замърсяване, сезон на раждане и тютюнопушене,
. Тези открития подкрепят идеята, че ранното измерване
МАТЕРИАЛИ И МЕТОДИ
Изследвахме 29 бременни жени. На всяка
една беше снета подробна акушерска, фамилна и лична анамнеза. Попълнен беше
подробен алергологичен въпросник.
Критерии за включване: ехографски потвърдена бременност. Критерии за изключване: придружаващи автоимунни, ендокринни или хронични инфекциозни заболявания.
Пациентките бяха разделени в две групи: ● Група А – с анамнеза за алергични заболявания (n = 13)
● Група В – без анамнеза за алергии (n = 16)
Кръвни проби от майките и новородените са анализирани за наличие на специфични IgE антитела чрез имуноблотен метод с Euroimmune® EUROLINE Atopy screen (54 алергена). Използван е полуколичествен in vitro
анализ за определяне на сенсибилизация при
класовете 0–6.
РЕЗУЛТАТИ
Средната възраст на изследваната група пациентките е 32.1 г. Средният ръст на паци -
ентките, включени в изследването е 165.25 см. Индексът на телесната маса (ИТМ) е 28.79 кг/м².
От параклиничните показатели се установиха средни стойности на хемоглобина 120 g/L при изследваните бременни жени.
ПРИ АНАЛИЗ НА ПОЛУЧЕНИТЕ ДАННИ
ЗА ОЦЕНКА НА СЕНСИБИЛИЗАЦИЯТА СЕ УСТАНОВИХА СЛЕДНИТЕ ДАННИ: Най-чести алергени с повишени стойности на sIgE са Dermatophagoides pteronyssinus, Betula verrucosa (бреза) и Secale cereale (културна ръж).
Класове на sIgE (по EUROLINE):
1. Apostolovic, Danijela, et al. "The Role of Maternal Immunoglobulin E in Fetal Sensitization and Allergy Development." Journal of Clinical Investigation, vol. 130, no. 3, 2020, pp. 1203–1215.
2. Berin, M. Cecilia, et al. "IgE-Allergen Immune Complexes and Transplacental Transfer in Fetal Sensitization." Pediatric Allergy and Immunology, vol. 34, no. 1, 2023.
3. Bundhoo A, et al. "Evidence that FcRn Mediates the Transplacental Passage of Maternal IgE in the Form of IgG Anti-IgE/
IgE Immune Complexes." Clinical and Experimental Allergy, 2015.
4. Herberth, Gerd, et al. "Influence of Maternal Stress and Pollutants on Fetal Immune Profile and Allergy Risk." Clinical Immunology, vol. 145, no. 1, 2022.
5. Hochwallner H, et al. "Mechanisms and Risk Factors for Perinatal Allergic Disease." Clinical and Experimental Allergy, 2024.
6. Kim, Jong S., et al. "Maternal Allergy and Risk of Atopic Dermatitis in the Offspring." Allergy, vol. 76, no. 11, 2021.
● Клас 0: <0.35 kU/L – без сенсибилизация ● Клас 1–2: лека сенсибилизация ● Клас ≥3: клинично значима сенсибилизация
Повечето майки с анамнеза за алергии показват стойности ≥ клас 2 към поне един инхалаторен алерген. Новородените остават основно в клас 0–1.
ДИСКУСИЯ Резултатите потвърждават, че бременните жени с анамнеза за алергии имат по-висо -
нива на специфичен IgE, включително към хранителни и инхалаторни алергени. Данните
подкрепят хипотезата, че майчиният IgE профил може да служи като прогностичен маркер за алергичен риск при потомството[4,5] Теоретично, трансферът на IgE през плацентата дълго време се смяташе за невъзможен, но последни данни показват, че това е осъществимо чрез IgE-IgG имунни комплекси, преносими чрез FcRn рецептори[1]. Друг меха -
низъм е преносът чрез амниотична течност, където феталният ГИ тракт може да абсорбира IgE[2].
Фактори като тютюнопушене, медикаменти и сезон на раждане също модулират риска[3].
ЗАКЛЮЧЕНИЕ
Майчиният алергичен статус и серумните IgE
нива са съществени предиктори за алергична сенсибилизация при новороденото. Ранното откриване на повишен IgE и събирането на анамнеза при бременната могат да подпомогнат стратификацията на риска и индивидуализираната постнатална превенция. Финансиране: Настоящото проучване е финансирано от проект по договор № Д-201/03.08.2023 г. с вх.№ 8269/23.11.2022 г. от конкурса „ГРАНТ - 2023” на МУ - София
7. Kraus TA, et al. "IgE Is Expressed on, but Not Produced by, Fetal Cells in the Human Placenta." Clinical and Experimental Allergy, vol. 33, no. 6, 2003, pp. 743–749.
8. Liu T, et al. "Differences in Total and Allergen-Specific IgE During Pregnancy and Their Correlation with Infant IgE." Allergy Asthma Clinical Immunology, 2014.
9. Martino, David J., et al. "Prenatal IgE and Cytokine Milieu: Fetal Programming of Allergic Disease." Frontiers in Immunology, vol. 9, 2018.
10. Msallam R, et al. "Fetal Mast Cells Mediate Postnatal Allergic Responses Dependent on Maternal IgE." Science, vol. 370, no. 6515, 2020, pp. 941–950.
11. Paveglio S, et al. "Evidence that FcRn Mediates the Transplacental Passage of Maternal IgE." Clinical and Experimental Allergy, 2015.
12. Riedler J, et al. "Atopy Risk Among School-Aged Children in Relation to Early Life Farm Exposures: A Systematic Review." Pediatric Allergy and Immunology, 2021.
15. Wright RJ, Bosquet Enlow M. "Maternal Stress and Perinatal Programming in the Expression of Atopy." Expert Review of Clinical Immunology, vol. 4, no. 5, 2008, pp. 759–772.
13. Simon D, et al. "Maternal IgE Influence on Fetal and Infant Health." Immunology Reviews, 2025. Wang Y, et al. "Effects of TMEM232 Variant on Infant Atopic Dermatitis According to Maternal 14. Factors." Genes (Basel), vol. 15, no. 11, 2024, article 1446.
естроген зависими гинекологични заболявания
М. Кръстева1, В. Карамишева2 , М. Владимиров
Спасова5 , Н. Христов 6
1Катедра по акушерство и гинекология,
2Клиника по обща и урогинекология, СБАЛАГ „Майчин дом“ - София
3Медицински факултет, МУ - София
4Клиника по оперативна гинекология, УМБАЛСП „Пирогов“ - София
5Катедра по Медицинска генетика, МУ - София
ВЪВЕДЕНИЕ
Естроген-зависимите гинекологич -
ни заболявания включват патологич -
ни състояния, чиито растеж и раз -
витие са тясно свързани с ефектите на естрогените. Миомата на матката (лейомиома), ендометриалният
карцином (предимно ендометриоидният тип) и ендометриалните по -
6Клиника по нервни болести , УМБАЛСП „Пирогов - София на естрогенните рецептори, метаболизма на естрогените, генетичните фактори (MED12, PTEN, ESR1, COMT), епигенетичните изменения, както и основните епидемиологични и клинични рискови фактори, свързани с миомата на матката, ендометриалния карцином и ендометриалните полипи.
липи са ключови примери за такива заболявания. Тези състояния, макар
и различаващи се по своя характер – от доброкачествени тумори (миоми, полипи) до злокачествени неоплазми (карцином) – споделят общо етиопатогенетично звено: стимулиращото действие на естрогените
МИОМА НА МАТКАТА (ЛЕЙОМИОМА) Миомата на матката е най-чести
стимулация[12]. Смята се, че естрогенът засилва ефектите на прогестерона в миомните клетки и по този начин подпомага клетъчната пролиферация и потиска апоптозата, докато прогестеронът директно стимулира растежа на миоматозната тъкан – комбинация,
ви изменения в екзон 2 на гена, са открити в различни популации и се приемат за универсален молекулен драйвер на голяма част от миомите[18]. Функционално, мутантният MED12 нарушава медиаторния комплекс на транскрипцията и влияе върху сигнални пътища като Wnt/β-катенин, което може да доведе до аберантна пролиферация на гладкомускулните клетки. В миоми с MED12 мутация са наблюдавани характерни фенотипни осо -
бености – обикновено са по-малки по размер и множествени, с по-изразено отлагане на колаген (екстрацелуларен матрикс) и на -
личие на тумор-асоциирани фибробласти[18]
За разлика от тях, около 30% от миомите са
MED12-негативни – те често се дължат на
други молекулни механизми. В тази група спадат миоми с хромозомни пренарежда -
ния и свръхекспресия на HMGA2 (в резултат на транслокации на 12q14–15) и редки случаи с бивалентни мутации в гена на фумарат-хи -
дратазата (FH)[3]. Смята се, че има поне четири основни драйвърни мутaции при лейомиомите – мутации в MED12, увличане на HMGA2, мутации във VOC и в COL4A5/COL4A6 – които дефинират молекулярно различни подтипове тумори[18]. Общото между тях обаче е зависимостта от половите стероиди: почти всички миоми, независимо от драйвъра си, експресират ERα/ERβ и PR и растежът им се стимулира от естрогенови сигнали[18]
ЕПИГЕНЕТИЧНИ ФАКТОРИ Все по-голямо внимание се обръща на епигенетичните изменения при миомите като ключ към тяхната патогенеза. Геномни проучвания показват, че профилът на ДНК метилиране на миоматозна тъкан се различава значимо от този на нормалния миометриум. Различни гени са хипо- или хиперметилирани в туморите, което променя експресията им и потенциално допринася за туморогенезата. Например, установено е, че в подгрупата MED12-негативни миоми често се наблюдава хипометилиране и свръхекспресия на онкогена HMGA2, което се свързва с развитието на единични, по-големи
например
на miR21, miR-200c, miR-29 и др. в миоматозната тъкан влияе върху гените на апоптозата и извънклетъчния матрикс (TGF-β, ACVR1 и др.), подпомагайки туморния растеж[3]. В допълнение, външни фактори като ендокринни дизруптори (напр. фталати, бисфенол), към които организмът е изложен във вътреутробното развитие или ранната детска възраст, може да "програмират" миометриалните стволови
клетки чрез епигенетични промени (напри -
мер ДНК метилиране), създавайки податливост за по-късно туморообразуване[18]. Тази
концепция за двоен "hit" – ранно епигенетично препрограмиране, последвано от придобита соматична мутация в зряла възраст
нараства през късните репродуктивни години (най-често 35-50 г.), като към 50-годишна възраст до 70-80% от жените имат поне една миома[18]. Расата също е мощен фактор – жените от афроамерикански произход имат 2-3 пъти по-висока честота на миоми в сравнение с европеидната раса[18]. Този диспаритет може да се дължи отчасти на по-високи нива на половите хормони при афроамериканки, както и на генетични вариации; например, полиморфизми в гена за катехол-О-метилтрансфераза (COMT) са проучвани като потенциално обяс -
нение за по-честата поява на миоми при различни етноси[18]. COMT е ключов ензим в метаболизма на естрогените (метилиране на катехол-естрогените); нискоактивният вариант (Val158Met, Met алел) води до натрупване на 4- и 2-хидрокси-естрагени, които могат да увредят ДНК. Някои изследвания установяват, че жени с COMT полиморфизъм имат
вероятност за миоми, вероятно поради периодите на аменорея и прогестероново доминиране по време на бременност, които намаляват нетната естрогенна експозиция. Затлъстяването умерено повишава риска, тъй като адипозната тъкан произвежда естрогени (чрез ароматазата) – установено е, че жени с индекс на телесна маса (ИТМ) >30 имат по-висока вероятност за миоми в сравнение с слабите[15]. Освен това, дефицитът
на витамин D – по-чест при хора
с по-тъмна кожа – се асоциира с миомна болест; витамин D притежа -
ва антипролиферативни ефекти вър -
ху
миомни клетки и недостатъчните му нива може да позволят по-свобо -
ден растеж на туморите[1]. На послед-
но място, изследвания сочат, че фак-
тори на околната среда също играят
роля: хроничният стрес и расовата
дискриминация (при афроамерикан -
ки) се обсъждат като допринасящи
за хормонален дисбаланс и възпале -
ние, благоприятстващи миомогене -
зата, а експозицията на ксеноестро -
гени и ендокринни дизруптори (напр.
някои пестициди, фталати) в околната среда се свързва с по-висок риск
от миоми[18]. Общото между тези раз -
нообразни рискови фактори е, че
много от тях конвергират към повишено естрогенно стимулиране или
генетична нестабилност на маточната тъкан, което на фона на податлива
генетична основа води до иницииране и промоция на лейомиомите.
ЕНДОМЕТРИАЛЕН КАРЦИНОМ
Ендометриалният карцином (рак на тялото на матката) е най-честото зло -
качествено заболяване на женската
полова система в развитите страни. Той се подразделя на два основни
патогенетични типа: тип
с хормонални (естрогенни) фактори.
МОЛЕКУЛЯРНИ И
често възниква на базата на продължителна естрогенова стимулация без противодействие от прогестерон (напр. при хронична ановулация или екзогенен естроген). На този фон се натрупват генетични увреждания в жлезистия епител на ендометриума. Едно от най-ранните и чести събития е инактивиране на тумор-супресорния ген PTEN (фосфатаза и тензин хомолог). Загубата на PTEN функция – поради мутация, делеция или промоторна хиперметилация – се наблюдава в около 30-50% от ендометриоидните карциноми и води до конститутивна активация на PI3K/AKT сигналния път, стимулиращ клетъчния растеж и преживяемост[8,9]. Дефектите в PTEN се смятат за иницииращо събитие при много случаи на атипична хиперплазия и последващ карцином. Освен PTEN, често срещани молекулни изменения при ендометриалния карцином тип I са мутации в онкогена KRAS (~15-25% от случаите), в β-катенин (CTNNB1, ~2030% от туморите) и в гена PIK3CA (кодира каталитичната субединица на PI3K) – всички те водят до свръхактивация на пролиферативни пътища (MAPK/ERK, Wnt, съответно PI3K/ AKT) и допринасят за туморогенезата[4]. Характерна за ендометриоидния карцином е и мутацията в гена ARID1A (~40% при високостепенните и ~25% при нискостепенните), който кодира подединица на SWI/SNF комплекса за
се наблюдава при ~20% от спорадичните карциноми и води до микросателитна нестабилност (MSI) и мутаторен фенотип. Подобни епигенетични инактивирания са описани и за други гени (напр. PTEN, CDKN2A/ p16, и др.) при подгрупа от туморите[4]. Едновременно с това, глобална хипометилация на повторими
та и потискайки апоптозата. МикроРНК профилът на ендометриалния карцином също е дерегулиран: наблюдавано е повишение на онкомиР като miR-21 (който таргетира PTEN и други супресори) и спад в нивата на т.нар. тумор-супресорни миРНК като miR-200 семейството, което води до засилена инвазия и епителиално-мезенхимна трансдиференциация. Тези промени вече се изследват и като потенциални биомаркери за ранна диагностика и прогноза[8].
ХОРМОНАЛНИ И ДРУГИ РИСКОВИ ФАКТОРИ Епидемиологията на ендометриалния карцином тип I ясно сочи прекомерната естрогенова стимулация като основен рисков фактор. Затлъстяването е най-значимият от тях – адипозната тъкан притежава ароматазна активност и превръща андростендиона в естрон, повишавайки нивата на естрогени при постменопаузални жени. Жени с ИТМ >30 имат няколкократно по-висок риск от ендометриален рак в сравнение със слабите, като рискът нараства пропорционално на степента на затлъстяване. Естроген-заместителната терапия (само с естрогени, без прогестин) при постме -
нопаузални жени значително увеличава риска – продължителният прием на естрогени води до непрекъсната митогенна стимулация на ендометриума, което може да инициира хиперплазия и карцином (добавянето на гестаген предпазва чрез противодействие на този ефект). Синдромът на поликистозните яйчници (СПКЯ), при който често има хронична ановулация и следователно ниски нива на прогестерон при относително високи естрогени, предразполага младите жени към ендометриална хиперплазия и по-късно карцином. Тамоксифенът, използван в адювантното лечение на естроген-позитивен рак на гърдата, действа като парциален естрогенен агонист в ендометриума; жени на продължителна тамоксифенова терапия имат 2-3 пъти по-висок риск от ендометриален карцином. Сред репроду-
високото съотношение на 16α-хидроксиестрон към 2-хидроксиестрон е асоциирано с увеличен риск от ендометриален карцином[4], тъй като 16α-метаболитът има по-продължително и мощно естрогенно действие върху ендометриума. Генетични варианти в ензими на естрогенния метаболизъм – освен споменатия COMT, също в CYP19A1 (ароматаза), CYP1B1 и др. – са изследвани за връзка с риска, но с нееднозначни резултати. Наред с хормоналните фактори, наследствени синдроми също трябва да се отбележат: жените с наследствен неполипозен колоректален рак (синдром на Lynch) имат силно повишен риск от ендометриален карцином (до 40-60% доживотен риск) поради зародишни мутации в ДНК-репараторните гени (MSH2, MSH6, MLH1 или PMS2). Макар този път на канцерогенеза да е независим от естрогените, той подчертава многофакторността на заболяването. Обобщено, ключовият сценарий за тип I ендометриален карцином е продължителна естрогенова стимулация на ендометриума, водеща до хиперплазия и натрупване на генетични (PTEN, KRAS и др.) и епигенетични промени, които отключват злокачествена трансформация. Този процес се модерира от изброените рискови фактори, а разбирането му насочва към профилактични мерки – контрол на теглото, разумна употреба на хормонална терапия и т.н.
ЕНДОМЕТРИАЛНИ ПОЛИПИ Ендометриалните полипи са често срещани доброкачествени лезии, представляващи локализирани израстъци на ендометриалната тъкан (жлези, строма и кръвоносни съдове), навлизащи в маточната кухина. Те се срещат при 10-25% от жените, най-често в късна репродуктивна възраст и перименопауза (40–50 години). Макар
имат повишена експресия на естро -
генни рецептори – особено ER-α – в
жлезистите клетки, съчетано с на -
малена експресия на прогестеронови рецептори (PR-A и PR-B) в сравнение с нормалния ендометриум[12]. С
други думи, тъканта на полипа е относително хиперчувствителна към естроген и хипорезистентна към прогестерон. Това хормонално съотношение обяснява защо полипните
жлези могат да пролиферират под
влиянието на дори нормални естрогенни нива, без да претърпят нормална секреторна трансформация и
десквамация (поради нисък отговор на прогестерон). В полипите често се
открива повишена експресия на Bcl-
2 (маркер, инхибиращ апоптозата) и
понижена апоптозна активност, което допринася за персистирането им
през менструалния цикъл[12,13]. Уста -
новено е още, че локалната арома -
тазна активност може да е повишена – ензимът P450 ароматаза и факторът
SF-1 са открити в стромата на полипи,
което предполага, че самият полип
може да синтезира естроген in situ и
допълнително да стимулира растежа си[12,14]. Интересен маркер е p16
(CDKN2A) – тумор-супресорен протеин, чиято изразеност в стромата на
полипите е по-висока и специфична, вероятно отражение на клетъчна стареене или реактивни промени, свързани с патогенезата на полипите[15]
ГЕНЕТИЧНИ И КЛОНАЛНИ АСПЕКТИ Макар ендометриалните полипи да не са злокачествени тумори, проучвания сочат, че те често са моноклонални образувания, възникнали от пролиферацията на единична предшественикова клетка. Цитогенетични изследвания откриват аномалии в приблизително половината от изследваните полипи – най-често хромозомни транслокации, засягащи ре -
6p21, 12q13–15 или 7q22[16,17]
на 6p21 и 12q13–15
неопластичен (макар и доброкачествен) процес със задвижващи мутации/ пренареждания. Около половината полипи обаче имат нормален кариотип – при тях вероятно патогенезата е по-скоро хиперпластична и реактивна, отколкото неопластична. В редките случаи на атипични полипи (с неоплазия в тях) често се откриват молекулни промени, припокриващи се с тези на ендометриалния карцином (например мутации в PTEN, KRAS или MSI), което потвърждава възможността ендометриален карцином да възникне на база на дълго съществуващ полип. Като цяло обаче рискът един доброкачествен полип да малигнизира е малък (<5%) и най-вече, ако носи клетъчна атипия.
та хиперплазия и ендометриозата, което загатва за обща хормонална среда – хиперестрогения – благоприятстваща тези разраствания[12]. Някои изследвания намират асоци
HMGA1 (6p21) и HMGA2 (12q15) – високомобилните протеини на хроматина, които
сими лезии, увеличената естрогенова стимулация – ендогенна или екзогенна – е ключов фактор за формирането на ендометриални полипи. Тамоксифенът е класически пример: до 36% от жените на продължителна тамоксифенова терапия за рак на гърдата развиват ендометриални полипи, което е значимо повече от общата популация[12]. Тамоксифен-свързаните полипи са често множествени, с фиброзна строма и характерни хистологични особености (напр. кистично разширени жлези). Интересно е, че в полипи при тамоксифен-пациенти се наблюдават понижени нива на ER и увеличени на PR, съпроводени с потисната апоптоза – механизъм, по който тамоксифен
може да са фактор в патогенезата[12]. Като цяло, ендометриалните полипи могат да се разглеждат като фокална проява на естрогенов ефект върху ендометриума, модифициран от локални молекулярни събития. Клиничното пове
ли, които, особено при липса на
на маточните тъкани. В същото време специфични генетични изменения (например драйвърните мутации в MED12 при миоми или в PTEN при ендометриален карцином) осигуряват „вътрешния двигател“ на туморния растеж. Епигенетичните модификации – ДНК метилиране, хистонови промени, микроРНК – модулират експресията на ключови гени и могат да бъдат както последица, така и причина за туморогенезата. Влиянието на външни фактори като начина на живот, метаболитния статус и експозицията на ендокринни дизруптори допълнително подчертава колко мултифакторни са тези заболявания. Общият знаменател обаче остава естрогенът:
заболявания. Откриването на MED12 мутациите при миомите, описанието на молекулярните подтипове на ендометриалния карцином (по данни от The Cancer Genome Atlas) и разкриването на ролята на епигенетиката при
1. Baranov, V. S., Osinovskaya, N. S., and Yarmolinskaya, M. I. “Pathogenomics of Uterine Fibroid Development.” International Journal of Molecular Sciences, vol. 20, no. 24, 2019, p. 6151.
2. Baird, Donna D., et al. “Vitamin D and the Risk of Uterine Fibroids.” Epidemiology, vol. 24, no. 3, 2013, pp. 447–453.
3. Heydari, M., Ghorbian, S., and Sayyah Melli, M. “The Catechol-OMethyltransferase (COMT) rs4680 G>A Polymorphism Is Associated with Uterine Leiomyoma Susceptibility.” Gene, Cell and Tissue, vol. 6, no. 1, 2019, p. e86258. Brieflands.com.
4. Maekawa, R., et al. “Different DNA
Methylome, Transcriptome and Histological Features in Uterine Fibroids with and without MED12 Mutations.” Scientific Reports, vol. 12, no. 1, 2022, p. 8912.
5. Nijkang, N. P., et al. “Endometrial Polyps: Pathogenesis, Sequelae and Treatment.” SAGE Open Medicine, vol. 7, 2019, p. 2050312119848247.
6. Yang, Q., et al. “Comprehensive Review of Uterine Fibroids: Developmental Origin, Pathogenesis, and Treatment.” Endocrine Reviews, vol. 43, no. 4, 2022, pp. 678–726.
7. Stewart, E. A., et al. “Epidemiology of Uterine Fibroids: A Systematic Review.” BJOG: An International Journal of
Obstetrics & Gynaecology, vol. 123, no. 10, 2016, pp. 1501–1512.
8. Bostan, I., et al. “Landscape of Endometrial Cancer: Molecular Mechanisms, Biomarkers, and Targeted Therapy.” Cancers (Basel), vol. 16, no. 11, 2024, p. 2027.
9. Placido, G. D., et al. “PTEN Mutations and Endometrial Cancer.” Frontiers in Oncology, vol. 9, 2019, article 848.
10. Li, Y., et al. “ESR1 Mutations and Hormone Therapy Resistance in Endometrial Cancer.” Journal of Clinical Investigation, vol. 132, no. 9, 2022, p. e157456.
11. Dunning, A. M., et al. “Association of
ESR1 and ESR2 Gene Polymorphisms with Endometrial Cancer Risk.” Carcinogenesis, vol. 25, no. 6, 2014, pp. 1129–1135.
12. Krivak, T. C., et al. “MicroRNAs in Endometrial Carcinogenesis.” Gynecologic Oncology, vol. 150, no. 2, 2018, pp. 223–229.
13. Taylor, L. J., et al. “Bcl-2 Expression in Endometrial Polyps.” Obstetrics & Gynecology, vol. 102, no. 2, 2003, pp. 298–303.
14. Su, H., and Sun, Y. “Aromatase Expression in Endometrial Polyps.” Gynecologic and Obstetric Investigation, vol. 79, no. 1, 2015, pp. 1–6.
15. Stewart, C. J. R., et al. “p16 Expression in Endometrial Polyps.” Histopathology, vol. 64, no. 3, 2014, pp. 444–450.
16. Dal Cin, P., et al. “Cytogenetic Analysis of Endometrial Polyps.” Cancer Genetics and Cytogenetics, vol. 82, no. 2, 1995, pp. 155–157.
17. Bakker, B., et al. “Chromosomal Aberrations in Endometrial Polyps.” International Journal of Gynecological Pathology, vol. 33, no. 4, 2014, pp. 339–344.
18. McGurgan, P., et al. “Endometrial Polyps in Tamoxifen-Treated Women.” Ultrasound in Obstetrics & Gynecology, vol. 27, no. 1, 2006, pp. 94–98.
1
2Медицински Университет – Пловдив
3Медицински Университет – София
4ВМА – София
ВЪВЕДЕНИЕ
Остеопорозата е сред водещите соци-
ално-значими заболявания с възмож-
ност за ранна диагноза и ефектив-
но лечение. За разлика от повечето
хронични заболявания, одобрени-
те терапии за лечение на остеопороза обикновено са ограничени до един
медикамент с фиксирана доза и честота. При повечето пациенти с осте -
опороза дългосрочната употреба на
антиостеопорозните медикаменти остава спорна, поради съображенията за ефективност и безопасност. Пре -
имуществено при пациентите с висок фрактурен риск се използва последо -
(секвенциално) приложениe
очертае препоръки за управление на фрактурния риск.
ДЕНОЗУМАБ, който е одобрен за лечение на остеопороза от 2010 г., е напълно хуманизирано моноклонално антитяло срещу цитокин, рецепторен активатор на ядрен фактор капа В лиганд (RANKL), който е ключов медиатор на образуването, функцията и оцеляването на остеокластите. Той се свързва и инактивира RANKL, предотвратявайки узряването на прекурсорни клетки в зрели остеокласти, насърчава
ват до изходното ниво 3 месеца след прекратяване. Впоследствие и двата маркера се покачват над базовите нива с 63% увеличение на CTX и 47% увеличение на P1NP, съответно на 30 и 36 месец. Когато Денозумаб се спре, КМП намалява във всички скелети зони[4].
Рискът от фрактури след преустановяване на приложението на Денозумаб е проучена в няколко проучвания с относително кратка продължителност на проследяване, където честотата на фрактурите
изглежда толкова висока при пациентите прекратили лечението, както при тези които не са получили лечение[3,5-7]. Докато костната загуба е очевидна на всички места на скелета, особено в лумбален гръбнак и бедро при остеодензитометрия[8], оттеглянето на Денозумаб все още не е доказано, че създава прекомерен риск от фрактура на бедро или дру-
ги големи остеопоротични фрактури. Това несъответствие между наблюдавани вертебрални фрактури и липсата на доказателства за невертебрални фрактури след преустановяване на Денозумаб е въпрос на дискусии. Фактът, че преимуществено костното ремоделиране настъпва върху повърхността на трабекуларната кост, а не в кортикалната кост[9], би могъл евентуално да обясни защо гръбначният стълб, който е структуриран предимно от трабекуларна кост е силно повлиян от „феномена на рикошет“, водещ до вертебрални фрактури.
ДЪЛГОСРОЧНО ПРИЛОЖЕНИЕ НА ДЕНОЗУМАБ
фемур в 10-годишното разширено изпитване на FREEDOM, което
изведе кумулативна честота коригирана спрямо експозицията от 0.8 на 10 000 участник-години[3]. По същия начин честотата на остеонекроза на челюстта е много ниска с приблизителна честота от 5.2 на 10 000 участник-години[3]
КОГА МОЖЕ ДА СЕ ПРЕУСТАНОВИ
ПРИЛОЖЕНИЕТО НА АНТИРЕЗОРБТИВНАТА ТЕРАПИЯ? През последните години все по-често се използва стратегия „treat-totarget“ при лечението
стратегия твърдят, че целенасочената терапия
обмен трябва да се мониторират 3 месеца след започване на перорален бифосфонат за проследяване на придържането
тъй като може да е необходима втора инфузия.
с T score са
за достигане на целта. Предполага се, че
подходяща цел[11]. Може да се спре
приема на антиостеопорозния медикамент, ако Т score е над стойност в която има приемливо нисък риск от фрактури. Т score над или равен на –2.5 е особено полезна цел за терапия с бифосфонати. Данните са свър -
зани с уникалния фармакокинетичен профил на бифосфонатите, които се задържат години в скелета и на -
лични доказателства
път в „Проучване за интервенция на фрактури“ (FIT). Лечението с ALN е свързано с почти 50% намаляване на новите вертебрални фрактури, намалена прогресия на гръбначните деформации и намалена загуба на височина[14]. Ефектът на ALN след спиране на денозумаб беше за първи път оценен в проучването Denosumab Adherence Preference Satisfaction (DAPS). Оценяват се 250 жени след менопауза, на които са назначени ALN за 1 година, последван от денозумаб
слаба, докато афинитетът му към ми -
нерализираната кост е висок, макар
и малко по-нисък в сравнение с ALN и ZOL[16]. Въпреки това е по-мощен in vitro от ALN и ибандронат (IBN) по от-
ношение на неговата биохимична ефективност, като инхибитор на остеокластите. При постменопаузални жени с вертебрални фрактури, RIS доказано намалява честотата на вертебрални и невертебрални фрактури.
ИБАНДРОНАТ (IBN)
Интересно е да се отбележи, че това е първият бифосфонат, при който се
показва значителна антифрактурна
ефикасност с интермитентно перорално приложение. Разширено про -
учване, което не е имало право да
анализира случаите на фрактури,
демонстрира че КМП на лумбален
гръбнак се увеличава леко, докато
КМП на бедрената кост остава ста -
билна за продължителността на лечението от 5 години[17].
ЗОЛЕДРОНАТ (ZOL)
ZOL (или золедронова киселина) е
така нареченото трето поколение бифосфонат, което се прилага интраве -
нозно и позволява интервали на ле -
чение на остеопороза от 12 месеца. Неговата антифрактурна ефикасност
е изследвана в няколко рандомизирани контролирани проучвания, включително HORIZON Pivotal Fracture Trial (HORIZON PFT), HORIZON и HORIZON Recurrent Fracture Trial (HORIZON RFT) [18,19]. В първото ZOL намалява риска от морфометрична (радиографска) вер -
тебрална фрактура със 70% и рискът
от фрактура на бедрото с около 40% в
постменопаузални жени. В последното, което включва мъже и жени е таргетирана фрактура на бедрото и е ус
морфометрични (рентгенографски) вертебрални фрактури е по-висока сред жени, които са спрели лечението след първите три години, докато честотата на невертебралните фрактури е сходена сред двете групи. В наскоро публикуван мрежов мета-анализ, който изследвана клиничната ефикасност на лекарствените интервенции за първична и вторична профилактика на остеопорозни фрактури, беше установено, че ZOL е единственото лекарство, което намалява както вертебралните, така и невертебралните фрактури.
АСПЕКТИ НА БЕЗОПАСНОСТТА Като цяло оралните и парентералните бифосфонати се понасят добре. Стомашно-чревни оплаквания, включително стомашна язва са най-честите
новните причини за прекратяване на лечението. Преходно понижаване на бъбречната функция след инфузия са докладвани при пациенти, получаващи интравенозно IBN и ZOL. Въпреки това, анализите за безопасността по отношение на бъбречната функция с перорални ALN, IBN и RIS, предоставят убедителни доказателства за краткосрочни или дългосрочни ефекти върху бъбречната функция[20]. За разлика от бифосфонатите, денозумабът не се елиминира от бъбреците, което позволява лечение дори при пациенти с хронично бъбречно заболяване.
ОСТЕОНЕКРОЗА НА ЧЕЛЮСТТА (ONJ) Първоначално появата и се смята, че се свързва изключително с употребата на бифосфовати. ONJ се определя


и 19 проучвания от реалната
практика[24]. Установено е, че фрактур -
ния риск е бил по-висок, ако пациентите са били в напреднала възраст, имали са ниска КМП на бедро, били са с поднормено тегло, слабо придържане към лечението и често среща-
1.
2025,
ISBN 978-6197353-91-4
2. NIH Consensus Development Panel on Osteoporosis Prevention D, Therapy. Osteoporosis prevention, diagnosis, and therapy. JAMA. 2001;285:785-95
3. Aziziyeh R, Amin M, Habib M, Perlaza JG, McTavish RK, Ludke A, et al. A scorecard for osteoporosis in four Latin American countries: Brazil, Mexico, Colombia, and Argentina. Arch Osteoporos. 2019;14:69
4. Akesson KE, Ganda K, Deignan C, Oates MK, Volpert A, Brooks K, et al. Post-fracture care programs for prevention of subsequent fragility fractures: a literature assessment of current trends. Osteoporos Int. 2022
5. Cosman F, de Beur SJ, LeBoff MS, Lewiecki EM, Tanner B, Randall S, et al. Clinician's Guide to Prevention and Treatment of Osteoporosis. Osteoporos
Int. 2014;25:2359-81.
6. Kanis JA, Cooper C, Rizzoli R, Reginster JY, Scientific Advisory Board of the European Society for C, Economic Aspects of O, et al. European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int. 2019;30:3-44
7. Kanis JA, Harvey NC, McCloskey E, Bruyere O, Veronese N, Lorentzon M, et al. Algorithm for the management of patients at low, high and very high risk of osteoporotic fractures. Osteoporos Int. 2020;31:1-12
8. Ballane G, Cauley JA, Luckey MM, ElHajj Fuleihan G. Worldwide prevalence and incidence of osteoporotic vertebral fractures. Osteoporos Int. 2017;28:1531-42
9. Shah ND, Steyerberg EW, Kent DM. Big Data and Predictive Analytics: Recalibrating Expectations. JAMA. 2018;320:27-8
10. Miller PD, Bilezikian JP, Lewiecki EM, Watts NB, Carey JJ. Re: A History of Pivotal
Advances in Clinical Research Into Bone and Mineral Diseases. J Bone Miner Res. 2018;33:1900-1
11. World Health Organisation (WHO). Assessment of Fracture Risk and its Application to Screening for Postmenopausal Osteoporosis. World Health Organ Tech Rep Ser 1994; 843:1 - 129
12. World Health Organisation (WHO). Prevention and Management of Osteoporosis: Report of a WHO Scientific Group. World Health Organ Tech Rep Ser 2003; 921:1-192
13. World Health Organisation (WHO). Screening Programmes: A Short Guide. World Health Organ 2020:1-59
14. Liberman UA, Weiss SR, Broll J, et al. Effect of oral alendronate on bone mineral density and the incidence of fractures in postmenopausal osteoporosis. The Alendronate Phase III Osteoporosis Treatment Study Group. N Engl J Med 1995;333: 1437e43
15. Riggs BL, Melton LJ, 3rd. The prevention and treatment of osteoporosis. N Engl J Med. 1992;327:620-7
16. Russell RG, Watts NB, Ebetino FH, Rogers MJ. Mechanisms of action of bisphosphonates: similarities and differences and their potential influence on clinical efficacy. Osteoporos Int 2008;19:733e59
17. Miller PD, Recker RR, Reginster JY, et al. Efficacy of monthly oral ibandronate is sustained over 5 years: the MOBILE long term extension study. Osteoporos Int 2012;23:1747e56
18. Black DM, Delmas PD, Eastell R, et al., HORIZON Pivotal Fracture Trial. Onceyearly zoledronic acid for treatment of postmenopausal osteoporosis. N Engl J Med 2007;356:1809e22
19. Lyles KW, Colon-Emeric CS, Magaziner JS, et al., HORIZON Recurrent Fracture Trial. Zoledronic acid and clinical fractures and mortality after hip fracture. N Engl J Med 2007;357:1799e809
20. Miller PD, Jamal SA, Evenepoel P, et al. Renal safety in patients treated with bisphosphonates for osteoporosis: a review. J Bone Miner Res 2013;28:2049e59
21. Goh SK, Yang KY, Koh JS, et al. Subtrochanteric insufficiency fractures in patients on alendronate therapy: a caution. J Bone Joint Surg Br 2007;89:349e53
22. Austin DC, Torchia MT, Klare CM, Cantu RV. Atypical femoral fractures mimicking metastatic lesions in 2 patients taking denosumab. Acta Orthop 2017;88:351e3
23. Odvina CV, Zerwekh JE, Rao DS, et al. Severely suppressed bone turnover: a potential complication of alendronate therapy. J Clin Endocrinol Metab 2005;90:1294e301
24. Black DM, Condra K, Adams AL, Eastell R. Bisphosphonates and the risk of atypical femur fractures. Bone 2022;156: 11629
25.
А. Кахтан МБАЛ „Уни Хоспитал“ – Панагюрище
Астма при
Ключови думи: Детска астма, вирусно „свиркане“, недостатъчна диагноза, свръхдиагностика, диференциална диагноза, лечение.
ВЪВЕДЕНИЕ
Детската астма е хетерогенно заболя-
ване, което обикновено се характеризира с хронично възпаление на дихателните пътища. Това се определя от
анамнеза за респираторни симптоми като „свиркане“, затруднено дишане, стягане в гърдите и кашлица с различна променливост, честота и интензивност, заедно с променлива обструкция на експираторния въздушен
семейна анамнеза Други алергични заболявания (атопичен дерматит
когато лечението се спре.
при малки деца, където обективното
изследване не е възможно е важно да се вземат решения за всяко дете поотеделно, за да се избегне прекомерно или недостатъчно лечение. С цел подпомагане на диагностичния процес на астмата при деца от преучилищ-
на възраст с чести епизоди на "свиркащо" дишане, бяха създадени прогностични преценки – т.нар. asthma predictive index (API) и след това негов модифициран вариант (mAPI), които определят кои от тези деца са изложени на
по-висок риск от развитие на астма. И въпре -
ки клиничната значимост на тези предиктивни идекси в прогнозирането за персистираща атопична астма, прилагането им би довело до съответно субдиагностициране на заболяването при неатопичните деца „свиркачи“ и
За положителен API е необходимо наличието на поне един голям или поне два малки критерия при малки деца с поне три епизода на „свиркане“ до момента. Големите критерии включват: Диагностицирана от лекар астма при родител; Диагностициран от лекар атопичен дерматит. Малките критерии са "свиркане", несвързано с настинка; Еозинофили ≥4% в кръвообращението; Диагностициран от лекар алергичен ринит. Докато модифицираният предсказващ астма индекс (mAPI) се прилага
при малки деца с четири или повече епизода на „свиркане“ годишно,
в началото (SaO2) >95% <92% Разговор с изречения/думи
риск от астма за деца в предучилищна възраст. Прогностичната способност на mAPI зависи до голяма степен от разпространението на астма в общата популация[6,7,8]. Едно проучване показва намалени екзацербации, намалена употреба на лекарства за контролиране
и увеличени дни без епизоди при 2- до 3-го -
дишни деца с положителен mAPI, лекувани с инхалаторни кортикостероиди в сравнение с плацебо[17].
ФЕНОТИПОВЕ НА „СВИРКАЩО” ДИШАНЕ[3] В миналото бяха предложени две основни класификации на „свиркания“, наречени фентипове на „свиркащо” дишане: 1. Класификация, базирана на симптоми: това се основава на това дали детето е имало само епизодично „свиркане” (свиркане през отделни периоди от време, често във връзка с URTI, с отсъствие на симптоми между епизодите) или многократни свиркания (епизодични свиркания със симптоми, появяващи се и между тези епизоди, напр. по време на сън или с тригери като активност, смях или плач).
2. Класификация, базирана на времевата тенденция: Включва преходни „свиркания“ (симптомите започват и завършват преди навършване на 3 години); перзистира
данни на GINA, симптомите/белезите, които предполагат астма при деца до 5 години са посочени в Табл. 2. Диагноза астма при малки деца със „свиркане“ е много вероятна, ако те имат:
• Свиркане или кашлица, които
Beclomethasone dipropionate (pMDI, standard particle)
Beclomethasone dipropionate (pMDI, extrafine particle)
µg (≥5)
µg (≥5)
Budesonide (nebules) 500 µg (≥1)
Mometasone furoate (pMDI, standard particle) 100 µg (≥5)
Fluticasone propionate (pMDI, standard particle) 50 µg (≥4)
съвет[3]: Изостава в развитието си; Неонатал -
на или много ранна поява на симптомите; Повръщане, свързано с респираторни симптом; Персистиращо „свиркане“ въпреки приложението на бронходилататор; Липса на отговор към лекарства за астма (ICS, перорални стероиди или SABA); Липса на асоциация на симптомите с типични отключващи фактори, като вирусна инфекция на горните дихателни пътища; Фокални белодробни или сърдечно-съдови признаци, или пръсти тип „бараба -
ни палки“ и нокти тип„часовниково стъкло“; Хипоксемия извън контекста на вирусно заболяване.
ОБОСТРЯНИЯТА НА АСТМА
Обострянето на астма при деца на възраст 5 години и по-малки се дефинира като остро или подостро влошаване на контрола на симптомите, достатъчно да причини дистрес или риск за здравето и да изисква посещение при медицинско лице или повторно лечение със системни кортикостероиди. Ранните симптоми на острия
ти, „намаляване на
риск“ – предотвратяване на обостранията и минимизиране на страничните ефекти от лекарствата. Глобалната инициатива за астма (GINA) предлага поетапен подход към лечението, който е персонализиран за всяко дете поотделно, като се взема предвид ефективността на наличните лекарства, тяхната безопасност и цената им за платеца или семейството. Според препоръките на GINA решението за започва -
не на ежедневна терапия с контролер зависи
от честотата, тежестта и продължителността на симптомите, наред с клиничните прояви и фамилната анамнеза за атопия. Ако диагнозата астма е потвърдена при деца, чиито симптоми не са овладени след 3 месеца на ниска доза ICS и са изключени
дикаменти[3,14]. Лечението с ICS е свързано с
по-нисък риск от рецидиви, по-малко хоспитализации и намалена нужда от облекчаващо средство като β2-агонисти[15-16]. ICS се препо -
ръчват при деца с персистираща симптоматика или при провеждани 2 или повече курса системни кортикостероиди, в рамките на 6 месечен период, тъй като е доказано, че намаляват тежестта на екзацербациите с 35%[17].
Въпреки това, все повече се налага мнението, че хетерогенността на свиркащото диша -
не в ранна детска възраст е свързано с различни модели на възпаление на дихателните пътища и е предпоставка ICS да не са ефективно лечение за всеки фенотип[18-20]. Устано -
вено е, че комбинацията от сенсибилизация към инхалаторни алергени и еозинофилия в периферна кръв >300 клетки/µl прогнозира положителен отговор към ICS[21]. Въпреки че алергенната сенсибилизация е маркер за чувствителен към стероиди фенотип, по-го -
важен, колкото и изборът на меди
камент, тъй като правилното боравене с ин
писаната доза. Инспираторните потоци и белодробните обеми до голяма степен зависят от ръста и нарастват с възрастта и телесната маса, следователно много деца няма да
могат да генерират достатъчен инспираторен поток за правилно използване на инхалаторното устройство до 5-6-годишна възраст.
Предпочитаният
са лекарство на избор, особено при деца до 5-годишна възраст. Прилагат се инхалаторно. Пероралното прилагане не се препоръчва, поради бавното начало на действие и чести странични ефекти[3,15-40] • Краткодействащи (SAMA) мускаринови ан
зъм, секрецията на бронхиална слуз и ин -
хибират бронхиалната експекторация. SAMA (основен представител е Ipratropium bromide) са втората важна група лекарства, които се препоръчват за фармакологичен
контрол като инхалаторни бронходилататори при астма и се препоръчват главно при пациенти, които или не понасят, или имат недостатъчен ефект от лечението със SABA. Ипратропиев бромид обикновено се
използва в комбинация със SABA при тежка екзацербация на астма[41-45].
• Системни кортикостероиди. Системните
кортикостероиди не предизвикват бърза бронходилатация, но въпреки това се из -
ползват поради силния си противовъзпалителен ефект за лечение на по-тежки астматични екзацербации.
Б. Лекарства за поддържане на астма. Те се използват ежедневно за дълго време за
постигане и поддържане на контрол на аст-
мата и включват:
▪ Антагонисти на левкотриенови рецептори (LTRA). LTRA включват монтелукаст и зафирлукаст.
▪ Инхалаторни и системни кортикоиди. Кортикостероидите, особено ICS, са средства на първи избор за поддържащо лечение на астма. Кортикостероидите имат мощен противовъзпалителен ефект, намаляват бронхиалната хиперреактивност, секрецията на слуз и отока на лигавиците, увеличават броя на бета-адренергичните рецептори в белите дробове и повишават тяхната чувствителност към действието на β2-агонистите. Ниските дози ICS осигуряват по -
вечето клинични ползи за повечето деца
с астма, но по-високите дози са свързани с повишен риск от странични ефекти. Употребата на перорални или системни кортикостероиди повишава риска от фрактури[46,40]. Препоръчва се да се проверява височината на деца с астма, лекувани с ICS, поне веднъж годишно (GINA 2018).
(SABA). Друга
възможносте интермитентен кратък курс ICS
при поява
необходимост. Като алтернатива
ежедневно LTRA или интермитентен кратък
курс на ICS в началото на вирусно заболяване. Като трябва да се имат предвид неблагоприятните ефекти на монтелукаст върху съня и поведението на децата (FDA изисква преду-
преждение за това).
Стъпка 3: За деца, чиито симптоми не са
овладени след 3 месеца ниска доза ICS, удвояването на първоначалната доза често е
най-добрият вариант и преоценка след 3 месеца. Друга възможност е добавяне на LTRA
към ниска доза ICS. Тази и следващата стъпка трябва да бъдат предшествана от изключване на други диагнози, проверка на
за експертна оценка.
Препоръки на NICE[12] за лечение на деца в предучилищна възраст със съмнение или по
твърдена астма или със симптоми на астма, които не са контролирани от текущото им лечение. Тези препоръки включват следните стъпки:
▪ SABA като облекчаваща терапия на деца под 5 години със съмнение за астма. ▪ 8-седмично изпитване на педиатрична умерена доза ICS при деца под 5 години със симптоми, които ясно показват необходимостта от поддържаща терапия (например симптоми, свързани с астма 3 пъти седмично или повече, или причиняващи събуждане през нощта) или подозирана астма, която не се контролира само със
SABA. ▪ След 8 седмици спира се лечението с ICS и
НА ОСТРИЯ АСТМАТИЧЕН ПРИСТЪП ПРИ ДЕЦА ДО 5 ГОДИНИ
• Прилагането на една или друга стъпка за -
виси от мястото където се провежда лечението – в дома, в амбулаторни или болнични условия или интензивно отделение.
• На родителите/болногледачите на малки деца с
▪ Всяко ограничение на активността поради астма
▪ Необходимост

ството
• Замърсяване на открито (NO2 и частици)
b. Рискови фактори за фиксирано ограничение на въздушния поток: Тежка астма с ня
колко хоспитализации и/ или Анамнеза за прекаран бронхиолит.
Рискови фактори за нежелани лекарствени реакции
• Системни: Чести курсове на
пропуските, разпознаване и управление на симптомите, обяснете им ролята на облекчаващото и превантивното лечение, правилното използване на инхалаторната техника, как да управляват извънредни ситуации и кога да потърсят медицинска помощ; ▪ Препоръчайте годишна ваксина срещу грип
▪ Проверявайте спазването при всяко посещение и адресирайте бариерите
▪ Всички деца трябва да имат писмен план за действие за дома и грижите за децата.
ЗАКЛЮЧЕНИЕ Предвид честите случаи на
респективно прекомерно или
лечение. Също така, преди поставяне на диагноза „вирусно свиркане”, „рецидивиращи инфекции с БОС” или „астма”, както и преди започване на контролно лечение на „астма”, се препоръчва консултация със специалист по детска пулмология или специалист по лечение на алергични заболявания и
1. Abdulhamid A.K. Differential diagnostic approach to cough in children. Scientific Polish Journal "Medical Sciences" 2025; 82: 10–13.
2. DIAGNOSIS, PREVENTION AND TREATMENT OF BRONCHIAL ASTHMANATIONAL CONSENSUS, SOFIA, 2000.
3. Global Strategy for Asthma Management and Prevention(2024).
4. Huffaker MF, Phipatanakul W. Utility of the Asthma Predictive Index in predicting childhood asthma and identifying diseasemodifying interventions. Ann Allergy Asthma Immunol. 2014;112:188–90. doi: 10.1016/j.anai.2013.12.001.[DOI]
5. Dong Hyeon Lee 1, Ji-Won Kwon 2, Hyung Young Kim 3, Ju-Hee Seo 4, HyoBin Kim 5, So-Yeon Lee 6, Gwang-Cheon Jang 7, Dae-Jin Song 8, Woo Kyung Kim 9, Young-Ho Jung 6, Soo-Jong Hong 6,✉, Jung Yeon Shim 1 . Asthma predictive index as a useful diagnostic tool in preschool children: a cross-sectional study in Korea. Clin Exp Pediatr. 2019 Nov 8;63(3):104–109. doi: 10.3345/ kjp.2019.00640
6. Timothy S. Chang PhD a, Robert F. Lemanske Jr. MD b c, Theresa W. Guilbert MD, MS b, James E. Gern MD b c, Michael H. Coen PhD a, Michael D. Evans MS a, Ronald E. Gangnon PhD a, C. David Page PhD a, Daniel J. Jackson MD b. Evaluation of the Modified Asthma Predictive Index in HighRisk Preschool Children. The Journal of Allergy and Clinical Immunology: In Practice Volume 1, Issue 2, March 2013, Pages 152156
7. Castro-Rodriguez JA, Holberg CJ, Wright AL, Martinez FD. A clinical index to define risk of asthma in young children with recurrent wheezing. Am J Respir Crit Care Med 2000; 162:1403-6.
8. Guilbert TW. Identifying and managing the infant and toddler at risk for asthma. J Allergy Clin Immunol 2010;126(2):417-22.
9. Yang CL, Gaffin JM, Radhakrishnan D. Question 3: Can we diagnose asthma in children under the age of 5 years? Paediatr Respir Rev 2019;29:25-30.
10. Schultz A, Devadason SG, Savenije OE, Sly PD, Le Souëf PN, Brand PL. The transient value of classifying preschool wheeze into episodic viral wheeze and multiple trigger wheeze. Acta Paediatr 2010;99(1):56-60.
11. Ducharme FM, Dell SD, Radhakrishnan D, Grad RM, Watson WT, Yang CL, et al. Diagnosis and management of asthma in preschoolers: A Canadian Thoracic Society and Canadian Paediatric Society position paper. Can Respir J 2015;22(3):135-43.
12. National Institute for Health and Care Excellence (NICE). Pharmacological treatment pathway for children under 5. NICE guideline [NG80]. Published: 29 November 2017. Last updated: 12 February 2020.
13. Castro-Rodriguez JA, Pedersen S. The role of inhaled corticosteroids in management of asthma in infants and preschoolers. Curr Opin Pulm Med. 2013;19(1):54–59.
14. Global Strategy for Asthma Management and Prevention. 2021. (accessed on 28 March 2022).
15. Bisgaard H, Allen DB, Milanowski J, et al. Twelve-month safety and efficacy of inhaled fluticasone propionate in children aged 1 to 3 years with recurrent wheezing. Pediatrics. 2004;113(2):e87–e94.
16. Hofhuis W, van der Wiel EC, Nieuwhof EM, et al. Efficacy of fluticasone propionate on lung function and symptoms in wheezy infants. Am J Respir Crit Care Med. 2005;171(4):328–333.
17. Guilbert TW, Morgan WJ, Zeiger RS, et al. Long-term inhaled corticosteroids in preschool children at high risk for asthma. N Engl J Med. 2006;354(19):1985–1997.
18. Schokker S, Kooi EM, de Vries TW, et al. Inhaled corticosteroids for recurrent
respiratory symptoms in preschool children in general practice: randomized controlled trial. Pulm Pharmacol Ther. 2008;21(1):88–
97.
19. Wolfgram PM, Allen DB. Effects of inhaled corticosteroids on growth, bone metabolism, and adrenal function. Adv Pediatr. 2017;64(1):331–345.
20. Fitzpatrick A. M., Jackson D. J., Mauger D. T. Individualized therapy for persistent asthma in young children, J Allergy Clin Immunol . 2016 Dec;138(6):1608-1618.
21. Robinson PFM, Pattaroni C, Cook J, et al. Lower airway microbiota associates with inflammatory phenotype in severe preschool wheeze. J Allergy Clin Immunol. 143(4): 1607–1610.e3. 2019.
22. Hayashi R., Wada H., Ito K., Adcock I.M. Effects of glucocorticoids on gene transcription. Eur J Pharmacol, 500 (2004), pp. 51-62
23. Castro-Rodriguez JA, Rodrigo GJ. Betaagonists through metered-dose inhaler with valved holding chamber versus nebulizer for acute exacerbation of wheezing or asthma in children under 5 years of age: a systematic review with meta-analysis. J Pediatr 2004;145:172-7.
24. Cohn RC. A review of the effects of medication delivery systems on treatment adherence in children with asthma. Curr Ther Res Clin Exp 2003;64:34-44.
25. FDA requires Boxed Warning about serious mental health side effects for asthma and allergy drug montelukast (Singulair); advises restricting use for allergic rhinitis. Risks may include suicidal thoughts or actions. Last updated 3-4-2020.
26. Global Initiative for Asthma (GINA). Pocket Guide for Asthma Management and Prevention in Children 5 Years and Younger, April 2015.
27. Szefler SJ, Chmiel JF, Fitzpatrick AM, Giacoia G, Green TP, Jackson DJ, et al. Asthma across the ages: knowledge gaps
OCS
ICS – inhaled corticosteroid
PAAPs – personalized asthma action plans
URTI – upper respiratory tract infection pMDI – pressured metered-dose inhaler
in childhood asthma. J Allergy Clin Immunol 2014;133(1):3-13.
28. Papadopoulos NG, Čustović A, Cabana MD, Dell SD, Deschildre A, Hedlin G, et al. Pediatric asthma: An unmet need for more effective, focused treatments. Pediatr Allergy Immunol 2019;30(1):7-16.
29. Ballas ZK. Asthma clinical practice guidelines: Time for an update. J Allergy Clin Immunol 2018;142(3):787.
30. Global Initiative for Asthma (GINA). Pocket Guide for Asthma Management and Prevention in Children 5 Years and Younger, April 2015. Available from www.ginasthma. org.
31. GINA Report 2017; Global Strategy of Asthma Management and Prevention.
32. GINA Report 2019; Global Strategy of Asthma Management and Prevention.
33. Ballas ZK. Asthma clinical practice guidelines: Time for an update. J Allergy Clin Immunol 2018;142(3):787.
34. British guideline on the management of asthma, SIGN 158. Scottish Intercollegiate Guidelines Network and British Thoracic Society. 2019 (viewed February 2023).
35. Cloutier M et al. 2020 focused updates to the asthma management guidelines: a report from the National Asthma Education and Prevention Program Coordinating Committee Expert Panel Working Group. Journal of Allergy and Clinical Immunology. 2020. 146(6), p1217-70.
36. Global Initiative for Asthma. 2022 GINA Report, Global Strategy for Asthma Management and Prevention. 2022.
37. McNamara D et al. New Zealand Child Asthma Guideline. Asthma and respiratory foundation NZ. 2020. (viewed May 2023)
38. National Asthma Council Australia. Australian Asthma Handbook. National Asthma Council Australia, Melbourne. 2022. http://www.asthmahandbook.org.au (viewed February 2023)
39. Yang CL et al. Canadian Thoracic Society
2021 guideline update: diagnosis and management of asthma in preschoolers, children and adults. Canadian Journal of Respiratory, Critical Care, and Sleep Medicine. 2021. 5(6), p348-61.
40. Guilbert TW, Morgan WJ,Krawiec M, Lemanske RF, Jr., Sorkness C, Szefler SJ, et al. The prevention of early asthma in kids study: Design, rationale and methods for the Childhood Asthma Research and Education network. Control Clin Trials. 2004;25:286310.
41. Cazzola M, Page CP, Calzetta L, Matera MG. Pharmacology and therapeutics of bronchodilators. Pharmacol Rev 2012; 64(3): 450-504.
42. Cazzola M, Matera MG. Bronchodilators: current and future. Clin Chest Med 2014; 35(1): 191-201.
43. Cazzola M, Segreti A, Matera MG. Novel bronchodilators in asthma. Curr Opin Pulm Med 2010; 16(1): 6-12.
44. Cazzola M, Matera MG. Emerging inhaled bronchodilators: an update. Eur Respir J 2009; 34(3): 757-69
45. Cazzola M, Matera MG. Novel long-acting bronchodilators for COPD and asthma. Br J Pharmacol 2008; 155(3): 291-9.
46. Castro-Rodriguez JA, Rodrigo GJ. Betaagonists through metered-dose inhaler with valved holding chamber versus nebulizer for acute exacerbation of age: A systematic review with meta-analysis. J Pediatr 2004;145:172-7.
47. Zhou J, Liu DF, Liu C, Kang ZM, Shen XH, Chen YZ, Xu T, Jiang CL, Allergy 2008: 63: 1177–1185. Glucocorticoids inhibit degranulation of mast cells in allergic asthma via nongenomic mechanism.
48. Lakupoch K, Manuyakorn W, Preutthipan A, et al. The effectiveness of newly developed written asthma action plan in improvement of asthma outcome in children. Asian Pac J Allergy Immunol 2018;36:88–92.
ВЪВЕДЕНИЕ Alopecia areata (AA) е Т-клетъчно
медиирано автоимунно заболява -
не, характеризиращо се със загуба
на имунната привилегия на космения фоликул (КФ). Клинично се про -
явява с нецикатрициален косопад под формата на единични или мно -
жество добре ограничени овални
обезкосмени полета с различен раз -
мер. Косопадът може да засегне це -
лия скалп (alopecia totalis, AT), ця -
лото тяло (alopecia universalis, AU)
или само части от тялото като брада (alopecia areata barbae), вежди и
мигли. Счита се, че Cornelius Celsus
за първи път описва АА, а терминът „alopecia areata“ е въведен от Sauvages през 1760 г.[1,2].
ЕПИДЕМИОЛОГИЯ,
Изчислено е, че при 60% от пациентите първият епизод на заболяването се появява преди 20 годишна възраст, а при 85.5% - преди 40-годишна възраст[1,2,6,7]. Епидемиологични проучвания, относно честотата на мястото на засягане, посочват че скалпът е най-често засегнат, като могат да бъдат засегнати и КФи на други места по тялото (като вежди, мигли и брада) [1,2,9,10]. По-късната
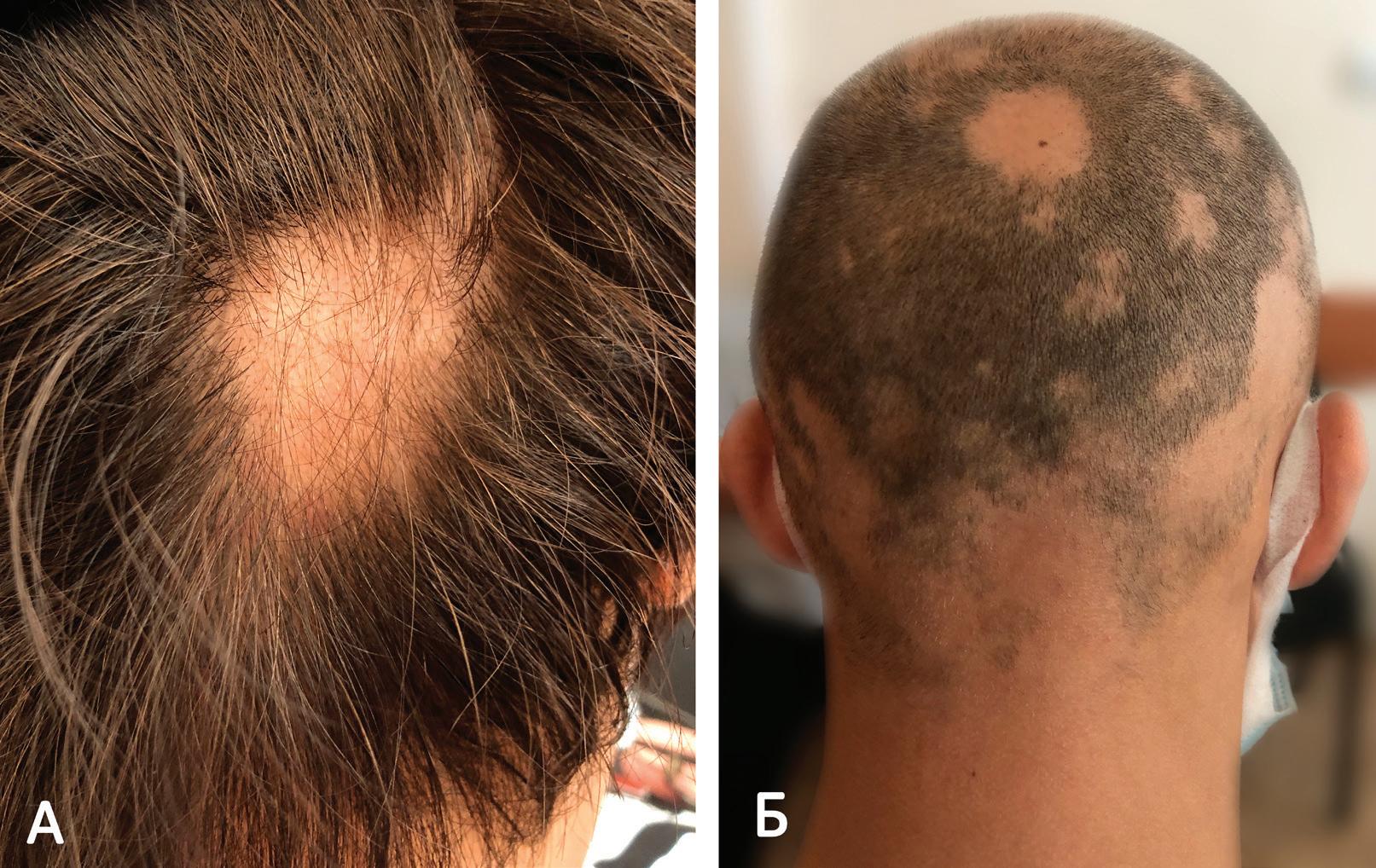
на косата. Въпреки имунните смущения,
КФи не се разруша -
ват, така че резултатът е нецикатрициа -
лен косопад. Освен
това, индуцираният от IFN-γ JAK/STAT
сигнален път може
да попречи на цикъ -
ла на растеж на косата, тъй като този
сигнален път е потиснат в КФ по време на анагена. JAK/STAT
сигналният път инхибира пролиферацията и активирането на стволовите клетки на косъма
анамнеза в семейството за орган-специфични автоимунни болести, генотип, индивидуалната анам -
неза за други автоимунни заболявания,
заболяване на щито -
видната жлеза, витилиго, атопия или
атопичен дерматит, стрес[1,2,15]
КЛИНИЧНА КАРТИНА
АА може да се прояви като единичен епизод или може да
има рецидивиращ ход. Най-често, първата проява е единично, постепен
обезкосмени области. Алопетичните полета обикновено се забелязват внезапно. Кожата в засегнатите участъци е нормална и гладка, рядко може да се наблюдава бледо розово оцветяване или залющване. Обезкосмените полета са безболезнени. Рядко се съобщават леко изтръпване, сърбеж, парене или дизестезия предшестващи косопада[1,2,4,5,16,17]. При
поява на космен растеж при АА често космите са без пигмент, последван от процес на репигментация. Често израстването на коса на едно място, така и образуването на гнездови -
ден косопад на друго място, може да се наблюдава едновременно при един и същи пациент[1,2,17,18]
Според модела на падане на коса, АА се категоризира като: петниста АА (AA partialis/AA circumscripta), едно или няколко обезкосме -
ни полета; ретикуларна или мултифокална АА (AA reticularis/AA multifocalis), сливането на отделните полета води до формирането на полициклични области; офиазна АА (AA ophiasis), лентовидна загубата на коса в париетална, темпорална и тилна
главно в андроген-зависимата зона, и се характеризира с остър дифузен телогенен косопад при липсата на типичните обезкосмени гнезда. АА също може да засегне само космите извън скалпа (вежди, мигли, брада, гърди, подмишници или окосмяването по пубиса)[4, 5,20]. Има случаи на АА с
обезкосмени полета само по брадата (AA barbae), или със засягане само
на вежди, мигли, тяло, но без проме -
ни по скалпа[1,2,16] (Фиг. 1. А. Alpecia partialis и Б. Alopecia mutifocalis).
АСОЦИИРАНИ ЗАБОЛЯВАНИЯ
АА често се свързва с коморбидни
състояния като атопия, автоимунитет и дисфункция на щитовидната
жлеза, витилиго, лупус еритематозус, псориазис, метаболитен синдром, инфекция с Helicobacter pylori, дефицит на желязо и витамин D, психиатрични заболявания, аудиологични и
офталмологични аномалии[1,2].
ДИАГНОЗА Диагнозата АА се поставя на базата на клиничния преглед и трихоскопията[1,2,4,5,15]. Биопсия е необходима
при наличие на единичен участък, който е резистентен на лечение, както и когато не може да се изключи
клинически цикатрициална алопеция[1,2,15]
ТРИХОСКОПИЯ Дермоскопският преглед на коса -
та и скалпа е известна под наименованието трихоскопия. Терминът е въведен Lidia Rudnicka и Malgorzata Olszewska през 2006. Трихоскопията е неинвазивен метод, разновид-
ност на дерматоскопията, при която се извършва оглед на скалпа и косата с помощта на стандартен дерма -
на косопада. Наличието на косми тип удивителен знак по границите на алопетичните участъци показва активността на заболяването. Други трихоскопски маркери за активността на АА са черни точки (пигментирани косъмчета, прекъснати или унищожени на нивото на скалпа), триангуларни косъмчета (имат дистален заострен край и проксимална част, скрита от белезникаво-сив воал), счупени косми (къси косми с нормални космени стебла, но с неправилните, накъсани дистални краища), заострени косми (дълги косми тип удивителен знак с проксималният стеснен край, а дисталният не може да се обхване от обектива на дерматскопа) и стеснения на Pohl-Pincus (зони с намалена дебелина по дължината на косменото стебло). Една от най-често срещаните трихоскопски характеристики на АА са жълтите точки. Те представлвяват празни фоликулярни отвори, изпълнени с кератин и себум. В АА те се появяват на групи, отразяващи броя на космите във фоликуларните единици. Тази находка преобладава при дълготрайно, неактивно заболяване. Въпреки това, може да присъства и при остра форма на АА. Възстановяването на косата може да се наблюдава, чрез трихоскопия. Знаците там са: новорастящи прави анагенни косми и/или кръгли косми (рав
или дифузен, цикатрициален или нецикатрициален. Например, при деца трябва да се има предвид tinea capitis, която обикновено се представя с инфламаторен инфилтрат в засегната зона и косми („тип черни точки“) отчупени на нивото на скалпа[1,2,4]; trichotillomania, тракционна алопеция, loose anagen hair syndrome, alopecia triangularis (alopecia congenitalis triangularis), конгенитални хипотрихози, ектодермални дисплазии. При парциално или дифузно засягане е необходимо да се мисли винаги и в посока syphilis secundaria[1,2,16]. АА може да се
заболяването има хроничен ход с
епизодична поява на единични обез -
космени полета. При 50 % от пациентите с АА partialis, спонтанен подраст
настъпва в рамките на 12 месеца, а при 66% - в рамките на 5 години.
Рискът от рецидив обаче е 85%. При АТ и АU шансът за пълно израстване на коса е 10%[1,2,16]. Предполага се, че ранната поява на АА има по-лоша
прогноза от късната. Децата с тежка и дълготрайна АА имат най-лоша прогноза. Приблизително при 80% от пациентите се наблюдава спонтанно израстване на коса или внезапни рецидиви. При други пациенти загубата на коса може да е постоянна[1,2,23]. От 5 до 10% от пациентите с АА partialis могат да преминат в АТ или АU. Ако АА се развие преди пубертета, рискът от АТ е 50 %, а при по-възрастните лица рискът е около 25%[1,2,19]. Изследванията показват, че началото на АА след 50-годишна възраст („АА с късно начало“) обикновено се свързва с по-слабо изразено заболяване и по-добра прогноза, и често антинуклеарните антитела са положителни[1,2,4,5]. Друг негативен прогностичен фактор е загубата на косми на веждите и/или миглите, както и косми извън скалпа. Точковидните депресии и трахионихията на ноктите предполагат повишен риск от развитие на АТ или AU, говорят за лоша прогнозата и сигнализи -
ИЗПОЛЗВАНА
1. Тодорова, Л. Клинични и терапевтични проучвания при алопеция ареата. Док. дис. МУ
2. 1. Абаджиева Ц. Нецикатризиращи
Лакс Бук, Пловдив, 2017; 12315. [ISSN 978-619-189-076-7]
1. Kavak A et al. HLA in alopecia areata. Int J Dermatol. 2000; 39(8): 589-92.
2. McMichael AJ et al. Alopecia in the united states: outpatient utilization and common prescribing patterns. J Am Acad Dermatol 2007; 57: S49-51
3. Mirzoyev SA et al. Lifetime incidence risk of alopecia areata estimated at 2.1% by Rochester Epidemiology Project, 19902009. J Invest Dermatol. 2014; 134(4): 11411142.
4. Rakowska A et al. Alopecia areata. Diagnostic and therapeutic recommendations of the Polish Dermatological Society. Part 1. Diagnosis and severity assessment.
лечението зависи от възрастта на пациента, продължителността и тежестта на АА. Целта на лечението при АА е възстановяване на косата и предотвратяване на заболяването. Обхватът от терапевтични възможности включва: локални, локално инжектирани или системни кортикостероиди (КС), топична имунотерапия, локален
Dermatology Review/Przegląd Dermatologiczny. 2023; 110(2): 89-100.
5. Rakowska A et al. Alopecia areata. Diagnostic and therapeutic recommendations of the Polish Society of Dermatology. Part 2: Treatment. Dermatology Review/Przegląd Dermatologiczny. 2023; 110(2): 101-120.
6. Villasante Fricke AC, Miteva M. Epidemiology and burden of alopecia areata: a systematic review. Clin Cosmet Investig Dermatol. 2015; 8:397-403.
7. Wasserman D et al. Alopecia areata. Int J Dermatol; 2007; 46: 121-131
8. Al-Mutairi N, Eldin ON. Clinical profile and impact on quality of life: seven years experience with patients of alopecia areata. Indian J Dermatol Venereol Leprol. 2011; 77(4): 489-93.
9. Tan E et al. The pattern and profile of alopecia areata in Singapore--a study of
219 Asians. Int J Dermatol. 2002; 41(11): 748-753.
10. Alkhalifah A et al. Alopecia areata update: part I. Clinical picture, histopathology, and pathogenesis. J Am Acad Dermatol. 2010; 62(2): 177-88.
11. Alkhalifah A. Alopecia Areata Update. Dermatol Clin. 2013; 31(1): 93–108.
12. Alkhalifah A et al. Alopecia areata update: part II. J Am Acad Dermatol. 2010; 62(2): 191–202.
13. Simakou et al. Alopecia areata: A multifactorial autoimmune condition. J Autoimmun. 2019; 98: 74-85.
14. Suchonwanit P, Kositkuljorn C, Pomsoong C. Alopecia Areata: An Autoimmune Disease of Multiple Players. Immunotargets Ther. 2021; 10: 299-312.
15. Meah N et al. The Alopecia Areata Consensus of Experts (ACE) study: Results of an international expert opinion on
minoxidil, локални иританти, системни имуносупресори, и други. Понастоящем, нововъведение при лечението на АА са JAK-инхибиторите, от които baricitinib се използва при възрастни и ritlicitinib от 12-годишна възраст [1,2] ЗАКЛЮЧЕНИЕ В заключение, алопеция ареата е сложно автоимунно заболяване с непредсказуемо протичане, чиято етиология включва генетични, имунологични и фактори на околната среда. Въпреки че спонтанни ремисии са възможни, заболяването често се свързва с различни коморбидни
терапевтични
включително инхибиторите на Janus-киназата, предлагат нови възможности за контрол на заболяването, но все още няма универсално ефективно лечение.
Благодарности: Към научния
treatments for alopecia areata. J Am Acad Dermatol. 2020; 83(1):123-130.
16. Finner AM. Alopecia areata: Clinical presentation, diagnosis, and unusual cases. Dermatol Ther. 2011; 24(3): 348–354.
17. Madani S, Shapiro J. Alopecia areata update. J Am Acad Dermatol. 2000; 42(4): 549-66.
18. Messenger AG. Alopecia areata. Disorders of hair. Rook’s text book of dermatology. 8th ed. In: Burns DA, Breathnach SM, Cox NH, Griffiths CE, editors. Oxford,UK: Blackwell publishing limited; 2010; 66: 31-38.
19. Seetharam, K. Alopecia areata: An update. Indian J Dermatol Venereol Leprol. 2013; 79(5), 563.
20. Waśkiel A et al. Trichoscopy of alopecia areata: An update. J Dermatol. 2018; 45(6), 692–700.
21. Dy LC, Whiting DA. Histopathology of alopecia areata, acute and chronic: Why is it important to the clinician? Dermatol Ther. 2011; 24: 369-374.
22. Whiting DA. The histopathology of alopecia areata in vertical and horizontal sections. Dermatol Ther. 2001; 14(4): 297–305.
23. Cho HH et al. Clinical characteristics and prognostic factors in early-onset alopecia totalis and alopecia universalis. J Korean Med Sci. 2012; 27(7): 799-802.
24. Dubois M et al. Quality of Life Group of the French Society of Dermatology. Quality of life in alopecia areata: a study of 60 cases. J Invest Dermatol. 2010; 130(12): 2830-3.
25. Gulec AT et al. The role of psychological factors in alopecia areata and the impact of the disease on the quality of life. Int J Dermatol. 2004; 43(5): 352–356.
Dermatofibrosarcoma protuberans (DFSP)
ВЪВЕДЕНИЕ Dermatofibrosarcoma protuberans
(DFSP) е рядък злокачествен мезенхимен тумор с нисък риск за метастазиране, бавен локален инвазивен
растеж и честа склонност към рецидивиране. Описан е за първи път от Taylor през 1890 г. като саркоматозен тумор, наподобяващ келоид. През 1924 г. Darier го обособява като от-
делно клиникопатологично състояние (фибросарком), а пълното му наименование е въведено
Счита се, че развитието на DFSP е свързано с хромозомна транслокация t(17;22)(q22;q13) имаща за резултат сливане на гените COL1A1 (collagen type I alpha 1) и PDGFB (platelet-derived growth factor subunit B). Тази генетична промяна активира рецептора и стимулира повишено производство на протеина PDGFB,
Диференциалната диагноза включва neurofibroma, leiomyoma, melanoma malignum, carcinoma basocellularis morpheaformis, keloid, sarcoma Kaposi, fibrosarcoma, dermatofibroma, nodular fasciitis и sarcoidosis[2,9,11]
При наличие на съмнителна лезия трябва да се извърши биопсия и хистопатологично изследване. DFSP е клетъчен тумор, съставен от мономорфни вретеновидни клетки с удължени ядра, минимална цитологична
атипия и нисък митотичен индекс (под 4 митози на поле с увеличение 10), разположени в колагенова строма. Туморните клетки често се разпространяват по протежение на септите на подкожната мастна тъкан. При имунохистохимично изследване DFSP показва в 80-90% от случаите силна дифузна експресия на CD34[2,4,9,11]. Хистопатологично DFSP може да има следните варианти: миксоиден, пигментен (Bednar tumor), миоиден, атрофичен, склерозиращ[17]
Като редки варианти се описват също тумори с инвазия на фасцията и тумори с фибросаркоматозна трансформация (DFSP-FS). При първите хистологично се наблюдават листоподобно разположение (“sheet-like pattern”), висока степен на клетъчен плеоморфизъм и множество митози, докато вторите са много по-агресивни и асоциирани с бърз растеж, висок риск от локални рецидиви, развитие на далечни метастази и дори летален изход. Във фибросаркоматозните участъци се наблюдават повече вретоновидни клетки, ядра и митози (средно 20 митози на поле с увеличение 10х), докато експресията на CD34 е пониска[1,2,4,9,10,12,16]
При пациентите с DFSP се препоръчва извършване на образни изследвания (рентгенография, ехографско изследване, КТ, ЯМР), които могат да дадат информация за големината на тумора, неговото локално разпространение и наличието на метастази, с което става възможно по-точно планиране на
дий 3 – наличие на отдалечени метастази. 2. Американски консенсус (American Joint Commission on Cancer for sarcomas) (2020):
TNM стадиране
T1 – тумор с размери до 5 cm и T2 – тумор с размери над 5 сm.
N0 – липса на метастази в лимфните възли и N1 – наличие на метастази в лимфните възли
Хистологични стадии: G1 – ниска степен или
добре диференциран тумор, G2 – средна степен или умерено диференциран тумор, G3 –
висока степен или недиференциран тумор. M0 – липса на далечни метастази и M1 – на -
личие на далечни метастази.
Клинични стадии I – Непротуберантни лезии вкл. атрофични или склеротични плаки, макулозни лезии или
малки нодулуси.
II – Протуберантен първичен тумор IIA – Повърхностен тумор без инвазия на под-
лежащата фасция IIB – Дълбок тумор с инилтриране на фасцията или разположен под нея III – Метастази в лимфните възли IV – Метастази в други органи Лечението на DFSP трябва да бъде мултидисциплинарно с участието на онколози, дерматолози, пластични хирурзи и хистопатолози[2,9,11]. Основен метод на лечение е оперативното отстраняване на тумора в широки граници (над 3 cm). Като най-подходящ се препоръчва методът на Mohs (Mohs surgery), при който се изрязват тънки слоеве кожа от засегнатия участък, които се изследват микроскопски и операцията продължава докато остане само здрава кожа. При ненапълно отстранени, неоперабилни и рецидивиращи ту-
мори се използва лъчетерапия[2]. При напреднали и метастазиращи тумори, както и за предоперативно намаляване на размера на тумора, се прилага системно таргетно лечение с Imatinib. При DFSP-FS се прилагат и три
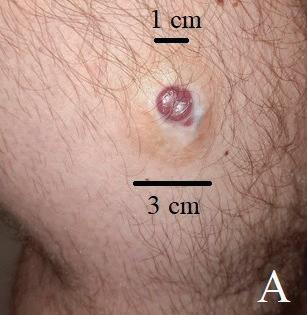
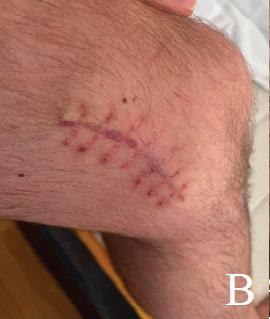
червено окръглено
образувание. Първоначално то било монето -
видно, но през последната година размерите му се увеличили значително.
Дерматологичен статус. На кожата на лявото бедро, по долно-медиалната повърхност,
има еритемно възловидно туморно изме -
нение с диаметър 1 cm, разположено върху
подлежащ дермохиподермален нодул с диа -
метър 3 cm. Кожата около централното образувание е белезникава, а в периферията леко кафеникава (Фиг. 1a). Не се палпират увеличени лимфни възли.
Параклиника. ПКК и биохимични
следоперативно лъчелечение.
Пациентът е проследен след 3
ОБСЪЖДАНЕ DFSP
рядък мезенхимен тумор,
локално агресивен растеж, нисък метастатичен потенциал и висока склонност към рецидивиране. Относителната 5, 10 и 15-годишна преживяемост на болните се определят съответно на 99.2%,
ция на крайниците и главата, хистологично по -
зитивни граници след недостатъчна резекция, повишен митотичен индекс. Локалното рецидивиране не е свързано с наличието на метастази[2]
Проучванията показват, че успехът на хирургичното лечение зависи от това, дали туморът е отстранен изцяло. При традиционната хирургия, поради близките граници на резекция, се съобщава 50-60% честота на рецидивите. Установено е, че при граница на резекция 1 cm около първичния тумор микроскопски остатъци от него остават в над 70% от пациентите, при 2 cm граници – при 20-40% от паци-
ентите, при 3 cm – при 9-15% от пациентите
и при 5 cm – при 5% от пациентите[2]. Пора-
ди това се препоръчва извършване на широ -
ка локална ексцизия (wide local excision; WLE)
в граници 5 сm, след която честотата на реци-
дивите е 0-6%. Широката резекция обаче има
някои недостатъци. При равномерно изрязва-
не в широки граници ненужно се отстраняват
здрави тъкани, което увеличава риска от ус-
ложнения, функционални и козметични дефе -
кти. Освен това, тя не може да се приложи при тумори със специална локализация, напр. на главата и шията. Обикновено туморите не са точна окръжност, а са асиметрични. Често те имат подобни на пипала странични проекции с дължина над 3 cm. Ето защо, като най-добър
хирургичен метод на лечение се приема т.нар. хирургия по Mohs (Mohs micrographic surgery; MMS). При нея се използват последователни хоризонтални срези с непосредствено микроскопско изследване след замразяване на отстранените тъкани. Това дава възможност микроскопски да се откриват разрастванията на тумора в съседните тъкани и те да бъдат отстранявани по-точно със съхраняване на здравите тъкани. Методът е предпочитан в определени анатомични зони и при лечение на деца. С MMS се получава по-ниска честота на рецидиви, отколкото при WLE – 2% срещу
замразените срези. Друг недостатък е, че MMS е по-комплексен и високо специализиран метод, който изисква обучение, отнема повече време, по-скъп е и не е наличен на всички места. Когато използването на MMS не е налично, извършването на широка ексцизия с хирургични граници минимум 3-5 сm
е обикновено достатъчно и приемливо[3,9,10,13].
Свързаната със заболяването смъртност след лечение с двата хирургични метода на класически DFSP е сходна (0.7% и 0.9%), докато след лечение на рецедивиращи тумори след MMS смъртността е 1%, докато след WLE смърт-
ността е 3-5%[5]
В някои случаи на DFSP се прилагат лъчетерапия и химиотерапия.
Лъчетерапията е показана при агресивни тумори, първично неоперативни тумори, пациенти с хистологично позитивни граници, когато по-нататъшна хирургия е невъзможна, или като допълнителна терапия след повторна резекция на рецидивиращ тумор. Препоръчва се курсова доза 50-70 Gy. Зоната на облъчване трябва да включва мястото на тумора и граници около него широки 3-5 cm. Лъчетерапия не трябва да се прилага при напълно отстранени тумори с негативни граници. Нейните странични ефекти включват оток, фиброза, некроза, отпадане на кожни пластики[2,6]
Химиотерапията при DFSP включва таргетна терапия с препарата Imatinib (инхибитор на tyrosine kinase), който е одобрен от FDA за лечение на заболяването. Установено е, че той инхибира растежа на туморните клетки, но само при индивидите с установена хромозомна транслокация t[17,22]. Поради това, преди започване на терапията се препоръчва изследване с флуоресцентен in situ хибридизационен метод (FISH) или обратно транскриптазна полимеразна верижна реакция (RT-PCR)
дневна доза 600 mg води
хипоцелуларни области, които
да съдържат джобове с жизнеспособна туморна тъкан. Освен това вече има описани случаи на резистентност, при които са открити нови
мутации в гените. При тези пациенти може да се приложи препаратът Sunitinib, като при 40% от тях настъпва частичен или пълен отговор. Страничните кожни ефекти на лечението с Imatinib включват макулопапулозни, лихеноидни, псориазиформени и пустулозни обриви, както и синдром
на Stevens-Johnson syndrome. Общите странични действия включват сърдечна недостатъчност, хематологична и хепатална токсичност[2]
При описания от нас случай се касае за първичен протуберантен дерматофибросарком, който преди установяване на диагнозата е третиран с лазер, а след нейното хистопатологично потвърждаване не е извършена допълнителна хирургична резекция на околните тъкани. Това вероятно е причина за непълно отстраняване
1. Achouri L., Triki A., Bouzaiene H. et al. Transformed dermatofibrosarcoma protuberans: A series of nine cases and literature review. J Dermatology & Dermatologic Surgery. 2015’ 64 (1). 2. Acosta A., Velez C. Dermatofibrosarcoma protuberans. Curr. Treat. Options in Oncol. 2017; 18: 56.
3. Alhabeeb A., Idrees A., Alhowaish T. et al. Outcome of Surgical Management of Dermatofibrosarcoma Protuberance: A Single-Institution Multidisciplinary Approach. Orthop Res Rev 2023; 15: 237243.
4. Apalla Z., Liopyris K., Kyrmanidou E. et al. Clinical and Dermoscopic Characteristics of Cutaneous Sarcomas: A Literature Review. Diagnostics 2023, 13, 1822.
5. Crum O., O'Hern K., Demer A.,
Brewer J. Disease-Specific Mortality of Dermatofibrosarcoma Protuberans After Mohs Surgery Versus Wide Local Excision: A Systematic Review and Meta-Analysis. Dermatol Surg 2024; 50 (4): 317-321.
6. Fionda B., Loperfido A., Di Stefani A. et al. The Role of Postoperative Radiotherapy in the Management of Dermatofibrosarcoma Protuberans: A Multidisciplinary Systematic Review. J Clin Med 2024; 13 (6): 1798.
7. Han H., Lim S., Park Y., Rhie J. Congenital Dermatofibrosarcoma Protuberans: A Case Report and Literature Review. Ann Dermatol 2015; 27 (5): 597-600.
8. Khan S., Yetiskul E., Niazi M. et al. Metastatic Fibrosarcomatous Transformation of Dermatofibrosarcoma Protuberans With Lung Metastasis: A Case Report. Cureus 2024; 16 (5): e59742.
9. Lim S., Ramaiya A., Levell N. et al. Review of dermatofibrosarcoma protuberans. Clin Exp Dermatol 2023; 48 (4): 297-302.
10. Marcoval J., Moreno-Vílchez C., Torrecilla-Vall-Llosera C. et al. Dermatofibrosarcoma Protuberans: A Study of 148 Patients. Dermatology. 2024; 240 (3): 487–493.
11. Menon G., Brooks J., Ramsey M. Dermatofibrosarcoma Protuberans. https:// www.ncbi.nlm.nih.gov/books/NBK513305/ Last Update: April 18, 2024
12. Mentzel T., Beham A., Katenkamp D. et al. Fibrosarcomatous ("highgrade") dermatofibrosarcoma protuberans: clinicopathologic and immunohistochemical study of a series of 41 cases with emphasis on prognostic significance. Am J Surg Pathol 1998; 22 (5): 576-87.
13. Rust D., Kwinta B., Geskin L. et al. Surgical management of dermatofibrosarcoma protuberans. J Surg Oncol 2023; 128 (1): 87-96.
14. Sanabria A., Pinillos P., ChiesaEstomba C. et al. Comparing Mohs micrographic surgery and wide local excision in the management of head and neck dermatofibrosarcoma protuberans: a scoping review. J Dermatolog Treat 2024; 35 (1): 2295816.
15. Segura S., Salgado R., Toll A. et al. Identification of t(17;22)(q22;q13) (COL1A1/ PDGFB) in dermatofibrosarcoma protuberans by fluorescence in situ hybridization in paraffin-embedded tissue microarrays. Hum Pathol 2011; 42 (2): 176-84.
17. Trinidad C., Wangsiricharoen S., Prieto V., Aung P. Rare Variants of Dermatofibrosarcoma Protuberans: Clinical, Histologic, and Molecular Features and Diagnostic Pitfalls. Dermatopathology (Basel) 2023; 10 (1): 54-62.
18. Zamora A., Apodaca J., Contreras D. A Review for Dermatofibrosarcoma Protuberans. International Journal of Medical Science and Clinical Research Studies. 2023; 3 (12): 3139-3141.
19. Zeaiter N., Aoun C., Sfeir J., et al. Dermatofibrosarcoma Protuberans Arising From a Chronic Wound in the Left Shoulder: A Case. Report. Cureus 2024; 16 (3): e55638. DOI 10.7759/cureus.55638
16. Szollosi Z., Nemes Z. Transformed dermatofibrosarcoma protuberans: a clinicopathological study of eight cases. J Clin Pathol 2005; 58:751–756





























































































































