

Mi sangremi salud

"Vinculando


UnprogramaexclusivodeHealCanadá
la salud con el saber y la difusión de la causa"
Qué es la terapia con células T CAR y cuál es su relevancia? Nueva esperanza para los pacientes con enfermedad de células falciformes y betatalasemia.
Finalmente, un tratamiento para pacientes anémicos con mielofibrosis! Nuevas alternativas terapéuticas para la leucemia mieloide aguda y la carencia de hierro. Estás preparado para ASH 2024?
Número 4 de diciembre de 2024
Bienvenido
Qué es la terapia con células T CAR y cuál es su relevancia?
Aprobación de Health Canada para trastornos hematológicos en 2024
Nuevaesperanzaparalospacientesconenfermedaddecélulas falciformesobeta-talasemia.
Finalmente,unaopcióndetratamientoefectivaparapacientes anémicosconmielofibrosis!
QuéavancesexistenparalospacientesconLMA?
Dosnuevasalternativasparapacientescondeficienciadehierro.
Estás preparado para ASH 2024?
Pruebas clínicas y cuestionarios a pacientes

Bienvenidos a la Publicación Digital Mi Sangre, Mi Salud
Bienvenidos al cuarto número de la revista "Mi sangre, mi salud". Esta edición de diciembre se centra en los enfoques innovadores de tratamiento. Recientemente, los pacientes con trastornos sanguíneos han tenidolaoportunidaddeaccederalascélulas CAR-T, la terapia génica y nuevos tratamientos dirigidos. Estas innovaciones son fundamentales para mejorar la expectativadevidaylacalidaddevidadelos pacientes.
Con esta publicación, nuestro objetivo es cumplir con la misión de Heal Canada de empoderaralospacientesparaqueaccedan a servicios de mayor calidad y equitativos. Agradecemos sinceramente a nuestros lectores por su continuo interés y apoyo. Su compromiso nos motiva a ofrecer contenido valioso y esclarecedor para promover la atenciónmédicacentradaenelpaciente.
Agradecemos tu participación en nuestro viaje y te damos la bienvenida a este reveladornúmero!
Departedenuestroequipocomprometido



Cheryl Petruk, MBA B.Mgt. Director general y fundador de Heal Canada

Brigitte Leonard, Doctora en Filosofía. Director científico de Mi sangre, mi salud.
Heal Canada es una entidad sin ánimo de lucro registrada en Canadá sanacanadaorg
Descargo de responsabilidad: La revista digital Patient Advocacy proporciona información general y recursos para fomentar el empoderamiento y la concienciación de los pacientes El contenido no reemplaza el asesoramiento o tratamiento médico profesional Siempre consulte con profesionales de la salud cualificados para recibir orientación personalizada sobre su condición o situación médica específica

Qué es la terapia con células T CAR y cuál es su relevancia?
Cheryl Petruk, Máster en Administración de Empresas
La terapia con células T que utilizan receptores de antígenos quiméricos (CAR) representa un avance significativo en el ámbito de la inmunoterapia y brinda esperanzas a los pacientes con ciertos tipos de cáncer que han mostrado resistencia a los tratamientos convencionales, como la quimioterapia y la radiación. Este enfoque innovador consiste en la modificación genética de las propias células inmunitarias del paciente para combatir el cáncer de manera más efectiva. Al aprovechar los mecanismos de defensa naturales del organismo, la terapia con células T CAR ha abierto nuevas oportunidades para el tratamiento de los cánceres hematológicos y se está ampliando hacia el tratamiento de los tumores sólidos.
En este artículo, examinamos los principios de la terapia con células T CAR, su relevancia en la batalla contra el cáncer, su funcionamiento, los tipos de enfermedades que aborda y el futuro de este tratamiento innovador. También abordamos los desafíos y los riesgos potenciales relacionados con la terapia con células T CAR y subrayamos la importancia de la defensa de los pacientes para aumentar el acceso y mejorar los resultados.
CómooperalaterapiaconcélulasTCAR?
En esencia, la terapia con células T CAR es un tipo de transferencia adoptiva de células. Se trata de una forma de inmunoterapia en la que se recogen las células inmunitarias de un paciente, se modifican y luego se reinfunden en el organismo para atacar las células cancerosas. La terapia con células T CAR se enfoca específicamente en las células T, un tipo de glóbuloblancoquedesempeñaunpapelfundamentalenlarespuestainmunitaria.

ElprocedimientodeterapiaconcélulasTCARcomprendevariospasosfundamentales: Obtención de células T: en primer lugar, se extrae sangre del paciente y se aíslan las células T a través de un procedimiento denominado leucoféresis. Posteriormente, estas células se envían a unlaboratorioparasumodificacióngenética.
Modificación genética: en el laboratorio, las células T son alteradas genéticamente para que expresen un receptor de antígeno quimérico (CAR) en su superficie. Este receptor permite que las células T identifiquen y se adhieran a un antígeno específico presente en la superficie de las célulascancerosas.
Expansión de células T alteradas: una vez alteradas, las células T CAR se multiplican en grandes cantidades. Este proceso asegura que haya suficientes células modificadas para atacar y eliminarelcáncerdemaneraeficaz.
Infusión: las células T CAR alteradas se infunden nuevamente en el paciente, donde inician la búsqueda y destrucción de las células cancerosas. Estas células alteradas siguen proliferando enelorganismodelpaciente,loqueofreceunavigilanciaconstantecontraelcáncer.
Ataque a las células cancerosas: las células T con CAR están diseñadas para identificar proteínas específicas en la superficie de las células cancerosas, como la CD19, que se encuentra frecuentemente en ciertos tipos de cáncer hematológico. Cuando las células T con CAR se adhieren a estas proteínas, provocan una fuerte respuesta inmunitaria que elimina las célulascancerosas.
LarelevanciadelaterapiaconcélulasTCAR
LaterapiaconcélulasTCARconstituyeunavanceimportanteeneltratamientodelcáncer pordiversasrazones:
Eficaciaeneltratamientodecánceresrefractarios:Unodelosaspectosmásdestacadosde laterapiaconcélulasTCARessuefectividadeneltratamientodecánceresquenohan respondidoaotrasmodalidadesterapéuticas.Lospacientesconcánceresavanzados, recidivantesorefractarioshanlogradoremisionescompletasconlaterapiaconcélulasTCAR cuandootrostratamientoshanfallado
Efectosprolongados:adiferenciadelostratamientosconvencionalescomolaquimioterapia, queamenudorequierenrepetición,lascélulasCARTpuedenpermanecerenelorganismo delpacientedurantemesesoinclusoaños.Estapermanenciaalargoplazopermitequeel sistemainmunitariocontinúeluchandocontralascélulascancerosas,loquedisminuyeel riesgoderecurrencia
Medicinapersonalizada:laterapiaconcélulasTCARrepresentauntratamientoaltamente individualizado.AlemplearlaspropiascélulasTdelpaciente,seajustaaltipodecáncer específicodecadapersona,loqueincrementalasprobabilidadesdeéxitoydisminuyeel riesgoderechazooreaccionesinmunitariasadversas.
Enfoqueinnovadorparalostumoressólidos:aunquelaterapiaconcélulasTCARhamostrado mayoreficaciaeneltratamientodecáncereshematológicos,seestánllevandoacabo esfuerzosparaextendersuaplicaciónatumoressólidos,comoelcáncerdemama,elcáncer depulmónyelglioblastoma.Apesardequelostumoressólidospresentandesafíos particulares,losavancesenlatecnologíadecélulasTCARsonalentadoresparael tratamientodeestoscánceresmáscomplejos
EnfermedadesabordadasconterapiadecélulasTCAR
LaterapiaconcélulasTCARhamostradounéxitosignificativoeneltratamientode determinadostiposdecáncerhematológico.Acontinuación,seenumeranalgunosejemplos deenfermedadesenlasqueseestáaplicandoestaterapia:
Leucemia linfoblástica aguda (LLA)
La terapia con células T CAR ha demostrado ser especialmente efectiva en el tratamiento de pacientes con leucemia linfoblástica aguda (LLA) de células B, un tipo de cáncer que afecta la sangre y la médula ósea, principalmente en niños Los pacientes con LLA que presentan recaídas o son refractarios han mostrado tasas de remisión notables tras recibir la terapia con células T CAR. Por ejemplo, Kymriah (tisagenlecleucel), la terapia con células T CAR aprobada por la FDA, fue la primera terapia génica autorizada en los EE. UU. para la LLA, y evidenció altas tasas de remisión duradera en los pacientes (Maude et al., 2018). Health Canada aprobó el medicamento desarrollado por Novartis en mayo de 2019.

2. Linfoma difuso de células B grandes (DLBCL)
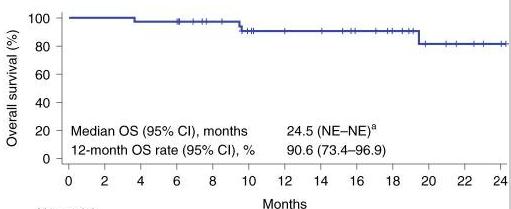
Otro ámbito en el que la terapia con células T CAR ha tenido un impacto significativo es el tratamiento del linfoma difuso de células B grandes (DLBCL), que es la forma más prevalente de linfoma no Hodgkin. Para los pacientes que no han tenido respuesta a otros tratamientos, las terapias con células T CAR como Yescarta (axicabtagene ciloleucel) han ofrecido nuevas esperanzas, resultando en altas tasas de respuesta (ORR) (a), respuesta prolongada (DOR) (b) y supervivencia prolongada (OS) (c) (Neelapu et al., 2017).

ORR:Tasaderespuestatotal
CR:RespuestacompletaSD: EnfermedadestablePR: Enfermedadenprogresiónn: cantidaddepacientes
DOR:TiempoderespuestaNR:No logradoNE:Noevaluado

OS:SupervivenciaglobalNE: Noevaluable
3. Mieloma múltiple
Si bien la terapia con células T CAR ha demostrado ser la más efectiva en las neoplasias malignas de células B, su uso en el mieloma múltiple está en aumento El mieloma múltiple es un cáncer de células plasmáticas, y las terapias con células T CAR dirigidas al antígeno de maduración de células B (BCMA) han mostrado resultados alentadores Ide-cel (idecabtagene vicleucel), la primera terapia con células T CAR aprobada para el mieloma múltiple, ha producido respuestas tumorales significativas en pacientes con enfermedad recidivante o refractaria (Munshi et al., 2021).
4. Leucemia linfocítica crónica (LLC)

Se está investigando la terapia con células T CAR en pacientes con leucemia linfocítica crónica (LLC), un cáncer hematológico de crecimiento más lento. Aunque la LLC ha mostrado mayor resistencia a la terapia con células T CAR en comparación con la LLA y el LDCBG, los ensayos clínicos en curso se centran en optimizar los tratamientos con células T CAR para esta población de pacientes.
Desafíos y riesgos de la terapia con células T CAR.
A pesar de su potencial transformador, la terapia con células T CAR enfrenta desafíos y riesgos.
Síndrome de liberación de citoquinas (SLC)
Uno de los efectos secundarios más serios de la terapia con células T CAR es el síndrome de liberación de citoquinas (SLC) Esto sucede cuando las células T modificadas genéticamente provocan una respuesta inmunitaria intensa, resultando en altos niveles de moléculas inflamatorias conocidas como citoquinas. Los síntomas pueden oscilar desde leves (fiebre, fatiga) hasta graves (presión arterial baja, dificultad para respirar) y, en ciertos casos, el SLC puede ser potencialmente mortal. La detección temprana y el tratamiento adecuado son fundamentales para reducir los riesgos asociados con el SLC.


2. Neurotoxicidad
Otro posible efecto secundario es la neurotoxicidad, que puede provocar confusión, convulsiones y otros síntomas neurológicos. Aunque no se comprende completamente el mecanismo exacto que causa la neurotoxicidad inducida por las células T CAR, parece estar vinculada a la intensa activación inmunitaria que desencadena la terapia La mayoría de los casos de neurotoxicidad son reversibles con la intervención médica adecuada

3. Accesibilidad y disponibilidad
La terapia con células T CAR es complicada y costosa, y el precio del tratamiento asciende a cientos de miles de dólares. Esto suscita preocupaciones sobre el acceso y la asequibilidad, especialmente para pacientes en entornos de bajos ingresos o en países con cobertura de atención médica limitada. Ampliar el acceso a la terapia con células T CAR demanda esfuerzos continuos en defensa de los pacientes, políticas de atención médica y modelos de financiamiento innovadores.
El porvenir de la terapia con células T CAR
A medida que la investigación avanza, el futuro de la terapia con células T CAR se presenta como prometedor. Los científicos están perfeccionando la tecnología de células T CAR para aumentar su seguridad, eficacia y aplicabilidad a una variedad más amplia de cánceres.
Algunas áreas de investigación en curso incluyen:
Abordaje de tumores sólidos: los científicos están trabajando en nuevas terapias con células T CAR que pueden superar los desafíos específicos de los tumores sólidos, como el denso microambiente tumoral y los mecanismos de evasión inmunológica.
Reducción de los efectos adversos: se están llevando a cabo iniciativas para crear terapias con células T CAR que reduzcan el riesgo de CRS y neurotoxicidad. Una estrategia alentadora implica el uso de interruptores de "activación y desactivación" que permitan a los médicos gestionar la actividad de las células T CAR con mayor exactitud.
Combinación de terapias: la integración de la terapia de células T CAR con otros tratamientos, como inhibidores de puntos de control o terapias convencionales contra el cáncer, puede aumentar su eficacia y ampliar su aplicación
Elroldeladefensadelpaciente
La defensa de los pacientes es esencial para aumentar el acceso a la terapia con células T CARyasegurarquelospacientesentiendansusopcionesdetratamiento Lasorganizaciones de defensa pueden contribuir a cerrar la brecha entre los pacientes, los proveedores de atención médica y los investigadores al promover la concienciación, apoyar la financiación de la investigación y abogar por cambios en las políticas que amplíen el acceso a estas terapiasquesalvanvidas.
Además,losdefensorespuedenesforzarseporasegurarquelosensayosclínicosparaterapias concélulasTCARsediseñenconsiderandolasnecesidadesdelospacientes,contribuyendo a optimizar los protocolos de tratamiento y a ampliar la elegibilidad para un espectro más ampliodepacientes.
Conclusión
La terapia con células T CAR representa uno de los avances más significativos en el tratamiento del cáncer, brindando esperanza a los pacientes con opciones limitadas. Su capacidad para lograr remisiones duraderas en cánceres previamente resistentes ha transformado el tratamiento de los cánceres hematológicos, y la investigación en curso está ampliando su aplicación a otros tipos de neoplasias malignas Aunque persisten desafíos, especialmente en la gestión de los efectos secundarios y la ampliación del acceso, el futuro delaterapiaconcélulasTCAResprometedor.Amedidaquelosdefensoresdelospacientes continúanabogandoporunaccesomásamplioyunamejorcomprensión,estaterapiatiene elpotencialdesalvarnumerosasvidas.




Tratamientos innovadores para enfermedades hematológicas: aprobación de Health Canada en 2024 Brigitte Leonard, Doctora en Filosofía.
Según la base de datos de Salud Canadá, la agencia evaluó y tomó decisiones sobre la comercialización de 53 productos en 2024. De estos 53, únicamente 44 fueron autorizados para su comercialización en Canadá (83%). De estos 44, solo 26 eran nuevas sustancias activas y siete estaban asociadas con enfermedades de la sangre.
En este artículo, encontrará un resumen de cinco productos aprobados en 2024 y cómo pueden impactar la vida del paciente. Entre ellos, se incluye una auténtica innovación revolucionaria y una aprobación de primera categoría.
Agradecemos a Vertex Pharmaceuticals, GSK, Servier, CSL Behring y KYE Pharmaceuticals por la creación de estos nuevos tratamientos. Agradecemos su apoyo a los canadienses que sufren enfermedades hematológicas para mejorar su calidad de vida.
Nueva esperanza para los pacientes con enfermedad de células falciformes o beta-talasemia.
Salud Canadá autorizó la venta de Casgevry en septiembre de 2024 para el tratamiento de dos trastornos sanguíneos hereditarios: la anemia de células falciformes y la beta-talasemia.
En estas dos enfermedades genéticas se ve comprometida la producción de hemoglobina, que se une al oxígeno en los pulmones y lo transporta a otras áreas del cuerpo (Figura 1). Cada glóbulo rojo que circula por los vasos sanguíneos contiene varios cientos de millones de moléculas de hemoglobina.
La hemoglobina siempre está compuesta por cuatro unidades denominadas cadenas, cada una de las cuales contiene un hemo asociado con hierro (Figura 2) Los tipos de cadenas de hemoglobina varían antes y después del nacimiento. La forma predominante de hemoglobina (Hemoglobina F) en el feto está compuesta por cuatro cadenas: dos alfa y dos gamma El organismo cesará la producción de esta variante aproximadamente a las 12 semanas tras el nacimiento. En ese momento, la variante de Hemoglobina A, que consta de cuatro cadenas (dos alfa y dos beta), se convertirá en la más predominante y se mantendrá durante el resto de nuestras vidas (Figura 2) La estructura y los tipos de cadenas son fundamentales para la función de la hemoglobina.


En la enfermedad de células falciformes y la beta-talasemia, ocurre una mutación en el gen responsable de la producción de la cadena beta en el cromosoma 11. Esta mutación resulta en la generación de cadenas beta anormales y afecta la producción de glóbulos rojos y el transporte de oxígeno.

Casgevy (exa-cel: exagamglogene autotemcel) es una terapia génica creada por Vertex Pharmaceuticals y CRISPR Therapeutics La FDA la autorizó en Estados Unidos para el tratamiento de la anemia de células falciformes en diciembre de 2023 y de la beta-talasemia en enero de 2024 La EMA la aprobó para el mercado europeo en febrero de 2024
Casgevy es la primera terapia génica autorizada que no emplea un vector viral. Esta terapia utiliza la tecnología CRISPR/Cas9 para modificar el ADN de las células del paciente responsables de la producción de glóbulos rojos Casgevy no corrige el gen mutado en el cromosoma 11, sino que estimula la producción de la forma fetal de hemoglobina, que se silencia tras el nacimiento. La forma fetal (cadenas gamma) sustituye las cadenas beta defectuosas en la estructura de la hemoglobina, lo que ayuda a resolver los problemas asociados con la cadena beta anormal
Casgevyenlaanemiadecélulasfalciformes
En el estudio clínico CLIMB SCD-121, los pacientes que sufrían más de tres crisis al año dejaron de experimentarlas tras el tratamiento con Casgevy. Durante un año, el 97 % de los pacientes con anemia falciforme permanecieron libres de crisis. Además, los participantes no requirieron hospitalización debido a crisis durante ese año. Los beneficios clínicos se atribuyen a la capacidad de los participantes para lograr aumentos tempranos y sostenidos en los niveles de hemoglobina total y fetal, alcanzando niveles casi normales a los 6 meses. Los pacientes lograron mantener un hemograma mejorado a lo largo del tiempo
Cómo opera?
En el hospital, se obtienen de la médula ósea las células madre progenitoras de los pacientes que generan células sanguíneas maduras.
Las células del paciente se remiten a una instalación central para su procesamiento:
Enriquecimiento de células madre
Modificación de células madre con Casgevy (denominada edición)
Proliferación de células madre modificadas
Las células serán analizadas, congeladas y enviadas de regreso al hospital
3) Una vez confirmadas las células modificadas viables, los pacientes se someterán a quimioterapia intensiva (busulfán) para eliminar todas las células madre progenitoras en su médula ósea.
4) Tras la quimioterapia, se infundirán nuevamente células madre progenitoras modificadas a los pacientes. Los pacientes requerirán un mes para recuperarse y alcanzar una producción de células sanguíneas normal o casi normal.

LosefectosadversosmásfrecuentesenelestudioCLIMBSCD-121puedenserprincipalmente atribuidos al tratamiento con busulfán. Estos incluyen plaquetas y glóbulos blancos bajos, llagas bucales, náuseas, dolor musculoesquelético, dolor abdominal, vómitos, neutropenia febril(fiebreyrecuentobajodeglóbulosblancos),cefaleaypicazón.
Casgevyenlatalasemiabeta
En el estudio clínico CLIMB THAL-111 se han incluido pacientes con una considerable necesidaddetransfusión.Estospacientesrecibieron,enpromedio,34unidadesdesangreal año,loqueequivaleaunatransfusióncadasemanaocadadossemanas.Apesardelnivel de transfusión recibido, presentaban un nivel de hemoglobina por debajo de lo normal. Además, estos pacientes mostraban un alto exceso de hierro en la sangre, el hígado y el corazón, lo que los exponía a un riesgo de complicaciones debido al daño orgánico. El tratamiento con Casgevy resultó en independencia transfusional en el 91% de los pacientes incluidos en el ensayo. El perfil de seguridad fue en general coherente con la quimioterapia intensivaconbusulfán.Noseregistraronmuertesnicasosdecáncer.
Enresumen
Los resultados de estos dos ensayos clínicos indican que una infusión única de Casgevy produce incrementos tempranos y sostenidos en los niveles de hemoglobina total y fetal, lo queconllevaunamejoraduraderaenlascondicionesylacalidaddevidadelospacientes.
Finalmente, una alternativa de tratamiento para pacientes anémicos con mielofibrosis!
Lamielofibrosisesuntipodecáncerpococomúnquesedistingueporlaproducciónexcesiva de células sanguíneas anormales y de marcadores inflamatorios conocidos como citocinas. Desde la aprobación del primer inhibidor de JAK, Jakavi, en 2011, el tratamiento de la mielofibrosis ha experimentado mejoras significativas Los inhibidores de JAK son terapias dirigidas para el cáncer, como la mielofibrosis, ya que la enfermedad se origina por mutacionesqueactivandemaneraexcesivalavíaJAK/STAT.
Actualmente,laFDAhaautorizadountotaldecuatroinhibidoresdeJAK: Jakafi/Jakavi(Ruxolitinib)2011
Inrebic(Fedratinib)enelaño2019
Vonjo(Pacritinib)enelaño2022
Ojjaara(Momelotinib)en2023
Hastaelmesanterior,HealthCanadasolohabíaaprobadodosinhibidoresdeJAK: Jakafi/Jakavi(Ruxolitinib)2012
Inrebic(Fedratinib)enelaño2023
Ennoviembrede2024,SaludCanadáotorgólaaprobaciónaOjjaara,fabricadoporGSK.
Por qué la inclusión de Ojjaara en las opciones de tratamiento canadienses es una buena noticiaparalospacientes?
La anemia generalmente se encuentra presente en el momento del diagnóstico y, con el tiempo, se desarrolla en casi todos los pacientes debido a la progresión del cáncer. La anemia y la transfusión de sangre son factores de riesgo asociados con la transformación leucémica y la mortalidad La mayoría de los tratamientos disponibles para la mielofibrosis agravanlaanemiarelacionadaconlaenfermedad.Paraprevenircomplicacionesasociadas con la anemia, los médicos prescribirán una dosis baja de inhibidor de JAK, lo que limita su eficacia.
Ojjaara es tan efectivo como otros inhibidores de JAK. No obstante, a diferencia de otras terapias, puede mejorar la anemia al facilitar la producción de células sanguíneas. Los ensayosSIMPLIFYhandemostradoquelospacientespuedenalcanzarnivelessanguíneosmás saludables y volverse independientes de las transfusiones. Algunos pacientes incluso podrían posponerprocedimientoscomplejoscomoeltrasplantegraciasaestetratamiento.
Este beneficio exclusivo de Ojjaara (MMB) se atribuye a su capacidad para influir en una molécula denominada ACVR1. Al inhibir ACVR1, Ojjaara disminuye la producción de hepcidina. Los niveles de hepcidina suelen ser superiores a lo normal en pacientes con mielofibrosis. La disminución de la hepcidina facilita una mejor regulación del hierro y promueve la producción de glóbulos rojos en pacientes con mielofibrosis.
Conclusión

Actualmente, los pacientes con mielofibrosis que sufren de anemia podrán acceder a un inhibidor de JAK que puede aliviar sus síntomas, disminuir el tamaño del bazo y extender su vida, al mismo tiempo que mejora su calidad de vida (CdV).
Qué avances existen para los pacientes con LMA?
En julio de 2024, Health Canada autorizó TIBSOVO para el tratamiento de dos tipos de cáncer con una mutación específica denominada IDH1: leucemia mieloide aguda (LMA) y colangiocarcinoma. Tibsovo (ivosidenib) fuedesarrolladoyrespaldadoporServier.
LospacientesconleucemiamieloideagudapositivaparaIDH1presentanun pronóstico menos favorable al ser tratados con la terapia actual en comparación con aquellos sin la mutación. Solo la mitad de los pacientes conleucemiamieloideagudaIDH1+suelensobrevivirdespuésdedosaños.
Durante el estudio clínico en LMA, la incorporación de TIBSOVO al tratamiento estándar ofreció significativos beneficios clínicos tanto a corto comoalargoplazo,manteniendounperfildeseguridadaceptable.

La incorporación de TIBSOVO al tratamiento estándar triplicó la tasa de respuesta completa.
La proporción de participantes que se convirtieron en independientes de las transfusiones también se triplicó Ser independiente de las transfusiones es fundamental para mejorar la calidad de vida de los pacientes.
La incorporación de TIBSOVO al tratamiento estándar incrementó las tasas de supervivencia, y la mejora se sostiene a lo largo del tiempo. Con TIBSOVO, las posibilidades de seguir vivo aumentan en un 67% y la supervivencia media es de 24 meses en comparación con 7,9 meses.



En resumen
Según especialistas médicos en LMA, incorporar TIBSOVO al tratamiento estándar debería establecerse como el nuevo estándar de atención para pacientes con LMA IDH1+ debido a que mejora la tasa de respuesta, extiende la supervivencia, disminuye las necesidades de transfusión y optimiza la calidad de vida.
Dos nuevas alternativas para pacientes con deficiencia de hierro.
Elhierro(Fe)esunmineralfundamentalquecumplediversasfunciones importantes en el organismo humano. Este mineral se asocia con varias proteínas necesarias para el correcto funcionamiento; el hierro es crucial para el transporte de oxígeno y la generación de energía. Sin hierro, el cerebro, los músculos y el sistema inmunológico no pueden operar de manera adecuada. Además, niveles apropiados de hierro son indispensables para el crecimiento y el desarrollo, especialmenteenbebés,niñosymujeresenestadodegestación.
El nivel de hierro se encuentra estrictamente controlado en un individuo sano, dado que un exceso de hierro puede ocasionar diversos problemas de salud graves debido al daño a los órganos. La regulación abarca varios mecanismos: la absorción de nutrientes y el reciclaje Adiferenciadeotrosminerales,elorganismonodisponede un mecanismo activo para eliminar el exceso de hierro, por lo que la regulacióndelaabsorciónresultafundamental.
La carencia de hierro puede presentarse por diversas razones, y entenderestascausaspuedefacilitarsucontrolyprevención.

Pérdida de sangre: menstruación, hemorragia gastrointestinal, intervención quirúrgica o traumatismo.
Ingestainsuficientedehierro:dietas
Incrementodelasnecesidadesdehierro:lactantes,niñosyembarazo
Absorcióndeficientedehierrocausadaporcondicionesmédicas,medicamentosydietas.
Lossuplementosdehierropuedensernecesarioscuandolospacientesmuestransíntomasde deficiencia de hierro, tales como baja energía, fatiga, falta de concentración y dificultad pararespirardurantelaactividadfísica
En agosto de 2024, Health Canada aprobó ACCRUFER (maltol férrico), un tratamiento oral para la anemia por deficiencia de hierro La FDA había aprobado este producto en 2019. KYE Pharmaceutical adquirió la licencia de Accrufer para el mercado canadiense de Shield Therapeutics. El estudio
AEGIS-H2H demostró que Accrufer no era inferior a la terapia con hierro intravenoso. Con Accrufer, es posible mejorar la anemia por deficiencia de hierro sin requerir administración hospitalaria. Además, se trata de una formulación sin sal de hierro férrico, lo que ofrece una alternativa a las terapias orales con hierro a base de sal. También presenta menos efectos secundarios gastrointestinales en comparación con los que se observan típicamente con las terapias a base de sal.
En marzo de 2024, Health Canada autorizó FERINJECT (carboximaltosa férrica), que fue distribuido por CSL Behring. Este es un suplemento intravenoso de hierro que se utiliza para tratar la anemia ferropénica en pacientes de un año o más cuando las formulaciones orales de hierro no son toleradas ni efectivas. FERINJECT también puede abordar la deficiencia de hierro en pacientes adultos con insuficiencia cardíaca para mejorar la capacidad de ejercicio.





Estás preparado para ASH 2024?
Se anticipa que más de 30.000 hematólogos e investigadores especializados en hematología participen en la 66.ª Reunión y Exposición Anual de la Sociedad EstadounidensedeHematología(ASH)enSanDiego.Elañoanterior,las32.000personas que asistieron a la conferencia presentaron sus investigaciones en representación de 113 países. Reserve la fecha ahora para participar en el evento de hematología más integraldelaño.
LareuniónanualdelaASHeseleventomásgrandeycompletodehematologíaanivel mundial Con cientos de sesiones que abordan las últimas tendencias en hematología, la ASH proporciona diversas oportunidades para que los asistentes encuentren exactamenteloquebuscan.
Enabrilde1958,tuvolugarlaprimerareuniónoficialdelaSociedadEstadounidensede Hematología (ASH) en Atlantic City, Nueva Jersey, donde más de 300 hematólogos se congregaronparadiscutirtemasclínicosydeinvestigaciónrelacionadosconlasangre y las enfermedades hematológicas Desde esa reunión inicial, la ASH ha jugado un papelactivoysignificativoeneldesarrollodelahematologíacomodisciplina.Alolargo demásdeseisdécadas,laASHhapatrocinadosureuniónanual,eleventoeducativoy científico más destacado en el ámbito de la hematología, y ha publicado la revista "Blood",lapublicaciónrevisadaporparesmáscitadaenestecampo.
La ASH se dedica a establecer y promover una comunidad y una fuerza laboral global en hematología que incorpore perspectivas, talentos y experiencias diversas, mientras avanzahaciaunobjetivocomún:ayudaraloshematólogosavencerlasenfermedades delasangreentodoelmundo.Conmásde18000miembrosdecasi100países,laASH es la sociedad profesional más grande del mundo y apoya tanto a médicos como a científicosqueseesfuerzanporerradicarlasenfermedadesdelasangre.

P r u e b a s
c l í n i c a s y
c u e s t i o n a r i o s



Asegúrate de que tu voz sea escuchada!
Visite el sitio web Mi Sangre Mi Salud y participe en nuestras distintas encuestas.
misangremisalud.ca monsangmasante.ca
Encuestas disponibles:
Calidad de vida (CdV) en individuos con cáncer
hematológico
Impacto de la transfusión de sangre en la calidad de vida
Impacto de la mielofibrosis en la calidad de vida.
El efecto de la leucemia mieloide aguda en la calidad de vida

A l i a n z a s y a s o c i a c i o n e s
Grupo de educación y defensa de pacientes de la Red MPN de Canadá.

Proporcionar asistencia y formación a los pacientes con MPN.
Información@canadianmpnnetwork.ca

Únete a nosotros
KYB invita a individuos, profesionales de la salud, líderes comunitarios y organizaciones a unirse a esta misión. Juntos, podemos colaborar para disminuir las disparidades en salud y mejorar los resultados para las personas con trastornos sanguíneos en la comunidad africana y caribeña. Ya sea a través de la donación de sangre, el voluntariado o simplemente compartiendo el mensaje, cada contribución ayuda a construir un futuro más saludable.
Para obtener más detalles sobre cómo puedes participar, envía un correo electrónico a: knowyourblood2024@gmail.com Conéctate con nosotros en las redes sociales: Instagram: @Knowyourblood; TikTok: descubre tu sangre
Juntos podemos marcar la diferencia.

Mejorando la calidad de vida de los pacientes con NMP. La Fundación Científica Global para NMP (GMPNSF) es una entidad benéfica sin ánimo de lucro que se dedica a fomentar la investigación y el tratamiento de las NMP. Nuestro objetivo principal es generar conciencia, promover la colaboración y mejorar la calidad de vida de las personas afectadas por MPN.
Nuestra finalidad
En la Fundación Científica Global MPN, comprendemos los retos y las deficiencias en la gestión actual de la MPN, tales como:
Falta de sensibilización y formación entre pacientes, médicos y científicos.
Acceso restringido a evaluaciones y atención especializada
Variación en los criterios diagnósticos y directrices de tratamiento
Información insuficiente sobre la historia natural y los resultados de la NMP Disponibilidad restringida de tratamientos eficaces y estudios clínicos
Por ello, nos comprometemos a ofrecer una fuente de información respaldada por expertos, a crear y facilitar una comunidad de MPN y a abogar por los pacientes afectados por este grupo poco común de cánceres hematológicos La Fundación Científica Global MPN está dirigida por voluntarios que incluyen pacientes con MPN y profesionales de la salud que comparten esta visión
En nuestra plataforma, encontrará una extensa variedad de información objetiva y respaldada por profesionales de la salud, que incluye folletos, boletines informativos y foros donde podrá informarse sobre las últimas investigaciones relacionadas con NMP. También conocerá nuestra inversión en investigación y el apoyo a los ensayos clínicos. Además, descubrirá cómo estamos estableciendo conexiones con grupos de NMP a nivel global para aumentar la visibilidad en la defensa de los pacientes con NMP.
Le invitamos a unirse a nuestra misión de mejorar la vida de las personas que padecen NMP. Ya sea un paciente, un médico o un representante farmacéutico, encontrará recursos valiosos y oportunidades para conectarse con otros que comparten su interés en la NMP
Unidos podemos marcar la diferencia! www.gmpnsf.org.




Establecida en 2017, la Red de Defensores de la Leucemia Aguda (ALAN, por sus siglas en inglés) es una red global independiente de organizaciones de pacientes que se dedica a mejorar los resultados de los pacientes con leucemia aguda mediante el fortalecimiento de la defensa de los pacientes en este ámbito. Nuestra misión en ALAN es apoyar a nuestros miembros en la asistencia a los pacientes y sus familias, aumentar la conciencia sobre la leucemia y llevar a cabo un trabajo que se realiza de manera más efectiva a nivel internacional, como la recopilación de datos y evidencia. Todas nuestras actividades son dirigidas por los pacientes, son colaborativas y se fundamentan en la evidencia.
Quiénes somos?
En marzo de 2024, la red está compuesta por 56 organizaciones miembros de 52 países y es administrada por un comité directivo. Todos los integrantes del comité directivo son líderes de organizaciones nacionales de pacientes enfocadas en la leucemia y los cánceres de la sangre de diversas regiones, asegurando así una representación global.
Cómo operamos?
En ALAN tenemos la firme creencia de que:
Una colaboración robusta entre los participantes de un proyecto con múltiples interesados probablemente producirá ventajas para todas las partes implicadas
Las perspectivas de los pacientes y sus defensores son singulares. Por lo tanto, deben considerarse como conocimientos especializados que complementan los de otros expertos, el ámbito académico y la industria.
Colaboramos en múltiples proyectos con la industria farmacéutica, diversas organizaciones de pacientes, sociedades médicas, investigadores, médicos y otros especialistas.
Qué realizamos?
1.Fortalecimiento de competencias:
2- Concienciación
3- Defensa fundamentada en evidencia



Fogonadura







Mi grupo sanguíneo, mi salud
Brigitte Leonard, Doctora en Filosofía.

Brigitte Léonard es la directora científica de My Blood, My Health, una organización sin fines de lucro registrada que fomenta el acceso equitativo a atención médica de calidad en todo Canadá. Ha tenido el privilegio de trabajar en el sector farmacéutico durante más de 20 años, contribuyendo a proporcionar tratamientos que transforman la vida de los pacientes con os más altos estándares éticos. En la actualidad, desea compartir su conocimiento y emplear sus habilidades científicas, estratégicas y de comunicación para apoyar a la comunidad de pacientes
Obtuvo su doctorado en Ciencias Biomédicas en la Universidad de Montreal en 2003. Su investigación doctoral se realizó bajo la supervisión del Dr Denis-Claude Roy en el Centro de Investigación del Hospital Guy-Bernier, Maisonneuve-Rosemont. Desarrolló un ensayo diagnóstico cuantitativo en el linfoma no Hodgkin y evaluó la importancia de este marcador en la evolución del paciente
Cheryl Petruk, MBA
B.Mgt.

Cheryl A. Petruk es una profesional polifacética cuya trayectoria incluye la defensa de los pacientes, el ámbito empresarial y la educación superior, lo que evidencia su compromiso por generar un impacto relevante en cada una de estas áreas.
La transición de Cheryl hacia la defensa de los pacientes fue motivada por la pasión que le generó su situación familiar y un profundo compromiso con la protección de los derechos de los pacientes y el acceso a la atención. Cheryl ha trabajado incansablemente para cerrar la brecha entre el sistema de atención médica, los pacientes y las partes interesadas de la industria farmacéutica, asegurándose de que se escuchen las voces de los pacientes y se satisfagan sus necesidades Su labor implica colaborar con las partes interesadas y las organizaciones de defensa de los pacientes, abogar por un enfoque centrado en el paciente y ofrecer apoyo y orientación a los pacientes El enfoque empático de Cheryl y su dedicación a la defensa la han convertido en una figura respetada en este ámbito, admirada por pacientes, profesionales de la salud y otros defensores.
Cheryl también es la directora y miembro principal del equipo docente de CACHeducation, Capacitación en Defensa del Paciente.
