5 minute read
Approbations récentes de Santé Canada en 2025
par Brigitte Leonard, Ph.D.
En 2025, Santé Canada a approuvé trois traitements innovants hautement ciblés pour des maladies rares et certains cancers. L’un concerne une maladie rare appelée sclérose latérale amyotrophique (SLA) (1), un autre est destiné au carcinome à cellules de Merkel métastatique ou récidivant localement avancé (2), et le troisième vise le cancer du sein avancé ou métastatique (3) Pour en savoir plus sur ces maladies et les traitements novateurs, je vous invite à lire les sections suivantes de cette publication
La sclérose latérale amyotrophique (SLA) est une maladie neurodégénérative progressive caractérisée par une fonte musculaire qui affecte le corps de multiples façons Elle compromet plusieurs fonctions motrices, notamment la mobilité, la respiration, la communication et la santé mentale Ces symptômes s’aggravent au fil du temps L’espérance de vie est généralement de 3 à 5 ans après l’apparition des premiers signes Environ 2 % des cas de SLA sont liés à des mutations dans le gène codant pour la superoxyde dismutase 1 (SOD1) (4) La protéine SOD1 mutée devient toxique et entraîne la dégénérescence des neurones (4)
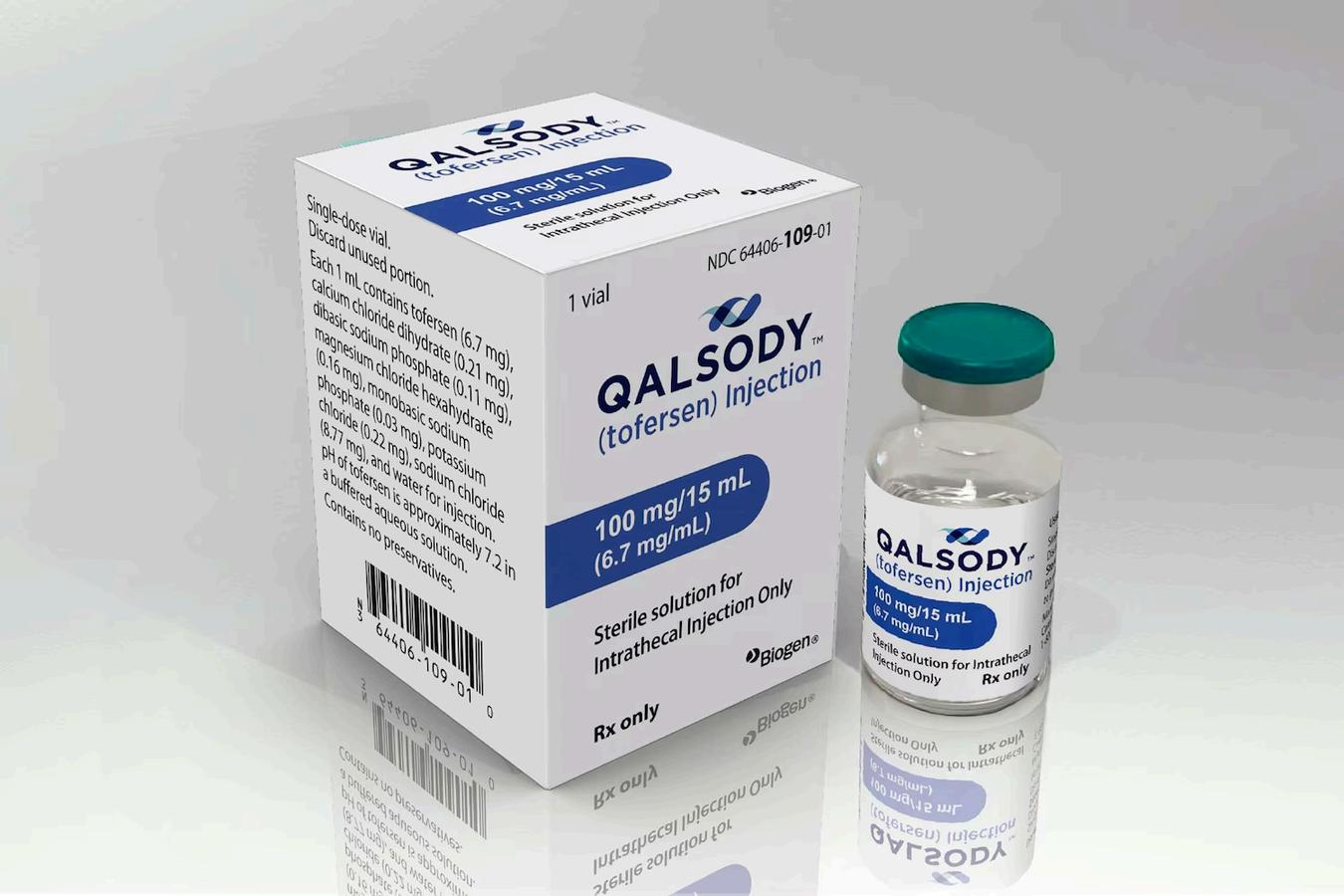
En février 2025, Biogen a reçu l’approbation de Santé Canada pour le QALSODY (Tofersen), un traitement destiné aux adultes atteints de SLA associée à une mutation du gène SOD1 (Figure 1). L’indication complète est disponible sur le site de Santé Canada ou sur celui de Biogen.
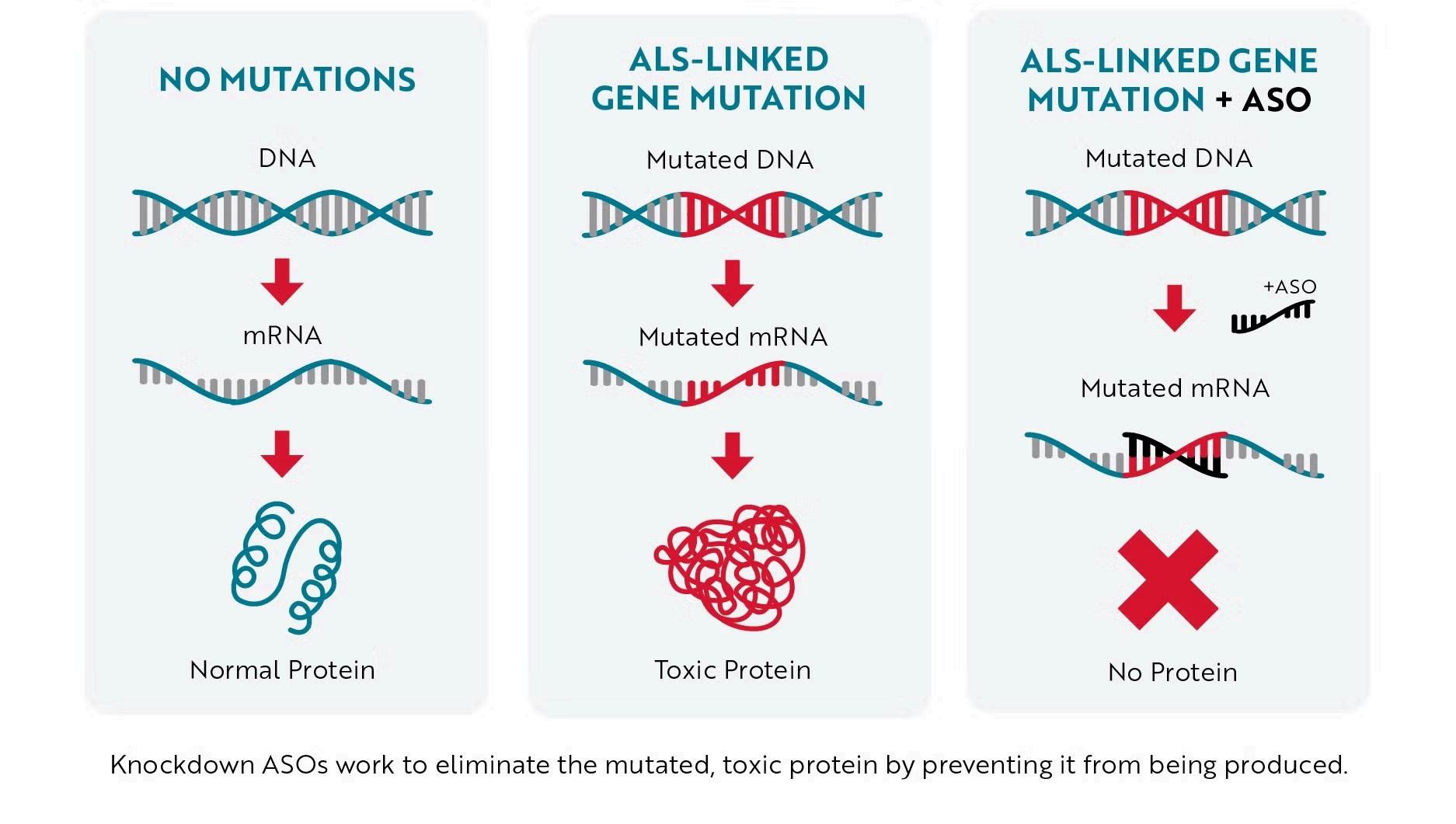
QALSODY est une molécule capable de se lier à l’ARN messager responsable de la production de la protéine mutée. En se fixant à cet ARN, QALSODY active un mécanisme de défense cellulaire qui détruit l’ARN muté. Ainsi, le produit toxique cesse d’être produit (Figure 2) (5).
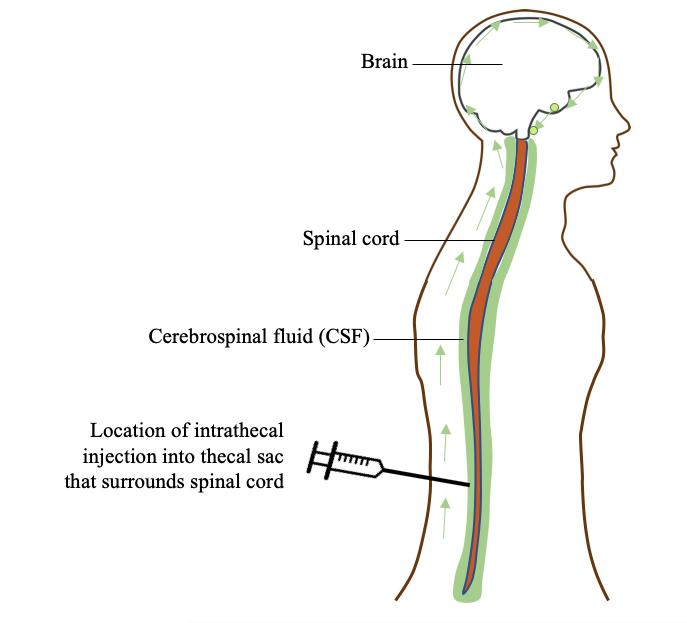
Le Tofersen est administré par injection intrathécale, c’est-à-dire injecté directement dans la région lombaire, près de la colonne vertébrale (Figure 3)
Approbations récentes de Santé Canada en 2025 suite
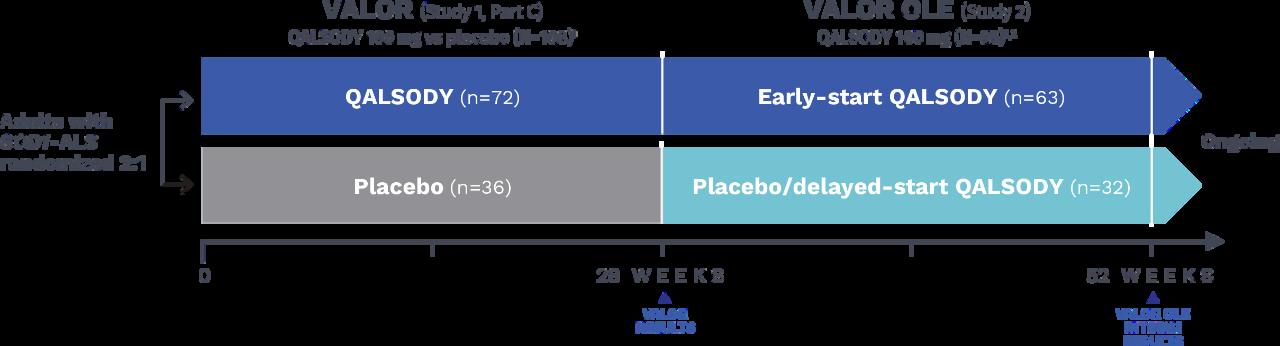
Santé Canada a approuvé QALSODY sous conditions, sur la base des résultats de l’essai clinique de phase III VALOR et de son extension (VALOR OLE) Le schéma de l’étude est présenté à la Figure 4
Pour évaluer l’efficacité de QALSODY, deux biomarqueurs ont été utilisés : 1) la concentration totale de protéine SOD1 dans le liquide céphalorachidien; 2) la concentration de chaînes légères de neurofilaments (NfL) dans le sang.
Comme illustré à la Figure 5, QALSODY permet une réduction significative de la protéine mutée par rapport au placebo, soit 35 % contre 2 %. De plus, la dégénérescence neuronale semble être atténuée chez les patients traités par QALSODY, avec une réduction de 55 %, alors qu’elle progresse chez les patients sous placebo (augmentation de 12 %)
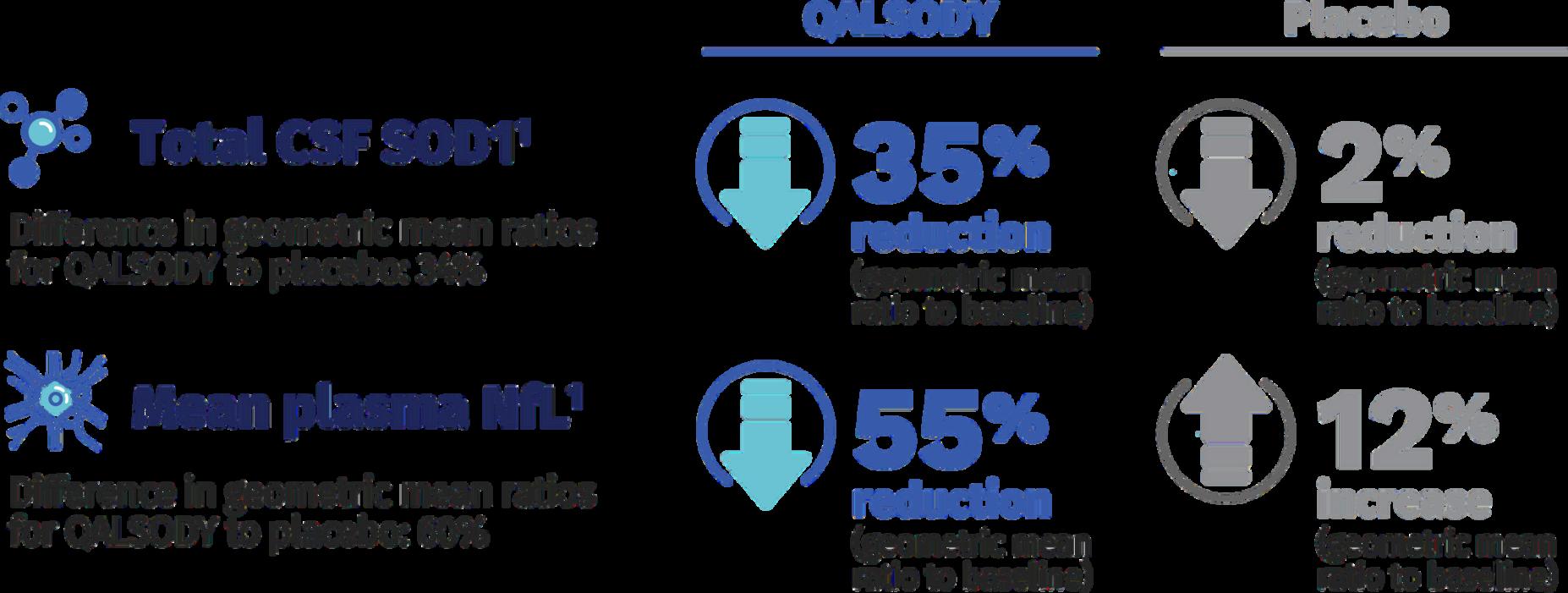
QALSODY a démontré des résultats positifs avec un profil de sécurité acceptable, offrant de l'espoir à ces patients
Le carcinome à cellules de Merkel (CCM) est un cancer rare de la peau, de type neuroendocrinien Il se caractérise par des récidives fréquentes et un taux de mortalité élevé Ces dernières années, le nombre de diagnostics de CCM a augmenté aux États-Unis, en Australie et en Europe (7)
Les facteurs fortement associés au développement du CCM incluent le vieillissement, une peau claire, un historique d’exposition prolongée au soleil, une immunosuppression chronique (par exemple à la suite d’une greffe de rein ou de cœur, ou dans le cas du VIH), ainsi que l’infection par le polyomavirus des cellules de Merkel (8).
Les cellules de Merkel se trouvent dans la couche inférieure de l’épiderme. Bien que leur fonction exacte ne soit pas entièrement élucidée, elles sont considérées comme des récepteurs sensoriels du toucher. Également appelées cellules neuroendocrines, elles présentent à la fois des caractéristiques des cellules nerveuses et des cellules endocrines sécrétrices d’hormones.

En février 2025, la société Incyte a obtenu l’approbation de Santé Canada pour le ZYNYZ (rétifanlimab) en tant que traitement de première intention du carcinome à cellules de Merkel (CCM) métastatique ou localement avancé L’indication complète est disponible sur le site de Santé Canada ou celui d’Incyte (Figure 6)

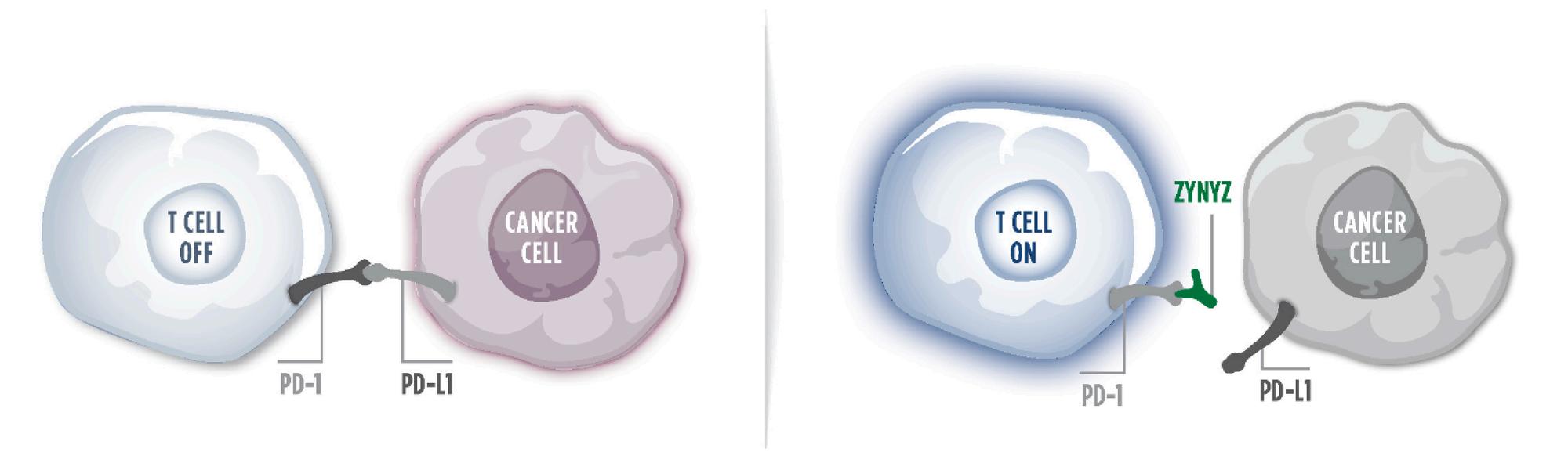
Les cellules cancéreuses peuvent exprimer une molécule appelée ligand du PD-1 (PD-L1) (Figure 7) Lorsque ce ligand se lie à la molécule PD-1 présente sur les lymphocytes T, il inhibe l’activation du système immunitaire. Ce mécanisme permet aux cellules cancéreuses d’échapper à la surveillance immunitaire. Le ZYNYZ agit en bloquant cette interaction : il se fixe au récepteur PD-1 des cellules T et empêche sa liaison au ligand PD-L1 exprimé par les cellules cancéreuses (9).
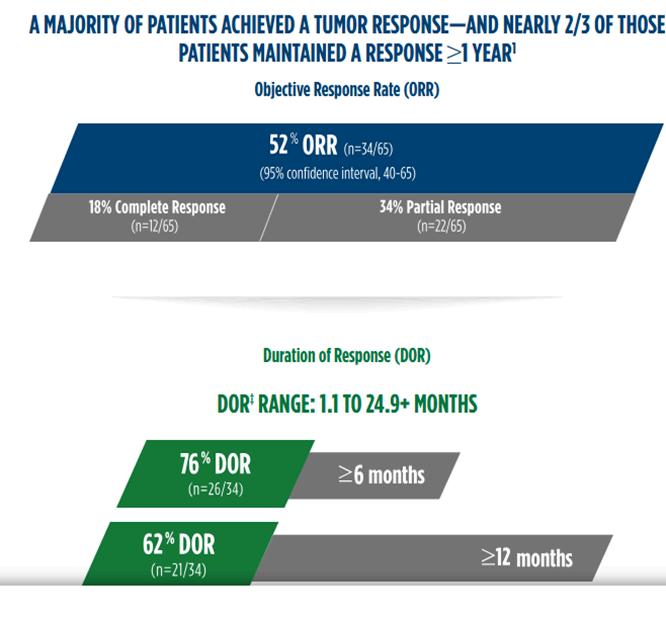
L’autorisation de mise sur le marché repose sur les taux de réponse tumorale et la durabilité de cette réponse observés dans l’essai clinique POD1UM-201 (Figure 8) (10) Cette nouvelle approbation représente un espoir important pour les personnes atteintes de CCM.
Au cours des deux dernières décennies, plusieurs stratégies cliniques ont été mises en place afin d’améliorer la survie des personnes recevant un diagnostic de cancer du sein Les recommandations en matière de prévention, le dépistage précoce et les thérapies ciblées en font partie Toutefois, la bataille est loin d’être terminée Certaines formes de cancer du sein demeurent particulièrement complexes à traiter
Le cancer du sein à récepteurs hormonaux positifs (RH+) est le type le plus fréquent, représentant environ 70 % de tous les cas (11) Ce sous-type se caractérise par des cellules tumorales exprimant des récepteurs qui se lient à l’œstrogène ou à la progestérone (ou aux deux), ce qui peut favoriser la croissance tumorale Les personnes atteintes d’un cancer du sein métastatique RH+ sont exposées à un risque élevé de progression de la maladie et d’effets indésirables liés au traitement, d’où le besoin constant d’options thérapeutiques supplémentaires (12) La voie de signalisation PI3K est fréquemment perturbée dans le cancer du sein RH+ en raison de mutations activatrices. Ces mutations sont reconnues comme un mécanisme possible de résistance intrinsèque aux traitements standards (13). Approbations

Approbations récentes de Santé Canada en 2025 suite
En février 2025, la société Roche a reçu l’approbation de Santé Canada pour l’ITOVEBI® (inavolisib), un traitement destiné au cancer du sein avancé ou métastatique (Figure 10) L’indication complète est disponible sur le site de Santé Canada ou celui de Roche ITOVEBI agit en inhibant une molécule appelée PI3K, ce qui permet de ralentir la croissance tumorale et d’induire la mort des cellules cancéreuses
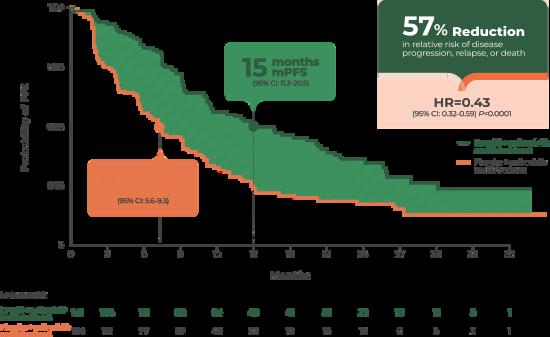
L’étude INAVO120 [NCT04191499] est un essai de phase III qui évalue l’efficacité et l’innocuité d’ITOVEBI® (inavolisib) en combinaison avec d’autres traitements standards (14) Les résultats ont montré que le schéma thérapeutique à base d’ITOVEBI a plus que doublé la survie sans progression dans la population de patientes étudiée (Figure 11), tout en maintenant un profil de sécurité jugé acceptable ITOVEBI représente une nouvelle possibilité pour ces femmes

par Brigitte Leonard, Ph.D
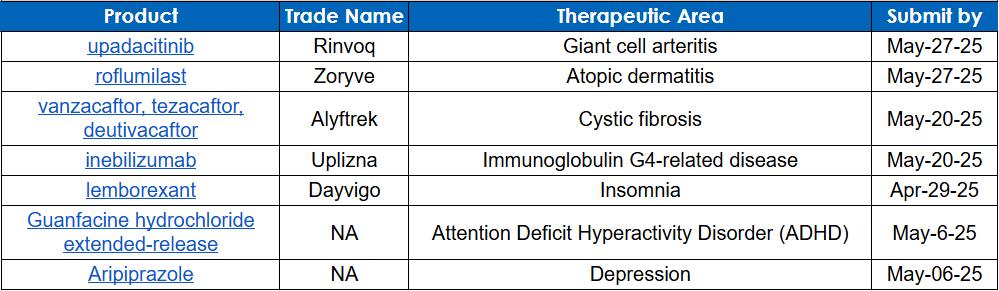
L'Agence canadienne des médicaments et des technologies de la santé (ACMTS) est un organisme indépendant à but non lucratif qui fournit des évaluations fondées sur des données probantes concernant les médicaments, les appareils médicaux et les technologies de la santé afin d'appuyer la prise de décisions éclairées dans le système de santé du Canada. L'ACMTS collabore avec les gouvernements fédéral, provinciaux et territoriaux (à l'exception du Québec) pour évaluer l'efficacité clinique, le rapport coût-efficacité et l'impact général des interventions de santé nouvelles et existantes. En effectuant des évaluations des technologies de la santé (ETS), en formulant des recommandations sur le remboursement et en élaborant des rapports d'orientation, l'ACMTS joue un rôle crucial dans l'élaboration des politiques de santé, en veillant à ce que les patients, les fournisseurs de soins de santé et les décideurs aient accès à des renseignements fiables et fondés sur la science afin d'améliorer les résultats pour la santé et d'optimiser l'affectation des ressources.
L'ACMTS et l'ACD demandent l'avis des patients sur les produits non oncologiques https://www.cda-amc.ca https://www.healcanada.org/empowering-voice-podcast/

Nouvelles excitantes de Heal Canada ! Nous sommes ravis d'annoncer le lancement de notre nouvelle série de podcasts, Empowering Voices, qui a pour but d'amplifier les histoires et les points de vue des patients, des professionnels de la santé et des défenseurs des droits dans les communautés des troubles sanguins et des maladies rares. Chaque épisode présentera des conversations intéressantes sur les expériences des patients, les recherches émergentes et l'évolution du paysage de la défense des soins de santé. Grâce à Empowering Voices, nous souhaitons éduquer, inspirer et favoriser le changement en mettant en avant des points de vue concrets. Restez à l'écoute pour notre premier épisode, qui sera bientôt disponibleparce que chaque voix compte !











