

ANIVER SARIO EDICIÓN

aprocitentan
Molécula del mes

Antibiótico especializado
Infecciones urinarias en mujeres
AÑOS

Opioide
Cuestionado
Semielaborados farmacéuticos
Simpli cando la producción
Efectos que generan dudas Terapia innovadora Nueva apuesta contra obesidad
Aprocitentan

Aprocitentan (Tryvio™) es un antagonista dual de los receptores de endotelina A (ETA) y B (ETB) de administración oral una vez al día, desarrollado por Idorsia Pharmaceuticals para el tratamiento de la hipertensión. Este antagonista inhibe la unión de la ET-1 a los receptores ETA y ETB.
El aprocitentan presenta un bajo potencial de interacción farmacológica y un mecanismo de acción ideal para reducir la presión arterial en pacientes adultos cuya hipertensión no se
Nombres alternativos
Nombre IUPAC
Clase
Mecanismo de acción
Ruta de administración
Farmacodinámica
Farmacocinética
Efectos adversos
Código ATC
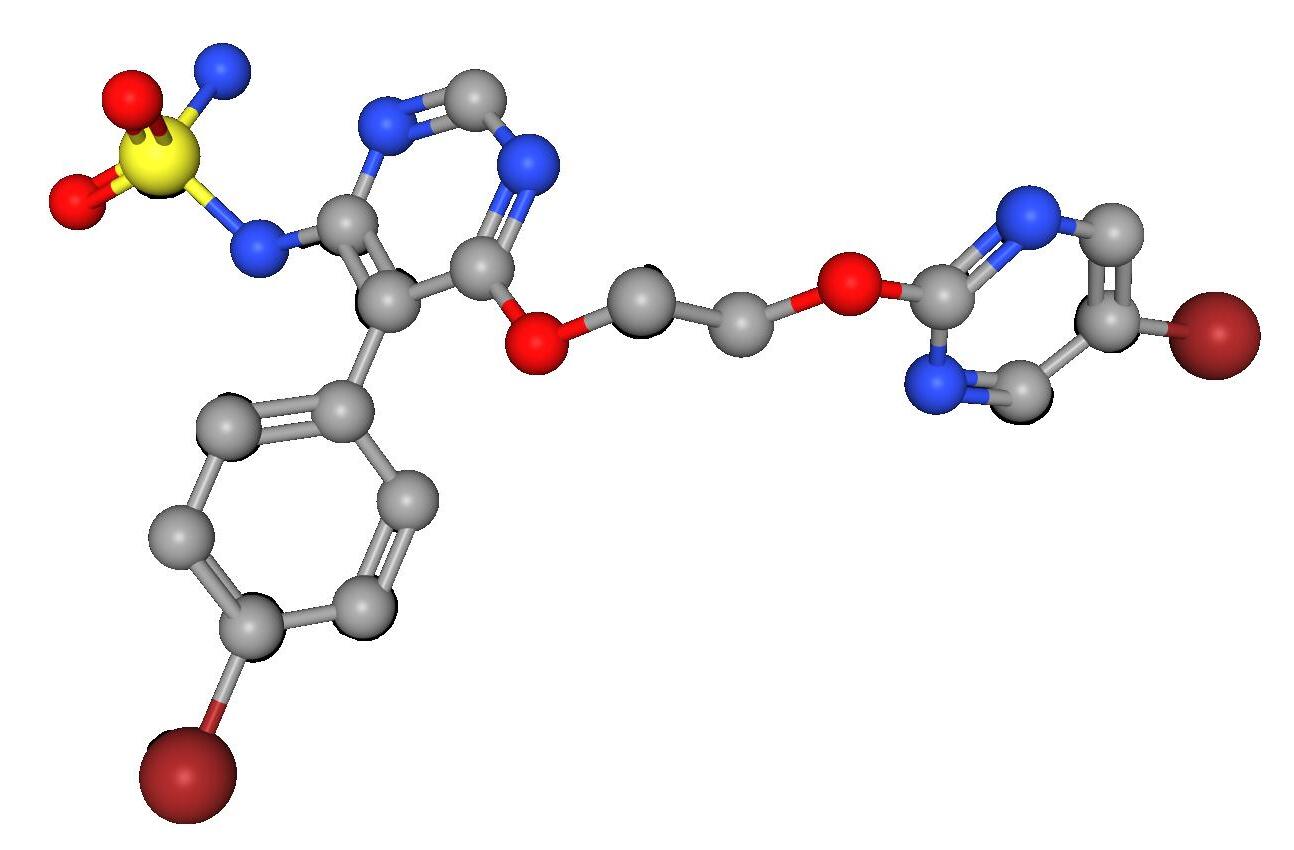
controla adecuadamente con otros fármacos. Es el metabolito activo del macitentan.

Aproximadamente entre el 10 % y el 15 % de los pacientes con hipertensión presentan hipertensión resistente, definida como presión arterial alta no controlada a pesar del uso combinado de un antagonista del sistema renina-angiotensina, un antagonista del calcio y un diurético a las dosis máximas toleradas.
Características y propiedades de Aprocitentan
ACT 132577; N-Despropil-macitentan; Tryvio
N-[5-(4-bromofenil)-6-[2-[(5-bromo-2-pirimidinil)oxi]etoxi]-4-pirimidinil]-sulfamida
Cardiovascular; Antihipertensivo; Sulfamida; Molécula pequeña
Inhibe la unión de Endotelina-1 (ET-1) a los receptores ET A y ET B. Mitiga los efectos hipertensivos de la sobreexpresión de ET-1, incluyendo disfunción endotelial, hipertrofia y remodelación vascular, activación simpática y aumento de la síntesis de aldosterona.
Oral
Inhibe receptores de endotelina;
Se desconoce la biodisponibilidad oral absoluta. La Cmáx media y el AUC 0-tau tras una dosis oral única de 25 mg son aproximadamente 1,3 mcg/ml y 23 mcg.h/ml, respectivamente, con un Tmáx de entre 4 y 5 horas. Edema, retención de fluidos, anemia
C02KN01 Otros antihipertensivos
El aprocitentan fue aprobado por la FDA en marzo de 2024 para el tratamiento de la hipertensión en pacientes que no se controlaban adecuadamente con la terapia estándar. Fue el primer antihipertensivo que empleaba un mecanismo novedoso en ser aprobado en casi 40 años.
La dosis recomendada de aprocitentan es de 12,5 mg por vía oral una vez al día.
Fuente: https://pubmed.ncbi.nlm.nih.gov/38833193/

Para recibir mayor información sobre este ingrediente activo, una fuente aprobada y documentación disponible no dude en ponerse en contacto con alguno de nuestros asesores comerciales al escanear el código QR.

Antibiótico especializado Gepotidacina



FDA aprueba primer antibiótico para infecciones urinarias, un hito que no solo entusiasma a la comunidad médica, sino que también ofrece esperanza concreta a millones de mujeres que viven atrapadas en el bucle interminable de dolor, antibióticos ineficaces y miedo al regreso de la infección.
Blujepa, cuyo principio activo es gepotidacina, es un antibiótico oral (tabletas 750 mg) desarrollado por GSK, fue aprobado por la FDA para tratar infecciones urinarias no complicadas y causadas por bacterias resistentes a tratamientos comunes. A diferencia de otros antibióticos que actúan en las fases iniciales de replicación del ADN bacteriano, Blujepa interfiere directamente con dos enzimas clave involucradas en la división celular de E. coli, el principal responsable de este tipo de infecciones.
Lo más relevante de Blujepa es que pertenece a una nueva clase de antibióticos, no relacionada con las fluoroquinolonas ni con los betalactámicos, lo que representa una alternativa crucial frente al creciente


problema de resistencia a los antimicrobianos. De hecho, su aprobación por la FDA se considera un avance estratégico en la lucha contra bacterias multirresistentes, una crisis que amenaza silenciosamente al sistema de salud global.
Según la FDA, los ensayos clínicos mostraron que Blujepa fue tan eficaz como la nitrofurantoína, pero con mejor perfil de resistencia y menor necesidad de repetir tratamientos.
Las infecciones del tracto urinario (ITU) son causadas por bacterias que ingresan a través de la uretra y colonizan la vejiga. Aunque pueden afectar a cualquier persona, son especialmente comunes en mujeres debido a razones anatómicas. Según Mayo Clinic, los síntomas más frecuentes son ardor al orinar, aumento en la frecuencia urinaria, urgencia, dolor pélvico y orina turbia o con olor fuerte. Aunque la mayoría de los casos se resuelven con antibióticos comunes, entre el 25 y el 30% de las mujeres desarrollan infecciones urinarias recurrentes, es decir, al menos dos episodios en seis meses o tres en un año.
Fuente: https://www.salud180.com/salud/fda-aprueba-primer-antibiotico-para-infec ciones-urinarias
Semielaborados farmacéuticos

intermedios de formulación son fundamentales para optimizar la fabricación de fármacos, garantizar la calidad y permitir un escalado eficiente. Entre ellos, los gránulos de compresión directa, los pellets para encapsulado y los polvos estériles para llenado de viales, destacan como intermedios críticos que simplifican la producción y cumplen
con las estrictas normas regulatorias. Estos semielaborados actúan como bloques funcionales, conectando las materias primas con las formas farmacéuticas finales, ofreciendo ventajas estratégicas que impactan en la eficiencia, calidad y costos de producción. A continuación, se detallan los principales valores que aportan en la práctica:

1. Simpli cación del Proceso de Fabricación
Reducción de pasos críticos: Los semielaborados integran etapas previas (ej.: mezcla, granulación, pelletización, recubrimiento, esterilización), eliminando la necesidad de repetir procesos y reduciendo la necesidad de equipos y personal. Menor manipulación de materiales: Al trabajar con semielaborados prevalidados, se reduce el manejo de materias primas individuales, disminuyendo riesgos de contaminación cruzada, errores humanos y costos de manipulación.

3. E ciencia Económica

2. Consistencia y Control de Calidad.
Variabilidad reducida: Los semielaborados están prehomogeneizados y caracterizados (ej.: distribución del tamaño de partícula, humedad), garantizando uniformidad en atributos críticos.
Puntos de control intermedios: Cada semielaborado actúa como un "checkpoint" de calidad, permitiendo detectar y corregir desviaciones antes de avanzar a etapas posteriores (ej.: validar la esterilidad de un polvo antes del llenado de viales).
Ahorro en costos de producción: Menor consumo energético, menor tiempo de proceso, hay una reducción signi cativa de pruebas analíticas repetitivas a ingredientes activos y excipientes, ya que los semielaborados cumplen especi caciones prede nidas. Optimización de inventarios: Los semielaborados son un sistema ingredientes integrados que recoge en un solo material las especi caciones de sus componentes, se reduce el manejo de materias primas individuales y la cali cación de proveedores.
4. Escalabilidad y Flexibilidad

Facilidad de escalado: Los procesos basados en semielaborados son más reproducibles al pasar de escala laboratorio a industrial, gracias a parámetros ya optimizados (ej.: ujo de gránulos en máquinas de compresión).
Adaptabilidad a múltiples productos: Los semielaborados permiten fabricar diferentes dosis o combinaciones sin reformular desde cero (ej.: mezclar pellets de liberación inmediata y extendida en una cápsula).
Ideal para plantas multipropósito: se prioriza la exibilidad y la reducción de tiempos de limpieza entre lotes.

6. Sostenibilidad y Reducción de Residuos
Menor generación de desechos: Al evitar reprocesos por fallas en etapas iniciales (ej.: mezclas inhomogéneas), se reduce el desperdicio de materias primas costosas.
Huella ambiental reducida: La eliminación de pasos redundantes (ej.: granulación húmeda) disminuye el consumo de agua, energía y solventes.
5. Cumplimiento Regulatorio

Documentación simpli cada: Los semielaborados bien caracterizados y diseñados sobre la base de criterios críticos de calidad bien de nidos permiten el cumplimiento de los estándares regulatorios más estrictos.
Fabricados por instalaciones certi cadas: los fabricantes de los semielaborados cumplen con los lineamientos de las guías de buenas prácticas de manufactura, lo que garantiza su idoneidad y robustez normativa.
Ejemplos Prácticos
1. Gránulos para compresión directa: Eliminan 3-4 etapas de procesamiento, reduciendo el tiempo de producción de tabletas en un 30-40%.
2. Polvos estériles para viales: Permiten llenado aséptico rápido, crítico para antibióticos o productos sensibles al tiempo.
3. Pellets para cápsulas: Habilitan terapias combinadas sin interacciones entre fármacos, gracias a recubrimientos funcionales.
Utilizar semielaborados farmacéuticos en lugar de materias primas individuales agrega valor al optimizar recursos, garantizar calidad y simplificar cumplimiento regulatorio. Estos intermediarios no solo reducen costos y tiempos, sino que también permiten una fabricación ágil y adaptable a las demandas del mercado. En un sector donde la precisión y la eficiencia son claves, los semielaborados se posicionan como pilares estratégicos para la innovación y competitividad farmacéutica.
Fuente: Redacción por Alejandro Restrepo, Gerente Técnico. Gaffel.

OpioideCuestionado
Grünenthal, la empresa familiar alemana que desarrolló el tapentadol, ha comercializado el fármaco como una alternativa más segura a los opioides tradicionales, restando importancia al riesgo de adicción de cara a los médicos e influyendo en la normativa que regula su prescripción, según revela esta investigación de The Examination y medios de comunicación de seis países.
En una revista médica, los empleados de Grünenthal promocionaron el supuesto «bajo nivel de abuso» del fármaco, una afirmación engañosa que se repite en un vídeo publicado en el sitio web educativo de la empresa para médicos latinoamericanos. El vídeo también minimiza el riesgo de depresión respiratoria del fármaco a pesar de que se trata de un efecto secundario bien conocido de los opioides y reconocido por las autoridades sanitarias de todo el mundo.
Grünenthal retiró el sitio web educativo a finales de febrero tras las preguntas de The Examination
Grünenthal y otros vendedores de opioides han financiado estudios y artículos relacionados con el tapentadol en revistas arbitradas que sugerían que era menos probable que el tapentadol causara dependencia o condujera al abuso que otros opioides Seis expertos independientes que revisaron esta investigación por pedido de The Examination y sus medios aliados llegaron a una conclusión unánime: No hay pruebas
convincentes que respalden tales afirmaciones.
Grünenthal ejerce una amplia influencia financiando a médicos, organizaciones médicas, grupos de pacientes e iniciativas educativas en América Latina y Europa. En la última década, Grünenthal ha pagado más de 9 millones de dólares para ayudar a financiar al menos 900 grupos de pacientes y organizaciones médicas europeas, según un análisis de datos realizado por The Examination. Una asociación financiada por la empresa hizo lobby al Congreso mexicano para que flexibilizara la normativa sobre la prescripción de tapentadol. Grünenthal reconoció en un comunicado que «unos pocos» documentos de la empresa describían erróneamente los riesgos de adicción del tapentadol.
En España, las prescripciones de tapentadol han superado ya a las de oxicodona. En Australia, el tapentadol se ha convertido en el opioide más recetado. CSL Seqirus, una de las compañías más grandes del mundo, líder en la producción y suministro de vacunas antigripales, que tiene una licencia para vender el medicamento, se jactó el año pasado de que el tapentadol ha sido el «único opioide con un crecimiento constante». En Colombia, las ventas de tapentadol aumentaron casi un 50% entre 2022 y 2023.
Fuente: https://saludconlupa.com/noticias/grunenthal-vendio-su-ultimo-opioide-como -una-opcion-mas-segura-personas-en-todo-el-mundo-resultaron-adictas/
Terapia innovadora

Roche ha firmado un acuerdo de colaboración y licencia exclusivo con Zealand Pharma en virtud del cual las dos empresas colaborarán para desarrollar y comercializar conjuntamente petrelintida, el análogo de amilina de Zealand Pharma, como terapia independiente, así como una combinación de dosis fija con el principal activo incretina de Roche, CT-388.
La petrelintida, actualmente en fase 2 de desarrollo clínico, es un análogo de amilina de acción prolongada, apto para administración subcutánea una vez a la semana. Los datos clínicos disponibles sugieren su potencial para convertirse en la mejor monoterapia con amilina, con mejor tolerabilidad en comparación con los tratamientos actuales para el control de peso, y para expandirse a indicaciones adyacentes
La combinación de petrelintida con el agonista dual del receptor GLP-1/GIP de Roche, CT-388, fortalecerá y ampliará la cartera de productos de Roche en el campo de las enfermedades del síndrome cardiovascular-renal-metabólico (CVRM). Esta combinación ofrece la oportunidad de lograr la máxima eficacia en la enfermedad, a la vez que ofrece una posible mejor tolerabilidad.
Este acuerdo de colaboración abarca el desarrollo y la comercialización conjunta de petrelintida para aprovechar al máximo el valor del activo. Como parte de este acuerdo, Zealand Pharma y Roche comercializarán conjuntamente petrelintida en EE. UU. y Europa, mientras que Roche obtendrá los derechos exclusivos de comercialización en el resto del mundo. Roche será responsable de la fabricación y el suministro comerciales.
El cierre de la transacción está sujeto a las aprobaciones regulatorias y otras condiciones de cierre habituales. Las partes esperan que la transacción se cierre en el segundo trimestre de 2025.
Fuente: https://www.contractpharma.com/breaking-news/roche-zealand-pharma-pa rtner-to-co-develop-co-commercialize-obesity-therapy/

AÑOS ANIVERSARIO

Tres años informando de los avances y tendencias que están transformando la industria farmacéutica




