12 minute read
Laboratoriedata og trombose/hæmostase-området
from DSTH-Forum 1. udgave 2021
by DSTH
Laboratoriedata
og trombose/hæmostase-området
Af: Kasper Adelborg, læge, ph.d., lektor1,2,3 1Blodprøver og Biokemi, Klinik for Koagulation, Aarhus Universitetshospital 2Klinisk Epidemiologisk Afdeling, Aarhus Universitetshospital 3Institut for Klinisk Medicin, Aarhus Universitet
Sundhedsregistre og laboratoriedata
De danske sundhedsregistre og biobanker har en lang historisk tradition, der giver danske forskere gode forudsætninger for at være blandt verdens førende (1). Flere forhold bidrager til at gøre Danmarks registre unikke. For det første samles data fra alle i befolkningen, og alle borgere har fri og lige adgang til det offentligt finansierede sundhedsvæsen. Videnskabsjournalisten Lone Frank har tidligere beskrevet dette under overskriften ”When an Entire Country Is a Cohort” (2). Vores CPR-numre muliggør, at data og information fra de forskellige registre kan sammenkøres med livslang og komplet opfølgning. Dette minimerer risikoen for selektionsbias. Endelig er der adgang til detaljerede sundhedsdata af høj kvalitet fra en lang række registre. Disse registre omfatter administrative registre (fx Landspatientregistret), specifikke sygdomsregistre (fx Cancerregistret) samt en lang række kliniske kvalitetsdatabaser.
Laboratoriesvar fra indlagte og ambulante patienter samt fra patienter i almen praksis udgør en stor informationsbank. I langt højere grad end andre danske registre indeholder laboratoriedata detaljerede biologiske data, herunder viden om sværhedsgraden af de specifikke sygdomme. Selvom laboratoriedata anvendes i stigende grad i forskning og i kvalitets- samt udviklingsmæssig sammenhæng, rummer data fortsat et stort uudnyttet potentiale. Formålet med denne artikel er at beskrive de danske laboratoriedatabaser, herunder at give eksempler på hvorledes data kan anvendes inden for trombose/ hæmostase-området.
Laboratoriedatakilder og opbygning
Oplysninger om patienters laboratoriesvar fra de kliniske biokemiske og immunologiske afdelinger registreres i hospitalslaboratoriernes IT-systemer, hvor informationer-ne er tilgængelige for og anvendes af sundhedsprofessionelle i det daglige kliniske arbejde (3). Biomarkørerne måles fortrinsvis i blod, men også svar fra urin, ledvæsker, samt spinalvæsker registreres. Resultaterne fra udvalgte pointof-care tests registreres ligeledes. Koagulationsanalyserne indbefatter svar på eksempelvis tromboelastometri målinger og rutine koagulationsanalyser som INR, aktiveret partiel tromboplastintid (APTT), antitrombin, fibrin d-dimer, fibrinogen samt trombocytmålinger. Derudover registreres svar fra trombofiliudredninger, højtspecialiserede blødningsudredninger samt udredning for en række sjældne tilstande (trombotisk trombocytopenisk purpura, heparin induceret trombocytopeni, og trombocytdefekter). Generelt er datakvaliteten af laboratoriedata høj, og de
fleste hospitalslaboratorier er akkrediteret af den Danske Akkrediteringsfond (DANAK) efter internationale standarder. Dette indebærer, at laboratorierne er underlagt veldefinerede kriterier omhandlende analysevirksomhed, svarafgivelse, personalekvalifikationer, IT og løbende uddannelse og kvalitetsmål. Desuden foreligger der en række krav til analysevalideringer og kontrolsystemer, som skal sikre analysernes høje kvalitet. På de kliniske biokemiske afdelinger anvendes udtræk fra laboratoriedatabasesystemer i kvalitetssikrings- og udviklingssammenhænge. Eksempelvis har man på Aarhus Universitetshospital anvendt laboratoriedata til at understøtte beslutninger om grænser for referenceintervaller på koagulationsanalyser hos børn. Derudover anvendes data til at monitorere svartider på bl.a. koagulationsanalyser for dermed at sikre rettidigt svar på blodprøverne.
Forskningsdatabaser
Laboratoriedata er værdifulde for forskning i forebyggelse, diagnostik og behandling af sygdomme. I Danmark findes en række forskningsdatabaser, som indeholder laboratoriedata. Disse er detaljeret beskrevet i en nylig oversigtsartikel (3). Internationalt set findes kun ganske få tilsvarende laboratoriedatabaser. Sundhedsdatastyrelsen har ansvaret for den nationale laboratoriedatabase, som beror på en kopi af data fra hospitalernes IT-systemer. Der findes også en række mere lokale laboratoriedatabaser som eksempelvis ”Copenhagen Primary Care Laboratory (CopLab) Databasen”, ”LABKA Databasen” og den fynske diabetesdatabase (3-4).
Fælles for alle forskningsdatabaserne er, at de indeholder en række nøglevariable. Hver biomarkør er kodet med et navn og en såkaldt Nomenclature for Property and Unit (NPU) kode eller lokalkode. Hertil registreres resultatet på biomarkøren (numerisk eller tekstsvar), rekvisitionstidspunkt, prøvetagningstidspunkt, rekvirent, laboratorie, enhed på biomarkøren, samt tilhørende referenceintervaller. Data opdateres løbende, og historiske data kan ligeledes anvendes (for nogle områder af Danmark tilbage til 1990’erne).
Selvom laboratoriedata hidtil har været anvendt i en lang række forskningsprojekter, har brugen været mere begrænset indenfor trombose/hæmostase-området. Nedenfor er beskrevet en række eksempler på projekter, hvor laboratoriedata har været anvendt. Eksempelvis har et studie bidraget til at øge forståelsen af risikoen for trombose og blødning hos patienter med kronisk immun trombocytopeni med fokus på betydningen af forskellige trombocyttalsniveauer (5). Andre studier har belyst sammenhængene mellem forskellige biomarkører og udviklingen af arterielle og venøse sygdomme (6-7). Endelig har studier opgjort prævalensen af trombofilier hos patienter med iskæmisk stroke (8) og portal venetromboser (9). Data har også været anvendt til at monitorere om patienter opnår de behandlingsmål som foreskrives i kliniske guidelines (10). I et studie af omkring 10.000 patienter med kronisk åreforforkalkningssygdom, fandt man at kun en mindre andel af patienterne (ca. 25%) opnåede de rekommenderede LDL-niveauer på 1.8 mmol/l, hvilket understreger, at der er mulighed for at optimere behandlingen og dermed potentielt forbedre prognosen for disse patienter. Endelig har laboratoriedata været anvendt til at belyse forekomsten af, risikofaktorer for og den prognostiske betydning af hyperkaliæmi hos patienter med kronisk hjertesvigt (11).
Begrænsninger
Brugen af laboratoriedata rummer en række begrænsninger og udfordringer. Databasernes indhold afspejler kun analyser, der anvendes som en del af klinisk praksis, idet biomarkører kun bliver målt såfremt, der er klinisk indikation for det. Hos nogle patientgrupper kan man forvente en højere grad af standardiseret brug af laboratorieanalyser (eksempelvis hos diabetikere og cancerpatienter i kontrolforløb). Analyseprincipper, herunder brug af metode, udstyr og reagens kan adskille sig markant mellem hospitalslaboratorier og kan ligeledes skifte over tid for det enkelte laboratorie. Det betyder, at niveauer af biomarkører, måleområder og referenceintervaller kan variere. Eksempelvis er der forskel på APTT analyser, idet der anvendes forskellige reagenser med varierende følsomhed for tilstedeværelse af lupus antikoagulans, og således skal analyseresultater tolkes i lyset heraf. Andre analyser som for eksempel INR er standardiset mellem laboratorierne. De nævnte metodemæssige udfordringer er vigtige at tage højde for i planlægningen af forskningsprojekter, der beror på laboratoriedata.
Konklusion
Sundhedsdata spiller en væsentlig rolle for udviklingen af det danske sundhedsvæsen og epidemiologisk forskning. Herunder udgør laboratoriedata en særlig vigtig datakilde, som også indenfor trombose/hæmostaseområdet har mange anvendelsesmuligheder.
Referencer
1) Schmidt M, Schmidt SAJ, Adelborg K, Sundbøll J, Laugesen K, Ehrenstein
V, Sørensen HT. The Danish health care system and epidemiological research: from health care contacts to database records. Clin Epidemiol. 2019
Jul 12;11:563-591 2) L Frank. Epidemiology. When an entire country is a cohort. Science 2000
Mar 31;287(5462):2398-9. 3) Arendt JFH, Hansen AT, Ladefoged SA, Sørensen HT, Pedersen L, Adelborg
K. Existing Data Sources in Clinical Epidemiology: Laboratory Information
System Databases in Denmark. Clinical Epidemiology 2020. 4) Adelborg K, Szentkúti P, Henriksen JE, Thomsen RW, Pedersen L, Sundbøll J,
Sørensen HT, Holther-Nielsen O, Beck-Nielsen H. The Funen Diabetes Database. BMJ Open 2020 5) Adelborg K, Kristensen NR, Nørgaard M, Bahmanyar S, Ghanima W, Cetin
K, Sørensen HT, Christiansen CF. Cardiovascular and Bleeding Outcomes in a
Nordic Cohort of Adult Patients with Chronic Immune Thrombocytopenia. J
Thromb Haemost. 2019 Jun;17(6):912-924 6) Adelborg K, Rasmussen TB, Layton B, Nørrelund H, Sørensen HT, Christiansen CF. Cardiovascular outcomes and all-cause mortality associated with endogeneous testosterone levels. Am J Cardiol. 2019 Jun 1;123(11):1757-1764 7) Arendt JFH, Farkas D, Pedersen L, Sørensen HT. Elevated plasma vitamin
B12 levels and risk of venous thromboembolism among cancer patients: A population-based cohort study. Thromb Res 2017 Aug;156:177-183 8) Pahus SH, Hansen AT, Hvas AM. Thrombophilia testing in young patients with ischemic stroke. Thromb Res. 2016 Jan;137:108-112 . 9) Kirkeby MH, Larsen JB, Grønbæk H, Hvas AM. Thrombophilia testing in patients with portal vein thrombosis. Scand J Clin Lab Invest. 2020
Dec;80(8):694-698 10) Sundbøll J, Larsen AP, Veres K, Adelborg K, Sørensen HT. Cardiovascular
Event Rates and Trajectories of LDL-Cholesterol Levels and Lipid-Lowering
Therapy in Patients with Atherosclerotic Cardiovascular Disease. Thromb
Res. 2019 Oct 23;183:124-130.
11) Thomsen RW, Nicolaisen SK, Hasvold P, Sanchez RG, Pedersen L, Adelborg
K, Egstrup K, Egfjord M, Sørensen HT. Elevated potassium levels in patients with congestive heart failure: occurrence, risk factors and clinical outcomes-a Danish population-based cohort study. J Am Heart Assoc. 2018
May 22;7(11)
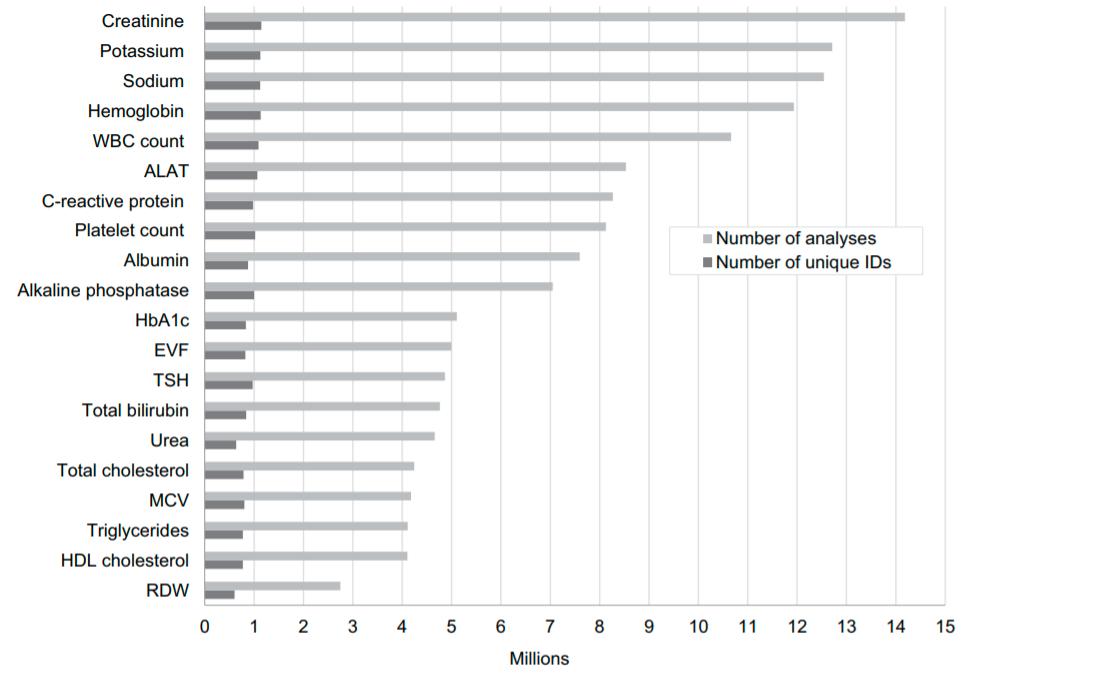
Figur 1: Fra artiklen af Arendt JFH et al3 som viser de 20 hyppigst anvendte laboratorieanalyser i Region Midtjylland i perioden 2008-2018.
Figur 1:
22.-24. NOVEMBER 2021 NORDISK KOAGULATIONSMØDE, SVERIGE 13.-15. OKTOBER 2021 ECHT, BELGIEN EFTERÅR 2021 DSTH EFTERÅRSMØDE

Xarelto (rivaroxaban) 15 mg, 20 mg og 10 mg (til forlænget behandling) filmovertrukne tabletter. Teksten er forkortet i
forhold til det godkendte produktresumé. Fuldstændigt produktresumé kan rekvireres vederlagsfrit fra Bayer
A/S, Tlf. 45 23 50 00. Læs venligst produktresuméet inden ordinering af lægemidlet. Indikation: Behandling af dyb venetrombose (DVT) og lungeemboli (PE) samt forebyggelse af recidiverende DVT og PE hos voksne. Dosering: Anbefalet dosis for indledende behandling af akut DVT eller PE er 15 mg to gange dagligt i de første 3 uger og derefter fortsat behandling og forebyggelse af recidiverende DVT og PE med 20 mg én gang dagligt. En kort behandlingsvarighed (mindst 3 måneder) bør overvejes hos patienter med DVT eller PE fremkaldt af større midlertidige risikofaktorer (f.eks. nyligt større kirurgisk indgreb eller traume). Længere behandlingsvarighed bør overvejes hos patienter med provokeret DVT eller PE, som ikke er forbundet med større midlertidige risikofaktorer, idiopatisk DVT eller PE, eller en anamnese med recidiverende DVT eller PE. Når forlænget forebyggelse af recidiverende DVT og PE er indiceret (efter mindst 6 måneders behandling af DVT eller PE), er den anbefalede dosis 10 mg én gang dagligt. Hos de patienter, hvor risikoen for recidiverende DVT eller PE anses for at være høj, f.eks. patienter med komplicerende comorbiditeter, eller patienter med recidiverende DVT eller PE under udvidet forebyggelses behandling med Xarelto 10 mg én gang dagligt, bør en dosis med Xarelto 20 mg én gang dagligt overvejes. Varighed af behandlingen og valg af dosis skal fastsættes individuelt efter omhyggelig afvejning af fordelen ved behandling mod risikoen for blødning.
Behandling og forebyggelse af recidiv DVT og PE Forebyggelse af recidiv DVT og PE Tidsperiode Doseringsplan
Total daglig dosis Dag 1-21 15 mg to gange dagligt 30 mg Fra og med dag 22 20 mg én gang dagligt 20 mg Efter mindst 6 måneders behandling for DVT eller PE 10 mg én gang dagligt eller 20 mg én gang dagligt 10 mg eller 20 mg
Til behandling af DVT, behandling af PE og forebyggelse af recidiverende DVT og PE, kræves der ingen dosisjustering af den anbefalede dosis hos patienter med let nedsat nyrefunktion (kreatinclearance 50-80 ml/min). Hos patienter med moderat nedsat nyrefunktion (kreatininclearance 30-49 ml/min) eller svært nedsat nyrefunktion (kreatininclearance 15-29 ml/min): Patienten skal behandles med 15 mg to gange dagligt i de første tre uger. Derefter, når den anbefalede dosis er 20 mg én gang dagligt, bør en dosisreduktion fra 20 mg én gang dagligt til 15 mg én gang dagligt overvejes, hvis det vurderes, at patientens risiko for blødning vejer tungere end risikoen for recidiverende PE og DVT. Når den anbefalede dosis er 10 mg én gang dagligt, kræves der ingen dosisjustering af den anbefalede dosis. Kontraindikationer: Overfølsomhed over for det aktive stof eller et/flere af hjælpestofferne. Aktiv, klinisk signifikant blødning. Læsion/tilstand med betydelig risiko for svær blødning (f.eks. nuværende/nylige ulcerationer i mavetarmkanalen, maligne tumorer med høj blødningsrisiko, nylige hjerne- eller spinale skader, nyligt gennemgået hjerne-, spinal- eller øjenkirurgi, nylig intrakraniel blødning, kendte eller mistænkte øsofagusvaricer, arteriovenøse misdannelser, vaskulære aneurysmer eller større intraspinale eller intracerebrale vaskulære abnormiteter). Samtidig behandling med andre antikoagulantia, f.eks. ufraktioneret heparin (UFH), lavmolekylære hepariner, heparinderivater, orale antikoagulantia bortset fra i de specifikke tilfælde, hvor der skiftes antikoagulations-behandling, eller når UFH gives i doser, der er nødvendige for at holde et centralt vene- eller arteriekateter åbent. Leversygdom, forbundet med koagulationsdefekt og klinisk relevant blødningsrisiko (inkl. Child-Pugh B og C). Graviditet og amning. Forsigtighed: Som ved andre antikoagulantia bør patienter, som får Xarelto, overvåges nøje for tegn på blødning. Forsigtighed bør udvises ved øget blødningsrisiko med klinisk overvågning for symptomer på blødning og evt. hæmoglobin/hæmatokrit. Blødningsrisiko kan øges med alderen. Behandling bør afbrydes ved svær blødning. Xarelto bør ikke anvendes til patienter med CrCl på < 15 ml/min. Xarelto skal bruges med forsigtighed hos patienter med CrCl 15-29 ml/min. Bør anvendes med forsigtighed i pt med nedsat nyrefunktion som samtidig behandles med andre lægemidler, der øger plasmakoncentrationerne af rivaroxaban. Frarådes til pt med kunstig hjerteklapper. Ved moderat nedsat leverfunktion kan ses øget blødningsrisiko. Som ved andre antitrombotika anbefales rivaroxaban ikke til patienter med øget blødningsrisiko. Spinal/epiduralanæstesi eller -punktur: Patienten skal overvåges hyppigt for symptomer på neurologisk svækkelse og hvis sådan opstår skal der øjeblikkeligt stilles diagnose og iværksættes behandling. Fjernelse af epiduralkateter skal ske mindst 18 timer for unge patienter og 26 timer for ældre patienter efter sidste dosis og næste dosis må tidligst gives 6 timer efter fjernelse. Ved traumatisk punktur pauseres i 24 timer. Ved kirurgi og invasive indgreb: Xarelto bør så vidt muligt seponeres mindst 24 timer før indgrebet baseret på en klinisk vurdering. Hvis indgrebet ikke kan udskydes må den øgede blødningsrisiko afvejes mod behovet for hurtig intervention. Rivaroxaban bør seponeres ved første forekomst af et alvorligt hududslæt eller andre tegn på overfølsomhed som f.eks. slimhinde læsioner. Interaktioner: Frarådes hos pt som samtidig får systemisk beh. med lægemiddel som er både kraftig hæmmer af CYP3A4- og P-gp (ketoconazol, itraconozol, voriconazol, posaconazol, HIV-proteasehæmmere, eks. ritonavir). Interaktion med clarithromycin, erythromycin, flucanazol kan potentielt være signifikant hos højrisikopatienter. Dronedaron, bør det ikke gives sammen med rivaroxaban. Der skal udvises forsigtighed hos patienter, der får samtidig behandling med NSAID (herunder acetylsalicylsyre), trombocytaggregationshæmmere og SSRI/SNRI-præparater. Samtidig brug af stærke CYP3A4-induktorer (f.eks. rifampicin, phenytoin, carbamazepin) bør undgås da det kan medføre et fald i plasmakoncentrationerne af rivaroxaban. Fertilitet, graviditet og amning: Bør ikke anvendes. Overdosering: Ingen antidot. Til begrænsning af absorption kan aktivt kul overvejes. Ved blødning skal næste rivaroxaban administration udsættes, eller seponeres efter lægens vurdering. Hensigtsmæssig symptomatisk behandling kan benyttes f.eks. mekanisk kompression, kirurgisk hæmostase, væskesubstitution og hæmodynamisk understøttelse, blodprodukter (pakkede røde blodlegemer eller friskfrosset plasma, blodplader). Såfremt blødningen ikke kan standses, skal der overvejes administration af protrombinkomplekskoncentrat (PCC), aktiveret protrombinkomplekskoncentrat (APCC) eller rekombinant faktor VIIa (r-FVIIa). Bivirkninger: Almindelige: Anæmi, svimmelhed, hovedpine, blødning i øjet herunder konjuktiva, hypotension, hæmatom, epistaxis, hæmoptyse, gingival blødning, blødning fra mave-tarmkanalen, gastrointestinale og abdominale smerter, dyspepsi, nausea, obstipation, diaré, opkastning, forhøjede aminotransferaser, pruritus, udslæt, ekkymose, kutan og subkutan blødning, smerter i ekstremitet, blødning i urogenitalkanalen (herunder hæmaturi og menoragi), nedsat nyrefunktion, feber, perifert ødem, nedsat generel styrke og energi, post-procedural blødning, kontusion, sårsekretion. Ikke almindelige: Trombocytose, trombocytopeni, allergisk reaktion, allergisk dermatitis, angioødem og allergisk ødem, cerebral og intrakraniel blødning, synkope, takykardi, mundtørhed, nedsat leverfunktion, forhøjet bilirubin, forhøjet basisk serumforfatase, forhøjet GGT, urticaria, hæmartrose, utilpashed, forhøjet LDH, forhøjet lipase, forhøjet amylase. Sjældne: Gulsot, stigning i konjungeret bilirubin, koletase, hepatitis, muskelblødning, lokalt ødem, vaskular pseudoaneurisme. Meget sjældne: Anafylaktiske reaktioner, inkl. anafylaktisk shock, Stevens–Johnsons syndrom/toksisk epidermal nekrolyse og DRESS syndrom. Ikke kendt hyppighed: Kompartmentsyndrom, nyresvigt/akut nyresvigt sekundært til blødning med hypoperfusion. Pakningsstørrelser: 15 mg: 28/42/98/100 tabletter. 20 mg: 28/98/100 tabletter. 10 mg: 10/30/100 tabletter. Receptpligtigt. Udlevering: B. Tilskud: Generelt tilskud. For aktuel pris se: www.medicinpriser.dk. Dato for SPC: November 2019. Indehaver af markedsføringstilladelsen: Bayer AG, 13342 Berlin, Tyskland. Dansk repræsentant: Bayer A/S, Arne Jacobsens Allé 13, 6. DK-2300 København S. Tlf. 45 23 50 00.
▼ Dette lægemiddel er underlagt supplerende overvågning. Dermed kan nye sikkerhedsoplysninger hurtigt tilvejebringes.
Læger og sundhedspersonale anmodes om at indberette alle formodede bivirkninger. PP-XAR-DK-0404-2 – Januar 2020







