Spis treści
3.3.
3.4.
3.5.
3.6. Skrót informacji na temat pacjentów z uszkodzeniami funkcji
3.7. Regulacje prawne wobec osób z otępieniem
3.7.1. Przemoc wobec osób starszych ......................................................................
3.7.2. Ochrona danych osobowych i ubezwłasnowolnienie
3.7.3. Usługi finansowe ..................................................................................................
3.8. Starszy kierowca .................................................................................................................
3.8.1. Badanie pacjentów / kierowców w podeszłym wieku
3.8.2. Leki u starszego kierowcy .................................................................................
3.8.3. Sytuacja w Polsce .................................................................................................
4. Będę miał operację
Elżbieta Pyrkosz-Cifonelli ..............................................................................................................
4.1. Zabieg operacyjny u starszego chorego – chirurgia geriatryczna
4.2. Ocena chorego w starszym wieku a ryzyko zabiegu .............................................
4.3. Całościowa ocena geriatryczna (COG) u pacjentów oddziału chirurgicznego .....................................................................................................................
4.4. Proaktywna opieka nad starszym pacjentem kierowanym do leczenia operacyjnego − POPS ...............................................................................
4.5. Wnioskowanie z raportów, audytów i dużych baz danych .................................
4.6. Czego chcę dla mojego operowanego pacjenta
4.7. W poszukiwaniu sposobu przedoperacyjnej oceny ryzyka zachorowalności i śmiertelności
4.8. Zakres
4.9. Optymalizacja przed operacją w trybie
5. Mobilizacja rezerw. Przygotowanie do planowego zabiegu operacyjnego osoby starszej – Elżbieta Pyrkosz-Cifonelli, Piotr Seiffert
5.1. Starszy chory z problemami medycznymi − choroba niedokrwienna serca .........................................................................................................
5.2. Przedoperacyjna ocena kardiologiczna u pacjentów z chorobą niedokrwienną serca i innymi stanami kardiologicznymi ...................................
5.3. Farmakologiczna optymalizacja przed planową operacją u starszych pacjentów z chorobą niedokrwienną serca i/lub czynnikami ryzyka sercowo-naczyniowego ...................................................
5.4. Przygotowanie do planowego zabiegu operacyjnego osoby starszej z nadciśnieniem tętniczym .............................................................................................
5.5. Przygotowanie do planowego zabiegu operacyjnego osoby starszej z niewydolnością serca ..................................................................................................... 279
5.6. Przygotowanie do planowego zabiegu operacyjnego starszego pacjenta ze stenozą aortalną .........................................................................................
5.7. Przygotowanie do planowego zabiegu operacyjnego osoby starszej z nadciśnieniem płucnym ................................................................................................
5.8. Przygotowanie do planowego zabiegu operacyjnego starszego chorego z przewlekłą niewydolnością nerek ...........................................................
5.9. Przygotowanie do planowego zabiegu operacyjnego starszego pacjenta z anemią ..............................................................................................................
5.10. Niedożywienie i leczenie żywieniowe. Przygotowanie do zabiegu operacyjnego .......................................................................................................................
5.11. Przygotowanie do planowego zabiegu operacyjnego osoby starszej. Prehabilitacja .........................................................................................
6. Biodro w dobrych rękach. Opieka nad starszym pacjentem ze złamaniem biodra
Elżbieta
6.2.
6.3. Rozpoznawanie i leczenie bólu oraz majaczenia w okresie
6.4. Przygotowanie do wypisu
6.5. Prewencja wtórna złamań – profilaktyka upadków
7. Jak statek z papieru. Frailty. Leczenie chorych
7.1.1.
7.1.2.
7.2.
7.3.
7.4.
8. Dolce vita − słodkie życie Janina Kokoszka-Paszkot .................................................................................................................
8.1. Diagnostyka i objawy cukrzycy w starszym wieku ................................................
8.1.1. Przydatność COG w prowadzeniu chorych z cukrzycą ...........................
8.1.2. Wysiłek fizyczny u pacjenta geriatrycznego z cukrzycą .........................
8.1.3. Postępowanie farmakologiczne – wybór terapii hiperglikemii ..........................................................................................................
8.1.4. Pochodne biguanidów – metformina ..........................................................
8.1.5. Pochodne sulfonylomocznika .........................................................................
8.1.6. Inhibitory DPP IV – gliptyny .............................................................................
8.1.7. Inhibitory kotransportera sodowo-glukozowego 2 (SGLT-2) ...............
8.1.8. Insulinoterapia ......................................................................................................
8.1.9. Modele terapii cukrzycy w geriatrii ...............................................................
8.1.10. Indywidualizacja drogi osiągania celów ......................................................
8.1.11. Modele
8.2. Hipoglikemia i hiperglikemia – motory napędowe zespołów
8.2.1. Czynniki ryzyka rozwoju cukrzycy w populacji geriatrycznej ............. 467
8.2.2. Wpływ hipoglikemii na ryzyko sercowo-naczyniowe i mózg ..............
8.2.3. Metaanalizy, badania randomizowane a pacjent geriatryczny z cukrzycą ......................................................................................
8.3. Podniesienie efektywności opieki nad chorym z zespołem
8.3.1. Patogeneza zespołu stopy cukrzycowej (ZSC) ..........................................
8.3.2. Jak pomóc pacjentowi z rozpoznanym zespołem stopy cukrzycowej ...............................................................................................
9. W labiryncie wyborów − doświadczenia własne
9.1. Podejście geriatryczne do pacjentów w zaawansowanej starości ................... 489
9.2. Cele badania geriatrycznego ......................................................................................... 495
9.3. Zasady prowadzenia badania geriatrycznego – warunki przeprowadzania COG ......................................................................................................
9.3.1. Miejsce badania ....................................................................................................
9.3.2. Jak poprowadzić wywiad? ................................................................................
9.3.3. Badanie geriatryczne i przydatny sprzęt ..................................................... 517
9.3.4. Testy i pytania, których nie powinno zabraknąć .......................................
9.4. ABC terapii geriatrycznych .............................................................................................. 535
9.5. Leczenie chorych z depresją i otępieniem ................................................................ 543
9.6. Majaczenie nakładające się na otępienie .................................................................. 552
9.7. Leczenie chorych ze spowolnieniem ruchowym .................................................... 555
9.8. Nie dość, że zaparcie, to jeszcze bezsenność – pozornie błahe problemy ............................................................................................................................... 561
9.9. Co będzie istotne w terapiach geriatrycznych w przyszłości ............................. 566
10.1. Pacjent zakażony SARS-CoV-2 – Dorota Religa ........................................................ 571
10.1.1. Dyskusja
10.2. Upadek u starszej osoby z powodu bloku przedsionkowo-komorowego III stopnia indukowanego riwastygminą – Elżbieta Pyrkosz-Cifonelli
10.3. Pacjentka z krwiopluciem – opis przypadku – Jarosław Derejczyk
10.4. Kobieta 81-letnia z powtarzającymi się upadkami – Piotr Seiffert
Całościowa ocena geriatryczna pacjentki ...................................................
10.5. Nawracające zakażenie Clostridioides difficile (Clostridioides difficile infection – CDI) – Piotr Seiffert ........................................................................................
10.6. Pacjent z zespołem stopy cukrzycowej – Janina Kokoszka-Paszkot
Dlaczego ta książka
Szanowni Państwo!
Niniejsza publikacja powstała w celu przybliżenia Czytelnikowi możliwości i wyzwań geriatrii w diagnostyce i leczeniu chorób związanych z procesami starzenia, stąd tytuł: Drogowskazy w Geriatrii. Jako młodą dziedzinę medyczną o 100-letniej historii, w 2021 roku zastajemy geriatrię w okresie przechodzenia z czasu dorastania w okres dojrzałości.
Przekonuje nas ona, jako pomysłodawców książki, oferowanym bogactwem interpretacji w podejściu do licznych problemów starszych schorowanych osób. Pozwala dostrzec między nagromadzonymi zagadkami, z jakimi mamy do czynienia podczas kolejnego badania starszego pacjenta, indywidualną ścieżkę, którą starać się będziemy go poprowadzić w kierunku zachowania i podtrzymania słabnących rezerw. Dzięki temu podejściu kategoria zmian określonych jako „nieodwracalne z powodu wieku” jest w geriatrii weryfikowana – prawda czy fałsz. Czasem jest to istotnie stwierdzenie braku rezerw, połączone z leczeniem podtrzymującym jakość życia w końcowym jego okresie. Zdecydowanie częściej udaje się jednak dodać lat życia i nie zawsze z udziałem medycyny opartej na faktach. Te „darowane” lata zaskakują wówczas leczących, opiekunów, rozradowując chorego, który wcześniej usłyszał, że w tym wieku zbyt wiele nie powinien oczekiwać.
Kolejnym powodem napisania książki była chęć przybliżenia lekarzom, pracownikom medycznym innych specjalności i branż, szczególnie medycyny rodzinnej, zabiegowej i pielęgniarstwa, mechanizmów patofizjologicznych chorób i zespołów geriatrycznych oraz języka komunikacji, którym posługuje się geriatria. Wyjątkowa złożoność procesu starzenia stanowiła trudne wyzwanie, by precyzyjnie opisać i połączyć zmiany zachodzące na poziomie cząsteczek, tkanek i narządów z objawami spotykanymi przy łóżku cierpiącego starszego człowieka. Dlatego autorzy zaproponowali, na przykładzie osób długowiecznych, posługiwanie się cechami fenotypowymi, które pozwalają rozróżnić odmienne kategorie i trajektorie starzenia, wykorzystując w opisie podstawowe pojęcia z zakresu biologii starzenia.
Ochrona najsłabszych pacjentów wśród populacji osób starszych, czyli osób z zespołem kruchości, jest również jednym z celów tej publikacji. W książce zamieszczono opisy stosowania wybranych narzędzi całościowej oceny geriatrycznej, zestawiając
je z doświadczeniami własnymi autorów, nabytymi w ośrodkach krajowych, angielskich i szwedzkich. Uczyniono to z nadzieją, że fragmenty książki, w których autorzy dzielą się własnymi doświadczeniami będą również przydatne dla lekarzy i pielęgniarek zaczynających specjalizację z geriatrii. Dużą część książki stanowią opisy geriatrii okołooperacyjnej.
Geriatria podnosi bezpieczeństwo terapii i najefektywniej, spośród innych dziedzin medycznych, poprawia skuteczność leczenia i opieki nad starszymi chorymi z wielochorobowością, zmniejszając koszty opieki medycznej przez redukcję częstości rehospitalizacji takich pacjentów, ograniczanie jatropatogenii i racjonalizację farmakoterapii.
Opisana w książce metoda podnosząca dbałość w podejściu do starszych chorych opiera się na zasadzie pracy w zespołach wielospecjalistycznych, z uwzględnieniem metodologii warsztatów stosowanych w neuropsychologii, rehabilitacji geriatrycznej i diabetologii geriatrycznej.
Przedstawiono też przydatne rozwiązania umożliwiające przygotowanie telekonsultacji geriatrycznych oraz zasady oceny starszych kierowców pod kątem podniesienia bezpieczeństwa prowadzenia przez nich pojazdów.
W geriatrii pełne wyzdrowienie i wyleczenie choroby zostaje zastąpione zazwyczaj zmniejszeniem dolegliwości i zahamowaniem tempa spadku sprawności funkcjonalnej. Radykalne usuniecie dolegliwości, typowe dla medycyny zabiegowej, w geriatrii jest kwestią skutecznego zmniejszenia zagrożenia. Temat ten znalazł swoje miejsce w książce, w części poświęconej terapiom geriatrycznym, w której autorzy dzielą się swoimi doświadczeniami – to część o przypadkach z życia wziętych. Faktyczne wartościowanie zdrowia seniorów zostało poddane poważanej próbie w roku 2020, w okresie pandemii COVID-19, szczególnie mocno w placówkach opieki długoterminowej, i pokazało celowość oraz konieczność poszukiwania lepszych rozwiązań organizacyjnych, z wykorzystaniem podejścia geriatrycznego. Piszemy również i o tym.
Od niedawna obserwujemy budzącą się pasję do wiedzy z geriatrii wśród studentów i młodych adeptów studiów medycznych, rozumiejących potrzebę oparcia pracy ze starszymi chorymi na zasadach gerontologii i geriatrii. Podejmują się oni zdobywania tej wiedzy bez względu na trudności, jakie stwarza praca z ciężko chorymi, i warunki zewnętrzne, w jakich zdarza się pracować. Również im dedykujemy tę publikację.
Historyczny dorobek życia osób starszych, ich godność i wkład, jaki wnieśli w rozwój kolejnych pokoleń, nakazują zapewnienie im ochrony i wsparcia w chwilach, gdy słabną w pokonywaniu chorób. Jest to powinnością ich następców i ten argument był dla nas kluczowy podczas prac nad książką.
Zachęcamy do lektury.
Dorota Religa Jarosław Derejczyk
mogą ją wzmocnić przez mobilizację wydajnych rezerw, a inną osobę z tym samym stanem obciążenia − mogą wyczerpać, przez zużycie słabszych osobniczo rezerw, które nie pozwoliły już na podtrzymanie mechanizmów dostosowawczych. Wpływ epigenetyczny polega na zmianach ekspresji genów, które nie są związane ze zmianami w sekwencji nukleotydów w DNA, a zależą od procesu metylacji, modyfikacji składu histonów, od aktywności niekodującego miRNA oraz od zmian w kondensacji i dekondensacji chromatyny w komórkach rozrodczych. Ekspresja ta jest modyfikowana przez czynniki zewnętrzne i podlega dziedziczeniu (55).
Jeżeli AL trwa długo, intensywnie wyczerpując zasoby adaptacyjne, to nawet u najwytrwalszych osób doprowadza do śmierci – śmierć allostatyczna. Ocena wskaźników Al, na podsatwie badań markerów biomedycznych, gromadzonych w trybie ciągłym, uzupełnionych badaniami neuropsychologicznymi oraz danymi na temat stylu życia, umożliwia estymację prawdopodobieństwa zachorowania i śmierci (56).
W obydwu przytoczonych sytuacjach, związanych z nasileniem stresów środowiskowych, opisano występowanie zmian w korze przedczołowej, hipokampie, ciele migdałowatym oraz mezolimbicznym szlaku dopaminergicznym. Zaobserwowano pojawienie się towarzyszącego im wzrostu stężenia mediatorów zapalnych, wzrostu aktywowanych monocytów i makrofagów we krwi oraz w płynie mózgowo-rdzeniowym. Znanymi konsekwencjami SES i AL są reakcje w postaci wzrostu ciśnienia tętniczego, większej częstości insulinooporności, otyłości, nadwagi, cukrzycy, przyspieszonego rozwoju miażdżycy, spadku libido i płodności oraz szybszego zużycia telomerów Szybko żyjący młody człowiek, nastawiony na rywalizację, pracoholizm i wyróżnianie się autami, zdzierając ich opony podczas szybkiej jazdy, czynić może podobnie ze swoimi telomerami.
Funkcjonowanie układów monoaminoergicznych mózgu, w przewlekłym stresie, wiąże się ze zmianą metylacji DNA, potranslacyjną modyfikacją histonów stabilizujących DNA w chromosomach i ze zmianami w aktywności miRNA. Zmiany wywołane czynnikami epigenetycznymi zostają inkorporowane na trwale do genomu osobnika i mogą ujawniać się w następnych pokoleniach po włączeniu zmian do linii komórek generatywnych. Czynniki stresujące, na jakie są wystawione zwierzęta doświadczalne w okresie zarodkowym powodują wzrost ekspresji mRNA receptora D2 i spadek miRNA-9 w prążkowiu, natomiast w okresie dorosłości nasilają ekspresję mRNA i poziom białka receptora D2, a także powodują spadek ekspresji miRNA-9 w jądrze półleżącym (nucleus accumbens − NAC). Zaobserwowane zmiany w okresie neonatalnym korelowały z nasileniem zachowań depresyjnych w późniejszym okresie życia (57).
2.2. Latarnia w ciemności
Osoby z cechami długowieczności pozostają oporne na stresy przez wyjątkowo długi okres, co świadczy, że muszą mieć sprawny system ochrony integralności genetycznej DNA i muszą skutecznie zmniejszać efekty impresji wielostresowej, na jakie przez całe życie narażane są ich komórki. W świetle nowych badań stres jest czynnikiem destabilizującym genom od urodzenia. Różnice w metylacji genomu już od okresu dzieciństwa są powiązane z natężeniem stresu. Ocena miejsc metylacji w DNA u dzieci narażonych na AL wykazuje zmienione stosunki ilościowe metylacji (oceniana w komórkach nabłonka jamy ustnej), co wiązano z rosnącym poziomem kortyzolu we krwi w stosunku do grupy normatywnej. Niedostateczne środki na utrzymanie rodziny i konsekwencje niskiego statusu społeczno-ekonomicznego rodziny wpływały u dzieci, przez metylację DNA, na regulację transkrypcji. Nadmierny poziom AL jest uznanym predyktorem zmienionej metylacji DNA, co przekłada się na zmienioną epigenetycznie transkrypcję i odpowiedź komórkową (59).
Ważną cechą modulującą indywidulane trajektorie starzenia poza opisanymi dotychczas jest utrzymanie sprawności nadzoru immunologicznego i kontroli onkogenezy, których wydolność spada w etapie poprokreacyjnym. Opisane zmiany w układzie odpornościowym, występujące w przebiegu starzenia (immunosenescencja) przedstawiono na rycinie 2.6.
Rycina 2.6.
Zmiany układu immunologicznego w przebiegu starzenia
• Inwolucja grasicy
• Obniżony stosunek „naiwnych” limfocytów T do komórek pamięci
• Dysfunkcje hematopoetycznych komórek macierzystych
• Nasilenie produkcji cytokin prozapalnych (np. IL-1 i IL-6)
• Wzrost produkcji interferonu γ (IFNγ) i czynnika mar twicy nowotworów α (TNF-α)
• Obniżona produkcja interleukiny-2, -3, -4 (IL-2, -3, -4)
• Przesunięcie profilu cytokin tworzonych z linii Th2, a nie z Th1 (odwrotnie niż u osobników młodych)
• Obniżenie liczby limfocytów B i monocytów, wzrost poziomu autoprzeciwciał
• Oligoklonalna ekspansja limfocytów T populacji CD8+
• Wzrost zawartości oksydacyjnych uszkodzeń w limfocytach T
• Akumulacja limfocytów T ze skróconymi telomerami
• Obniżona produkcja wtórnych przekaźników sygnału w limfocytach T
• Osłabienie zdolności przekazywania sygnału przezbłonowego w limfocytach T
• Osłabienie autofagocytozy
Wybrane zmiany układu immunologicznego występujące w przebiegu procesu starzenia. Odpowiadają one za większą liczbę chorób z autoagresji, podatność na infekcje bakteryjne, wirusowe i grzybicze oraz za częstszą kolonizację bakteriami lekoopornymi, spotykanymi w starszym wieku. Opracowano na podstawie (59).
Rehabilitacja po operacji naprawczej złamania biodra powinna uwzględnić odrębności stwierdzane u każdego starszego pacjenta. Jedni są zdeterminowani, aby wstać z łóżka i zacząć chodzić, by jak najszybciej pójść do domu, a inni są głęboko przestraszeni niedawnym urazem i tracą pewność siebie, rozwijając zespół poupadkowy. Są też pacjenci z długo trwającymi problemami w chodzie i równowadze, z wcześniejszymi upadkami, po leczeniu poprzednich złamań kości. Przebieg rehabilitacji dla każdej z tych grup chorych różni się, ale „usprawnienie” wszystkich pacjentów zawiera te same elementy obowiązujące w pierwszym tygodniu po operacji. Zazwyczaj sesje fizjoterapii są złożone, składają się z ćwiczeń poprawiających mobilność, równowagę, siłę i wytrzymałość mięśni celem uniknięcia przyszłych upadków i uszkodzeń, aby starszy pacjent odzyskał pewność siebie po złamaniu biodra. Największy nacisk kładzie się na odzyskanie zdolności do chodzenia i przemieszczania się między łóżkiem a krzesłem z oparciem. Są to najważniejsze elementy wczesnej rehabilitacji podejmowane po operacji z powodu złamania biodra, determinujące, jak szybko pacjent wróci do domu. W ciągu następnych dni pooperacyjnego usprawniania rehabilitacja jest wzbogacona o inne elementy. Przeciętny czas sesji fizjoterapii to około pół godziny i zmniejsza się w ciągu następnych dni (do około 15 minut dziennie). Każdemu pacjentowi terapeuta poświęca około 2 godzin w pierwszym tygodniu po operacji. Komponenty rehabilitacji podczas pierwszego tygodnia po operacji naprawczej biodra u pacjentów w wieku powyżej 65. r.ż. przedstawiono na rycinie 6.13.
Wyniki analizy audytu wskazują, że w blisko 40% oddziałów szpitalnych pooperacyjne uruchomienie starszych pacjentów odbywa się przez wszystkie dni tygodnia.
Rycina 6.13.
Liczba pacjentów (%)
Uruchomienie
Przenoszenie
Chód
Zakres ruchu
Siła Równowaga Dzień 1Dzień 2Dzień 3Dzień 4Dzień 5Dzień 6Dzień 7
Komponenty rehabilitacji (uruchomienie, przenoszenie, chód, zakres ruchu, siła, równowaga) podczas pierwszego tygodnia po operacji naprawczej biodra u starszych pacjentów − raport audytu Hip SPRINT z 2018 r.
W sesjach rehabilitacji biorą udział fizjoterapeuta wraz ze swoim pomocnikiem lub z terapeutą zajęciowym. Obecność terapeuty zajęciowego wynika z rozpoznawania zakresu usprawniania nakierowanego na inne, niż funkcja chodu, potrzeby związane z aktywnością motoryczną.
W miarę postępu procesu rehabilitacji usprawnienie przejmują w Wielkiej Brytanii pomocnicy fizjoterapeutów i pielęgniarki. Cały czas opieka ma charakter pracy zespołowej dostosowanej do indywidualnych potrzeb pacjenta (ryc. 6.14).
Funkcjonowanie pacjentów przed złamaniem ma silny wpływ na przebieg rehabilitacji. Rehabilitacja pacjentów o osłabionej funkcji chodu przed urazem wymaga zaangażowania większej liczby osób oraz więcej sprzętu rehabilitacyjnego. Ci pacjenci, którzy przed urazem poruszali się za pomocą wózka inwalidzkiego lub byli leżący, mają mniejsze potrzeby rehabilitacji ruchowej na wczesnym okresie pooperacyjnym. Wyniki rehabilitacji starszych pacjentów po złamaniu biodra ocenia się na podstawie stopnia, w jakim odzyskali poprzednią jakość życia pod względem ich stanu psychicznego, fizycznego, życia rodzinnego, społecznego, ewentualnie zatrudnienia.
Na oddziałach szpitalnych w Wielkiejj Brytanii fizjoterapeuci używają różnych wskaźników oceny poprawy sprawności ruchowej. Nie jest to jednak powszechne. Powtarzane testy „Timed Up and Go” są wykorzystywane u 8% pacjentów, a skala Barthel u 5%. Częściej fizjoterapeuci dążą do usprawnienia pacjentów prowadzącego do osiągnięcia funkcjonalności umożliwiającej im chodzenie po mieszkaniu i/lub wychodzenie na zewnątrz. Tak dzieje się u 25% chorych. U pozostałych nie są stosowane żadne środki monitorowania wyników funkcjonalnych. Większość pacjentów kończy rehabilitację przed 4. miesiącem po złamaniu biodra.
Dane z FLS (Fracture Liaison Service) wskazują, że wśród znacznego odsetka monitorowanych pacjentów po wypisie z oddziału ortopedycznego i ortogeriatrycznego poziom sprawności funkcjonalnej wielu z nich ulega znacznym zmianom w stosunku do stanu sprzed złamania. Ponad 1/3 przed upadkiem chodziła samodzielnie i sprawnie (to zapewne osoby aktywne, ale w dużej części z nieświadomością obecności osteoporozy). Po 4 miesiącach od operacji grupa „pełnego sukcesu”, czyli pacjentów powracających do pełnej sprawności z chodem bez laski stanowi 10%, z kolei grupa „powodzenia”, która po wypisie na stałe przemieszczała się, używając laski lub balkonika, stanowiła 18%. Grupa „częściowego powodzenia”, czyli ci, którzy utracili zdolność do przemieszczania się, stanowiła 9%, a 54% to osoby używające również laski przed złamaniem (ryc. 6.15).
Mózg jest organem związanym z permanentną, całożyciową transmisją miliardów sygnałów przez bardzo liczne receptory, w tym przez receptory insulinowe w neuronach, które są włączone w tworzenie śladów pamięci. Zarówno hiperinsulinemia, jak i insulinooporność obwodowa pozostają w związku z upośledzoną sygnalizacją na poziomie transferu receptorowego w neuronach, zmniejszając neuronalny wychwyt insuliny i jej oddziaływanie na neurony i komórki mikrogleju. Prowadzi to do upośledzenia sprawności pamięci, zwiększenia poziomu mediatorów zapalnych i intensywniejszego odkładania β-amyloidu w mózgu.
Kolejnymi elementami łańcucha patofizjologicznych zmian stwierdzanych w cukrzycy jest zaobserwowana zwiększona produkcja glutaminianu w hiperglikemii, z następowym rozregulowaniem napływu jonów Ca2+ i uszkodzenie bariery krew–płyn mózgowo-rdzeniowy (6).
Pojawiają się kolejne dowody, że zmiany obserwowane w obrocie zaawansowanymi produktami glikacji (advanced glycation end products – AGE), jakie towarzyszą starzeniu i cukrzycowej hiperglikemii oraz ich zaburzony transport receptorowy w neuronach są włączone w tworzenie zmian (płytki starcze i splątki fibrylarne) towarzyszących procesowi neurodegeneracji (7).
Wydawało się, że wprowadzenie intensywnego wyrównania metabolicznego cukrzycy, monitorowanego natężeniem glikacji (na podstawie stężenia HbA1c) powinno mieć według założeń hipotezy o pamięci metabolicznej pozytywny efekt na powikłania sercowo-naczyniowe w cukrzycy. Tak się nie stało i w badaniu ACCORD (Action to Control Cardiovascular Risk in Diabetes) opublikowanym w 2008 r. wykazano, że intensywna kontrola glikemii wiązała się ze zwiększoną śmiertelnością, zwłaszcza w przypadku chorych w starszym wieku, z długim czasem trwania cukrzycy typu 2 i wysokim ryzykiem sercowo-naczyniowym (17).
Okazało się, że w przypadku pacjentów w starszym wieku z cukrzycą hipoglikemia, określana od stężenia glukozy we krwi żylnej poniżej 70 mg/dl (< 3,9 mmol/l), jest częstsza niż sądzono w trakcie intensywnej terapii cukrzycy typu 1 i 2. Porównanie ryzyka następstw przewlekłej hiperglikemii i zmian w ekspresji genów, decydujących o powstaniu odległych objawów powikłań naczyniowych powiązanych z pamięcią metaboliczną, wykazało mniejsze ryzyko następstw hiperglikemii niż hipoglikemii podczas terapii normalizującej glikemię (14).
To odkrycie przyczyniło się do ostrożniejszego spoglądania na restrykcyjne zalecenia dotyczące m.in. poziomu hemoglobiny glikowanej HbA1c < 6%, jako wartości
8.2. Hipoglikemia i hiperglikemia – motory napędowe zespołów geriatrycznych
referencyjnej prawidłowego wyrównania cukrzycy. Prawdziwa rewolucja w podejściu do leczenia pacjentów zwłaszcza w starszych grupach wiekowych nastąpiła po publikacji kolejnych badań na temat związku wyrównania cukrzycy i następstw sercowo-naczyniowych. Były to badania ADVANCE (Action in Diabetes and Vascular Disease: Preterax and Diamicron Modified Release Controlled Evaluation) oraz VADT (Veterans Affairs Diabetes Trial) (18).
Badanie ADVANCE wykazało, że przy intensywnej terapii cukrzycy obserwuje się zmniejszenie postępu albuminurii, ale nie było zmian w częstości występowania ciężkiej nefropatii, retinopatii ani incydentów sercowo-naczyniowych. Wyniki badania VADT wskazały, że intensywna kontrola glikemii nie jest związana ze zmniejszeniem częstości incydentów makronaczyniowych lub mikronaczyniowych w porównaniu ze standardową terapią glikemiczną u pacjentów ze słabo kontrolowaną cukrzycą typu 2 i wiążę się ze zwiększeniem częstości występowania zdarzeń niepożądanych wynikających z powodu hipoglikemii (19).
8.2.2. Wpływ hipoglikemii na ryzyko sercowo-naczyniowe i mózg
Wiele randomizowanych badań i metaanaliz wykazało pozytywny wpływ intensywnej kontroli metabolicznej na ograniczenie ryzyka rozwoju mikroangiopatii. Co istotne, aby intensywna terapia hipoglikemizująca skutecznie hamowała postęp zmian o charakterze mikroangiopatii, musi trwać 8 lat. Zmniejszenie ryzyka rozwoju makroangipopatii nie jest już tak oczywiste ze względu na zwiększone ryzyko epizodów hipoglikemii. Równocześnie należy mieć na uwadze, że intensywna kontrola glikemii w badaniach ACCORD i ADVANCE prowadziła do częstszego występowania zdarzeń sercowo-naczyniowych. Badanie ACCORD obejmujące 10 251 pacjentów z cukrzycą typu 2, ze względu na 22% większą częstość zgonów z przyczyn sercowo-naczyniowych zostało przerwane. Wykazano, że wyższa śmiertelność u tych chorych była skorelowana z większą częstością epizodów hipoglikemii. Z punktu widzenia patofizjologicznego hipoglikemia ma negatywny wpływ na układ sercowo-naczyniowy.
Przez aktywację układu współczulnego, wyrzut katecholamin i wzrost oporu obwodowego dochodzi do zwyżki ciśnienia tętniczego krwi, uszkodzeniu ulega śródbłonek naczyniowy, nasilają się stres oksydacyjny, zaburzenia zakrzepowo-zatorowe, podnosi się stężenie parametrów zapalnych. Obserwowane są destabilizacja blaszki miażdżycowej, zaburzenia rytmu, tachykardia, napadowe migotanie przedsionków, komorowe zaburzenia rytmu, występowanie wydłużonego odstępu QT, skrócenie
Rycina 9.3.
Sprawność funkcjonowania neuronów DA Wiek w latach
Model starzenia neuronów w chorobie Parkinsona. Sprawność obrotu dopaminy w neuronach DA maleje w chorobie z powodu podatności i aktywnego metabolizmu
DA przebiegającego z szybszą degeneracją neuronów. Mniejsza wydolność układu
DA w zespole parkinsonowskim identyfikowana jest często już od 30. r.ż. W celu rozpoznania ukrytego zespołu parkinsonowskiego, w postaci łagodnych objawów parkinsonowskich, podczas oceny geriatrycznej wymagane jest rutynowe przeprowadzenie testów identyfikujących ten zespół od okresu wczesnej starości. Opracowano na podstawie (16).
Wpływ A. Spadek zdolności regulacyjnych zaobserwowano w: mechanizmie tworzenie DA, w syntezie transporterów DA, w regulacji równowagi oksydoredukcyjnej i proteostazy. Nazwano ten stan dyshomeostazą układu neuronów DA.
Wpływ B. Nasileniu ulega dysfunkcja komórek produkujących DA z nagromadzeniem innych patologii w postaci: kumulacji RFT, przeciążenia neuronów jonami wapnia, zwiększenia liczby mutacji w mitochondrialnym DNA, nasilenia apoptozy neuronów, zaburzeń układu ubikwityna–proteasom, nagromadzenia w neuronach jonów metali, α synukleiny, parkiny oraz nagromadzenia ciałek Lewy’ego1. Widoczna jest manifestacja kliniczna.
Wpływ C. Kumulowanie następstw powstających równolegle licznych zmian odpowiada za progresję choroby i ubytek sprawności, często pozostający w związku z chorobą małych naczyń (SVD). Klinicznie jest to faza zależności opiekuńczej
1 Masato A., Plotegher N., Daniela Boassa D i wsp.: Impaired dopamine metabolism in Parkinson’s disease pathogenesis. Molecular Neurodegeneration, 2019; 14: 35; https://doi.org/10.1186/s13024-019-0332-6.
Poza regułą stosowania uznanych i zewaluowanych testów, kiedy pojawiają się presja czasu i ograniczenia w organizacji pracy zespołowej, bo część pracowników już poszła do domu, a za drzwiami gabinetu lub na liście do konsultacji jest nadal spora grupa pacjentów, przydatna jest znajomość wersji testów do szybkiego wykonania. Dlatego niejednokrotnie geriatra sięga po przesiewowe metody oceny, dające mu porównanie i wgląd w obecny stan pacjenta. Nawet pod presją czasu nie powinniśmy tracić celu w badaniu, jakim jest wskazanie osób, u których wprowadzenie leczenia prokognitywnego i/lub podnoszącego tonus dopaminergiczny poprawi ich stan funkcjonalny. Podobnie nie wolno pominąć włączenia terapii antydepresyjnej, gdy wymaga tego starszy pacjent, u którego stwierdzamy pierwszy raz depresję lub jej nawrót.
Nie bez znaczenia jest kolejność wykorzystania narzędzi testowych, ponieważ sprawniejsi chorzy uczą się ich elementów i potrafią przypomnieć sobie schematy zadań pamięciowych „jabłko, telefon, rzeka” nawet przy następnej wizycie po trzech miesiącach. Jeżeli chcemy użyć testu Mini-Cog, to osłabiamy efekt testu MoCA (w obu jest rysownie zegara). Jeżeli jako pierwszy do oceny sprawności poznawczej zostanie użyty test AMTS, można w następnych etapach wykonać MMSE lub test MoCA.
Test fluencji słownej (TFS) polega na wymienieniu w ciągu 60 sekund jak największej liczby słów zgodnie z określonym kryterium w zaproponowanej kategorii pojęć (przedmioty ostre, sprzęt wojskowy, zwierzęta czworonożne) lub w kategorii literowej, w której prosimy o podanie słów na daną literę. Norma to wymienienie większej niż 16 liczby wyrazów z kategorii pojęć lub więcej niż 12 z kategorii literowej (33).
Test wymieniania miesięcy wstecz (MW) jest też prostym i szybkim testem potwierdzającym sprawność poznawczą i nieobecność majaczenia. Zdrowa osoba wykonuje go w czasie do 30 sekund, wymieniając miesiące od grudnia do stycznia. W wyniku zapisujemy czas wykonania i liczbę prawidłowo wymienionych miesięcy. Zapis 12/25 świadczy o prawidłowym wymienieniu 12 miesięcy w 25 sekund, a 7/90 – o prawidłowym wymienieniu 7 miesięcy w czasie 90 sekund (34). Jest on składową częścią testu 4AT.
W określaniu sprawności funkcjonalnej niedoceniona pozostaje ocena motoryki, a fałszywa opinia, że im starszy człowiek, tym ma prawo być mniej ruchliwy, usprawiedliwia jedynie diagnostyczny i terapeutyczny nihilizm. Pomiar siły uścisku dłoni dominującej, choć użyteczny, nie wszedł do praktyki w gabinetach lekarskich jako element badań konsultacyjnych. Pewnie wynika to z małej dostępności i wagi dynamometrów oraz przydatności kontrolnych pomiarów.
9.3. Zasady prowadzenia badania geriatrycznego
Poniżej przedstawiono pięć testów sprawdzonych i z powodzeniem używanych przez autora w ocenie motoryki starszych pacjentów: TUG, test pięciokrotnego wstawania (T5KW), test sprawności ruchowej ręki (TSRR), test równowagi i test z L-Dopą.
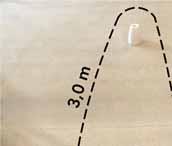
U osób starszych do oceny motoryki najczęściej wykonywany jest test „Wstań i idź” (TUG), który pozwala też przy małej modyfikacji (1,5–2 m dystansu na rozpoczęcie chodu przed linią rozpoczęcia pomiaru) na pomiar prędkości chodu. Pacjent na dany sygnał (po wcześniejszej próbie) wstaje sam z krzesła o wysokości siedziska około 46 cm, idzie w linii prostej, zawraca, obchodząc znacznik na podłodze ustawiony w odległości 3 m od przednich nóg krzesła, powraca do krzesła i siada na nim (35).
Test TUG zaprezentowano na rycinie 9.9.
Rycina 9.9.
Test „Wstań i idź”.
Norma graniczna wykonania testu, który prognozuje ryzyko upadków dla osób z upośledzoną sprawnością poznawczą, to czas powyżej 14 sekund, dla osób sprawnych – poniżej 12 sekund, a wykorzystana w kryteriach zespołu kruchości norma prędkości chodu dla osób chorych to wartość poniżej 0,8 m/sekundę.
17. https://www.mp.pl/covid19/zalecenia/248659, zalecenia-diagnostyki-i-terapii-zakazen-sars-cov2-polskiego-towarzystwa-epidemiologow-i-lekarzy-chorob-zakaznych,1 (dostęp: 12.01.2021 r.)
18. Chen P., Nirula A., Heller B. i wsp.: SARS-CoV-2 Neutralizing Antibody LY-CoV555 in Outpatients with Covid-19. N. Engl. J. Med., 2020; 1–9. doi: 10.1056/ NEJMoa2029849.
10.2. Upadek u starszej osoby z powodu bloku przedsionkowo-komorowego III stopnia indukowanego riwastygminą
Elżbieta Pyrkosz-Cifonelli
Na początku 2018 r. przyjęto na oddział geriatryczny 87-letnią pacjentkę przywiezioną po upadku związanym przyczynowo z przemijającą utratą świadomości. Chora nie zgłaszała występowania innych objawów zwiastunowych typu zawroty głowy czy uczucie kołatania serca. Nie było też świadków upadku.
Na podstawie dostępnej dokumentacji medycznej (wypisowe karty informacyjne ze szpitali, opisy konsultacji specjalistycznych, zapisy EKG, wyniki aktualnych badań dodatkowych) okazało się, że od 4 lat pacjentka jest leczona inhibitorem acetylocholinesterazy z powodu choroby Alzheimera. Początkowo przyjmowała donepezil, ale z powodu skutków ubocznych ze strony przewodu pokarmowego, w październiku 2013 r. zmieniono terapię i zaczęto stosować riwastygminę w plastrach w dawce 4,6 mg/dobę. Częstość akcji serca pacjentki przed rozpoczęciem leczenia wynosiła 93 uderzenia na minutę, a jej EKG było prawidłowe.
Dawka riwastygminy po 3 miesiącach została zwiększona do 9,5 mg/dobę. W tym czasie oceniono funkcje poznawcze pacjentki według skali MoCA (Montreal Cognitive Assessment Score) − wynik 22/30. Od momentu rozpoczęcia leczenia riwastygminą wynik testu MoCA się nie pogarszał. W subiektywnej ocenie zdolności poznawcze pozostawały niezmiennie dobre i dlatego życzeniem chorej było kontynuowanie wcześniejszej terapii. Nigdy wcześniej nie leczyła się neurologicznie lub z powodu chorób układu krążenia. Według dostępnej dokumentacji, w 2017 r. (w poprzednim roku od upadku) pacjentka miała upadek, który spowodował uraz biodra lewego bez złamania nasady bliższej kości udowej. W owym czasie jej zapis EKG wskazywał na miarową akcję serca (64 uderzenia na minutę) i nieco przedłużony czas PR, który wynosił 210 ms, poza tym bez zmian. Kobieta mieszkała we własnym domu z mężem, była niezależna i mogła wykonywać samodzielnie wszystkie czynności dnia codziennego według skali ADL.
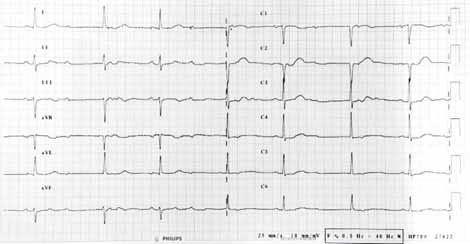
Rycina 10.1.
EKG pacjentki podczas przyjęcia do szpitala, przed podjęciem optymalizacji stanu przed operacją naprawczą złamania biodra. Bradykardia 40/min z blokiem przedsionkowo-komorowym zaawansowanym Mobitza II / III stopnia. Przesuw 25 mm/s.
Podczas opisywanego aktualnego przyjęcia do szpitala ciśnienie chorej wynosiło 220/45 mm Hg, częstość akcji serca – 47 uderzeń na minutę. Zapis EKG wskazywał na okresowo występującą bradykardię z blokiem przedsionkowo-komorowym zaawansowanym Mobitza II / III stopnia (ryc. 10.1).
W trakcie badania tony serca pacjentki były prawidłowe. Neurologicznie bez zmian. Jej kończyna dolna lewa była skrócona i zrotowana na zewnątrz. Bez obwodowych ubytków neurologicznych. Zdjęcie RTG miednicy mniejszej i kości udowej wskazało na wewnątrztorebkowe złamanie szyjki kości udowej lewostronne. Poza riwastygminą pacjentka nie przyjmowała innych leków, które mogłyby spowodować chronotropowo ujemny bądź dromotropowo ujemny efekt na układ przewodzący serca. Z wyjątkiem nieznacznie podwyższonych markerów zapalenia z powodu złamania inne wyniki krwi były prawidłowe.
Badanie echokardiograficzne nie wykazało nieprawidłowości w strukturze serca, frakcja wyrzutowa lewej komory była prawidłowa.