2.2.2.
2.4. Badania mikroskopowe – histologiczne, immunohistochemiczne, genetyczne
2.4.2.
2.5. Diagnostyka fotodynamiczna i zarys terapii fotodynamicznej
Alina Morawiec-Sztandera
2.5.1. Autofluorescencja
2.5.2. Fluorescencja indukowana (wywołana) 61
2.6. Spektroskopia i obrazowanie Ramana – Halina Abramczyk .............................. 72
2.6.1. Wprowadzenie 72
2.6.2. Rozpraszanie Ramana 74
2.6.3. Przygotowanie próbek do analizy z wykorzystaniem spektroskopii i obrazowania Ramana 77
2.6.4. Obrazowanie i spektroskopia Ramana w analizie próbek biologicznych 79
2.7. Obrazowanie molekularne guzów głowy i szyi – Dariusz Kaczmarczyk 89
2.7.1. Scyntygrafia .....................................................................................
2.7.2. Pozytonowa tomografia emisyjna
2.7.3. Biopsja węzła wartowniczego w nowotworach głowy i szyi
3. Leczenie nowotworów głowy i szyi
3.1. Wprowadzenie – Alina Morawiec-Sztandera
3.2. Leczenie chirurgiczne wybranych nowotworów głowy i szyi ............................
3.2.1. Operacje chirurgiczne nowotworów nosa i zatok przynosowych – Dariusz Kaczmarczyk
3.2.2. Operacje chirurgiczne guzów jamy ustnej i gardła – Dariusz Kaczmarczyk ..... 110
3.2.3. Operacje chirurgiczne nowotworów krtani – Dariusz Kaczmarczyk 126
3.2.4. Operacje chirurgiczne gruczołów ślinowych – Alina Morawiec-Sztandera 145
3.2.5. Operacje chirurgiczne nowotworów ucha – Alina Morawiec-Sztandera .... 165
3.2.6. Chirurgia laserowa nowotworów głowy i szyi – Alina Morawiec-Sztandera 171
3.2.7. Operacje chirurgiczne układu chłonnego szyi – Alina Morawiec-Sztandera 188
3.2.8. Operacje rekonstrukcyjne w nowotworach głowy i szyi w zarysie – Alina Morawiec-Sztandera 202
3.3. Nowoczesne podejście do radioterapii nowotworów głowy i szyi – Jacek Fijuth 220
3.3.1. Wprowadzenie 220
3.3.2. Radioterapia frakcjonowana konwencjonalnie i niekonwencjonalnie ... 221
3.3.3. Techniki radioterapii 222
3.3.4. Taktyka leczenia 224
3.3.5. Rola chemioterapii indukcyjnej i radiochemioterapii 224
3.3.6. Odczyn wczesny i późny w radioterapii .............................................. 226
3.4. Zastosowanie chemioterapii w nowotworach narządów głowy i szyi – Piotr Potemski
3.4.1. Wstęp ..............................................................................................
3.4.2. Leczenie radykalne
3.4.3. Leczenie paliatywne
4. Rehabilitacja w laryngologii
4.1. Główne zasady rehabilitacji onkologicznej – Alina Morawiec-Sztandera 239
4.1.1. Rola fizjoterapeuty w terapii onkologicznej
4.1.2. Rola fizjoterapeuty w medycynie paliatywnej
4.2. Rehabilitacja głosu u chorych po laryngektomii – Joanna Zimmer-Nowicka 248
4.2.1. Laryngektomia całkowita i jej następstwa 248
4.2.2. Przygotowanie pacjenta do rehabilitacji głosu .................................... 249
4.2.3. Rehabilitacja głosu klasyczna – opanowanie mowy przełykowej 249
4.2.4. Rehabilitacja głosu z wytworzeniem mowy przetokowo-protezowej 251
4.2.5. Przeciwwskazania do implantacji protezy głosowej ............................. 252
4.2.6. Etapy rehabilitacji foniatrycznej u pacjentów po laryngektomii całkowitej 253
4.2.7. Sposoby oceny skuteczności rehabilitacji głosu 254
4.2.8. Przyczyny wymian protez głosowych .................................................. 255
4.2.9. Rehabilitacja głosu z zastosowaniem laryngofonu 257
4.3. Rehabilitacja odczuć węchowo-smakowych u chorych po całkowitym usunięciu krtani – Alina Morawiec-Sztandera .................................................... 260
4.4. Fizjoterapia chorych po leczeniu nowotworów głowy i szyi – Dariusz Kaczmarczyk, Anna Świątkowska 266
4.4.1. Fizjoterapia pacjentów z zespołem „zamrożonego barku” 266
4.4.2. Fizjoterapia blizn po leczeniu nowotworów głowy i szyi ...................... 267
4.4.3. Fizjoterapia ograniczeń ruchomości odcinka szyjnego kręgosłupa, obręczy barkowej i stawu ramiennego 269
4.4.4. Fizjoterapia chorych z obrzękiem limfatycznym 271
4.4.5. Rehabilitacja po całkowitym usunięciu krtani .................................... 271
4.4.6. Fizjoterapia w zaburzeniach czynności nerwu twarzowego 276
4.5. Kinesiology taping u chorych po leczeniu chirurgicznym nowotworów głowy i szyi – Anna Świątkowska ..................................................................... 282 Skorowidz 291
2.7.
obrazowanie molekularne guzów głowy i szyi
Dariusz Kaczmarczyk
Medycyna nuklearna zajmuje się diagnostyką oraz terapią z zastosowaniem radioizotopów – pierwiastków promieniotwórczych, które w połączeniu ze związkami chemicznymi mają powinowactwo do określonych struktur organizmu żywego, takich jak błona komórkowa, cytoplazma, organelle komórkowe czy białka, dzięki czemu możliwa jest ocena stanu czynnościowego komórki, a także fazy cyklu komórkowego. Obrazowanie molekularne guzów głowy i szyi obejmuje scyntygrafię, pozytonową tomografię emisyjną (positron emission tomography, PET) i pozytonową tomografię emisyjną połączoną z tomografią komputerową (PET/TK) oraz biopsję węzła wartowniczego (sentinel lymph node biopsy, SLNB).
2.7.1.
Scyntygrafia
Scyntygrafia jest metodą obrazowania czynnościowego narządów z użyciem niewielkich dawek radioizotopów, które mogą być podane drogą dożylną lub doustną. Najczęściej używane radioizotopy to 99Tc, 131I, 201Tl, 67Ga. Radioizotopy są zwykle związane z odpowiednimi związkami chemicznymi, co ułatwia ich wychwyt przez komórki i tkanki. W guzach głowy i szyi najszersze zastosowanie ma scyntygrafia tarczycy z użyciem 131I.
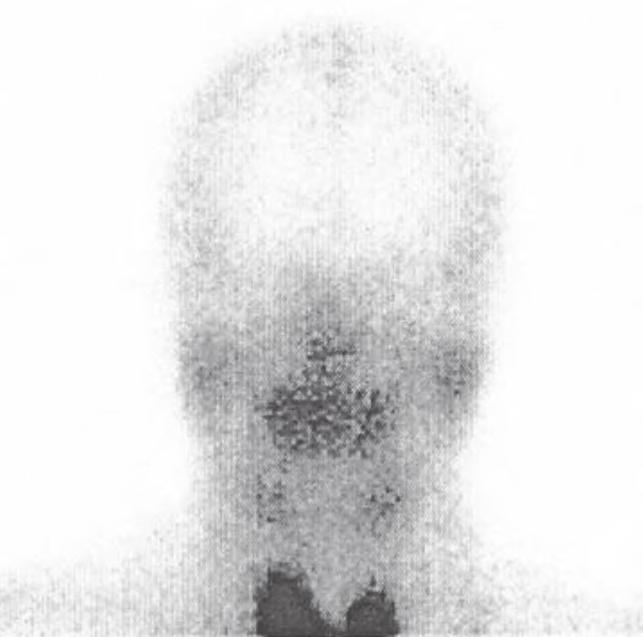
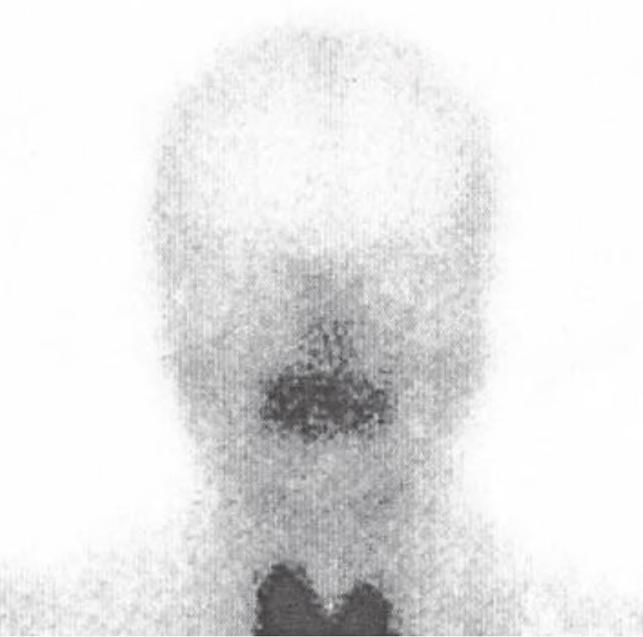
Scyntygrafia ślinianek wykonywana jest z użyciem 99mTc, a wskazaniami do jej wykonania są guzy ślinianek, zaburzenia wydzielania śliny (zwłaszcza jednostronne) oraz monitorowanie funkcji ślinianek po uprzedniej radioterapii (ryc. 2.43).
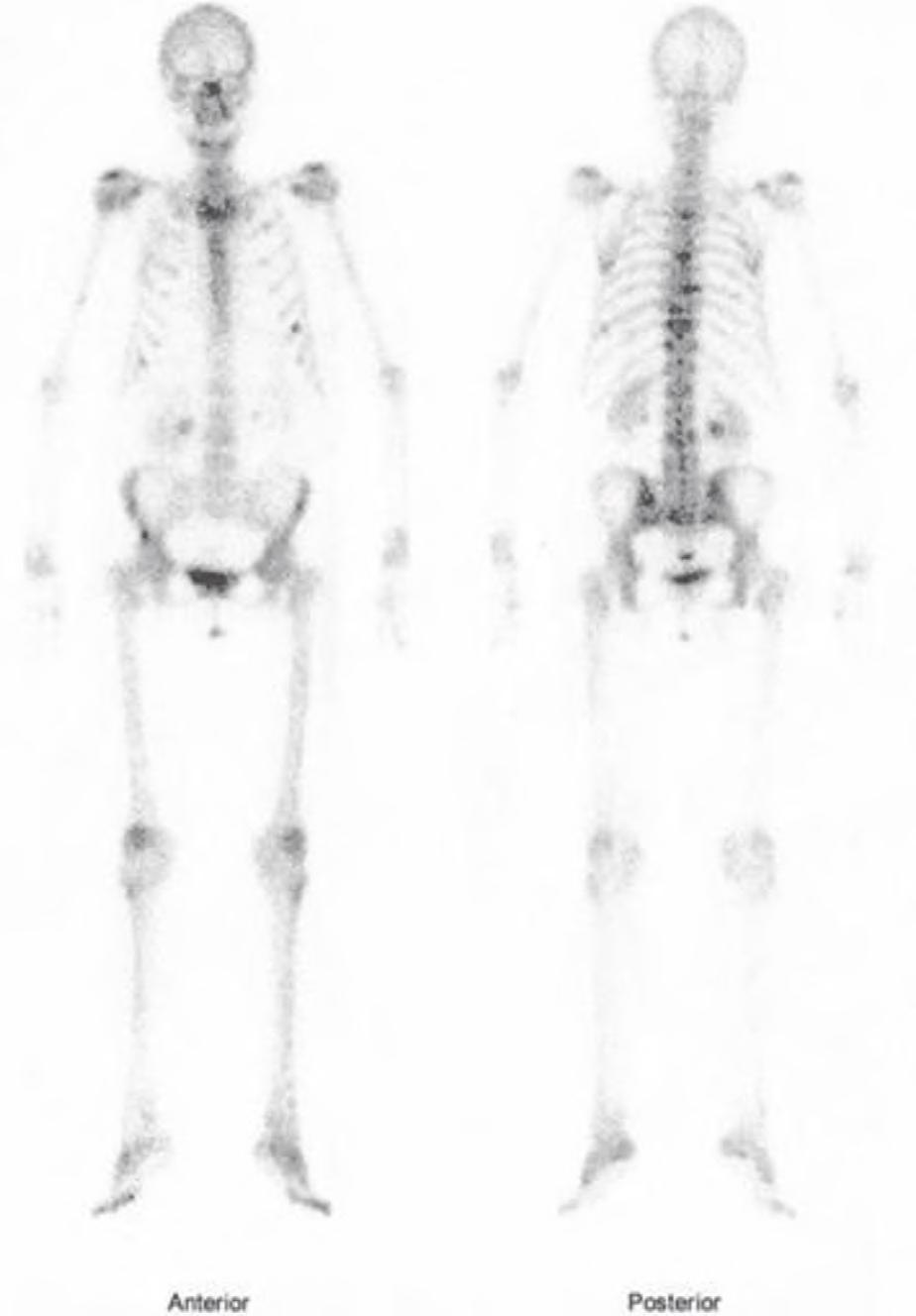
Scyntygrafia kości wykonywana jest z użyciem metylenodifosfonianu technetu (99mTc-MDP) (ryc. 2.44), aby ocenić pierwotne i wtórne zmiany w układzie kostnym, progresję choroby nowotworowej, np. w przypadku wzrostu markerów nowotworowych, oraz by ocenić wyniki leczenia.
2.7. Obrazowanie molekularne guzów głowy i szyi
Czynnościowa scyntygrafia prawidłowych ślinianek: A – w spoczynku (widoczny wychwyt w śliniankach); B – po podaniu soku z cytryny (brak wychwytu w śliniankach).
Scyntygrafia kości – podejrzenie rozsiewu nowotworu do kości kręgosłupa i żeber.
RYCINA
RYCINA
2.7.2.
Pozytonowa tomografia emisyjna
Pozytonowa tomografia emisyjna (PET) jest diagnostycznym badaniem czynnościowym z wykorzystaniem radionuklidów emitujących promieniowanie β+ , czyli elektrony o dodatnim ładunku elektrycznym (pozytony), które po zderzeniu z elektronami emitują promieniowanie γ. W badaniu PET wykorzystywane są radioizotopy o krótkim czasie połowicznego rozpadu (od kilkunastu minut do kilku godzin). Zastosowanie mają takie izotopy, jak: 11C, 15O, 13N, 18F, 82Rb, 68Ga, 64Cu, 124I, 86Y. Najszersze zastosowanie znalazł izotop 18F, którego czas połowicznego rozpadu wynosi 108 minut.
Po chemicznym połączeniu radioizotopu jest on podawany choremu, najczęściej dożylnie, a następnie w tomografie pozytonowym rejestrowany jest obraz promieniowania uzyskanego w wyniku rozpadu radioizotopu, który gromadzony jest w strukturach patologicznych (guz, tkanki zmienione zapalnie). Obraz poddawany jest analizie komputerowej, dzięki czemu otrzymuje się rekonstrukcję przestrzenną.
Obecnie stosowane aparaty PET są urządzeniami hybrydowymi, z których otrzymujemy obraz PET w połączeniu z obrazem z tomografii komputerowej (PET/TK). Tomografy komputerowe scalone z detektorami PET mają różną rozdzielczość (16–128), dzięki czemu obrazy mogą być automatycznie nakładane na siebie, a wyższa rozdzielczość sprawia, że dawka zastosowanego radionuklidu może być mniejsza od standardowej (badanie niskodawkowe). Połączenie obrazów PET oraz TK pozwala na precyzyjną lokalizację zmiany; rozdzielczość obecnie stosowanych aparatów oceniana jest na 3 mm.
W onkologii, w zależności od obrazowanego procesu, zastosowanie mają różne radiofarmaceutyki. Najczęściej stosowana jest fluorodeoksyglukoza (18F-FDG), za jej pomocą obrazuje się procesy glikolizy oraz metabolizmu glukozy (tab. 2.6).
TabEL a 2.6. Wybrane radiofarmaceutyki, stosowane w diagnostyce onkologicznej, i obrazowane przez nie procesy
Radiofarmaceutyk
Obrazowany proces
18 F-FDG nasilenie metabolizmu glukozy
18 F-anneksyna V apoptoza komórek
11 C-octan synteza lipidów
11 C-tymidyna
18 F-fluorotymidyna
11 C-metionina
synteza DNA i białek, proliferacja komórek
18 F-mizonidazol hipoksja guza
2.7. Obrazowanie molekularne guzów głowy i szyi
Wskazaniem do badania PET i PET/TK jest poszukiwanie ogniska pierwotnego choroby w przypadkach CUP-syndrome, ocena stopnia zaawansowania choroby nowotworowej (ocena TNM), ocena odpowiedzi na leczenie oraz ocena wznowy po leczeniu. Badania te przydatne są również w planowaniu radioterapii (zwłaszcza u pacjentów poddanych wcześniej leczeniu operacyjnemu).
2.7.3.
Biopsja węzła wartowniczego w nowotworach głowy i szyi
Węzeł wartowniczy jest pierwszym węzłem na drodze spływu chłonki z ogniska pierwotnego. Idea biopsji węzła wartowniczego zaproponowana przez Cabañasa w 1977 roku nie zmieniła się pomimo wprowadzenia nowych technik diagnostycznych oraz operacyjnych. Cabañas jako pierwszy zastosował technikę znakowania węzła wartowniczego w raku prącia przy użyciu barwnika. W 1991 roku Morton i wsp. zaproponowali zastosowanie limfoscyntygrafii przedoperacyjnej. Biopsja węzła wartowniczego znajduje się w standardowej procedurze czerniaka skóry i raka sutka we wczesnych stadiach zaawansowania.
W nowotworach głowy i szyi, zwłaszcza w rakach płaskonabłonkowych, biopsja węzła wartowniczego nie jest uznawana za procedurę obowiązującą. Wynika to głównie ze złożonego układu węzłów i naczyń chłonnych szyi, rygorystycznych kryteriów zastosowania tej metody oraz trudności w zaopatrzeniu w instrumentarium niezbędne do jej wykonania.
Kryteria kwalifikacji do biopsji węzła wartowniczego chorych z nowotworami w obrębie głowy i szyi są precyzyjnie wyznaczone. Zaawansowanie guza pierwotnego nie może być większe niż T2. Niektórzy autorzy uważają, że jedynie zaawansowanie T in situ i T1 spełnia kryteria kwalifikacji, gdyż w przypadku zaawansowania T2 ryzyko mikroprzerzutów sięga 30%, zwłaszcza dla nowotworów dna jamy ustnej i języka.
Kwalifikacja chorych pod względem cechy N nie budzi wątpliwości. Do biopsji węzła wartowniczego można zakwalifikować jedynie chorych, u których węzły chłonne nie są klinicznie powiększone (cN0). Czułość badania palpacyjnego oceniana jest na 64% przypadków. Cecha N0 powinna zostać potwierdzona w badaniach obrazowych, aczkolwiek czułość badania USG wynosi 72%, a tomografii komputerowej 85% w porównaniu z późniejszym badaniem śródoperacyjnym.
Po zakwalifikowaniu chorych do procedury biopsji węzła wartowniczego na jedną dobę przed planowanym zabiegiem operacyjnym wykonywana jest limfoscyntygrafia. Guz pierwotny ostrzykuje się podśluzówkowo w kilku miejscach (najczęściej czterech) roztworem nanokoloidu. Powszechnie używane preparaty