Diseño&DesarrollodeDispositivosMédicos
SistemadeGestióndeCalidadenelProcesodeDiseñoyDesarrollodeun
DispositivoMédico




SistemadeGestióndeCalidadenelProcesodeDiseñoyDesarrollodeun




Módulo1

RegulaciónSanitaria

SolicituddeRegistro Sanitario

Módulo2

ModelosdeInnovación Tecnológica

SistemadeGestiónde CalidadparaDM.


IdentificacióndeNecesidades Matrizrequerimientos EstrategiaRegulatoria


GestióndeRiesgospara DM

VerificaciónPre-Clínica+ GestióndeRiesgos
Módulo6

ValidaciónClínica+ GestióndeRiesgos

MatrizdeRequerimientos Esenciales,Matrizde Trazabilidad,ProcesoD&D, EstructuraDocumental


PlandeGestióndeRiesgos, matrizderiesgos,

Protocolos-Reportesde laboratorioeinvestigación pre-clínica.

ExpedienteProtocolo Investigación Expedienteregistro




Conjuntodeelementosinterrelacionadosoqueinteractúan

paraquelaorganización/Establecimientodirijaycontrolelas
actividadesencaminadasaqueelconjuntodecaracterísticas
inherentesdesuproducto/serviciocumplaconlosrequisitos
Fuente:ColegiodeIngenierosBiomédicosdeMéxico,A.C.







 ecosistema
ecosistema
RLGS NOM012
AlcancedelSistemadeGestióndeCalidad
ISO14971–Gestiónde Riesgos
ISO62366–Usabilidad
ISO16142–Selección deEstándares

IEC60601
ISO62304 *Otrasaplicables NOM012
ISO14155 NOM241

LGS,RIS,FEUM
Suplementodeestablecimientos/SuplementodeDispositivosMédicos




•Qué
•Cómo
•Quién
•Cuándo
•Dónde
Manuales
Procedimientos/PNOs
Protocolos
Especificaciones
Políticas
Entreotros

•Evidencia

Informes
Reportes
Bitácoras
Pruebasdelaboratorio
Estudios
Entreotros


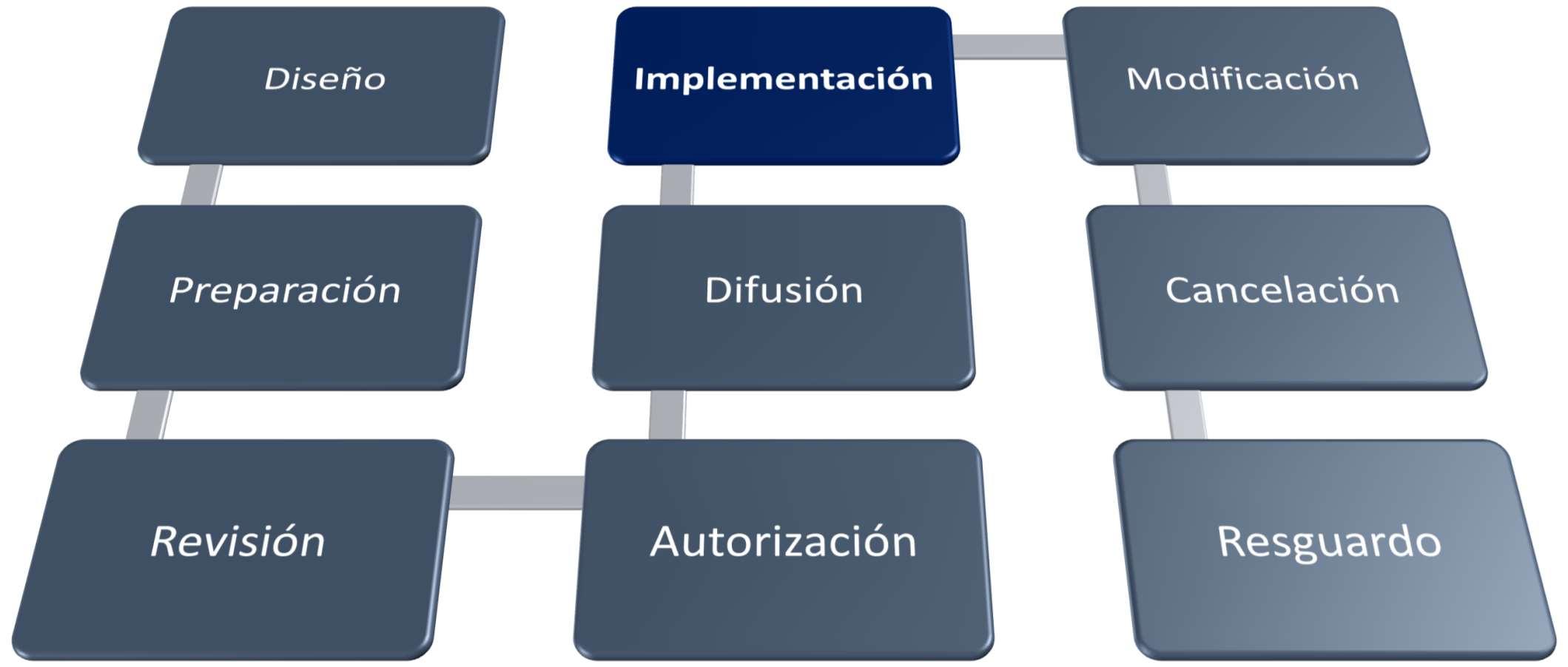
6.2DocumentaciónNOM-241-SSA-2021



6.2DocumentaciónNOM-241-SSA-2021


•Revisaloestablecidoen elnumeral6.2 Documentacióndela NOM-241-SSA-2021

•Enequipo,diseñatu procedimiento(s)parael controldocumental


Losprocedimientosdediseñoydesarrollo.
(8.1.1/7.3.1)

Procedimientosparalatransferencia
(8.8.1/7.3.8)
ProcedimientosparaControlarlos
Cambios(8.9.1/7.3.9)
Losdocumentosrequeridosenla planificacióndeldiseñoydesarrollo(8.2.2/7.3.2)
LosPlanesdeVerificación(8.6.2/7.3.6)

ISO13485/NOM241
LosPlanesdeValidación(8.7.2/7.3.7)


Entradasdediseñoydesarrollo(8.3/7.3.3)

ISO13485/NOM241
Productos/Salidasdediseñoydesarrollo(8.4.3/7.3.4)
Resultadosdelasrevisionesycualquieracciónnecesaria eincluirlaidentificacióndeldiseñobajorevisión, participantesinvolucradosyfechadelarevisión(8.5.3/7.3.5)
Resultadosylasconclusionesdelaverificacióny lasaccionesnecesarias(8.6.4/7.3.6)
Elfundamentodelaeleccióndelproductoutilizadoparala validación(8.7.3/7.3.7)
Resultadosylasconclusionesdelavalidacióny lasaccionesnecesarias(8.7.8/7.3.7)
Resultadosyconclusionesdelatransferencia(8.8.2/7.3.8)
Cambios,surevisiónycualquieracciónnecesaria(8.9.5/7.3.9)


IdentificalaspartesinteresadasqueserelacionancontuSGC
IdentificalosprocesosqueintegrantuSGC
DefineelalcancedetuSGC



ISO9001:2015Sistemasdegestióndelacalidad—Requisitos,




Investigación




Requisitos
ISO13485/NOM241
Entradas delD&D

•Requisitode sudesempeño/ funcionales,de funcionamiento, funcionalidad,deaptitud deusoyseguridad,de acuerdoconlafinalidadde uso/finalidadprevista
•Requisitosydisposiciones aplicables,requisitos reglamentariosynormas aplicables
•Resultado(s)aplicable(s)de laGestióndelRiesgo
•Informaciónderivadade diseñossimilaresanteriores
•Otrosrequisitosesenciales paraeldiseñoydesarrollo delproductoylosprocesos
Salidas/ Productos delD&D

•Cumplirlosrequisitosde loselementosdeentrada paraeldiseñoydesarrollo
•Proporcionarlainformación adecuada/apropiadapara lacompra,produccióny prestacióndelservicio
•Contenerohacer referenciaaoconsultar loscriteriosdeaceptación delproducto
•Especificarlas característicasdel productoqueson esencialesparasuuso seguroyadecuado/ utilizaciónseguray correcta

Proyecto
Etapasde Diseñoy Desarrollo

Laintenciónobjetivaconrespectoalusodeunproducto,proceso oserviciocomosereflejaenlasespecificaciones,instruccionese informaciónproporcionadaporelfabricante.
ISO13485=>Finalidadprevista
NOM241=>Finalidaddeuso
Fuente:Numeral3.18,IMDRFGRRPWG/N47FINAL:2018)













Cambios Expediente
NOM-241-SSA1-2021Disponibleen:https://dof.gob.mx/nota_detalle.php?codigo=5638793&fecha=20/12/2021/Accesosoctubre2022


AlcancedelSGC
Partesinteresadas
Procesos

Documentos DeterminatuprocesodeDiseñoyDesarrollo


