




1. Materia y sus Clasificaciones
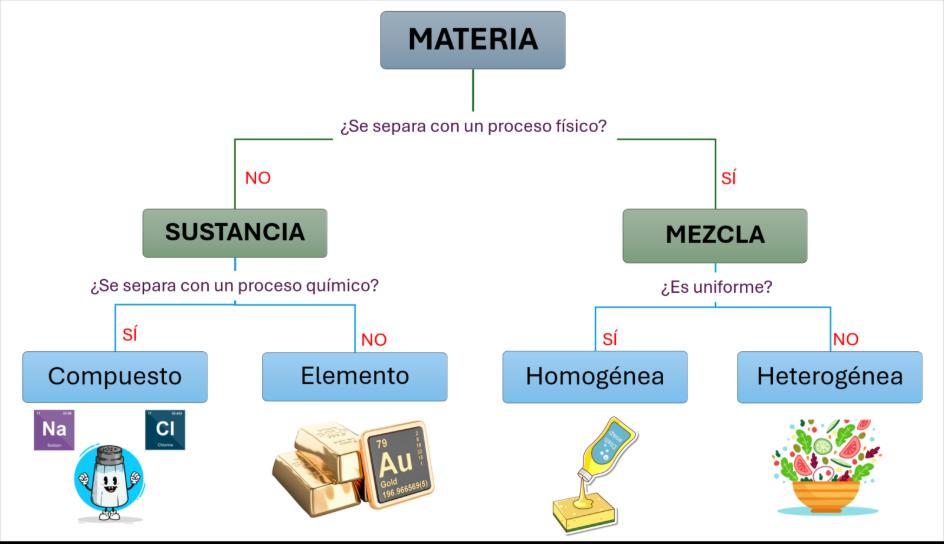
La materia es todo aquello que tiene masa y ocupa un lugar en el espacio. Se presentaendiferentesformasypuedeclasificarseensustanciaspurasymezclas.
• Elementos: Son sustancias formadas por un solo tipo de átomo. No pueden descomponerse en sustancias más simples por métodos químicos ordinarios.
Ejemplo: Oxígeno(O₂),hierro(Fe),oro(Au).
• Compuestos: Son sustancias formadas por dos o más elementos químicamente combinadosenproporcionesfijas.Sepuedendescomponerensustanciasmás simples mediante reacciones químicas.
Ejemplo: Agua(H₂O),clorurodesodio(NaCl),dióxidodecarbono(CO₂).
Lasmezclassoncombinacionesfísicasdedosomássustancias,queconservansus propiedadesindividualesypuedensepararsepormétodosfísicos.
• Mezclas homogéneas: Tienen una composición uniforme y no se distinguen sus componentes a simple vista.
Ejemplo: Aire,aguaconazúcardisuelta,solucionessalinas.
• Mezclas heterogéneas: Suscomponentessondistinguiblesynoestándistribuidos uniformemente.
Ejemplo: Ensalada,aguaconarena,aceiteyagua.
2. Diferencias clave entre Elementos, Compuestos y Mezclas
CARACTERÍSTICA ELEMENTO COMPUESTO MEZCLA
COMPOSICIÓN
Unsolotipode átomo
Dos o más elementos combinados
Dos o más sustancias físicas
SEPARACIÓN No se puede separar Se puede separar químicamente Se puede separar físicamente
PROPIEDADES
Propiedades únicas
Propiedades diferentes a sus elementos
Propiedades de los componentes
EJEMPLO Oxígeno(O₂) Agua(H₂O) Aguaconsal
3. Introducción a la Nomenclatura Química Inorgánica
Lanomenclaturaquímicaeselsistemaqueusamosparanombrarloscompuestosquímicos demaneraclarayuniversal.
Reglas básicas
• Se usan prefijos numéricos para indicar la cantidad de átomos (mono-,di-,tri-, tetra-, etc.).
Ejemplo: CO=monóxidodecarbono,CO₂ =dióxidodecarbono.
• El nombre del elemento más electronegativo sueleiralfinalyterminaen“-uro”o “ -óxido” si es oxígeno.
Ejemplo: NaClsenombraclorurodesodio.
• Para los números de oxidación,seusannúmerosromanosentreparéntesispara indicar la carga del elemento central cuando puede variar.
Ejemplo: FeCl₂ esclorurodehierro(II),FeCl₃ esclorurodehierro(III).
Paramásejemplos,serecomiendarevisarelsiguientedocumento:
https://iupac.org/wp-content/uploads/2016/07/20151106GuiaBreveNQIEspayol.pdf
