
11 minute read
Effektive Aufnahme von CBD und THC
Die Rolle der Bioverfügbarkeit und neuer Technologien
Die therapeutischen Wirkungen von Cannabinoiden erhalten stetig mehr Aufmerksamkeit, doch nur ein Bruchteil der eingenommenen Menge dieser Wirkstoffe erreicht den Ort, an dem sie ihre Wirkung im Körper entfalten können. Der vorliegende Artikel vertieft das Verständnis der Bioverfügbarkeit von CBD, THC und anderen Cannabinoiden, beleuchtet innovative Formulierungstechniken zur Optimierung ihrer Aufnahme und gibt einen Einblick in den aktuellen Stand der Forschung und klinischen Studien. Von Sung Min Pyo
Die wachsende Faszination für Cannabinoide, insbesondere für Cannabidiol (CBD) und Tetrahydrocannabinol (THC), ist unbestreitbar. Beide Verbindungen, die hauptsächlich in der Cannabispflanze vorkommen, sind für ihre therapeutischen Wirkungen bekannt und stoßen daher in der Pharma- und Nahrungsergänzungsmittelindustrie auf besonders großes Interesse. Ein entscheidender Aspekt bleibt jedoch vielen Verbrauchern verborgen: Von der eingenommenen Menge erreichen nur etwa 6-10 % tatsächlich den Ort, an dem sie ihre Wirkung im Körper entfalten können. Diese Diskrepanz zwischen eingenommener und aufgenommener Menge wird durch die sogenannte “Bioverfügbarkeit” erklärt.
Von Kapsel zu Kreislauf: Die Odysee eines Wirkstoffes
In der Welt der Pharmakologie und der Gesundheitswissenschaften nimmt die Bioverfügbarkeit eine Schlüsselstellung ein. Ein Großteil der Bevölkerung nimmt in regelmäßigen Abständen Medikamente oder Nahrungsergänzungsmittel ein, ohne sich über die komplexe Reise dieser Wirkstoffe in unserem Körper bewusst zu sein. Im Folgenden wird beschrieben, wie unser Körper die Aufnahme von Wirkstoffen steuert und warum nicht alle Substanzen zu 100 % absorbiert werden.
Die Reise eines Wirkstoffs beginnt mit dem Schlucken einer Kapsel oder Tablette, die durch die Speiseröhre in den Magen gelangt. Dort setzt sich der Wirkstoff aus der Formulierung frei und gelangt in den Dünndarm, wo er durch die Darmwand in den Blutstrom gelangt. Das mit dem Wirkstoff angereicherte Blut wird anschließend über die Pfortader zur Leber transportiert, von wo aus es in den allgemeinen Kreislauf abgegeben wird. Auf diese Weise erreicht der Wirkstoff schließlich seinen Bestimmungsort im Körper. Doch an welcher Stelle gehen auf dieser Reise Teile des Wirkstoffs verloren? Abbildung 1 veranschaulicht die drei Hauptursachen für Verluste auf dem Weg des Wirkstoffes von der Kapsel bis zum Wirkort.
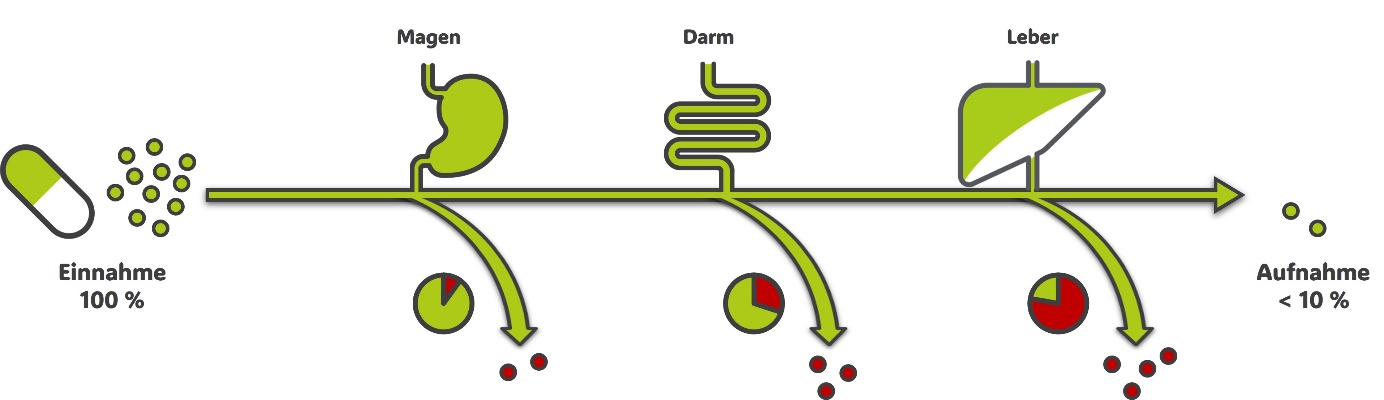
1. Löslichkeit des Wirkstoffes:
Bereits beim ersten Schritt können Verluste entstehen, wenn ein Wirkstoff nicht vollständig aus seiner Formulierung freigesetzt wird. Dies trifft besonders auf schlecht wasserlösliche Wirkstoffe zu, da sie nur bedingt in die Flüssigkeiten des Verdauungstraktes übergehen. Die Folge ist, dass nicht die gesamte Menge des Wirkstoffs für die Aufnahme aus dem Darm in den Blutkreislauf zur Verfügung steht.
2. Wenn Größe eine Rolle spielt:
Wirkstoffe mit einer hohen Molekülmasse können oft nur schwer die Darmwand passieren, da ihre Größe das Eindringen erschwert. Dadurch wird ihre Überführung in den Blutkreislauf limitiert. Für lebenswichtige Stoffe, die eigentlich zu groß für die Aufnahme wären, verfügt der Körper durch evolutionäre Anpassungen über spezielle Transporter in der Darmwand, die es ermöglichen, dass die Aufnahme trotz der Größe effektiv erfolgt, wie zum Beispiel bei Aminosäuren und Peptiden.
3. Die Leber als Kontrollzentrum:
Nachdem ein Wirkstoff die Darmwand passiert hat und ins Blut aufgenommen wurde, steht er einer weiteren potenziellen Verlustquelle gegenüber, dem „First-Pass-Effekt“. Das mit dem Wirkstoff angereicherte Blut wird zur Leber transportiert, wo die Leber wie ein kritischer „Türsteher“ agiert und entweder für die Verteilung des Wirkstoffs im gesamten Körper sorgt oder ihn enzymatisch inaktiviert, um ihn schnellstmöglich auszuscheiden.
Dieser ausgeklügelte Schutzmechanismus veranschaulicht eindrücklich, wie der menschliche Körper im Laufe der Evolution Strategien entwickelt hat, um eine Balance zwischen der Aufnahme von Nährstoffen und dem eigenen Schutz zu gewährleisten. Moderne Arzneistoffe sowie auch CBD und THC sind in vielerlei Hinsicht für unseren Körper fremd, weshalb dieser Schutzmechanismen besonders stark zum Tragen kommt. Beispielsweise sind CBD und THC weder wasserlöslich noch haben sie dedizierte Transportmechanismen, die ihre Absorption aus dem Darm ins Blut erleichtern. Hinzu kommt, dass sie durch Leberenzyme schnell und fast vollständig inaktiviert und eliminiert werden, wodurch ihre tatsächlich verfügbare Menge stark beschränkt wird. Die Weltgesundheitsorganisation (WHO) hat 2018 konkrete Zahlen veröffentlicht, wonach nur etwa 6 % der eingenommenen CBD-Menge tatsächlich vom Körper aufgenommen wird[1]. Dies stellt die Effizienz vieler gängiger Präparate in Frage.
Die Vorstellung, dass eine niedrige Bioverfügbarkeit einfach durch eine Erhöhung der Dosierung ausgeglichen werden könnte, erweist sich als trügerisch. Überhöhte Dosierungen bergen das Risiko einer Toxizität, können die Leber überfordern und deren Funktionsfähigkeit einschränken. Dies kann paradoxerweise dazu führen, dass der Körper unerwartet hohe Mengen des Wirkstoffes aufnimmt, was das Gleichgewicht zwischen Wirksamkeit und Sicherheit stört.
Formulierungstechnologie: Vom Molekül zur maßgeschneiderten Medizin
Ein eleganter Lösungsansatz für diese Herausforderungen kann in der modernen Formulierungstechnologie gefunden werden. Diese pharmazeutische Disziplin beschäftigt sich intensiv damit, wie die Aufnahme therapeutisch wertvoller Wirkstoffe so verbessert werden kann, dass sie eine tatsächliche und spürbare Wirkung im Körper entfalten. Vereinfacht ausgedrückt, handelt es sich dabei um die Kunst und Wissenschaft, Wirkstoffe so zu gestalten, dass sie genau zum richtigen Zeitpunkt, in der richtigen Menge und am gewünschten Ort im Körper wirken. Ihr Ziel ist es, die Effizienz des Wirkstoffs zu steigern und gleichzeitig Nebenwirkungen, die durch Überdosierungen eintreten können, zu minimieren.
Für Cannabinoide war die anfängliche Medikamentenformulierung oft simpel, wie im Fall von Epidyolex (Handelsname), das neben CBD nur vier zusätzliche Inhaltsstoffe enthielt:
Sesamöl und Ethanol zum Lösen des CBD sowie Erdbeeraroma und Sucralose zur Geschmacksgebung. Die derzeit auf dem Markt erhältlichen oder noch in klinischen Studien getesteten Formulierungen zeichnen sich durch eine deutlich komplexere Zusammensetzung aus. Die US-amerikanische National Library of Medicine bietet über ihre Website ClinicalTrials.gov Zugang zu globalen klinischen Studien[2]. Ebenso kann das Europäische Clinical Trials Register als Informationsquelle genutzt werden[3]. Bei der Suche nach „Tetrahydrocannabinol“, „Dronabinol“ und „THC“ ergeben sich aktuell 684 Studien, während „Cannabidiol” und “CBD” 998 Studien aufzeigen. Eine Fokussierung auf aktive Studien mit Formulierungstechnologien verengt die Ergebnisse deutlich. Zu finden sind neben einfachen öligen Lösungen auch Liposome, SEDDS (Self-Emulsifying Drug Delivery Systems), Cyclodextrine, und viele weitere Formulierungstechnologien. Der nachfolgende Abschnitt gibt einen detaillierteren Blick auf jede dieser Technologien.
Von Tradition zu Innovation: Eine Übersicht von Formulierungsansätzen
Liposome
Liposome sind in der Welt der CBD-Produkte weit verbreitet und gehören zu den am häufigsten vertretenen Formulierungen auf dem freiverkäuflichen Markt. Ihre Beliebtheit verdanken sie ihrer besonderen Struktur: Sie besitzen eine Phospholipid-Doppelschicht, die in ihrer Beschaffenheit der menschlichen Zellmembran ähnlich ist. Diese Ähnlichkeit erlaubt den Liposomen, mit den Zellmembranen zu interagieren, was zu einer verbesserten Bioverfügbarkeit führt. Viele Firmen greifen daher auf diese Technologie zurück und nutzen die Vorteile der liposomalen Formulierung. Verschiedene Marken betonen hierbei unterschiedliche Vorteile. Zum Beispiel hebt Hempamed die „4-fache Wirksamkeit“ ihrer Formulierung hervor, während Natura Vitalis und CBD Vital die „rasche Wirkung und Absorption“ ihrer Produkte betonen. Allerdings werden von diesen Unternehmen keine konkreten Daten oder Verweise auf wissenschaftliche Studien geliefert, die ihre Aussagen untermauern. Schaut man in die Fachliteratur, so findet man Untersuchungen, die die Wirkung von liposomalem CBD mit Standard-CBD-Formulierungen vergleichen. Bei der Behandlung von Osteoarthritis etwa zeigte eine Studie, dass 20 mg liposomales CBD dieselben therapeutischen Effekte erzielten wie 50 mg Standard-CBD[4]. Dies unterstreicht die Effizienz liposomaler Formulierungen in bestimmten Anwendungsbereichen.
Nanoemulsion
Eine Nanoemulsion beschreibt die feine Verteilung von Öl in Wasser, wobei die Größe der Tröpfchen im Nanometerbereich liegt. Um die Vorstellung von „nano“ greifbarer zu machen: Das Verhältnis von 1 Nanometer zu 1 Meter ist vergleichbar mit dem Durchmesser einer Murmel im Verhältnis zum Durchmesser der Erde. Unternehmen wie HempRise mit ihrem Produkt HempNANO und Green Pharmaceutics mit der Nano-CBD-Tinktur setzen auf Nanoemulsionen. Sie werben damit, dass ihre Produkte bis zu zehnmal wirksamer seien als konventionelle CBD-Öle. Trotz intensiver Recherche konnten auch hier keine konkreten Daten gefunden werden, die diese Werbeaussagen unterstützen. In der wissenschaftlichen Literatur finden sich jedoch Anhaltspunkte dafür, dass die Verwendung von Nanoemulsionen die Bioverfügbarkeit von Cannabinoiden tatsächlich erhöhen kann. So wurde beispielsweise in einer Studie nachgewiesen, dass THC in Form einer Nanoemulsion doppelt so gut absorbiert wurde wie herkömmliches, in Öl gelöstes THC[5].
SEDDS
SEDDS (Self-Emulsifying Drug Delivery Systems) sind Systeme, welche in der Lage sind, selbstständig eine Nanoemulsion auszubilden, wenn sie in Kontakt mit Wasser kommen. Historisch wird diese Technologie in der Fachliteratur oft als „Mikroemulsion“ beschrieben, was irreführend ist, da sich tatsächlich eine Nanoemulsion ausbildet. In der Fachliteratur zu Formulierungstechnologien fallen SEDDS in jüngster Zeit durch eine deutliche Zunahme von Veröffentlichungen auf. Dieser Trend spiegelt sich auch im Bereich der klinischen Studien wider, wo SEDDS ebenfalls eine hohe Präsenz aufweisen. So befindet sich beispielsweise das GelPell von Satipharm, das eine um 31-34 % höhere Bioverfügbarkeit besitzt, in der Phase II für die Behandlung von Epilepsie. Zugleich befindet sich Arvisol von Echo Pharmaceuticals für die Behandlung von Schizophrenie in Phase I. Ein Beispiel für ein bereits auf dem Markt befindliches SEDDS-Produkt ist VESIsorb von VESIfact. Dieses zeichnet sich durch eine
4,4-fache Steigerung der Bioverfügbarkeit gegenüber einer Standardformulierung aus[6]. Hervorzuheben ist, dass das Unternehmen die zugrunde liegende Forschung auf ihrer Website öffentlich und nachvollziehbar beschreibt.
Co-Kristallisation
Die Co-Kristallisation, ein in der Pharmazie etabliertes Verfahren, hat im Kontext von Cannabinoiden bislang wenig Beachtung gefunden. Sie ermöglicht die Bildung von Mischkristallen, die aus dem pharmazeutischen Wirkstoff und einem oder mehreren Kristallbildnern zusammengesetzt sind. Diese sogenannten Co-Former können die Materialeigenschaften modifizieren, ohne die intrinsische pharmakologische Aktivität des Arzneimittels zu kompromittieren. Ein innovativer Ansatz in dieser Richtung ist ART12.11, entwickelt von Artelo Biosciences. Bei diesem Verfahren wird Tetramethylpyrazin als Co-Former eingesetzt, wofür das Unternehmen ein Patent hält. In prä-klinischen Untersuchungen zeigte ART12.11 nach eigenen Angaben nicht nur die erwarteten angstlösenden Effekte, sondern auch eine schützende Wirkung auf das räumliche und kurzfristige Gedächtnis.
Cyclodextrine
Cyclodextrine bestehen aus sechs bis acht Glukose-Zucker-Bausteinen, die kreisförmig angeordnet sind. Ihre Fähigkeit, fettlösliche Wirkstoffe in diesem Kreis einzuschließen, erhöht die Löslichkeit und damit die Bioverfügbarkeit von Arzneimitteln erheblich und kann zudem unangenehme Geschmacks- oder Geruchseigenschaften maskieren. Die Firma AOP Orphan Pharmaceuticals hat unter anderem eine schnell zerfallende, kontrolliert freisetzende Formulierung von Nabilon, einem synthetischen THC-Derivat, entwickelt[7]. Dieses Produkt befindet sich derzeit in Phase III der klinischen Studie zur Behandlung von Parkinsonsymptomen bei älteren Patienten. Ferner entwickeln Unternehmen wie Medexus Pharmaceuticals und Vireo Health LLC Cyclodextrine-Formulierungen mit CBD. Beide Unternehmen berichten von erheblichen Verbesserungen der Bioverfügbarkeit, detaillierte Studienergebnisse konnten jedoch nicht gefunden werden.
Weitere Technologien
Neben den klassischen Formulierungstechnologien existieren innovative Ansätze, die in der pharmazeutischen Landschaft als eher unkonventionell gelten. Ein Beispiel wäre ein Kaugummi, der von Axim Biotechnologies Inc. entwickelt wurde[8]. Diese Formulierung kombiniert zwei Cannabinoide in einem Verhältnis von 1:1 mit einer Gesamtdosis von 5 mg pro Kaugummi. Der Kaugummi zielt auf die Linderung der Symptome bei Multipler Sklerose, Parkinson, Demenz, Restless-Legs-Syndrom und post-herpetischer Neuralgie. In den USA finden bereits präklinische Untersuchungen für post-herpetische Neuralgie und psychotische Störungen statt. Bislang liegen keine Fortschritte oder Ergebnisse vor.
Die Vielfalt der vorgestellten Formulierungstechnologien unterstreicht eindrücklich, dass es keinen universellen Ansatz oder ein „One-size-fits-all“-Prinzip in diesem Bereich gibt. Jede Technologie besitzt ihre spezifischen Vorteile sowie Limitierungen. Entsprechend kann keine Technologie als überlegen angesehen werden, sondern jede hat in Abhängigkeit von den konkreten Anforderungen und Zielen ihre Daseinsberechtigung. Dies betont die Notwendigkeit individueller Lösungen in der Entwicklung, um den spezifischen Bedürfnissen und Herausforderungen gerecht zu werden.
Abschließend sei angemerkt, dass die Herausforderung einer suboptimalen Bioverfügbarkeit kein exklusives Charakteristikum von Cannabinoiden ist. Eine Reihe anderer wertvoller Substanzen, darunter Omega-3-Fettsäuren, Curcumin und Vitamin D, stoßen auf ähnliche Hindernisse hinsichtlich der Absorption durch den menschlichen Körper. Diese Stoffe könnten erheblich an therapeutischem Wert gewinnen, wenn ihre Bioverfügbarkeit durch fortschrittliche Formulierungstechnologien verbessert würde. Wer eine Optimierung der Bioverfügbarkeit solcher Substanzen anstrebt, findet in versierten Pharmazeuten mit Spezialisierung auf Formulierungstechnologie nicht nur Berater, sonern auch Wegbereiter für innovative Gesundheitslösungen.
Schlussbetrachtung: Cannabinoide, Bioverfügbarkeit und der Weg vorwärts
Cannabinoide, insbesondere CBD und THC, sind in jüngster Zeit wegen ihrer potenziellen therapeutischen Vorteile ins Rampenlicht gerückt. Ein zentrales Problem dabei ist jedoch ihre geringe Bioverfügbarkeit. Innovative Formulierungstechnologien wie Liposome, Nanoemulsionen, SEDDS und Co-Kristallisation bieten hierfür jedoch wirksame und raffinierte Lösungsmöglichkeiten. Einige dieser Technologien, wie CBD-haltige Liposome und Nanoemulsionen, sind bereits als Nahrungsergänzungsmittel auf dem Markt verfügbar. Obwohl sie eine erhöhte Wirksamkeit versprechen, fehlen in den meisten Fällen konkrete Nachweise hierfür. Die Formulierungen, die sich aktuell in klinischen Phasen befinden, haben in präklinischen Tests bereits beeindruckende Ergebnisse erzielt und sind daher sehr vielversprechend. Es wird interessant sein zu beobachten, wie sich die Forschung im Bereich der Cannabinoide in den nächsten Jahren weiterentwickelt und welche dieser Formulierungen schließlich als anerkannte Medikamente den Weg in die Apothekenregale finden werden. ↙
[1] https://www.who.int/medicines/access/controlled-substances/ CannabidiolCriticalReview.pdf;
[2] https://clinicaltrials.gov/;
[3] https://www.clinicaltrialsregister.eu/;
[4] https://doi.org/10.1097/j.pain.0000000000001896;
[5] https://doi.org/10.1016/j.jddst.2022.104004;
[6] https://doi.org/10.3390/molecules24162967;
[7] U.S. Patent Application No. US20130295026A1;
[8] U.S. Patent Application No. US20180110730A1

Aufmacher: Crystalweed Cannabis/Unsplash.com







