

Skrøpelighet og sarkopeni ved leversykdom s.
Kronisk koronarsyndrom i 2025 s. 20 Moderne nyrebeskyttende behandling – Medikamenter og annet s. 25





Skrøpelighet og sarkopeni ved leversykdom s.

Kronisk koronarsyndrom i 2025 s. 20 Moderne nyrebeskyttende behandling – Medikamenter og annet s. 25



Helsedirektoratet anbefaler at DIFICLIR vurderes til behandling av C. difficileinfeksjon (CDI) hos pasienter på sykehus og med høy risiko for residiv

Vennligst se retningslinjer for fullstendig behandlingsanbefaling
Elektronisk søknadsløsning for individuell refusjon, scan her
200 mg tabletter og granulat til mikstur, 40 mg/ml
Indikasjoner: For behandling av Clostridioides difficile-infeksjoner (CDI), også kjent som C. difficile-assosiert diaré (CDAD). Tabletter: Hos voksne og pediatriske pasienter med en kroppsvekt på minst 12,5 kg. Granulat: Hos voksne, ungdom og barn 0 - < 18 år. For både tabletter og granulat skal det tas hensyn til offisielle retningslinjer for korrekt bruk av antibakterielle midler. Vanligste bivirkninger: Vanlige: Forstoppelse, kvalme, oppkast Vanligste alvorlige bivirkninger: Overfølsomhetsreaksjoner inkl. alvorlig angioødem. Interaksjoner: Forsiktighet utvises ved samtidig bruk av potente P-gp-hemmere. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Forsiktighetsregler: Fidaksomicin bør brukes med forsiktighet ved kjent allergi mot makrolider. Hvis det oppstår en alvorlig allergisk reaksjon, skal legemidlet seponeres og egnede tiltak igangsettes. Bør brukes med forsiktighet ved pseudomembranøs kolitt eller fulminant eller livstruende CDI, ved nedsatt lever- og nyrefunksjon. Granulat bør brukes med forsiktighet hos spedbarn < 6 måneder/< 4 kg. Graviditet, amming og fertilitet: Graviditet: Det anbefales å unngå bruk under graviditet. Amming: Det må tas en beslutning om amming skal opphøre eller behandling avstås fra, basert på nytte-/risikovurdering. Fertilitet: Dyrestudier indikerer ingen effekt på fertilitet. Dosering: Tabletter: Standard dosering: Voksne og barn ≥12,5 kg: Anbefalt dose er 200 mg (1 tablett) administrert 2 ganger daglig (1 tablett hver 12. time) i 10 dager. Utvidet pulsdosering: Voksne: 200 mg tabletter administreres to ganger daglig for dag 1–5 (ingen tablett på dag 6) og deretter én gang daglig annenhver dag for dag 7–25. Hvis en dose blir glemt, skal den glemte dosen tas så snart som mulig, men hvis det snart er tid for neste dose, skal tabletten hoppes helt over. Granulat: Voksne: Standard dosering: Anbefalt dose er 200 mg (5 ml) 2 ganger daglig (5 ml hver 12. time) i 10 dager Utvidet pulsdosering: Tas 2 ganger daglig på dag 1-5 (ingen dose på dag 6) og deretter 1 gang daglig annenhver dag på dag 7-25. Ungdom og barn 0 - < 18 år: Anbe falt dose baseres på kroppsvekt og tas 2 ganger daglig (1 dose hver 12. time) i 10 dager. Administrering: Tabletter: Kan tas med eller uten mat. Svelges hele sammen med et glass vann. Granulat: Rekonstitueres av farmasøyt eller helsepersonell. Tas peroralt, med eller uten mat, eller ved behov via en enteral sonde med sprøyte. Pakninger og priser: Tabletter 20 stk. (blister) kr 18 099,90. Granulat til mikstur: 1 stk. (glassflaske) kr 18 288,90. Reseptgruppe C. DIFICLIR er tilgjengelig til rabattert pris via LIS-anbud og er gjenstand for individuell refusjon for blå resept, for mer informasjon; se Helsedirektoratets hjemmeside. Basert på SPC godkjent av DMP/EMA: 01.12.2023.
For utfyllende informasjon om dosering, forsiktighetsregler, interaksjoner og bivirkninger - se felleskatalogen.no
Referanse: 1. https://www.helsedirektoratet.no/retningslinjer/antibiotika-i-sykehus/infeksjoner-i-abdomen#clostridioides-difficile-infeksjon. Sist faglig oppdatert 01.03.2022.
Tillotts Pharma AB | Gustavslundsv. 135, 167 51 Bromma, Sverige | Tel: +46 8-704 77 40 | nordicinfo@tillotts.com
Styret i Norsk indremedisinsk forening:
Trond Vartdal
Leder
Knut Lundin
Nestleder
Cecilie H Nordmo
Styremedlem
Runa Andreassen
Styremedlem
Hamza Nahoui Leder NYI
Redaktører:
Stephen Hewitt (ansvarlig redaktør)
OUS Aker
stehewi@online.no
T: 913 72 199
Ole Kristian H. Furulund (assisterende redaktør)
Kommuneoverlege i Bærum
Fagredaktører:
Bernt Aarli (Lungemedisin)
Haukeland universitetssykehus
Eystein Husebye (Endokrinologi)
Haukeland universitetssykehus
Gunnar Einvik (Lungemedisin) Akershus universitetssykehus/NTNU
Indremedisineren er et fagtidsskrift rettet mot norske leger som arbeider innen fagomådet indremedisin, med dets ulike retninger. Indremedisineren sendes ut til alle medlemmer av Norsk indremedisinsk forening (Nif), som for tiden er ca 3 400, samt til andre med interesse for faget.
Stephen Hewitt Redaktør Indremedisineren
Maria Seferowicz Høstmøtetkomitéen
Andrea Dobloug Spesialitetskomiteen
Rune Eilertsen Vara
Anita Suntharalingam Vara NYI
Maya Bass
Akuttmottaket, Bærum sykehus, mctbass@hotmail.com
Tone Svilaas OUS Aker tosvil@ous-hf.no
Trine Finnes (Endokrinologi) Sykehuset Innlandet/OUS
Guri Hagberg (Geriatri) OUS Ullevål
Camilla Hem (Geriatri) Diakonhjemmet
Foreningsnytt
av materiale fra Indremedisineren må skje etter tillatelse fra redaksjon og forfatter.
Indremedisineren vil presentere relevant faglig og fagpolitisk stoff fra norske miljøer, samt noe internasjonalt rettet stoff av allmen interesse. Vi ønsker å legge til rette for at terskel og takhøyde gir rom for en allment engasjert indremedisiner å ytre seg.
Forsidebilde
Foto: Bilde fra kongressområdet.
Utgivelsesplan
Bestillingsfrist/ Levering Forfatterfrister Materiellfrist annonsører Posten
Nr. 3 1/9 9/9 8/10
Nr. 4 1/11 11/11 10/12
Annonsepriser 2025
Bakside 24.500,Omslagsside 22.000,Helside 20.500,1/2 side liggende 14.500,-
Årsavtale
Med fire innrykk oppnås min. 20% rabatt.
Annonseformat
Bredde x Høyde
1/1 side 210 mm x 297 mm + 5 mm
1/2 side liggende 210 mm x 148,5 mm + 5 mm
1/2 side stående 105 mm x 297 mm + 5 mm
Bakside 210 mm x 230 mm + 5 mm
Annonsemateriell
Høyoppløste PDF-filer, der fonter og høyoppløste bilder er inkludert.
Layout, produksjon og annonsesalg
Apriil Media AS E-post: ragnar.madsen@apriil.no www.apriil.no




Disclaimer














• Informasjon, meninger og synspunkter som utgis i Indremedisineren tilhører forfatterne, og ikke nødvendigvis Norsk indremedisinsk forening eller redaksjonen.
• Publisering av artikler, annonser eller annen informasjon, betyr ikke nødvendigvis støtte eller aksept for disse.
• Redaksjonen og utgiver anstrenger seg for ikke å publisere unøyaktige eller misvisende data, men forfatterne må selv ta ansvar for data,

uttalelser og meninger som blir utgitt på deres vegne.
• Redaksjonenen og utgiver gjør sitt beste for å sikre at legemiddeldoser og andre kvantiteter presenteres nøyaktig, men vi anbefaler leserne å bruke legemidler i samsvar med Felleskatalogen/Norsk legemiddelhåndbok.
• Indremedisineren og/eller utgiver kan ikke holdes ansvarlig for evt. feil eller konsekvenser som oppstår som følge av bruk av informasjon i tidsskriftet.
Kalcipos brukes for forebygging og behandling av kalsium og vitamin D-mangel hos eldre.1 osteoporosebehandling hos pasienter med risiko for vitamin D- og kalsiummangel.1 Tablettene er beregnet for voksne over 18 år og doseres daglig.1 Svelges hele med vann. Kan ev. knuses eller deles ved behov.1
Mengde kalsium i preparatet er under vanlig anbefalt daglig inntak.1 Preparatet er derfor primært beregnet til pasienter med behov for vitamin D- tilskudd utover inntak av 500-1000 mg kalsium daglig via maten.1 Kalsiuminntak via maten bør beregnes av forskriver.1

Utvalgt sikkerhetsinformasjon:1
• Kalcipos er kontraindisert ved: Hyperkalsemi, hyperkalsiuri samt sykdommer og/ eller tilstander som fører til hyperkalsemi og/eller hyperkalsiuri (f.eks. myelom, benmetastaser, primær hyperparatyreoidisme), nefrolitiasis, nefrokalsinose, hypervitaminose D, og nyresvikt.
•
• Kalcipos bør forskrives med forsiktighet til pasienter med sarkoidose.

Ved graviditet skal daglig inntak ikke overskride 1500 mg kalsium og 600 IE vitamin D.1 Skal derfor ikke brukes rutinemessig for forebygging av kalsium- og vitamin D-mangel i svangerskapet, men kan brukes til gravide som har stor risiko for å utvikle hypokalsemi, eller som allerede har kalsium- og vitamin D-mangel.1
Kan brukes under amming. Kalsium og vitamin D3 går over i morsmelk.1
Oppbevaring: Oppbevares i originalpakningen for å beskytte mot lys. Hold beholderen tett lukket for å beskytte mot fuktighet.1
Kalcipos (kalsiumkarbonat, vitamin D3): refusjon og pris Reseptgruppe C. Pakninger og priser: 90 tabletter koster: 196,80.2
Kalcipos kan for enkelte diagnoser gis individuell stønad på blå resept, se vedlegg 1, til folketrygdloven § 5-14, blåreseptforskriften.3
Få oversikt over aktuelle diagnosekoder og vilkår i fulltekst på Helsedirektoratets nettsider ved å skanne QR-koden.

Ytterligere informasjon preparatomtalen, SPC: Kalcipos (11.11.2024)

Referanser:
1. Kalcipos SPC (11.11.2024), avsnitt 2., 3., 4,1, 4.2, 4.3, 4.6. og 6.4.
2. Kalcipos, Felleskatalogtekst basert på SPC 11.11.2024
3. Helsedirektoratet, rundskriv, kapittel 5, stønad til helsetjenester, Vedlegg 1 til § 5-14 legemiddellisten, legemidler, kalsiumpreparater Sist faglig oppdatert: 23.04.2024
Viatris AS Hagaløkkveien 26 | Pb 194 – 1371 Asker, Norge infonorge@viatris.com | D-vitaminmangel.no
| 12.2024
Det er (forhåpentligvis) de færreste som går rundt og lurer på hvordan sykehusene styres. De fleste leger synes det er helt greit å vite nokså lite om dette, og heller bruke energien på å være en dyktig kliniker og gi optimal pasientbehandling. Det er selvsagt mye som avgjør hvordan sykehusene må planlegge og prioritere. Først og fremst økonomi og fordeling mellom faste utgifter som lønn og avskrivinger, nye bygg og investering i nytt utstyr. Videre er det helsepolitikere som ønsker å sette sitt preg på helsevesenet, som Høies «Pasientens Helsevesen» og disse dagers Ventetidsløfte. I tillegg til dette kommer oppdrag. Oppdragene sendes fra Helse- og omsorgsdepartementet (HOD) til Helsedirektoratet (HDir) og til de regionale helseforetakene (RHF’ene). Disse to siste setter sitt eget preg på oppdraget og sender det videre til sykehusene, som så skal etterleve oppdragene. Disse kan være ganske omfattende og konkrete. Oppdraget leveres i januar og skal svares ut tidlig på høsten, til RHF’ene og/eller HDir, og disse sender sine samlede svar til HOD. Og slik går året.
Et av årets oppdrag er sendt likt til alle sykehusene, og kommer til å påvirke alle indremedisinere i norske sykehus enten man arbeider med «generell indremedisin» eller innen de ulike variantene av de indremedisinske spesialiteter. Oppdraget lyder slik: «De regionale helseforetakene skal legge til rette for gode karriereløp og tilgang til breddekompetanse innen indremedisin og kirurgi. Det innebærer blant annet å styrke spesialistutdanningen mtp. disse spesialitetene og å vurdere organisering og faginndeling. Berørte parter skal involveres i arbeidet. Det vises til rapporten « Breddekompetanse i indremedisin og kirurgi – viktige veivalg» fra 2024.» Breddekompetanse der, altså. Som man ser berører oppdraget ikke bare utdanning, men også sykehusenes organisering og faginndeling.
Når det gjelder utdanning, så er det på generelt grunnlag tre måter å oppnå breddekompetanse på:
• Utdanne og ansette leger med dobbelspesialitet . Det har vi mange av pr. nå, da alle indremedisinere og de fleste kirurgene utdannet før 2019 har dette. Disse går av med pensjon de neste 2025 årene, og det utdannes relativt få nye med to spesialiteter.
• Satse på noen få spesialiteter som er definert som « breddespesialiteter », som generell kirurgi og generell indremedisin. Og la disse arbeide i større enheter i sykehusene.
• Styrke « LIS2 ». 10 indremedisinske og 8 av de kirurgiske spesialiteter har felles læringsmål i hhv. indremedisin (FIM) og kirurgi (FKI). Det er estimert 2-4 år å oppnå denne kompetanse. For de fleste skjer dette samtidig som man er LIS3 i en av disse 18 spesialitetene, og dermed er det usikkert hvor robust kompetansen er, f.eks. om hvorvidt FIM/FKI gjør legen vaktkompetent for flere spesialiteter (enn sin egen).
Sykehusene skal beskrive styrket spesialistutdanning i breddespesialitetene og karriereløp i disse. Det gir liten mening å utdanne leger i generell kirurgi og indremedisin om det ikke er noen overlege stillinger i sikte. Videre skal sykehusene beskrive aktuelle endringer i organisering, faginndeling og vakter. Hvor mange vaktlag skal man unne seg? Hvor høyspesialisert utredning og behandling skal foregå på vakt? Hva er egentlig tilstrekkelig vaktkompetanse? Hvor inngripende strukturelle endringer bør sykehusene gjøre på sengeposter og poliklinikker? Disse er spennende og utfordrende spørsmål som skal diskuteres i løpet av sommeren og høsten.
Videre har Helsedirektoratet satt ned to arbeidsgrupper, en for
indremedisin og en for kirurgi, og tilhørende referanse grupper. Disse skal svare ut konkrete spørsmål fra Helsedirektoratet, som inkluderer blant annet å endre tittel fra «indremedisin» til «generell indremedisin», revisjon av felles del 2 (LIS2), gjennomgå alle læringsmål (LIS3) i spesialiteten indremedisin («…hva spesialiteten skal være i fremtiden…»).
Det er altså snakk om å vurdere reelle endringer. Nå kan vi forme spesialiteten(e) på nytt og bruke erfaringer siden 2019 (da dagens spesialiststruktur ble innført) til å sette et varig preg. Jeg håper flest mulig engasjerer seg i diskusjonen og i aktuelle arbeidsgrupper både lokalt, regionalt og nasjonalt.
Og jeg håper det også blir tid til en skikkelig ferie - med ønsker om en flott sommer!
Hilsen
Trond Vartdal
Leder, Norsk Indremedisinsk forening








Vi lever i en tid med økende uro – og på årets høstmøte vil vi få høre innlegg om hva vi bør forberede oss på i en ny verden samt en mer praktisk tilnærming om å være indremedisinere i krig, temaer som dessverre er altfor aktuelle!
Som hvert år kommer en rekke spennende innlegg fra forskjellige grener av indremedisinen - vanskelige trombocytopenier med vanskelige forkortelser, antibiotikautfordringer i fremtiden, lungekasuistikker og mer om vaping, hvordan håndtere akutt leversvikt og behandling av hjertesykdom hos gravide. Erfaringer fra arbeid med long-covid pasienter og å hjelpe folk med kroniske sammensatte helseplager tilbake i
livene og jobbene sine, samt mer om eldre på intensiv. Andre spennende temaer er råd om stressmestring hos leger og hvordan det har gått med implementeringen av kloke valg på sykehuset i Vestfold.
Med ønske om en riktig god sommer - og hold av datoen - så sees vi i oktober!
Vennlig hilsen, Høstmøtekomiteen
Påmelding
Vi har begrenset antall plasser, så meld dere på tidlig. I år er Høstmøtet gratis for alle yrkesaktive medlemmer i Norsk indremedisinsk forening, inkludert lunsj begge dager. Bindende påmelding sikrer plass, faglig påfyll og riktig matbestilling. gyroconference.eventsair.com/nif-hostmote
En fantastisk vår ligger bak oss, og det går mot en etterlengtet sommer. Dette nummeret er en samling av innsikt, som spenner over både velkjente og mindre kartlagte temaer.
Det første temaet er sarkopeni og skrøpelighet, som er hyppige og alvorlige følgetilstander hos pasienter med leversykdom i endestadiet, og som viser en klar sammenheng til sykelighet og redusert overlevelse. Ina Marie Andersen, Kristine Wiencke og Trine Folseraas gir en oversikt over mekanismer bak tilstandene og anbefalinger for diagnose. Verktøy som Liver Frailty Index og Psoas Muscle Index omtales. Forfatterne vektlegger tidlig identifisering og tiltak med optimalisert ernæring og fysisk trening.
Johan Lunding ved Diakonhjemmet sykehus gjør videre rede for Kronisk obstipasjon, som er en ganske så vanlig tilstand i befolkningen – blant eldre angis en forekomst hos opptil 50% hos personer innlagt på institusjon. I artikkelen omtales symptomer, livsstilens og legemidlers betydning for tarmtransitt, ulike årsaker til obstipasjon samt utredning og behandling. Det er viktig å huske på at det også finnes sekundære årsaker til obstipasjon og at det er mer enn en form for behandling.
Håndtering av pasienter med kronisk koronar sykdom har vært i endring. Kristina Fladseth, Jan Mannsverk, Andreas Kristensen og Henrik Schirmer skriver i sin oversiktsartikkel om hvordan ny teknologi og kunnskap endrer utredning og

behandling av denne pasientgruppen. De viser til nye retningslinjer fra European Society of Cardiology og sentrale endringer, som er relevante for norske indremedisinere. Ikke-invasiv bilde diagnostikk tar over som hjørnesteinen i diagnostikken, og livsstilsendringer og medisinsk behandling bør optimaliseres hos flere pasienter før invasiv koronar angiografi.
Trond Jenssen gir en konsis og praksisorientert oversikt over utviklingen innen nyrebeskyttende behandling ved diabetes og kronisk nyre sykdom. Nye medikamenter har vist lovende resultater. Med særlig vekt på SGLT2-hemmere, diskuteres behandlingsgevinst, praktiske utfordringer og oppfølging. Artikkelen tydeliggjør hvordan disse medikamentene har flyttet grensene for nefrologisk forebygging og gjør oss mer fortrolig i bruken i relevante pasientforløp.
I en tankevekkende artikkel om palliasjon, utfordrer Nina Marie Undeland, Vilde Holand Juberg og Margrethe Aase Schaufel den tradisjonelle forståelsen for dette feltet innen indremedisin. Forfatterne peker på at mange pasienter med alvorlig, ikke-kurativ sykdom i dag får for lite systematisk lindrende behandling. Palliasjon bør i større grad inngå som en integrert del av vårt indre medisinske arbeid, også utenfor kreftfeltet, og det pekes på behovet for økt bevissthet, tverr faglig samarbeid og kompetanseheving blant leger.

Ole Kristian H. Furulund belyser i sin engasjerte faglige kommentar et viktig, men ofte nedprioritert felt –vaksinasjon av voksne. Han viser til betydelige mangler i dekningen blant eldre og kronisk syke, og skriver at indremedisinske leger må ta et større ansvar. Artikkelen omtaler dagens anbefalinger og nye vaksiner som er på vei. Furulund understreker at vaksinasjon bør integreres bedre i vårt forebyggende arbeid i klinikken.
Vi viser videre til artikler under Foreningsnytt. Det følger et rikt reisebrev fra European Congress of Internal Medicine (ECIM) 2025 i Firenze, der Ole Kristian H. Furulund med deltagere deler av høydepunktene med særlig vekt på sarkopeni, hjerte svikt, nye diabetesstrategier og utfordringer innen geriatrisk medisin. Det følger også omtaler fra Hematologisk vintermøte i Ålesund og Endokrinologisk vintermøte i Tromsø, som rapporterer om gode faglige innlegg og diskusjoner, og sosialt felleskap. Vi formidler i tillegg en historisk og faglig markering av 30-årsjubileet for 4S-studien, som har vært en milepæl i kardiovaskulær forskning.
Vi viser stor omtanke til dere som holder fortet i sommermånedene –forhåpentligvis blir det en fin og velfortjent ferie også på dere etter hvert! Redaksjonen ønsker med det alle våre lesere god lesning og en riktig god sommer fylt av varme, ro og inspirasjon!


13-19 mmol/mol‡
Redusert risiko for alvorlige kardiovaskulære hendelser*3,7 26 %
Redusert risiko for progresjon av nyresykdom*3,8 24 %
3,5-6,5 kg‡
Vektreduksjon#3-6
Ozempic® er indisert til behandling av voksne med utilstrekkelig kontrollert diabetes mellitus type 2 som tillegg til diett og fysisk aktivitet
• som monoterapi når metformin er vurdert uegnet grunnet intoleranse eller kontraindikasjoner.
• i tillegg til andre legemidler til behandling av diabetes.
For resultater fra studier vedrørende kombinasjoner, effekt på glykemisk kontroll, kardiovaskulære hendelser, renale hendelser og populasjoner som ble undersøkt, se preparatomtale (SPC) avsnitt 4.4, 4.5 og 5.1.
9-11
Ozempic® skal ikke brukes hos pasienter med diabetes mellitus type 1, hos gravide eller ammende. Ozempic® er ikke et erstatningspreparat for insulin. Kvinner i fertil alder anbefales å bruke prevensjon når de behandles med Ozempic®
• Gastrointestinale bivirkninger: Hyppigste rapporterte (svært vanlige ≥ 1/10) bivirkninger: Kvalme og diare. Generelt var disse reaksjonene milde eller moderate i alvorlighetsgrad og av kort varighet.
• Hypoglykemi: Kombinasjon med sulfonylureapreparat eller insulin kan øke risiko for hypoglykemi (svært vanlige ≥ 1/10). Egenmåling av blodglukose er nødvendig for å justere dosen av sulfonylurea og insulin, spesielt når behandling med Ozempic® startes opp og insulin reduseres. En trinnvis tilnærming til dosereduksjon av insulin anbefales.
• Diabetisk retinopati: Observert økt risiko for å utvikle komplikasjoner av retinopati hos pasienter med eksisterende diabetisk retinopati som behandles med insulin og Ozempic® (vanlig ≥ 1/100 til < 1/10). Forsiktighet bør utvises. Rask forbedring av glukosekontroll er blitt forbundet med midlertidig forverring av diabetisk retinopati.
• Diabetisk ketoacidose: Diabetisk ketoacidose har blitt rapportert hos insulinavhengige pasienter etter rask seponering eller dosereduksjon av insulin når behandling med en GLP-1 reseptoragonist ble startet.
• Akutt pankreatitt: Akutt pankreatitt er observert ved bruk av GLP-1-reseptoragonister (mindre vanlig ≥ 1/1 000 til < 1/100). Pasientene bør informeres om de karakteristiske symptomene på akutt pankreatitt. Ved mistanke om pankreatitt bør semaglutid seponeres.
Dosering x1 per uke2
Ozempic® skal administreres én gang per uke, subkutant i abdomen, i låret, eller i overarmen.
Start
0,25 mg
én gang per uke i 4 uker*
Titrér
0,5 mg
én gang per uke i minst 4 uker. Kan brukes som vedlikeholdsdose
* Ozempic® 0,25 mg: En ubrukt penn inneholder fire doser à 0,25 mg. Etter at
Alder
Nyrefunksjon
Kan benyttes uten dosejustering Anbefales ikke
Det er ikke nødvendig med dosejustering på grunnlag av alder
Lett, moderat eller alvorlig nedsatt funksjon.
Barn/ungdom under 18 år
Terminal nyresykdom Erfaring med bruk av semaglutid hos pasienter med terminal nyresykdom er begrenset
Hjertesvikt NYHA klasse I-III NYHA klasse IV
Leverfunksjon
Mild, moderat og alvorlig nedsatt funksjon. Begrenset erfaring ved alvorlig nedsatt leverfunksjon, forsiktighet bør utvises
Vedlikehold 1 mg for ytterligere glykemisk kontroll

igjen i pennen. Pennen skal kastes.
Individuell stønad og pris12,13
Ozempic® er ikke tilgjengelig på forhåndsgodkjent refusjon.
Vikår for individuell stønad for Ozempic® Fra og med 01.07.2024 kan det søkes om individuell stønad etter folketrygdens § 3 til Ozempic® Du kan lese mer om individuell stønad på www.helsedirektoratet.no
Reseptgruppe: C
Pakninger og priser: 0,25 mg: 1,5 ml ferdigfylt penn kr 1 120,00. 0,5 mg: 1,5 ml ferdigfylt penn kr 1 120,00. 1 mg: 3 ml ferdigfylt penn kr 1 120,00. (Pris per april 2025).
Les fullstendig preparatomtale eller felleskatalogen.no før forskrivning.
Referanser: 1. Ozempic® SPC, avsnitt 4.1. 2. Ozempic® SPC, avsnitt 4.2. 3. Ozempic® SPC, avsnitt 5.1. 4. Capehorn MS, Catarig A-M, Furberg JK, et al. Efficacy and safety of once-weekly semaglutide 1.0 mg vs once-daily liraglutide 1.2 mg as add-on to 1–3 oral antidiabetic drugs in subjects with type 2 diabetes (SUSTAIN 10), Diabetes & Metabolism, 2020; 46(2):100-109. 5. Ahrén B, Masmiquel L, Kumar H, et al. Efficacy and safety of once-weekly semaglutide versus once-daily sitagliptin as an add-on to metformin, thiazolidinediones, or both, in patients with type 2 diabetes (SUSTAIN 2): a 56-week, double- blind, phase 3a, randomised trial. Lancet Diabetes Endocrinol. 2017;5(5):341-354. 6. Pratley RE, Aroda VR, Lingvay I, et al. Semaglutide versus dulaglutide once weekly in patients with type 2 diabetes (SUSTAIN 7): a randomised, open-label, phase 3b trial. Lancet Diabetes Endocrinol. 2018;6(4):275-286. 7. Marso SP, Bain SC, Consoli A, et al. Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med. 2016;375:1834-1844. 8. Perkovic V, Tuttle KR, Rossing P, et al. Effects of Semaglutide on Chronic Kidney Disease in Patients with Type 2 Diabetes. N Engl J Med. 2024;391:109-121. 9. Ozempic® SPC, avsnitt 4.4. 10. Ozempic® SPC, avsnitt 4.8. 11. Ozempic® SPC, avsnitt 4.6. 12. Helsedirektoratet. Individuell stønad for Ozempic®. Tilgjengelig fra: https://www.helsedirektoratet.no/rundskriv/kapittel-5-stonad-ved-helsetjenester/vedlegg-1-til--5-14-legemiddellisten/ virkestoffer semaglutid-2 (Lest 28.04.2025). 13. Felleskatalogen. Pakning og pris Ozempic®. Tilgjengelig fra: https://www.felleskatalogen.no/medisin/ozempic-novonordisk-653285?markering=0 (Lest 28.04.20.25)



Skrøpelighet og sarkopeni er svært vanlig hos pasienter med leversykdom i endestadiet, og er assosiert med økt dødelighet. Tidlig diagnostikk og optimalisering av ernæring påvirker overlevelse. I denne artikkelen vil vi gi en introduksjon til bakgrunn, patofysiologi, diagnostikk og behandling ved skrøpelighet og sarkopeni ved leversykdom.
Definisjon
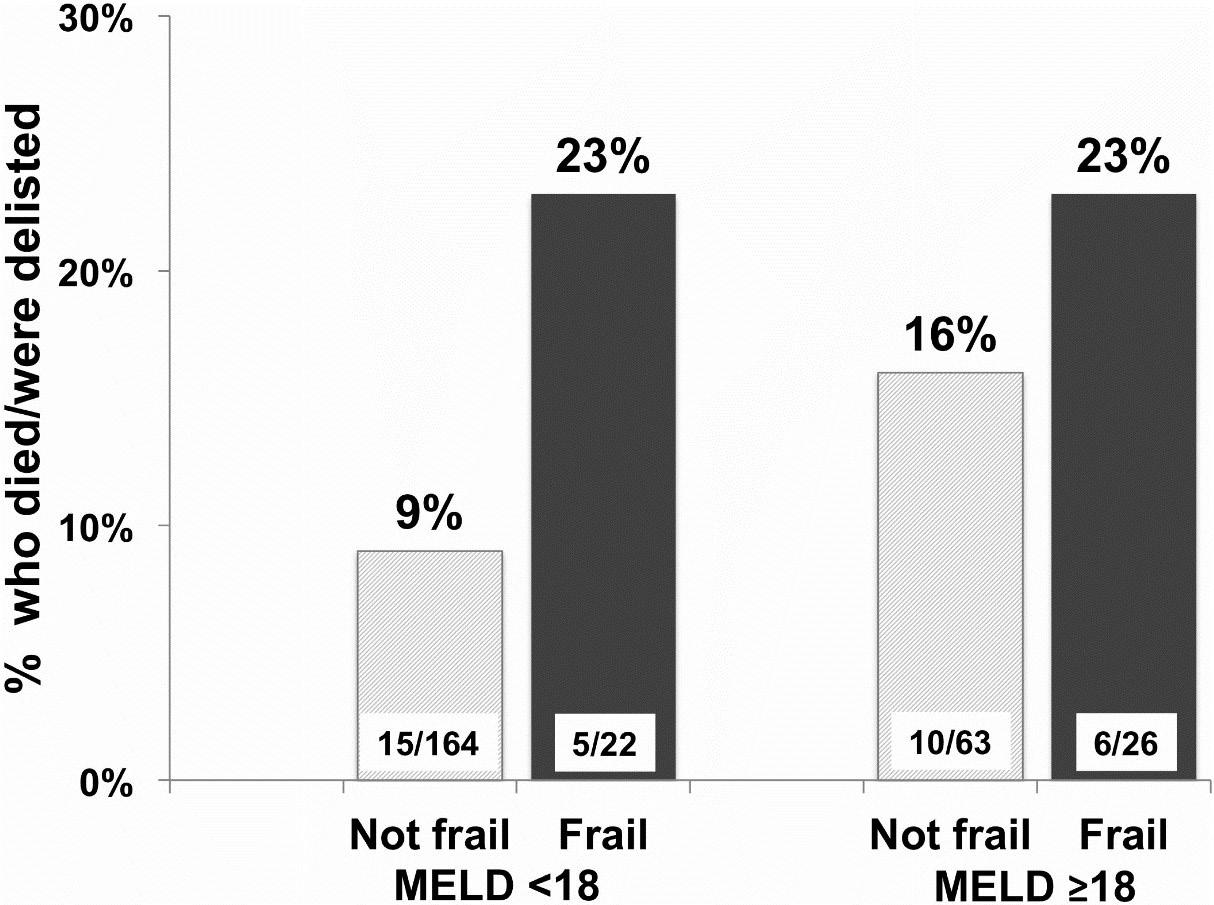
Skrøpelighet (“frailty”) er et begrep først brukt i geriatrien, og beskriver et syndrom av fysiologisk forfall som gir redusert reservekapasitet og økt sårbarhet mot helserelaterte stressfaktorer. Det forekommer hos opp mot 60% av pasienter med lever sykdom i endestadiet (ELS), og er assosiert med økt dødelighet (1). Kronisk systemisk inflammasjon sekundært til hepatisk inflammasjon, redusert muskelproteinsyntese grunnet syntesesvikt, økt muskelnedbryting grunnet hyperammonemi, endret smaksopplevelse grunnet encefalopati, og anoreksi/tidlig metthetsfølelse grunnet ascites er alle leverspesifikke årsaker som bidrar til skrøpelighet. I tillegg svekkes pasienter med ELS av kronologisk aldring, økt immobilitet og komorbiditet (2). Andel skrøpelige pasienter som settes på venteliste for levertransplantasjon (LTX) antas å øke i takt med at flere eldre og komorbide pasienter aksepteres for LTX. Skrøpelige pasienter har signifikant høyere Model for End Stage Liver Disease (MELD) score enn ikke-skrøpelige pasienter, og skrøpelighet er en sterk uavhengig prediktor for død på venteliste til LTX (3) (figur 1).
Sarkopeni er karakterisert av lav muskelstyrke og -masse (4). Det er
betydelig klinisk overlapp mellom skrøpelighet og sarkopeni, hvor sistnevnte både er en risikofaktor for, og den viktigste komponenten i skrøpelighetssyndromet. Sarkopeni er assosiert med økt risiko for levermessig dekompensering, encefalopati og infeksjon, og representerer en uavhengig risikofaktor for død hos pasienter med levercirrhose (5).
Etiologi
Sarkopeni er en multifaktoriell tilstand, og skyldes en kombinasjon av feil- og/eller underernæring, redusert fysisk aktivitet, leverdysfunksjon, hypogonadisme og systemisk inflammasjon. Flertallet pasienter med dekompensert cirrhose er feilernært (6), noe som vanligvis skyldes en kombinasjon av redusert appetitt, malabsorpsjon, medikamenter og fasteperioder/proteintap i forbindelse med diagnostiske og terapeutiske prosedyrer. Ved cirrhose vil faste over natten gi økt glukoneogenese og medføre at de forgrenede aminosyrene leucin, isoleucin og valin brukes som energikilde (7). Dette reduserer “mechanistic target of rapamycin complex 1” (mTORC1)signalering og gir økt autofagi, som igjen bidrar til sarkopeniutvikling. Ved aldersrelatert sarkopeni forekommer «anabol resistens», dvs. redusert muskelsynteserespons på inntak av aminosyrer eller trening. En lignende
mekanisme er foreslått hos pasienter med ELS, men ingen studier har undersøkt dette eksplisitt.
Hos pasienter med cirrhose vil forhøyet ammoniakk som ledd i manglende hepatisk eliminasjon og/eller shunting gi økt opptak av ammoniakk i muskelvev, aktivering av NF-kB og økte nivåer av myostatin. Myostatin er et myokin som hemmer muskeldannelse og vekst, og dermed bidrar til redusert muskelmasse og sarkopeni (8). Overforbruk av alkohol er også assosiert med økt nivå av myostatin og redusert signalering via mTORC1, som i sum gir sarkopeniutvikling. Hos mannlige pasienter med cirrhose er nivå av testosteron ofte lavt, som igjen kan bidra til økt tap av muskelmasse.
Diagnostikk
Klinisk blikk kan brukes med ganske god presisjon for å avgjøre om det foreligger skrøpelighet og sarkopeni, men flere metoder og scorings systemer er utarbeidet for objektivisering (7). Ved Avdeling for transplantasjonsmedisin, Rikshospitalet, brukes Liver Frailty Index (LFI), som er vist å kunne predikere mortalitet hos pasienter med ELS. Den vurderer håndgrepsstyrke, tid på å reise seg fra sittende til stående og balanseøvelser (antall sekunder med føtter ved siden av
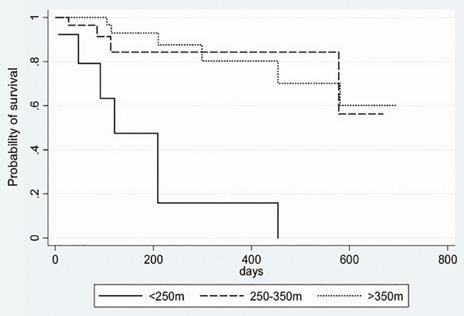
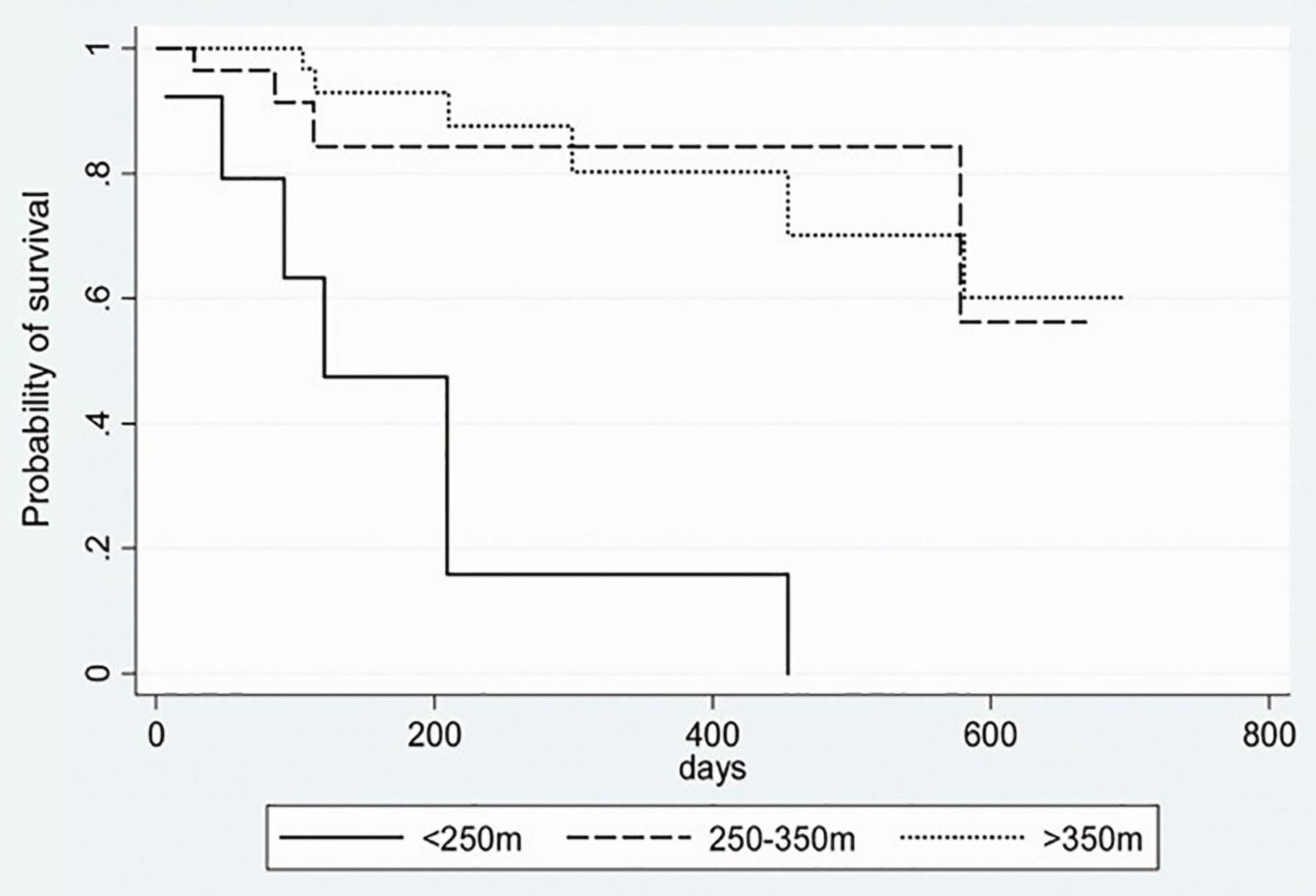
hverandre, i tandem og semitandem posisjon) (9). LFI score ≤ 3.2 indikerer at pasienten er robust, 3.3-4.4 preskrøpelig og ≥ 4,5 skrøpelig. Kalkulator finnes på https://liverfrailtyindex. ucsf.edu/. Andre lett tilgjengelige målinger er Psoas Muscle Index, dvs bilateralt psoasmuskelareal målt i nivå med virvel L3 i cm² dividert med pasientens høyde i meter², hvor <4.25 cm²/m² for menn og <3.64 cm²/ m² for kvinner tidligere er brukt som cut-off for sarkopeni hos pasienter med ELS (10). Dårlig gangdistanse på 6 minutters gangtest er assosiert med skrøpelighet hos pasienter med cirrhose og med økt mortalitet hos LTX-kandidater (11) (figur 2), men så vidt vi kjenner til er ingen eksakt cutoff grense for skrøpelighet etablert for denne testen. For diagnostikk av sarkopeni er European Working Group for Sarcopenias (EWGSOP-2) definisjon av sarkopeni mest brukt, og inkluderer lav muskelmasse målt ved Dual Energy X-ray Absorptiometry (DEXA) (menn <20 kg, kvinner <15 kg), lav håndgrepsstyrke (menn <27 kg, kvinner <16 kg) og lav fysisk funksjon (for eksempel tid brukt på 400 meter gange, hvor ≥ 6 minutter indikerer lav fysisk funksjon).
Behandling Majoriteten (85-95%) av pasienter som vurderes for LTX har inadekvat næringsinntak. Hovedfokus
ved behandling av sarkopeni ved ELS retter seg derfor mot optimalisering av ernæringssituasjonen. The European Society for Clinical Nutrition and Metabolism (ESPEN) anbefaler daglig inntak på 25-35 kcal/kg og 1,2-1,5 g/kg protein ut fra tørrvekt hos kompenserte pasienter. Pasienter med dekompensert cirrhose trenger ytterligere økt energi og proteininntak, og bør ha et daglig inntak på 35-40 kcal/kg og 1,5-2 g protein/kg daglig. Det anbefales å spise hyppige måltider og et sent karbohydratrikt kveldsmåltid, og lange fasteperioder inkludert lang nattfaste bør unngås. Vitaminmangel er vanlig hos pasienter med ELS, spesielt mangel på B-vitamin og fettløselige vitaminer. Pasientene bør derfor få tilskudd av multivitamin og eventuelt D vitamin basert på målinger av D-vitaminnivå. Pasienter med ELS har redusert evne til å omdanne kolekalsiferol til aktivt D vitamin, og bør ved mangeltilstand heller få tilskudd av aktivt D vitamin, kalsitriol. Tilskudd av forgrenede aminosyrer er ikke indisert hos pasienter med stabil leversykdom, men har vist effekt på overlevelse hos pasienter med ELS og hepatisk encefalopati (12). Pasienter som ikke klarer å dekke ernæringsbehovet selv bør få tilskudd, i første rekke enteral ernæring (EN) med energitett løsning. Unntaket er pasienter med hyper-
Figur 1. Frailty predikerer risiko for død på venteliste over MELD alene (9)
akutt leversvikt med encefalopati og høy ammoniakk, hvor EN kan utsettes 1-2 døgn til ammoniakknivået er under kontroll. Det er ikke grunnlag for å gi proteinrestriksjon ved kronisk hepatisk encefalopati (12). Dersom pasienter skal faste >12 timer i forbindelse med undersøkelser anbefales glukose iv 2-3 g/kg/døgn. Ved faste >72 timer bør det gis tilskudd av total parenteral ernæring (TPN). TPN er generelt andrevalg etter EN, men bør brukes når man ikke kommer i mål med andre tiltak eller når EN er kontraindisert. TPN kan både utløse og forverre leversykdom, og i verste fall bidra til forverring av cirrhose og økt transplantasjonsbehov. Dette er imidlertid sjelden, og frykt for TPNrelaterte komplikasjoner bør ikke hindre behandlingsforsøk med TPN hos pasienter hvor dette er indisert. Ved tegn på TPN-relatert leveraffeksjon må man se på muligheten for å seponere, alternativt bruke andre typer TPN som fiskeoljebaserte lipidemulsjoner (13). ESPEN fraråder bruk av perkutan endoskopisk gastrostomi (PEG) hos pasienter med INR >1.5, aktivert partiell tromboplastintid (APTT) > 50 s, eller alvorlig ascites (14), og er forbundet med fare for prosedyrerelaterte komplikasjoner eller ascitesvæskelekkasje. Behandling av ernæring i en ELS-setting kan være sammensatt, og pasientene bør
henvises til klinisk ernæringsfysiolog for optimalisering.
Kombinasjon av styrke- og kondisjonstrening med moderat intensitet øker muskelmasse- og funksjon hos pasienter med cirrhose uten at dette har gitt negative hendelser, selv om man teoretisk kunne tenke seg at dette ville gi akutt økning i ammoniakk, økt portaltrykk eller variceblødning (8). God preoperativ ernæringsmessig og fysisk tilstand gir raskere rehabilitering etter LTX. Det er viktig å komme tidlig til for å unngå, alternativt stabilisere og bedre, graden av sarkopeni før LTX. Enkelte svært skrøpelige pasienter
kan ha nytte av prehabilitering, enten ambulant eller ved innleggelse i rehabiliteringsinstitusjon, for å bedre fysiologisk reserve før kirurgi.
Resultater
Til tross for full normalisering av lever funksjon etter LTX, blir ikke alltid sarkopeni normalisert. Enkelte pasienter kan også utvikle de novo sarkopeni etter LTX. Patofysiologi bak dette fenomenet er ikke kjent, men feilernæring og redusert fysisk aktivitet grunnet bivirkninger fra medikamenter, residiverende infeksjoner, og gjentatte hospitaliseringer etter LTX kan tenkes å bidra (15). Kraftig vektoppgang etter LTX er
imidlertid også vanlig, og beskrevet hos omkring en fjerdedel av ikke tidligere overvektige pasienter 3 år etter LTX, uavhengig av steroidbruk (16). Årsaken kan være at pasienter som har vært oppfordret til å spise en høykaloridiett før LTX ikke endrer dette når de ikke lengre er i en katabol situasjon. Tap av afferente og efferente signalveier mellom lever og hypothalamus kan også bidra til redusert varighet av metthetsfølelse og overspising (16). Enkelte pasienter utvikler også høy kroppsmasse men lav muskelmasse, en fenotype som ligner sarkopen overvekt. Dette fenomenet er ikke korrelert til overspising, men etiologien bak er foreløpig ukjent (17).
Oppsummering
Skrøpelighet og sarkopeni er svært vanlig hos pasienter med ELS, og påvirker sykelighet og overlevelse før og etter LTX. Årsaken til høy forekomst av skrøpelighet og sarkopeni ved ELS er sammensatt og ikke fullt ut kartlagt. Tidlig diagnostikk med bruk av objektiviserte kartleggingsverktøy og behandling med fokus på optimalisert ernæring og fysisk aktivitet bedrer sykelighet og overlevelse ved ELS og LTX. Oppfølgning av ernæring og muskelstyrke bør derfor anses like viktig som tradisjonell oppfølgning med biokjemi og radiologi ved ELS.
Artikkelen ble først publisert i NGFNytt 3/24 og er gjengitt med tillatelse
Referanser
1. Lai JC, Rahimi RS, Verna EC, Kappus MR, Dunn MA, McAdams-DeMarco M, et al. Frailty Associated With Waitlist Mortality Independent of Ascites and Hepatic Encephalopathy in a Multicenter Study. Gastroenterology. 2019;156(6):1675-82.
2. Lai JC, Sonnenday CJ, Tapper EB, Duarte-Rojo A, Dunn MA, Bernal W, et al. Frailty in liver transplantation: An expert opinion statement from the American Society of Transplantation Liver and Intestinal Community of Practice. Am J Transplant. 2019;19(7):1896906.
3. Lai JC, Feng S, Terrault NA, Lizaola B, Hayssen H, Covinsky K. Frailty predicts waitlist mortality in liver transplant candidates. Am J Transplant. 2014;14(8):1870-9.
4. Cruz-Jentoft AJ, Bahat G, Bauer J, Boirie Y, Bruyere O, Cederholm T, et al. Sarcopenia: revised European consensus on definition and diagnosis. Age Ageing. 2019;48(4):601.
5. Dolgin NH, Martins PN, Movahedi B, Lapane KL, Anderson FA, Bozorgzadeh A. Functional status predicts postoperative mortality after liver transplantation. Clin Transplant. 2016;30(11):1403-10.
6. Campos-Varela I, Gomez-Gavara C, Augustin S. Recommendations and Guidance on Nutritional Supplementation in the Liver Transplant Setting. Transplantation. 2021;105(12):2528-37.
7. Liapakis A, Morris E, Emre S. Frailty in liver transplantation: A comprehensive review. Hepatol Forum. 2021;2(2):80-8.
8. Allen SL, Quinlan JI, Dhaliwal A, Armstrong MJ, Elsharkawy AM, Greig CA, et al. Sarcopenia in chronic liver disease: mechanisms and countermeasures. Am J Physiol Gastrointest Liver Physiol. 2021;320(3):G241G57.
9. Lai JC, Covinsky KE, Dodge JL, Boscardin WJ, Segev DL, Roberts JP, et al. Development of a novel frailty index to predict mortality in patients with end-stage liver disease. Hepatology. 2017;66(2):564-74.
10. Rodge GA, Goenka U, Jajodia S, Agarwal R, Afzalpurkar S, Roy A, et al. Psoas Muscle Index: A Simple and Reliable Method of Sarcopenia Assessment on Computed Tomography Scan in Chronic Liver Disease and its Impact on Mortality. J Clin Exp Hepatol. 2023;13(2):196-202.
11. Carey EJ, Steidley DE, Aqel BA, Byrne TJ, Mekeel KL, Rakela J, et al. Six-minute walk distance predicts
mortality in liver transplant candidates. Liver Transpl. 2010;16(12):1373-8.
12. Abdelsayed GG. Diets in Encephalopathy. Clin Liver Dis. 2015;19(3):497-505.
13. Mitra A, Ahn J. Liver Disease in Patients on Total Parenteral Nutrition. Clin Liver Dis. 2017;21(4):687-95.
14. Bischoff SC, Bernal W, Dasarathy S, Merli M, Plank LD, Schutz T, et al. ESPEN practical guideline: Clinical nutrition in liver disease. Clin Nutr. 2020;39(12):353362.
15. Leunis S, Vandecruys M, Van Craenenbroeck AH, Cornelissen V, Bogaerts S, De Smet S, et al. Sarcopenia in end-stage liver disease and after liver transplantation. Acta Gastroenterol Belg. 2023;86(2):32334.
16. Richards J, Gunson B, Johnson J, Neuberger J. Weight gain and obesity after liver transplantation. Transpl Int. 2005;18(4):461-6.
17. Schutz T, Hudjetz H, Roske AE, Katzorke C, Kreymann G, Budde K, et al. Weight gain in longterm survivors of kidney or liver transplantation-another paradigm of sarcopenic obesity? Nutrition. 2012;28(4):378-83.
Leading Experts from EMEA Answer Procedure-Related FAQs.
There’s nothing quite as effective as learning from experts in their respective fields. With our new Lung-Term Learning initiative, we want to further elevate the standard of care by creating a pulmonology community and broaden our offer for education beyond our medical expert trainings.
We would like to invite you to watch our “Lung-Term Learning” videos, where renowned experts will be sharing procedure-and education-related tips and tricks on how to further improve procedural outcomes and to help in our efforts to further elevate the standard of care in lung cancer diagnosis and staging.
Check out the first episodes of our FAQ series and stay tuned for upcoming videos.
www.olympus.eu/pulmonology
#LoveForLungs

Obstipasjon er en av våre vanligst forekommende gastroenterologiske tilstander, med en forekomst på 1-20 % hos voksne, avhengig av hvordan det blir spurt og i hvilken befolkningsgruppe. I den eldre befolkningen ses obstipasjon hos ca. 20 % av de som er oppegående og hos opp til 50% blant personer innlagt på institusjon (1). I denne store gruppen, hvor de fleste vil ha livsstilsårsaker til sin obstipasjon, gjemmer det seg imidlertid også nevroinflammatoriske og sekundære tilstander som vil kreve livslang, avansert behandling.
Johan Lunding, overlege, dr. med, Diakonhjemmet Sykehus
Symptombeskrivelse Vi deler opp obstipasjon ut fra om pasientene har normal eller langsom tarmtransit, og om en forstyrret bekkenbunnfunksjon påvirker symptombildet.
Rome IV-kriteriene (2) for funksjonelle mage-tarm-sykdommer (jf. figur 1) forsøker, ut fra symptombeskrivelsen, å skille kronisk funksjonell obstipasjon fra forstoppningsdominert irritabel tarmsyndrom og obstipasjon sekundær til sykdom og legemidler.
Rome IV-kriteriene er først og fremst ment som tilstandsdefinisjoner for inkludering til kliniske studier, mens vi i en klinisk hverdag må forsøke å tolke dem for å passe med det pasienten beskriver. Kriterienes fokus på heterogeniteten i symptom -
Funksjonell obstipasjon
Tids-kriterier
Symptom oppfylte under siste 3 mån
Symptomdebut mer enn 6 mån siden
Spesifikke kriterier:
≥2 av:
bildet gir likevel en pekepinn om at obstipasjon forstås ulikt av ulike mennesker. Det er dermed viktig å få pasienten til selv å beskrive hva de mener. Mens vi som leger ofte forsøker få pasienten å oppgi hvor mange dager som har gått mellom tarmtømmingene, er det den harde konsistensen, eller behovet for å trykke, som er det sentrale hos mange pasienter. Ofte beskriver pasientene avføring som harde klumper eller klumper som så vidt holder sammen. Dette tilsvarer type 1 og 2 på Bristol stool form scale, som beskriver avføringsformen fra harde klumper, type 1, til vandig, type 7 (3). Det er også konsistensen som vil ha betydning for hvilken utredning en bør gjøre, hvilken behandling en bør velge og hva pasienten vurderer behandlingseffekten ut fra.
Gjelder minst 1 av 4 defekasjoner
IBS-kriteriene ikke oppfylt
Sjelden eller aldri løs avføring uten laksermiddel
Trykke
Klumper eller hard avføring
Følelse av ufullstendig tømming
Følelse av anorektal blokkering
Manipulering for att få ut avføringen
Mindre enn 3 tarmtømminger ukentlig
Forutsetting: Ikke sekundært til annen sykdom
Livsstilsfaktorers betydning for tarmtransit
Transit gjennom tarmkanalen varierer blant annet med hva en spiser, drikker og hvor mye en beveger seg. Fravær av fiber og gassproduserende matvarer vil forlenge transit. De som har byttet ut det grove norske brødet mot bagetter og croissanter mens de har vært på ferie, skjønner nok hva det innebærer. Det mest ekstreme eksempelet på dette ser vi ved anorexia nervosa da mangel på både kalorier og fiber gir svak peristaltikk, med markert forlenget transit-tid. Ved stort inntak av gassproduserende matvarer, som kål, løk, frukt og søtningsmiddel vi finner i halspastiller og tyggis, forventes det at konsistensen blir løsere og tømmingene hyppigere. Disse matvarene inneholder FODMAP, dvs. Fermenter-
Irritabel tarm syndrom (IBS)
Tids-kriterier
Symptom oppfylte under siste 3 mån
Symptomdebut mer enn 6 mån siden
1.Intermittente episoder med buksmerte
2.Assosiert med minst 2 av følgende:
a) Endres vid defekasjon (mer/mindre smerte)
b) Påvirkes av endring i avføringsfrekvens
c) Påvirkes av endring i avføringskonsistens
Figur 1: Rome IV kriteriene for Funksjonell obstipasjon sammenliknet med kriteriene for Irritabel tarmsyndrom (IBS) (2)
Analgetika
NSAID
Opioider
Anticholinerge
Antipsykotika
Antihistaminer (H1)
Tricykliske
antidepressiva
Scopolamin
Antiepileptika
Gabapentin/pregabalin
Fenytoin
bare oligo- d i-, m ono-sakkarider o g p olyoler, som er karbohydrater som bare delvis absorberes av tynntarmen og dermed gir mye rester for mikrobiotaen i tykktarmen å jobbe med, med følgende produksjon av gass og bioaktive stoffer som kan påvirke tarmfunksjonen. FODMAP er et viktig konsept innen funksjonelle magetarmsykdommer, da begrensing av inntaket brukes for å redusere symptomnivået ved IBS. Også pasienter med funksjonell obstipasjon vil ha nytte av å forstå hvordan FODMAP påvirker.
Legemidlers betydning for tarmtransitt
Mange legemiddelgrupper kan bidra til en langsommere transit eller nedsatt sekresjon i tarmen, som gir tørrere avføring. Opioider gir langsommere passasjetid ved å forstyrre koordinasjonen i hele tarmen. I tykktarmen gir opioider færre propulsive kontraksjoner, uten påvirkning på retroperistaltikken, som skal holde distale delen av tarmen tom. Legemidler med antikolinerge bivirkninger (antipsykotika, antihistaminer, tricykliske antidepressiva, spasmolytika), antihypertensiva (ca-blokkere, betablokkere, alfaadrenerge agonister), diuretika og NSAID, mineraler (jern, calsium), parkinson-legemidler og cytostatika er eksempler på lege midler som forsinker tarmenpassasjen (figur 2) (4).
Antihypertensiva
α-adrenerge agonister (klonidin)
β-blokkere
Kalsium-blokkere
Diuretika
Elektrolytter: Kalsium
Jern
Cellegifter
Vincristin
Cyclofosfamid
Sekundære årsaker til obstipasjon Mange sykdommer og tilstander vil kunne gi obstipasjon som et
Tarmstoppende
Loperamid (opioid)
Bindere
Cholestyramine
Parkinson-legemiddel
Antiemetika
Ondasetron
Metoklopramid (antipsyk)
sekundært fenomen, uavhengig av medisinering. Systemsykdommer som påvirker sentralnervesystemet eller det autonome nervesystemet vil kunne affisere det enteriske nerve system. Eksempler på dette er Parkinsons sykdom som kan gi obstipasjon og dysfagi, med påvisbare Levi-legemer i tarmens slimhinne, flere år før de velkjente skjelvingene begynner. MS vil kunne gi obstipasjon både ved å påvirke innerveringen av bekkenbunnen og tarmens peristaltikk. Sykdommer som påvirker muskelfunksjon, som amyloidose og dermatomyositt, vil kunne gi en svakere kontraktilitet i glatt muskulatur og dermed mindre effektiv propulsjon. Mange tilstander kan gi obstruksjoner i tarmen både i dess forløp, som kreft og divertikulose, og i dess utløp, som rektumprolaps og analfissurer (figur 3).
Den geriatriske pasient
Skal den aldrende pasient vurderes annerledes enn andre voksne?
Magetarmfunksjonen påvirkes ikke i utgangspunktet av alder, men alder medfører ofte en endring av kost og livsstil, en økt forekomst av sykdommer og medisinering, som alle kan bidra til obstipasjon. Risikoen for sykdom i tarmen øker, særlig kreftrisikoen.
Enda viktigere enn for den yngre pasient er det å forstå hva den eldre pasienten mener når pasienten klager over obstipasjon. Ordene som velges er ofte annerledes, med omskrivnin-
ger og antydninger, som kan være ukjent for en yngre lege. Hos eldre pasienter med kognitiv svikt eller nedsatt kommunikasjonsevne, vil ofte obstipasjon kunne gi uspesifikke tegn som agitasjon, funksjonssvikt eller appetittløshet.
Immobilitet, redusert væskeinntak og diettendringer, med mindre mengder fiber, er vanlig hos eldre. Det er viktig å spørre om dette og forsøke, innenfor mulighetenes grenser, å korrigere. Økt inntak av koffein gir stimulering av tarmens motorikk. Regelmessige dovaner vil kunne regulere avføringen. Slike enkle råd har lav evidens, men regnes likevel som relevante (5).
Utredning
Alarmsymptomer
Nytilkommen obstipasjon regnes som et alarmsymptom med hensyn til tykktarmskreft. Særlig gjelder dette ved symptomdebut over 50 års alder. Ved redusert diameter i av føringen, obstruktive symptomer, rektal prolaps, blødning, positiv fekal Hb, anemi eller vekttap bør en vurdere koloskopi. Hvis en koloskopi av god kvalitet allerede blitt utført under de seneste årene endrer på prioritet av slike nyoppståtte fenomen.
Oro-anal transit
En passasjetid som varierer med diett- og livsstilsvaner kalles normaltransit og er det vi vanligvis ser ved tilfeldig og funksjonell obstipasjon. Den overlapper med obstipasjonsdominert IBS hvor
Mekanisk obstruksjon
Colorektal cancer
Divertikulose
Striktur
Kompresjon fra tumor/annet
Stort rektocele
Megacolon
Postoperativ status
Analfissur (reflektorisk spasm)
Nevrologisk sykdom/nevropati
Autonom nevropati
Stroke
Kognitiv svikt
Depresjon
MS
Parkinson
Ryggmargspatologi
Endokrine/metabole tilstander
Kronisk nyresvikt
Dehydrering
Diabetes mellitus
Tungmetaller
Hypercalsemi
Hypermagnesemi
Hyperparathyroidisme
Hypokalemi
Hypomagnesemi
Hypothyroidisme
Multippel endokrin neoplasi II
Porphyri
Myopati
Amyloidose
Dermatomyositt
Sklerodermi/ Systemisk sklerose
Gastrointestinale tilstander
IBS
Abscess
Analfissur
Fistel
Hemorroider
Levator ani syndrom
Megacolon
Proctalgia fugax
Rektalprolaps
Rektocele
Volvulus
skillelinjen vanligvis er forekomst av smerte, som er karakteristisk for IBS. Det innebærer at en normaltransit obstipasjon kan forbedres av kostog livsstilsråd.
En kronisk langsom transit, med obligat behov for motorikkstimulerende laksermiddel, gir mistanke om slow transit obstipasjon. Her vil avføringsmønsteret være uavhengig av kostfaktorer, væskeinntak og grad av bevegelse. Det er en kronisk alvorlig nevrogastroenterologisk tilstand med sin årsak i forstyrret koordinasjon (nevropati) eller muskelkraft (myopati) i tarmveggen. Peristaltikken kan dermed enten være for svak og langsom eller kraftig og ukoordinert. Slow transit obstipasjon ses som isolert fenomen, eller sammen med tilsvarende forstyrrelse av andre deler av magetarmkanalen. Det kan være sekundært til sykdom i nervesystem eller muskulatur eller være en idiopatisk tilstand. Etiologisk behandling er som regel vanskelig.
Transit-tiden gjennom magetarmkanalen måles med en enkel undersøkelse hvor pasienten får innta et antall røntgentette markører som påvises med røntgen abdomen. Med den hyppigst forekommende kommersielt tilgjengelige testen tas røntgenbildet på dag 7 etter inntak av 10 markører daglig i 6 dager. Antallet retinerte markører beregnes med en enkel formel gir transittiden i dager. Øvre normalgrense for oro-anal transit er 4 ,0 døgn for kvinner, og 2,2 døgn for menn. Undersøkelsen
kan gi en indikasjon på hvilken del av tarmen som har ineffektiv propulsjon, eller om det foreligger et tømmingshinder. En forutsetning for en transitmåling er at pasienten under undersøkelsen ikke bruker legemiddel som forsinker passasjetiden, fremfor alt opioider. Hvis pasienten bruker legemiddel som forsinker transit, men som ikke kan unngås under undersøkelsen, f.eks. legemiddel for Parkinson, må en forsøke å tolke svaret med dette forbehold.
Bekkenbunnsforstyrrelser Nedsatt kraft og/eller koordinasjon av bekkenbunnens skjelettmuskulatur, slimhinneprolaps, rektocele, enterocele og andre mekaniske hinder i bekkenet kan komplisere både normaltransit- og slow transit obstipasjon. Det er en ikke helt uvanlig årsak til at en habituell lavgradig forstoppelse over noen uker plutselig forverres. Det er vanlig er at den kommer raskt etter fødselsskader. Tilstanden kan imidlertid også komme etterhvert hos den eldre kvinne når muskulaturen, som tidligere har kunnet kompensere for fødsels skaden, med alderen blir svakere. Hos unge kvinner som ennå ikke har født, eller hos unge menn, bør en mistenke medfødt bindevevssykdom, f.eks. Ehlers Danlos Syndrom, hvis en ser slike hinder. Pasienten vil ofte beskrive at det er vanskelig å trykke ut avføringen selv om den er myk. I noen tilfeller må de hjelpe til med å trykke med en finger mot perineum eller fra vagina. Å ikke påvise bekkenbunnsforstyrrelser som
Dietære
Slanking
Uttørking
Lavt fiberinntakt
Anorexia nervosa
Demens
Depresjon
Diverse
Hjertesvikt
Degenerativ leddsykdom
årsak til en forverret obstipasjon vil ofte lede til eskalerende legemiddelbruk og unødvendige utredningsforløp.
Bekkenbunnsforstyrrelser utredes i første linje ved palpasjon, hvor tonus og muskulær kontroll av sfinkter og muskulus puborektalis vurderes. En utvidet vurdering kan gjøres av proktolog med inspeksjon av anorektums strukturer, med og uten trykk under anorektoskopi. En røntgen defekografi, hvor et barium-klyster tømmes under gjennomlysning, gir god oversikt over den dynamiske rektumfunksjonen, antyder dyskoordinasjon i bekkenbunnens muskler og påviser mekaniske hinder som prolaps og invaginasjoner. Tilgangen på defekografi er begrenset i Norge, men vil i mange tilfeller kunne erstatte kirurgens vurdering, særlig for å utelukke patologi. Anorektal ultralyd kan behøves for vurdering av underliggende anatomiske skader. Anorektal manometri (trykkmåling) vil objektivt kunne dokumentere den muskulære koordinasjonen, noe som er relevant når flere profesjoner er involvert i behandlingen. I mange land anbefales en funksjonell test, «balloon expulsion test», hvor en latexballong på tid trykkes ut rektum, men resultatets validitet er omdiskutert (4).
Behandling av obstipasjon
Anbefalinger for behandling av obstipasjon skiller ikke mellom eldre og andre voksne. De samme rådene og legemidlene er aktuelle å bruke,
men en må naturligvis ta hensyn til andre legemidler pasienten står på. Hvis en kan identifisere et hemmende legemiddel (figur 1) (4), som er mulig å redusere eller aller helst seponere, vil det ofte kunne få pasientens tarmvaner tilbake til slik de var før oppstart. I tilfeller med opioider, finnes det perifert virkende anti- opioider både i tablettform (Naloxegol, Naldemedin) og for subkutan injeksjon (Metylnaltrexonbromid) som kan reversere alle nivåer av opioidpåvirkning på tarmen uten stor påvirkning av den sentrale smertelindrende effekten.
Legemidlene kan deles opp etter virkningsmekanisme, i mykgjørende og motorikkstimulerende. De må gjerne kombineres for å oppnå bedre propulsjon, men det er som oftest ikke noe poeng å blande to preparater innenfor samme gruppe.
Vanligvis startet man behandlingen av obstipasjon med et mykgjørende legemiddel. Mildest effekt har vannløselige fiber, enten som komponent i maten, i form av fast inntak av havre eller linfrø, eller som lege middel i form av pulver av linloppefrø. Vannløselige fiber binder vann til en gelform som holder seg stabil gjennom tarmkanalen. Jo høyere dose en bruker, jo mer grøtet blir avføringen. Uløselige fiber, som hvetekli, vil ikke binde vann på samme måte og vil ofte fermenteres med gassproduksjon som ofte oppleves som hemmende.
Mer lakserende effekt får en av lactulose, et for tarmen ufordøyelig sukker som osmotisk binder vann. Det er et billig preparat som er lett å administrere, men hvor bruk hemmes, av den gassproduksjon som skjer ved bakteriell fermentering. Et godt alternativ er makrogol, også dette et stort vannbindende molekyl som holder seg i flytende form, men uten å fermenteres i noen større utstrekning. Jo høyere dose en bruker av lactulose og makrogol, jo mer flytende blir avføringen.
Når ikke de osmotiske legemidlene gir tilstrekkelig effekt, eller gir for mye bivirkninger, kan en forsøke Linaklotid tabletter. Linaklotid binder til de samme klorkanalene som
kolera-bakterier og gir en kraftig økt sekresjon i tynntarm. Den lakserende effekten tilsvarer 2-3 doser makrogol daglig og kommer innen 2-4 timer etter inntak av en tablett. Legemiddelet skal brukes daglig og kan skrives på blå resept av gastroenterolog ved IBS-diagnose, og kan søkes for blå resept ved andre obstipasjonsformer. Det har en oppstartseffekt, hvor effekten den første uken er kraftigere enn den senere vil være, noe pasienten bør informeres om.
Medisinsk parafin mykgjør avføringen ved å gjøre den fettet og lettglidende. Det får regnes som et spesialpreparat som brukes fremfor alt ved obstruktiv problematikk.
Hvis de mykgjørende legemidlene er ineffektive bør en legge til motorikkstimulering. Særlig ved påvist slow transit obstipasjon, må en regne med at pasienten vil trenge et motorikkstimulerende laksermiddel resten av livet. Klassiske irritative laksermiddel, f.eks. senna eller pikosulfat, gir svært kraftig peristaltikk i tykktarm etter at de har blitt fermentert av mikrobiotaen. Dette gir en forsinkelse på 4-8 timer fra inntak til en effekt som ofte er så kraftig at store deler av tarmen tømmes for innehold. Siden neste spontane tarmtømming kan forventes først etter 2-4 dager, er disse midlene vanskelige i bruk, og får nok betraktes mest som et tømmingsmiddel når defekasjonen har uteblitt over lenger tid. Det går an å dosere disse preparatene lavere for en mildere effekt, men det er vanskelig å få en forutsigbar effekt. Irritative laksermiddel har ingen dokumentert negativ langsiktig effekt på tarmens peristaltikk.
Et mer skånsomt og moderne alternativ til irritative laksermiddel, er prucaloprid som binder til en serotoninreseptor i tarmen og gir motorikkstimulering allerede innen et par timer fra å ha tatt tabletten. Middelet skal brukes daglig ved kronisk obstipasjon (6). I kombinasjon med et mykgjørende middel vil det i de fleste tilfeller fungere godt, selv ved en slow transit obstipasjon. I de senere år har det blitt lettere å søke prucaloprid på blå resept ved kronisk obstipasjon, forutsatt at det kroniske
behovet kan dokumenteres og andre legemidler er prøvd på forhånd. Ved opioidforårsaket forstoppelse vil det, når ikke enkel lakserende behandling hjelper, være en fordel å reversere med et antiopioid, før en legger til motorikkstimulerende legemidler.
Hos eldre multisyke eller skrøpelige pasienter må en tenke seg om. Osmotisk aktive laksermidler kan bidra til dehydrering, nyresvikt, og elektrolyttforstyrrelser da de trekker vann fra blodbanen. Noen midler, særlig parafin, anses risikable med hensyn til aspirasjon.
Ved bekkenbunnsdysfunksjon er legemiddelbehandling vanskelig, utover at en mykere avføring er lettere å trykke ut. Førstevalg for behandling er bekkenbunnsfysioterapi. Fysioterapien styrker muskulatur og bedrer koordinasjon for å forbedre defekasjonsevnen. Norsk Fysioterapiforbund har lister over lokale spesialister på bekkenbunnsfysioterapi som pasientene kan henvende seg til (7).
Hos noen pasienter med bekkenbunnsdysfunksjon eller slow transit obstipasjon, vil transanal irrigasjon være en behandlingsmulighet. Med spesialdesignet utstyr skylles innhold i rektum og distale del av tykktarmen ut med kranvann.
Kirurgisk intervensjon, kolektomi med ileorektal anastomose, kan i unntakstilfeller bli aktuelt ved slow transit obstipasjon som har vist seg refraktær for intensiv lakserende behandling.
Referanser:
1 Walter, S., Hallböök, O., Gotthard, et al. A Population-based Study on Bowel Habits in a Swedish Community: Prevalence of Faecal Incontinence and Constipation. Scandinavian Journal of Gastroenterology, 37(8), 911–916. (2002).
2 ROME IV Diagnostic Criteria Disorders of GutBrain Interaction https://theromefoundation.org/ resources/rome-iv-criteria-booklet/
3 Lewis, S. J., Heaton, K. W. Stool Form Scale as a Useful Guide to Intestinal Transit Time. Scandinavian Journal of Gastroenterology, 32(9), 920–924. (1997)
4 World Gastroenterology Organisation Global Guidelines Constipation—A Global Perspective. Journal of Clinical Gastroenterology 45(9):p 838, October 2011. https://www.worldgastroenterology. org/guidelines/constipation/constipation-english
5 Schuster BG, Kosar L, Kamrul R. Constipation in older adults.Canadian Family Physician Feb 2015, 61 (2) 152-158;
6 Camilleri M, Ford AC, Mawe GM et al, Chronic constipation. Nat Rev Dis Primers. 2017 Dec 14;3:17095. doi: 10.1038/nrdp.2017.95. Review
7 Norsk Fysioterapiforbund - https://fysio.no/ kvinnehelse
som tillegg til diett med redusert kaloriinntak og økt fysisk aktivitet1
gjennomsnittlig vektreduksjon opprettholdt i 2 år*2,3
Mer enn 1/3 av pasienter gikk ned 20 % eller mer med Wegovy®**2,3
Les mer på www.wegovy.no
* STEP 5: -2,6 % for placebo og -15,2 % for Wegovy®, som tillegg til diett med redusert kaloriinntak og økt fysisk aktivitet for begge grupper (500 kcal/dag + 150 min/ uke fysisk aktivitet + individuell oppfølging hver 4. uke) 12,6 % forskjell fra placebo, [KI 95 % -15,3; -9,8], p < 0,0001.2,3
** STEP 5: I uke 104 etter baseline oppnådde 74,7 % av pasientene et vekttap på ≥ 5 % (primært endepunkt), 59 % et vekttap på ≥ 10 % og 50 % et vekttap på ≥ 15 % (bekreftende sekundære endepunkt). 36 % av pasientene oppnådde et vekttap på ≥ 20 % ( supporterende sekundært endepunkt)2,3
Novo Nordisk Norway AS Nydalsveien 28 · NO-0484 Oslo Telefon: + 47 22185050 · Kundeservice: +47 2218 5051 · www.novonordisk.no
Indikasjon:
Voksne: Tillegg til diett med redusert kaloriinntak og økt fysisk aktivitet for vektkontroll, inkl. vekttap og vedlikehold av vekt, hos voksne med initial BMI ≥ 30 kg/m2 (fedme), eller ≥ 27 til < 30 kg/m2 (overvekt) ved forekomst av minst én vektrelatert komorbiditet, som dysglykemi (prediabetes eller diabetes mellitus type 2), hypertensjon, dyslipidemi, obstruktiv søvnapné eller kardiovaskulær sykdom.
For resultater fra studier vedrørende kardiovaskulær risikoreduksjon, fedmerelatert hjertesvikt og populasjoner som ble undersøkt, se pkt. 5.1 i Wegovy ® preparatomtale.
Ungdom (≥ 12 år): Tillegg til diett med redusert kaloriinntak og økt fysisk aktivitet for vektkontroll hos ungdom ≥ 12 år med fedme1 og kroppsvekt > 60 kg. Behandling skal seponeres og reevalueres etter 12 uker dersom ungdomspasienten ikke oppnår en reduksjon i BMI på minst 5 % etter 12 ukers behandling med (Wegovy ®) 2,4 mg eller maks. tolererte dose.1
Fedme (BMI ≥ 95-prosentil) som definert i kjønns- og aldersspesifikk BMI-vekstkurve (CDC.gov).
Wegovy® – utvalgt sikkerhetsinformasjon
De hyppigst rapporterte bivirkningene var gastrointestinale (svært vanlige, ≥ 1/10), inkludert kvalme, diaré, forstoppelse, oppkast og magesmerter. Generelt milde eller moderate i alvorlighetsgrad, og av kort varighet. Årsak til seponering hos 4,3 %. Kan forårsake dehydrering som i sjeldne tilfeller kan forverre nyrefunksjon. Unngå væskemangel
• Andre svært vanlige (≥ 1/10) bivirkninger: Hodepine, fatigue
• Andre vanlige (≥ 1/100 til < 1/10) bivirkninger: Dysestesi, dysgeusi, svimmelhet, gastritt, gastroøsofageal reflukssykdom, dyspepsi, raping, flatulens, abdominal distensjon, gallestein, hårtap, reaksjoner på injeksjonsstedet. Hos pasienter med diabetes type 2: hypoglykemi (særlig i kombinasjon med insulin eller sulfonylurea), retinopati
Gallestein: Vanlig bivirkning ved bruk av semaglutid. Ble rapportert hos 1,6 % av de som fikk semaglutid og 1,1 % hos de som fikk placebo. Førte til kolecystitt hos 0,6 % og 0,3 % hos de som fikk henholdsvis semaglutid og placebo
• Pankreatitt: 0,2 % for semaglutid og < 0,1 % for placebo. I den kardiovaskulære endepunktsstudien SELECT var frekvensen av akutt pankreatitt, bekreftet ved avklaring (adjudikering), 0,2 % for semaglutid og 0,3 % for placebo. Ved mistanke bør semaglutid seponeres. Semaglutid skal ikke gjenopptas etter bekreftet pankreatitt. Forsiktighet bør utvises hos pasienter som tidligere har hatt pankreatitt
• Tarmobstruksjon: En alvorlig form for forstoppelse med tilleggssymptomer som magesmerte, oppblåsthet og oppkast. Rapportert med ukjent frekvens etter markedsføring
Puls: Gjennomsnittlig økning på 3 slag per minutt observert
• Skal ikke brukes av gravide eller ved amming. Semaglutid skal på grunn av den lange halveringstiden seponeres minst 2 måneder før en planlagt graviditet
• Forsiktighet bør utvises hos pasienter med inflammatorisk tarmsykdom eller gastroparese Ungdom (12 - < 18 år): Generelt var frekvens, type og alvorlighetsgrad av bivirkninger hos ungdom tilsvarende det som sees hos voksne. Gallestein ble sett hos 3,8 % av pasientene behandlet med Wegovy® og 0 % behandlet med placebo. Ingen effekt på vekst eller pubertetsutvikling ble funnet etter 68 uker med behandling
Dosering – én gang per uke
Alder
Nyrefunksjon
Hjertesvikt
Leverfunksjon
Kan benyttes uten dosejustering
Voksne og ungdom ≥ 12 år
Begrenset erfaring hos pasienter ≥ 85 år
Lett og moderat nedsatt eGFR > 30 ml/min 1,73m2
Anbefales ikke
Barn/ungdom under 12 år
Alvorlig nedsatt, eller terminal nyresykdom eGFR < 30 ml/min 1,73m2
NYHA klasse I-III NYHA klasse IV
Lett og moderat nedsatt Forsiktighet bør utvises
Alvorlig nedsatt
Diabetes Diabetes type 2 Diabetes type 1
Wegovy® skal injiseres subkutant i abdomen, i låret eller i overarmen og administreres én gang per uke når som helst i løpet av dagen, til måltid eller utenom måltid. For å redusere sannsynligheten for gastrointestinale symptomer bør dosen trappes opp i løpet av en 16-ukers periode til en vedlikeholdsdose på 2,4 mg én gang per uke.
For ungdom i alderen 12 år og eldre benyttes samme doseopptrappingsplan som for voksne. Dosen bør økes opptil 2,4 mg, eller til maksimalt tolererte dose oppnås. Se preparatomtale for mer informasjon om dosering.
Reseptgruppe og pris
Legemiddelgruppe: GLP-1-analog Reseptgruppe: C ATC-nr.: A10B J06
Pakninger og priser: 0,25 mg: 1,5 ml (ferdigfylt penn) kr 1773,50. 0,5 mg: 1,5 ml (ferdigfylt penn) kr 1773,50. 1 mg: 3 ml (ferdigfylt penn) kr 1773,50. 1,7 mg: ml (ferdigfylt penn) kr 2597,20. 2,4 mg: 3 ml (ferdigfylt penn) kr 3189,40 (Priser per desember 2024).
Behandling med Wegovy® er ikke refundert og kan ikke skrives på blå resept
For individuell stønad se vedlegg 1 til folketrygdloven § 5-14 (legemiddellisten) på www.helsedirektoratet.no4
Referanser 1. Wegovy® SPC, avsnitt 4.1 2. Wegovy® SPC, avsnitt 5.1 3. Garvey WT, Batterham RL, Bhatta M, et al. Two-year effects of semaglutide in adults with overweight or obesity (STEP 5) Nature medicine 2022; 28(10), 2083-2091 4. Informasjon om vilkår for individuell refusjon er hentet fra: https://www.helsedirektoratet.no/rundskriv/kapittel-5-stonad-vedhelsetjenester/vedlegg-1-til--5-14- legemiddellisten/virkestoffer/semaglutid (Lest 06.12.2024)




Ny teknologi og kunnskap endrer hvordan vi utreder og behandler pasienter med kronisk koronarsyndrom. CT hjerte og annen ikke-invasiv bildediagnostikk tar over som hjørnesteinen i diagnostikken. Behandlingen bør fokusere på en aggressiv tilnærming til livsstilsendringer og medikamentell behandling, også i asymptomatiske perioder. Revaskularisering gir ingen prognostisk gevinst hos flertallet av pasientene og får en mindre viktig rolle framover.
Kristina Fladseth1-3, Jan Mannsverk 1,3, Andreas Kristensen1,3 og Henrik Schirmer4-5
1Hjertemedisinsk avdeling, Universitetssykehuset Nord-Norge, Tromsø
2Institutt for indremedisinsk forskning, Oslo universitetssykehus, Rikshospitalet, Oslo
3 Institutt for klinisk medisin, UiT Norges arktiske universitet, Tromsø
4 Hjertemedisinsk avdeling, Akershus universitetssykehus, Lørenskog
5Institutt for klinisk medisin, Campus Ahus, Universitetet i Oslo, Oslo
Innledning
Retningslinjer fra European Society of Cardiology (ESC) introduserte i 2019 begrepet kronisk koronarsyndrom (chronic coronary syndrome [CCS]) som erstatning for stabil koronar sykdom (1). Begrepet er mer dekkende for den dynamiske, progredierende prosessen i koronararteriene, som kan akselerere ved manglende behandling, bremses og i noen tilfeller reverseres ved livsstilsendringer og optimal medisinsk behandling. Nye retningslinjer fra ESC ble publisert høsten 2024 (2). Definisjonen av kronisk koronarsyndrom er utvidet til å inkludere både strukturelle og funksjonelle endringer i koronararteriene og mikrosirkulasjonen. Det kliniske spekteret inkluderer nå angina med obstruktiv koronarsykdom, angina uten obstruktiv koronarsykdom (ANOCA), stabile individer etter akutt koronarsyndrom (AKS), perkutan koronarintervensjon (PCI) eller koronar bypassoperasjon, venstre ventrikkel dysfunksjon eller hjertesvikt av iskemisk opprinnelse og asymptomatiske individer med unormale anatomiske eller funksjonelle koronarundersøkelser. Denne artikkelen beskriver kronisk koronarsyndrom med hovedvekt på innførte endringer som er relevante for indremedisinere. Forfatterne har også skrevet en oversiktsartikkel om kronisk koronarsyndrom i Hjerteforum i 2024 (3).
Symptomer og initial utredning Individer med brystsmerter eller mulige anginaekvivalente symptomer
skal kartlegges ut fra kardiovaskulære risikofaktorer, tidligere sykehistorie og symptomkarakteristikker. Figur 1 viser symptomkarakteristikker som øker og reduserer sannsynligheten for koronarsykdom. Fokuset bør være å utelukke AKS og differensiere mot andre ikke-kardielle årsaker til symptomene. Det må gjøres klinisk undersøkelse, tas hvile-EKG og blodprøver. Spirometri og røntgen thorax bør vurderes. Ved mistanke om arytmi bør det gjøres langtids-EKG-registrering. Dersom det fortsatt er mistanke om kronisk koronar syndrom går man videre til risikostratifisering.
Oppdatert og mer nyansert risikostratifisering
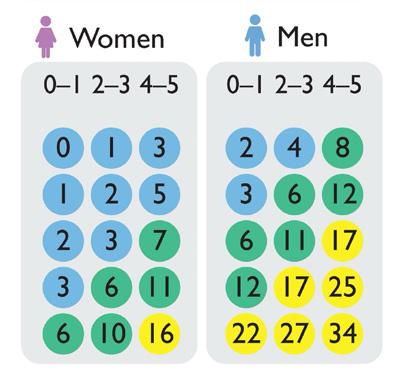
Tidligere modeller overestimerer risikoen for obstruktiv koronarsykdom (1, 4). Det er derfor laget en ny og oppdatert modell (Risk-factorweighted clinical likelihood [RF-CL]), som ut fra symptomskår (0-3 poeng), alder, kjønn og antall risikofaktorer (0-5 poeng; familiehistorie, røyking, diabetes, hypertensjon og dyslipidemi) plasserer individer i svært lav (≤ 5 %), lav (6-15 %) eller moderat (16-50 %) pretest sannsynlighet for obstruktiv koronarsykdom (figur 2) (2, 5). Nytt fra ESC 2024 er at den svært lave, lave eller moderate pretest sannsynligheten deretter kan justeres opp eller ned ut fra øvrige kliniske data, inkludert koronarkalk på tidligere CT thorax, unormale funn ved hvile-EKG eller arbeidsEKG, ekkokardiografi med regionale utfall eller alvorlig venstre ventrikkedysfunksjon, ventrikulær arytmi og
perifer karsykdom (2). Ved flere slike funn eller svært suspekt anamnese for obstruktiv koronarsykdom kan pasienten plasseres i høy (51-85 %) eller veldig høy (> 85 %) pretest sannsynlighet for obstruktiv koronarsykdom. Pasienter med svært lav pretest sannsynlighet bør ikke henvises til videre utredning. Normalt arbeids-EKG eller lav koronar kalsiumskår kan brukes for å reklassifisere pasienter med lav til svært lav pretest sannsynlighet. Koronarkalk på CT thorax gir ikke grunnlag for videre utredning alene.
Enkeltpasienter kan ha en langt høyere risiko for obstruktiv koronarsykdom enn RF-CL tilsier. Dette inkluderer pasienter med familiær hyperkolesterolemi, svært høye nivåer av lipoprotein(a) (Lp(a)), mangeårig diabetes mellitus, alvorlig kronisk nyre sykdom, inflammatorisk reumatisk sykdom og HIV (2, 6-9). Vurderingen av dyslipidemi bør inkludere en engangsmåling av Lp(a) (10). Erfaringsvis kan risikoskårer som NORRISK 2 og SCORE2 være nyttig: Sistnevnte tar også høyde for høyere forekomst av koronarsykdom i andre land (11, 12). Det finnes også egne risikoskårer for individer med diabetes og etablert kardiovaskulær sykdom (13, 14).
RF-CL-tabellen er verd å granske for ulike scenarioer. F.eks. har menn > 50 år og kvinner > 70 år med typiske symptomer minst moderat pretest sannsynlighet for obstruktiv koronarsykdom. Kvinner < 50 år med 0-1 risikofaktorer har svært lav pretest
sannsynlighet for obstruktiv sykdom, også ved typiske symptomer.
ESC anbefaler ekkokardiografi som en del av initial utredning hos alle pasienter, men dette er det trolig ikke kapasitet til i dag. Kvalitetsutvalget til Norsk Cardiologisk Selskap anbefalte i 2020 at det måles proBNP hos alle med mistenkt angina, og gjøres ekkokardiografi hos alle individer med tungpust, bilyd eller forhøyet proBNP (15). Alle med påvist kronisk koronarsyndrom eller persisterende symptomer bør også undersøkes med ekkokardiografi.
Ikke-invasiv bildeundersøkelse – hjørnesteinen i diagnostikk Ikke-invasiv bildeundersøkelse er førstevalget til utredning av pasienter med lav til høy pretest sannsynlighet for obstruktiv koronarsykdom. CT hjerte anbefales ved lav til moderat pretest sannsynlighet (5-50 %), mens funksjonelle bildeunder søkelser anbefales ved moderat til høy pretest sannsynlighet (16-85 %). CT hjerte anbefales som tilleggsunder søkelse ved inkonklusive funksjonelle bildeundersøkelser, og motsatt. Lokal kompetanse og kapasitet skal vektlegges i valg av undersøkelse. I Norge vil dette i stor grad bety CT hjerte, og mindre grad stressekko og single photon emission computed tomography (SPECT). Fordelen med CT hjerte er at også ikke-obstruktiv koronarsykdom avbildes godt, mens fordelen med funksjonelle tester er kartlegging av iskemi, inkludert iskemi på grunn av mikrovaskulær sykdom. CT hjerte kan brukes ved høyere kroppsmasseindeks (KMI) og alder enn tidligere, men krever at pasienten har en regelmessig, normofrekvent hjerterytme. Også ved kjent kronisk koronarsyndrom er ikke-invasive bildeundersøkelser viktig for seleksjon til invasiv koronar angiografi og revaskularisering. Moderne CT hjerte-maskiner kan også benyttes ved tidligere PCI og koronar bypassoperasjon, men erfaringen varierer hos ulike sentre.
Arbeids-EKG – inne eller ute?
Arbeids-EKG er dårlig egnet til å påvise eller utelukke obstruktiv koronar sykdom med 58 % sensitivitet og 62 % spesifisitet, men har en akseptabel prediksjon for hjerte -
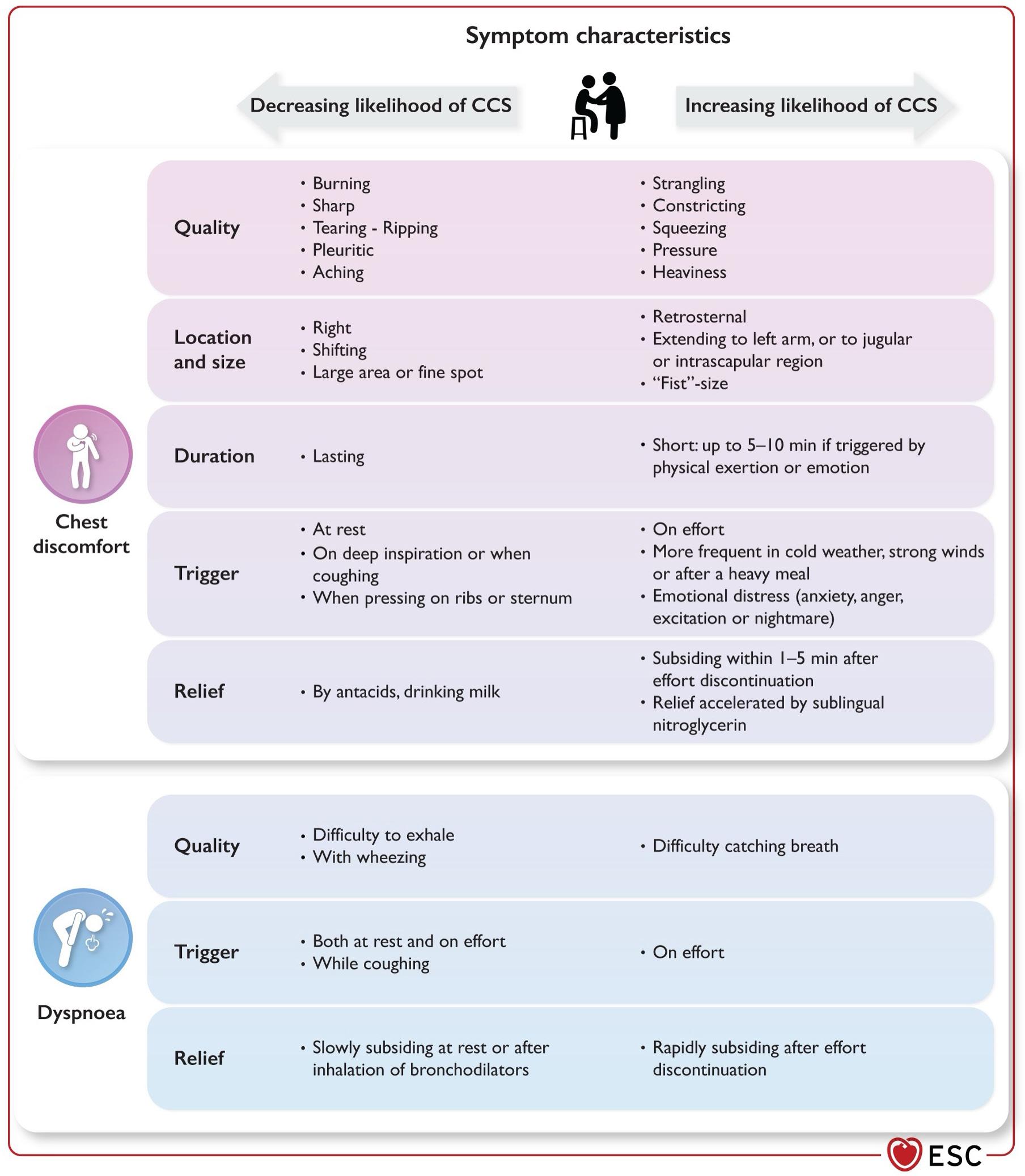
Figur 1. Symptomkarakteristikker ved brystubehag og tungpust som øker og reduserer sannsynligheten for kronisk koronarsyndrom. Figur fra European Society of Cardiology (ESC) 2024. Gjengitt med tillatelse fra Oxford University Press på vegne av ESC (2).
infarkt og død, særlig ytterpunktene med normalt arbeids-EKG ved høy belastning og unormalt arbeidsEKG ved lav belastning (2, 16-18). Retningslinjene fra ESC åpner opp for at arbeids-EKG kan benyttes til å reklassifisere individer med lav risiko (6-15 %) og normalt arbeids-EKG, til svært lav risiko (≤ 5 %) der videre utredning ikke er nødvendig (2, 17). Videre kan arbeids-EKG benyttes til å bekrefte symptomer og vurdere fysisk kapasitet hos pasienter med tidligere etablert kronisk koronarsyndrom og nye symptomer. I praksis vil en poliklinisk vurdering som også inkluderer arbeids-EKG fortsette å spille en viktig rolle ved mange sykehus i Norge.
Når skal vi gjøre invasiv koronar angiografi?
Få pasienter med mistenkt kronisk koronarsyndrom skal direkte til invasiv koronar angiografi. Mange kan diagnostiseres og behandles uten invasiv koronar angiografi. Livsstilsendringer og medisinsk behandling bør optimaliseres hos flere pasienter før invasiv koronar angiografi, også ved tidligere hjerteinfarkt og revaskularisering. Invasiv koronar angiografi er indisert ved symptomer refraktære til antianginøs behandling, utbredt iskemi på funksjonelle bildeundersøkelser eller høyrisikosykdom på CT hjerte (≥ 50 % stenose i venstre hovedstamme, 3-karssykdom med ≥ 70 % stenose,
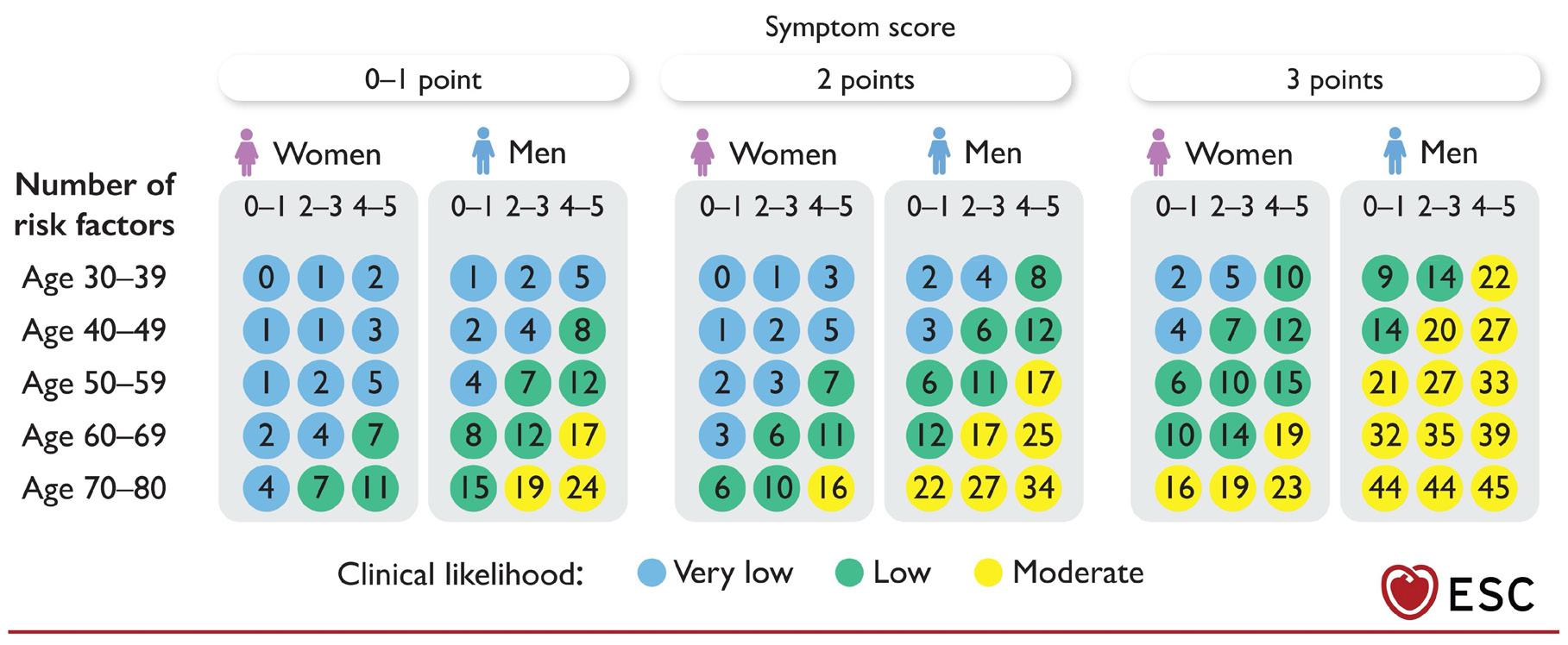
Figur 2. Klinisk pretest sannsynlighet for obstruktiv koronarsykdom etter symptomskår, alder, kjønn og antall risikofaktorer. Brystsmerter gir 0-3 poeng ut fra: typisk lokalisasjon og karakter, forverres ved fysisk eller psykisk stress og lindres i hvile eller av nitrater. Tungpust som forverres av aktivitet gir 2 poeng. Risikofaktorer inkluderer hereditet for prematur koronarsykdom (menn < 55 år, kvinner < 65 år), nåværende eller tidligere røyker, dyslipidemi, hypertensjon og diabetes. Tilpasset figur fra European Society of Cardiology (ESC) 2024. Gjengitt med tillatelse fra Oxford University Press på vegne av ESC (2).
1- og 2-karssykdom inkludert ≥ 70 % stenose i proksimale LAD). Invasiv koronar angiografi bør vurderes som første undersøkelse hos pasienter med svært høy risiko for obstruktiv koronarsykdom (≥ 85%), nyoppstått angina ved lav belastning eller andre høyrisiko funn som alvorlig redusert venstre ventrikkelfunksjon, ventrikulær arytmi eller hypotensjon under belastning.
Screening
ESC anbefaler opportunistisk screening med risikoskårer som NORRISK 2 hos alle voksne (2, 11). Øvrig screening anbefales hovedsakelig ikke, men koronar kalsiumskår eller ultralyd halskar kan vurderes hos enkelte. Det anbefales å justere risikovurderingen hos pasienter som får påvist koronarkalk som et bifunn på CT thorax.
Optimal medisinsk behandling
Statin til alle og platehemmer ved hjerteinfarkt, revaskularisering og obstruktiv koronarsykdom
Maksimal tolererbar dose statin er førstelinjebehandling for å redusere risikoen for død og nye hendelser. Behandlingsmålet er LDL-kolesterol < 1,4 mmol/L og ≥ 50 % reduksjon fra utgangsverdi (2, 19). Hver 1 mmol/L reduksjon i LDL-kolesterol
reduserer årlig risiko for kardiovaskulære hendelser med 22 %, død av koronarsykdom med 20 % og totaldød med 10 % (20). Oppnås ikke behandlingsmålet på statin alene, anbefales tillegg av ezetimib og deretter PCSK9-hemmer. Tillegg av PCSK9-hemmer reduserer LDL-kolesterol opptil 60 % og gir 15 % reduksjon i kardiovaskulære hendelser (21). Nåværende kriterier for blåresept er kronisk koronarsyndrom og vedvarende LDLkolesterol > 3,6 mmol/L til tross for høyest tolererte dose statin og ezetimib, eller LDL-kolesterol > 2,6 mmol/L dersom pasienten i tillegg har diabetes, familiær hyperkolesterolemi, gjennomgått hjerteinfarkt eller tilbakevendende kardiovaskulære hendelser.
Acetylsalisylsyre, alternativt klopidogrel, anbefales til alle pasienter med tidligere hjerteinfarkt, revaskularisering eller kjent obstruktiv koronarsykdom. Det er ikke vist total gevinst av platehemmende behandling til pasienter med ikke-obstruktiv sykdom eller ANOCA (2, 22). Standard dobbel platehemmende behandling (DAPT) gis i 12 måneder etter AKS og 6 måneder etter PCI ved kronisk koronarsyndrom. Det er økt fokus på individuell tilpasning ut fra risiko for blødning og iskemiske hendelser.
Iskemisk risiko er avhengig av PCI kompleksiteten og må vurderes av invasiv kardiolog.
Annen prognostisk medikamentell behandling Angiontensinkonverterende enzymhemmer, mineralkortikoidreseptorantagonist og natrium-glukose-kotransportør 2 (SGLT2)-hemmer bør benyttes ved andre indikasjoner inkludert hjertesvikt, hypertensjon, diabetes og kronisk nyresykdom. Ved kronisk koronar syndrom og diabetes anbefales glukagonlignende peptid-1 (GLP-1)-analoger og SGLT2-hemmer (23). GLP-1-analog kan også redusere risikoen for hendelser ved kronisk koronarsyndrom og overvekt (24).
Betablokker har ingen sikker prognostisk effekt hos de fleste pasienter med kronisk koronarsyndrom. Det er ingen randomiserte kontrollerte studier (RCT) som støtter bruk av betablokker etter gjennomgått hjerteinfarkt med vellykket revaskularisering og bevart ejeksjonsfraksjon ≥ 50 %, inkludert svenske REDUCE-AMI (2, 25). Resultatene fra norsk-danske BETAMI/DANBLOCK forventes publisert til høsten.
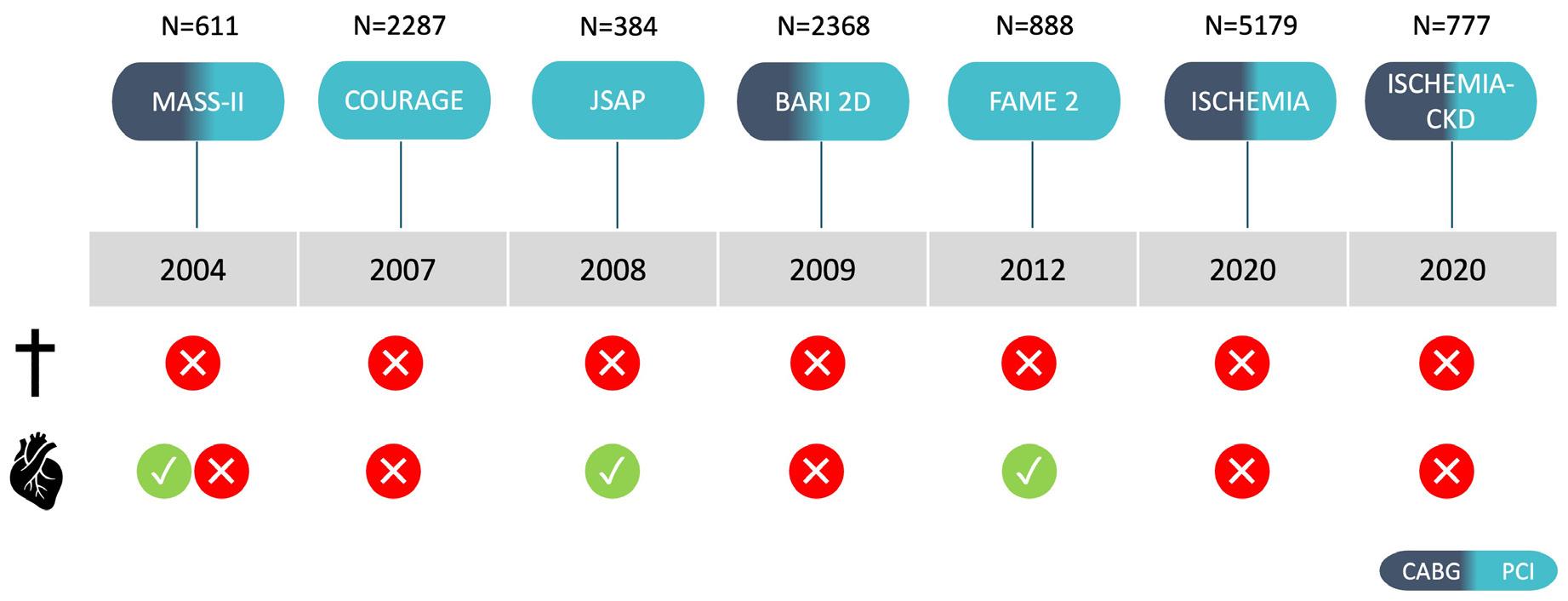
Figur 3. Randomiserte kontrollerte studier som sammenligner effekten av revaskularisering og medikamentell behandling. Ingen forskjell i dødelighet (øvre rad). JSAP og FAME 2 fant lavere risiko for kardiovaskulære hendelser etter PCI, mens MASS-II fant lavere 5-års og 10-års risiko for kardiovaskulære hendelser etter CABG, men ikke PCI (nedre rad). BARI 2D inkluderte kun pasienter med diabetes type 2, og ISCHEMIA-CKD inkluderte kun pasienter med kronisk nyresykdom. CABG = koronar bypasskirurgi; PCI = perkutan koronarintervensjon. Figur tilpasset fra prøveforelesning «Hvilke pasienter bør til invasiv koronarutredning og hvem bør revaskulariseres?» av Kristina Fladseth, UiT Norges arktiske universitet, 2022. Gjengitt med tillatelse.
Årlig influensavaksine reduserer kardiovaskulær – og total død hos pasienter med kronisk koronarsyndrom og anbefales til alle (26).
Retningslinjene fra 2024 anbefaler å vurdere kolkisin for å redusere risiko for hjerteinfarkt, slag og revaskularisering, men en nylig publisert RCT fant ingen effekt av kolkisin tre år etter hjerteinfarkt (2, 27).
Antianginøs behandling
Det er ikke godt evidensgrunnlag for å anbefale en spesifikk antianginøs behandling. Behandlingen bør tilpasses hver enkelt pasient ut fra preferanser, komorbiditet og hvilepuls, med mål om symptomkontroll og akseptable bivirkninger. Førstelinjebehandling er betablokker eller kalsiumblokker, eller kombinasjonen av disse. Hurtigvirkende nitrater bør tilbys som anfallsbehandling. Langtidsvirkende nitrater er andrelinjebehandling og bør doseres i laveste effektive dose og én gang i døgnet på grunn av fare for toleranseutvikling.
Revaskularisering – god symptomlindring til mange, prognostisk effekt hos få Revaskularisering med PCI og/eller koronar bypassoperasjon kan gi effektiv symptomlindring, økt livskvalitet og bedre prognosen for
enkelte pasienter. Valget mellom medisinsk behandling, PCI og koronar bypassoperasjon fattes i tverrfaglig team, og pasientens synspunkt bør vektlegges. Optimal medisinsk behandling må ligge til grunn ved alle alternativer, og pasienter bør forsøke livsstilsendringer og optimal medisinsk behandling før beslutningen om revaskularisering tas.
Ingen nyere RCTer har vist bedre overlevelse av revaskularisering, og flertallet av studiene finner heller ikke lavere risiko for kardiovaskulære hendelser (figur 3) (28-37). Studiene med lavere risiko for hendelser er primært drevet av lavere risiko for revaskularisering og ustabil angina (32, 34, 35). Det debatteres likevel rundt utfordringer i studiedesign med overkrysning til revaskulariseringsarmen, kort oppfølgingstid, få deltagere med uttalt angina og komplisert koronarsykdom, og eksklusjon av venstre hovedstammesykdom. Videre har foreløpige resultater fra oppfølgingsstudien ISCHEMIA-EXTEND funnet lavere risiko for kardiovaskulær død, men høyere risiko for ikke-kardiovaskulær død ved revaskularisering versus medikamentell behandling (38). Retningslinjene fra 2024 anbefaler revaskularisering hos pasienter med venstre hovedstamme sykdom for
å redusere totalmortalitet, og ved funksjonelt signifikant 3-karssykdom og 1-2-karssykdom med affeksjon av proksimale LAD for å redusere kardiovaskulær død på lang sikt og risiko for hjerteinfarkt (2).
Det er bred enighet om å tilby revaskularisering til pasienter med persisterende angina til tross for optimal medisinsk behandling.
Dette kan lindre anginaplager, bedre livskvalitet og fysisk kapasitet, og redusere behovet for antianginøse legemidler og medfølgende bivirkninger (35). Angina er assosiert med redusert livskvalitet og fysisk kapasitet, depresjon og gjentatte kontakter med helsevesenet (39).
Data fra ISCHEMIA har vist mindre anginaplager ved revaskularisering enn ved medikamentell behandling (40). ORBITA-2 viste at PCI reduserer anginaplager sammenlignet med en placeboprosedyre (41). Et annet viktig perspektiv i behandlingen av angina er at en stor multinasjonal registerstudie har vist at opptil 40 % blir kvitt symptomene sine i løpet av ett år også uten revaskularisering (42).
Angina med ikke-obstruktiv koronarsykdom
Over 50 % av pasientene får ikke påvist obstruktiv koronarsykdom i utredningen av sine plager (43, 44).
Noen av disse vil ha vedvarende angina og omtales som ANOCA. Indremedisineren har nylig publisert en egen artikkel om ANOCA (45). Oppsummert anbefales invasiv fysiologisk testing hos pasienter med persisterende anginaplager til tross medikamentell behandling (2). Pasientene må også sikres aggressive livsstilstiltak og behandling av risikofaktorer og komorbiditeter (46).
Oppfølgning, hjerteskole og hjerterehabilitering Kronisk koronarsyndrom er en progressiv tilstand som krever kontinuerlig oppfølging. ESC anbefaler årlig oppfølgning hos fastlege for å vurdere klinisk status, risikoprofil og komorbiditet, samt optimalisering av livsstil og behandling, eller videre utredning. Trenings-
Referanser:
1. Knuuti J, Wijns W, Saraste A, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J 2020; 41: 407-77.
2. Vrints C, Andreotti F, Koskinas KC, et al. 2024 ESC Guidelines for the management of chronic coronary syndromes. Eur Heart J 2024; 45: 3415-537.
3. Fladseth K, Mannsverk J, Schirmer H. Kronisk koronarsyndrom. Hjerteforum 2024; 1/2024.
4. Genders TS, Steyerberg EW, Alkadhi H, et al. A clinical prediction rule for the diagnosis of coronary artery disease: validation, updating, and extension. Eur Heart J 2011; 32: 1316-30.
5. Winther S, Schmidt SE, Mayrhofer T, et al. Incorporating Coronary Calcification Into Pre-Test Assessment of the Likelihood of Coronary Artery Disease. J Am Coll Cardiol 2020; 76: 2421-32.
6. Restivo V, Candiloro S, Daidone M, et al. Systematic review and meta-analysis of cardiovascular risk in rheumatological disease: Symptomatic and non-symptomatic events in rheumatoid arthritis and systemic lupus erythematosus. Autoimmun Rev 2022; 21: 102-925.
7. Shah ASV, Stelzle D, Lee KK, et al. Global Burden of Atherosclerotic Cardiovascular Disease in People Living With HIV: Systematic Review and MetaAnalysis. Circulation 2018; 138: 1100-12.
8. Sarnak MJ, Amann K, Bangalore S, et al. Chronic Kidney Disease and Coronary Artery Disease. J Am Coll Cardiol 2019; 74: 1823-38.
9. Kamstrup PR, Tybjærg-Hansen A, Nordestgaard BG. Extreme lipoprotein(a) levels and improved cardiovascular risk prediction. J Am Coll Cardiol 2013; 61: 1146-56.
10. Kronenberg F, Mora S, Stroes ESG, et al. Lipoprotein(a) in atherosclerotic cardiovascular disease and aortic stenosis: a European Atherosclerosis Society consensus statement Eur Heart J 2022; 43: 3925-46.
11. Selmer R, Igland J, Ariansen I, et al. NORRISK 2: A Norwegian risk model for acute cerebral stroke and myocardial infarction. Eur J Prev Cardiol 2017; 24: 773-82.
12. Hageman S, Pennells L, Ojeda F, et al. SCORE2 risk prediction algorithms: new models to estimate 10-year risk of cardiovascular disease in Europe. Eur Heart J 2021; 42: 2439-54.
13. Group SC-DW, the ESCCRC. SCORE2-Diabetes: 10year cardiovascular risk estimation in type 2 diabetes in Europe. Eur Heart J 2023; 44: 2544-56.
14. Dorresteijn JA, Visseren FL, Wassink AM, et al. Development and validation of a prediction rule for recurrent vascular events based on a cohort study of patients with arterial disease: the SMART risk score. Heart 2013; 99: 866-72.
15. Munk PS, Juliebø V, Schirmer H. NCS - Kvalitetsutvalget: 2019 ESC guidelines for the diagnosis and management of chronic coronary syndromes. 2020.
16. Knuuti J, Ballo H, Juarez-Orozco LE, et al. The performance of non-invasive tests to rule-in and rule-out significant coronary artery stenosis in patients with stable angina: a meta-analysis focused on post-test disease probability. Eur Heart J 2018; 39: 3322-30.
17. Rasmussen LD, Schmidt SE, Knuuti J, et al. Exercise electrocardiography for pre-test assessment of the
basert hjerte rehabilitering reduserer risikoen for kardiovaskulær død, og bør tilbys til alle pasienter med kronisk koronarsyndrom (2, 47). Lav og varierende deltakelse på hjerte rehabilitering er en utfordring i Norge. Fra 2018 til 2021 deltok kun 26 % av hjerteinfarktpasienter på hjerterehabilitering eller hjerteskole (48). Flere sykehus oppretter tilbud om polikliniske oppfølgningstimer etter hjerteinfarkt. I Norsk hjerteinfarktregister er det et frivillig skjema for sekundærprofylaktisk oppfølging. I 2023 oppnådde kun 44 % av pasientene LDL-kolesterol < 1,4 mmol/L innen ett år, men det var lav svar prosent (49). De fleste kommuner tilbyr gratis trening, kostholdsveiledning og hjelp til røyke slutt gjennom frisklivssentraler.
likelihood of coronary artery disease. Heart 2024; 110: 263-70.
18. Mark DB, Shaw L, Harrell FE, Jr., et al. Prognostic value of a treadmill exercise score in outpatients with suspected coronary artery disease. N Engl J Med 1991; 325: 849-53.
19. Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2020; 41: 111-88.
20. Baigent C, Blackwell L, Emberson J, et al. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170,000 participants in 26 randomised trials. Lancet 2010; 376: 1670-81.
21. Sabatine MS, Giugliano RP, Keech AC, et al. Evolocumab and Clinical Outcomes in Patients with Cardiovascular Disease. N Engl J Med 2017; 376: 1713-22.
22. Ford TJ, Stanley B, Good R, et al. Stratified Medical Therapy Using Invasive Coronary Function Testing in Angina: The CorMicA Trial. J Am Coll Cardiol 2018; 72: 2841-55.
23. Marx N, Federici M, Schütt K, et al. 2023 ESC Guidelines for the management of cardiovascular disease in patients with diabetes. Eur Heart J 2023; 44: 4043140.
24. Lincoff AM, Brown-Frandsen K, Colhoun HM, et al. Semaglutide and Cardiovascular Outcomes in Obesity without Diabetes. N Engl J Med 2023; 389: 2221-32.
25. Yndigegn T, Lindahl B, Mars K, et al. Beta-Blockers after Myocardial Infarction and Preserved Ejection Fraction. N Engl J Med 2024; 390: 1372-81.
26. Clar C, Oseni Z, Flowers N, et al. Influenza vaccines for preventing cardiovascular disease. Cochrane Database Syst Rev 2015; 2015.
27. Jolly Sanjit S, d’Entremont M-A, Lee Shun F, et al. Colchicine in Acute Myocardial Infarction. N Engl J Med 2025; 392: 633-42.
28. Hueb W, Lopes N, Gersh BJ, et al. Ten-year follow-up survival of the Medicine, Angioplasty, or Surgery Study (MASS II): a randomized controlled clinical trial of 3 therapeutic strategies for multivessel coronary artery disease. Circulation 2010; 122: 949-57.
29. Hueb W, Lopes NH, Gersh BJ, et al. Five-year followup of the Medicine, Angioplasty, or Surgery Study (MASS II): a randomized controlled clinical trial of 3 therapeutic strategies for multivessel coronary artery disease. Circulation 2007; 115: 1082-9.
30. Hueb W, Soares PR, Gersh BJ, et al. The medicine, angioplasty, or surgery study (MASS-II): a randomized, controlled clinical trial of three therapeutic strategies for multivessel coronary artery disease: one-year results. J Am Coll Cardiol 2004; 43: 1743-51.
31. Boden WE, O’Rourke RA, Teo KK, et al. Optimal medical therapy with or without PCI for stable coronary disease. N Engl J Med 2007; 356: 1503-16.
32. Nishigaki K, Yamazaki T, Kitabatake A, et al. Percutaneous coronary intervention plus medical therapy reduces the incidence of acute coronary syndrome more effectively than initial medical therapy only among patients with low-risk coronary artery disease a randomized, comparative, multicenter study. JACC Cardiovasc Interv 2008; 1: 469-79.
Fremtidsperspektiver
Aldersjustert insidens av obstruktiv koronarsykdom forventes å falle videre, men prevalensen av kronisk koronarsykdom øker som følge av høyere levealder og bedret overlevelse etter hjerteinfarkt (50). Selv om antall elektive invasive prosedyrer faller, blir prosedyrene mer komplekse på grunn av eldre pasienter med mer koronarkalk og komorbiditet (51). Retningslinjer anbefaler økt bruk av invasiv fysiologisk utredning hos ANOCA-pasienter (2). Videre må tilbudet om ikke-invasive bildeundersøkelser utbedres og vi må fokusere på livsstilsendringer og optimal medikamentell behandling fremfor revaskularisering. Hvert pasientmøte i sykehus gir mulighet til å optimalisere primær- og sekundærforebygging av hjerte- og karsykdom.
33. Frye RL, August P, Brooks MM, et al. A randomized trial of therapies for type 2 diabetes and coronary artery disease. N Engl J Med 2009; 360: 2503-15.
34. De Bruyne B, Pijls NHJ, Kalesan B, et al. Fractional Flow Reserve–Guided PCI versus Medical Therapy in Stable Coronary Disease. N Engl J Med 2012; 367: 991-1001.
35. Xaplanteris P, Fournier S, Pijls NHJ, et al. Five-Year Outcomes with PCI Guided by Fractional Flow Reserve. N Engl J Med 2018; 379: 250-9.
36. Maron DJ, Hochman JS, Reynolds HR, et al. Initial Invasive or Conservative Strategy for Stable Coronary Disease. N Engl J Med 2020; 382: 1395-407.
37. Bangalore S, Maron DJ, O’Brien SM, et al. Management of Coronary Disease in Patients with Advanced Kidney Disease. N Engl J Med 2020; 382: 1608-18.
38. Hochman JS, Anthopolos R, Reynolds HR, et al. Survival After Invasive or Conservative Management of Stable Coronary Disease. Circulation 2023; 147: 8-19.
39. Steg PG, Greenlaw N, Tendera M, et al. Prevalence of Anginal Symptoms and Myocardial Ischemia and Their Effect on Clinical Outcomes in Outpatients With Stable Coronary Artery Disease: Data From the International Observational CLARIFY Registry. JAMA Intern Med 2014; 174: 1651-9.
40. Spertus JA, Jones PG, Maron DJ, et al. Health-Status Outcomes with Invasive or Conservative Care in Coronary Disease. N Engl J Med 2020; 382: 1408-19.
41. Rajkumar CA, Foley MJ, Ahmed-Jushuf F, et al. A Placebo-Controlled Trial of Percutaneous Coronary Intervention for Stable Angina. N Engl J Med 2023; 389: 2319-30.
42. Mesnier J, Ducrocq G, Danchin N, et al. International Observational Analysis of Evolution and Outcomes of Chronic Stable Angina: The Multinational CLARIFY Study. Circulation 2021; 144: 512-23.
43. Newby DE, Adamson PD, Berry C, et al. Coronary CT Angiography and 5-Year Risk of Myocardial Infarction. N Engl J Med 2018; 379: 924-33.
44. Patel MR, Peterson ED, Dai D, et al. Low diagnostic yield of elective coronary angiography. N Engl J Med 2010; 362: 886-95.
45. Madssen E. Angina med ikke-obstruktiv koronarsykdom (ANOCA). Indremedisineren 2025; 2025/01.
46. Virani SS, Newby LK, Arnold SV, et al. 2023 AHA/ ACC/ACCP/ASPC/NLA/PCNA Guideline for the Management of Patients With Chronic Coronary Disease. Circulation 2023; 148: e9-e119.
47. Dibben GO, Faulkner J, Oldridge N, et al. Exercisebased cardiac rehabilitation for coronary heart disease: a meta-analysis. Eur Heart J 2023; 44: 45269.
48. Norekvål TM, Bale M, Bedane HK, et al. Cardiac rehabilitation participation within 6 months of discharge in 37 136 myocardial infarction survivors: a nationwide registry study. Eur J Prev Cardiol 2024; 31: 1977-80.
49. Nasjonalt seketeriat for hjerteinfarktregisteret. Årsrapport for 2023. Norsk hjerteinfarktregister, 2024.
50. Folkehelseinstituttet. Folkehelserapporten - Helsetilstanden i Norge. Hjerte- og karsykdommer. 2018.
51. Hovland S, Skåre K, Autenried MG, et al. Årsrapport for 2023. Norsk register for invasiv kardiologi (NORIC), 2024.
De siste 10 årene har gitt nye gjennombrudd i forståelsen og behandlingen av kronisk nyresykdom. Nye medikamenter som SLGT 2-hemmere, ikke-steroide mineralkortikoider og GLP-1-agonister har alle vist gunstige nyrebeskyttende effekter. Artikkelen tar for seg sentrale poenger i forståelsen.
Trond Geir Jenssen, overlege og professor ved Nyreseksjonen, OUS Rikshospitalet og Universitetet i Oslo
Introduksjon
«Det var ingenting nytt» sa min nefrolog-kollega etter at vi i 1998 kom hjem fra Philadelphia og den årlige amerikanske nyrekongressen (American Society of Nephrology –ASN). Og det måtte jeg egentlig si meg enig i, i alle fall hva angikk ny behandling av kronisk nyresykdom. Det hadde egentlig ikke vært mye nytt etter at Ed Lewis fra Chicago i 1993 (i Boston) presenterte den første studien med ACE-hemmer hvor 409 personer med type 1 diabetes og nefropati ble behandlet med kaptopril eller placebo i 4 år. Behandling med kaptopril halverte forekomsten av dialyse, transplantasjon eller død hos disse pasientene (1). Det var dramatiske funn.
Hva skjedde videre?
Det kom studier som viste at den nyrebeskyttende effekten av ACEhemming ved kronisk nyresykdom også gjaldt personer uten diabetes. Og i 2001 fikk vi demonstrert at angiotensin2-receptor-blokkade hadde tilsvarende gunstig effekt på nyresykdom hos personer med type 2 diabetes (2, 3). Ved type 2 diabetes har opptil 2/3 av pasientene ikke-diabetisk nyresykdom, oftest hypertensjonsnyrer eller immunologisk nyresykdom så som IgA-nefritt (4), mens det i litteraturen feilaktig blir referert til ‘diabetisk nyresykdom’ hos alle disse pasientene. Så ble det stille igjen…
Gjennombruddet – SGLT 2-hemmer
Gjennombruddet i behandling av kronisk nyresykdom, utover bruk av RAS (Renin-Angiotensin-AldosteronSystem)-blokkade, startet for 10 år
siden. Dette skjedde først ved at SGLT 2-hemmeren empagliflozin viste seg å kunne ha nyrebeskyttende effekt hos personer med type 2 diabetes, og da som et sekundært endepunkt i en studie hvor hovedmålet var å senke blodsukkeret (5). Senere har 2 store studier på henholdsvis dapagliflozin og empagliflozin vist at behandlingen som tillegg til RAS -blokkade forsinker fall i glomerulær filtrasjonsrate hos pasienter med kronisk nyresykdom (med eller uten type 2 diabetes), i alle fall for en 3- års periode (6, 7) Initialt senker SGLT 2-hemming nyrefunksjonen litt gjennom et gunstig trykkfall i glomeruli, før den kroniske funksjonskurven stabiliserer seg. I Dapa-CKD-studien (figur 1) var forskjellen i årlig fall for eGFR 1.8/ml/min/år mellom behandlingsgruppen og placebogruppen. Både dapagliflozin og empagliflozin har også vist seg å forebygge hospitalisering og død hos personer med hjertesvikt. Studier på personer med type 1 diabetes er foreløpig ikke utført. Det er viktig å understreke at alle disse studiene har vist effekt av SGLT 2-hemmer kun i kombinasjon med RAS-blokkade. Det foreligger ikke tilsvarende studier på effekt av monoterapi med SGLT 2-hemmer. I praksis starter man behandlingen først med RAS-blokkade, og innen 14 dager legger man til SGLT 2-hemmer når blodtrykk og kontrollprøver så som kreatinin og kalium er i orden. Det er ikke er rapportert fare for akutt nyresvikt når SGLT 2-hemmer legges til RAS-blokkade.
Nye gjennombrudd
Finerenon. Parallelt med nyrestudiene på SGLT 2-hemming pågikk
to store studier på bruk av den ikkesteroide mineralkortikoid receptorantagonisten finerenon hos personer med type 2 diabetes og kronisk nyresykdom. Resultatene ble publisert i 2 store studier, FIDELIO- og FIGAROstudiene (8, 9), og begge viste både nyre- og hjertebeskyttende effekt av medikamentet i kombinasjon med RAS-blokkade. Disse to studiene ble oppsummert i den store FIDELITYanalysen med 13.000 personer inkludert i analysen, og som viste at personer med type 2 diabetes og estimert GFR (eGFR) 25-75 ml/ min/1.73 m2 hadde en 23 % relativ risikoreduksjon for alvorlig progresjon i nyresykdom (10). Dessverre var det bare 6% av pasientene som samtidig fikk behandling med SGLT 2-hemmer i tillegg til RAS-blokkaden, slik at det endelige beviset for ytterligere effekt av trippel nyrebeskyttende behandling enda ikke foreligger.
Inkretin-basert behandling og vektreduksjon Allerede de første behandlingsstudiene med semaglutid viste at GLP-1-receptor agonisme senker albuminuri hos personer med type 2 diabetes. Studiene var ikke designet for å påvise endringer i GFR. Ett av de første signalene på at inkretinbasert behandling kunne beskytte mot fall i nyrefunksjon fikk man i SURPASS-4 studien med GLP-1/GIPreceptoragonisten tirzepatid. I en prespesifisert posthoc endepunktsanalyse fant man at gruppen med tirzepatid hadde et langsommere fall i eGFR enn placebo hos personer med type 2 diabetes (11). Sommeren 2024 kom så den første randomiserte, blindede og placebokontrollerte studien hvor pasienter

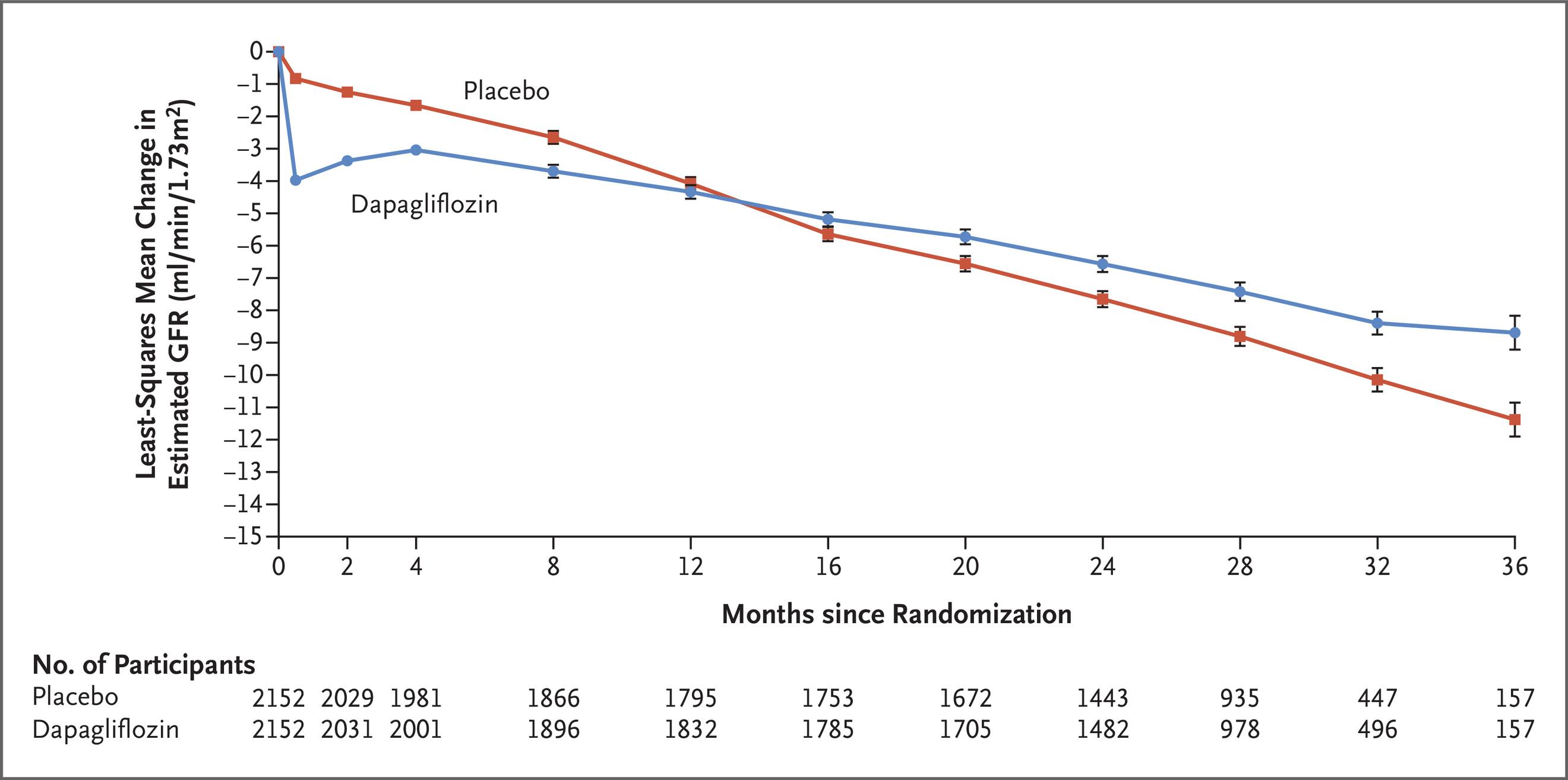
med type 2 diabetes ble inkludert på basis av kronisk nyre sykdom, ikke overvekt. Dette var FLOW-studien som sammenlignet semaglutid 1 mg ukentlig mot placebo hos personer med type 2 diabetes og eGFR 25-75 ml/min/1.73 m2 (i gjennomsnitt 47 ml/ min/m2) i tillegg til albuminuri (12).
Dette var «add-on» behandling til allerede eksisterende RAS-blokkade. Gjennomsnittlig BMI ved inklusjon var 32.0 kg/m2, og semaglutidgruppen hadde 4 kg større vektreduksjon enn kontrollgruppen. Det primære endepunktet, et kombinert renalt og kardiovaskulært endepunkt, ble redusert med 24% i behandlingsgruppen, og i et sekundært endepunkt så man et langsommere fall i eGFR i behandlingsgruppen (en forskjell på 1.1 ml/min/ år). Tilsvarende ble funnet i et sekundært nyre endepunkt i SELECT-studien med semaglutid 2.4 mg ukentlig (13).
I FLOW-studien fikk bare 15% av pasientene samtidig behandling med SGLT 2-hemmer, noe som vanskeliggjør fortolkningen av studien i forhold til etablert nyrebeskyttende behandling. En del av den nyrebeskyttende effekt med GLP-1-agonisme kan ligge i økt renal saltutskillelse (14), noe som allerede er stimulert med SGTL2-hemming.
Det er ingen tvil om at de nevnte studiene demonstrerer en nyrebeskyttende effekt, men størrelsen
av effekten på selve nyrefunksjonen (GFR) kan diskuteres så lenge man kun benytter estimert GFR som endepunkt. Ved uttalt vektreduksjon mister man også muskelmasse, og ved kreatinin-baserte eGFR-ligninger vil dette medføre lavere kreatininverdier som dermed gir høyere eGFR enn det nyrefunksjonen tilsier. Det samme gjelder for cystatin C-baserte ligninger, siden cystatin C produseres i inflammatorisk vev/hvite blodceller. Reduksjon i fettvev kan i seg selv medføre lavere inflammatorisk profil, lavere cystatin C og «høyere eGFR». Disse svakhetene både med kreatinin- og cystatin C-baserte ligninger er utmerket gjort rede for i en norsk publikasjon (15). Håpet nå er at intervensjonsstudier med inkretin-basert agonisme (GLP-1, GIP og andre) også vil inkludere grupper med målt GFR, for nøyaktig å avklare i hvor stor grad nyrefunksjonen beskyttes. Det finnes dyreeksperimentelle studier som gir holdepunkter for at GLP-1-respetoragonisme kan virke nyrebeskyttende i seg selv (14).
Hva betyr overvekt for nyrefunksjon og kronisk nyresykdom?
En klassisk epidemiologisk studie fra Kayser-Permanente databasen i California publisert i 2006 viste at høyere BMI var assosiert med høyere risiko for endestadium nyresykdom (16). Funnet kunne imidlertid ikke reproduseres i andre studier.
I dag tilsier observasjonelle data at det neppe er kroppsmasse eller fettmasse i seg selv som skader nyrene, men heller sentral fedme, insulinresistens syndrom og inflammasjon. I en studie fant man ved hjelp av Cockgrauft-Gault bestemt kreatinin clearance at grad av hyperfiltrasjon (som gjerne forutgår nefrontap og fall i nyrefunksjon) økte med antall tilstedeværende komponenter i det metabolske syndrom, så som lav HDL, høyt blodtrykk, triglyserider og glukose (17). I Tromsø-studien RENIS-6 viste man med målt GFR (iohexol clearance) at det ikke var BMI, men heller det metabolske syndrom og ganske spesielt triglyseridene (som surrogatparameter på insulinresistens) som predikerte fall i GFR i studiepopulasjonen (18). Dette er senere bekreftet i en stor østerriksk database som så på fall i estimert GFR (19).
Epidemiologiske data tilsier altså at det metabolske syndrom og insulinresistens bidrar til kronisk nyresykdom når menn og kvinner undersøkes samlet. Det viser seg imidlertid at kvinner er mest utsatt for progresjon i kronisk nyresykdom etter menopausen. Dette ble tydelig vist i et materiale fra Sør-Korea, hvor forekomsten av kronisk nyresykdom økte jamt med alder og det metabolske syndrom i begge kjønn frem til 50-årsalder (20). Etter fylte 50 år kom det en ytterligere brå økning
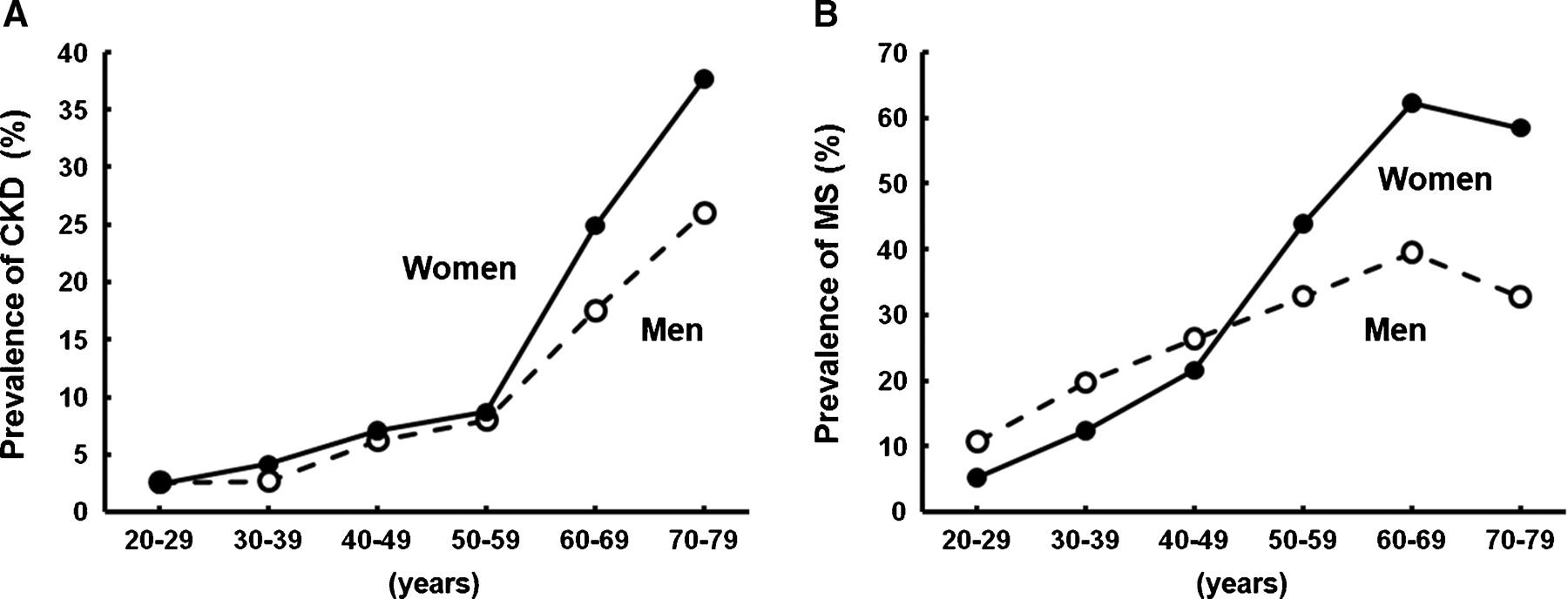
Figur 2: Prevalence of ( A ) chronic kidney disease (CKD) and ( B) metabolic syndrome (MS) by age and gender. (Fra referanse 20, trykkes med tillatelse).
Forfatteren har mottatt foredragshonorar fra NovoNordisk, AstraZeneca, Boehringer Ingelheim, Bayer og Eli Lilly Nephrol Dial Transplant, Volume 25, Issue 2, February 2010, Pages 469–477, https://doi.org/10.1093/ndt/gfp483
i forekomst hos kvinnene (Figur 2). I en amerikansk studie, hvor man fulgte kvinner som var bilateralt oophorektomert pga. cancer, var risikoen for kronisk nyresykdom betydelig økt hos kvinner yngre enn 45 år, men ikke hos dem eldre enn 45 år, sammenlignet med kvinner som ikke var oophorektomert (21). Etter eksperimentelle studier å dømme, har østrogen en uttalt nyrebeskyttende effekt både på glomeruli og interstitiet/tubuli, blant annet ved å hemme inflammasjon og fibrose (22, 23). Dessverre har vi ingen kliniske studier på østrogenbehandling hvor nyreproteksjon har vært et definert endepunkt.
Referanser
1. Lewis EJ, Hunsicker LG, Bain RP, Rohde RD. The effect of angiotensin-converting-enzyme inhibition on diabetic nephropathy. The Collaborative Study Group. N Engl J Med. 1993;329(20):1456-62.
2. Brenner BM, Cooper ME, de Zeeuw D, Keane WF, Mitch WE, Parving HH, et al. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Engl J Med. 2001;345(12):861-9.
3. Lewis EJ, Hunsicker LG, Clarke WR, Berl T, Pohl MA, Lewis JB, et al. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes. N Engl J Med. 2001;345(12):851-60.
4. Sharma SG, Bomback AS, Radhakrishnan J, Herlitz LC, Stokes MB, Markowitz GS, et al. The modern spectrum of renal biopsy findings in patients with diabetes. Clin J Am Soc Nephrol. 2013;8(10):1718-24.
5. Wanner C, Inzucchi SE, Lachin JM, Fitchett D, von Eynatten M, Mattheus M, et al. Empagliflozin and Progression of Kidney Disease in Type 2 Diabetes. N Engl J Med. 2016;375(4):323-34.
6. Heerspink HJL, Stefansson BV, Correa-Rotter R, Chertow GM, Greene T, Hou FF, et al. Dapagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2020;383(15):1436-46.
7. The E-KCG, Herrington WG, Staplin N, Wanner C, Green JB, Hauske SJ, et al. Empagliflozin in Patients with Chronic Kidney Disease. N Engl J Med. 2023;388(2):117-27.
8. Bakris GL, Agarwal R, Anker SD, Pitt B, Ruilope LM, Rossing P, et al. Effect of Finerenone on Chronic Kidney Disease Outcomes in Type 2 Diabetes. N Engl
Oppsummering. I de siste 10 årene har det vært nærmest en revolusjon i kunnskap rundt nyrebeskyttende behandling, primært ved hjelp av nye legemidler. De nye medikamentstudiene innebærer alle «add-on»-behandling til RAS-blokkade. Standard medikamentell nyrebeskyttende behandling i dag er optimal blodrykkskontroll, hvor kombinert RAS-blokkade og SGLT 2 hemming i kombinasjon inngår som den sentrale delen av behandlingen. Finerenon og GLP-1-receptor agonisme (foreløpig semaglutid) er sannsynligvis også nyrebeskyttende behandling, men de er foreløpig ikke fullt utprøvd i
J Med. 2020;383(23):2219-29.
9. Pitt B, Filippatos G, Agarwal R, Anker SD, Bakris GL, Rossing P, et al. Cardiovascular Events with Finerenone in Kidney Disease and Type 2 Diabetes. N Engl J Med. 2021;385(24):2252-63.
10. Agarwal R, Filippatos G, Pitt B, Anker SD, Rossing P, Joseph A, et al. Cardiovascular and kidney outcomes with finerenone in patients with type 2 diabetes and chronic kidney disease: the FIDELITY pooled analysis. Eur Heart J. 2022;43(6):474-84.
11. Heerspink HJL, Sattar N, Pavo I, Haupt A, Duffin KL, Yang Z, et al. Effects of tirzepatide versus insulin glargine on kidney outcomes in type 2 diabetes in the SURPASS-4 trial: post-hoc analysis of an open-label, randomised, phase 3 trial. Lancet Diabetes Endocrinol. 2022;10(11):774-85.
12. Perkovic V, Tuttle KR, Rossing P, Mahaffey KW, Mann JFE, Bakris G, et al. Effects of Semaglutide on Chronic Kidney Disease in Patients with Type 2 Diabetes. N Engl J Med. 2024;391(2):109-21.
13. Colhoun HM, Lingvay I, Brown PM, Deanfield J, Brown-Frandsen K, Kahn SE, et al. Long-term kidney outcomes of semaglutide in obesity and cardiovascular disease in the SELECT trial. Nat Med. 2024;30(7):2058-66.
14. van Baar MJB, van der Aart AB, Hoogenberg K, Joles JA, Heerspink HJL, van Raalte DH. The incretin pathway as a therapeutic target in diabetic kidney disease: a clinical focus on GLP-1 receptor agonists. Ther Adv Endocrinol Metab. 2019;10:2042018819865398.
15. Melsom T, Fuskevag OM, Mathisen UD, Strand H, Schei J, Jenssen T, et al. Estimated GFR is biased by non-traditional cardiovascular risk factors. Am J Nephrol. 2015;41(1):7-15.
kombinasjon med RAS-blokkade og SGLT 2-hemming. Pasienter med visceral fedme og det metabolske syndrom er spesielt utsatt for progresjon av nyresykdom. Utover medikamentelle studier har vi des sverre ingen intervensjonsstudier som kan gi oss kunnskap om livsstil som reverserer det metabolske syndrom også kan bety noe for nyrene.
16. Hsu CY, McCulloch CE, Iribarren C, Darbinian J, Go AS. Body mass index and risk for end-stage renal disease. Ann Intern Med. 2006;144(1):21-8.
17. Tomaszewski M, Charchar FJ, Maric C, McClure J, Crawford L, Grzeszczak W, et al. Glomerular hyperfiltration: a new marker of metabolic risk. Kidney Int. 2007;71(8):816-21.
18. Stefansson VTN, Schei J, Solbu MD, Jenssen TG, Melsom T, Eriksen BO. Metabolic syndrome but not obesity measures are risk factors for accelerated age-related glomerular filtration rate decline in the general population. Kidney Int. 2018;93(5):1183-90.
19. Fritz J, Brozek W, Concin H, Nagel G, Kerschbaum J, Lhotta K, et al. The Association of Excess Body Weight with Risk of ESKD Is Mediated Through Insulin Resistance, Hypertension, and Hyperuricemia. J Am Soc Nephrol. 2022;33(7):1377-89.
20. Yu M, Ryu DR, Kim SJ, Choi KB, Kang DH. Clinical implication of metabolic syndrome on chronic kidney disease depends on gender and menopausal status: results from the Korean National Health and Nutrition Examination Survey. Nephrol Dial Transplant. 2010;25(2):469-77.
21. Kattah AG, Smith CY, Gazzuola Rocca L, Grossardt BR, Garovic VD, Rocca WA. CKD in Patients with Bilateral Oophorectomy. Clin J Am Soc Nephrol. 2018;13(11):1649-58.
22. Gluhovschi G, Gluhovschi A, Anastasiu D, Petrica L, Gluhovschi C, Velciov S. Chronic kidney disease and the involvement of estrogen hormones in its pathogenesis and progression. Rom J Intern Med. 2012;50(2):135-44.
23. Ma HY, Chen S, Du Y. Estrogen and estrogen receptors in kidney diseases. Ren Fail. 2021;43(1):619-42.
KRONISK NYRESYKDOM
• FORXIGA reduserte risikoen for det redusert eGFR ≥ 50 %, terminal nyresvikt,
• KUN FORXIGA, blant SGLT2-h, har sekundære endepunktet død uansett
HJERTESVIKT
DIABETES TYPE 2
• FORXIGA reduserte risikoen for det og forverring av hjertesvikt.*1
• KUN FORXIGA, blant SGLT2-h, reduserer alene, uavhengig av ejeksjonsfraksjon.
DIABETES TYPE 2
• FORXIGA reduserte risikoen for det eller sykehusinnleggelse for hjertesvikt UTEN kjent hjerte- og karsykdom.
• FORXIGA økte ikke risikoen for det MACE.*1
• FORXIGA reduserte risikoen for det primære endepunktet vedvarende redusert eGFR ≥ 50 %, terminal nyresvikt, renal eller CV død.*1
• KUN FORXIGA, blant SGLT2-h, har vist å redusere risikoen for det sekundære endepunktet død uansett årsak.**1,3
KRONISK
• FORXIGA reduserte risikoen for det primære endepunktet CV død og forverring av hjertesvikt.*1
• KUN FORXIGA, blant SGLT2-h, reduserer risikoen for CV død alene, uavhengig av ejeksjonsfraksjon.**1,3
HJERTESVIKT
KRONISK NYRESYKDOM
• FORXIGA reduserte risikoen for det primære endepunktet CV død eller sykehusinnleggelse for hjertesvikt hos pasienter MED og UTEN kjent hjerte- og karsykdom.*1
• Forxiga 10 mg skal ikke brukes ved T1D, hos gravide eller ammende.
• FORXIGA økte ikke risikoen for det andre primære endepunktet MACE.*1
• Behandlingen skal avbrytes midlertidig hos pasienter innlagt på sykehus for større kirurgiske inngrep eller ved akutte, alvorlige medisinske sykdommer
•
Referanse: 1. Felleskatalogen.no (20.nov. 2024) 2. Forxiga SPC pkt. 4.1, 4.2, 4.4
det primære endepunktet vedvarende nyresvikt, renal eller CV død.*1
INDIKASJONER:
har vist å redusere risikoen for det uansett årsak.**1,3
Praktisk informasjon:
• Behandling av utilstrekkelig kontrollert diabetes mellitus type 2 (T2D) hos voksne og barn ≥10 år, som tillegg til diett og fysisk aktivitet: Som monoterapi når metformin er uhensiktsmessig pga. intoleranse eller som tillegg til andre legemidler til behandling av T2D.
komplikasjonene ved 1
det primære endepunktet CV død
mg
Forxiga 10 mg skal ikke brukes ved T1D, hos gravide eller ammende. Brukes med forsiktighet ved økt risiko for diabetisk ketoacidose.
• Behandling av kronisk nyresykdom hos voksne.
• Behandling av symptomatisk kronisk hjertesvikt hos voksne.
eduserer risikoen for CV død ejeksjonsfraksjon.**1,3
REFUSJONSBERETTIGET BRUK:
DIABETES TYPE 2
det primære endepunktet CV død hjertesvikt hos pasienter MED og karsykdom.*1
det andre primære endepunktet
Behandlingen skal avbrytes midlertidig hos pasienter innlagt på sykehus for større kirurgiske inngrep eller akutte, alvorlige medisinske sykdommer.
• Som tillegg til annen blodsukkersenkende behandling ved diabetes type 2 (unntatt GLP-1analoger). Refusjonskoder: ICPC: T90 Diabetes type 2. ICD: E11 Diabetes mellitus type 2. Vilkår 264: Refusjon ytes i kombinasjon med metformin til pasienter som ikke oppnår glykemisk kontroll på behandling med metformin. Pasienter med etablert hjerte- og karsykdom og/eller nyresykdom kan starte med SGLT2 hemmer i kombinasjon med metformin som førstevalg.
KRONISK NYRESYKDOM
DOKUMENTERT EFFEKT2
Refusjonskoder
Vilkår
• Behandling av pasienter med kronisk nyresykdom med bekreftet albuminuri (eGFR 25-75 mL/ min/1.73m² og albumin/kreatinin-ratio i urin over 20 mg/mmol). Refusjonskoder: ICPC: U99 Nyresvikt kronisk. ICD: N18 Kronisk nyresykdom.Vilkår 260: Refusjon ytes kun i kombinasjon med optimalisert behandling med RAAShemmer, enten ved bruk av ACE-hemmer eller angiotensin II-reseptorblokker (ARB).
HJERTESVIKT
Praktisk informasjon:
Forxiga 10 mg skal ikke brukes ved T1D, hos gravide eller ammende.
• Behandling av symptomatisk kronisk hjertesvikt hos voksne. Refusjonskoder: ICPC: K77. Hjertesvikt. ICD: I50 Hjertesvikt.
T2D og etablert hjerte- og karsykdom og/eller nyresykdom*
VIKTIG INFORMASJON
Brukes med forsiktighet ved økt risiko for diabetisk ketoacidose.
Metformin
FORXIGA reduserte risikoen for det primære endepunktet vedvarende redusert eGFR ≥ 50 %, terminal nyresvikt, renal eller CV død.*1
FORXIGA + metformin T2D
CKD med min/1.73m uAKR
Behandlingen skal avbrytes midlertidig hos pasienter innlagt på sykehus for større kirurgiske inngrep eller akutte, alvorlige medisinske sykdommer.
Anbefalt dosering: 10 mg 1 gang daglig. Det er ikke anbefalt å starte behandling ved GFR < 25 ml/min. Ved GFR < 45 ml/min skal ekstra glukosesenkende behandling vurderes hos T2D pasienter med behov for ytterligere glykemisk kontroll.
Ved alvorlig nedsatt leverfunksjon er anbefalt startdose 5 mg.
Utvalgt sikkerhetsinformasjon:
• Brukes med forsiktighet ved økt risiko for diabetisk ketoacidose.
KUN FORXIGA, blant SGLT2-h, har vist å redusere risikoen for det sekundære endepunktet død uansett årsak.**1,3
• Pasienter med albuminuri kan ha mer nytte av behandling med Forxiga. Ingen erfaring med behandling av kronisk nyresykdom hos pasienter uten diabetes som ikke har albuminuri.
• Begrenset erfaring med Forxiga i NYHA-klasse IV.
FORXIGA
• Forsiktighet utvises der Forxiga-indusert blodtrykksfall kan utgjøre risiko.
Praktisk informasjon:
2. linje behandling
(Dersom man ikke oppnår glykemisk kontroll med metformin alene)
Forxiga 10 mg skal ikke brukes ved T1D, hos gravide eller ammende.
• Kan gi økt nyreutskillelse av litium. Pasienten skal henvises til forskrivende lege for overvåking av serumkonsentrasjon.
FORXIGA reduserte risikoen for det primære endepunktet CV død og forverring av hjertesvikt.*1
• Kan gi økt hematokrit. Pasienter med uttalte økninger i hematokrit skal overvåkes og undersøkes for underliggende hematologisk sykdom.
Bivirkninger: Svært vanlige: Hypoglykemi (når brukt med sulfonylurea (SU) eller insulin)). Vurder en lavere dose av insulin/ SU for å redusere denne risikoen ved T2D. Vanlige: Genitale infeksjoner, urinveisinfeksjoner. Mindre vanlige: Volumdeplesjon inkl. hypotensjon. Sjeldne bivirkninger: Diabetisk ketoacidose (ved T2D). Svært sjeldne: Fourniers gangren.
Reseptgruppe C.
KUN FORXIGA, blant SGLT2-h, reduserer risikoen for CV død alene, uavhengig av ejeksjonsfraksjon.**1,3
Refusjonskoder Vilkår
T90, E11 264 1. linje behandling
Pakninger og priser: 10 mg: 28 stk. kr 450. 98 stk. kr 1432,30. For mer info. om Forxiga, les FK tekst på www.felleskatalogen.no eller SPC
NO-12728-08-24-CVRM
FORXIGA reduserte risikoen for det primære endepunktet CV død eller sykehusinnleggelse for hjertesvikt hos pasienter MED og UTEN kjent hjerte- og karsykdom.*1

Skann QR-koden for å registrere din e-post slik at du kan motta invitasjoner til møter, e-læringsprogrammer og mer digitalt.
FORXIGA økte ikke risikoen for det andre primære endepunktet MACE.*1
Brukes med forsiktighet ved økt risiko for diabetisk ketoacidose.
Behandlingen skal avbrytes midlertidig hos pasienter innlagt på sykehus for større kirurgiske inngrep eller akutte, alvorlige medisinske sykdommer.



– en litteraturstudie av kommunikasjon mellom leger og pasienter med ikke-malign
Både nasjonale og internasjonale retningslinjer anbefaler integrering av palliasjon ved uhelbredelig sykdom, også for andre diagnosegrupper enn kreft. Kommunikasjon mellom leger og pasienter om palliasjon ved uhelbredelig, ikke-malign lungesykdom, forekommer ikke like ofte som pasientene ønsker. Helsevesenet bør ha rutiner for å fange opp pasientenes behov tidlig i forløpet.
Nina Marie Undeland1 og Vilde Holand Juberg 1*, stud. med., Universitetet i Bergen og Margrethe Aase Schaufel, overlege og førsteamanuensis, Lungeavdelingen, Haukeland Universitetssykehus og Universitetet i Bergen, Forskningsleder, Kompetansesenter i lindrande behandling Helseregion Vest, *delt førsteforfatterskap
Introduksjon Palliasjon defineres av Verdens helse organisasjon som «en tilnærmingsmåte som har til hensikt å forbedre livskvaliteten til pasienter og deres familier i møte med livstruende sykdom, gjennom forebygging og lindring av lidelse, ved tidlig identifisering, grundig kartlegging, vurdering og behandling av smerte, og andre problemer av fysisk, psykososial og åndelig art» (1). Helsedirektoratets faglige råd for forhåndssamtaler og planlegging ved begrenset forventet levetid slår fast at dette bør tilbys pasienter med alvorlig, uhelbredelig sykdom eller høy risiko for alvorlige sykdomsepisoder (2). Dette omfatter en stor del av den lungemedisinske populasjonen, og integrering av palliasjon er understreket i retningslinjer både for kols og interstitielle lungesykdommer (3,4). Det kan være utfordrende både for helsepersonell og pasienter med lungesykdom å snakke om temaer knyttet til begrenset levetid, og vanskelig å etablere rutiner for dette på travle sengeposter eller poliklinikk (5,6). Vi ville undersøke hvordan og når i sykdomsforløpet leger snakker om prognose og palliasjon med pasienter med ikke-malign lungesykdom, hva som er det ideelle tidspunktet for samtalene, samt å identifisere barrierer og tilretteleggende faktorer.
Metode
Vi gjennomførte et systematisk litteratur søk høsten 2023 i PubMed etter PRISMA-retningslinjer i samarbeid med universitetsbibliotekar (figur 1). Vi brukte både fritekstsøk og MeSH-søk, med søkeelementer i fire kategorier; ikke-malign lungesykdom, dårlig prognose, kommunikasjon og lege-pasient forhold. Utvelgelse av materialet ble gjort i to trinn ved hjelp av Rayyan screeningverktøy. Det første søket i PubMed gav 194 treff. I et supplerende søk la vi til søkeord som omhandlet «prognose». Det totale antallet artikler i førstetrinnssorteringen ble derfor n=376. NMU og VHJ leste abstraktene hver for seg og sorterte ved hjelp av inklusjons- og eksklusjonskriterier. Artikler som omhandlet pasienter med uhelbredelig, ikke-malign sykdom uten malign komorbiditet, personer over 18 år, kommunikasjon mellom lege og pasient om prognose eller palliativ behandling og var basert på empiriske studier (både kvalitative og kvantiative) ble inkludert. Vi ekskluderte artikler med pasienter med alvorlig demens eller uten samtykkekompetanse, teori- eller oversiktsartikler, studier som hovedsakelig omhandlet valg av prognostiske verktøy og artikler som ikke var tilgjengelig på engelsk eller norsk. Ved gjennomgang av
abstraktene ble 48 artikler inkludert. Etter gjennomgang av fulltekst manuskripter inkluderte vi 14 artikler publisert mellom 2001 og 2023, og sammenstilte resultater på tvers av de ulike studiene.
Resultat
14 artikler ble inkludert. Vi identifiserte fire hovedfunn i studiene: 1) forekomst av samtaler om palliasjon og livets slutt mellom lege og pasient; 2) barrierer for slike samtaler; 3) tilretteleggende faktorer; og 4) timing og det ideelle tidspunkt for å ha slike samtaler.
Forekomst av samtaler om palliasjon mellom lege og pasient
Forekomst av samtaler mellom lege og pasient om palliasjon og prognose ble beskrevet noe ulikt i de inkluderte studiene. Cicak og kolleger avdekket at 77% av pasientene med kols > 65 år ved et universitetssykehus i Kroatia ikke hadde hatt samtaler om palliasjon med helsepersonell, samtidig som et flertall ønsket dette (7). Curtis og medarbeidere fant at 74,8% av pasientene med alvorlig kols ved tre sykehus i USA ikke hadde hatt samtaler om prognose (8). En annen måte å belyse temaet på, er å undersøke hvorvidt pasienter har hatt samtaler med sin lege om hvilken type behandling de ønsker å få dersom de
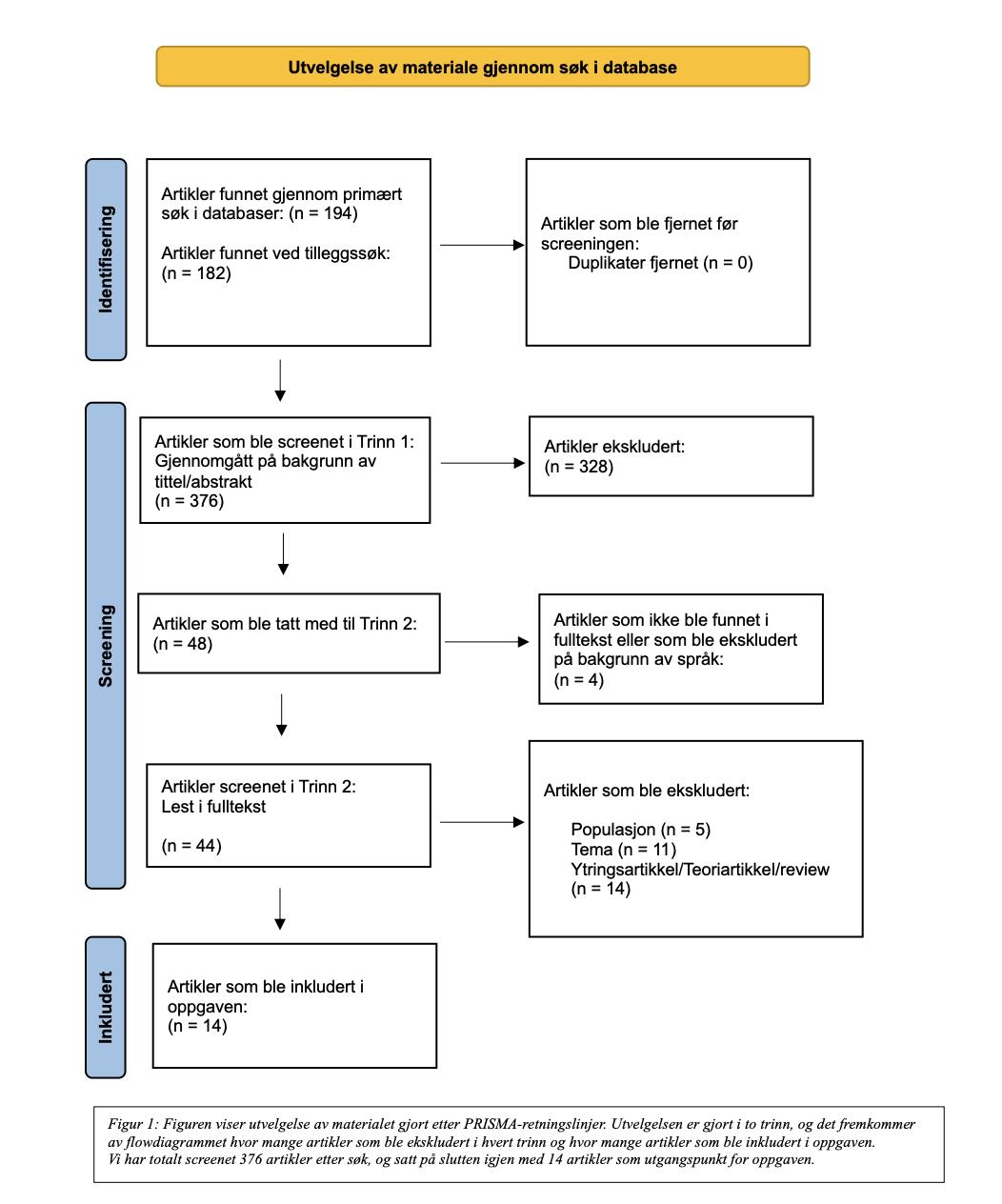
Figur 1: Figuren viser utvelgelse av materialet gjort etter PRISMA-retningslinjer. Utvelgelsen er gjort i to trinn, og det fremkommer av flowdiagrammet hvor mange artikler som ble ekskludert i hvert trinn og hvor mange artikler som ble inkludert i oppgaven. Vi har totalt screenet 376 artikler etter søk, og satt på slutten igjen med 14 artikler som utgangspunkt for oppgaven.
blir for syke til å kunne snakke for seg selv. Knauft og kolleger studerte dette hos pasienter med kols og oksygenkrevende respirasjonssvikt, hvor det kommer frem at kun en tredjedel av pasientene (32%) hadde diskutert slike ønsker med sin behandler (9). En studie av portugisiske lungeleger fant at 67,1% sjeldent eller aldri hadde tatt initiativ til diskusjoner med pasientene sine om behandling og omsorg ved livets slutt (10).
Barrierer for samtaler om palliasjon Mange av studiene identifiserte faktorer som hindret at samtaler om palliasjon og prognose fant sted. Akiyama og medarbeidere intervjuet behandlere av pasienter med lungefibrose, og kategoriserte barrierene i seks ulike domener: lite etablert behandling og vanskeligheter med å beregne prognose, diskrepans i forståelse og behandlingsmål blant pasienter, familie
og medisinsk personell, inadekvat kommunikasjon om behandlingsmål, urealistiske forventninger hos pasientene, urealistiske forventninger hos familien og mangel på trening i palliativ behandling hos behandleren (11). Det ble rapportert press på behandlere og ønske om å få beholde en positiv innstilling, som hindret samtaler om prognose og behandlingsalternativer (12). Barrierene kunne også kategoriseres
som lege-identifisert eller pasientidentifisert, og både leger og pasienter pekte på emosjonelle og systematiske barrierer. Ecenarro og kolleger viste at hele 75,7% av legene mente det var en barriere for kommunikasjon at det ikke fantes egnede rutiner og retningslinjer ved deres arbeidssted (13). Andre studier påviste tilbakeholdenhet med å tilby palliativ behandling til pasienter med kols sammenlignet med kreftpasienter (14) og at mange leger ikke var klar over at disse pasientene ville ha behov for palliativ behandling (15). I tillegg følte ikke legene seg tilstrekkelig forberedt til å ha slike samtaler med pasientene, og 87,5% av behandlere opplevde mangel på erfaring med og kunnskap om kommunikasjon (13). En emosjonell barriere var frykt fra legenes side om å ødelegge pasientens håp ved å introdusere samtaler om livets slutt (9,10,13). Tidsaspektet ble trukket frem både av leger og pasienter i flere av studiene, der lav bemanning, lange ventetider og økt arbeidsbyrde for helsepersonell gav mindre tid til hver pasient (14). I en studie mente 64% av legene at det var for lite tid til å ta opp alle temaene som burde diskuteres under en konsultasjon (9), og 38,2% av legene i en annen studie oppgav å ha for lite tid til å prioritere samtaler om palliasjon (10). Noen pasienter rapporterte at fastlegen hadde lite tid til å diskutere slike temaer, og at de derfor foretrakk å ha slike samtaler med en spesialist (16).
Tilretteleggende faktorer for samtaler om palliasjon
De aller fleste inkluderte studiene understreket viktigheten av et godt lege-pasient-forhold som en tilrettelegger for å snakke om vanskelige temaer. Åpen, tydelig og ærlig forklaring av sykdomsforløp og behandlingsalternativer var ønsket av mange pasienter, og kommunikative ferdigheter (17, 18) og kunnskap om pasientens preferanser (19) kunne fremme samtaler om livets sluttfase. De tre vanligste tilretteleggerne fra
pasientens side var at pasientens familie eller venner hadde gått bort (88%), at pasienten stolte på legen (87%), at legen var flink til å behandle lungesykdom (83%) og at legen «bryr seg om meg som person» (83%) (9). En av flere legestrategier for å legge til rette for samtaler om prognose og palliasjon var å begynne samtalene tidlig og gradvis i sykdomsforløpet, fordi man da hadde bedre mulighet for å gi pasientopplæring og gjennom dette introdusere informasjon om forventet levetid (14,15). Et av argumentene for å ta initiativ til samtaler om palliativ behandling og prognose, var kunnskapen om at mange pasienter ønsker det og at det kan ha en positiv effekt. En av studiene viste at 67,7 % av pasientene med kols ønsket å ha diskusjoner med sin behandler om preferanser rundt behandling ved livets slutt (19), og det kom også frem at majoriteten mente slike samtaler var viktige (7). Elkington og medarbeidere rapporterte at 72,5 % av fastlegene mente samtaler om prognose ofte var «nødvendig» eller «essensielt» i håndteringen av kols, men at dette likevel var vanskelig i praksis grunnet flere barrierer (20).
Timing og det ideelle tidspunkt for samtaler om palliasjon. Ni av de inkluderte artiklene kom inn på timingen av samtale om behandling i livets siste fase, palliativ behandling eller forhåndssamtaler. I Akiyamas studie blant lungeleger om palliativ behandling for pasienter med idiopatisk lungefibrose, fremkom det at legene mente samtaler med pasientene om behandling og omsorg ved livets slutt ble gjennomført signifikant senere enn det ideelle tidspunktet (11). Nesten halvparten av legene (46,9%) mente at det beste tidspunktet var ved oppstart av oksygenbehandling hjemme, mens 19 % mente at det var ved sykehusinnleggelse på grunn av akutt forverring. Bare 10 % mente at den ideelle timingen var ved diagnosetidspunktet. Den faktiske timingen
var imidlertid hovedsakelig under syke husinnleggelser på grunn av akutte forverringer (59,1 %), etterfulgt av ved oppstart av hjemmebehandling med oksygen (20%). I bare 3,6 % av tilfellene ble samtalen innledet ved diagnostiseringstidspunktet. Gaspar og kolleger fant at 29,4 % av lungelegene mente samtalene burde skje under en alvorlig kolsforverring, mens 25 % mente tidspunktet vare best ved langtkommet sykdom, men hvor pasienten var stabil (10). En annen studie fant at 53 % av pasientene mente at samtalene om palliativ behandling og omsorg ved livets slutt burde skje i en fase med hyppige sykehusinnleggelser (7). Noen av studiene påpekte imidlertid at det kan være problematisk å innlede en samtale om palliasjon under en sykdomsforverring, da pasientene kan være for dårlige til å delta i diskusjoner på en optimal måte (16-18).
Diskusjon
Resultatene i denne litteraturstudien viser at det er begrenset hvor mye behandlere og pasienter med uhelbredelig, ikke-malign lungesykdom snakker om palliasjon og livets siste fase. I enkelte studier kommer det frem at nesten 90% av de intervjuede pasientene ikke har snakket om livets siste fase og døden med sin lege (8), mens et flertall av pasientene ønsker å ha samtaler med sin behandler om dette (7, 19). Vi mener disse resultatene viser at denne pasientgruppen har et behov som ikke dekkes i tilstrekkelig grad av helsevesenet. Flere av studiene peker på mangelfullt kunnskapsgrunnlag om palliasjon hos behandlere (9, 13). Selv om ingen av studiene konkret peker på lite kunnskap som en barriere for samtaler om behandling og omsorg ved livets slutt, er det likevel vårt inntrykk at mangel på kunnskap om hva palliativ behandling innebærer nettopp fungerer som dette. Døden og livets siste fase er et følelsesladd og vanskelig tema, og antallet emosjonelle barrierer som trekkes frem i flere av studiene illustrerer dette godt. Både leger,
pasienter og pårørende trekker frem behov for å ha en positiv innstilling, og at samtaler som omhandler livets siste fase kan hindre dette.
Flere av studiene peker på mangel på retningslinjer og protokoller som barrierer mot å snakke om palliasjon. Når man nå skal implementere Helsedirektoratets faglige råd for forhåndssamtaler i Norge, tror vi at disse funnene er interessante både med tanke på barrierer, tilrettelegging og timing. Både primær- og spesialisthelsetjenesten bør ha et system for gjennomføring av forhåndssamtaler, som innebærer en kommunikasjonsprosess med oppfølgende samtaler ved vendepunkter i sykdomsforløpet (2). Eksempler på vendepunkter er forverring, alvorlige sykdomsepisoder, endring eller avslutning av behandling, herunder livsforlengende behandling. Av tilretteleggende faktorer som kan gjøre det lettere å ta initiativ til samtaler om palliativ behandling og prognose, er det lite tvil om at lege-pasientforholdet er
Referanser:
1 Helsedirektoratet. Nasjonalt handlingsprogram med retningslinjer for palliasjon i kreftomsorgen. Oslo: Helsedirektoratet; 2019. https://www.helsedirektoratet.no/retningslinjer/palliasjon i kreftomsorgenhandlingsprogram
2 Helsedirektoratet. Forhåndssamtaler og planlegging ved begrenset forventet levetid. Oslo: Helsedirektoratet; 2023. https://www.helsedirektoratet.no/faglige rad/Forhandssamtaler ogplanleggingved begrensetforventet levetid/ forhandssamtaler#pasientermed begrensetforventet levetid borfatilbud omforhandssamtaler
3 Janssen DJA, Bajwah S, Boon MH, Coleman C, et al. European Respiratory Society clinical practice guideline: palliative care for people with COPD or interstitial lung disease. Eur Respir J. 2023 Aug 17;62(2):2202014. doi: 10.1183/13993003.02014-2022. PMID: 37290789.
4 Norsk forening for lungemedisin. Veileder for kols Den norske legeforeningen: Den norske legeforeningen; 2022. https://www.legeforeningen.no/foreningsledd/ fagmed/norskforening for lungemedisin/fag/ obstruktive lungesykdommer/retningslinjerforkols/?chapter=1
5 Hjorth NE, Haugen DF, Schaufel MA. Advance care planning in life-threatening pulmonary disease: a focus group study. ERJ Open Res. 2018 May 18;4(2):00101-2017. doi: 10.1183/23120541.001012017. PMID: 29796390; PMCID: PMC5958273.
6 Hjorth NE, Schaufel MA, Sigurdardottir KR, Haugen DRF. Feasibility and acceptability of introducing advance care planning on a thoracic medicine inpatient ward: an exploratory mixed method study. BMJ Open Respir Res. 2020 Feb;7(1):e000485. doi: 10.1136/ bmjresp-2019-000485. PMID: 32107203; PMCID: PMC7047484.
7 Čič ak P, Thompson S, Popović -Grle S, Fijač ko V, Lukinac J, Lukinac AM. Palliative and End-of-Life Care Conversations with Older People with Chronic Obstructive Pulmonary Disease in Croatia-A Pilot
viktig. Pasienter er mer komfortable med å være sårbare i samtaler med leger som de selv oppfatter er gode på å lytte, og hvor de selv føler at de har kontroll over samtalen (18). Et økende fokus på lege-pasientforholdet og kommunikasjonstrening på medisinstudiet og i spesialiseringen kan gjøre leger bedre rustet til å ha samtaler om vanskelige tema.
Vi kan ikke utelukke at vi ved å begrense søket til én database har gått glipp av noen relevante artikler som kunne ha vært fanget opp ved et bredere søk. Under sorteringen valgte vi også å ekskludere studier som omhandler både malign og ikke-malign lungesykdom for å få et rent ikke-malignt fokus. Vi er kjent med at det foreligger kunnskap også fra norske fagmiljøer som har inkludert pasienter med både malign og ikke-malign lungesykdom i sitt materiale (5,6). Dette gjør at vi kan ha gått glipp av relevant kunnskap. Vi valgte å inkludere eldre artikler som vi vurderte kunne ha viktige
Study. Healthcare (Basel). 2020 Aug 20;8(3):282. doi: 10.3390/healthcare8030282. PMID: 32825316; PMCID: PMC7551859.
8 Curtis JR, Engelberg RA, Nielsen EL, Au DH, Patrick DL. Patient-physician communication about end-of-life care for patients with severe COPD. Eur Respir J. 2004 Aug;24(2):200-5. doi: 10.1183/09031936.04.00010104. PMID: 15332385.
9 Knauft E, Nielsen EL, Engelberg RA, Patrick DL, Curtis JR. Barriers and facilitators to end-of-life care communication for patients with COPD. Chest. 2005 Jun;127(6):2188-96. doi: 10.1378/chest.127.6.2188. PMID: 15947336.
10 Gaspar C, Alfarroba S, Telo L, Gomes C, Bárbara C. End-of-life care in COPD: a survey carried out with Portuguese pulmonologists. Rev Port Pneumol. 2014 May-Jun;20(3):123-30. English, Portuguese. doi: 10.1016/j.rppneu.2014.01.008. Epub 2014 Mar 21. PMID: 24661960.
11 Akiyama N, Fujisawa T, Morita T, Mori K, Yasui H, Hozumi H, et al. Palliative Care for Idiopathic Pulmonary Fibrosis Patients: Pulmonary Physicians’ View. J Pain Symptom Manage. 2020;60(5):933-40.
12 Braithwaite M, Philip J, Tranberg H, Finlayson F, Gold M, Kotsimbos T, Wilson J. End of life care in CF: patients, families and staff experiences and unmet needs. J Cyst Fibros. 2011 Jul;10(4):253-7. doi: 10.1016/j. jcf.2011.03.002. Epub 2011 Mar 27. PMID: 21444251.
13 Ecenarro PS, Iguiñiz MI, Tejada SP, Malanda NM, Imizcoz MA, Marlasca LA, Navarrete BA. Management of COPD in End-of-Life Care by Spanish Pulmonologists. COPD. 2018 Apr;15(2):171-176. doi: 10.1080/15412555.2018.1441274. Epub 2018 Mar 20. PMID: 29558226.
14 Tavares N, Jarrett N, Wilkinson TMA, Hunt KJ. Patient-Centered Discussions About Disease Progression, Symptom, and Treatment Burden in Chronic Obstructive Pulmonary Disease Could Facilitate the Integration of End-of-Life Discussions in the Disease Trajectory: Patient, Clinician, and Literature Perspectives: A Multimethod Approach. J Palliat Med. 2023
funn, men dette gjør at erfaringer og meninger kan ha endret seg fra publisering til dagens praksis.
Konklusjon
Basert på de inkluderte studier synes kommunikasjon om palliasjon å forekomme sjeldnere enn pasientene ønsker. For at dette skal kunne forbedres, må man overkomme barrierer som mangel på kunnskap og frykt for å ødelegge pasientenes håp og positive innstilling. God relasjon mellom lege og pasient, rutiner for å fange opp pasientenes behov tidlig i behandlingsforløpet, som systematisk invitasjon til og opplæring i forhåndssamtaler, kan fungere som tilretteleggende faktorer.
Artikkelen er en forkortet versjon av Undeland og Jubergs hovedoppgave ved Det medisinske fakultet, Universitetet i Bergen. Oppgaven i sin helhet kan formidles på forespørsel.
Mar;26(3):353-359. doi: 10.1089/jpm.2022.0028. Epub 2022 Oct 12. PMID: 36251863.
15 Halliwell J, Mulcahy P, Buetow S, Bray Y, Coster G, Osman LM. GP discussion of prognosis with patients with severe chronic obstructive pulmonary disease: a qualitative study. Br J Gen Pract. 2004 Dec;54(509):904-8. PMID: 15588534; PMCID: PMC1326107.
16 Tavares N, Hunt KJ, Jarrett N, Wilkinson TM. The preferences of patients with chronic obstructive pulmonary disease are to discuss palliative care plans with familiar respiratory clinicians, but to delay conversations until their condition deteriorates: A study guided by interpretative phenomenological analysis. Palliat Med. 2020 Dec;34(10):1361-1373. doi: 10.1177/0269216320937981. Epub 2020 Jul 28. PMID: 32720555.
17 Owusuaa C, van Lent LGG, van ‘t Spijker A, van der Rijt CCD, van der Heide A. Discussing prognosis and the end of life with patients with advanced cancer or COPD: A qualitative study. PLoS One. 2022 Sep 9;17(9):e0274201. doi: 10.1371/journal.pone.0274201. PMID: 36084060; PMCID: PMC9462714.
18 Hobler MR, Engelberg RA, Curtis JR, Ramos KJ, Zander MI, Howard SS, Goss CH, Aitken ML. Exploring Opportunities for Primary Outpatient Palliative Care for Adults with Cystic Fibrosis: A Mixed-Methods Study of Patients’ Needs. J Palliat Med. 2018 Apr;21(4):513-521. doi: 10.1089/jpm.2017.0259. Epub 2018 Jan 3. PMID: 29298400; PMCID: PMC5915258.
19 Au DH, Udris EM, Engelberg RA, Diehr PH, Bryson CL, Reinke LF, Curtis JR. A randomized trial to improve communication about end-of-life care among patients with COPD. Chest. 2012 Mar;141(3):726-735. doi: 10.1378/chest.11-0362. Epub 2011 Sep 22. PMID: 21940765; PMCID: PMC3415164.
20 Elkington H, White P, Higgs R, Pettinari CJ. GPs’ views of discussions of prognosis in severe COPD. Fam Pract. 2001 Aug;18(4):440-4. doi: 10.1093/fampra/18.4.440. PMID: 11477053.
Norske indremedisinere har stor glede og nytte av Indremedisineren (IM). IM bidrar til faglig utvikling og er både et viktig bindeledd i miljøet, og mellom styret i NIF og det enkelte medlem.
Redaksjonen og alle bidragsytere jobber på dugnad. Dere annonsører bidrar til at vi kan utgi et flott IM og at vi kan drifte indremedisineren.no, der trafikken er sterkt økende. Uten deres hjelp hadde det ikke vært mulig.
Vi håper det gode samarbeidet fortsetter, og at dere blir med videre!















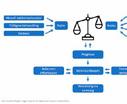









Indikasjon: Tezspire er indisert som tillegg til vedlikeholdsbehandling hos voksne og ungdom i alderen 12 år og eldre med alvorlig astma som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling.
Dosering: Anbefalt dose: 210 mg s.c. hver 4. uke. Tezspire er til langtidsbehandling. Forsiktighetsregler: Skal ikke brukes til å behandle akutte astmaeksaserbasjoner. Astmarelaterte symptomer eller eksaserbasjoner kan oppstå. Pasienten bør instrueres om å oppsøke lege hvis astmaen forblir ukontrollert eller forverres. Alvorlige infeksjoner bør behandles før oppstart av behandling. Ved utvikling av alvorlig infeksjon under behandling, bør behandlingen seponeres inntil denne er over. Graviditet og amming: Bruk under graviditet bør unngås med mindre forventet nytte for den gravide oppveier mulig risiko for fosteret.
Vanlige bivirkninger: Faryngitt, utslett, artralgi, reaksjon på injeksjonsstedet.
Pakninger og priser: Injeksjonsvæske, oppløsning i ferdigfylt penn (210 mg): 1 stk: kr. : 15 053,40. Injeksjonsvæske, oppløsning i ferdigfylt sprøyte (210 mg): 1 stk. kr. : 15 053,40
Reseptgruppe: C. Refusjon: H-resept. Refusjonsberettiget bruk: Der det er utarbeidet nasjonale handlingsprogrammer/nasjonal faglig retningslinje og/eller anbefalinger fra RHF/LIS spesialistgruppe skal rekvirering gjøres i tråd med disse. Vilkår: 216 Refusjon ytes kun etter resept fra sykehuslege eller avtalespesialist. Tezspire inngår i RHF anbefalinger for alvorlig ukontrollert T2-høy astma.
Beslutning i Beslutningsforum for nye metoder 18.03.2024. Tezepelumab (Tezspire) innføres som tillegg til vedlikeholdsbehandling ved alvorlig astma med eosinofili hos voksne og ungdom i alderen 12 år og eldre som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling.
For fullstendig informasjon, les mer på www.felleskatalogen.no
Referanser:
ID: NO-13578-01-2025-TEZ
1. Busse WW. Biological treatments for severe asthma: a major advance in asthma care. Allergol Int 2019;68:158-66. 2. Tran TN, Zeiger RS, Peters SP et al. Overlap of atopic, eosinophilic, and T 2-high asthma phenotypes in a general population with current asthma. Ann Allergy Asthma Immunol 2016;116:37-42. 3. Kupczyk M, Dahlén B, Sterk PJ et al. Stability of phenotypes defined by physiological variables and biomarkers in adults withasthma. Allergy 2014;69:1198-1204. 4. Chipps BE, Soong W, Panettieri Jr RA et al. Number of patient-reported asthma triggers predicts uncontrolled disease among specialist-treated patients with severe asthma. Ann Allergy Asthma Immunol 2023;130:784-90. 5. Menzies-Gow A, Wechsler ME, Brightling CE. Unmet need in severe, uncontrolled asthma: can anti-TSLP therapy with tezepelumabprovide a valuable new treatment option? Respir Res 2020;21:268. 6. Gauvreau GM, Sehmi R, Ambrose CS et al. Thymic stromal lymphopoietin: its role and potential as a therapeutic target in asthma. Expert Opin Ther Targets 2020;24:777–92. 7. Gauvreau GM, Sehmi R, Ambrose CS et al. Thymic stromal lymphopoietin: its role and potential as a therapeutic target in asthma. Expert Opin Ther Targets 2020;24:777-92. 8. Tezspire SPC. 4.1, 4.2, 4.4, 4.8, 5.1. 9. Corren J, Karpefors M, Hellquist A et al. Tezepelumab reduces exacerbations across all seasons in patients with severe, uncontrolled asthma: a post hoc analysis of the PATHWAY phase 2b study. J Asthma Allergy 2021;14:1-11.

Har du pasienter med alvorlig allergisk eosinofil astma, med symptomer som forverres under pollensesongen? Eller av andre triggere gjennom ulike årstider?
Alvorlig astma er sammensatt og individuell1-4, ofte utløst av ulike triggere som aktiverer signalcytokinet TSLP* i luftveisepitelet5. TSLP kan sette i gang multiple inflammasjonsdrivere, som kan variere gjennom hele året.6
Tezspire (tezeplumab) blokkerer TSLP fra toppen av inflammasjonskaskaden5,7,8 og reduserer forverringer med mellom 67 og 82 % gjennom de ulike årstidene - hele året9
Les mer på azconnect.no/astma-triggere
Indikasjon:8 Tezspire er indisert som tillegg til vedlikeholdsbehandling hos voksne og ungdom i alderen 12 år og eldre med alvorlig astma som er utilstrekkelig kontrollert til tross for høye doser inhalasjonskortikosteroider i tillegg til et annet legemiddel for vedlikeholdsbehandling.
Forsiktighetsregler:8 Skal ikke brukes til å behandle akutte astmaeksaserbasjoner.
Vanlige bivirkninger:8 Faryngitt, utslett, artralgi, reaksjon på injeksjonsstedet.
* TSLP: tymisk stromal lymfopoietin
Dagens barnevaksinasjonsprogram inkluderer 12 vaksiner, som beskytter barn mot en rekke infeksjonssykdommer slik som f.eks. difteri, tetanus og pertussis (DTP). Folkehelseinsituttet (FHI) har foreslått et tilsvarende vaksinasjonsprogram for voksne, og Stortinget har vedtatt å etablere et Voksenvaksinsjonsprogram for eldre og enkelte risikogrupper. Hva innebærer voksenvaksinasjonsprogrammet? Hvorfor ønsker regjeringen og Stortinget å etablere et slikt program, og hva er fordelene og ulempene ved det forslaget som er vedtatt?

Hva foreslår regjeringen i Voksenvaksinasjonsprogrammet?
Til tross for at også voksne, eldre og personer i risikogrupper er anbefalt å ta flere vaksiner, har vi frem til nå ikke hatt noe tilsvarende vaksinasjonsprogram for voksne som for barn. Regjeringen vil imidlertid nå endre forskriften om nasjonalt vaksinasjonsprogram før sommeren 2025, slik at vaksinasjon av eldre og personer i risikogrupper vil kunne starte høsten 2025 (1).
Programmet som nå er vedtatt, vil innebære:
- Årlig vaksinasjon mot sesonginfluensa til personer 65 år og eldre, samt personer 0-64 år i andre risikogrupper.
- Årlig vaksinasjon mot Covid19 for personer 65 år og eldre, samt personer 0-64 år i andre risikogrupper.
- Vaksinasjon mot pneumokokksykdom for alle kommende årskull med 65-åringer.
Det er også foreslått en påminnelsesløsning for personer med aldersindikasjon for vaksinene i programmet, som det vil være mulig å reservere seg fra.
Hvorfor ønsker regjering og Storting å innføre voksenvaksinasjonsprogrammet? Folkehelseinstituttet (FHI) utredet i 2018 en modell for et vaksinasjonsprogram for voksne og risikogrupper på oppdrag fra Helse- og omsorgsdepartementet (HOD). I utredningen
fra 31. oktober 2018 anbefalte FHI å etablere et vaksinasjonsprogram for voksne og risikogruppe for å bl.a. forbedre folkehelsen, redusere helsetjenestekostnader og utjevne sosiale ulikheter. Andre mål med vaksinasjonsprogrammet, er å øke forebygging av sykdommer, redusere antibiotikabruk, og sikre likeverdig tilgang til vaksiner (2).
Helse- og omsorgsminister Jan Christian Vestre uttalte ved sin presentasjon av forslaget til Statsbudsjettet i oktober 2024 at det er viktig å gi et vaksinasjonstilbud til hele den voksne befolkningen, og styrke vår beredskap (3).
Hva er fordelene og ulempene ved voksenvaksinasjonsprogrammet?
En av fordelene ved et vaksinasjonsprogram for voksne, er at det kan bidra til at færre innleggelser av voksne, eldre og personer i risikogruppene, pga. influensa, Covid19 og pneumokokkinfeksjon. Dette vil forebygge sykdom og død for de som får vaksinere mot disse infeksjonene og minske antall innleggelser på medisinske avdelinger. Legeforeningen viste i sin høringsuttalelse til at Folke helseinstituttet (FHI) i en bekymringsmelding høsten 2024 skrev at mer enn 13.000 personer ble innlagt på norske sykehus på grunn av influensa- eller koronasykdom forrige vinter, samtidig som antall personer som tok vaksine mot de to sykdommene gikk ned (4). Vaksinene er derfor viktige for å forebygge sykdom og sykehusinnleggelser.
Det er kommunene som skal gjennomføre vaksineringen. En utfordring med voksenvaksinasjonsprogrammet som er vedtatt, er at finansieringen vil komplisere kommunenes administrering av vaksinene, vanskeliggjøre informasjon til de som skal få vaksinene og kan svekke oppslutningen om vaksineringen (5): Dette har sammenheng med at de som skal ta vaksinene, må betale 100% for influensavaksinen og 25% egenbetaling for korona- og pneumokokkvaksinene. Dette vil kunne gjøre det vanskeligere for kommunene å sikre høy vaksinasjonsdekning, spesielt for influensavaksinen, som inbyggerne må betale fullt ut selv. For å sikre best mulig vaksinasjonsdekning, burde vaksinene vært kostnadsfrie for innbyggerne å ta. Selv om de fleste har råd til å betale hele eller eller deler av vaksinene, kan det gjøre terskelen for at alle tar vaksinene, høyere og det bør man unngå for å sikre best mulig oppslutning om vaksinene. Siden det er viktig med vaksiner mot influensa, Covid-19 og pneumokokk for å forebygge alvorlig sykdom og død, burde vaksinene vært gratis å ta. Detter er viktig for å sikre at flest mulig tar vaksinene og for å sikre et mest mulig likeverdig vaksinasjonsprogram. Det at de som skal ta vaksinene, må betale ulik andel av kostnadene, gjør det også vanskeligere for kommunene å informere om ordningen: Det kan være vanskelig å forklare hvorfor de som skal ta vaksinene, skal betalt fullt for influensavaksinen og kun delvis for korona- og
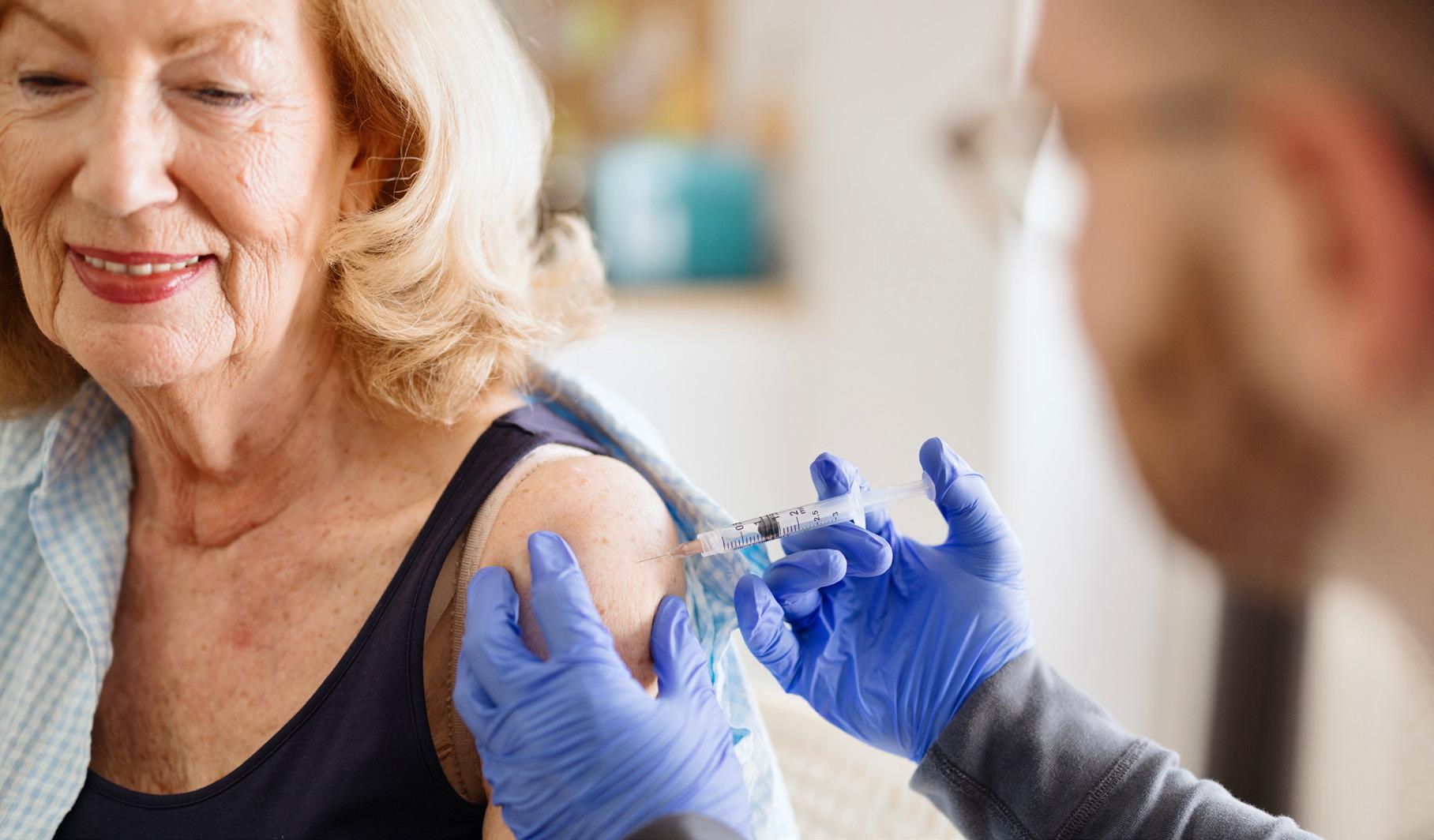
Illustrasjonsfoto: GettyImage
pneumokokk vaksinen. Det kan gi inntrykk av at det er mindre viktig å ta influensa enn Covid-19 og pneumokokkvaksinen siden man må betale fullt ut for influensavaksinen og kun delvis for korona- og pneumokokkvaksinene. Det at de som skal ta vaksinene må betale fullt eller delvis for vaksinene, er derfor en ulempe ved voksenvaksinasjonsprogrammet slik det er vedtatt. Forhåpentligvis vil regjering og Storting innse dette etter hvert og gjøre vaksinene gratis for de som skal ta dem.
En annen ulempe ved voksenvaksinasjonsprogrammet, er at det kun inneholder vaksine mot influensa, Covid-19 og pnemokokk: Det kan argumenteres for at flere vaksiner burde vært inkludert: Legeforeningen anbefalte f.eks. i sin høringsuttalelse at vaksineprogrammet burde utvides til å gjelde kikhoste, respiratorisksyncytialt virus (RSV) og herpes zoster (4). Samtidig legger Voksenvaksinasjonsprogrammet til rette for at det kan utvides med vaksiner mot flere sykdommer etterhvert, f.eks. påfyllingsvaksine mot difteri, stivkrampe, kikhoste og poliomyelitt.
Referanser
1 Folkehelseinstituttets informasjonsbrev nr. 1 om Voksenvaksinasjonsprogrammet, datert 17. mars 2025
2 Helse- og omsorgsdepartmentets Høringsnotat om Forslag til endringer nasjonalt vaksinasjonsprogram m.m.
Folkehelseinsituttet (FHI) har tatt til orde for å utvide vaksinasjonsprogrammet og støttet dette i sin høringsuttalelse (6).
En viktig fordel med voksenvaksinasjonsprogrammet er påminnelsesordningen, der det sendes varsel til: - personer 65 år og eldre som ikke er registrert med den årlige influensa- og/eller koronavaksinen i SYSVAK-registeret, etter 15. november hver høst.
- årskullet 65-år som ikke er registrert med pneumokokkvaksine (polysakkaridvaksine) siste 6 år i SYSVAK-registeret.
En potensiell ulempe med en slik påminnelsesordning er personvernhensyn: En konsekvens av påminnelsesordningen med tanke på personvern, er at det trekkes ut informasjon om at man er uvaksinert, at denne informasjonen sendes til og lagres på Helse-Norge, og brukes på en måte som kan oppleves som vaksinasjonspress. Helse- og omsorgsdepartmentet mener at en eventuell opplevelse av vaksinasjonspress, kan minskes ved at den
3 Helse- og omsorgsdepartementet: Nyhet 07.10.24: Regjeringen etablerer voksenvaksinasjonsprogram
4 Den norske legeforening: Høringsuttalelse til forslag til endringer forskrift om nasjonalt vaksinasjonsprogram mv. (Voksenvaksinasjonsprogram)
5 Kommunesektorens organisasjon (KS): Høringssvar
enkelte gis mulighet til å reservere seg mot å få påminnelsen. På den måten kan man ivareta personvernet for de som evt. vil oppleve påminnelsesordningen som vaksinepress eller ubehag, samtidig som man kan bidra til å øke vaksinasjonsdekningen i befolkningen. Helse- og omsorgsdepartementet oppgir at de vurderer at samfunnsnytten ved å øke vaksinasjonsdekningen i befolkningen generelt, og sikre at alle de som ønsker å ta vaksine får mulighet til det, veier tyngre enn inngrepet i den enkeltes personvern.
Konklusjon
Det synes fornuftig at Norge etablerer et offentlig vaksinasjonsprogram også for voksne. I første omgang vil det inkludere vaksiner mot influensa, Covid-19 og pneumokokk. Dette kan bidra for å minske sykeligheten av disse sykdommene, og død og sykehusinnleggelser. Det er betenkelig at ikke vaksinene er gratis. Antall vaksiner i ordningen bør også utvides etterhvert. Etableringen av Voksenvaksinasjonsprogrammet kan være en god start til noe som kan bli enda bedre.
på Høring av forslag til endringer i forskrift om nasjonalt vaksinasjonsprogram mv. (Voksenvaksinasjonsprogram)
6 Folkehelseinsituttets høringssvar til forslag til endringer i forskrift om nasjonalt vaksinasjonsprogram mv. (Voksenvaksinasjonsprogram)



































































3-5






Anyone can develop autoimmune T1D,6,7 but some people have a greater risk such as those with a family history or those living with other autoimmune conditions.7-10 Proactive screening can detect autoimmune T1D months or years before symptoms emerge, protecting more people from the consequences of a later diagnosis.3,11,12
Scan the QR to learn more about people who are at risk of developing autoimmune T1D and what are the reasons to proactively discuss testing for presymptomatic T1D with people at risk.










DKA, diabetic ketoacidosis; T1D, type 1 diabetes. Globally, the incidence of autoimmune T1D is increasing by approximately 2–3% per year.13 An increase in autoimmune T1D cases from ~8.4 million in 2021 to 13.5–17.4 million in 2040 was predicted using a discrete-time cohort-level Markov illness-death model.6 Up to 70% of all people who are diagnosed with autoimmune T1D are diagnosed with DKA at onset of autoimmune T1D 14 Approximately 30% of youths in Northern Europe with autoimmune T1D are diagnosed as a result of a DKA event.15
References: 1. Ozen G, et al. Int J Endocrinol. Volume 2020, Article ID 2630827, https://doi.org/10.1155/2020/2630827. 2. Dayan CM, et al. Science. 2021;373(6550): 506-510. 3. Insel RA, et al. Diabetes Care. 2015;38(10):1964-1974. 4. ElSayed NA, et al. Diabetes Care. 2023;46(Suppl 1):S19-S40. 5. Jacobsen LM, et al. Front Endocrinol (Lausanne). 2018;9:70. 6. Gregory GA, et al. Lancet Diabetes Endocrinol. 2022;10(10):741-760. 7. Karges B, et al. Diabetes Care. 2021;44(5):1116-1124. 8. Besser REJ, et al. Pediatr Diabetes. 2022;23(8):1175-1187. 9. Ludvigsson JF, et al. Diabetes Care. 2006;29(11):2483-2488. 10. Skov J, et al. Eur J Endocrinol. 2022;186(6):677-685. 11. Narendran P. Diabetologia. 2019;62(1):24-27. 12. Besser REJ, et al. Arch Dis Child. 2022;107(9):790-795. 13. DiMeglio LA, et al. Lancet. 2018;391(10138):2449-2462. 14. Wolfsdorf JI, et al. Pediatr Diabetes. 2018;19 Suppl 27:155-177. 15. Birkebaek NH, et al. Lancet Diabetes Endocrinol. 2022;10(11):786‐794.
Intended for healthcare professionals Sanofi, Professor Kohts vei 5, 1366 Lysaker, Norge. ©2025 Sanofi Inc. All rights reserved. MAT-NO-2500133-v1.0-04/2025
Kolesterolbehandling er blitt en standard del av vår praksis. Et kveldsmøte på Ous Ullevål ble arrangert for å feire 30-års jubileet til Scandinavian Simvastatin Survival Study (4S), som satte det norske kardiologmiljøet på verdenskartet. Et par av oss i redaksjonen deltok og deler her av våre inntrykk.


Introduksjon
Kjetil Retterstøl og Dan Atar arrangerte 8. april i år 30-års jubileumsmøte for Scandinavian Simvastatin Survival Study (4Sstudien), i samarbeid med MSD og Merethe Brevik-Andersen. Studien slo fast at reduksjon av LDL-kolesterolet forlenger livet hos pasienter med koronar hjertesykdom. Møtet var til ære for Terje K. Pedersen som var initiativ taker til studien i samarbeid med John Kjekshus, som ledet styringskomiteen. Stor takk ble også uttrykt til MSD for sitt engasjement i denne endepunktsstudien. Det ble vist et filmatisert sammendrag av studien med intervjuer av dens nøkkelpersoner.
Historisk perspektiv på kolesterol og aterosklerose Møtet fortsatte med et innlegg av Knut Gjesdal om kolesterol og aterosklerose i et historisk perspektiv. Han viste til at åreforkalkning har vært dokumentert gjennom år tusener, etter funn fra mumier i Kina og Egypt. Gjesdal formidlet videre utviklingen av kunnskap om lipider, inkludert oppdagelsen av kolesterol og dens sammenheng med hjertesykdom. Viktige bidrag fra norske forskere som Paul Leren og Ingvar Hjermann ble nevnt, med fokus på intervensjoner for å redusere risikoen for hjerteinfarkt.
4S-studiens betydning John Kjekshus fortsatte med sine refleksjoner om månelandingen, og det nye kardiovaskulære satsingssenteret i San Diego,
hvor han befant seg på 1960-tallet. Kjekshus fortalte hvordan 4S-studien ble til, og han viste til Terje Pedersens store initiativ og gjennomføringskraft. Kolesterolsenking med simvastatin reduserte dødeligheten med hele 30%, og satte i 1994 samtidig skandinavisk kardiologi på verdenskartet. Studien definerte en ny standard for behandling av hjertesykdom, og stimulerte til økt klinisk forskning og samarbeid på tvers av sykehus og landegrenser.
Tilbakeblikk over de siste 30 år Dan Atar understrekte også betydningen 4S-studien hadde som gjennombrudd for norsk kardiologi, og fremhevet Terje Pedersens pionerarbeid. Pedersens arbeid har vært avgjørende for å etablere sammenhengen mellom LDL-reduksjon og bedring av kardiovaskulære utfall. Ulike studier har vist at for hver reduksjon på 1 mmol/l i LDL-kolesterol ble risikoen for CVD-hendelser redusert med 20-30 %. Med prinsippet «lower is better » har man nå etablert et lipidmål med LDL under 1,4 mmol/l for aterosklerotiske hjertepasienter, med Pedersens arbeid som grunnlag for trygg moderne lipidbehandling.
Ole Christian Mjølstad, leder av Norsk kardiologisk selskap, viste til de mange store priser studien og Terje Pedersen har mottatt. Mjølstad fremhevet videre hvor krevende det var å organisere hele 94 sentre i Skandinavia, samtidig som dette satte en ny standard med store randomiserte blindede studier.
Han så 4S-resultatene i sammenheng med nedgangen vi har sett i hjerteog karsykdom i løpet av de senere årene.
Internasjonale perspektiver
Peter Libby fra USA beskrev via videolink hvordan 4S har formet amerikansk og global hjertebehandling. Han viste til at resultatene var starten på å etablere LDL-reduksjon som en standard i behandling og forebygging av koronarsykdom. Libby beskrev utviklingen av andre lipidsenkende medikamenter, samt nye teknologier, inkludert siRNA og Clustered Regularly Interspaced Short Palindromic Repeats (CRISPR). Disse nye og mer presise terapeutiske alternativene kan potensielt forbedre lipidbehandlingen ytterligere. Libby fremhevet også behovet for å fortsette forskningen knyttet til andre lipidkomponenter, som lipoprotein(a). Han uttrykte at internasjonalt samarbeid og utveksling av kunnskap har blitt nøkkelen til fremgangen innen kardiologi.
Pasientperspektiv
Margaretha Hamrin fra FH-foreningen belyste kolesterolbehandlingens betydning for pasienter med familær hyperkolesterolemi (FH). Hun delte personlige refleksjoner om hvordan statiner har forbedret livet for pasienter som tidligere hadde stor risiko for hjertesykdom. Hamrin ser stor viktighet av tidlig diagnostisering og effektive behandlingsstrategier for FH-pasienter, og utviklingen innen lipidsenkende medisiner har gitt håp til mange familier. Hun takket
overlege Leiv Ose som tidlig innså sammenhengen mellom familiær hyperkolesterolemi og hjertesykdom, og som for mer enn 40 år siden etablerte Lipidklinikken på Rikshospitalet for behandling av og forskning på kolesterolsykdommer.
Videre utvikling og moderne medikamenter
Kjetil Retterstøl presenterte deretter dagens og fremtidens lipidsenkende medikamenter, inkludert PCSK9hemmere, antisense teknologi, og kommende behandlingsmuligheter for lipoprotein(a) og triglyserider. Han understreket at statiner forblir det sentrale behandlingsprinsippet, og han rede gjorde for potensialet med de nye medikamentene.
Avslutning
Terje Pedersen takket avslutningsvis deltakerne og delte anekdoter fra
4S-planleggingen, samtidig som han understreket studiens betydning for moderne hjertebehandling. Pedersen påpekte behovet for nasjonalt og internasjonalt samarbeid for å fremme medisinsk forskning. Han takket de involverte og oppfordret til fortsatt arbeid for forbedret kardiologisk praksis.
Som tilhørere fikk vi slik en interessant gjennomgang og oppdatering av kolesterolhistorien og dagens kolesterolbehandling. Kvelden illustrerte tydelig hvor avgjørende enkeltpersoner er i pionerarbeidet for medisinske fremskritt, og hvilken utholdenhet og standhaftighet som kan være nødvendig.

Fra venstre står John Kjekshus og Terje Pedersen, som sto sentralt i 4S-studien, og Merethe Brevik-Andersen (MSD) og Kjetil Retterstøl. Dan Atar hadde gått ved bildetaking. (Foto: Kathrin Pedersen)


We are delighted to share significant research opportunities from EFIM and the Foundation for the Development of Internal Medicine in Europe (FDIME) designed to support and advance the careers of young internists:
FDIME is pleased to launch two new grant initiatives for 2025. These grants aim to support innovative research that advances the field of internal medicine across Europe. You can find more information and documents to download from our website by using the links.
Grant for Research on the Use of Artificial Intelligence in Internal Medicine
efim.org/education/fdime announcesgrant research ai use internal medicine
Internal Medicine Research Grants efim.org/education/fdime announces internal medicine research grants 2025
Eligibility: Young internists up to the age of 38 from EFIM member countries.
Application Deadline: 30 June 2025
20th FDIME-EFIM Clinical Research Course, Paris Seminar dates: 06-08 October 2025.
This educational resource is available again for EFIM Young Internists who are interested to advance their Clinical Research skills. Sponsor ship is provided by the Foundation for the Development of Internal Medicine in Europe (FDIME).
Read more information on: efim.org/events/clinical research course/ fdime efim 20th clinical research seminar
Application Deadline: 15 July 2025
Norske indremedisinere har stor glede og nytte av Indremedisineren (IM). IM bidrar til faglig utvikling og er både et viktig bindeledd i miljøet, og mellom styret i NIF og det enkelte medlem.
Redaksjonen og alle bidragsytere jobber på dugnad. Dere annonsører bidrar til at vi kan utgi et flott IM og at vi kan drifte indremedisineren.no, der trafikken er sterkt økende. Uten deres hjelp hadde det ikke vært mulig.
Vi håper det gode samarbeidet fortsetter, og at dere blir med videre!







































Familiær hyperkolesterolemi* FH – sekundærprevensjon LDL-C >2,6 mmol/l, FH – primærprevensjon (barn og voksne fra og med 8 år) LDL-C >3,6 mmol/l.
Hyperkolesterolemi ved etablert aterosklerotisk sykdom** (sekundærprevensjon) med en av følgende risikofaktorer: tidligere hjerteinfarkt, med tilbakevendende CV-hendelser, diabetes mellitus LDL-C >2,6 mmol/l, uten tilleggsrisiko LDL-C >3,6 mmol/l. Krav til tidligere behandling: Refusjon ytes når alirokumab brukes som tillegg til statin og/eller ezetimib hos pasienter som ikke oppnår LDL-nivåer under grenseverdiene nevnt ovenfor. Se følgende krav.***
Spesialistkrav: Forskrivning skal være instituert av spesialist i indremedisin, kardiologi, endokrinologi, geriatri, pediatri, nevrologi eller av lege ved tilsvarende sykehusavdeling.
* Gentest må være utført.
** Sekundærprofylakse etter akutt koronarsykdom (hjerteinfarkt, ustabil angina med sykehusinnleggelse), koronar- eller annen arteriell revaskularisering, angina pectoris, iskemisk hjerneslag eller symptomatisk perifer arteriell sykdom.
*** For brukere som tåler statiner: Høyeste tolererbare dose statin i kombinasjon med ezetimib. For brukere som ikke tåler statiner (statinintoleranse): Minst to forskjellige statiner i laveste dose i kombinasjon med ezetimib. Intoleranse må dokumenteres i journal av forskrivende lege. Ved absolutt kontraindikasjon mot statiner: ezetimib i monoterapi. Refusjonskoder ICD: -26 etablert aterosklerotisk sykdom (sekundærprevensjon) og E78 ren hyperkolesterolemi. ICPC: -26 etablerte atersklerotisk sykdom og T93 hyperkolesterolemi.
Referanser:
1. Praluent SPC 18.11.2024 pkt 4.2.
2. https://www.felleskatalogen.no/medisin/blaarev-register/c10ax14-1 (15.05.2025).
MAT-NO-2500180 (V1.0) 05.2025 sanofi-aventis Norge AS - Pb 133, 1325 Lysaker - Tel.: 67 10 71 00 www.sanofi.no
godkjent preparatomtale


C Praluent «sanofi-aventis»
Lipidmodifiserende middel, humant monoklonalt antistoff (IgG1).
ATC-nr.: C10A X14
INJEKSJONSVÆSKE, oppløsning 75 mg/ml, 150 mg/ml og 300 mg/2 ml: Hver ferdigfylt penn inneh.: Alirokumab 75 mg, 150 mg resp. 300 mg, histidin, sukrose, polysorbat 20, vann til injeksjonsvæsker.
PRALUENT er indisert ved: Primær hyperkolesterolemi eller blandet dyslipidemi: Til voksne med primær hyperkolesterolemi (heterozygot familiær og ikke-familiær) eller blandet dyslipidemi, og hos pediatriske pasienter >8 år med heterozygot familiær hyperkolesterolemi (HeFH) som tilleggsbehandling til diett: I kombinasjon med et statin eller statin med annen lipidsenkende behandling hos pasienter som ikke oppnår LDL-kolesterol (LDL-C)-mål med høyeste tolererte dose av et statin, eller alene eller i kombinasjon med annen lipidsenkende behandling hos pasienter som er statinintolerante, eller der et statin er kontraindisert.
Påvist aterosklerotisk kardiovaskulær sykdom: Til voksne med påvist aterosklerotisk kardiovaskulær sykdom for å redusere kardiovaskulær risiko ved å senke LDL-C-nivåene, som tillegg til korreksjon av andre risikofaktorer: I kombinasjon med den maks. tolererte dosen av et statin med eller uten andre lipidsenkende behandlinger, eller, alene eller i kombinasjon med andre lipidsenkende behandlinger hos pasienter som er statinintolerante, eller der et statin er kontraindisert. For informasjon om studieresultater i forhold til effekt på LDL-C, kardiovaskulære hendelser og studerte pasientgrupper, se SPC. Dosering: Vanlig oppstartsdose er 75 mg 1 gang hver 2. uke. Hvis ønsket LDL-C-reduksjon er >60%, gis 150 mg 1 gang hver 2. uke, eller 300 mg 1 gang hver 4.uke (månedlig).
Utvalgt sikkerhetsinformasjon:
Bivirkninger: Vanlige (≥1/100 til <1/10): Generelle: Reaksjon på injeksjonsstedet inkl. erytem/rødhet, kløe, hevelse, smerter/ømhet. Hud: Kløe. Luftveier: Tegn og symptomer fra de øvre luftveiene inkl. smerter i orofarynks, rhinoré, nysing. Sjeldne (≥1/10 000 til <1/1000): Hud: Nummulært eksem, urtikaria. Immunsystemet: Overfølsomhet, overfølsomhetsvaskulitt. Ukjent frekvens: Generelle: Influensalignende sykdom. Hud: Angioødem. Kontraindikasjoner: Overfølsomhet for innholdsstoffene. Forsiktighetsregler: Brukes med forsiktighet ved alvorlig nedsatt lever- eller nyrefunksjon. Interaksjoner: Klinisk relevante interaksjoner forventes ikke. Pakninger og listepriser: 75 mg/ml: 2 stk. kr 4453. 6 stk. kr 13286,60. 150 mg/ml: 2 stk. kr 4453. 6 stk. kr 13286,60. 300 mg/2 ml: 3 stk. kr 13286,60. Refusjonsprisen er rabattert: Anbudskode: 2580. For fullstendig informasjon les godkjent FK-tekst eller SPC for Praluent. Praluent «Sanofi» - Felleskatalogen. Basert på Praluent SPC godkjent av DMP/EMA 18.11.2024.
sanofi-aventis Norge AS - Pb 133, 1325 Lysaker - Tel.: 67 10 71 00 www.sanofi.no

Tromsø med Guri Grimnes og Ragnar Joakimsen i spissen overgikk seg selv med vintermøte på Sommarøy. Verken norske endokrinologer, barneleger eller inviterte foredragsholdere lot seg skremme av avstander, risiko for uvær eller utfordrende logistikk, og det var >90 deltakere på møtet.
Trine Finnes, leder, Norsk endokrinologisk forening
Barn med kroniske tilstander blir en dag voksne Samarbeidet med barnelegene er blitt en naturlig del av møtet. På fellesdelen av programmet fikk vi høre om steroid-indusert binyrebarksvikt ved Felix Bauschlein, Zürich. Om vi skal dele et viktig klinisk poeng fra forelesningen med den jevne leser, så må det være at det ikke har noen hensikt å utrede for binyrebarksvikt før man er kommet ned i fysiologiske steroiddoser eller lavere. Lars Krogvold fra barneavdelingen på OUS var nestemann ut og slo elegant over til engelsk i sitt innlegg om muligheter for å screene for diabetes type 1, mens vitsen om «fÅrebygging» forble på norsk. Det ble nok ingen konklusjon på spørsmålet «screene eller ikke-screene»,
men vi lærte enda litt mer immunologi og fikk noen å tenke på, på vegne av dem som får påvist antistoffer og skal skal gå rundt å vente på om de blir syke eller ikke. Kersitn Landin Wilhelmsen (Sahlgrensak) tok oss med på en livsreise for Turner-jenter og kvinner. Det er fascinerende å lære av ekspertise med godt klinisk blikk som har samlet erfaringer gjennom årtier. Langtidsoppfølging var også temaet for Maryam Saeed (OUS / UiO) som snakket om risiko for hjerte sykdom og alvorlig nyresykdom hos pasienter med type 1 diabetes med debut før 15 årsalder -1973-2017. Dette er et viktig arbeid som i tillegg til å si noen om prognose peker på hva som er viktig i oppfølgingen av type 1 diabetes. Vi slipper heller ikke unna overvekt

når endokrinologene samles i 2025, og Dag Hofsø fra Sykehuset i Vestfold ga oss en nyttig gjennomgang av behandlingen av postprandial hypoglykemi. I år er også de europeiske kongressene for endokrinologer og barneleger innen endokrinologi, ECE og ESPE samorgansiert i København, og vi ser frem til å fortsette samarbeidet der.
Verdige prisvinnere
Det blir for mye å gå gjennom hele det faglige programmet her, men det kan oppsummeres med høyt faglig nivå og gode formidlinger. Det har blitt populært å sende in abstracts, og siden alle holdt et vitenskapelig godt nivå, endte vi for første gang på mange år opp med å ha noen poster-presentasjoner i stedet for å avvise. Vi er spent på hvordan trenden blir for 2026. Det ser ut til at programkomiteen får stadig større utfordringer med å få plass til alt som fortjener å formidles til nytte for pasienter og fagfolk. Det har blitt en tradisjon å sette av en dag før vintermøtet til oppdatering av Nasjonal veileder i endokrinologi som med tiden er blitt et uunnværlig oppslagsverk for norske klinikere både på sykehus og i allmennpraksis (metodebok.no/endokrinologi), og 2025 var ikke noe unntak. Dugnads arbeidet med vedlikehold og oppdateringer pågår selvfølgelig kontinuerlig, og vi sender herved en stor takk til alle bidragsytere. En særlig takk gikk i år til medlem i redaksjonskomitéen, Kiarash Tazmini, som trofast møter opp i uke 10 år etter år og holder i det teknologiske, mens bursdagen forbigås i stillhet. Han var ikke den
finnes ikke fnugg av vitenskapelige bevis for at isbading har noen som helst varige helseeffekter.
eneste som fikk ekstra applaus under festmiddagen. I sin historisk prospektive studie fra Helse Vest stiller Ann-Elin Meling Stokland spørsmålet: Har prognosen ved Graves’ sykdom endret seg? Et klinisk relevant spørsmål kombinert med meget god formidlingsevne resulterte i pris for beste vitenskapelige abstract. Nytt av året var også pris til beste kasuistikk. Den gikk til Lars Medjell Hektoen som tok oss gjennom en sykehistorie hvor han pekte på alle aspekter fra patofysiologi til økonomi ved behandling av medfødt generalisert lipodystrofi.
«Det finnes ikke fnugg av vitenskapelige bevis for at isbading har noen som helst varige helseeffekter».
Til tross for tett faglig program ble det også litt tid badstue, badestamp og vinterbading. Vi var så heldige å ha professor emeritus Rolf Jorde som deltaker på møtet, så alle var vel vitende om at aktivitetene kun var for fornøyelsen skyld. Det var ingen forventninger om noen som helst helsegevinst utover at «en god latter forlenger livet». Det vi på overordnet nivå sitter igjen med etter å ha vært gjennom det faglige og sosiale programmet, er at det er viktig og nyttig for det nasjonale faglige samarbeidet av og til å møtes fysisk og få muligheten til å snakkes ansikt til ansikt.
Dialogen blir en annen når vi treffes på denne måten, enn når vi sliter med metalliske høyttaler lyder, frys i bildet og «gamle hender». Vi gleder oss dermed til Vintermøtet i 2026. Bergen har nå overtatt stafettpinnen og er allerede i gang med planleggingen.




Vintermøtet var så vidt over da vi fikk nyheten om at vår tidligere leder og nåværende nestleder professor Eystein S Husebye er tatt opp som medlem i Norsk Vitenskapsakademi. Dette er en høythengende anerkjennelse for høy vitenskapelig aktivitet og standard. I tillegg til å ha fokus på grunnforskning som kunnskapsgrunnlag for nytteforskning, er Akademiet også en uavhengig formidler av vitenskapelig kunnskap med ønske om å gjøre denne tilgjengelig som grunnlag for utforming av aktuell politikk. Som eksempel kan vi nevne at Akademiets møteserie i 2024 var «Grønn omstilling – vitenskapens rolle for en bærekraftig framtid». I en politisk urolig tid er det også betryggende å vite at Akademiet har deltatt i offentlig debatt om politikernes bruk av forskning.
Trine Finnes, leder, Norsk endokrinologisk forening
Huseby leder Endokrinforskningsgruppe ved UiB med fokus på binyresykdommer. Denne forskningen har tiltrukket seg betydelige midler og gjort det mulig for gruppen å publisere i ledende tidsskrifter. Forskningen spenner fra helserelatert livskvalitet og epidemiologi til genetikk og patogenese av autoimmune endokrine sykdommer. Nasjonale pasientregistre og biobanker har vært helt essensielt i dette arbeidet. Gjennom registre og nasjonale studier har Huseby evnet å involvere alle de endokrinologiske avdelingene i landet i kliniske studier og oppfølgingskohorter. Gruppen hans har videre fokusert på å forbedre pasientbehandlingen ved å øke presisjonen i diagnostiske prosedyrer og ved å studere metoder for å gjenopprette hormonrytmer. Dette har resultert i at de var de første til å prøve ut kortisolerstatningsterapi med insulinpumpe, og har utviklet en teknikk for ambulatorisk prøvetaking av mikrodialysevaske over 24 timer. Huseby har også vært aktiv i utvikling av både nasjonale og internasjonale retningslinjer og har hatt en rekke verv i European Society of Endocrinology (ESE). Han har blant annet vært klinisk leder for fokusområde binyre- og kardiovaskulær endokrinologi, 2021-2025 og har ledet retningslinjeutvalget for endokrine bivirkninger av sjekkpunkthemmere. Han er nå nylig også tatt opp i ESE sin vitenskapelige komite. Vi vet alle at opptaket som medlem i Norsk Vitenskapsakademi er høyst fortjent, og gratulerer Eystein med utnevnelsen!


Dosering og administrering1
RA: Voksne inkl. eldre: Anbefalt dose er 100 mg 1 gang daglig CAPS: Voksne inkl. eldre, ungdom og barn ≥8 måneder og ≥10 kg: Anbefalt startdose 1-2 mg/kg dag.
FMF og Stills sykdom: Anbefalt dose 100 mg/dag ved kroppsvekt ≥50 kg. Ved kroppsvekt <50 kg justeres dosen etter kroppsvekt, med startdose 1-2 mg/kg/dag. Hos barn med utilstrekkelig respons kan dosen økes opptil 4 mg/kg/dag.
Kineret skal gis subkutant i daglige injeksjoner.
Utvalgte advarsler og forsiktighetsregler1
Hepatiske hendelser: I kliniske studier har det blitt observert forbigående økning i leverenzymer. Rutinemessig testing av leverenzymer i løpet av den første måneden bør vurderes, særlig hvis pasienten har predisponerende faktorer eller utvikler symptomer som antyder leverdysfunksjon. Alvorlige infeksjoner: Kineretbehandling skal ikke initieres hos pasienter med aktive infeksjoner. Med nøye overvåking kan behandlingen med Kineret fortsettes også ved en alvorlig infeksjon. Behandling med Kineret for covid 19 kan fortsette til tross for (sekundære) infeksjoner. Nøytropeni: Kineret bør ikke initieres hos pasienter med nøytropeni (ANC < 1,5 x 109/l).
Annet: Varier injeksjonssted for å unngå tegn og reaksjoner på injeksjonsstedet.
Swedish Orphan Biovitrum AS Dronning Eufemias gate 16, 0191 Oslo Tlf.: 66 82 34 00 mail.no@sobi.com www.sobi.com/norway

Revmatoid artritt: Voksne med revmatoid artritt (RA) i kombinasjon med metotreksat hos de som ikke oppnår tilstrekkelig effekt med metotreksat alene. Autoinflammatoriske periodiske febersyndromer hos voksne, ungdom, barn og spedbarn (≥8 måneder med kroppsvekt ≥10 kg): Cryopyrinassosierte periodiske syndromer (CAPS) inkl. NOMID/CINCA , MWS og FCAS.
Familiær middelhavsfeber (FMF), hvis hensiktsmessig i kombinasjon med kolkisin. Stills sykdom: systemisk juvenil idiopatisk artritt (sJIA) og Stills sykdom i voksen alder (AOSD), med aktive systemiske trekk av moderat til høy sykdomsaktivitet, eller ved fortsatt sykdomsaktivitet etter behandling med NSAID eller glukokortikoider. Kan gis som monoterapi eller i kombinasjon med andre antiinflammatoriske legemidler og DMARD.
Svært vanlige: Reaksjon på injeksjonsstedet, hodepine.
Vanlige: Nøytropeni, trombocytopeni, alvorlige infeksjoner.
For fullstendig oversikt over bivirkninger og forsiktighetsregler: se godkjent SPC på www.felleskatalogen.no
Varenummer: 418642 Styrke: 100mg/0,67 ml
Pakning: 7 x 0,67 ml (ferdigfylt sptøyte) Pris (AUP): 2875,30 Refusjon: H-resept, R.gr.: C
For mer informasjon om Kineret: www.kineret.no eller scan QR-koden PP-27823- april 2025


Norsk selskap for hematologi har ca 210 ordinære medlemmer og engasjerer seg aktivt i utviklingen av det hematologiske fagområdet. En spesialist i blodsykdommer har kompetanse innen et vidt felt av sykdommer og tilstander, blant annet venøs trombose, leukemier, hemoglobinopatier, myelomatose og lymfomer. Mye av tiden til en hematolog går med til utredning av pasienter med mistenkt blodsykdom, til rådgiving av kolleger rundt unormale hematologiske blodverdier og til behandling av pasienter blant annet med kjemoimmunterapi for ulike maligne tilstander. Faget ligger i krysningspunktet mellom indremedisin og onkologi, noe som bidrar til bredden og det spennende og utfordrende ved faget.
Hege Frøen og Ellen Brodin, Norsk selskap for hematologi


Foreningen arrangerer to fagmøter i året: Et høstmøte der vi inviterer internasjonale foredragsholdere med fokus på oppdateringer på det siste innen faglige tema, og et vintermøte der vi inviterer nasjonale foredragsholdere og diskuterer felles utfordringer og problemstillinger i faget som utdanning, organisering etc. På vintermøtet arrangeres også årsmøtet, det deles ut priser til beste abstracts, og ærespriser for lang og tro tjeneste.
I år ble hematologisk vintermøte avholdt 12. og 13. mars i Ålesund og samlet hematologer fra hele landet til to dager med faglig oppdatering, diskusjoner og nettverksbygging.
Dag 1 inneholdt en rekke spennende oppdateringer:
• Behandling av akutt lymfoblastleukemi – nye behandlingsstrategier og erfaringer med individualisert behandling ved Petter Q Paulsen og Hilde Skuterud Wik.
• Erfaringer med BITE-terapi (behandling med bispesifikke antistoffer) ved myelomatose –hvilke pasientgrupper har størst nytte av behandlingen, og hvordan
håndterer man best bivirkninger ved Tobias Slørdahl (Bilde 1)
• Tromboserisiko ved myelomatose – oppdaterte retningslinjer og praktiske erfaringer med forebygging og behandling ved Anette Eilertsen
En egen bolk var viet LIS-legenes erfaringer og fremtiden for hematologifaget, hvor unge leger delte innsikt om karriereløpet i hematologi og forslag til hvordan faget kan tiltrekke seg og beholde nye spesialister.
Et annet viktig tema var fremtidens lokalsykehus og hvordan små spesialiserte hematologiske fagmiljøer kan styres fra større enheter. Nils Leknes fra UNN Tromsø holdt et innlegg som illustrerte hvordan man kan sikre høy kvalitet i behandlingen gjennom samarbeid mellom store og små enheter.
Årsmøtet ble avholdt etter møteslutt dag en, og det ble blant annet opprettet en bærekraftgruppe og valgt nytt styre. Christian Qvigstad som har vært leder og Tobias Slørdahl sekretær ble takket av, og Eirik Tjønnfjord og Magnus Moksnes ble nye medlemmer av styret. Hege Frøen ble ny leder, og Eivind
Samstad, Ellen Brodin og Tor Henrik Tvedt fortsetter.
Sosial ramme – festmiddag i Hjørundfjorden
På vintermøtet står også det sosiale i sentrum, og på kvelden var det festmiddag innerst i Hjørundfjorden på Christian Gaard Bygdetun på Trandal. Deltakerne ble fraktet med båt i lett fuktig vær, og fikk servert nydelig, kortreist mat av et entusiastisk vertskap i autentiske omgivelser (Bilde 2 og 3)
Under middagen ble det delt ut priser for beste foredrag:
• Lege i spesialisering Aba Sarr fra AHUS mottok prisen for sitt arbeid med pårørendesamarbeid satt i system.
• Overlege Magnus Moksnes fra Tønsberg ble tildelt pris for en spennende kasuistikkpresentasjon - ”En flått til besvær – DAT-negativ hemolytisk anemi hos immunsupprimerte”.
I tillegg ble Robert Brudevold tildelt utmerkelse og takket for lang og tro tjeneste etter at han har gått av med pensjon.

Dag 2 – Bærekraft i helsetjenesten Første bolk dag to var viet til behovet for økt fokus på bærekraft i helsetjenesten, og hvordan hematologifaget kan bidra til en mer miljøvennlig helsetjeneste.
• Erlend Aasheim, avdelingsdirektør i Helsedirektoratet, belyste klima- og miljøutfordringer i helsetjenesten og presenterte konkrete tiltak hematologer kan iverksette for å redusere fagets klimaavtrykk. Han trakk frem Helseminister Vestre sitt veikart for bærekraft i helsetjenesten, som inneholder strategier for grønn omstilling i helsevesenet.
• Grete Teigset Solli, avdelingsleder i Sykehusinnkjøp, forklarte hvordan Sykehusinnkjøp jobber for å redusere klimagassutslipp og hvordan sirkulær økonomi bør spille en større rolle i spesialisthelsetjenesten. Hun utfordret deltakerne til å tenke nytt rundt bruk av engangsutstyr, forbedrede innkjøpsrutiner og livsløps analyser av medisinsk utstyr.
Hege Frøen ledet paneldiskusjonen i etterkant av innleggene.
Selskapet har opprettet en egen ressursgruppe som skal jobbe videre med temaet bærekraft,
miljø og overbehandling. Gruppen skal arbeide med konkrete tiltak for å gjøre hematologifaget mer miljøvennlig og gruppen vil starte med å jobbe med å utforme “Gjør kloke valg” temaer for spesialiteten.
Dagen ble avsluttet med en bolk om myeloproliferative sykdommer med kasuistikker i regi av Marko Pavicevic, om myelofibrose i regi av Hoa Tran og kronisk myelomonocyttleukemi ved Anders Myhre
Hematologisk Vintermøte 2025 var preget av høy faglig kvalitet, engasjerende diskusjoner og en hyggelig sosial ramme. Konferansen ga deltakerne verdifulle oppdateringer innen behandling, organisering av helsetjenesten og fremtidens bærekraftige løsninger. Ålesund viste seg som en veldig fin by å ha møte i, vi kommer gjerne tilbake!
En stor takk rettes til programkomiteen – Eirik Tjønnfjord, Kristoffer Sand, Nils Morten Leknes og Øystein Sefland – for deres innsats med å sette sammen et spennende og aktuelt program.
Ved styret i Norsk selskap for hematologi





ECIM 2025 kongressen samlet indremedisinere fra hele Europa og ble i år arrangert 5.-8. mars. Møtet ble holdt i Firenze i Italia – renessansens arnested. Vi beskriver her litt av innholdet fra årets kongress, og forhåpentligvis frister det enda flere til å reise til den 24. europeiske kongressen i indremedisin 25.-28. mars 2026 i Wien i Østerrike.
Ole Kristian H. Furulund, Stephen Hewitt, Anita Suntharalingam Kvist, deltakere på ECIM-kongressen 2025
Artikkelen er basert på notater og hukommelse fra konferansen og det må derfor tas forbehold om at det kan forekomme feil.
Onsdag 5. mars 2025: Overvekt, revmatologi, sepsis, og konferanseåpning.
Alle oss som kom fra Norge, deltok på litt ulike deler av programmet. I Behandling av overvekt hos voksne, påpekte bl.a. Eleonora Poggiogalle fra Italia at man hos overvektige også må være oppmerksom på sarkopeni, og at trening er viktig for å forebygge sarkopeni hos disse pasientene. Ellers snakket Paolo Sbraccia fra Italia og Dror Dicker fra Israel om medikamentell behandling av overvekt ved hjelp av medikamenter som trizepatide og semaglutide, som også hjelper mot de kardiovaskulære risikofaktorene og komplikasjonene som følger med overvekt. Jeg, som også er samfunnsmedisiner, synes det var påfallende lite fokus på forebygging
og vanlige bivirkninger i de sesjonene jeg deltok på.
I nye fremskritt i revmatologi, foreleste Luc Mouton fra Frankrike om bruk av rituximab, stamcelle transplantasjon, CART-T og det antifibrotiske medikamentet nintedanib ved systemisk sklerose. Tilsvarende pekte Enrica Cipriano fra Italia på viktigheten av alltid å undersøke for temporalis artritt ved polymyalgia rheumatika, og henvise til revmatolog ved atypiske tilfeller. Det ble også presentert to abstracter: Den ene var en multisenter studie om behandling av blandet bindevevssykdom (MCTD) ved Kevin Chevalier og den andre handlet om idiopatisk gjentakende akutt perikarditt ved Ruggiero Mascola. De viste hhv. at mange var behandlet med immundempende

medisiner forut for glukokortikoider ved MCTD og at anakinra kan være et egnet medikament hos utvalgte pasienter med idiopatisk gjentakende akutt perikarditt.
Deretter var det fokus på immunmodellering hos pasienter med sepsis ved Joost Wiersinga fra Nederland. Det ble vist til at reaksjonen den enkelte har på sepsis, kan være viktig for utfallet av denne tilstanden. Derfor hadde man forsøkt å finne ut om det fantes ulike fenotypiske reaksjoner på sepsis som kan forklare den høye dødeligheten og om bruk av immundempende medisiner kunne bedre prognosen, men her gjenstår det mer forskning for å kunne konkludere.


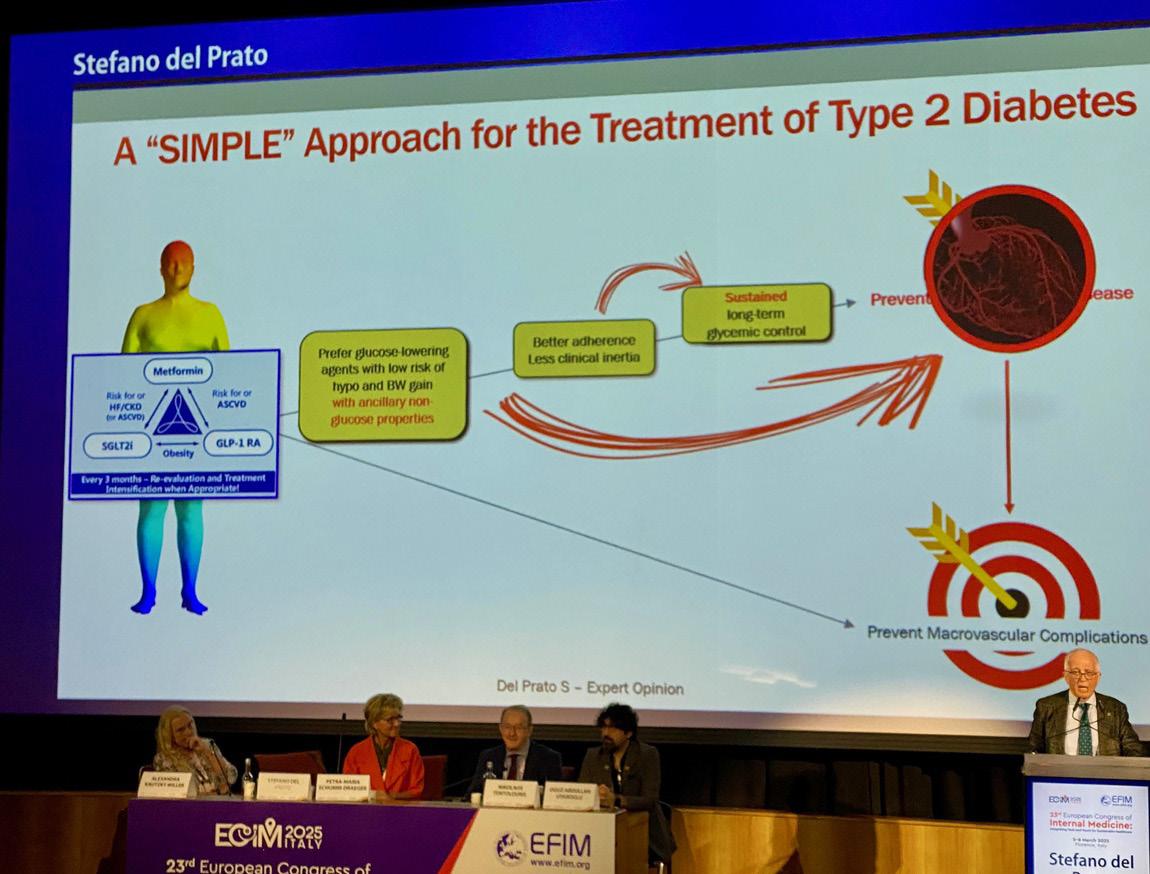
Deretter var det offisiell åpning av ECIM ved president i European Federation of Internal Medicine (EFIM), Riccardo Gomez Huelgas med ECIM Honorary Lifetime Achievement Award til professor Daniel Sereni fra det franske indremedisinske selskap og professor Giovanni Gasbarrini fra det italienske indre medisinske selskap, jf. bilde 2.
Xavier Corbella Viros fortalte om de mange liv man kan leve som indremedisiner, jf. bilde 3. Han hadde jobbet klinisk i mange år og blitt mer og mer opptatt av ledelse og økonomi, og slik ble han etterhvert sykehusdirektør. Han opplevde dette som vanskelig og gikk tilbake til å være seksjonsleder. Så en dag ble han kontaktet av noen som ikke ville si hvem han skulle snakke med og knapt nok hvor han skulle møte da de ønsket å tilby ham en jobb: Til sin store overraskelse ble han møtt av direktøren for Barcelona fotball klubb. Etter å ha bekreftet at han hadde heiet på Barcelona siden han var barn, og var fan av klubben, ble han tilbudt jobben som medisinsk direktør for Barcelona fotball klubb. Han opplevde dette som kjempeinteressant og trivdes i denne jobben hvor han jobbet for å forebygge skader og behandle fotballspillerne slik at klubben skulle vinne!
Torsdag 6. mars 2025: Antikoagulasjon, vaksiner, behandling diabetes type 2 m.m. Den andre konferansedagen var det foredrag om antikoagulasjon hos kreftpasienter ved Giancarlo Agnelli fra Italia. Han pekte på at kreft er
en hyperkoagel tilstand, som bl.a. induseres av spesifikke protrombotiske egenskaper ved kreftceller, og at venøs tromboembolisme forekommer blant 4-5% av pasientene. Det er god dokumentasjon for at antikoagulasjon forebygger residiv og død, men gir også blødning. Det er uenighet om hvor lenge behandlingen skal foregå etter endt behandling. Han viste til at det pågår en studie om et nytt risiko-skåringssystem for å evaluere risikoen for stor blødning, som vil kunne bidra til å avklare dette og at denne artikkelen skulle publiseres i NEJM ila. mars måned.
Deretter var det et spennende foredrag om hvilke vaksiner man bør forskrive til pasienter som har ulike immunsvikt tilstander ved Aurelien Sokal fra Henri Mondor Hospital i Paris. Han tok for seg flere kasustikker: Bl.a. om en pasient som var dobbeltsidig lungetransplantert og fikk intensiv immundempende behandling, som utviklet 3 dagers feber med tørrhoste. Etter lungetransplanta sjonen hadde han hatt CMV-infeksjon. Det var normale funn ved undersøkelsen, med unntak av basale knatrelyder. CRP var 4. Han testet positiv på influensa og ble behandlet med oseltamir 75 mg po. to ganger daglig i 10 dager. Spørsmålet var så hvilke vaksiner han burde få etter dette? Aurlien Sokal mente det var viktig å sikre basis vaksinering og gjennomgå hvilke vaksiner pasientene hadde hatt tidligere. Vaksiner basert på inaktiverte, levende agens er teoretisk kontraindisert. Siden RSV kunne føre til kronisk allograft rejeksjon, anbefalte
han RSV-vaksinasjon for å unngå dette samt vaksine mot HZV. Han tok for seg flere andre kasustikker, men av plasshensyn kan man ikke gå inn på alle disse her.
The European Association for the study of Diabetes (EASD) hadde en sesjon der Stefano del Prato fra Italia gjennomgikk hvordan man hadde gått fra glukose senkende medikamenter som metformin og sulfonylureapreparater til sykdomsmodifiserende legemidler som SGLT2-hemmere og GLP1reseptor agonister i 2020-årene. Og videre til «SIMPLE» tilnærming til behandlingen av type 2 dia betes: Enkel (Simple) kombinasjonsterapi, Multippel (M) risiko reduksjon, Primær helsetjeneste (P) team, Livsstilsendring (L)/ forebygging og re-Evaluering (E), jf. bilde 4. For de fleste pasienter, vil livsstilsendringer + metformin og sykdomsmodifiserende medikamenter være aktuelt.
Ved HbA1c over 9% (tilsvarende 75 mmol/mol) eller symptomatisk hypoglykemi, kunne man vurdere korttids basal insulin (evt. med tillegg av GLP-1 reseptor agonist). Han anbefalte å foretrekke glukose reduserende medikamenter med lav risiko for hypoglykemi og blodsukkervariasjon med tilleggs ikke-glukose relaterte egenskaper, f.eks. også reduserer risiko for hjerte- og karsykdom.
Ved risiko for hjertesvikt/kronisk nyresykdom, vil SGLT2-hemmer (f.eks. empaglifozin) være aktuelt.
Ved etablert eller risiko for ateroskleroserelatert hjerte- og karsykdom


kombinert med overvekt, vil GLP1reseptor agonist (f.eks. liraglutide og semaglutide) kunne være aktuelt.
Diabetisk ketoacidose (DKA) ble belyst av flere. Professor Gian Paolo Fadini fra Universitetet i Padova, Italia viste til at immun-inflammatoriske prosesser kan føre til DKA . En kasuistikk fra Ajit i Ankara omtalte euglykemisk DKA hos en pasient med type 2-diabetes med SGLT2hemmeren empagliflozin: Kirurgisk stress og redusert matinntak kan begge utløse DKA, selv ved normale blodsukkernivåer. Det er slik viktig å gjenkjenne og behandle tidlig.
Neste sesjon var om nye perspektiver i behandlingen av Alzheimers demens Carlos Reyes Zavala fra Mexico gjorde rede for Alzheimers sykdom som en av de mest vanlige nevrodegenerative sykdommene, som stiger fra rundt 5% ved 65-74 års alder og opptil 33% over 74 års alder. Jose Manuel Barrers fra Mexico viste hvordan man hadde gått fra symptomatisk behandling med acetylinkolinesterase hemmere (f.eks. donepezil) og NMDA-hemmer (memantin) til medikamenter som skal bremse utviklingen av Alzheimers demens: Den første av disse som ble godkjent av FDA i USA i 2021, var aducanumab, men dette preparatet ble trukket tilbake av fabrikant i 2024. I 2023, godkjente FDA lecanemab og donanemab, som også er monoklonale antistoffer som fjerner betaamyloid og som kan være aktuelt ved behandling av tidlig Alzheimers sykdom. Disse medikamentene har imidlertid også vist seg å ha bivirkninger i form av Amyloid-
Related Imaging Abnormalities (ARIA). Brexpiprazol ble godkjent av FDA i 2023 for agitasjon ved Alzheimers demens, men dette medikamentet er et antipsykotikum, som ifølge Felleskatalogen kun er indisert for behandling av schizofreni i Norge.
I oppdatering om dyslipidemi behandling, understreket Avishay Elis fra Israel betydningen av tidlig og aggressiv behandling av hyperkolestrolemi. Jose Lopez Miranda fra Spania foreleste om inclisiran i behandlingen av hyperkolestrolemi: Gitt sammen med maksimal dose av statin, har inclisiran vist opptil 60% reduksjon i LDL-nivå, en sikkerhetsprofil på linje med placebo samt bedre etterlevelse. Sistnevnte er kanskje ikke så overraskende, gitt at medikamentet injiseres med ny dose etter henholdsvis 3 og deretter hver 6. måned. Til slutt gjorde Evangelos Liberopoulos fra Hellas rede for ikospentetyl som en mulig behandling av høye triglyceridverdier hos 58 år gammel mannlig pasient med akutt hjerteinfarkt til tross for statinbehandling. Den vanligste uønskede effekten å være oppmerksom på er blødning, slik at dette må man være oppmerksom på.
The European Association for the Study of the Liver (EASL), the European Association for the study of Diabetes (EASD) og the European Association for the Study of Obesity (EASO) har utarbeidet retningslinjer for metabolsk dysfunksjons-assosiert steatotisk lever sykdom (MASLD) som nå erstatter tidligere betegnelser og har som
mål å redusere stigma. I sesjonen der man gjennomgikk nåværende retningslinjer for dette, fremkom det at man hadde endret definisjonen og fokuserer på en holistisk (kardiometabolsk) behandling. Det ble fremhevet at hele 30 % av verdens, og 25% europeiske befolkning er berørt, og at tidlig identifisering gjennom ikke-invasive tester som FIB-4 og målrettet screening av risikogrupper er avgjørende. Behandlingen bør inkludere livs stilsendringer, GLP-1reseptoragonister og i enkelte tilfeller fedmekirurgi. Målrettet medikamentell behandling mot MASH (metabolsk dysfunksjon-assosiert steatohepatitt) blir viktig i fremtiden. Anti-fedme medikamenter (f.eks. semaglutide, tirzepatide) har blitt en del av behandlingen og det første medikamentet mot MASH har blitt godkjent (resmetirom), jf. bilde 5. Retningslinjene understreker behovet for tverrfaglig samarbeid og forebygging i møte med denne voksende folkehelseutfordringen.
I parallell sesjonen om infeksjonssykdommer, gjennomgikk Miriam Stegemann fra Frankrike hvordan man skiller en bakteriell infeksjon fra kolonisering: Kolonisering av bakterier innebærer at bakterier slår seg ned i områder der det er god næring uten å gi infeksjon, i motsetning til infeksjoner forårsaket av bakterier. Førstnevnte behandles ikke med antibiotika mens sistnevnte gjerne vil behandles med antibiotika. Det ble påpekt at et skille mellom disse er av betydning for å gi korrekt behandling og unngå antimikrobiell resistens. For å gjøre dette, burde man vurdere lokalisasjon, måten

Bilde 7: Behandling av komorbiditet ved kronisk nyresykdom, herunder betydningen av å informere pasienten om medikamenter de bør ta en pause fra ved interkurrent sykdom
prøven er tatt på, gram-farging, symptomer og evt. påvisning av andre mikrober. Påvisning av candida på endotracheale tuber er f.eks. vanlig, og skal selvfølgelig ikke behandles med antibiotika. Så lenge pasienten er stabil, kan man deeskalere og fokusere på behandlingen av infeksjonen, ble det påpekt.
Emanuele Durante Mangoni gjorde deretter rede for nye antibiotika . Det har vært lite utvikling av dette i de senere 10-år , men det har kommet noen: Delafloxacin - tilhører gruppen flourokinoloner, og har god transmembran penetrans, som favoriserer akkumulering i bakterier. Legemidlet har god «minimum inhibitory concentration» (MIC), er et nytt behandlingsvalg for stafylococcus aureus infeksjoner og finnes både for peroral og intravenøs behandling. Per i dag finner man ikke dette legemiddelet i Felleskatalogen. Et annet legemiddel som ble nevnt var cefepim/ entmetazobactam, et kombinasjonspreparat som består av et fjerde generasjons cefalosporin i form av cefepime, og entametazobactam, som gjør at cefepidime virker mot bakterier som ellers er resistente mot legemidlet. Dette kombinasjons-preparatet er indisert ved kompliserte urinveisinfeksjoner, har god MIC og har effekt mot flere resistente mikrober. Dette kombinasjonsprepratet finner man heller ikke i Felleskatalogen i Norge, men Cefepim finnes for intravenøs bruk. Det tredje antibiotikum som ble nevnt, var ervacyklin, som er et nytutviklet tetracyklin som kan brukes til behandling av kompliserte intraabdominale infeksjoner forårsaket av bakterier. Dette legemidlet
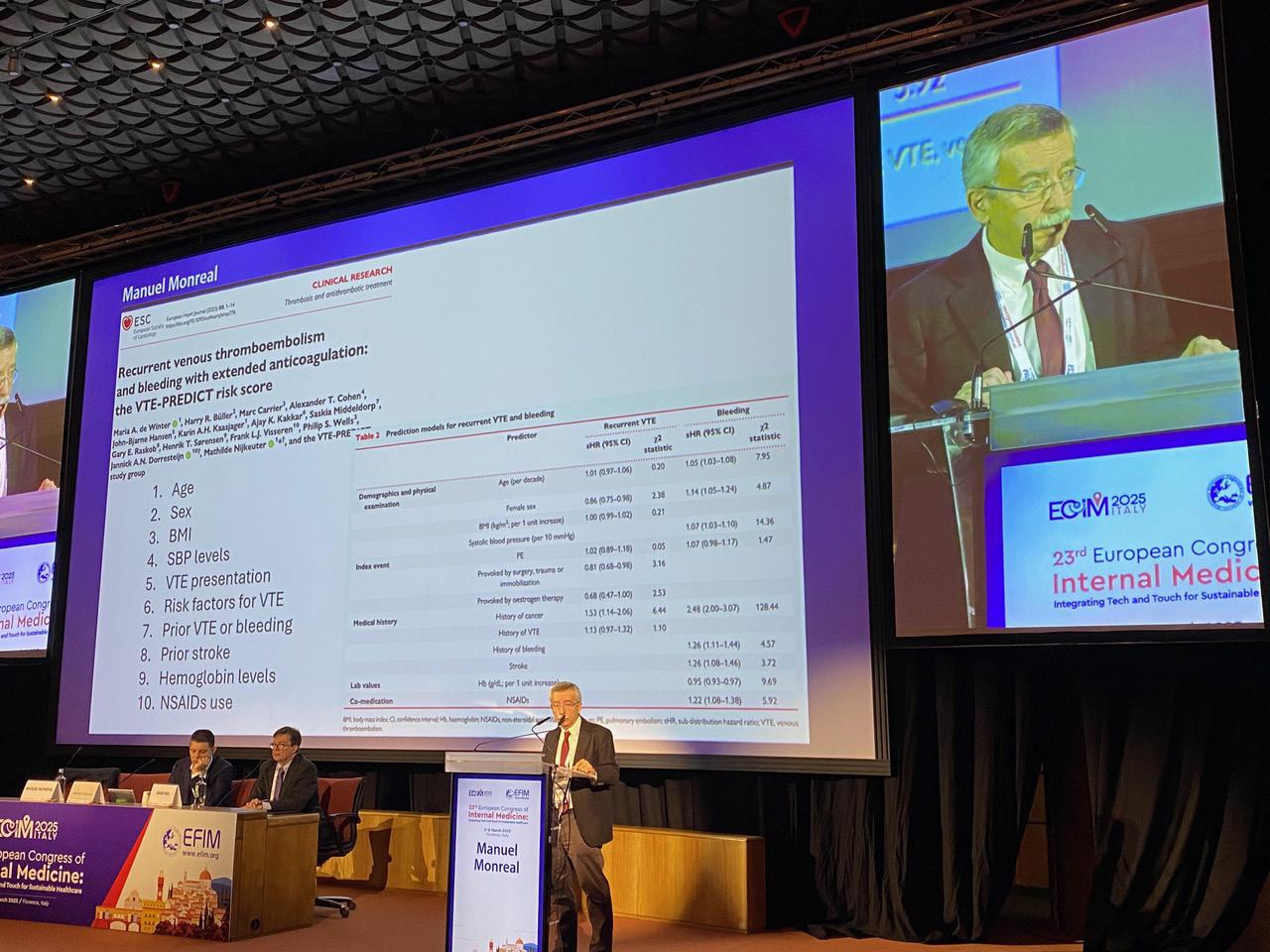
Bilde 8: Man burde eller burde ikke fortsette med antikoagulantia 3-6 måneder etter venøs tromboembolisme
finnes heller ikke i Felleskatalogen. Det er positivt at det utvikles nye antibiotika, men det er samtidig en påminnelse om at det er viktig å motvirke den utviklingen som man ser i antimikrobiell resistens.
Fredag 7. mars 2025: Komorbiditet, antikoagulantia, sarkopeni, hypertensjon, sepsis m.m. Julita Voicehovska fra Latvia startet morgenforelesning om Behandling av komorbiditet ved kronisk nyresykdom. Hun pekte på at komorbiditet er vanlig blant pasienter med kronisk nyresykdom, og at dette, sammen med økende alder på pasientene, øker kompleksiteten i behandlingen. Multimorbiditet ble definert som å ha 2 eller flere kroniske sykdommer, og antall pasienter med komorbiditet er forventet å øke globalt i årene som kommer. Dette øker bruken av helsevesenet og lengde på sykehusopphold. Voicehovska pekte på betydningen av å behandle grunnsykdommen: F.eks. behandle blodtrykk til under 130 mmHg og bruke RAAS-inhibitorer ved proteinurisk, kronisk nyresykdom. Samtidig er det viktig at lege gjør pasienten oppmerksom på risiko ved bruk av medikamenter: F.eks. at diuretika kan øke risiko for dehydrering, lavt blodtrykk, og redusert nyreperfusjon, slik at det er viktig å redusere bruken av diuretika, ACE-hemmere o.l. hvis pasienten får væsketap grunnet diare e.l., jf. bilde 7. Det er også viktig å redusere proteinuri for å forsinke progresjon av kronisk nyresykdom og individualisere behandlingen til den enkelte pasient.
Deretter var det debatt om man skal fortsette med antikoagulantia 3-6 måneder etter uprovosert venøs tromboembolisme (VTE)? Francesco Dentali fra Italia presenterte argumentene for: Han viste til CHEST retningslinjen som tilsa 3 måneders behandling med antikoagulantia, men at risikoen for ny VTE er høy og at risikoen for blødning (ofte) er lav. Manuel Monreal fra Spania presenterte argumentene mot: Han pekte på at studier som ser på VTEgjentakelse gjerne underestimerer blødningsrisiko, men at de gir en indikasjon på risiko. Samtidig er gjentakelse av VTE lav hos de som behandles og øker når de ikke lenger behandles. Begge pekte på betydningen av å bruke en risikoskår ved vurdering, og begge anbefalte VTEPREDICT risiko skår, jf. bilde 8.
I sesjonen om Hjertesvikt, ble betydningen av å behandle pasienten og ikke kun sykdommen understreket. Stephan von Haehling omtalte sarkopeni og hjertesvikt som «farlige følgesvenner»: Ufrivillig vekttap inntreffer gjerne sent i mange sykdommer, og er en uavhengig prediktor for mortalitet. 20% av pasientene har tegn til sarkopeni, også overvektige. Det er derfor viktig med trening og sunn ernæring også ved hjertesvikt. Antonio Cittadini pekte på at hjertesvikt også kan medføre mangel på flere hormoner slik som subklinisk hypothyreose, lav IGF-1 og lav T3. Han mente det derfor er viktig å undersøke for dette og behandle evt. mangler med hormon erstatningsterapi.


The European Society of Hypertension (ESH) hadde en oppdatering om de nåværende europeiske retningslinjene for behandling av hypertensjon ved Thomas Weber fra Østerrike, jf. bilde 9. Han pekte på at ved blodtrykk målt 120-139/7089 med samtidig kardiovaskulær risiko eller blodtrykk 140-159/90-99 mmHg på kontoret, anbefalte man ambulatorisk måling eller blodtrykksmåling hjemme. Det ble anbefalt måling av blodtrykk to ganger for å bekrefte diagnosen. Hvis blodtrykket er over eller lik 140/90 mmHg, bør antihypertensiv behandling startes. Hvis pasienten er voksen og har kardiovaskulær sykdom, bør antihypertensiv behandling startes når blodtrykket er 130/80 mmHg. I trinn 1 av behandlingen anbefales to medikamenter slik som ACE-hemmer/ARB + kalsiumblokker eller diuretikum. Som trinn 2 anbefales tre medikamenter slik som ACE-hemmer/ARB + kalsiumblokker + thiazid-liknende diuretikum. Hos eldre pasienter er det viktig å individualisere behandlingen.
Dragan Lovic fra Singidunum Universitet i Serbia, holdt innlegg om forekomsten og kontroll av hyper tensjon i Europa. Han pekte på at Verdens helseorganisasjon anslo at 1,28 milliarder mennesker mellom 30-79 års alder har hypertensjon, hvorav 46% ikke vet at de har hypertensjon og mindre enn 50% behandles. Hypertensjon er en viktig årsak til morbiditet og mortalitet i verden. Antallet med hypertensjon er forventet å øke i årene som kommer. Lovic fortalte at 78% av antihypertensiva brukes i Europa.
I sesjonen om Tidlig oppdagelse av sepsis, var redaktør Stephen Hewitt en av møtelederne. Mihai Netea fra Radboud Universitet medisinsk senter, fortalte om akutt fase proteiner og at hypothalamus jobber mot infeksjon, samt at stoffer som frigjøres lokalt ved sepsis kan bli skadelige når de frigjøres systemisk. Foredragsholderne beskrev hvordan sepsis er en kompleks immunrespons, der både hyperinflammasjon og immunparalyse kan øke dødeligheten. Tidlig antibiotika er avgjørende, men Nikea trakk også frem målrettet immunterapi basert på pasientens immunstatus. Han viste til identifiserte immunfenotyper hos sepsispasienter, som kan ha betydning for behandlingsstrategier. For eksempel har behandling med IL-1-reseptorantagonisten anakinra vist lovende resultater hos pasienter med hyperinflammatoriske profiler. Biomarkører som ferritin og interferon synes å kunne skille mellom ulike sepsisprofiler, slik at man kan tilpasse behandlingen deretter. Lignende immunologiske mekanismer er også observert ifm. Covid-19, og behovet for personalisert immunterapi er tilsvarende.
Jacques Hugon ved Universitet av Paris, pekte på at GLP1-agonister. hadde vist seg å ha en positiv effekt på kognitiv svikt og søvnforstyrrelser. Han hevdet også at GLP1-agonister hadde vist redusert insidens av demens i forhold til andre anti-diabetika, og at de så ut til å redusere risiko for kognitiv svikt. Dette var imidlertid blant pasienter med diabetes – ikke blant pasienter med nevrodegenerative sykdommer. Det er derfor nødvendig med
mer forsk ning før man kan si noe mer sikkert om GLP-1 agonister og nevrodegenerativ beskyttelse, jf. bilde 10.
På kongressen presenterte Anita Suntharalingam Kvist deres funn fra en studie av kvinner med tidligere svangerskapsdiabetes, der man sammenlignet interaksjonen mellom fettvev og lever hos sørasiatiske og nordiske kvinner bosatt i Oslo- området. I foredraget la hun særlig vekt på hvordan nedsatt nedregulering av frie fettsyrer, forhøyede nivåer av inflammasjonsmarkører og redusert adiponektin tyder på økt insulinresistens i fettvev hos sørasiatiske kvinner – selv i normoglykemisk tilstand. De viste også at høyere nivåer av leverproteinet fetuin-A delvis forklarte de etniske forskjellene i insulinresistens, og at dette kan være en viktig brikke i hvorfor sørasiatiske kvinner har høyere risiko for å utvikle type 2 diabetes etter svangerskapsdiabetes. De konkluderte med viktigheten av etniske forskjeller i metabolsk risiko og behovet for mer persontilpasset forebygging av type 2 diabetes, jf. bilde 11.
Det ble også tid til konsert og til en tur i den vakre byen Firenze, jf. bilde 6 og 12.
Lørdag 8. mars 2025: Screening, kardiovaskulærnyre-metabolsk syndrom m.m. Den siste offisielle dagen av ECIM, holdt Philippe Authier fra International Prevention Research Institute i Frankrike et innlegg om screening programmer for tidlig oppdagelse av sykdom. Målet er


bl.a. å hindre død ved tidlig oppdagelse og behandling av sykdom, redusere insidensen av sykdommen ved å oppdage og behandle det som forårsaker sykdommen, redusere alvorligheten av sykdommen ved å identifisere personer som har sykdommen og å tilby effektiv behandling. Han viste til Wilson & Jungners 10 prinsipper for screening programmer fra 1968:
1. TIlstanden skal være et viktig helseproblem.
2. Det skal være akseptabel behandling til stede.
3. Fasiliteter for å diagnostisere og behandle sykdommen skal være til stede.
4. Det skal være erkjennbar latent eller tidlig fase av sykdommen.
5. Det skal være en passende test eller undersøkelse til stede.
6. Testen skal være akseptabel.
7. Den naturlige utviklingen av sykdommen, fra latent stadium til erkjent sykdom, skal være tilstrekkelig forstått.
8. Man skal være enig om hvem man skal behandle.
9. Kostnaden ved å finne frem til og behandle pasientene, skal være økonomisk akseptabel.
10. Å finne frem til tilfellene skal være et kontinuerlig, og ikke et en-gang-for-alle prosjekt.
Som eksempel på sykdom man kunne tenke seg å screene for viste han til tarmkreft, som det pågår forskning på i flere land, men som fortsatt er noe uavklart. Han minnet også om å være oppmerksom på at case-control studier har en tendens til substansiell overlevelses-bias, og at overbehandling kan være problematisk, jf. f.eks. prostatakreft.
Jose R. Gonzalez Juanatey fra Spania foreleste om kardiovaskulærnyre-metabolsk syndrom. Dette er en helsetilstand som skyldes sammenheng mellom fedme, diabetes, kronisk nyresykdom og kardiovaskuær sykdom. Han pekte på at det f.eks. er en toveis sammenheng mellom progresjon av nyresykdom og kardiovaskulære hendelser hos pasienter med type 2 diabetes. Han viste også til at studier kunne tyde på at epicardielt og visceralt fettvev har en parakrin effekt på annet vev som kan påvirke forekomst av atrieflimmer og hjertesvikt. I tillegg kan middelhavsdiett påvirke det viscerale fettet. Det skal bli interessant å se hvordan forskning fremover vil avdekke mer om bakgrunnen for sammenhengen mellom disse sykdommene.
I et møte om kunstig intelligens (KI) i indremedisin delte Javid Galeria (Spania) og António Martins (Portugal) innsikter i hvordan KI kan forbedre klinisk praksis. Galeria fremhevet rollen til vitenskapelige selskaper i å utvikle strategier for KI-implementering, med fokus på utfordringer som aldrende befolkninger, poly farmasi og fragmentert omsorg. Han under-
streket behovet for å styrke digitale ferdigheter blant helsepersonell og integrere KI-verktøy i medisinsk utdanning og klinisk arbeid. Martins påpekte viktigheten av digital kompetanse i helsevesenet og oppfordret til kontinuerlig læring for å møte fremtidige utfordringer. Begge talerne fremholdt at indremedisinere er godt posisjonert og har gode forutsetninger til å lede an i den digitale transformasjonen av helsetjenestene.
Kongressen hadde noe over 2200 deltaker. Den er slik av begrenset størrelse, men vi fant likevel utfordringer å velge hvilken av parallellsesjonene å gå på. Man treffer likevel hverandre såpass mange ganger at det hele virket oversiktlig. Ifølge vår telling var vi totalt 7 norske deltakere, med fire aksepterte innlegg for presentasjon.
Vi som deltok fra Norsk indremedisinsk forening, hadde under oppholdet en felles middag på en restaurant i nærheten og påfølgende dag reiste vi hjem med mange inntrykk fra en fantastisk vakker by og en lærerik konferanse. Kanskje reise til ECIM i Wien i 2026?

ATTR-CM behandling med fem års overlevelsesdata3
TRANSTYRETIN AMYLOID KARDIOMYOPATI (ATTR-CM) ER EN UNDERDIAGNOSTISERT ÅRSAK TIL HJERTESVIKT1,2
Etter 30 måneder reduserte Vyndaqel risiko vs. placebo for 4,‡:
Død uansett årsak

Kardiovaskulære sykehusinnleggelser


HR: 0,70 (95 % KI: 0,51-0,96)



Relativ risikoratio: 0,68 (95 % CI 0,56-0,81)
Etter fem år var relativ risikoreduksjon for død uansett årsak 41 % (HR: 0,59 (95% KI: 0,44-0,79))3
Se et variert utvalg av foredrag som dekker ulike emner innen kardiologi
▼Vyndaqel® (tafamidis) 61 mg er indisert til behandling av villtype eller arvelig transtyretin amyloid kardiomyopati (ATTR-CM). Anbefalt dosering er 1 kapsel 1 gang daglig. Forsiktighet anbefales ved alvorlig nedsatt leverfunksjon. Kan gi interaksjoner ved klinisk relevante konsentrasjoner med BCRP-substrater (f.eks. metotreksat, rosuvastatin, imatinib). Utvalgte bivirkninger: Økte verdier i leverfunksjonsprøver og reduksjon i tyroksin kan forekomme. Pris: Det er fremforhandlet en konfidensiell, kostnadseffektiv pris til norske helseforetak og enkelte private sykehus. Denne er betydelig lavere enn maksimal utsalgspris i apotek, som er kr 129 737,10.
Pakning: Myke kapsler, 30 stk. Reseptgruppe: C. Refusjon: H-resept. ICD10: E85
Kriterier for forskrivning på H-resept:
1. Oppstart av behandling kan kun gjøres av kardiolog med erfaring i behandling av transtyretin amyloidose (ATTR), ansatt ved universitetssykehus eller annet helseforetak med kardiologisk enhet med kompetanse på behandling for denne pasientgruppen.Pasienten må ha en sikkert diagnostisert ATTR kardiomyopati, vanligvis med nukleærmedisinsk påvist amyloid i myokard. Pasienten skal ved oppstart være i NYHA-klasse I eller II.
2. Pasienten må ha en sikkert diagnostisert ATTR kardiomyopati, vanligvis med nukleærmedisinsk påvist amyloid i myokard. Pasienten skal ved oppstart være i NYHA-klasse I eller II.
3. Pasienten skal ha en forventet gjenstående levetid betydelig over 18 måneder.
4. Ved progresjon til vedvarende (minst 6 måneder) NYHA-klasse III, skal beslutning om å fortsette behandlingen tas i samråd med kardiolog med erfaring i behandling av ATTR, ansatt ve universitetssykehus eller annet helseforetak med kardiologisk enhet med kompetanse på behandling for denne pasientgruppen.
5. Ved rask progresjon til vedvarende NYHA-klasse III i løpet av 6 måneder etter initiert behandling, bør behandlingen avsluttes.
Før forskrivning, konsulter preparatomtalen på www.legemiddelsok.no
‡Hjertetransplantasjon, kombinert hjerte- og levertransplantasjon og hjertemekanisk hjelpemiddelimplantasjon (CMAD) ble behandlet som likeverdig med død i denne analysen. ATTR-ACT=Tafamidis in Transthyretin Cardiomyopathy Clinical Trial; TTR=Transtyretin; HR=Hazard ratio Referanser: 1. Witteles RM, et al. JACC Heart Fail. 2019;7(8):709-716. 2. Maurer MS, et al. J Am Coll Cardiol. 2016;68(2):161-172. 3. Eliott P, et al. Long-term survival with tafamidis in patients with transthyretin amyloid cardiomyopathy. Circ Heart Fail. 2022;15:4-11. 4. Maurer MS, et al. N Engl J Med. 2018;379(11):1007-1016.