PROFESSIONAL EDITION

Investigación procura más tratamientos contra el Alzheimer
a Organización Mundial de la Salud (OMS) ha fijado el objetivo de eliminar la hepatitis C como amenaza de salud para el 2030. La nueva definición de eliminación de la OMS establece que una reducción en un 65% de la mortalidad y nuevas infecciones en un 90%.1
LLa Organización Mundial de la Salud (OMS) ha fijado el objetivo de eliminar la hepatitis C como amenaza de salud para el 2030. La nueva definición de eliminación de la OMS establece que una reducción en un 65% de la mortalidad y nuevas infecciones en un 90%.1
Debido a la eficacia limitada de las pruebas de hepatitis C basadas en el riesgo por sí solas, el Centro para el Control y la Prevención de Enfermedades (CDC) consideró estrategias para aumentar la proporción de personas infectadas que conocen su estado y están vinculadas a la atención.2
Debido a la eficacia limitada de las pruebas de hepatitis C basadas en el riesgo por sí solas, el Centro para el Control y la Prevención de Enfermedades (CDC) consideró estrategias para aumentar la proporción de personas infectadas que conocen su estado y están vinculadas a la atención.2
Por lo tanto, en abril de 2020, los CDC aumentaron la orientación anterior con dos nuevas recomendaciones:2
Por lo tanto, en abril de 2020, los CDC aumentaron la orientación anterior con dos nuevas recomendaciones:2
1. Hacer prueba de Hepatitis C una vez en la vida a individuos con 18 años o más.
1. Hacer prueba de Hepatitis C una vez en la vida a individuos con 18 años o más.
2. Realizar pruebas de la hepatitis C para todas las mujeres embarazadas durante cada embarazo, excepto en los entornos en los que la prevalencia de la infección por el VHC es <0.1%.
2. Realizar pruebas de la hepatitis C para todas las mujeres embarazadas durante cada embarazo, excepto en los entornos en
La recomendación para las pruebas del VHC que se mantiene sin cambios es que, independientemente de la edad o de la prevalencia del entorno, todas las personas con factores de riesgo deben someterse a las pruebas de la hepatitis C, con pruebas periódicas mientras persistan los factores de riesgo.
La recomendación para las pruebas del VHC que se mantiene sin cambios es que, independientemente de la edad o de la prevalencia del entorno, todas las personas con factores de riesgo deben someterse a las pruebas de la hepatitis C, con pruebas periódicas mientras persistan los factores de riesgo.
Cuando se aborda específicamente la barrera de las visitas adicionales para confirmar un diagnóstico, las directrices de la Asociación Americana para el Estudio de las Enfermedades del Hígado y la Sociedad de Enfermedades Infecciosas de América (AASLD-IDSA) recomiendan el uso de la prueba de reflejo de la hepatitis C para la prueba inicial del VHC. Una prueba de anticuerpos de la hepatitis C positiva indica una infección actual, una infección previa resuelta o un falso positivo.3
Cuando se aborda específicamente la barrera de las visitas adicionales para confirmar un diagnóstico, las directrices de la Asociación Americana para el Estudio de las Enfermedades del Hígado y la Sociedad de Enfermedades Infecciosas de América (AASLD-IDSA) recomiendan el uso de la prueba de reflejo de la hepatitis C para la prueba inicial del VHC. Una prueba de anticuerpos de la hepatitis C positiva indica una infección actual, una infección previa resuelta o un falso
PRUEBA DE REFLEJO: UNA ESTRATEGIA PARA MEJORAR EL CERNIMIENTO Y DIAGNÓSTICO DE HEPATITIS C
Por: Dra. Nancy Agront, RPh. Pharm. D., Director Médico de MPH, AbbVie Puerto Rico
PRUEBA DE REFLEJO: UNA ESTRATEGIA PARA MEJORAR EL CERNIMIENTO Y DIAGNÓSTICO DE HEPATITIS C
Por: Dra. Nancy Agront, RPh. Pharm. D., Director Médico de MPH, AbbVie Puerto Rico
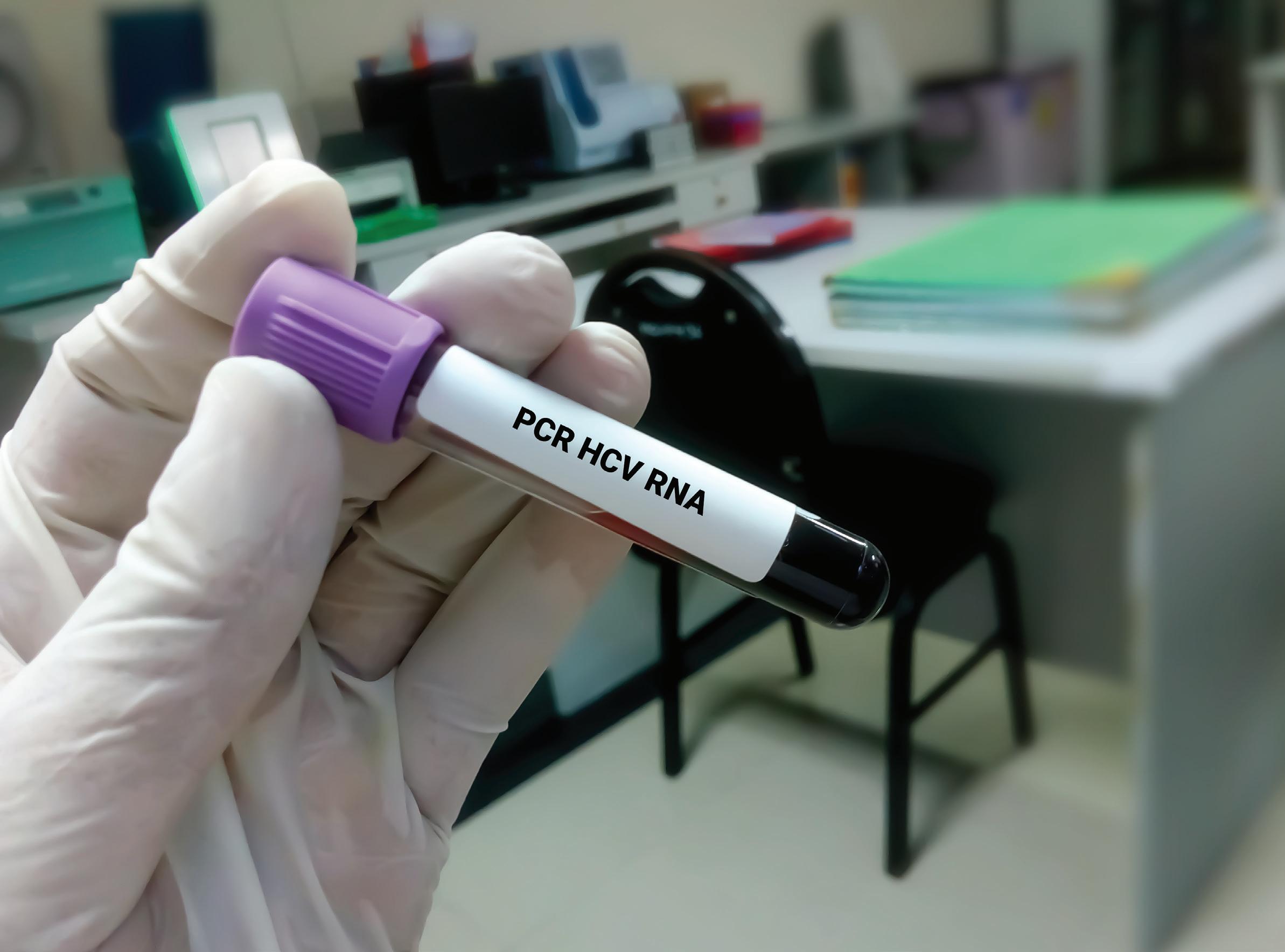
La detección de la presencia del virus en la sangre se realiza con una prueba de PCR del ARN del virus de la hepatitis C para confirmar una infección actual.3
La detección de la presencia del virus en la sangre se realiza con una prueba de PCR del ARN del virus de la hepatitis C para confirmar una infección actual.3
Una prueba de reflejo inmediato del VHC debería ser el foco de detección en la mayoría de los entornos clínicos, ya que sólo requiere una única muestra de sangre sin que el paciente necesite una segunda visita para una prueba de confirmación, considerada hoy en día como una barrera principal en la vinculación con el tratamiento y la curación de la hepatitis C. La orden del médico debería incluir el tipo de prueba que debe utilizar el técnico.3
Una prueba de reflejo inmediato del VHC debería ser el foco de detección en la mayoría de los entornos clínicos, ya que sólo requiere una única muestra de sangre sin que el paciente necesite una segunda visita para una prueba de confirmación, considerada hoy en día como una barrera principal en la vinculación con el tratamiento y la curación de la hepatitis C. La orden del médico debería incluir el tipo de prueba que debe utilizar el técnico.3
Tras la confirmación del paciente, un profesional sanitario debe evaluarlo, incluyendo la valoración de la enfermedad hepática y/o las comorbilidades para una selección adecuada del tratamiento del paciente. También debe ofrecerse asesoramiento para reducir la progresión de la enfermedad hepática y prevenir la transmisión del virus de la hepatitis C (VHC).3
Tras la confirmación del paciente, un profesional sanitario debe evaluarlo, incluyendo la valoración de la enfermedad hepática y/o las comorbilidades para una selección adecuada del tratamiento del paciente. También debe ofrecerse asesoramiento para reducir la progresión de la enfermedad hepática y prevenir la transmisión del virus de la hepatitis C (VHC).3
Referencias:
Referencias:
1. WHO guidelines on hepatitis B and C testing. Geneva: World Health Organization; 2017.
1. WHO guidelines on hepatitis B and C testing. Geneva: World Health Organization; 2017.
2. Schillie S, Wester C, Osborne M, Wesolowski L, Ryerson AB. CDC recommendations for hepatitis C screening among adults - United States, 2020. MMWR Recomm Rep. 2020;69(2):1-17.
2. Schillie S, Wester C, Osborne M, Wesolowski L, Ryerson AB. CDC recommendations for hepatitis C screening among adults - United States, 2020. MMWR Recomm Rep. 2020;69(2):1-17.
3. American Association for the Study of Liver Diseases-Infectious Disease Society of America. Recommendations for testing, managing, and treating hepatitis C. https://www.hcvguidelines.org/. Updated October 5, 2021. Accessed February 3, 2021..
3. American Association for the Study of Liver Diseases-Infectious Disease Society of America. Recommendations for testing, managing, and treating hepatitis C. https://www.hcvguidelines.org/. Updated October 5, 2021. Accessed February 3, 2021..
US-VHCV-210177
US-VHCV-210177
CONTENIDO 18 En Portada
Investigación

Bodegas

30 52
GRUPO EDITORIAL
Enesta edición de Bienestar Total Professional Edition compartimos valiosa información sobre las investigaciones que se realizan en la Isla relacionadas al Alzheimer, el cáncer de próstata y el cáncer de pulmón.
Nuestro tema de portada está relacionado a la investigación que realizan la Dra. Ivonne Jiménez-Velázquez, quien es internista, geriatra y principal investigadora, y el Dr. Christian Schenk Aldahondo, neurólogo, ambos del Recinto de Ciencias Médicas de la Universidad de Puerto Rico.
Este año el Recinto de Ciencias Médicas comenzó un estudio de prevención de la demencia en Puerto Rico: El Finnish Geriatric Intervention Study to Prevent Cognitive Impairment and Disability (FINGER Study).
El FINGER original se llevó a cabo en Finlandia con mucho éxito y se replicó luego en Europa y en los Estados Unidos como el POINTER Study. Ambos demostraron que con algunas simples intervenciones y cambios de estilo de vida, personas de 60 a 77 años de edad mejoraron la salud cerebral y disminuyeron el riesgo de desarrollar demencia, aun aquellos con el factor de riesgo genético Apo-E4 positivo.
La Dra. Jiménez-Velázquez y su equipo de investigación recibió fondos de la Asociación de Alzheimer (Alz.org) — FINGER-LATAM— para llevar a cabo el estudio en personas mayores, en 13 países latinoamericanos.
Siguiendo con los temas de investigación, el equipo de científicos, clínicos y psicólogos compuesto por los doctores Jaime Matta, Gilberto Ruiz-Deyá, Carmen Ortiz, Julio Jiménez y Melissa Marzán, colaboran junto a los doctores Jamie Teer y Jong Park —dos investigadores de Moffitt Cancer Center— en un estudio sobre el cáncer de próstata letal en los hombres
puertorriqueños, para el cual utilizan el biobanco del Ponce Health Sciences University (PHSU). Esta investigación sin precedente en Puerto Rico recibió fondos del Departamento de Defensa —$1,175,000— a través del Ponce Research Institute (PRI).
Con esta investigación, que tendrá una duración de tres años, se espera conocer más sobre los factores de riesgo que impactan el desarrollo del cáncer de próstata letal en los hombres puertorriqueños, con la meta de reducir la prevalencia de esta enfermedad. El estudio cubrirá tres áreas: genómica, molecular y alcance comunitario, con el objetivo de lograr la detección temprana del cáncer de próstata e identificar las barreras socioculturales que impiden la detección.
Por su parte, la doctora Marcia Cruz nos explica que su equipo de investigación en PanOncology Trials, participa en un estudio nacional que estará monitoreando 15 mil personas con historial activo o pasado de tabaquismo, para evaluar una tecnología novel para detectar el ADN en plasma. Esta prueba molecular en sangre examina los cambios en el genoma circulante para identificar alteraciones moleculares y lograr la detección temprana del cáncer de pulmón, aun antes de que las pruebas radiológicas lo muestren.
La Dra. Cruz indicó que estarán evaluando personas entre los 50-80 años de edad, con historial activo o pasado de tabaquismo, para adelantar el desarrollo de una prueba de detección de cáncer del pulmón.
Con esta edición cerramos un exitoso 2022 y los esperamos el próximo año 2023, listos para compartir información relevante sobre las investigaciones que realiza nuestra clase médica científica.
¡Felices fiestas y próspero 2023!
VICEPRESIDENTE DE CONTENIDO EDITORIAL Juan Miguel Muñiz
EDITORA Yaira Solís Escudero REPORTERA Melissa Cruz Ríos
DIRECTOR DE ARTE Héctor L. Vázquez Berríos GRUPO ADMINISTRATIVO
PRESIDENTE Salvador Hasbún
VICEPRESIDENTE DE MERCADEO Y OPERACIONES COMERCIALES Michelle Pérez

EJECUTIVAS DE CUENTAS
Marión Fernández Carranza Lissa M. García-Padró
DIRECTORA DE TRÁFICO
Johanna Hance
Bienestar Total Professional Edition es propiedad exclusiva de PUBLI-INVERSIONES, Inc. y es publicada trimestral por la empresa para ser distribuida en Puerto Rico.
No se permite la reproducción parcial o total del contenido sin previa autorización escrita de la empresa.
EL VOCERO DE PUERTO RICO, PO Box 15074, San Juan, Puerto Rico 00902 Bienestartotal@elvocero.com
4 Bienestartotal | Professional Edition
CARTA
Yaira Solís Escudero
Continúa la investigación de vanguardia en Puerto Rico
PROFESSIONAL EDITION
La verdad celos y el control son a tambiénmrato es que los
La verdad te necesita para cambiar realidades. La verdad no tiene precio.

FRANKLYN ROCHA-CABRERO, MD

El Dr. Rocha-Cabrero es médico-neurólogo certificado por el American Board of Psychiatry and Neu rology (ABPN). Es escritor, líder comunitario, educador y director ejecutivo de Imperium RevDoc (IRD) Neuroanalysis, desde donde brinda servicios de consultoría profesional en temas de neurohospitalista y epilepsia. Es intérprete de electroencefalogramas para hospitales, consultorios privados y neurólogos individuales.
Estudió Microbiología Industrial y Biología en la Universidad de Puerto Rico, Recinto Universitario de Mayagüez. Obtuvo su educación médica en la Universidad de Illinois, Urbana-Rockford Campus. En 2017 completó su internado en Medicina General en Riverside Community Hospital (HCA)/Universidad de California-Riverside y culminó su residencia en Neurología para adultos en Jackson Memorial Coun ty-Universidad de Miami (2021). Continuó su formación académica como sub-especialista en neurofisio logía clínica (2021-2022) con enfoque en epilepsia y monitoreo neuro-intraoperatorio en la Universidad de California-Irvine (UCI), en el condado de Orange, California.
Participa activamente en organizaciones profesionales como líder, asesor, mentor y miembro de la junta de directores, de varias entidades médicas a nivel nacional (EE. UU.) e internacional, entre ellas: la Aca demia Estadounidense de Neurología (AAN), la Asociación Latina de Estudiantes de Medicina (LMSA), la Asociación Médica Estadounidense (AMA), la Asociación Médica Nacional Hispana (NHMA), la Alianza de Médicos de California (CAPA), y The Pathway Initiative Inc (TPI), entre otras.

LCDA. ALANA MARRERO GONZÁLEZ, MHSN, LND

La Lcda. Marrero González es nutricionista y dietista desde 2009. Completó un bachillerato en Nutrición en la Universidad de Puerto Rico, Recinto de Río Piedras, seguido de una maestría en Ciencias de la Salud y Nutrición, en el Recinto de Ciencias Médicas. Su doctorado en Nutrición Clínica, lo completó en la Universidad de North Florida. Fue Presidenta de la Academia de Nutrición y Dietética de Puerto Rico y actualmente es afiliada a la junta. Trabaja en el Centro Ararat, y tiene práctica privada. Sigue activa en áreas de investigación relacionada con poblaciones de minorías


LCDO. JAVIER O. BERBERENA
En el mundo del vino, el Lcdo. Berberena es: diplomado de la Wine & Spirit Education Trust (WSET), educador certificado de vinos, sommelier certificado de la Corte de Master Sommelier, y especialista en vinos de la Society of Wine Educators, entre otros. Comenzó su carrera en educación de vinos y licores en 1995 en la Escuela Hotelera de Puerto Rico, seguido de la Universidad de Puerto Rico, la Universidad del Este - International School of Tourism & Hotel Management, y en Wine & Spirit Educa tion Trust, a través del Wine Center de Puerto Rico. Es el primer puertorriqueño en presidir un recinto del Wine & Spirit Education Trust (WSET) conocido como Approve Programm Provider Academy of the WSET. Completó su diploma de la WSET con certificación del nivel más alto de la WSET, y requisito para la admisión del programa de Master of Wine en Inglaterra. Recibió la certificación de nivel avanzado, Level 3 Spirti Award con honores, en enero de 2020. Es el instructor primario y educador especializado para los cursos de Certificación Avanzada en Vinos y Licores Nivel 3, y de la Certificación Intermedia en Vinos y Licores. Su afiliación con la industria de vinos y licores comenzó en 1990. Es miembro activo en: The Rummeliers; Society of Wine Educators, Court of Master Sommelier (London England), The Worship Company of Distillers (Great Britain), American Sommelier Association, Institute of Wines and Spirits y varias asociaciones de vinos en Puerto Rico, Florida y New York.
COLABORADORES
IVONNE Z. JIMÉNEZ VELÁZQUEZ, MD



La Dra. Jiménez Velázquez se desempeña como profesora y directora del Departamento de Medicina Interna, así como directora del Centro de Investigación y Becas de Geriatría de la Escuela de Medicina del Recinto de Ciencias Médicas de la Universidad de Puerto Rico. Desde 1989 hasta el presente es profesora adjunta en la Mount Sinai School of Medicine, en Nueva York. Estudió medicina en el Recinto de Ciencias Médicas y se especializó en Medicina Interna en el Hospital Universitario. Realizó la subespecialidad en Geriatría en el Hospital Mount Sinai Medical Center, en Nueva York. Al regresar a la Isla, entre otros proyectos, inició el programa para adiestrar médicos internistas en el área de Geriatría, que lleva más de 20 años de establecido en el Recinto de Ciencias Médicas. En 2002, comenzó a colaborar con el Dr. Richard Mayeux, director del Departamento de Neurología en la Universidad de Columbia, en New York, evaluando familias con personas mayores de 65 años que padecen de la enfermedad de Alzheimer (EA).
MARCIA CRUZ-CORREA, MD, PHD, AGAF, FASGE




La Dra. Cruz-Correa es la directora ejecutiva del Centro Comprensivo de Cáncer de la Universidad de Puerto Rico. Completó estudios de medicina en la Universidad de Puerto Rico (UPR). Hizo la residencia en Medicina Interna en la UPR y un fellowship en Gastroenterología y Hepatología, en la Universidad Johns Hopkins, en Maryland. Completó el doctorado en Investigación Clínica y Epidemiología Genética en la Escuela de Salud Pública de Jophns Hopkins Bloomberg, en Maryland. Es profesora de Medicina en la UPR, profesora asociada adjunta de Medicina en la Universidad Johns Hopkins, en Baltimore, Maryland, y profesora adjunta de Oncología quirúrgica en el MD Anderson Cancer Center, en Houston, Texas. Es la investigadora principal en múltiples becas auspiciadas por los Institutos Nacionales de Salud (NIH) de Estados Unidos, y dirige un programa de investiga ción enfocado en el cáncer gastrointestinal, cáncer hereditario y la quimioprevención. También es la principal oficial médico (CMO) de PanOncology Trials, organización dedicada a la conducción de protocolos clínicos para el diagnóstico, tratamiento y prevención del cáncer. Participa activamente en organizaciones profesionales, incluida la Asociación Americana para la Investigación del Cáncer (AACR), de la que actualmente es miembro de la junta directiva. En 2021 fue elegida miembro de la junta directiva de la Asociación Americana del Instituto del Cáncer (AACI) y de la Fundación Alianza para la Oncología Clínica. Recientemente fue elegida como la primera mujer puertorriqueña miembro de la Asociación Científica Honoraria de Médicos Americanos. Fue nombrada por el presidente Barack Obama a la Junta Nacional Asesora Sobre Cáncer, del Instituto Nacional de Cáncer.



La Fuerza Alivia está de tu lado siempre Envíenos sus recetas Médico especialista: Única farmacia especializada con acceso a todos los planes médicos 787-925-1989 (Pacientes) 787-925-1999 (Médicos) 787-925-1015 (Fax) www.aliviahealth.com Contáctanos
Tratamiento percutáneo de osteoma osteoide utilizando ablación termal guiada por imágenes
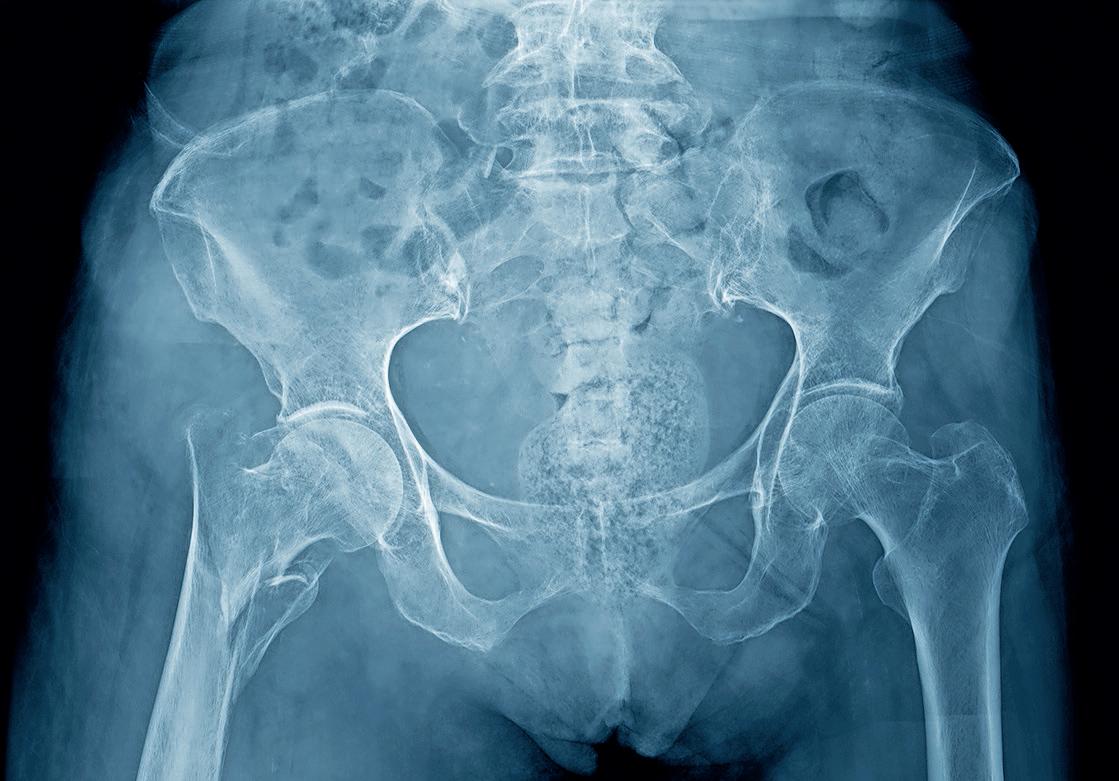
Laablación térmica por microondas (MWA) es una forma de cirugía mínimamente invasiva en donde se utilizan ondas energéticas a través de una antena causando fricción en las moléculas de un tejido que se disipa como calor.
Esta tecnología ha sido aplicada en el manejo de tumores pequeños y aislados en riñón, hígado, pulmón y hueso. Al aplicar esta tecnología mínimamente invasiva, los pacientes se recuperan más rápido y de manera segura, con menos riesgos a complicaciones quirúrgicas y con resultados comparables.
8 Bienestartotal | Professional Edition TECNOLOGÍA
POR JAVIER NAZARIO LARRIEU, MD, DABR Radiólogo Intervencional Centro Comprensivo de Cáncer de la Universidad de Puerto Rico
El osteoma osteoide es un tumor benigno de hueso que se manifiesta fundamentalmente en la segunda década de vida y se caracteriza por un dolor intenso, de predominio nocturno, e independiente del ejercicio.
Usualmente responde al tratamiento con medicamentos antiinflamatorios no esteroideos. El dolor es causado por una reacción inflamatoria en el hueso alrededor del nidus (2-10 mm en diámetro), que se teoriza es una colección de osteoblastos que producen hueso de manera descontrolada con aumento de vascularidad al área.
El tumor es diagnosticado a través de radiografía convencional, tomografía computarizada (CT), resonancia magnética (MRI) y estudios de medicina nuclear (e.g. gammagrafía ósea).
Se estima que el osteoma osteoide representa entre el 10-14% de los tumores benignos de hueso. Mayormente el osteoma osteoide se desarrolla en los huesos largos del cuerpo, pero puede ocurrir en cualquier hueso del cuerpo. Frecuentemente están localizados en la corteza del hueso, pero también pueden ocurrir en la parte medular.
El manejo de este tipo de tumor benigno inicialmente se realiza administrando medicamentos (NSAIDs) para manejar la sintomatología. Algunos osteomas osteoide desaparecen entre 2 a 6 años después de su presentación inicial. Sin embargo, la gran mayoría de ellos continúa
causando dolor y limitando las actividades físicas del paciente.
Tradicionalmente estos casos eran manejados quirúrgicamente con resección en bloque y curetaje. No obstante, la morbilidad asociada con estas intervenciones es alta y la recuperación toma mucho tiempo.
Actualmente, la mayoría de estos pacientes son tratados con ablación termal de manera ambulatoria. El radiólogo intervencional utiliza la guía por CT para insertar una cánula dentro del nido del osteoma osteoide. La antena de microonda es insertada a través de esta cánula y se aplica una energía determinada para causar la ablación termal del nido con una efectividad mayor de 95%. La desaparición del dolor relacionado al tumor es casi instantáneo. Los pacientes son dados de alta el mismo día sin inmovilización y con pocas restricciones relacionadas a su actividad física. Adicionalmente, no hay cicatriz percibida ya que es un procedimiento mínimamente invasivo.
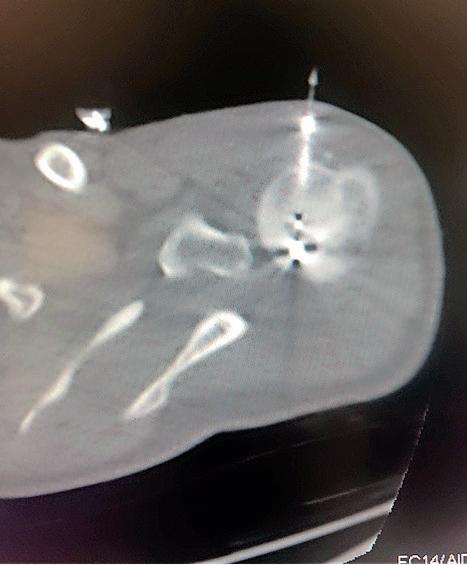
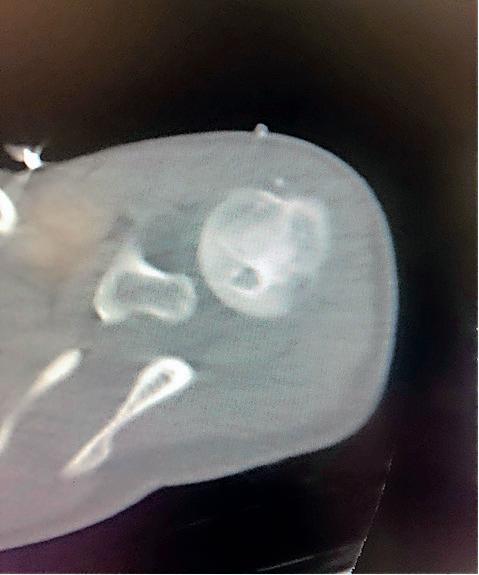
La eficacia y seguridad al realizar ablaciones termales de hueso ha reemplazado el manejo quirúrgico de estos tumores benignos de hueso. Más aún, es una técnica económica, con buena relación costo-efectividad, que se realiza de manera ambulatoria y con reincorporación rápida a la rutina normal del paciente.
Este procedimiento se realiza en el Centro Comprensivo de Cáncer de la Universidad de Puerto Rico.
9
Reacción proinflamatoria causante de mielitis necrótica aguda
Lección sobre una de las consecuencias neurológicas severa del covid-19
Quizás a los pacientes jóvenes, sería difícil imaginar que una infección del SARS-CoV-2, covid-19 tenga un impacto significativo en su salud a largo plazo. Con la amplia disponibilidad de vacunas y tratamientos orales como los son Paxlovid, hay oportunidad de disminuir los efectos adversos severos del coronavirus. Sin embargo, en pacientes que no decidan vacunarse, el riesgo para efectos adversos neurológicos severos aumenta.
POR FRANKLYN ROCHA-CABRERO MD
CEO-IRD Neuroanalysis
Neurólogo General y Neurofisiólogo clínico (Epilepsia/Monitoreo Neuro-intraoperatorio)
Diplomado de la Junta Estadounidense de Psiquiatría y Neurología
Academia Americana de Neurología (AAN)
Comité de Educación
En el caso de una pareja de jóvenes latinos y su hijo, aún no vacunados contra el covid-19, el curso de sus vidas cambió para siempre. Cuando contrajeron el virus inicialmente, todos tuvieron síntomas comunes como fatiga, dolores de cabeza, fiebre, pérdida de olfato entre otros síntomas leves por dos a tres días con lo que sería una recuperación sin complicaciones.
La madre, y mujer joven de 31 años (sin factores de riesgos y sin ningún historial médico), se presentó al hospital de la Universidad de Miami tres semanas después de tener síntomas iniciales. Sufrió síntomas neurológicos inesperados que progresaron rápidamente poniendo su vida en peligro. Esto comenzó como entumecimiento y hormigueo del dedo izquierdo, ascendiendo con parestesias en las extremidades inferiores en cuestión de días y paraplegia del cuello hacia abajo en tan solo dos a cuatro semanas.

10 Bienestartotal | Professional Edition ACTUALIDAD
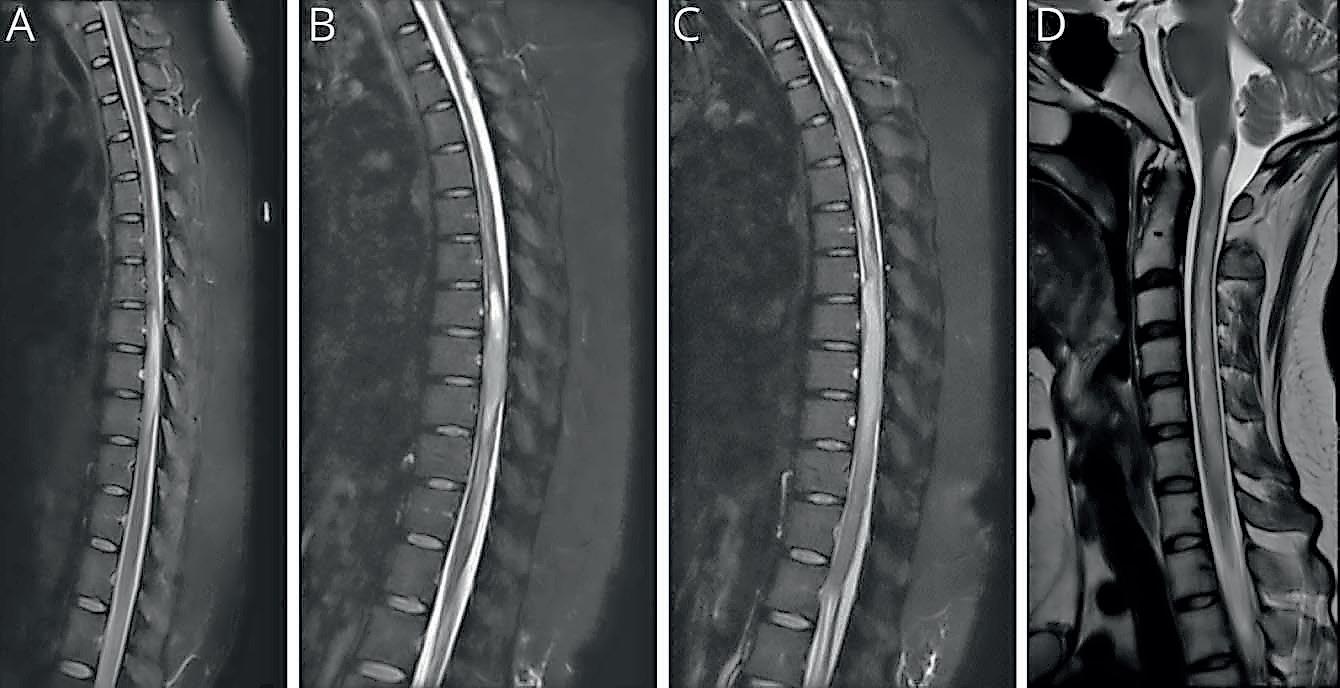
Imágenes sagitales ponderadas en T2 que muestran parches de la lesión intraespinal a nivel T7-T9 el 5 de abril de 2021 (A); y en el nivel T6-T9 el 10 de abril de 2021 (B). Sagital T2-imágenes ponderadas que muestran la lesión que se extiende a C7 cordón el 17 de abril de 2021 (C); y para bajar la médula el 4 de mayo de 2021 (D).
Otros síntomas neurológicos en el examen clínico, incluyeron incontinencia de la vejiga y defecación involuntaria.
Imágenes radiográficas de resonancia magnética (MRI) de la espina dorsal torácica (T) reveló una lesión extensa en los niveles T7-T9. Subsecuentemente, la lesión se extendió a T4-T11, toda la espina cervical (C) llegando muy cerca de la parte inferior de la conjunción entre la espina cervical y la médula. Una punción lumbar reveló un proceso inflamatorio con la presencia de una alta cantidad de linfocitos y proteína, señalando un posible proceso inmunológico o infeccioso.
Varios estudios radiográficos y del líquido cerebroespinal descartaron la posibilidad de una infección aguda, infarto de la espina dorsal, y otros procesos inmunológicos como esclerosis múltiple, neuromielitis óptica, o sarcoidosis. Entre los varios tratamientos que el equipo de Neurología consideró, incluyeron aquellos usados comúnmente para el tratamiento de mielitis transversa aguda.
Una vez que descartamos —el grupo médico también incluyó al Dr. Luis Guada Delgado, jefe residente de servicio y la Dra. Nicole Baldwin, residente júnior de la Universidad de Miami en 2021— una etiología infecciosa , y dado el rápido progreso de sus síntomas y la evidencia radiográfica de que el proceso inflamatorio empeoró, fuimos agresivos con el tratamiento de su condición. Tratamos el paciente con altas dosis repetidas de metilprednisolona (1 g/día) y immunologlobulina G (IVIG), plasmaféresis (cinco sesiones a 40 ml/kg/día), ciclofosfamida (1g/día) y finalmente un tratamiento experimental de eculuzimab (600 mg/día).
En total, estos tratamientos concurrentes se realizaron entre cuatro a seis semanas y el paciente parcialmente recuperó la función neurológica y pudimos detener el proceso inflamatorio que estaba al borde de llegar al centro respiratorio del cerebro, en la médula. Una laminectomía y biopsia de la lesión de los niveles T5-T6 —hecho por el neurocirujano Dr. Allan Levi, jefe del Departamento Neurocirugía en la Universidad de Miami—, reveló una infiltración masiva de neutrófilos,
linfocitos T, macrófagos y evidencia de mielitis necrótica del tejido. Este es uno de los únicos reportes en el mundo que incluyen un análisis histopatológico de una reacción inmunológica post-infecciosa relacionada al covid-19 de una de las peores consecuencias vistas en el mundo relacionada a la infección: parálisis neurológica, analizado por jefe del Departamento de Patología-Neuropatología, el Dr. Sakir H. Gultekin.
Según el Dr. Ashok Verma, jefe del Departamento Neuromuscular de la Universidad de Miami, la paciente finalmente recibió terapia intensiva en una facilidad de rehabilitación treinta cuatro (34) días después de ser admitida. Ella recuperó la función motora de los brazos, pero desafortunadamente quedó parapléjica en ambas piernas. Sin embargo, la paciente estaba muy agradecida de estar viva para su esposo y su hijo.
Este caso demuestra con claridad los riesgos de no vacunarse contra el covid-19, aún en pacientes sin factores de riesgo. La comunidad profesional en Puerto Rico, tanto neurólogos como de otras especialidades pueden usar este caso como una advertencia a sus pacientes, del impacto de algunas de las consecuencias neurológicas severas de este virus.
Los médicos neurólogos plantean en el reporte científico publicado en la revista de alto impacto, Neurology Clinical Practice en Junio 2022, que el mecanismo detrás de esta mielitis neurótica aguda está relacionado con una super reacción inmunológica provocada por el virus, causando que el cuerpo desarrolle anti-cuerpos contra la espina dorsal.
En el reporte, los médicos-científicos proveen un resumen de los 43 casos en 21 países reportados en el mundo de mielitis aguda necrótica relacionados al covid-19. La mayoría de los casos reportados en la literatura indican que este fenómeno raro tiende a ocurrir entre 10 días a 6 semanas después de la infección inicial. La recuperación de este tipo de reacción inmunológica contra el covid-19 tiende a ser pobre cuando comparas los casos reportados mundialmente.
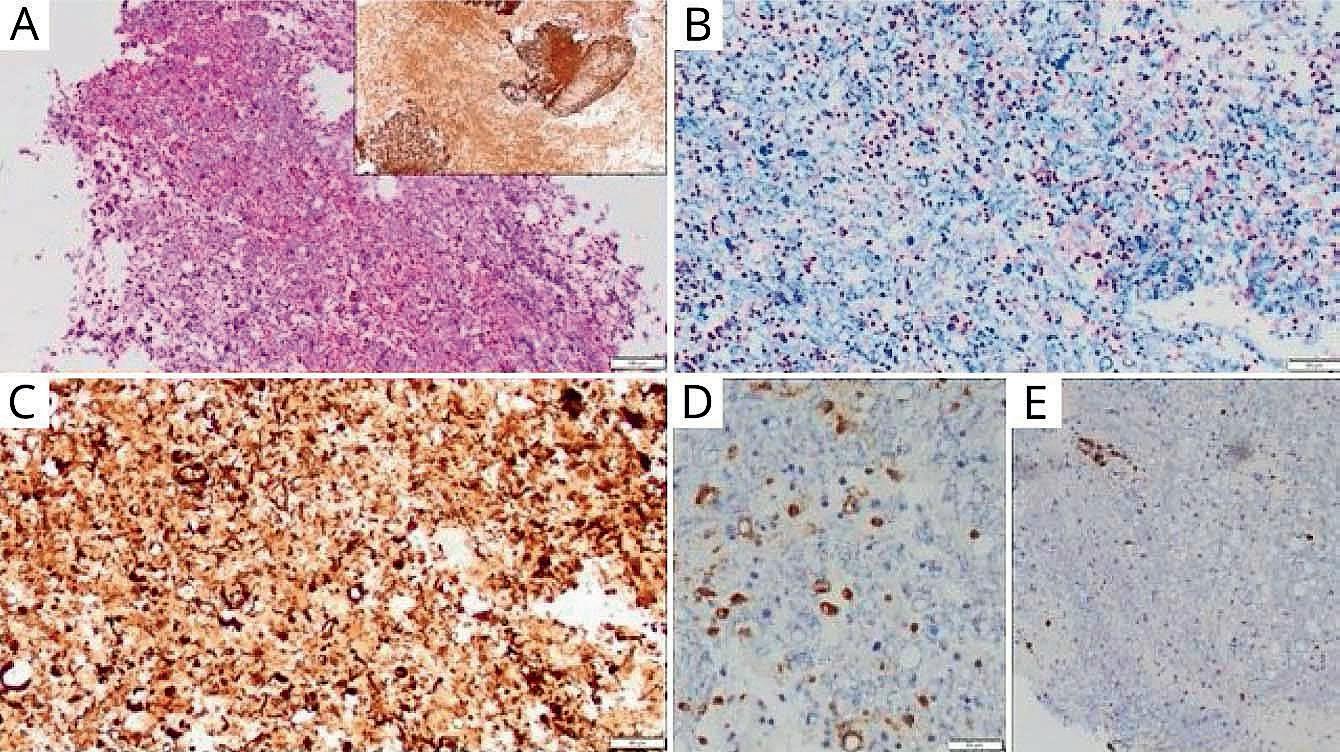
(A) La tinción con hematoxili na-eosina muestra un foco de necrosis con fondo granular, vacuolado. Recuadro muestra una tinción de proteína ácida fibrilar glial con parches de áreas viables glióticas de color marrón oscuro en el fondo de zonas necróticas amorfas que etiqueta marrón claro.
(B) Muestra la tinción azul rápi da de Luxol pérdida de mielina.
(C) Inmunohistoquímica de neurofilamentos estudio muestra fragmentación y pérdida de axones.
(D) Estudio inmunohistoquímico de CD68 muestra numerosos macrófagos en el necrótico áreas
(E) El estudio inmunohistoquími co de CD3 muestra raras células T maduras perivasculares y parenquimatosas.
11
Imperante educar sobre salud mental de niños y adolescentes
Según datos de la Administración de Servicios de Salud Mental y Contra la Adicción (Assmca), hasta el mes de agosto de 2022, se habían reportado 986 casos de comportamiento suicida en menores de 17 años, a través de la línea de Prevención al Suicidio (Línea PAS).
POR MELISSA M. CRUZ RÍOS
Percibir
rechazo de sus pares, sufrir acoso, burlas o sentirse humillado pueden detonar en niños, adolescentes y jóvenes sentimientos de desesperanza, depresión y desenlazar en la muerte por suicidio.
El suicidio, más allá de ser “un acto destructivo, autoinfligido, fatal, realizado con la intención implícita o explícita de morir”, es un acto complejo que, según el Departamento de Salud, está fundamentado en una multiplicidad de factores (biológicos, sociales y psíquicos) y deben examinarse individualmente en el contexto de cada caso en particular”.
Ya que durante el mes de octubre se conmemora en la Isla el Mes de la Salud Mental, en EL VOCERO procuramos hacer de la discusión una oportunidad para educar sobre temas relacionados a esta dura realidad, como la del suicidio entre nuestros niños
y adolescentes: el futuro de nuestro País. Es imperante prestar atención a esta situación y hacer un llamado a la acción.
Según datos de la Administración de Servicios de Salud Mental y Contra la Adicción (Assmca), a través la línea de Prevención al Suicidio —Línea PAS— hasta el mes de agosto de 2022, se reportaron 986 casos de comportamiento suicida en menores de 17 años. Además, el informe mensual de Suicidios en Puerto Rico del Departamento de Salud evidencia que entre 2016 a 2021 se reportaron 34 suicidios de jóvenes entre 10 a 19 años.
No es cuestión de números porque “uno solo es demasiado”, por lo cual entidades especializadas en la salud mental hacen un llamado a estar atentos a las conductas que pudiesen ser potencialmente riesgosas. “La educación es la piedra angular para la prevención. Con la educación a padres, maestros, familiares,

12 Bienestartotal | Professional Edition
amigos y la comunidad en general se pueden prevenir situaciones lamentables”, manifestó la doctora Beatriz Ramírez, psiquiatra de niños y adolescentes.
Algunas señales de alerta sobre que “algo no está bien con el niño o el adolescente” pueden relacionarse a manifestar tristeza profunda, falta de motivación, deterioro en el rendimiento académico, conducta agresiva o retraída, mala alimentación o conducta autodestructiva como la automutilación.
De acuerdo con la especialista de salud mental, la principal bandera roja es cuando el niño, adolescente o joven “no se comporta igual”. Incluso, si se han identificado estresores a nivel familiar o escolar que puedan provocar que sea vulnerable a completar un acto que pueda poner en peligro la vida, es razón suficiente para referir para evaluación profesional. “Los profesionales de las escuelas —orientadores y trabajadores sociales— están más educados en cuanto a identificar a los adolescentes que presentan factores de riesgo. Lo sabemos porque nos están llegando más jóvenes para evaluación”, indicó la psiquiatra.
“Estamos viviendo con prisa y mucho estrés. También, están pasando muchas cosas a nivel de sociedad, sin contar que los adultos estamos sumergidos en nuestras preocupaciones de trabajo, económicas, entre otras, y no nos detenemos a ver ese niño. No porque no queremos, sino porque a veces no identificamos señales. Por eso es importante que todos como sociedad estemos educados. De esta manera, lo que a los padres se nos escapa, un maestro o alguien de la comunidad lo puede capturar, y provocar que acuda a una evaluación que se traduzca en una intervención a tiempo”, agregó.
MANEJO DE CONDUCTAS RIESGOSAS
Sobre la evaluación o tratamiento, la Dra. Ramírez señaló que puede realizarse en una clínica o en una Sala de Emergencia. Aunque, confesó que el acceso a servicios a través de psiquiatras pediátricos puede resultar complicado dado al limitado grupo de profesionales en el campo. Sin embargo, al ser referidos a una institución hospitalaria enfocada en la salud mental la intervención de los menores resulta más ágil.
“Con la evaluación lo que se busca es identificar si existe ‘peligrosidad’. Que un menor sea referido a una institución psiquiátrica para evaluación no quiere decir que se quedará recluido. Un profesional lo evaluará para determinar el nivel de cuidado que va a necesitar ese joven según los indicadores que encuentre. Hay distintos niveles de cuidados para brindar la ayuda necesaria. Por ejemplo: si el niño o joven no representa un peligro inminente se le ofrecen servicios ambulatorios. Siempre pretendemos
que reciban el tratamiento en un nivel que sea los menos restrictivo posible. La hospitalización se reserva para cuando existe peligrosidad. Si tiene factores de riesgo que pueden poner en peligro su vida, entonces se queda en hospital para proveerle un ambiente de estructura, supervisión 24 horas al día, los siete días de la semana”, explicó la psiquiatra.
LA COMUNICACIÓN ES LA CLAVE
Para la Dra. Ramírez es importante abordar el tema de salud mental en las escuelas desde edades tempranas a través de talleres y en un lenguaje sencillo.
“Conocer y manejar las emociones es importante. A los menores se les puede explicar lo que es una depresión sin entrar en un lenguaje rebuscado. Lo importante es que puedan reconocer e identificar cuando una tristeza es normal o no. Cuando esta comienza a afectarlo en la escuela, la relación con sus pares y con su familia, deben saber que podría ser algo más. También deben saber que cuando se sienten mal por mucho tiempo y que ese malestar está acompañado con ansiedad o angustia, es necesario buscar ayuda. Por eso la educación ¡lo es todo!”, sostuvo la especialista en psiquiatría y medicina psicosomática con práctica privada en el área metropolitana.
Las condiciones de salud emocional son normales, se relacionan a cambios químicos en el cerebro y existen tratamientos para ellas. No obstante, para la psiquiatra lo importante es “identificarlas y dejarse ayudar”. Asimismo, insta a procurar mantener una sana alimentación, actividad física y realizar actividades de interés, sea artístico, deportivo o recreativo.
“Los padres tienen que identificar lo que les gusta a sus hijos para cultivar su relación con ellos, para que lo disfruten. Deben involucrarse con ellos para ser modelos”, enfatizó.
Con lo que respecta a la tecnología y el uso de las redes sociales, la Dra. Ramírez recomendó limitar el acceso a plataformas digitales o incrementar la supervisión.
“Se recomienda evaluar o monitorear lo que los niños y adolescentes están viendo en las redes sociales. Hay que educarlos sobre el contenido digital, la presión de pares, uso de sustancias, los contenidos de adultos y sobre la sexualidad saludable. Los medios sociales tienen sus cosas buenas y no tan buenas como todo. Lo importante es supervisar y comunicarse con ellos de manera que perciban que lo quieres ayudar, no como que le quiere estar prohibiendo. Por ejemplo: puedes enfatizarle que, aunque es muy inteligente, quieres orientarle sobre algunas cosas que lucen bonitas en estos medios, pero que realmente son peligrosas, porque es importante saber qué o no hacer. Hay que educar mucho”, concluyó.
SEÑALES DE PELIGRO EN LA NIÑEZ
• Cambios en los hábitos alimenticios
• Trastorno de sueño
• Comportamiento pasivo, retraído
• Comportamiento agresivo
• Miedo a la separación
• Cambios en la personalidad
• Cambios en el estado de ánimo
• Poco interés en la escuela
• Decir que se quiere morir o habla sobre la muerte
• Ausencia de amigos
• Actos de autoagresión (golpearse la cabeza o rascarse hasta lastimarse, etc.)
• Exposición a situaciones de riesgo o peligro
• Constantes accidentes domésticos
• Llamadas de atención de padres o maestros con carácter humillante
Señales de peligro en la adolescencia:
• Ánimo deprimido
• Pérdida de interés en actividades que antes disfrutaba
• Aumento o pérdida de peso
• Fatigabilidad
• Sentimientos de culpa
• Dificultad para concentrarse
• Insomnio
• Cambios evidentes en el comportamiento
• Comportamiento agresivo o extremadamente pasivo
• Descuido en la apariencia física
• Bajo aprovechamiento académico
• Se aleja de amigos y familiares
• Expresa ideas de muerte o suicidio
• Uso de drogas y alcohol
• Dificultad para comer o dormir
• Regalar pertenencias favoritas
13
Factores de riesgo del cáncer de próstata en los puertorriqueños
POR MELISSA M. CRUZ RÍOS
Lapróstata es un órgano del tamaño de una nuez que se encuentra debajo de la vejiga y delante del recto del hombre. Su función principal es la producción del fluido que se encarga de proteger a los espermatozoides, favoreciendo su movilidad y aumentando las posibilidades de fecundar el óvulo.
El cáncer de próstata (CaP) es una enfermedad en la que las células de la próstata se reproducen descontroladamente y pierden su función normal, es el tipo de cáncer más común en hombres y se presenta principalmente en 6 de cada 10 hombres mayores de 65 años. Algunas señales de alerta relacionadas al CaP pueden incluir: dificultad para comenzar a orinar, flujo de orina débil o interrumpido, orinar con
14 Bienestartotal | Professional Edition INVESTIGACIÓN
frecuencia —especialmente durante la noche—, sangre en la orina o en el semen, dolor o ardor al orinar, dolor persistente en la espalda, la pelvis o las caderas, o dolor al eyacular. No obstante, ninguno de estos síntomas es específicos del CaP y pueden estar asociados a otras condiciones. Sin embargo, en algunos casos no se presentan síntomas hasta que la enfermedad llega a los estadios avanzados o metastáticos.
Se estima que cerca del 18% de las muertes de hombres por cáncer en Puerto Rico (PR) se relacionan a este tipo de cáncer en particular.
Con esto en mente, un equipo de investigadores puertorriqueños, a través del Ponce Research Institute (PRI) de la Ponce Health Sciences University (PHSU), comenzó una investigación que estudia el CaP letal en los puertorriqueños. Se espera que esta investigación interdisciplinaria arroje luz sobre la disparidad en el acceso
a la salud de los hombres con CaP en la población puertorriqueña— y factores como: identificar las características biológicas y genómicas de tumores letales de CaP; estudiar la reparación del ADN —material genético— para desarrollar una prueba de sangre para la detección temprana del CaP, y aumentar la educación y el cernimiento en tres comunidades en PR con alta mortalidad de CaP y ancestría africana, para reducir la incidencia de la enfermedad.
El equipo de científicos, clínicos y psicólogos está compuesto por los doctores Jaime Matta, Gilberto Ruiz-Deyá, Julie Dutil, Carmen Ortiz Sánchez, Julio Jiménez y Melissa Marzán.
Colaboran, además, los doctores Jaime Teer y Jong Y. Park, investigadores de Moffitt Cancer Center, y como recurso adicional se utiliza el Puerto Rico Biobank y los doctores Idhaliz Flores
y José Oliveras. La investigación inició el 15 de julio de 2021 y se extenderá hasta el 15 de julio de 2024. Cubre tres áreas principales: genómica, molecular y alcance comunitario. Es subsidiada por el Departamento de la Defensa de los Estados Unidos (DOD, por sus siglas en inglés).
“Cada área de estudio tiene metas bastante diferentes. Cada una tiene su ‘target’ de reclutamiento, análisis de muestra o trabajo con la comunidad. Así que el progreso de la investigación dependerá de lograr las metas de reclutamiento para cada una de las tres áreas”, explicó el doctor Jaime Matta, quien es toxicólogo, biólogo de cáncer e investigador principal del estudio.
A un año de iniciada la investigación, el equipo de especialistas involucrados publicó los resultados preliminares de uno de los componentes de este proyecto.
15
El artículo de 13 páginas fue publicado en la prestigiosa revista científica Cancers. La publicación resume el proceso, avances y hallazgos de la investigación en curso, como la realización de un estudio con el potencial de proporcionar la primera evidencia con respecto a la reducción en reparación de ADN (DRC, en inglés) en hombres puertorriqueños con CaP. Además, explora la relación entre DRC y la agresividad tumoral. Asimismo, demuestra que los resultados de este estudio podrían representar un paso innovador en el desarrollo de una prueba de detección en sangre para el CaP, basada en los niveles de DRC.
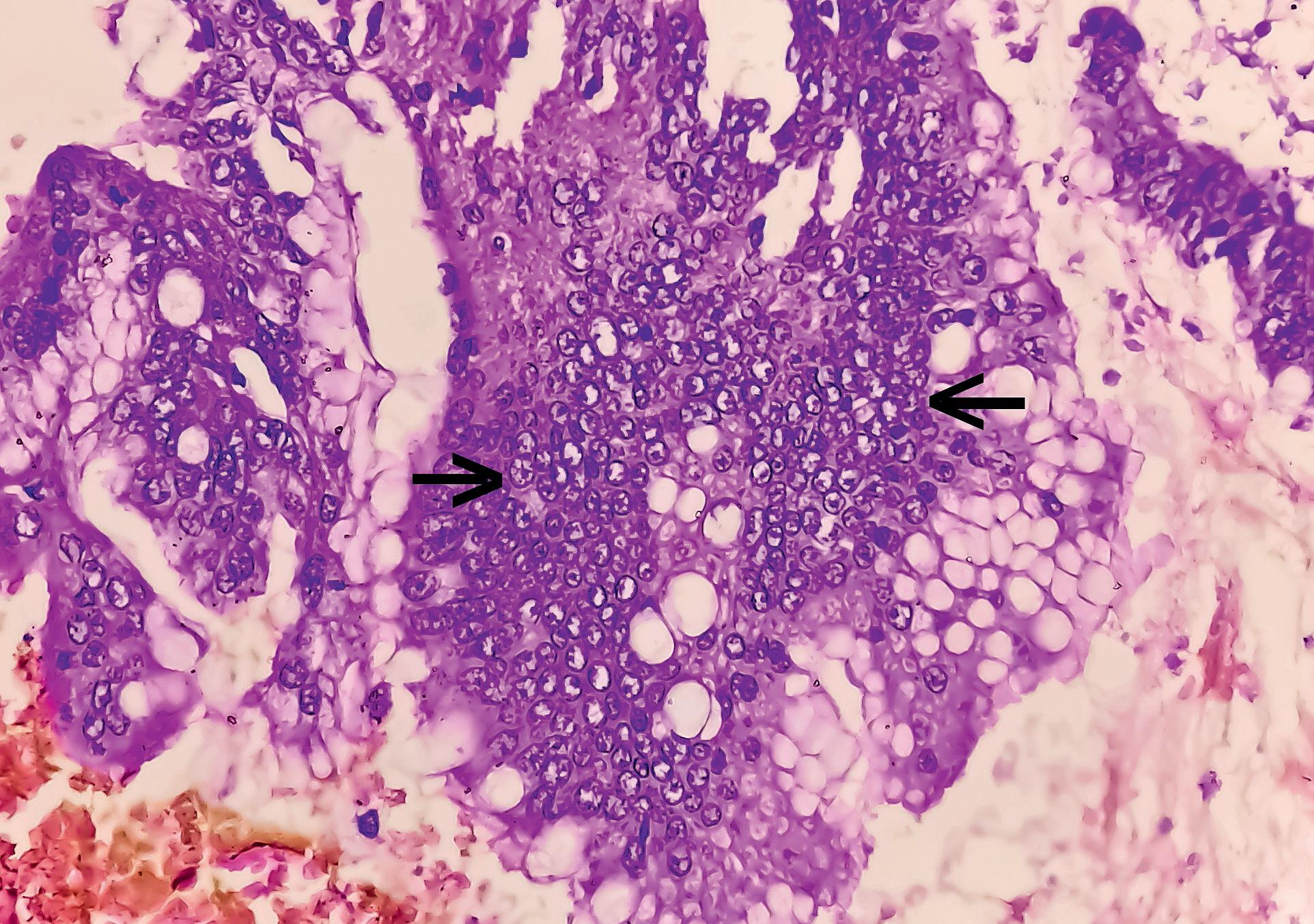
El primer objetivo del estudio implica la parte genómica y tiene como meta analizar 50 tumores indolentes —el más común—, otros 50 tumores agresivos de CaP y 50 tumores del tipo metastático.
Hasta el pasado mes de mayo de 2022, el equipo investigador reportó haber reunido 35 tumores indolentes, 17 agresivos y 2 metastáticos.
“Se han procesado aproximadamente
16 Bienestartotal | Professional Edition
14 tumores para hacer el estudio molecular y ver qué genes están envueltos en la enfermedad en hombres puertorriqueños. Tenemos alrededor de 40 tumores más que estamos en proceso de incorporar. Esto es un proceso bastante complejo. Hemos logrado progreso en el reclutamiento de tumores indolentes, pero la dificultad más grande son los tumores agresivos. Esto representa un reto a nivel mundial para conseguirlos”, explicó el Dr. Matta.
En cuanto al segundo de los objetivos, el científico indicó que se han propuesto identificar algún marcador en la sangre para la detección temprana del CaP, basado en los niveles de DRC.
La meta en esta segunda parte es reunir 155 participantes, divididos en cuatro grupos de hombres con CaP en diferentes niveles de agresividad, para ser comparados con el grupo control. Cada uno de los grupos debe constar de 31 participantes. Hasta la fecha han sido reclutados 114 participantes y resta por reclutar otros 41.
“La meta central de este estudio es tratar de entender el cáncer de próstata letal en los puertorriqueños”, expresó el investigador.
Un elemento que abonó al desarrollo de la investigación sobre el CaP letal en Puerto Rico, según el Dr. Matta, fue la investigación de la Universidad de Miami, a cargo del Dr. Félix Chinea (2017).

Se trata de un estudio que comparó la mortalidad de grupos hispanos en Florida en un periodo de 13 años, entre hombres blancos y afroamericanos, que reflejó que el grupo de hombres puertorriqueños —1,284 participantes, del total de 487 mil hombres— tenía la mortalidad más alta entre todos los grupos.
“Eso nos llamó la atención y ha sido el catalítico para tratar de identificar qué es lo que está pasando con el CaP letal en la Isla. Sabemos muy poco. Este es el primer estudio enfocado en ese aspecto”, detalló el científico sobre la investigación en curso, que aún no ha conseguido el tamaño de muestra, sobre todo en los aspectos moleculares de los tumores.
“El segundo objetivo de este estudio consiste en evaluar las variaciones en DRC en hombres puertorriqueños con CaP”, establece el informe.
“En esta parte hemos analizado la sangre de 75 participantes reclutados en un entorno hospitalario. El grupo de
participantes comprendió 52 hombres con CaP y 23 controles (sin CaP), para comparar”, agregó el Dr. Matta.
El informe preliminar de la investigación detalla que en este punto se aislaron linfocitos de muestras de sangre de casos de CaP (41) y controles (14). Se midieron los niveles de DRC a través de la reparación por escisión de nucleótidos (NER, en inglés). También se evaluó la relación entre DRC y la agresividad tumoral, y se realizaron comparaciones adicionales para evaluar las contribuciones de la edad, las medidas antropométricas y los niveles de antígeno prostático específico (PSA, en inglés). Se encontró
detección, cernimiento de CaP con pruebas que miden niveles de PSA”, adelantó el Dr. Matta.
Aclaró que aunque el análisis de PSA es “controversial” y no representa la principal prueba de detección para este tipo de cáncer, el resultado es útil y sirve como referencia a la clase médica.
“Si los valores de PSA están muy elevados es una alarma. También sirve a los urólogos para evaluar cuán rápido cambian estos valores. La prueba más eficaz y utilizada es el examen rectal digital donde el urólogo o médico palpa la próstata para identificar si está saludable o si hay alguna anomalía para así determinar otros pasos a seguir”, subrayó.
A largo plazo, este objetivo tiene como meta facilitar el acceso al cuidado de la salud llevando una clínica móvil con urólogos y profesionales salubristas a las comunidades con alta ancestría africana en la Isla, para educar sobre la prevención, detección temprana y estrategias efectivas para reducir la mortalidad a causa del CaP.
La investigación también estudia la ancestría de los participantes, ya que en Puerto Rico la ancestría es mixta. En Estados Unidos, en hombres afroamericanos, el riesgo a desarrollar CaP se duplica debido a la ancestría.
que los pacientes tenían una reducción de 59% en la reparación, comparados con los controles, la cual fue significativa estadísticamente.
El tercer objetivo está enfocado en el alcance comunitario y fue dividido en dos fases. La fase uno, correspondiente al primer año, se concretó con la realización de grupos focales en las regiones que de acuerdo con datos del Registro de Cáncer de Puerto Rico, presentan alta mortalidad de CaP y alta ancestría africana. Los municipios de Patillas, Las Piedras y Maunabo, son las comunidades que cumplieron con ambos criterios.
La fase dos, que corresponde al segundo año de investigación, conlleva un impacto directo de educación y cernimiento en las comunidades seleccionadas.
“El próximo año contemplamos visitar las comunidades, junto con una unidad móvil que tiene la Universidad, para ofrecer talleres de educación, prevención,
En este renglón, el equipo ha analizado cerca de medio centenar de hombres y en promedio, han arrojado 64% ancestría europea, 22% africana y 14% amerindia o taíno.
“Este estudio tiene el potencial de reducir las disparidades de salud asociadas a la mortalidad del CaP entre puertorriqueños y otras poblaciones hispanas y latinas —al identificar alteraciones genéticas específicas que caractericen la letalidad de tumores cancerosos en la próstata—, el desarrollo de una prueba de sangre nueva basada en la reparación del ADN (DRC y ayuda a evaluar la contribución que tiene la ancestría sobre la mortalidad relacionada al CaP. Además, se anticipa que el estudio de DRC entre hombres con y sin CaP, sirva como base para desarrollar un nuevo biomarcador para la detección temprana. Conocer el papel que juega la genética y la reparación del ADN en el CaP, ayudará a identificar con mejor precisión estrategias terapéuticas que puedan beneficiar a los puertorriqueños”, concluyó.
17
Dr. Jaime Matta

EN PORTADA — INVESTIGACIÓN
Tratamientos para la enfermedad de Alzheimer: El Horizonte
Hay pistas alentadoras en los nuevos tratamientos para esta enfermedad
ElRecinto de Ciencias Médicas de la Universidad de Puerto Rico (UPR-RCM) celebra el comienzo de un estudio de prevención de demencia en Puerto Rico: El FINGER Study cuyo nombre en inglés es Finnish Geriatric Intervention Study to Prevent Cognitive Impairment and Disability o, el Estudio Finlandés de Intervención Geriátrica para Prevenir el Deterioro Cognitivo y la Discapacidad.

El FINGER original se llevó a cabo en Finlandia con mucho éxito y se replicó luego en Europa y en los Estados Unidos como el POINTER Study. Estos estudios han demostrado en personas de 60 a 77 años de edad, cómo algunas simples intervenciones y cambios de estilo de vida saludables mejoraron la salud cerebral y disminuyeron el riesgo de demencia, aun para aquellos con el factor de riesgo genético Apo-E4 positivo.

19
POR IVONNE Z. JIMÉNEZ-VELÁZQUEZ, MD, FACP
Profesora y Directora Departamento de Medicina Interna Directora Centro de investigación y Becas de Geriatría Escuela de Medicina de la Universidad de Puerto Rico
Los participantes que recibieron intervenciones de dieta y ejercicio, junto con el entrenamiento cognitivo y el manejo del riesgo vascular, mostraron efectos beneficiosos en la función cognitiva.
La Asociación de Alzheimer (Alz.org) concedió fondos a un grupo de investigadores sobre la enfermedad de Alzheimer, conocido como FINGER-LATAM, con el fin de demostrar la factibilidad de llevar a cabo el estudio en personas mayores en un total de 13 países latinoamericanos.
El primer grupo consistirá de 100 personas de 60 a 77 años. La mitad del grupo (50) estará en una metodología supervisada y el otro grupo de 50 personas tendrá toda la información para que pueda seguir las recomendaciones por su cuenta. La selección será al azar. Un examen médico completo y neurológico, además de muestras de laboratorio que incluyen la genética, será provisto de forma gratuita en el Centro de Investigaciones del Recinto de

Ciencias Médicas, de la Universidad de Puerto Rico, conocido como The Alliance (La Alianza Hispana para la Investigación Clínica y Traslacional en Puerto Rico - https://alliance.rcm. upr.edu/). Este estudio se une a otros estudios en el Centro de Investigaciones de UPR-RCM, basados en la diversidad de presentaciones de la Enfermedad de Alzheimer (EA); el FINGER enfocado en personas a riesgo de la forma esporádica de la EA, y el estudio DIAN-TU, que investiga la forma más rara y genética / familiar de la EA de comienzo temprano, antes de los 60 años de edad.
LA ENFERMEDAD
La enfermedad de Alzheimer (EA), como todas las enfermedades neurodegenerativas, es complicada. Se reconoce que el nombre de EA es confuso, y muchas veces se desconoce que significa tener EA o demencia. Antes de adentrar en los
20 Bienestartotal | Professional Edition
“Queremos demostrar que podemos hacer una diferencia, con una dieta adaptada a nuestras costumbres, con ejercicio físico y mental, buena socialización y un enfoque preventivo cardiovascular”
— Dra. Ivonne Jiménez-Velázquez
— Dr. Christian Schenk Aldahondo, Médico Internista, Geriatra e Neurólogo Investigadora Principal del Estudio
Recinto
de Ciencias Médicas, Universidad de Puerto Rico
hallazgos científicos recientes de la EA, es importante reconocer algunos puntos claves:
1La EA fue descrita originalmente en pacientes con demencia progresiva de comienzo temprano antes de los 60 años, como una forma rara de la enfermedad, causada por una mutación genética que se hereda en la familia.
2El término EA se ha generalizado a una demencia similar a la que ocurre en personas mayores de 65 años de edad, sin mutación genética, y que desarrollan deterioro cognitivo de pensamiento y memoria gradual, causado por patología o por proteínas toxicas en la disección de cerebros de personas afectadas, similar a la que se descubrió hace 100 años en los primeros pacientes.
3Son dos proteínas principales o “patología de Alzheimer”, las que se postulan como que producen muerte neuronal en el cerebro y progresivamente la demencia o pérdida de facultades en tareas sencillas y de cuidado personal: la placa Amiloide y la proteína Tau.
4La pérdida de memoria que producen estas proteínas de Alzheimer en el cerebro es mayor a la esperada o leve pérdida de memoria “benigna” que se asocia con el envejecimiento común.
senescentes se acumulan en el cuerpo, y se piensa que contribuyen a la aparición y progresión de múltiples patologías como cáncer, y trastornos neurológicos. ¿Será que algunas personas pueden eliminar estas células senescentes mejor que otras?
7Los tratamientos actuales de la enfermedad de Alzheimer mejoran temporalmente los síntomas de pérdida de memoria y problemas con el pensamiento y el razonamiento. Estos aumentan el rendimiento de las sustancias químicas en el cerebro que transportan información de una neurona a la próxima, pero no detienen el deterioro de fondo y la muerte de las células cerebrales. A medida que mueren más células, la enfermedad de Alzheimer continúa progresando.
8Podemos predecir el curso de la enfermedad de Alzheimer de forma genética (DIAD), por el historial en la familia y la presencia de la misma mutación en el ADN. Es mucho más difícil predecir quien va a desarrollar la forma esporádica o la común de Alzheimer, de comienzo tardío, pero una vez comienzan los síntomas, se puede diagnosticar con una alta certidumbre con estudios clínicos hechos por un médico experto en demencia, como un geriatra, psiquiatra o neurólogo.
5Todos
desarrollamos cierta cantidad mínima de placa Amiloide en el cerebro al pasar del tiempo. No significa que vayamos a desarrollar la EA. Los afectados con la EA desarrollan la proteína de manera abundante, primero en áreas específicas del cerebro y luego se generaliza a casi todo el cerebro, seguido de la presencia de la proteína tau y la muerte neuronal.
9Se buscan biomarcadores: signos o pruebas que diagnostiquen y describan el estadio de enfermedad de Alzheimer en personas afectadas. Se pueden medir niveles de amiloide y tau en el líquido espinal (CSF o líquido cefalorraquídeo), pero esto requiere de una punción lumbar, método invasivo reservado para estudios de investigación o para el diagnóstico de meningitis y otras emergencias neurológicas. Se busca arduamente la manera de encontrar niveles de proteínas en sangre que sean lo suficiente sensitivos para capturar las personas a riesgo de la EA lo antes posible, y mientras más joven, mejor.
6Existen
innumerables libros y autores de teorías que prometen “curar el Alzheimer” o prevenir el deterioro cognitivo asociado al envejecimiento. Por otro lado, existen múltiples teorías científicas oficiales bajo estudio, y no existe consenso de que haya un solo proceso como “causa principal” de la EA. Entre las múltiples teorías, vamos a revisar tres de las cuales se discuten en gran medida en las conferencias anuales de la Asociación de Alzheimer:
a. Las arterias y la circulación de la sangre: La presión alta prolongada se ha demostrado que es uno de los factores de riesgo más potentes para la EA. ¿Es que el cerebro necesita una presión normal para poder filtrar las toxinas fuera del sistema?
b. El sistema inmunológico: la proteína de Amiloide se postula que tiene un rol defensivo en el cuerpo y el cerebro, como parte del sistema inmune. Las personas mayores de 65 años que han sido vacunadas contra la influenza demostraron tener un menor riesgo de desarrollar la EA, hasta 40% menos en cuatro años. (PMID: 35723106). ¿Será que el sistema inmunológico necesita activarse para remover la placa del cerebro? Similarmente, modelos de la enfermedad se han encontrado en personas con problemas en la proteína TREM2, que regula el sistema inmunológico cerebral, mediante las células llamadas astrocitos y microglía.
c. Células senescentes: La senescencia es una respuesta al daño y el estrés en la célula, que se caracteriza por la detención del ciclo celular. Con el tiempo, grandes cantidades de células
Los tratamientos futuros para la enfermedad de Alzheimer pueden incluir la combinación de medicamentos, similar a la forma en que los tratamientos para muchos tipos de cáncer o el VIH/sida incluyen más de un medicamento. Las siguientes opciones de tratamiento se encuentran entre las estrategias actualmente en estudio.
ENFOQUE EN LAS PLACAS
Algunos de los nuevos tratamientos de la enfermedad de Alzheimer en desarrollo están dirigidos a las aglomeraciones microscópicas de la proteína Amiloide, en específico la beta amiloide (placas). Las placas son un signo característico de la enfermedad de Alzheimer.
Las estrategias dirigidas a la beta amiloide incluyen:
• Reclutamiento del sistema inmunitario. Varios medicamentos —conocidos como anticuerpos monoclonales— pueden evitar que la beta amiloide se acumule en placas o eliminar las placas de beta amiloide que se hayan formado y ayudar al cuerpo a eliminar la beta amiloide del cerebro. Los anticuerpos monoclonales imitan a los anticuerpos que el cuerpo produce naturalmente como parte de la respuesta del sistema inmunitario a los invasores extraños o a las vacunas.
En junio de 2021, la Administración de Alimentos y Medicamentos (FDA) avaló bajo “aprobación acelerada” especial, el tratamiento Aducanumab para de algunos casos de
21
la enfermedad de Alzheimer. Este es el primer fármaco en su categoría, modificador de enfermedad” y no es como los otros medicamentos que sólo mejoran los síntomas, pero no es el único.

Entre Aducanumab se han estudiado más de 15 anticuerpos en contra de la amiloide, de los que los resultados son difíciles de analizar, por el hecho de que demostrar que un medicamento arresta el proceso de Alzheimer, en un órgano tan complicado como el cerebro, no es una tarea fácil, ni se puede hacer en un corto periodo. Los cambios producidos por la EA se producen desde 15 hasta 20 años antes del comienzo de los síntomas, y estos medicamentos se han ido probando en personas con síntomas leves o moderados, en la etapa de predemencia o demencia leve.
La FDA aprobó el medicamento con la condición de que se realicen más estudios para confirmar su beneficio, pero luego se retiró del mercado al no tener suficiente evidencia de su eficacia o evidencia de que el medicamento modifica la enfermedad de Alzheimer, a pesar de que los estudios han demostrado que varios de estos tratamientos biológicos —usualmente terminan en “mab”— logran reducir la placa amiloide del cerebro, después de seis a doce meses de tratamiento.
Entre otros “mabs”, se encuentran Lecanemab, el cual resulta prometedor para eliminar el amiloide y ha pasado a la fase 3 de los ensayos clínicos, y el Donanemab, otro anticuerpo monoclonal que se mostró prometedor en los ensayos de fase 2 y está pasando a la fase 3 de estudios. En estudios previos, el anticuerpo monoclonal Solanezumab no demostró ningún beneficio para las personas con enfermedad de Alzheimer leve o moderada. Es posible que el Solanezumab sea más eficaz
cuando se administra en una etapa más temprana del curso de la enfermedad. El fármaco parecía seguro en estudios recientes y se continúa evaluando el Solanezumab en la etapa preclínica de la enfermedad.
• Prevención de la destrucción: Un fármaco inicialmente desarrollado como posible tratamiento contra el cáncer, el Saracatinib, ahora se está evaluando para la enfermedad de Alzheimer.
En ratones, el fármaco desactivó una proteína que permitió que las sinapsis volvieran a funcionar, y los animales experimentaron una reversión parcial de la pérdida de memoria. Los ensayos en humanos de Saracatinib como posible tratamiento para la enfermedad de Alzheimer están en curso. De forma similar se está explorando el reposicionamiento y reutilización de medicamentos conocidos que puedan demostrar mejoría en pacientes con EA, y según la literatura, se han mencionado medicamentos como Alopurinol, Bromocriptina, Bupropion, Raloxifeno, Talidomida y Zidovudine (PMID: 32939050).
• Bloqueadores de producción: Estas terapias pueden reducir la cantidad de beta amiloide que se forma en el cerebro. La investigación ha demostrado que la beta amiloide se produce a partir de una proteína parental en dos pasos realizados por diferentes enzimas.
Varios fármacos experimentales tienen como objetivo bloquear la actividad de estas enzimas. Se los conoce como inhibidores de la beta-secretasa y la gamma-secretasa. Estudios recientes demostraron que el uso de los inhibidores de la beta-secretasa no ralentizó el deterioro cognitivo y se asociaron con efectos
Hacer juegos de mesa, es importante para mantener la agilidad mental.
>Archivo
secundarios significativos en las personas con enfermedad de Alzheimer leve o moderado, lo que ha hecho disminuir el entusiasmo por los fármacos de este tipo.
Evitar que la proteína tau forme “ovillos”
Un sistema de transporte vital de las células cerebrales colapsa cuando una proteína llamada “tau” forma fibras microscópicas llamadas “ovillos”, que son otra anomalía cerebral frecuente de la enfermedad de Alzheimer. Los investigadores están buscando una forma de evitar que la proteína tau forme ovillos. Actualmente, se están estudiando en ensayos clínicos los inhibidores de agregación de tau y las vacunas contra la proteína tau.
Reducción de la inflamación
La enfermedad de Alzheimer causa inflamación crónica y de bajo nivel de las células cerebrales. Los investigadores están estudiando formas de tratar los procesos inflamatorios que ocurren en la enfermedad de Alzheimer. El medicamento Sargramostim (Leukine) se encuentra actualmente en investigación. Se cree que este medicamento podría estimular el sistema inmunitario para que proteja al cerebro de las proteínas dañinas. Los investigadores estudiaron el medicamento para la diabetes Pioglitazona (Actos) para determinar si puede disminuir la beta amiloide y la inflamación en el cerebro. Pero la investigación demostró que el medicamento no es eficaz.
Investigación de la resistencia a la insulina
Los investigadores están estudiando los efectos de la insulina en el cerebro y en la función de las células cerebrales, y los cambios de insulina en el cerebro que pueden estar relacionados con el Alzheimer. Un ensayo en el que se probó un atomizador nasal de insulina determinó que el fármaco no era eficaz para frenar la progresión de la enfermedad de Alzheimer. El análogo de GLP-1 (Glucagon like peptide-1) de larga duración Semaglutide y Liraglutide, que estimula la producción de insulina en el páncreas y mejora la resistencia a la insulina; Semaglutide se encuentra en investigación fase 3 después del análisis de la data de estudios cardiovasculares que redujeron el riesgo de Alzheimer en 53% en pacientes con diabetes tipo II.
Estudio de la conexión entre el corazón y la cabeza
La creciente evidencia sugiere que la salud del cerebro está estrechamente relacionada con la salud del corazón y de los vasos sanguíneos. El riesgo de desarrollar demencia parece aumentar como resultado de muchas afecciones que dañan el corazón o las arterias. Estos incluyen presión arterial alta, enfermedad cardíaca, accidente cerebrovascular, diabetes y colesterol alto. Varios estudios están explorando la mejor manera de aprovechar esta conexión. Las estrategias bajo investigación incluyen:
• Fármacos actuales para los factores de riesgo de una enfermedad cardíaca: Los investigadores están investigando si los fármacos —como los medicamentos para la presión arterial que ahora se usan para tratar la enfermedad vascular también— pueden ser beneficiosos para las personas con enfermedad de Alzheimer o pueden reducir el riesgo a desarrollar demencia.
• Fármacos dirigidos a nuevos objetivos: El análisis exhaustivo de cómo funciona a nivel molecular la conexión entre la enfermedad cardíaca y la enfermedad de Alzheimer para encontrar nuevas dianas terapéuticas.
• Opciones de estilo de vida: Se sugiere por estudios como el FINGER, que las opciones de estilo de vida con beneficios
cardíacos conocidos —como hacer ejercicio la mayoría de los días y consumir una dieta saludable para el corazón— pueden ayudar a prevenir la enfermedad de Alzheimer o retrasar su aparición.
Hormonas
En un estudio, recibir una terapia hormonal basada en estrógenos al menos un año durante la perimenopausia o la menopausia temprana pareció proteger el razonamiento y la memoria en mujeres con un mayor riesgo de padecer la enfermedad de Alzheimer. Pero las investigaciones posteriores han arrojado resultados contradictorios, ya que algunos estudios indican que el estrógeno no ofreció ningún beneficio. Antes de poder hacer recomendaciones, es necesario seguir investigando y comprender mejor la relación entre el estrógeno y la función cognitiva.
Balance de Excitación – Inhibición
El cerebro es una computadora eléctrica súper compleja, con billones de conexiones y utilizando azúcar de la sangre, formando y transmitiendo señales de excitación e inhibición por medio de neurotransmisores como dopamina, serotonina y acetilcolina.
Se ha encontrado que las personas que progresan en la EA puede que tengan desbalances de Excitación e Inhibición similar a la de personas con Epilepsia. Se investiga la detección de estos microcampos eléctricos y maneras de tratamiento eficaces que prolongan la vida de las neuronas afectadas.
ACELERAR EL DESARROLLO DE TRATAMIENTOS
El estudio de la EA envuelve una comunidad diversa, desde científicos, médicos, farmacéuticas, pacientes, grupos de apoyo y política pública.
La Asociación de Alzheimer une estas comunidades mediante su plataforma ISTAART (@ISTAART). Se busca no solo tratamientos, sino pruebas de detección temprana, mejorar la calidad de vida de la creciente población de envejecientes mediante la optimización de los sistemas de salud, programas sociales y planificación urbana.
El desarrollo de nuevos medicamentos es un proceso lento y meticuloso. El ritmo puede ser especialmente frustrante para las personas con Alzheimer y sus familias, que esperan nuevas opciones de tratamiento.
La Coalition Against Major Diseases (CAMD, Coalición contra las Enfermedades Importantes), alianza de compañías farmacéuticas, fundaciones sin fines de lucro y asesores gubernamentales, ha forjado una asociación de primera clase para compartir datos sobre los ensayos clínicos de Alzheimer. Colabora con el Clinical Data Interchange Standards Consortium (CDISC, Consorcio de Estándares de Intercambio de Datos Clínicos) para crear estándares de manejo de datos —para facilitar el intercambio de los datos de más de 6,500 participantes del estudio— y acelerar el desarrollo de terapias más efectivas. Similarmente existen varios repositorios de información compartida, entre ellos el ADNI, NACC y AMP-AD, basados en el Instituto Nacional de Salud (NIH), o el BioFINDER, ADDI y GAAIN.
Los expertos tienen una cautelosa esperanza de desarrollar tratamientos para el Alzheimer que puedan detener o retrasar significativamente la progresión de la enfermedad. Una comprensión cada vez mayor de cómo la condición altera el cerebro ha dado lugar a posibles tratamientos para el Alzheimer, que provocan un cortocircuito en los procesos básicos de la enfermedad, y arrestan la progresión.
23
RINVOQ met primary (ACR20 or ACR50 at Week 12 or 14) and ranked secondary endpoints in clinical trials, with some patients achieving ACR20 as early as Week 1 in SELECT-BEYOND1-3,a,b
LONG-TERM REMISSION AND LOW DISEASE ACTIVITY DATA observed up to 84 weeks with or without MTX1,3-6
• DAS28-CRP<2.6* and DAS28-CRP≤3.2 evaluated at Week 12 or 14, with response rates from 60 to 84 weeks (in SELECT-BEYOND and SELECT-MONOTHERAPY, respectively)
*Clinical remission does not mean drug-free remission or complete absence of disease activity.
LONG-TERM SAFETY DATA
AEs observed in long-term analysis with ~4.5 years maximum and ~2.6 years median exposure to RINVOQ 15 mg as of 6/30/207,a,b
• >4400 patients evaluated on upadacitinib,c with >7000 patientyears of long-term exposure to RINVOQ 15 mg as of 6/30/207,a,b
to exceptional access and patient support at RinvoqHCPPR.com

a SELECT-EARLY (RA-I; MTX-naïve) [primary endpoint at Week 12: ACR50 response vs MTX, select ranked secondary endpoint at Week 24: Δ mTSS vs MTX]; SELECT-MONOTHERAPY (RA-II;
INDICATION1


RINVOQ is indicated for the treatment of adults with moderately to severely active rheumatoid arthritis who have had an inadequate response or intolerance to one or more TNF blockers.
Limitation of Use: Use of RINVOQ in combination with other JAK inhibitors, biologic DMARDs, or with potent immunosuppressants, such as azathioprine and cyclosporine, is not recommended.

SAFETY CONSIDERATIONS1

Serious Infections: Patients treated with RINVOQ are at increased risk for developing serious infections that may lead to hospitalization or death. These infections include tuberculosis (TB), invasive fungal, bacterial, viral, and other infections due to opportunistic pathogens. Most patients who developed these infections were taking concomitant immunosuppressants, such as methotrexate or corticosteroids.
Mortality: A higher rate of all-cause mortality, including sudden cardiovascular (CV) death, was observed with a Janus kinase (JAK) inhibitor in a study comparing another JAK inhibitor with tumor necrosis factor (TNF) blockers in rheumatoid arthritis (RA) patients ≥50 years of age with at least one CV risk factor.
Malignancies: Lymphoma and other malignancies have been observed in RINVOQ-treated patients. A higher rate of malignancies (excluding non-melanoma skin cancer [NMSC]), lymphomas, and lung cancer (in current or past smokers) was observed with another JAK inhibitor when compared with TNF blockers in RA patients. Patients who are current or past smokers are at additional increased risk.
Major Adverse Cardiovascular Events: A higher rate of CV death, myocardial infarction, and stroke was observed with a JAK inhibitor in a study comparing another JAK inhibitor with TNF blockers in RA patients ≥50 years of age with at least one CV risk factor. Current or past smokers are at additional increased risk.
Thrombosis: Thrombosis, including deep venous thrombosis, pulmonary embolism, and arterial thrombosis have occurred in patients treated with JAK inhibitors used to treat inflammatory conditions. A higher rate of thrombosis was observed with another JAK inhibitor when compared with TNF blockers in RA patients.
Hypersensitivity: RINVOQ is contraindicated in patients with known hypersensitivity to upadacitinib or any of its excipients.
Other Serious Adverse Reactions: Hypersensitivity Reactions (anaphylaxis and angioedema), Gastrointestinal Perforations, Laboratory Abnormalities (neutropenia, lymphopenia, anemia, lipid elevations, liver enzyme elevations), and Embryo-Fetal Toxicity.
Safety Information, including BOXED WARNING on Serious Infections, Mortality, Malignancies, Major Adverse Cardiovascular Events, and Thrombosis, on the
Summary
of this advertisement.
of this advertisement.
Please see additional Important
previous page
Please see Brief
of full Prescribing Information on previous pages
MTX-IR) [primary endpoint at Week 14: ACR20 response vs MTX, select ranked secondary endpoints at Week 14: DAS28-CRP<2.6 vs MTX, DAS28-CRP≤3.2 vs MTX]; SELECT-NEXT (RA-III; csDMARD-IR) [RINVOQ + csDMARD; primary endpoint at Week 12: ACR20 response vs placebo + csDMARD]; SELECT-COMPARE (RA-IV; MTX-IR) [RINVOQ + MTX; primary endpoint at Week 12: ACR20 response vs placebo + MTX, select ranked secondary endpoints at Week 26: Δ mTSS vs placebo + MTX]; SELECT-BEYOND (RA-V; bDMARD-IR) [RINVOQ + csDMARD; primary endpoint at Week 12: ACR20 response vs placebo + csDMARD, select ranked secondary endpoints at Week 12: DAS28-CRP≤3.2 vs placebo + csDMARD.] 1,2 bSELECT-CHOICE (bDMARD-IR) [RINVOQ + csDMARDs; primary endpoint at Week 12: Δ DAS28-CRP (noninferiority) vs active comparator + csDMARDs]. 8 c RINVOQ 15 mg; upadacitinib 30 mg; RINVOQ 15 mg is the approved dose.1,7 ACR=American College of Rheumatology; AEs=adverse events; bDMARD=biologic DMARD; csDMARD=conventional synthetic DMARD; DAS28-CRP=Disease Activity Score 28 joints, C-reactive protein; DMARD=disease-modifying antirheumatic drug; HAQ-DI=Health Assessment Questionnaire Disability Index; IR=intolerance or inadequate response; JAK=Janus kinase; mTSS=modified total Sharp score; MTX=methotrexate; TNFi=tumor necrosis factor inhibitor. CHALLENGE TREATMENT GOALS IN RA WITH A ONCE-DAILY ORAL JAK INHIBITOR EXPECTATIONS For moderate to severe rheumatoid arthritis (RA) in adult TNFi-IR patients1 Discover our commitment
IMPORTANT
SERIOUS INFECTIONS
Patients treated with RINVOQ are at increased risk for developing serious infections that may lead to hospitalization or death. Most patients who developed these infections were taking concomitant immunosuppressants, such as methotrexate or corticosteroids. If a serious infection develops, interrupt RINVOQ until the infection is controlled.
Reported infections include:
• Active tuberculosis (TB), which may present with pulmonary or extrapulmonary disease. Test patients for latent TB before RINVOQ use and during therapy.
Consider treatment for latent TB infection prior to RINVOQ use.
• Invasive fungal infections, including cryptococcosis and pneumocystosis.
• Bacterial, viral, including herpes zoster, and other infections due to opportunistic pathogens.
Carefully consider the risks and benefits of treatment with RINVOQ prior to initiating therapy in patients with chronic or recurrent infection. Monitor patients closely for the development of signs and symptoms of infection during and after treatment with RINVOQ, including the possible development of TB in patients who tested negative for latent TB infection prior to initiating therapy.
MORTALITY
In a large, randomized, postmarketing safety study comparing another Janus kinase (JAK) inhibitor with tumor necrosis factor (TNF) blockers in rheumatoid arthritis (RA) patients ≥50 years old with at least one cardiovascular (CV) risk factor, a higher rate of all-cause mortality, including sudden CV death, was observed with the JAK inhibitor. Consider the benefits and risks for the individual patient prior to initiating or continuing therapy with RINVOQ.
MALIGNANCIES
Lymphoma and other malignancies have been observed in patients treated with RINVOQ.
In a large, randomized, postmarketing safety study comparing another JAK inhibitor with TNF blockers in RA patients, a higher rate of malignancies (excluding non-melanoma skin cancer [NMSC]), lymphomas, and lung cancer (in current or past smokers) was observed with the JAK inhibitor. Patients who are current or past smokers are at additional increased risk.
With RINVOQ, consider the benefits and risks for the individual patient prior to initiating or continuing therapy, particularly in patients with a known malignancy (other than a successfully treated NMSC), patients who develop a malignancy when on treatment, and patients who are current or past smokers. NMSCs have been reported in patients treated with RINVOQ. Periodic skin examination is recommended for patients who are at increased risk for skin cancer. Advise patients to limit sunlight exposure by wearing protective clothing and using sunscreen.
MAJOR ADVERSE CARDIOVASCULAR EVENTS
In a large, randomized, postmarketing study comparing another JAK inhibitor with TNF blockers in RA patients ≥50 years old with at least one CV risk factor, a higher rate of major adverse cardiovascular events (MACE) (defined as cardiovascular death, myocardial infarction, and stroke) was observed with the JAK inhibitor. Patients who are current or past smokers are at additional increased risk. Discontinue RINVOQ in patients that have experienced a myocardial infarction or stroke.
Consider the benefits and risks for the individual patient prior to initiating or continuing therapy with RINVOQ, particularly in patients who are current or past smokers and patients with other CV risk factors. Patients should be informed about the symptoms of serious CV events and the steps to take if they occur.
THROMBOSIS
Thrombosis, including deep venous thrombosis, pulmonary embolism, and arterial thrombosis have occurred in patients treated with JAK inhibitors used to treat inflammatory conditions. Many of these adverse events were serious and some resulted in death.
In a large, randomized, postmarketing study comparing another JAK inhibitor to TNF blockers in RA patients ≥50 years old with at least one CV risk factor, a higher rate of thrombosis was observed with the JAK inhibitor. Avoid RINVOQ in patients at risk. Patients with symptoms of thrombosis should discontinue RINVOQ and be promptly evaluated.
HYPERSENSITIVITY
RINVOQ is contraindicated in patients with known hypersensitivity to upadacitinib or any of its excipients. Serious hypersensitivity reactions, such as anaphylaxis and angioedema, were reported in patients receiving RINVOQ in clinical trials. If a clinically significant hypersensitivity reaction occurs, discontinue RINVOQ and institute appropriate therapy.
GASTROINTESTINAL PERFORATIONS
Gastrointestinal (GI) perforations have been reported in clinical trials with RINVOQ. Monitor RINVOQ-treated patients who may be at risk for gastrointestinal perforation (e.g., patients with a history of diverticulitis or taking NSAIDs). Promptly evaluate patients presenting with new onset abdominal pain for early identification of GI perforation.
LABORATORY ABNORMALITIES
Neutropenia
Treatment with RINVOQ was associated with an increased incidence of neutropenia (absolute neutrophil count [ANC] <1000 cells/mm3). Treatment with RINVOQ is not recommended in patients with an ANC <1000 cells/mm3. Evaluate neutrophil counts at baseline and thereafter according to routine patient management.
Lymphopenia
Absolute lymphocyte counts (ALC) <500 cells/mm3 were reported in RINVOQtreated patients. Treatment with RINVOQ is not recommended in patients with an ALC <500 cells/mm3. Evaluate at baseline and thereafter according to routine patient management.
Anemia
Decreases in hemoglobin levels to <8 g/dL were reported in RINVOQ-treated patients. Treatment should not be initiated or should be interrupted in patients with hemoglobin levels <8 g/dL. Evaluate at baseline and thereafter according to routine patient management.
Lipids
Treatment with RINVOQ was associated with increases in lipid parameters, including total cholesterol, low-density lipoprotein (LDL) cholesterol, and high-density lipoprotein (HDL) cholesterol. Manage patients according to clinical guidelines for the management of hyperlipidemia. Evaluate patients 12 weeks after initiation of treatment and thereafter according to the clinical guidelines for hyperlipidemia.
Liver enzyme elevations
Treatment with RINVOQ was associated with increased incidence of liver enzyme elevation compared to placebo. Evaluate at baseline and thereafter according to routine patient management. Prompt investigation of the cause of liver enzyme elevation is recommended to identify potential cases of drug-induced liver injury. If increases in aspartate aminotransferase (AST) or alanine aminotransferase (ALT) are observed during routine patient management and drug-induced liver injury is suspected, RINVOQ should be interrupted until this diagnosis is excluded.
EMBRYO-FETAL TOXICITY
Based on findings in animal studies, RINVOQ may cause fetal harm when administered to a pregnant woman. Advise pregnant women of the potential risk to a fetus. Advise females of reproductive potential to use effective contraception during treatment with RINVOQ and for 4 weeks after the final dose. Verify pregnancy status of females of reproductive potential prior to starting treatment with RINVOQ.
VACCINATION
Avoid use of live vaccines during, or immediately prior to, RINVOQ therapy. Prior to initiating RINVOQ, patients should be brought up to date on all immunizations, including varicella zoster or prophylactic herpes zoster vaccinations, in agreement with current immunization guidelines.
LACTATION
There are no data on the presence of RINVOQ in human milk, the effects on the breastfed infant, or the effects on milk production. Available data in animals have shown the excretion of RINVOQ in milk. Advise patients that breastfeeding is not recommended during treatment with RINVOQ and for 6 days after the last dose.
HEPATIC IMPAIRMENT
RINVOQ is not recommended for use in patients with severe hepatic impairment.
ADVERSE REACTIONS
The most common adverse reactions in RINVOQ clinical trials were upper respiratory tract infections, herpes zoster, herpes simplex, bronchitis, nausea, cough, pyrexia, acne, headache, increased blood creatine phosphokinase, hypersensitivity, folliculitis, abdominal pain, increased weight, influenza, fatigue, neutropenia, myalgia, influenzalike illness, elevated liver enzymes, and rash.
Inform patients that retinal detachment has been reported in clinical trials with RINVOQ. Advise patients to immediately inform their healthcare provider if they develop any sudden changes in vision while receiving RINVOQ.
Dosage Forms and Strengths: RINVOQ is available in 15 mg, 30 mg, and 45 mg extended-release tablets.
arthritis. Poster presented at: The European Congress of Rheumatology; June 2-5, 2021; E-Congress. 8. Rubbert-Roth A, Enejosa J, Pangan AL, et al. Trial of upadacitinib or abatacept in rheumatoid arthritis. N Engl J Med. 2020;383(16):1511-1521.
RINVOQ® and its design are registered trademarks of AbbVie Biotechnology Ltd. ©2022 AbbVie Inc. North Chicago, IL 60064 US-RNQR-220149 April 2022 Printed in Puerto Rico
Please see Brief Summary of full Prescribing Information on previous pages of this advertisement. References: 1. RINVOQ [package insert]. North Chicago, IL: AbbVie Inc; 2022. 2. Data on file, AbbVie Inc. ABVRRTI68885. 3. Genovese MC, Fleischmann R, Combe B, et al. Safety and efficacy of upadacitinib in patients with active rheumatoid arthritis refractory to biologic disease-modifying anti-rheumatic drugs (SELECT-BEYOND): a double-blind, randomised controlled phase 3 trial. Lancet. 2018;391(10139): 2513-2524. 4. Smolen JS, Emery P, Rigby W, et al. Upadacitinib as monotherapy in patients with rheumatoid arthritis and prior inadequate response to methotrexate: results at 84 weeks from the SELECTMONOTHERAPY study. Poster presented at: The European Congress of Rheumatology; June 3-6, 2020; E-Congress. 5. Smolen JS, Pangan AL, Emery P, et al. Upadacitinib as monotherapy in patients with active rheumatoid arthritis and inadequate response to methotrexate (SELECT-MONOTHERAPY): a randomised, placebo-controlled, double-blind phase 3 study. Lancet. 2019;393(10188):2303-2311. Erratum in: Lancet. 2019;393(10191):2590. 6. Genovese MC, Combe B,
Hall
S, et al.
Upadacitinib in patients with rheumatoid arthritis and inadequate response or intolerance to biological DMARDs: Results at 60
weeks
from the SELECT-BEYOND
study.
Poster presented at: The American College of Rheumatology; November 8-13, 2019. 7. Cohen SB, van Vollenhoven R, Curtis JR, et al. Integrated safety profile of
upadacitinib with up to 4.5 years of exposure in patients with rheumatoid
SAFETY INFORMATION1
extended-release tablets, for oral use
CONTRAINDICATIONS
PROFESSIONAL BRIEF SUMMARY
INSERT
WARNING: SERIOUS INFECTIONS, MORTALITY, MALIGNANCY, MAJOR ADVERSE CARDIOVASCULAR EVENTS, and THROMBOSIS
SERIOUS INFECTIONS
Patients treated with RINVOQ are at increased risk for developing serious infections that may lead to hospitalization or death [see Warnings and Precautions, Adverse Reactions]. Most patients who developed these infections were taking concomitant immunosuppressants such as methotrexate or corticosteroids.
If a serious infection develops, interrupt RINVOQ until the infection is controlled.
Reported infections include:
• Active tuberculosis, which may present with pulmonary or extrapulmonary disease. Patients should be tested for latent tuberculosis before RINVOQ use and during therapy. Treatment for latent infection should be considered prior to RINVOQ use.
• Invasive fungal infections, including cryptococcosis and pneumocystosis.
• Bacterial, viral, including herpes zoster, and other infections due to opportunistic pathogens.
The risks and benefits of treatment with RINVOQ should be carefully considered prior to initiating therapy in patients with chronic or recurrent infection.
Patients should be closely monitored for the development of signs and symptoms of infection during and after treatment with RINVOQ, including the possible development of tuberculosis in patients who tested negative for latent tuberculosis infection prior to initiating therapy [see Warnings and Precautions].
MORTALITY
In a large, randomized, postmarketing safety study in rheumatoid arthritis (RA) patients 50 years of age and older with at least one cardiovascular risk factor comparing another Janus kinase (JAK) inhibitor to tumor necrosis factor (TNF) blockers, a higher rate of all-cause mortality, including sudden cardiovascular death, was observed with the JAK inhibitor [see Warnings and Precautions]
MALIGNANCIES
Lymphoma and other malignancies have been observed in patients treated with RINVOQ. In RA patients treated with another JAK inhibitor, a higher rate of malignancies (excluding non-melanoma skin cancer (NMSC)) was observed when compared with TNF blockers. Patients who are current or past smokers are at additional increased risk [see Warnings and Precautions]
MAJOR ADVERSE CARDIOVASCULAR EVENTS
In RA patients 50 years of age and older with at least one cardiovascular risk factor treated with another JAK inhibitor, a higher rate of major adverse cardiovascular events (MACE) (defined as cardiovascular death, myocardial infarction, and stroke), was observed when compared with TNF blockers. Patients who are current or past smokers are at additional increased risk. Discontinue RINVOQ in patients that have experienced a myocardial infarction or stroke [see Warnings and Precautions].
THROMBOSIS
Thrombosis, including deep venous thrombosis, pulmonary embolism, and arterial thrombosis have occurred in patients treated with JAK inhibitors used to treat inflammatory conditions. Many of these adverse events were serious and some resulted in death. In RA patients 50 years of age and older with at least one cardiovascular risk factor treated with another JAK inhibitor, a higher rate of thrombosis was observed when compared with TNF blockers. Avoid RINVOQ in patients at risk. Patients with symptoms of thrombosis should discontinue RINVOQ and be promptly evaluated [see Warnings and Precautions]
INDICATIONS AND USAGE
Rheumatoid Arthritis
RINVOQ® is indicated for the treatment of adults with moderately to severely active rheumatoid arthritis who have had an inadequate response or intolerance to one or more TNF blockers.
• Limitations of Use: Use of RINVOQ in combination with other JAK inhibitors, biologic disease-modifying antirheumatic drugs (DMARDs), or with potent immunosuppressants such as azathioprine and cyclosporine, is not recommended.
Psoriatic Arthritis
RINVOQ is indicated for the treatment of adults with active psoriatic arthritis who have had an inadequate response or intolerance to one or more TNF blockers.
• Limitations of Use: Use of RINVOQ in combination with other JAK inhibitors, biologic DMARDs, or with potent immunosuppressants such as azathioprine and cyclosporine, is not recommended.
Atopic Dermatitis
RINVOQ is indicated for the treatment of adults and pediatric patients 12 years of age and older with refractory, moderate to severe atopic dermatitis whose disease is not adequately controlled with other systemic drug products, including biologics, or when use of those therapies are inadvisable.
• Limitations of Use: RINVOQ is not recommended for use in combination with other JAK inhibitors, biologic immunomodulators, or with other immunosuppressants.
Ulcerative Colitis
RINVOQ is indicated for the treatment of adult patients with moderately to severely active ulcerative colitis who have had an inadequate response or intolerance to one or more TNF blockers.
• Limitations of Use: RINVOQ is not recommended for use in combination with other JAK inhibitors, biological therapies for ulcerative colitis, or with potent immunosuppressants such as azathioprine and cyclosporine.
Ankylosing Spondylitis
RINVOQ is indicated for the treatment of adults with active ankylosing spondylitis who have had an inadequate response or intolerance to one or more TNF blockers.
• Limitations of Use: Use of RINVOQ in combination with other JAK inhibitors, biologic DMARDs, or with potent immunosuppressants such as azathioprine and cyclosporine, is not recommended.
RINVOQ is contraindicated in patients with known hypersensitivity to upadacitinib or any of its excipients [see Warnings and Precautions].
WARNINGS AND PRECAUTIONS Serious Infections
Serious and sometimes fatal infections have been reported in patients receiving RINVOQ. The most frequent serious infections reported with RINVOQ included pneumonia and cellulitis [see Adverse Reactions]. Among opportunistic infections, tuberculosis, multidermatomal herpes zoster, oral/esophageal candidiasis, and cryptococcosis, were reported with RINVOQ.
Avoid use of RINVOQ in patients with an active, serious infection, including localized infections. Consider the risks and benefits of treatment prior to initiating RINVOQ in patients:
• with chronic or recurrent infection
• who have been exposed to tuberculosis
• with a history of a serious or an opportunistic infection
• who have resided or traveled in areas of endemic tuberculosis or endemic mycoses; or
• with underlying conditions that may predispose them to infection.
Closely monitor patients for the development of signs and symptoms of infection during and after treatment with RINVOQ. Interrupt RINVOQ if a patient develops a serious or opportunistic infection.
A patient who develops a new infection during treatment with RINVOQ should undergo prompt and complete diagnostic testing appropriate for an immunocompromised patient; appropriate antimicrobial therapy should be initiated, the patient should be closely monitored, and RINVOQ should be interrupted if the patient is not responding to antimicrobial therapy. RINVOQ may be resumed once the infection is controlled.
Tuberculosis
Evaluate and test patients for latent and active tuberculosis (TB) infection prior to administration of RINVOQ. Patients with latent TB should be treated with standard antimycobacterial therapy before initiating RINVOQ. RINVOQ should not be given to patients with active TB. Consider anti-TB therapy prior to initiation of RINVOQ in patients with previously untreated latent TB or active TB in whom an adequate course of treatment cannot be confirmed, and for patients with a negative test for latent TB but who have risk factors for TB infection.
Consultation with a physician with expertise in the treatment of TB is recommended to aid in the decision about whether initiating anti-TB therapy is appropriate for an individual patient.
During RINVOQ use, monitor patients for the development of signs and symptoms of TB, including patients who tested negative for latent TB infection prior to initiating therapy.
Viral Reactivation
Viral reactivation, including cases of herpes virus reactivation (e.g., herpes zoster) and hepatitis B virus reactivation, were reported in clinical trials with RINVOQ [see Adverse Reactions]. The risk of herpes zoster appears to be higher in patients treated with RINVOQ in Japan. If a patient develops herpes zoster, consider temporarily interrupting RINVOQ until the episode resolves. Screening for viral hepatitis and monitoring for reactivation should be performed in accordance with clinical guidelines before starting and during therapy with RINVOQ. Patients who were positive for hepatitis C antibody and hepatitis C virus RNA, were excluded from clinical trials. Patients who were positive for hepatitis B surface antigen or hepatitis B virus DNA were excluded from clinical trials. However, cases of hepatitis B reactivation were still reported in patients enrolled in the Phase 3 trials of RINVOQ. If hepatitis B virus DNA is detected while receiving RINVOQ, a liver specialist should be consulted.
Mortality
In a large, randomized, postmarketing safety study of another JAK inhibitor in RA patients 50 years of age and older with at least one cardiovascular risk factor, a higher rate of all-cause mortality, including sudden cardiovascular death, was observed in patients treated with the JAK inhibitor compared with TNF blockers.
Consider the benefits and risks for the individual patient prior to initiating or continuing therapy with RINVOQ.
Malignancy and Lymphoproliferative Disorders
Malignancies, including lymphomas, were observed in clinical trials of RINVOQ [see Adverse Reactions]
In a large, randomized, postmarketing safety study of another JAK inhibitor in RA patients, a higher rate of malignancies (excluding non-melanoma skin cancer (NMSC)) was observed in patients treated with the JAK inhibitor compared to those treated with TNF blockers. A higher rate of lymphomas was observed in patients treated with the JAK inhibitor compared to those treated with TNF blockers. A higher rate of lung cancers was observed in current or past smokers treated with the JAK inhibitor compared to those treated with TNF blockers. In this study, current or past smokers had an additional increased risk of overall malignancies.
Consider the benefits and risks for the individual patient prior to initiating or continuing therapy with RINVOQ, particularly in patients with a known malignancy (other than a successfully treated NMSC), patients who develop a malignancy when on treatment, and patients who are current or past smokers.
Non-Melanoma Skin Cancer
NMSCs have been reported in patients treated with RINVOQ. Periodic skin examination is recommended for patients who are at increased risk for skin cancer.
Exposure to sunlight and UV light should be limited by wearing protective clothing and using a broad-spectrum sunscreen.
Major Adverse Cardiovascular Events
In a large, randomized, postmarketing safety study of another JAK inhibitor in RA patients 50 years of age and older with at least one cardiovascular risk factor, a higher rate of major adverse cardiovascular events (MACE) defined as cardiovascular death, non-fatal myocardial infarction (MI), and non-fatal stroke was observed with the JAK inhibitor compared to those treated with TNF blockers. Patients who are current or past smokers are at additional increased risk.
Consider the benefits and risks for the individual patient prior to initiating or continuing therapy with RINVOQ, particularly in patients who are current or past smokers and patients with other cardiovascular risk factors. Patients
PRESCRIBING
should be informed about the symptoms of serious cardiovascular events and the steps to take if they occur. Discontinue RINVOQ in patients that have experienced a myocardial infarction or stroke.
Thrombosis
Thrombosis, including deep venous thrombosis (DVT), pulmonary embolism (PE), and arterial thrombosis, have occurred in patients treated for inflammatory conditions with JAK inhibitors, including RINVOQ. Many of these adverse events were serious and some resulted in death.
In a large, randomized, postmarketing safety study of another JAK inhibitor in RA patients 50 years of age and older with at least one cardiovascular risk factor, higher rates of overall thrombosis, DVT, and PE were observed compared to those treated with TNF blockers.
If symptoms of thrombosis occur, patients should discontinue RINVOQ and be evaluated promptly and treated appropriately. Avoid RINVOQ in patients that may be at increased risk of thrombosis.
Hypersensitivity Reactions
Serious hypersensitivity reactions such as anaphylaxis and angioedema were reported in patients receiving RINVOQ in clinical trials. If a clinically significant hypersensitivity reaction occurs, discontinue RINVOQ and institute appropriate therapy [see Adverse Reactions].
Gastrointestinal Perforations
Gastrointestinal perforations have been reported in clinical trials with RINVOQ.
Monitor RINVOQ-treated patients who may be at risk for gastrointestinal perforation (e.g., patients with a history of diverticulitis or taking NSAIDs). Evaluate promptly patients presenting with new onset abdominal pain for early identification of gastrointestinal perforation.
Laboratory Abnormalities
Neutropenia
Treatment with RINVOQ was associated with an increased incidence of neutropenia (ANC less than 1000 cells/mm3).
Evaluate neutrophil counts at baseline and thereafter according to routine patient management. Avoid RINVOQ initiation and interrupt RINVOQ treatment in patients with a low neutrophil count (i.e., ANC less than 1000 cells/mm3).
Lymphopenia
ALC less than 500 cells/mm3 were reported in RINVOQ-treated patients in clinical trials.
Evaluate lymphocyte counts at baseline and thereafter according to routine patient management. Avoid RINVOQ initiation or interrupt RINVOQ treatment in patients with a low lymphocyte count (i.e., less than 500 cells/mm3).
Anemia
Decreases in hemoglobin levels to less than 8 g/dL were reported in RINVOQ-treated patients in clinical trials.
Evaluate hemoglobin at baseline and thereafter according to routine patient management. Avoid RINVOQ initiation or interrupt RINVOQ treatment in patients with a low hemoglobin level (i.e., less than 8 g/dL).
Lipids
Treatment with RINVOQ was associated with increases in lipid parameters, including total cholesterol, low-density lipoprotein (LDL) cholesterol, and high-density lipoprotein (HDL) cholesterol [see Adverse Reactions] Elevations in LDL cholesterol decreased to pre-treatment levels in response to statin therapy. The effect of these lipid parameter elevations on cardiovascular morbidity and mortality has not been determined.
Assess lipid parameters approximately 12 weeks after initiation of treatment, and thereafter according to the clinical guidelines for hyperlipidemia. Manage patients according to clinical guidelines for the management of hyperlipidemia.
Liver Enzyme Elevations
Treatment with RINVOQ was associated with increased incidence of liver enzyme elevations compared to treatment with placebo.
Evaluate liver enzymes at baseline and thereafter according to routine patient management. Prompt investigation of the cause of liver enzyme elevation is recommended to identify potential cases of drug-induced liver injury.
If increases in ALT or AST are observed during routine patient management and drug-induced liver injury is suspected, RINVOQ should be interrupted until this diagnosis is excluded.
Embryo-Fetal Toxicity
Based on findings in animal studies, RINVOQ may cause fetal harm when administered to a pregnant woman. Administration of upadacitinib to rats and rabbits during organogenesis caused increases in fetal malformations. Verify the pregnancy status of patients of reproductive potential prior to starting treatment. Advise females of reproductive potential of the potential risk to the fetus and to use effective contraception during treatment with RINVOQ and for 4 weeks following completion of therapy [see Use in Specific Populations]
Vaccinations
Avoid use of live vaccines during, or immediately prior to, RINVOQ therapy. Prior to initiating RINVOQ, it is recommended that patients be brought up to date with all immunizations, including varicella zoster or prophylactic herpes zoster vaccinations, in agreement with current immunization guidelines.
ADVERSE REACTIONS
The following clinically significant adverse reactions are described elsewhere in the labeling:
• Serious Infections [see Warnings and Precautions]
• Mortality [see Warnings and Precautions]
• Malignancy and Lymphoproliferative Disorders [see Warnings and Precautions]
• Major Adverse Cardiovascular Events [see Warnings and Precautions]
• Thrombosis [see Warnings and Precautions]
• Hypersensitivity Reactions [see Warnings and Precautions]
• Gastrointestinal Perforations [see Warnings and Precautions]
• Laboratory Abnormalities [see Warnings and Precautions]
Clinical Trials Experience
Because clinical trials are conducted under widely varying conditions, adverse reaction rates observed in the clinical trials of a drug cannot be directly compared to rates in the clinical trials of another drug and may not reflect the rates observed in practice.
RINVOQ® (RIN-VOKE) (upadacitinib)
CONSULT PACKAGE
FOR FULL
INFORMATION
Adverse Reactions in Patients with Rheumatoid Arthritis
A total of 3833 patients with rheumatoid arthritis were treated with upadacitinib in the Phase 3 clinical trials of whom 2806 were exposed for at least one year.
Patients could advance or switch to RINVOQ 15 mg from placebo, or be rescued to RINVOQ from active comparator or placebo from as early as Week 12 depending on the trial design.
A total of 2630 patients received at least 1 dose of RINVOQ 15 mg, of whom 1860 were exposed for at least one year. In trials RA-I, RA-II, RA-III and RA-V, 1213 patients received at least 1 dose of RINVOQ 15 mg, of which 986 patients were exposed for at least one year, and 1203 patients received at least 1 dose of upadacitinib 30 mg, of which 946 were exposed for at least one year.
Table 1: Adverse Reactions Reported in ≥ 1% of Rheumatoid Arthritis Patients Treated with RINVOQ 15 mg in Placebo-controlled Trials
Adverse Reaction Placebo RINVOQ 15 mg n=1042 (%) n=1035 (%)
Upper respiratory tract infection (URTI)* 9.5 13.5 Nausea 2.2 3.5 Cough 1.0 2.2 Pyrexia 0 1.2
*URTI includes: acute sinusitis, laryngitis, nasopharyngitis, oropharyngeal pain, pharyngitis, pharyngotonsillitis, rhinitis, sinusitis, tonsillitis, viral upper respiratory tract infection
Other adverse reactions reported in less than 1% of patients in the RINVOQ 15 mg group and at a higher rate than in the placebo group through Week 12 included pneumonia, herpes zoster, herpes simplex (includes oral herpes), and oral candidiasis.
Four integrated datasets are presented in the Specific Adverse Reaction section:
Placebo-controlled Trials: Trials RA-III, RA-IV, and RA-V were integrated to represent safety through 12/14 weeks for placebo (n=1042) and RINVOQ 15 mg (n=1035). Trials RA-III and RA-V were integrated to represent safety through 12 weeks for placebo (n=390), RINVOQ 15 mg (n=385), and upadacitinib 30 mg (n=384). Trial RA-IV did not include the 30 mg dose and, therefore, safety data for upadacitinib 30 mg can only be compared with placebo and RINVOQ 15 mg rates from pooling trials RA-III and RA-V.
MTX-controlled Trials: Trials RA-I and RA-II were integrated to represent safety through 12/14 weeks for MTX (n=530), RINVOQ 15 mg (n=534), and upadacitinib 30 mg (n=529).
12-Month Exposure Dataset: Trials RA-I, II, III, and V were integrated to represent the long-term safety of RINVOQ 15 mg (n=1213) and upadacitinib 30 mg (n=1203).
Exposure adjusted incidence rates were adjusted by trial for all the adverse events reported in this section.
Specific Adverse Reactions
Infections
Placebo-controlled Trials: In RA-III, RA-IV, and RA-V, infections were reported in 218 patients (95.7 per 100 patient-years) treated with placebo and 284 patients (127.8 per 100 patient-years) treated with RINVOQ 15 mg. In RA-III and RA-V, infections were reported in 99 patients (136.5 per 100 patient-years) treated with placebo, 118 patients (164.5 per 100 patient-years) treated with RINVOQ 15 mg, and 126 patients (180.3 per 100 patient-years) treated with upadacitinib 30 mg.
MTX-controlled Trials: Infections were reported in 127 patients (119.5 per 100 patient-years) treated with MTX monotherapy, 104 patients (91.8 per 100 patient-years) treated with RINVOQ 15 mg monotherapy, and 128 patients (115.1 per 100 patient-years) treated with upadacitinib 30 mg monotherapy.
12-Month Exposure Dataset: Infections were reported in 615 patients (83.8 per 100 patient-years) treated with RINVOQ 15 mg and 674 patients (99.7 per 100 patient-years) treated with upadacitinib 30 mg.
Serious Infections
Placebo-controlled Trials: In RA-III, RA-IV, and RA-V, serious infections were reported in 6 patients (2.3 per 100 patient-years) treated with placebo, and 12 patients (4.6 per 100 patient-years) treated with RINVOQ 15 mg. In RA-III and RA-V, serious infections were reported in 1 patient (1.2 per 100 patientyears) treated with placebo, 2 patients (2.3 per 100 patient-years) treated with RINVOQ 15 mg, and 7 patients (8.2 per 100 patient-years) treated with upadacitinib 30 mg.
MTX-controlled Trials: Serious infections were reported in 2 patients (1.6 per 100 patient-years) treated with MTX monotherapy, 3 patients (2.4 per 100 patient-years) treated with RINVOQ 15 mg monotherapy, and 8 patients (6.4 per 100 patient-years) treated with upadacitinib 30 mg monotherapy.
12-Month Exposure Dataset: Serious infections were reported in 38 patients (3.5 per 100 patient-years) treated with RINVOQ 15 mg and 59 patients (5.6 per 100 patient-years) treated with upadacitinib 30 mg. The most frequently reported serious infections were pneumonia and cellulitis.
Tuberculosis
Placebo-controlled Trials and MTX-controlled Trials: In the placebo-controlled period, there were no active cases of tuberculosis reported in the placebo, RINVOQ 15 mg, and upadacitinib 30 mg groups. In the MTX-controlled period, there were no active cases of tuberculosis reported in the MTX monotherapy, RINVOQ 15 mg monotherapy, and upadacitinib 30 mg monotherapy groups.
12-Month Exposure Dataset: Active tuberculosis was reported for 2 patients treated with RINVOQ 15 mg and 1 patient treated with upadacitinib 30 mg. Cases of extra-pulmonary tuberculosis were reported.
Opportunistic Infections (excluding tuberculosis)
Placebo-controlled Trials: In RA-III, RA-IV, and RA-V, opportunistic infections were reported in 3 patients (1.2 per 100 patient-years) treated with placebo, and 5 patients (1.9 per 100 patient-years) treated with RINVOQ 15 mg. In RA-III and RA-V, opportunistic infections were reported in 1 patient (1.2 per 100 patient-years) treated with placebo, 2 patients (2.3 per 100 patient-years) treated with RINVOQ 15 mg, and 6 patients (7.1 per 100 patient-years) treated with upadacitinib 30 mg.
MTX-controlled Trials: Opportunistic infections were reported in 1 patient (0.8 per 100 patient-years) treated with MTX monotherapy, 0 patients
treated with RINVOQ 15 mg monotherapy, and 4 patients (3.2 per 100 patient-years) treated with upadacitinib 30 mg monotherapy.
12-Month Exposure Dataset: Opportunistic infections were reported in 7 patients (0.6 per 100 patient-years) treated with RINVOQ 15 mg and 15 patients (1.4 per 100 patient-years) treated with upadacitinib 30 mg.
Malignancies
Placebo-controlled Trials: In RA-III, RA-IV, and RA-V, malignancies excluding NMSC were reported in 1 patient (0.4 per 100 patient-years) treated with placebo, and 1 patient (0.4 per 100 patient-years) treated with RINVOQ 15 mg. In RA-III and RA-V, malignancies excluding NMSC were reported in 0 patients treated with placebo, 1 patient (1.1 per 100 patient-years) treated with RINVOQ 15 mg, and 3 patients (3.5 per 100 patient-years) treated with upadacitinib 30 mg.
MTX-controlled Trials: Malignancies excluding NMSC were reported in 1 patient (0.8 per 100 patient-years) treated with MTX monotherapy, 3 patients (2.4 per 100 patient-years) treated with RINVOQ 15 mg monotherapy, and 0 patients treated with upadacitinib 30 mg monotherapy.
12-Month Exposure Dataset: Malignancies excluding NMSC were reported in 13 patients (1.2 per 100 patient-years) treated with RINVOQ 15 mg and 14 patients (1.3 per 100 patient-years) treated with upadacitinib 30 mg.
Gastrointestinal Perforations
Placebo-controlled Trials: There were no gastrointestinal perforations (based on medical review) reported in patients treated with placebo, RINVOQ 15 mg, and upadacitinib 30 mg.
MTX-controlled Trials: There were no cases of gastrointestinal perforations reported in the MTX and RINVOQ 15 mg group through 12/14 weeks. Two cases of gastrointestinal perforations were observed in the upadacitinib 30 mg group.
12-Month Exposure Dataset: Gastrointestinal perforations were reported in 1 patient treated with RINVOQ 15 mg and 4 patients treated with upadacitinib 30 mg.
Thrombosis
Placebo-controlled Trials: In RA-IV, venous thrombosis (pulmonary embolism or deep vein thrombosis) was observed in 1 patient treated with placebo and 1 patient treated with RINVOQ 15 mg. In RA-V, venous thrombosis was observed in 1 patient treated with RINVOQ 15 mg. There were no observed cases of venous thrombosis reported in RA-III. No cases of arterial thrombosis were observed through 12/14 weeks.
MTX-controlled Trials: In RA-II, venous thrombosis was observed in 0 patients treated with MTX monotherapy, 1 patient treated with RINVOQ 15 mg monotherapy and 0 patients treated with upadacitinib 30 mg monotherapy through Week 14. In RA-II, no cases of arterial thrombosis were observed through 12/14 weeks. In RA-I, venous thrombosis was observed in 1 patient treated with MTX, 0 patients treated with RINVOQ 15 mg and 1 patient treated with upadacitinib 30 mg through Week 24. In RA-I, arterial thrombosis was observed in 1 patient treated with upadacitinib 30 mg through Week 24.
12-Month Exposure Dataset: Venous thrombosis events were reported in 5 patients (0.5 per 100 patient-years) treated with RINVOQ 15 mg and 4 patients (0.4 per 100 patient-years) treated with upadacitinib 30 mg. Arterial thrombosis events were reported in 0 patients treated with RINVOQ 15 mg and 2 patients (0.2 per 100 patient-years) treated with upadacitinib 30 mg.
Laboratory Abnormalities
Hepatic Transaminase Elevations
In placebo-controlled trials (RA-III, RA-IV, and RA-V) with background DMARDs, for up to 12/14 weeks, alanine transaminase (ALT) and aspartate transaminase (AST) elevations ≥ 3 x upper limit of normal (ULN) in at least one measurement were observed in 2.1% and 1.5% of patients treated with RINVOQ 15 mg, and in 1.5% and 0.7% of patients treated with placebo, respectively. In RA-III and RA-V, ALT and AST elevations ≥ 3 x ULN in at least one measurement were observed in 0.8% and 1.0% of patients treated with RINVOQ 15 mg, 1.0% and 0% of patients treated with upadacitinib 30 mg and in 1.3% and 1.0% of patients treated with placebo, respectively.
In MTX-controlled trials, for up to 12/14 weeks, ALT and AST elevations ≥ 3 x ULN in at least one measurement were observed in 0.8% and 0.4% of patients treated with RINVOQ 15 mg, 1.7% and 1.3% of patients treated with upadacitinib 30 mg and in 1.9% and 0.9% of patients treated with MTX, respectively.
Lipid Elevations
Upadacitinib treatment was associated with dose-related increases in total cholesterol, triglycerides and LDL cholesterol. Upadacitinib was also associated with increases in HDL cholesterol. Elevations in LDL and HDL cholesterol peaked by Week 8 and remained stable thereafter. In controlled trials, for up to 12/14 weeks, changes from baseline in lipid parameters in patients treated with RINVOQ 15 mg and upadacitinib 30 mg, respectively, are summarized below:
• Mean LDL cholesterol increased by 14.81 mg/dL and 17.17 mg/dL.
• Mean HDL cholesterol increased by 8.16 mg/dL and 9.01 mg/dL.
• The mean LDL/HDL ratio remained stable.
• Mean triglycerides increased by 13.55 mg/dL and 14.44 mg/dL.
Creatine Phosphokinase Elevations
In placebo-controlled trials (RA-III, RA-IV, and RA-V) with background DMARDs, for up to 12/14 weeks, dose-related increases in creatine phosphokinase (CPK) values were observed. CPK elevations > 5 x ULN were reported in 1.0%, and 0.3% of patients over 12/14 weeks in the RINVOQ 15 mg and placebo groups, respectively. Most elevations >5 x ULN were transient and did not require treatment discontinuation. In RA-III and RA-V, CPK elevations > 5 x ULN were observed in 0.3% of patients treated with placebo, 1.6% of patients treated with RINVOQ 15 mg, and none in patients treated with upadacitinib 30 mg.
Neutropenia
In placebo-controlled trials (RA-III, RA-IV, and RA-V) with background DMARDs, for up to 12/14 weeks, dose-related decreases in neutrophil counts, below 1000 cells/mm3 in at least one measurement occurred in 1.1% and <0.1% of patients in the RINVOQ 15 mg and placebo groups, respectively. In RA-III and RA-V, decreases in neutrophil counts below 1000 cells/mm3 in at least one measurement occurred in 0.3% of patients treated with placebo, 1.3% of patients treated with RINVOQ 15 mg, and 2.4% of patients treated with upadacitinib 30 mg. In clinical trials, treatment was interrupted in response to ANC less than 1000 cells/mm3
Lymphopenia
In placebo-controlled trials (RA-III, RA-IV, and RA-V) with background DMARDs, for up to 12/14 weeks, dose-related decreases in lymphocyte counts below 500 cells/mm3 in at least one measurement occurred in 0.9%
and 0.7% of patients in the RINVOQ 15 mg and placebo groups, respectively. In RA-III and RA-V, decreases in lymphocyte counts below 500 cells/mm3 in at least one measurement occurred in 0.5% of patients treated with placebo, 0.5% of patients treated with RINVOQ 15 mg, and 2.4% of patients treated with upadacitinib 30 mg.
Anemia
In placebo-controlled trials (RA-III, RA-IV, and RA-V) with background DMARDs, for up to 12/14 weeks, hemoglobin decreases below 8 g/dL in at least one measurement occurred in <0.1% of patients in both the RINVOQ 15 mg and placebo groups. In RA-III and RA-V, hemoglobin decreases below 8 g/dL in at least one measurement were observed in 0.3% of patients treated with placebo, and none in patients treated with RINVOQ 15 mg and upadacitinib 30 mg.
Adverse Reactions in Patients with Psoriatic Arthritis
A total of 1827 patients with psoriatic arthritis were treated with upadacitinib in clinical trials representing 1639.2 patient-years of exposure, of whom 722 were exposed to upadacitinib for at least one year. In the two Phase 3 trials, 907 patients received at least 1 dose of RINVOQ 15 mg, of whom 359 were exposed for at least one year.
Two placebo-controlled trials were integrated (640 patients on RINVOQ 15 mg once daily and 635 patients on placebo) to evaluate the safety of RINVOQ 15 mg in comparison to placebo for up to 24 weeks after treatment initiation.
Overall, the safety profile observed in patients with active psoriatic arthritis treated with RINVOQ 15 mg was consistent with the safety profile observed in patients with rheumatoid arthritis. During the 24-week placebo-controlled period, the frequencies of herpes zoster and herpes simplex were ≥1% (1.1% and 1.4%, respectively) with RINVOQ 15 mg and 0.8% and 1.3%, respectively with placebo. A higher incidence of acne and bronchitis was also observed in patients treated with RINVOQ 15 mg (1.3% and 3.9%, respectively) compared to placebo (0.3% and 2.7%, respectively).
Adverse Reactions in Patients with Atopic Dermatitis
Three Phase 3 (AD-1, AD-2, and AD-3) and one Phase 2b (AD-4) randomized, double-blind, placebo-controlled, multicenter trials evaluated the safety of RINVOQ in patients with moderate-to-severe atopic dermatitis. The majority of patients were White (68%) and male (57%). The mean age was 34 years (ranged from 12 to 75 years) and 13% of the patients were 12 to less than 18 years. In these 4 trials, 2612 patients were treated with RINVOQ 15 mg or 30 mg orally once daily, with or without concomitant topical corticosteroids (TCS).
In the Phase 3 clinical trials (AD-1, AD-2, and AD-3), a total of 1239 patients received RINVOQ 15 mg, of whom 791 were exposed for at least one year and 1246 patients received RINVOQ 30 mg, of whom 826 were exposed for at least one year.
Trials AD-1, AD-2, and AD-4 compared the safety of RINVOQ monotherapy to placebo through Week 16. Trial AD-3 compared the safety of RINVOQ + TCS to placebo + TCS through Week 16.
Weeks 0 to 16 (Trials AD-1 to AD-4)
In RINVOQ trials with and without TCS (Trials AD-1, 2, 3 and 4) through Week 16, the proportion of patients who discontinued treatment because of adverse reactions in the RINVOQ 15 mg, 30 mg and placebo groups were 2.3%, 2.9% and 3.8%, respectively. Table 2 summarizes the adverse reactions that occurred at a rate of at least 1% in the RINVOQ 15 mg or 30 mg groups during the first 16 weeks of treatment.
Table 2: Adverse Reactions Reported in ≥ 1% of Patients with Atopic Dermatitis Treated with RINVOQ 15 mg or 30 mg
Adverse Reaction
Placebo RINVOQ 15 mg RINVOQ 30 mg n=902 (%) n=899 (%) n=906 (%)
Upper respiratory tract infection (URTI)* 17 23 25 Acne** 2 10 16 Herpes simplex*** 2 4 8 Headache 4 6 6 Increased blood creatine phosphokinase 2 5 6 Cough 1 3 3 Hypersensitivity**** 2 2 3 Folliculitis 1 2 3 Nausea 1 3 3 Abdominal pain***** 1 3 2 Pyrexia 1 2 2 Increased Weight 1 2 2 Herpes zoster****** 1 2 2 Influenza <1 2 2 Fatigue 1 1 2 Neutropenia <1 1 2 Myalgia 1 1 2 Influenza like illness 1 1 2
* Includes: laryngitis, laryngitis viral, nasopharyngitis, oropharyngeal pain, pharyngeal abscess, pharyngitis, pharyngitis streptococcal, pharyngotonsillitis, respiratory tract infection, respiratory tract infection viral, rhinitis, rhinolaryngitis, sinusitis, tonsillitis, tonsillitis bacterial, upper respiratory tract infection, viral pharyngitis, viral upper respiratory tract infection
** Includes: acne and dermatitis acneiform
*** Includes: genital herpes, genital herpes simplex, herpes dermatitis, herpes ophthalmic, herpes simplex, nasal herpes, ophthalmic herpes simplex, herpes virus infection, oral herpes
**** Includes anaphylactic reaction, anaphylactic shock, angioedema, dermatitis exfoliative generalized, drug hypersensitivity, eyelid oedema, face oedema, hypersensitivity, periorbital swelling, pharyngeal swelling, swelling face, toxic skin eruption, type hypersensitivity, urticaria
***** Includes abdominal pain and abdominal pain upper ****** Includes herpes zoster and varicella
Other adverse reactions reported in less than 1% of patients in the RINVOQ 15 mg and/or 30 mg group and at a higher rate than in the placebo group through Week 16 included anemia, oral candidiasis, pneumonia, and the adverse event of retinal detachment.
The safety profile of RINVOQ through Week 52 was generally consistent with the safety profile observed at Week 16.
Overall, the safety profile observed in patients with AD treated with RINVOQ was similar to the safety profile in patients with RA. Other specific adverse reactions that were reported in patients with AD included eczema herpeticum/Kaposi’s varicelliform eruption.
Eczema Herpeticum/Kaposi’s Varicelliform Eruption
Placebo-controlled Period (16 weeks): Eczema herpeticum was reported in 4 patients (1.6 per 100 patient-years) treated with placebo, 6 patients (2.2 per 100 patient-years) treated with RINVOQ 15 mg and 7 patients (2.6 per 100 patient-years) treated with RINVOQ 30 mg.
12-Month Exposure (Weeks 0 to 52): Eczema herpeticum was reported in 18 patients (1.6 per 100 patient-years) treated with RINVOQ 15 mg and 17 patients (1.5 per 100 patient-years) treated with RINVOQ 30 mg.
Adverse Reactions in Patients with Ulcerative Colitis
RINVOQ was studied up to 8 weeks in patients with moderately to severely active ulcerative colitis in two randomized, double-blind, placebo-controlled induction studies (UC-1, UC-2) and a randomized, double-blind, placebo controlled, dose-finding study (UC-4; NCT02819635). Long term safety up to 52-weeks was evaluated in patients who responded to induction therapy in a randomized, double-blind, placebo-controlled maintenance study (UC-3) and a long-term extension study.
In the two induction studies (UC-1, UC-2) and a dose finding study (UC-4), 1097 patients were enrolled of whom 719 patients received RINVOQ 45 mg once daily.
In the maintenance study (UC-3), 746 patients were enrolled of whom 250 patients received RINVOQ 15 mg once daily and 251 patients received RINVOQ 30 mg once daily.
Adverse reactions reported in ≥2% of patients in any treatment arm in the induction and maintenance studies are shown in Tables 3 and 4, respectively.
Table 3. Adverse Reactions Reported in ≥2% of Patients with Ulcerative Colitis Treated with RINVOQ 45 mg in Placebo-Controlled Induction Studies (UC-1, UC-2 and UC-4)
Adverse Reaction Placebo RINVOQ 45 mg Once Daily N= 378 (%) N = 719 (%)
Upper respiratory tract infection* 7 9 Acne* 1 6 Increased blood creatine phosphokinase 1 5 Neutropenia* <1 5 Rash* 1 4
Elevated liver enzymes** 2 3 Lymphopenia* 1 3 Folliculitis 1 2 Herpes simplex* <1 2 * Composed of several similar terms
** Elevated liver enzymes composed of elevated ALT, AST, GGT, ALP, liver transaminases, hepatic enzymes, bilirubin, drug-induced liver injury and cholestasis.
Other adverse reactions reported in less than 2% of patients in the RINVOQ 45 mg group and at a higher rate than in the placebo group through Week 8 included herpes zoster and pneumonia.
Table 4. Adverse Reactions Reported in ≥2% of Patients with Ulcerative Colitis Treated with RINVOQ 15 mg or 30 mg in the Placebo-Controlled Maintenance Study (UC-3)1
Adverse Reaction Placebo RINVOQ 15 mg Once Daily
Upper respiratory tract infection* 18
Increased blood creatine phosphokinase 2
Neutropenia* 2
Elevated liver enzymes** 1
Rash* 4
Herpes zoster 0
Folliculitis 2 2
Hypercholesterolemia* 1 2
Influenza 1 3
Herpes simplex* 1 2 3 Lymphopenia* 2 3 2 Hyperlipidemia* 0 2 2
1 Patients who were responders to 8 weeks induction therapy with RINVOQ
*
**
The
Specific Adverse Reactions Serious Infections
Induction Studies: In UC-1, UC-2, and UC-4, serious infections were reported in 5 patients (8.4 per 100 patient-years) treated with placebo and 9 patients (8.4 per 100 patient-years) treated with RINVOQ 45 mg through 8 weeks.
Placebo-controlled Maintenance Study: In UC-3, serious infections were reported in 8 patients (6.3 per 100 patient-years) treated with placebo, 8 patients (4.5 per 100 patient-years) treated with RINVOQ 15 mg, and 6 patients (3.1 per 100 patient-years) treated with RINVOQ 30 mg through 52 weeks.
Laboratory Abnormalities
Hepatic Transaminase Elevations
In studies UC-1, UC-2, and UC-4, elevations of ALT to ≥ 3 x ULN in at least one measurement were observed in 1.5% of patients treated with RINVOQ 45 mg, and 0% of patients treated with placebo for 8 weeks. AST elevations to ≥ 3 x ULN occurred in 1.5% of patients treated with RINVOQ 45 mg, and 0.3% of patients treated with placebo. Elevations of ALT to ≥ 5 x ULN occurred in 0.4% of patients treated with RINVOQ 45 mg and 0% of patients treated with placebo.
In UC-3, elevations of ALT to ≥ 3 x ULN in at least one measurement were observed in 4% of patients treated with RINVOQ 30 mg, 2% of patients treated with RINVOQ 15 mg, and 0.8% of patients treated with placebo for 52 weeks. Elevations of AST to ≥ 3 x ULN in at least one measurement were observed in 2% of patients treated with RINVOQ 30 mg, 1.6% of patients treated with RINVOQ 15 mg and 0.4% of patients treated with placebo.
Elevations of ALT to ≥ 5 x ULN were observed in 0.8% of patients treated with 30 mg, 0.4% of patients treated with 15 mg, and 0.4% of patients treated with placebo.
Overall, laboratory abnormalities observed in patients with ulcerative colitis treated with RINVOQ were similar to those described in patients with RA.
Adverse Reactions in Patients with Ankylosing Spondylitis
A total of 596 patients with ankylosing spondylitis were treated with RINVOQ 15 mg in the two clinical trials representing 577.3 patient-years of exposure, of whom 228 were exposed to RINVOQ 15 mg for at least one year.
Overall, the safety profile observed in patients with active ankylosing spondylitis treated with RINVOQ 15 mg was consistent with the safety profile observed in patients with rheumatoid arthritis and psoriatic arthritis.
During the 14-week placebo-controlled period in Trial AS-I, the frequency of headache was 5.4% with RINVOQ 15 mg and 2.1% with placebo. During the 14-week placebo-controlled period in Trial AS-II, the frequency of headache was 3.3% with RINVOQ 15 mg and 1.4% with placebo.
DRUG INTERACTIONS
Strong CYP3A4 Inhibitors
Upadacitinib exposure is increased when RINVOQ is co-administered with a strong CYP3A4 inhibitor (such as ketoconazole and clarithromycin), which may increase the risk of RINVOQ adverse reactions. Monitor patients closely for adverse reactions when co-administering RINVOQ 15 mg once daily with strong CYP3A4 inhibitors.
For patients with atopic dermatitis, coadministration of RINVOQ 30 mg once daily with strong CYP3A4 inhibitors is not recommended.
For patients with ulcerative colitis taking strong CYP3A4 inhibitors, reduce the RINVOQ induction dosage to 30 mg once daily. The recommended maintenance dosage is 15 mg once daily.
Strong CYP3A4 Inducers
Upadacitinib exposure is decreased when RINVOQ is co-administered with strong CYP3A4 inducers (such as rifampin), which may lead to reduced therapeutic effect of RINVOQ. Coadministration of RINVOQ with strong CYP3A4 inducers is not recommended.
USE IN SPECIFIC POPULATIONS
Pregnancy Risk Summary
Available data from the pharmacovigilance safety database and postmarketing case reports on use of RINVOQ in pregnant women are not sufficient to evaluate a drug-associated risk for major birth defects or miscarriage. Based on animal studies, RINVOQ has the potential to adversely affect a developing fetus. Advise patients of reproductive potential and pregnant patients of the potential risk to the fetus.
In animal embryo-fetal development studies, oral upadacitinib administration to pregnant rats and rabbits at exposures equal to or greater than approximately 1.6 and 15 times the 15 mg dose, 0.8 and 7.6 times the 30 mg dose, and 0.6 and 5.6 times the maximum recommended human dose (MRHD) of 45 mg (on an AUC basis) resulted in dose-related increases in skeletal malformations (rats only), an increased incidence of cardiovascular malformations (rabbits only), increased post-implantation loss (rabbits only), and decreased fetal body weights in both rats and rabbits. No developmental toxicity was observed in pregnant rats and rabbits treated with oral upadacitinib during organogenesis at exposures approximately 0.29 and 2.2 times the 15 mg dose, 0.15 times and 1.1 times the 30 mg dose, and at 0.11 and 0.82 times the MHRD (on an AUC basis).
In a pre- and post-natal development study in pregnant female rats, oral upadacitinib administration at exposures approximately 3 times the 15 mg dose, 1.4 times the 30 mg dose, and the same as the MRHD (on an AUC basis) resulted in no maternal or developmental toxicity (see Data)
The background risks of major birth defects and miscarriage for the indicated populations are unknown. All pregnancies have a background risk of birth defect, loss, or other adverse outcomes. In the U.S. general population, the estimated background risk of major birth defects and miscarriages are 2-4% and 15-20%, respectively.
Report pregnancies to the AbbVie Inc.’s Adverse Event reporting line at 1-888-633-9110, or FDA at 1-800-FDA-1088 or www.fda.gov/medwatch.
Clinical Considerations
Disease-Associated Maternal and/or Embryo/Fetal Risk
Published data suggest that increased disease activity is associated with the risk of developing adverse pregnancy outcomes in women with rheumatoid arthritis or ulcerative colitis. Adverse pregnancy outcomes include preterm delivery (before 37 weeks of gestation), low birth weight (less than 2500 g) infants, and small for gestational age at birth.
15 mg dose, 0.9 times the 30 mg dose, and 0.6 times the MRHD (on an AUC basis at maternal oral doses of 5 mg/kg/day and higher). Additional skeletal malformations (bent forelimbs/hindlimbs and rib/vertebral defects) and decreased fetal body weights were observed in the absence of maternal toxicity at an exposure approximately 84 times the 15 mg dose, 43 times the 30 mg dose, and 31 times the MRHD (on an AUC basis at a maternal oral dose of 75 mg/kg/day).
In a second oral embryo-fetal development study, pregnant rats received upadacitinib at doses of 1.5 and 4 mg/kg/day during the period of organogenesis from gestation day 6 to 17. Upadacitinib was teratogenic (skeletal malformations that included bent humerus and scapula) at exposures approximately 1.6 times the 15 mg dose, 0.8 times the 30 mg dose, and 0.6 times the MRHD (on an AUC basis at maternal oral doses of 4 mg/kg/day). No developmental toxicity was observed in rats at an exposure approximately 0.29 times the 15 mg dose, 0.15 times the 30 mg dose, and 0.11 times the MRHD (on an AUC basis at a maternal oral dose of 1.5 mg/kg/day).
In an oral embryo-fetal developmental study, pregnant rabbits received upadacitinib at doses of 2.5, 10, and 25 mg/kg/day during the period of organogenesis from gestation day 7 to 19. Embryolethality, decreased fetal body weights, and cardiovascular malformations were observed in the presence of maternal toxicity at an exposure approximately 15 times the 15 mg dose, 7.6 times the 30 mg dose, and 5.6 times the MRHD (on an AUC basis at a maternal oral dose of 25 mg/kg/day). Embryolethality consisted of increased post-implantation loss that was due to elevated incidences of both total and early resorptions. No developmental toxicity was observed in rabbits at an exposure approximately 2.2 times the 15 mg dose, 1.1 times the 30 mg dose, and 0.82 times the MRHD (on an AUC basis at a maternal oral dose of 10 mg/kg/day).
In an oral pre- and post-natal development study, pregnant female rats received upadacitinib at doses of 2.5, 5, and 10 mg/kg/day from gestation day 6 through lactation day 20. No maternal or developmental toxicity was observed in either mothers or offspring, respectively, at an exposure approximately 3 times the 15 mg dose, 1.4 times the 30 mg dose, and at approximately the same exposure as the MRHD (on an AUC basis at a maternal oral dose of 10 mg/kg/day).
Lactation Risk Summary
There are no data on the presence of upadacitinib in human milk, the effects on the breastfed infant, or the effects on milk production. Available pharmacodynamic/toxicological data in animals have shown excretion of upadacitinib in milk (see Data). When a drug is present in animal milk, it is likely that the drug will be present in human milk. Because of the potential for serious adverse reactions in the breastfed infant, advise patients that breastfeeding is not recommended during treatment with RINVOQ, and for 6 days (approximately 10 half-lives) after the last dose.
Data
A single oral dose of 10 mg/kg radiolabeled upadacitinib was administered to lactating female Sprague-Dawley rats on post-partum days 7-8. Drug exposure was approximately 30-fold greater in milk than in maternal plasma based on AUC0-t values. Approximately 97% of drug-related material in milk was parent drug.
Females and Males of Reproductive Potential Pregnancy Testing
Verify the pregnancy status of females of reproductive potential prior to starting treatment with RINVOQ [see Use in Specific Populations]
Contraception Females
Based on animal studies, upadacitinib may cause embryo-fetal harm when administered to pregnant women [see Use in Specific Populations]. Advise female patients of reproductive potential to use effective contraception during treatment with RINVOQ and for 4 weeks after the final dose.
Pediatric Use
Juvenile Idiopathic Arthritis, Psoriatic Arthritis, and Ankylosing Spondylitis
The safety and effectiveness of RINVOQ in pediatric patients with juvenile idiopathic arthritis, psoriatic arthritis, and ankylosing spondylitis have not been established.
Atopic Dermatitis
The safety and effectiveness of RINVOQ in pediatric patients 12 years of age and older weighing at least 40 kg with atopic dermatitis have been established. A total of 344 pediatric patients aged 12 to 17 years with moderate to severe atopic dermatitis were randomized across three trials (AD-1, AD-2 and AD-3) to receive either RINVOQ 15 mg (N=114) or 30 mg (N=114) or matching placebo (N=116) in monotherapy or combination with topical corticosteroids. Efficacy was consistent between the pediatric patients and adults. The adverse reaction profile in the pediatric patients was similar to the adults [see Adverse Reactions].
The safety and effectiveness of RINVOQ in pediatric patients less than 12 years of age with atopic dermatitis have not been established.
Ulcerative Colitis
The safety and effectiveness of RINVOQ in pediatric patients with ulcerative colitis have not been established.
Geriatric Use
Rheumatoid Arthritis and Psoriatic Arthritis
Of the 4381 patients treated in the five clinical trials, a total of 906 rheumatoid arthritis patients were 65 years of age or older, including 146 patients 75 years and older. Of the 1827 patients treated in the two psoriatic arthritis Phase 3 clinical trials, a total of 274 patients were 65 years of age or older, including 34 patients 75 years and older. No differences in effectiveness were observed between these patients and younger patients; however, there was a higher rate of overall adverse events, including serious infections, in patients 65 years of age and older.
Atopic Dermatitis
profile of RINVOQ
Overall, the safety profile observed in patients
with RINVOQ
to the
in patients
Data Animal Data
In an oral embryo-fetal development study, pregnant rats received upadacitinib at doses of 5, 25, and 75 mg/kg/day during the period of organogenesis from gestation day 6 to 17. Upadacitinib was teratogenic (skeletal malformations that consisted of misshapen humerus and bent scapula) at exposures equal to or greater than approximately 1.7 times the
Of the 2583 patients treated in the three Phase 3 clinical trials, a total of 120 patients with atopic dermatitis were 65 years of age or older, including 6 patients 75 years of age. No differences in effectiveness were observed between these patients and younger patients; however, there was a higher rate of serious infections and malignancies in those patients 65 years of age or older in the 30 mg dosing group in the long-term trials.
Ulcerative Colitis
Of the 1097 patients treated in the controlled clinical trials, a total of 95 patients with ulcerative colitis were 65 years and older. Clinical studies of RINVOQ did not include sufficient numbers of patients 65 years of age and older with ulcerative colitis to determine whether they respond differently from younger adult patients.
RINVOQ 30 mg Once Daily n = 245 (%) n = 250 (%) n = 251 (%)
16 20
6 8
3 6
6 4
5 5
4 4
4
4
3
45 mg once daily
Composed of several similar terms
Elevated liver enzymes composed of elevated ALT, AST, GGT, ALP, liver transaminases, hepatic enzymes, bilirubin, drug-induced liver injury, and cholestasis.
safety
in the long-term extension study was similar to the safety profile observed in the placebo-controlled induction and maintenance periods.
with ulcerative colitis treated
was generally similar
safety profile
with RA and AD.
Renal Impairment
For patients with rheumatoid arthritis, psoriatic arthritis, and ankylosing spondylitis, no dosage adjustment is needed in patients with mild (eGFR 60 to < 90 mL/min/1.73 m2), moderate (eGFR 30 to < 60 mL/min/1.73 m2), or severe renal impairment (eGFR 15 to < 30 mL/min/1.73 m2).
For patients with atopic dermatitis, the maximum recommended dosage is 15 mg once daily for patients with severe renal impairment. No dosage adjustment is needed in patients with mild or moderate renal impairment.
For patients with ulcerative colitis, the recommended dosage for severe renal impairment is 30 mg once daily for induction and 15 mg once daily for maintenance. No dosage adjustment is needed in patients with mild or moderate renal impairment.
RINVOQ has not been studied in patients with end stage renal disease (eGFR <15 mL/min/1.73m2). Use in patients with atopic dermatitis or ulcerative colitis with end stage renal disease is not recommended.
Hepatic Impairment
The use of RINVOQ has not been studied in patients with severe hepatic impairment (Child Pugh C), and therefore not recommended for use in patients with rheumatoid arthritis, psoriatic arthritis, atopic dermatitis, ulcerative colitis, or ankylosing spondylitis.
For patients with rheumatoid arthritis, psoriatic arthritis, atopic dermatitis, and ankylosing spondylitis, no dosage adjustment is needed in patients with mild (Child Pugh A) or moderate (Child Pugh B) hepatic impairment.
For patients with ulcerative colitis, the recommended dosage for mild to moderate hepatic impairment is 30 mg once daily for induction and 15 mg once daily for maintenance
PATIENT COUNSELING INFORMATION
Advise the patient to read the FDA-approved patient labeling (Medication Guide).
Serious Infections
Inform patients that they may be more likely to develop infections when taking RINVOQ. Instruct patients to contact their healthcare provider immediately during treatment if they develop any signs or symptoms of an infection [see Warnings and Precautions]
Advise patients that the risk of herpes zoster is increased in patients taking RINVOQ and in some cases can be serious [see Warnings and Precautions]
Malignancies
Inform patients that RINVOQ may increase their risk of certain cancers and that periodic skin examinations should be performed while using RINVOQ.
Advise patients that exposure to sunlight and UV light should be limited by wearing protective clothing and using a broad-spectrum sunscreen [see Warnings and Precautions]
Major Adverse Cardiovascular Events
Inform patients that RINVOQ may increase their risk of major adverse cardiovascular events (MACE) including myocardial infarction, stroke,
and cardiovascular death. Instruct all patients, especially current or past smokers or patients with other cardiovascular risk factors, to be alert for the development of signs and symptoms of cardiovascular events [see Warnings and Precautions]
Thrombosis
Inform patients that events of deep venous thrombosis and pulmonary embolism have been reported in clinical trials with RINVOQ. Instruct patients to seek immediate medical attention if they develop any signs or symptoms of a DVT or PE [see Warnings and Precautions]
Hypersensitivity Reactions
Advise patients to discontinue RINVOQ and seek immediate medical attention if they develop any signs and symptoms of allergic reactions [see Warnings and Precautions].
Gastrointestinal Perforations
Inform patients that gastrointestinal perforations have been reported in clinical trials with RINVOQ and that risk factors include the use of NSAIDS or history of diverticulitis. Instruct patients to seek medical care immediately if they experience new onset of abdominal pain, fever, chills, nausea, or vomiting [see Warnings and Precautions].
Retinal Detachment
Inform patients that retinal detachment has been reported in clinical trials with RINVOQ. Advise patients to immediately inform their healthcare provider if they develop any sudden changes in vision while receiving RINVOQ [see Adverse Reactions]
Laboratory Abnormalities
Inform patients that RINVOQ may affect certain lab tests, and that blood tests are required before and during RINVOQ treatment [see Warnings and Precautions]
Vaccinations
Advise patients to avoid use of live vaccines with RINVOQ. Instruct patients to inform their healthcare practitioner that they are taking RINVOQ prior to a potential vaccination [see Warnings and Precautions]
Embryo-Fetal Toxicity
Advise pregnant women and females of reproductive potential that exposure to RINVOQ during pregnancy may result in fetal harm. Advise females to inform their healthcare provider of a known or suspected pregnancy [see Warnings and Precautions and Use in Specific Populations]
Advise females of reproductive potential that effective contraception should be used during treatment and for 4 weeks following the final dose of upadacitinib [see Use in Specific Populations]
Advise females patients who are exposed to RINVOQ during pregnancy to contact AbbVie Inc. at 1-800-633-9110 or FDA at 1-800-FDA-1088 or www.fda.gov/medwatch.
Lactation
Advise women not to breastfeed during treatment with RINVOQ and for 6 days after the last dose [see Use in Specific Populations] Administration
Advise patients not to chew, crush, or split RINVOQ tablets.
Manufactured by: AbbVie Inc., North Chicago, IL 60064, USA
RINVOQ® is a registered trademark of AbbVie Biotechnology Ltd. ©2019-2022 AbbVie Inc.
Ref: 20071734 Revised: April 2022 LAB-7082 MASTER
US-RNQR-220149
 POR MARCIA CRUZ-CORREA, MD, PHD, AGAF, FASGE Investigadora PanOncology Trials Catedrática Medicina & Bioquímica Universidad de Puerto Rico, Recinto de Ciencias Médicas
POR MARCIA CRUZ-CORREA, MD, PHD, AGAF, FASGE Investigadora PanOncology Trials Catedrática Medicina & Bioquímica Universidad de Puerto Rico, Recinto de Ciencias Médicas

¿Cuán común es el cáncer de pulmón en Puerto Rico?
Elcáncer de pulmón continúa siendo uno de los más comunes tanto en hombres como en mujeres en la Isla. Según estadísticas del Registro Central de Cáncer de Puerto Rico, durante el periodo de 2014-2018, este fue la tercera causa de muerte por cáncer en el País, con cerca de 550 fallecimientos por año y es dos veces más común en hombres que en mujeres (95% CI 1.8-2.1).
Lamentablemente, la sobrevida a cinco años, en los pacientes diagnosticados con cáncer de pulmón es de aproximadamente 20%. Estadios tempranos están asociados a mejor pronóstico, permite intervenciones quirúrgicas y el tratamiento sistémico con quimioterapias, inmunoterapias y terapias biológicas dirigidas a los marcadores moleculares.
La incidencia y mortalidad asociada al cáncer de pulmón aumenta a partir de los 40 años tanto en hombres como en mujeres (Figura 1). La incidencia de cáncer de pulmón a través de los diversos municipios de Puerto Rico, muestra un patrón variable con las regiones del noreste y sureste con la mayor incidencia (Figura 2).
¿CUÁLES SON LOS FACTORES DE RIESGO Y SÍNTOMAS ASOCIADOS AL CÁNCER DE PULMÓN?
El tabaquismo es la causa principal del desarrollo de cáncer de pulmón y se le atribuye cerca del 40% de todos los cánceres pulmonares.
Otros factores de riesgo para el cáncer de pulmón incluyen: la exposición ambiental al tabaco — fumadores pasivos—, exposición a radón, asbesto, contaminación ambiental, tuberculosis e historial familiar de cáncer de pulmón.

La mayoría de los pacientes con cáncer de pulmón no presentan síntomas hasta las etapas avanzadas. Algunos de estos síntomas pueden incluir tos, esputo con sangre, dolor de pecho, ronquera, pérdida de apetito, dificultad respiratoria, pérdida de peso y cansancio.
¿CUÁLES SON LOS TIPOS DE CÁNCER DE PULMÓN?
El cáncer de pulmón se clasifica histológicamente basado en el tipo de célula tumoral en diversas categorías: escamoso, no-escamoso, de célula pequeña y adenocarcinoma.
La terapia oncológica sistémica incluye la quimioterapia, la inmunoterapia (i.e. antiPDL1), y la terapia de anticuerpos dirigida a los biomarcadores tumorales presentes en el tumor. Entre los principales biomarcadores que se evalúan en el cáncer de pulmón están el Epitermal Growth Factor Receptor (EGFR), al igual que las mutaciones o sobreexpresiones en genes como el KRAS, ROS, ALK, NTRK y RET, entre otros.
La presencia de biomarcadores en el tumor permite guiar la terapia oncológica y están mejorando la sobrevida significativamente en los pacientes con cáncer de pulmón.
31
Figura 1. Tazas de incidencia y mortalidad ajustadas por edad para cáncer de pulmón y bronquios presentadas por género: Puerto Rico, 2014-2018.
Actualmente ya tenemos disponibles múltiples protocolos de tratamiento en los que se evalúan las terapias biológicas que están en etapa de investigación clínica —‘clínical trials’— para pacientes con cáncer de pulmón avanzado, evaluando combinaciones de agentes biológicos e inmunoterapias noveles.
¿CUÁLES SON LOS MÉTODOS DE DETECCIÓN TEMPRANA PARA EL CÁNCER DE PULMÓN?
Existen varios grupos profesionales que han publicado recomendaciones para la detección temprana del cáncer de pulmón, entre estos la Sociedad Americana Contra el Cáncer y el Grupo de Trabajo de Servicios Preventivos de los Estados Unidos (USPSTF). Recientemente, las guías del USPSTF incluyeron como prueba de detección temprana la tomografía computarizada de baja dosis (Low-doce CT Scan; LDCT) en personas con un riesgo elevado a desarrollar cáncer de pulmón debido a un historial de tabaquismo crónico.
Las guías actuales recomiendan el LDCT para personas: (i) entre los 50 a los 80 años, (ii) que son fumadores activos o dejaron de fumar dentro de los últimos 15 años, y (iii) que tengan una exposición al tabaco de 20-paquete-año (i.e. fumar por 10 años 2 cajas de cigarrillos al día o fumar por 20 años 1 cajetilla al día). La recomendación incluye además un programa de cesación de fumar y evaluación en una clínica con experiencia en prevención, detección y manejo del cáncer de pulmón.
Las guías actuales recomiendan la LDCT anual para identificar hallazgos que pudieran representar el cáncer de pulmón en etapas tempranas. Aquellos con hallazgos sospechosos en el LDCT requieren evaluaciones adicionales con biopsias para obtener tejido y descartar el cáncer. Para aquellos cuyos LDCT estén negativos —sin hallazgos anormales— se recomienda una prueba de vigilancia anual con LDCT.
Desde la recomendación original de la guía USPSTF, en 2013, el cumplimiento observado con esta recomendación continua muy bajo, con una taza de vigilancia muy baja donde solo un 5% de las personas con alto riesgo de cáncer de pulmón se han realizado el estudio de imagen (LDCT).
Es importante destacar que el LDCT podría demostrar hallazgos radiológicos benignos pero que requieren evaluación con pruebas adicionales, incluyendo biopsias, broncoscopias transbronquiales o cirugía. Por lo tanto, el desarrollo de tecnologías no invasivas con una alta capacidad diagnostica son necesarios.
DESARROLLO DE PRUEBAS MOLECULARES EN SANGRE PARA LA DETECCIÓN DEL CÁNCER DE PULMÓN
Se necesitan herramientas adicionales para aumentar los beneficios, la adherencia con las pruebas de prevención y métodos no-invasivos que utilicen la biología de la carcinogénesis para aumentar la detección del cáncer de pulmón. El desarrollo de metodología basada en sangre utilizando marcadores del ADN del plasma y proteínas está en desarrollo. Actualmente, nuestro equipo en PanOncology Trials participa en un estudio nacional donde se estarán evaluando 15 mil personas con historial activo o pasado de tabaquismo, para evaluar una tecnología novel para detectar ADN en plasma.
Esta prueba molecular en sangre examina cambios en el genoma circulante para identificar cambios moleculares y la detección temprana del cáncer de pulmón, aun antes de que las pruebas radiológicas lo muestren.
El uso de tecnologías moleculares que analizan ADN liberado por la división de células malignas puede tener un impacto positivo en la detección temprana del cáncer de pulmón, mayor aceptación por la población y así aumentar el diagnóstico temprano del cáncer de pulmón y la sobrevida.
En Puerto Rico, estaremos evaluando personas entre los 50-80 años con historial activo o pasado de tabaquismo, para apoyar el desarrollo de una prueba de detección de cáncer del pulmón. La integración de la biología molecular y la tecnología de precisión oncológica augura un panorama muy alentador para nuestra población a riesgo de cáncer de pulmón.
REFERENCIA PARA LOS DATOS DEL REGISTRO CENTRAL DE CÁNCER DE PUERTO RICO
Figura 2. Tasas de incidencia ajustada por edad para el cáncer de pulmón y bronquios por muni cipio en Puerto Rico, 2014-2018.
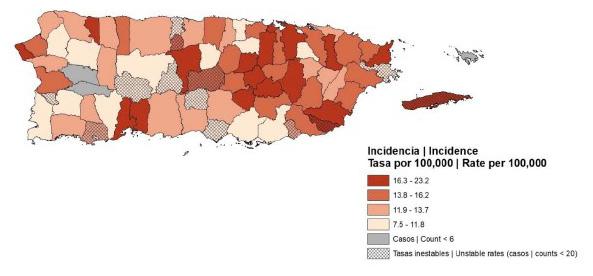
Torres-Cintrón CR, AlvaradoOrtiz M, Román Ruiz Y et al. Cáncer in Puerto Rico, 2014-2018. Puerto Rico Cáncer Registry. San Juan, PR.
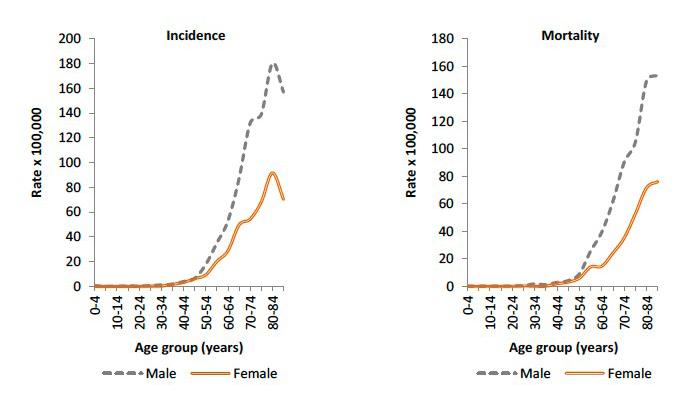
32 Bienestartotal | Professional Edition


 Actor portrayals
Actor portrayals
‡
Safety Assessment in Infants and Children Receiving Catch-Up Vaccination
The safety of VAXNEUVANCE in healthy infants and children 7 months through 17 years of age was assessed in a double-blind, multi-regional, clinical study (Study 12, NCT03885934). Participants were randomized to receive 1 to 3 doses of VAXNEUVANCE (N=303) or Prevnar 13 (N=303), depending on age at enrollment. All infants and children less than 2 years of age were pneumococcal vaccine-naïve. Among 352 children 2 through 17 years of age, 42.9% had a history of previous vaccination with a lower valency pneumococcal conjugate vaccine. Among participants 7 through 11 months of age, the median age was 8.0 months, 48.4% were female, 82.8% were Asian, 17.2% were White and none were of Hispanic or Latino ethnicity. Among participants 12 through 23 months of age, the median age was 18.0 months, 54.0% were female, 83.3% were Asian, 16.7% were White and 0.8% were of Hispanic or Latino ethnicity. Among participants 2 through 17 years of age, the median age was 4.0 years, 47.7% were female, 66.8% were White, 33.0% were Asian, and none were of Hispanic or Latino ethnicity. The safety assessment was consistent with that used in Studies 8-11, as described above with the exception that in children 3 years of age and older, oral or axillary temperature measurements were obtained. The duration of the safety follow-up period for serious adverse events following the last dose of vaccine within each age cohort was 6 months.
5:
Local Reactions† Pain‡ Any Moderate Severe
Swelling Any 2.6-7.6 cm >7.6 cm
Erythema Any 2.6-7.6 cm >7.6 cm
Induration Any 2.6-7.6 cm >7.6 cm
Systemic Reactions†‡ Myalgia§ Any Moderate Severe
Fatigue§ Any Moderate Severe
Solicited Adverse Reactions in Children Receiving Catch-Up Vaccination
Among participants 7 through 11 months of age who received 3 doses of VAXNEUVANCE (N=64) or Prevnar 13 (N=64), the percentage of participants reporting solicited local and systemic adverse reactions that occurred within 14 days following any dose (VAXNEUVANCE participants vs. Prevnar 13 participants) were: fever ≥38.0°C (21.9% vs. 14.1%), irritability (32.8% vs. 43.8%), injection-site erythema (28.1% vs. 34.4%), somnolence (21.9% vs. 15.6%), injection-site swelling (18.8% vs. 15.6%), injection-site pain (18.8% vs. 7.8%), injection-site induration (17.2% vs. 14.1%), decreased appetite (15.6% vs. 18.8%) and urticaria (1.6% vs. 4.7%).
Among participants 12 through 23 months of age who received 2 doses of VAXNEUVANCE (N=62) or Prevnar 13 (N=64), the percentage of participants reporting solicited local and systemic adverse reactions that occurred within 14 days following any dose (VAXNEUVANCE participants vs. Prevnar 13 participants) were: fever ≥38.0°C (11.3% vs. 9.4%), irritability (35.5% vs. 21.9%), injection-site pain (33.9% vs. 23.4%), somnolence (24.2% vs. 17.2%), decreased appetite (22.6% vs. 18.8%), injection-site erythema (21.0% vs. 21.9%), injection-site swelling (14.5% vs. 12.5%) and injection-site induration (8.1% vs. 9.4%).
In children 2 through 17 years of age, the percentage of participants with solicited adverse reactions that occurred within 14 days following administration of a single dose of VAXNEUVANCE or Prevnar 13 is shown in Table 5.
of Participants with Solicited Local and Systemic Adverse Reactions in Children and Adolescents 2 Years Through 17 Years of Age Using a Catch Up Vaccination Schedule (Study 12)*
VAXNEUVANCE (%) N=177 Prevnar 13 (%) N=175
27.7 4.5
20.9 10.2 0.0
19.2 6.2 1.1
6.8 3.4 0.0
23.7 14.7 0.6
15.8 6.2 2.8
22.9 1.7
24.0 12.0 0.6
21.1 7.4 0.6
14.9 5.7 0.0
16.6 6.9 0.6
17.1 5.7 0.6
Systemic Reactions†‡ (continued)
Headache§ Any Moderate Severe
Somnolence§ Any Moderate Severe
Irritability§ Any Moderate Severe
Decreased appetite§ Any Moderate Severe
Urticaria§ Any Moderate Severe
Fever¶# ≥38.0°C ≥38.0°C to <39.0°C ≥39.0°C to <40.0°C ≥40.0°C
VAXNEUVANCE (%) N=177 Prevnar 13 (%) N=175
11.9 6.2 0.6
2.8 1.7 0.0
2.8 0.6 0.0
2.3 0.6 0.0
1.1 0.0 0.0
4.0 2.8 1.1 0.0
*Study 12 (NCT03885934) was a randomized, double-blind, active comparator-controlled clinical study. Safety was monitored using a Vaccination Report Card (VRC) for up to 14 days postvaccination † Day 14 postvaccination following each dose.
urticaria were solicited from Day 1 through Day 14 following va § remely distressed or unable to do usual activities. ¶Solicited on Day 1 through Day 7 postvaccination following each dose.
#
N=Number of participants vaccinated.
Clinical Trials Experience in Adults
Safety Assessment in Clinical Studies
The safety of VAXNEUVANCE was assessed in 7 randomized, double-blind clinical
18 years of age and older received VAXNEUVANCE and 1,808 adults received Prevnar 13. In Studies 1-3 (NCT03950622, NCT03950856, and NCT03480763), a total of 3,032 adults 50 years of age and older with no history of pneumococcal vaccination received VAXNEUVANCE and 1,154 participants received Prevnar 13. In Study 4 (NCT03547167), adults 18 through 49 years of age with no history of pneumococcal vaccination, including individuals with increased risk of developing pneumococcal disease, received VAXNEUVANCE (N=1,134) or Prevnar 13 (N=378), followed by PNEUMOVAX 23 six months later. In Study 5 (NCT02573181), adults 65 years of age and older previously vaccinated with PNEUMOVAX 23 (at least 1 year prior to study entry) received VAXNEUVANCE (N=127) or Prevnar 13 (N=126). In Study 6 (NCT03615482), adults 50 years of age and older received VAXNEUVANCE Quadrivalent; QIV) (Group 1, N=600) or nonconcomitantly 30 days after QIV (Group 2, N=585). In this study population, 20.9% of individuals had a history of prior vaccination with PNEUMOVAX 23. In Study 7 (NCT03480802), HIV-infected adults 18 years of age and older received VAXNEUVANCE (N=152) or Prevnar 13 (N=150), followed by PNEUMOVAX 23 two months later.
13.7 8.6 0.6
2.9 1.1 0.6
4.0 0.6 0.0
2.9 1.7 0.0
1.1 0.0 0.0
1.7 1.7 0.0 0.0
The clinical studies included adults with stable underlying medical conditions (e.g., diabetes mellitus, renal disorders, chronic heart disease, chronic liver disease, chronic lung disease including asthma) and/or behavioral risk factors (e.g., smoking, increased alcohol use) that are known to increase the risk of pneumococcal disease. Overall, the mean age of the participants was 58 years and 54.6% were female. The racial distribution was as follows: 72.3% were White, 9.9% were Asian, 8.1% were American Indian or Alaska Native, 7.4% were Black or African American, and 18.1% were of Hispanic or Latino ethnicity.
In all studies, safety was monitored using a Vaccination Report Card (VRC) for up to 14 days postvaccination. Study investigators reviewed the VRC with the participants
by the study investigators. Oral body temperature and injection-site adverse reactions were solicited on Day 1 through Day 5 postvaccination. Systemic adverse reactions were solicited on Day 1 through Day 14 postvaccination. Unsolicited adverse events were reported on Day 1 through Day 14 postvaccination. The duration of the safety follow-up period for serious adverse events postvaccination with VAXNEUVANCE was 1 month in Study 5; 2 months in Study 7; 6 months in Studies 1, 2, 4 and 6; and 12 months in Study 3.
Solicited Adverse Reactions
The percentage of participants with solicited adverse reactions that occurred within 5 or 14 days following administration of VAXNEUVANCE or Prevnar 13 in 3 studies are shown in Tables 6-8. The majority of solicited adverse reactions lasted ≤3 days.
Table
Percentage
54.8
56.6
Brief Summary of the Prescribing Information for VAXNEUVANCE™ (Pneumococcal 15-valent Conjugate Vaccine) (continued)
Estudio revela alta prevalencia de diabetes en la Isla
REDACCIÓN BTP
Laprevalencia de diabetes en Puerto Rico podría ser mucho mayor a lo estimado y registrado por las entidades gubernamentales, de acuerdo con un nuevo estudio transversal realizado por la empresa de tecnología de salud Abartys Health y la Asociación Puertorriqueña de la Diabetes. El estudio mide también por primera vez la prevalencia de la prediabetes en la población de la Isla.
El estudio reveló que para el 2021, Puerto Rico tuvo una prevalencia estimada de diabetes de más del 19.3% de los adultos, de 20 años o más. Asimismo, la prevalencia estimada hasta el mes de septiembre de este año ya alcanzó el 20%. Ambas cifras superan ampliamente la prevalencia de la condición en los Estados Unidos, que se registra en 14.7%, según datos de los Centros para el Control y Prevención de Enfermedades (CDC, en inglés).
“Es la primera vez que la prevalencia de la diabetes en Puerto Rico ha sido analizada en esta escala, permitiéndonos ver tendencias basadas en datos del mundo real. Las cifras oficiales actuales están basadas en información reportada por los propios individuos y recopilada mediante encuestas telefónicas, por lo que no toman en cuenta los casos no diagnosticados. Esto nos da un panorama incompleto de la prevalencia de la condición”, explicó Florian Gaa, gerente general de Abartys Health. “En el manejo de la diabetes en la población general, nosotros abogamos por que se ponga un mayor énfasis en los datos y en la prevención”, agregó.
“La diabetes es un gran reto de salud. La condición aumenta la mortalidad y los costos de cuidado de salud en todas las poblaciones afectadas”, puntualizó Brenda Padilla, directora ejecutiva de la Asociación Puertorriqueña de Diabetes (APD). “Queremos llamar la atención pública a lo que es una verdadera crisis de salud y al mismo tiempo hacer disponible nuevas herramientas para las autoridades de salud, proveedores y pacientes,” expresó.
El análisis apunta además a una alta prevalencia de la prediabetes en Puerto Rico. Durante el período de 2019 al 2022, el análisis reveló el incremento de 25.7% a 28.6% en la prevalencia de prediabetes, lo que sumado con los casos de pacientes ya diagnosticados con la enfermedad, se traduce en que casi el 50% de la población de la Isla está afectada por la condición metabólica.

Se atribuye a la diabetes ser la causa principal de condiciones tales como la ceguera, ataques cardiovasculares y cerebro vasculares, amputación de extremidades y fallo renal, así como mayor riesgo de complicaciones y muerte por covid-19.
Los resultados del estudio están basados en una revisión de datos clínicos que abarcó más de 2.6 millones de resultados anónimos provistos por los laboratorios del País. La revisión se condujo en una población de pacientes únicos, no identificables, en estricto cumplimiento con las regulaciones estatales y federales de salud.
De acuerdo a los resultados, la prevalencia de la enfermedad renal crónica (CKD, en inglés) para el presente año alcanzó el 24% de la población con diabetes, comparado con 9.4% en la población con niveles normales de glucosa. Es decir, en los pacientes con diabetes en la Isla, la prevalencia de enfermedad renal es 3.2 veces mayor que en personas sin diabetes.
En esa misma dirección, los niveles bajos de colesterol de lipoproteínas de alta densidad (HDL por sus siglas en inglés), conocido como el colesterol “bueno” y los niveles altos de triglicéridos, fueron dos y tres veces mayor, respectivamente, en personas con diabetes que en personas con niveles normales de glucosa.
En términos geográficos, los 10 municipios con la mayor prevalencia de diabetes al momento son Camuy, Quebradillas, Hatillo, Lares, Yauco, Utuado, Arecibo, San Lorenzo, Adjuntas y Lajas.
Para completar la revisión de datos y el análisis correspondiente, Abartys Health trabajó de cerca con la Asociación Puertorriqueña de Diabetes (APD) para desarrollar el primer tablero clínico para el manejo de diabetes en la Isla. El tablero, basado en la plataforma de manejo de datos clínicos ClinicLynk, ofrece información en tiempo real, proveyendo un panorama de la condición por género, geografía, edad y proveedores de salud, entre otros factores.
“Típicamente, el 70% de las decisiones clínicas se toman a base de datos clínicos, ahora tenemos visibilidad real y precisa sobre la prevalencia de la diabetes y prediabetes, basada en datos reales. Esto nos permite tomar acción para identificar y manejar casos de prediabetes en tiempo real, para evitar el deterioro de la condición. En conjunto con las autoridades de salud pública, también podemos planificar, implementar y medir iniciativas de prevención”, destacó Padilla.
Actualmente el gobierno de Puerto Rico descansa en el Behavioral Risk Factor Surveillance System (PRBRFSS) del CDC, para medir la prevalencia de la diabetes y otras condiciones. El sistema de encuestas telefónicas establecido en el 1984, recoge información acerca de comportamientos de salud riesgosos, prácticas de salud preventiva, acceso al cuidado de salud relacionados primordialmente a enfermedades crónicas y lesiones.
39
Los alimentos y su rol protector contra el
Alzheimer
POR LCDA. ALANA MARRERO GONZÁLEZ, MHSN, LND
Laprevalencia de la demencia, incluyendo la enfermedad del Alzheimer ha aumentado de forma alarmante en los últimos años.
El Alzheimer es la cuarta causa de muerte más común en Puerto Rico. Es un trastorno neurodegenerativo del cerebro y la forma más común de demencia. Actualmente se estima que el número de personas que presentan esta enfermedad a escala mundial se encuentra entre 15 y 20 millones. Suele ser más común en personas mayores de los 65 años.
FACTORES DE RIESGO
• Factores genéticos
• Eventos vasculares
• Hipertensión
• Diabetes
• Niveles elevados de lípidos en sangre
• Alteraciones hormonales
• Factores de estilo de vida: fumar y la inactividad física
EL CEREBRO Y LA NUTRICIÓN
Todos los alimentos que consumes tienen un rol en mantener la salud cerebral. Estos alimentos pueden mejorar funciones específicas, como la memoria y concentración.
Así como no existe una pastilla mágica que ayude a prevenir la pérdida de memoria, no existe un alimento único que pueda asegurar la función del cerebro. Los estudios científicos sí nos revelan los mejores alimentos que protegen el cerebro y la memoria.

NUTRICIÓN
NUTRIENTES QUE AYUDAN A PROTEGER EL CEREBRO
• ÁCIDOS GRASO OMEGA-3 — Un 60% del cerebro se compone de este tipo de grasa y la utiliza para construir células nerviosas y del cerebro. Estas grasas son esenciales para aprender y para la memoria.
• ÁCIDO FÓLICO — Las neuronas son particularmente sensibles al ácido fólico y una deficiencia puede causar anormalidad en su función.
• MAGNESIO — La deficiencia de este mineral ha sido vinculada con el desarrollo del Alzheimer.
• ZINC — El cerebro tiene el mayor contenido de zinc y es esencial para su funcionamiento normal. Este mineral ha sido señalado muchas veces como uno de los nutrientes implicados en el deterioro de la función cognitiva.

• SELENIO — Tiene como función principal proteger a las células del daño oxidativo producido por los radicales libres generados durante el metabolismo. Un estudio realizado en ancianos utilizando como indicador el estatus nutricional del selenio a largo plazo, constató que la deficiencia de selenio contribuye al deterioro de la función cognitiva.
ALIMENTOS CLAVES PARA UN CEREBRO CON SALUD ÓPTIMA
• CEREZAS (berries) – En este grupo se incluyen las cerezas rojas, azules y negras. Todas contienen flavonoides, estos pigmentos naturales dan el color brillante a las cerezas, y a su vez ayudan a mejorar la memoria. Estudios han demostrado que consumir un servicio o más cada semana, ayuda a retardar el proceso de pérdida de memoria.
• BRÉCOL – Los vegetales de color verde intenso contienen nutrientes perfectos para la salud del cerebro. Estos son la vitamina K, folato y betacaroteno. La ciencia nos dice que el brécol puede retardar la perdida de función cognitiva.
• NUECES – Son una excelente fuente de proteína y grasas saludables. Un estudio en 2015 encontró que consumir nueces diariamente mejora la función cerebral, consumir nueces también se relaciona a una mejor función cardíaca y arterias más limpias.
Referencias:
1- Nehlig A. Effects of coffee/caffeine on brain health and disease: What should I tell my patients? Pract Neurol. 2016;16(2):89-95. doi:10.1136/practneurol-2015-001162
2- Kalt W, Cassidy A, Howard LR, et al. Recent Research on the Health Benefits of Blueberries and Their Anthocyanins. Adv Nutr. 2020;11(2):224-236. doi:10.1093/advances/nmz065
3- Han QQ, Shen TT, Wang F, Wu PF, Chen JG. Preventive and Therapeutic Potential of Vitamin C in Mental Disorders. Curr Med Sci. 2018;38(1):1-10. doi:10.1007/s11596-018-1840-2
4- Reddy PH, Manczak M, Yin X, et al. Protective Effects of
• CAFÉ Y TÉ VERDE – La cafeína en tu café o té mañanero ofrecen más que un empujón de energía y concentración. Un estudio en 2014 encontró que las personas que consumían café y té diariamente presentaron mejores resultados en su función cerebral. La cafeína puede ayudar a mantener por más tiempo la memoria, el consumo moderado se ha visto relacionado a evitar condiciones degenerativas como el Parkinson y el Alzheimer.
• CHINAS – No solo aportan casi todos los requisitos de vitamina C al día, esta súper fruta ayuda a mejorar la memoria. De acuerdo con estudios, la mayor concentración de vitamina C en nuestro sistema, se asocia con mejora en el enfoque, atención y rapidez en la toma de decisiones.
• CÚRCUMA – Esta especia de color anaranjado tiene entre sus ingredientes múltiples beneficios para el cerebro. Es antiinflamatoria y antioxidante, dos factores que se asocian a mejoras en la memoria, crecimiento de células nuevas en el cerebro y aumento en la secreción de dopamina y serotonina, hormonas que regulan nuestro estado de ánimo. Añade esta especia a guisos y sopas.
• CHOCOLATE OSCURO – Este sabroso alimento está lleno de compuestos que incluyen flavonoides, cafeína y antioxidantes. ¡Cuidado! El chocolate oscuro debe tener 70% o más de contenido de cacao y se conoce como “chocolate oscuro”. Estos beneficios no se observan en el chocolate regular con leche —que solo contiene de 10%-50% de cocoa— o chocolate blanco, que en verdad se elabora con crema de cacao. El chocolate oscuro se ha asociado a mejoras en la memoria y función cerebral, y su consumo debe ser moderado, a razón de un pequeño cuadrito diario. Pregunta a tu nutricionista o médico de cabecera.
En fin, muchos alimentos pueden ayudarte a mantener la salud cognitiva. Algunos alimentos como las frutas y vegetales incluidas en esta lista, otros como el té y el café contienen antioxidantes que protegen al cerebro de daños causados por el estrés y hasta el mismo ambiente.
Otros alimentos como las nueces contienen nutrientes que apoyan la memoria y el desarrollo del cerebro. Puedes apoyar la función de tu cerebro y mejorar la memoria y estado de humor diariamente seleccionando algunos de estos alimentos.
Indian Spice Curcumin Against Amyloid-β in Alzheimer’s Disease. J Alzheimers Dis. 2018;61(3):843-866. doi:10.3233/JAD170512
5- Crichton GE, Elias MF, Alkerwi A. Chocolate intake is associated with better cognitive function: The Maine-Syracuse Longitudinal Study. Appetite. 2016;100:126-132. doi:10.1016/j. appet.2016.02.010
6- Wysoczański T, Sokoła-Wysoczańska E, Pękala J, et al. Omega-3 Fatty Acids and their Role in Central Nervous System - A Review. Curr Med Chem. 2016;23(8):816-831. doi:10.2174/092 9867323666160122114439

Relación entre la nutrición y el VIH/SIDA
En1981 el Centro para el Control y Prevención de las Enfermedades (CDC, en inglés) indicó que el virus de la inmunodeficiencia humana (VIH) ataca el sistema inmunitario del cuerpo, y cuando no se trata puede causar el Síndrome de Inmunodeficiencia Adquirida (SIDA). La infección por el VIH en los seres humanos provino de un tipo de chimpancé de África Central.
maneras: transmisión sexual, transfusión de sangre, sus derivados u órganos de una persona que vive con VIH/SIDA —incluyendo el uso compartido de jeringuillas— y cuando una mujer que vive con el VIH/SIDA le trasmite el virus a su hijo(a) durante la gestación, el parto o en la lactancia materna. El virus actúa sobre el sistema inmune, en particular sobre los linfocitos CD4, que están involucrados en la protección del cuerpo contra las infecciones.
 POR ALANA MARRERO GONZÁLEZ, MHSN, LND
POR ALANA MARRERO GONZÁLEZ, MHSN, LND
Según datos del CDC, el origen de este virus en el ser humano provino de la versión del virus en los chimpancés —llamado virus de inmunodeficiencia símica (VIS)— que se pudo haber transmitido a los seres humanos cuando cazaban los chimpancés por su carne y entraron en contacto con sangre infectada. Estudios muestran que el VIH pudo haber pasado de los chimpancés a los seres humanos a finales del 1800. Entonces, a lo largo de varias décadas, el virus se propagó lentamente por toda África y posteriormente, a otras partes del mundo, incluido Estados Unidos en la mitad de los años 70.
El VIH es un virus que mata o daña las células del sistema inmunológico del organismo. Puede transmitirse de persona a persona de las siguientes

La mala nutrición, el poco acceso a las cantidades recomendadas de alimentos y la progresión de la enfermedad, han sido relacionados con el deterioro de la salud de las personas con VIH/SIDA y, finalmente, conduce a un aumento en la mortalidad. La relación entre el estado nutricional y el VIH/SIDA ha sido una característica clave de estudio desde el comienzo de la epidemia.
RELACIÓN ENTRE LA NUTRICIÓN Y EL VIH/SIDA
La infección de VIH afecta el estado nutricional de la persona causando problemas en la ingesta de alimentos, aumento en los requerimientos de energía, problemas de absorción de nutrientes y complejas alteraciones metabólicas que culminan en pérdida
de peso y descompensación del estado nutricional. La desnutrición, pérdida de peso y las deficiencias de micronutrientes son comúnmente observadas en los individuos con VIH/ SIDA y están asociados con un aumento de la morbilidad y la mortalidad.

La descompensación del estado nutricional es una consecuencia común de la infección por VIH, que contribuye a desarrollar un pobre estado nutricional, así como a la frecuencia y gravedad de las infecciones oportunistas relacionadas con la condición. Muchos estudios han indicado que la desnutrición es causada por múltiples factores y está influenciada por la etapa de la enfermedad, así como por la naturaleza de las complicaciones relacionadas.
El estado nutricional es un factor importante en la supervivencia de la condición. La intervención nutricional eficaz, la consejería y apoyo ayudan
a mejorar el estado nutricional y son considerados componentes esenciales en el tratamiento del VIH / SIDA.
Una nutrición adecuada es también necesaria para optimizar los beneficios de los medicamentos antirretrovirales que son esenciales para prolongar la vida de las personas infectadas con el VIH.
TRATAMIENTO Y COMPLICACIONES NUTRICIONALES
El tratamiento utilizado para el VIH/ SIDA es la combinación potente de drogas retrovirales (HAART) cuyo objetivo es suprimir la replicación del VIH utilizando combinaciones de drogas que inhiben las enzimas del VIH.
La supresión total es lo que se identifica cuando la condición se encuentra en niveles no detectables, esto es posible siempre y cuando el paciente cumpla en más del 95% con su terapia. Mantener este grado de adherencia al tratamiento es difícil y en muchos casos los efectos
son adversos. Algunos de los efectos secundarios más notables son la anemia, pancreatitis, hepatitis y la intolerancia a la glucosa.
Los efectos metabólicos de la condición consisten en síndromes interrelacionados de redistribución de la grasa, como la hiperlipidemia y resistencia a la insulina.
Las complicaciones metabólicas como la resistencia a la insulina, intolerancia a la glucosa, ácido láctico, la acidosis, alteraciones de las enzimas hepáticas, anemia, osteopenia y alteraciones en los niveles de lípidos en sangre —lipodistrofia y dislipidemia— se han asociado con la infección VIH y el uso a largo plazo de los medicamentos. Además de las complicaciones metabólicas, los pacientes a menudo tienen dificultades para comer debido a efectos secundarios como náuseas, vómitos, pérdida de apetito y diarrea.
44 Bienestartotal | Professional Edition
TERAPIA MÉDICO NUTRICIONAL
El manejo del estado nutricional es un componente vital para todas las personas con VIH/SIDA (19) en todas las etapas de la enfermedad. La eficacia de la intervención nutricional se ha documentado así como el asesoramiento nutricional por ser considerado fundamental en el tratamiento del VIH / SIDA. Se ha demostrado que la evaluación nutricional, el apoyo y el asesoramiento influencian de manera positiva la salud y ayudan a mejorar el estado nutricional del paciente. También, mejora la eficacia de la terapia HAART a través de un mejor cumplimiento.
La intervención nutricional debe tener como objetivo mejorar el conocimiento nutricional de los pacientes sobre su condición a través de la educación. Esto permitirá que la persona se sienta empoderada y procure alcanzar una calidad de vida. La evaluación del estado
nutricional forma parte de las estrategias de intervención nutricional y debe abordar cualquier deficiencia de nutrientes, trastornos metabólicos, mantener el estado de la proteína y estimular la adhesión a la terapia retroviral.
REQUERIMIENTOS DE MACRONUTRIENTES
Proteína
Las dietas altas en proteína pueden promover un balance positivo de nitrógeno y una reposición de la masa corporal magra.
Las personas —con y sin la condición— tienen una respuesta metabólica normal a las dietas altas en proteína; la suplementación proteica estimula el metabolismo de proteínas. Los requerimientos de proteína pueden ser estimados en 1.0 a 1.4 g/kg para mantenimiento y 1.5 a 2.0 g/kg para reposición de proteínas. La restricción proteica solamente se recomienda en aquellas personas con daños hepáticos y renales severos. Si el paciente tiene problemas hepáticos y renales, el tratamiento nutricional debe ser igual al de personas sin la infección.
Añadir proteína a la dieta de personas con la infección puede resultar beneficioso, para mantener las células viscerales. Sin embargo, se requiere de estudios que evalúen los efectos de aumentar la ingesta de proteínas.

Grasa
La tolerancia a las grasas varía de individuo a individuo. En personas con malabsorción o diarrea se recomienda utilizar dietas bajas en grasa. Se recomienda el uso de los triglicéridos de cadena mediana (MCT) por su fácil absorción y el uso del aceite de pescado (omega-3) en combinación con los triglicéridos de cadena mediana para mejorar la función inmune.
Fluidos y electrolitos
Los requerimientos de líquidos en los individuos con la condición son similares a los individuos sin la condición. Se calculan utilizando la fórmula 30 a 35ml/kg —de 8 a 12 tazas para adultos— al día. Se deben aumentar los requerimientos si tienen complicaciones como náuseas, diarrea, vómitos, sudores nocturnos y fiebres prolongadas. Se recomienda el remplazo de electrolitos —sodio, potasio y cloro— en la presencia de vómitos y diarreas.
Vitaminas y minerales micronutrientes
Las investigaciones sobre los micronutrientes y sus efectos en el sistema inmune son usualmente contradictorias. Se
requieren estudios aleatorios controlados para identificar las relaciones entre las ingestas de vitaminas, minerales, deficiencias, necesidades y las personas con VIH/SIDA. Usualmente, los dietistas recomiendan utilizar suplementos de multivitaminas y minerales que provean el 100% de los requerimientos dietarios recomendados y un suplemento básico de vitaminas del complejo B. En los adultos, también se ha encontrado que el suplementar hasta el 55% de los requerimientos dietarios para riboflavina y tiamina ha mejorado las tasas de sobrevivencia.
Ejercicios
Se considera importante realizar una cantidad adecuada de ejercicios de resistencia para evitar la pérdida de masa magra. Realizar ejercicios físicos moderados de tres a cuatro veces a la semana aumenta el conteo de linfocitos CD4+ y ofrece un efecto protectivo. Se revisaron 18 publicaciones en las cuales se evaluó el efecto de la actividad física en personas con la condición. Las revisiones sistemáticas de Cochrane concluyeron que realizar intervalos o ejercicios aeróbicos, ejercicios de resistencia o una combinación de ambos —por el tiempo mínimo de 20 minutos por sesión en una frecuencia de tres veces en semana— puede mejorar significativamente la condición cardiovascular y minimizan los síntomas de depresión.
Se deben tomar consideraciones especiales con aquellas personas que padecen de fatiga, historial de abuso de substancias controladas y alcohol.
Referencias Bibliográficas
1. Fee, E. and Brown, T.M. Michael S Gottlieb and the identification of AIDS. American Journal of Public Health. 2006; vol. 96, no. 6, pp. 982.
2. Tabi, M. and Vogel, R.L. Nutritional counseling: an intervention for HIV-positive patients. Journal of Advanced Nutrition. 2006; vol. 54, no. 6, pp.676-682.
3. Gottlieb, M.Pneumocystis pneumonia. 1981:30, 250.
4. Rosenberg, E.S. and Walker, B.D. HIV 1-specific helper t cells: Acritical host defence. AIDS Research Human Retrovirus. 1998; vol. 14, pp. S143-S147.
5. Fenton, M. and Silverman, E. C. Medical nutrition therapy for human immunodeficiency virus disease, In Krause’s Food and Nutrition Therapy. Ed.by Mahan, L.K. and Escott-Stump, S. 12th edition. Philadelphia,Pennsylvania: W.B Saunders Company. 2008; pp. 991-1020.
45
¿Qué dice la ciencia?
Implicaciones nutricionales para personas de experiencia trans
Durante la pasada década, la comunidad LGBTQ ha ganado mayor reconocimiento, y como resultado, en el 2016, el Instituto Nacional de Salud (NIH) designó de forma oficial a las comunidades de minoría como poblaciones con disparidades de salud, pero estas barreras se agudizan aún más en la población trans.

Cada día son más las personas que deciden utilizar terapia hormonal como tratamiento de afirmación de género, y muchas de ellas van a tener consideraciones nutricionales específicas. Sin embargo, hasta el momento, no hay guías o recomendaciones nutricionales específicas para la población trans.
Las investigaciones sobre los requisitos nutricionales específicos para la población son pocos, sin embargo, los resultados han sido contundentes. Uno de los grandes resultados obtenidos, nos indica que las personas de la comunidad trans que deciden utilizar terapia hormonal han tenido resultados favorables en su estado de ánimo, entiéndase disminución de ansiedad o depresión, además de los cambios físicos, que por ende, repercuten en calidad de vida.
Es importante destacar que no toda la comunidad trans experimenta disforia de género, definida como la sensación de incomodidad o angustia por sentir que su identidad de género difiere del sexo asignado al nacer, o de las características físicas relacionadas con el sexo. Es también pertinente mencionar que no toda la población trans utiliza terapia de hormonas. La población es muy diversa y todas las identidades dentro de la población trans son válidas.
Al igual que con muchos medicamentos, el utilizar terapia hormonal puede tener efectos secundarios que alteran el
estado nutricional.
Los resultados obtenidos en investigaciones nos han dado poderosas observaciones sobre el impacto a la salud de la terapia hormonal.
El estradiol, por ejemplo, una de las hormonas utilizadas como terapia hormonal, puede provocar reducción de masa muscular, aumento en peso y riesgo de aumento en el nivel de triglicéridos. Mientras que la espironolactona —que se utiliza como bloqueador de los niveles de testosterona— la ciencia nos indica que puede aumentar los niveles de potasio en sangre, sobre todo en aquellas personas que tengan condiciones de salud previas como enfermedades del corazón o del riñón.
Por otro lado, el uso de testosterona se ha relacionado a niveles elevados de presión arterial, así como con el aumento del colesterol LDL y reducción del colesterol HDL. Estos resultados son de gran valor para la comunidad trans y los profesionales de la salud, pues visibilizan la necesidad de orientación en nutrición. Estos resultados validan la necesidad de asegurar que la comunidad trans sea visibilizada para que pueda recibir la consejería nutricional necesaria como parte de los servicios de su tratamiento.
Aunque los esfuerzos para entender las implicaciones nutricionales en esta población están en marcha, falta mucho camino por recorrer. Por ahora, se les recomienda a las personas de experiencia trans, buscar ayuda y orientación con profesionales en la salud cualificados para trabajar con la población. Al igual que todas las poblaciones de minoría, la comunidad trans merece cuidado y apoyo en todos los aspectos de la salud.
46 Bienestartotal | Professional Edition
POR LCDA. ALANA MARRERO GONZÁLEZ, MHSN, LND
Dos recetas saludables
POR AGRAEL OROZCO
Si estás en la onda de comer sano y por dicha razón procuras elaborar tus almuerzos para llevar a la oficina, en breve te comparto dos recetas de wraps elaborados con plantillas plantillas de espinacas y tomate Planitas. Son de fácil elaboración, además de pocas calorías.
WRAPS CON ENSALADA DE POLLO CON ARÁNDANOS Y QUESO CREMA
Ingredientes:
4 plantillas de espinaca
2 tazas de pechuga de pollo cocida a la plancha, picada en trozos
1/3 tz. de taza de apio picado
1/3 tz. de queso crema
1/3 tz. de mayonesa ¼ tz. de nueces picadas 1/3 tz. de arándanos secos
1 cda. de azúcar
1 cda. de vinagre de sidra 1/8 cdta. de semillas de apio ¼ cdta. de eneldo seco ¼ cdta. de ajo en polvo sal y pimienta al gusto
Procedimiento:
En un tazón o bol, combina el pollo, las nueces, el apio y los arándanos secos. En otro bol mezcla la mayonesa, el queso crema, el vinagre de sidra, el apio,
el azúcar, la sal y la pimienta. Vierte la cantidad deseada sobre la mezcla de pollo, incorpora bien y deja aparte.
Ahora debes calentar las plantillas de espinaca en una sartén, de 10 a 15 segundos, por cada lado, a fuego medio alto. Si deseas calentarlas en el microondas, deberás colocar las plantillas entre dos hojas de papel toalla húmedas, y calentarlas entre 30 y 45 segundos.
Una vez las plantillas estén listas, solo te falta agregar el pollo. Dobla los lados y enrolla para servir a gusto.
WRAPS DE PAVO

Ingredientes:
8 plantillas de tomate
2 pechugas de pavo sin piel y deshuesadas
1 tz. de queso crema
2 cdas. de queso parmesano
2 cdas. de cebolln verde, finamente picado
6 lonjas de tocineta de pavo, cocidas en término crujiente, y cortadas en trozos
1 pimiento rojo cortado en tiras delgadas
1 pimiento amarillo cortado en tiras delgadas
1 pepino cortado en tiras medianas
1 cda. de jugo de limón
½ lechuga romana cortada en tiras sal y pimienta al gusto
Ingredientes para adobar el pavo:
1 cda. de mostaza
2 cdtas. de tomillo
½ cda. de aceite de oliva ¼ tz. de jugo de naranja 1 cda. de ajo picado
Procedimiento:
Precalienta el horno a 350 grado F. En un bol pequeño combina la mostaza, jugo de naranja, aceite, tomillo y ajo, mezcla bien y adoba las pechugas de pavo.
Una vez aplicado el adobo, coloca las pechugas de pavo en una bandeja apta para el horno y hornéalas por 30 minutos. Una vez cocidas las pechugas, retira del horno y déjalas enfriar.
En otro envase, mezcla el queso crema con jugo de limón, cebollín, queso parmesano y pimienta al gusto. Prueba y si es necesario, agrega sal. Deja reposar.
Calienta las plantillas de tomate en una sartén, de 10 a 15 segundos, por cada lado, a fuego medio alto. Si deseas calentarlas en el microondas, deberás colocarlas entre dos hojas de papel toalla húmedas, y calentarlas entre 30 y 45 segundos. Una vez listas las plantillas, deja reposar aparte.
Con la ayuda de una espátula, unta la salsa de queso parmesano sobre cada plantilla y esparce ligeramente la lechuga. Coloca los pedacitos de tocineta, las tiras de pavo y los vegetales. Cierra la plantilla por los dos extremos, enrolla y córtala por la mitad.
Tiempo de trufas
POR YAIRA SOLÍS ESCUDERO
Latrufa es un hongo más, de los tantos que nos regala la naturaleza, pero se diferencia de los demás por su aroma penetrante y delicado. Es la trufa un manjar de tierra adentro que crece parásitamente en las raíces de árboles como encinas, avellanos y robles a 10 o 60 pulgadas bajo la tierra. La temporada de las trufas negras de verano suele ser de mayo a septiembre y la de invierno es desde noviembre hasta abril, y las trufas blancas de invierno se recolectan entre septiembre a enero mientras que las blancas de primavera se encuentran disponibles solo durante el mes de mayo.
Sabiamente dosificada, la trufa aporta distinción a una pastelería salada, a recetas con pastas y cualquier carne como protagonista, y ni hablar en sopas y salsas... Se utilizan crudas o cocidas, cortadas en láminas, en rodajitas o en dados, en forma de jugo, de esencia y hasta, simplemente de perfume para exquisitos platos de pastas.
Según indica el diccionario Larousse Gastronomique, los antiguos egipcios comían la trufa rebozada en grasa y cocida en papillote, y los griegos y los romanos le
atribuían un alto valor afrodisíaco.
La palabra “trufa” proviene del latín ‘tuber’ que significa excrecencia, por lo que en la Edad Media se consideraba una manifestación del diablo, llevándole a caer en el olvido culinario por varias décadas. Con el Renacimiento la trufa volvió a tomar notoriedad convirtiéndose en manjar de paladares aristocráticos, gracias a los cocineros reales de la época.
En la antigüedad se utilizaban los cerdos para encontrar las trufas porque el potente olor atraía su olfato, pero como las estropeaban mucho en el proceso de recogerlas —incluso se las comían— los buscadores de este manjar encontraron en el perro a su mejor aliado.
Las trufas se venden frescas, conservadas en grasa de cerdo, vino o aceite de oliva, desecadas, cocidas y en latas soldadas o frascos de cristal herméticamente cerrados, para que se preserve su materia aromática que se encuentra, sobre todo, en la parte externa la trufa.
Por fortuna, en nuestro mercado existen establecimientos de venta de productos gourmets que ofrecen al consumidor la oportunidad de adquirir exquisito aceite

48 Bienestartotal | Professional Edition COCINA

de trufas para acentuar platos de pastas, ensaladas y carnes. Incluso, usted podrá encontrarlo en el supermercado.
CREMA DE PAPAS CON ESENCIA DE TRUFAS BLANCAS
Ingredientes:
1 papa, cortada en cuadros y frita 4 tzs. de caldo de pollo 4 papas hervidas y majadas 1/2 mazo de cilantro fresco picado finamente aceite de esencia de trufas blancas, al gusto sal y pimienta al gusto

Procedimiento:
En una cacerola con agua y sal, hierve las papas, y una vez cocidas maja con un
poco del agua en la que fueron hervidas; deja refrescar. Aparte, en otra cacerola hierve el caldo de pollo y una vez hierva retira del fuego; cuando la papa y el caldo de pollo estén bastante fríos, vierte en un procesador de alimentos o en una licuadora y procesa. Recuerda que los alimentos calientes que se mezclan en el procesador o la licuadora tienden ha liberar el calor una vez inicies el proceso, por lo que debes hacerlo cuando estén bastante fríos y debes tapar bien el procesador o la licuadora antes de combinarlos, para evitar que la tapa salga expulsada. Salpimienta al gusto. Vierte en una cacerola profunda y a temperatura baja para mantener la crema caliente. Al servir, espolvorea el cilantro, incorpora las papas fritas y añade la esencia
de trufas blancas.
VIEIRAS CON ACEITE DE TRUFAS
Ingredientes para las vieiras y las habas: 1 libra de habas agua con sal al gusto 24 vieiras, bien limpias 2 cdas. de aceite de oliva sal y pimienta negra al gusto
Para adornar 4 cdas. de aceite de pimientos amarillos 4 cdas. de aceite de trufas 1 pimiento amarillo
Procedimiento:
Corta las habas por la mitad y hierva en agua salada hasta que se tornen tiernas.
50 Bienestartotal | Professional Edition
Remueve y coloca aparte. Calienta en una sartén dos cucharadas de aceite de oliva, sazona las vieiras con sal y pimienta, cocina por aproximadamente un minuto por cada lado.
Al momento de servir, a modo de líneas, distribuye el aceite de trufas sobre el plato, luego coloca las vieiras y las habas, añade a forma de línea horizontal el aceite de pimientos amarillos y adorna con lascas de pimiento amarillo.
TOURNEDOS DE BUEY CON SALSA DE TRUFAS
Ingredientes:
2 lbs. de solomillo de buey sal al gusto 1 lata pequeña de trufas
2 tazas de caldo de res pimienta al gusto vegetales (de tu preferencia)
1 tz. de brandy, de tu preferencia 3 cdas. de mantequilla
2 tazas de vino Oporto
Procedimiento:
Corta los tournedos y saltéalos con la mantequilla, cuando estén a punto, añade el brandy y flamea. Aparte, en una cacerola reduce el Oporto, añade las trufas cortadas a la juliana e incluye el jugo, en el cual vienen conservadas. Salpimienta al gusto.
En plato un plato, sirve tus vegetales favoritos, añade los tournedos que servirás sobre un poco de la salsa. Sirve aparte la salsa restante para quien desee más.
TORTILLA DE TRUFAS
Ingredientes:
2 huevos enteros y batidos previamente
½ trufa de lata
2 cucharadas de crema de leche
1 cucharada de aceite de oliva
1 pizca de sal ralladura de queso parmesano
Procedimiento:
En el bol donde bates los huevos, añade la crema de leche, la pizca de sal y la trufa rallada, mezcla bien. Déjalo reposar a temperatura ambiente por varios minutos para que la trufa perfume al huevo. Una vez pasado un tiempo de reposo, procede a pintar el fondo de la sartén con un poco de aceite de oliva y vierte la mezcla del huevo para que se cocine a fuego medio. Recuerda distribuir la mezcla por todo el fondo de la sartén y una vez cocida —con la ayuda de una espátula de cocinar— despega una mitad de la tortilla del fondo y dóblala por la mitad —como si fuera una empanadilla— y voltea la tortilla para que se cocine por ambos lados. Cuando falten varios segundos para retirarla del fuego, espolvoréale ralladura de queso parmesano y una vez la sirvas en el plato, añádele un toque de ralladura de trufa. Acompaña con tus vegetales favoritos.

VINAGRETA DE TRUFAS NEGRAS
Ingredientes:
2 onzas trufas negras trituradas
1 cda. de vinagre balsámico
4 cdas. de vinagre de vino tinto 4 cdas. de aceite de girasol
3 cdas. de aceite de oliva virgen extra 2 cl. de Oporto
pimienta negra recién molida, al gusto sal al gusto azúcar al gusto
Procedimiento:
En un envase de cristal con cierre hermético, vierte las trufas trituradas y agrega una cucharada de aceite de girasol y el Oporto; cierra el envase y agita para que todos los ingredientes se mezclen bien. Luego, añade la sal, el azúcar, la pimienta negra y el aceite de oliva. Vuelve a cerrar el envase y agita por varios segundos para que todos los sabores se combinen, e incorpora el vinagre balsámico y el vinagre de vino tinto. Vuelve a cerrar el frasco de cristal y agita hasta que notes que todos los ingredientes estén mezclados. Cierra el frasco y guarda en un lugar fresco por un día antes de utilizarlo.
SABÍAS QUE...
Existen alrededor de 70 especies de trufas. Aunque cada una es muy diferente sobresalen tres tipos:
• La trufa negra ‘melanosporum’ o mejor conocida como la Trufa del Périgord, que se recolecta de diciembre a febrero; la trufa blanca del Piamonte, Italia —la más cotizada— que se recolecta durante el otoño (septiembre hasta diciembre) y la Trufa de verano o ‘tuber estivium’.
• A la trufa negra del Périgord se le conoce también como “el diamante negro de la cocina”, por su perfume intenso y delicado, de pulpa blanca al principio, luego gris marrón y negra violácea. Presenta venas blancas cuando ha llegado a su completa madurez y para considerarse de gran calidad, debe ser redonda y de una sola pieza. Adquiere todo su valor cuando está madura.
• Las trufas blancas, ‘tuber magnatum’ provienen del Piamonte y presentan un color gris perlado y un delicado sabor a ajo; se consumen preferiblemente crudas, cortadas a láminas casi transparentes, y con ellas se aderezan diversos platos de la cocina piamontesa: como la cremosa y compacta Fonduta de las Langhe y los risottos tartufato, entre otros.
51

BODEGAS
Sugerencias de maridajes con platos típicos navideños
POR LCDO. JAVIER O. BERBERENA Diplomado WSET Certified Sommelier Certified Wine Educator
Ya casi comienza nuestra época más preciada, la Navidad. En la mayor parte de las actividades a las que asistimos encontramos nuestro tan esperado y rico menú navideño. Para poder maridar nuestros platos típicos con el vino preciso, debemos tomar en cuenta los sabores, la sazón y la intensidad de nuestra comida. Un vino reúne todos los requisitos para poder llevar a cabo tan difícil tarea de maridar exitosamente el menú boricua navideño: ¡Champagne!
UN POCO DE TRANSFONDO
La mayoría de los países productores de vinos del viejo mundo —Europa— tienen en común al menos un elemento gastronómico: sus vinos maridan casi a la perfección con la comida típica de su país. Aunque en Puerto Rico no producimos vino, somos uno de los países noproductores que más los disfruta, conoce y consume vino de todo el mundo.
Dado a la localización geográfica de la región de Champagne, en Francia, la vid no recibe la cantidad de luz necesaria para que pueda madurar lo suficiente y pueda producir el contenido de azúcar necesaria para la elaboración de un vino agradable. Por ello, hace varios siglos los productores de este vino crearon un sistema basado en mezclar vinos de diferentes añadas, diferentes viñedos y diferentes varietales de uvas. Esto, con el propósito de crear una consistencia en sus vinos que hoy
día ha sido el éxito de Le Champagne, y ha sido copiado por países con interés en producir vinos espumosos de calidad.
Los vinos producidos en Champagne, por consiguiente, son vinos con una acidez pronunciada, una marcada presión gaseosa (CO2) que produce burbujas pequeñas, finas, consistentes y de larga duración. Estos vinos se clasifican de varias formas, la primera y más importante de estas, por su nivel de azúcar residual. Legalmente el champagne posee las siguientes clasificaciones de grados de azúcar residual: Extra Brut, Brut, Extra Sec (Extra Dry), Sec (Dry), Demi-Sec (Médium Dry), Doux (Sweet). Mientras más dulce sea el champagne, más dulce debe ser la comida que le acompañe, y viceversa.
DETALLES A CONSIDERAR
Varios elementos contribuyen a que el champagne sea —sin discusión— el mejor vino espumoso del mundo, y su estilo de cuerpo: ligero —elegante, liviano—, mediano y completo, tiene un factor determinante a la hora de maridar con la comida típica puertorriqueña.
Nuestra gastronomía, especialmente el menú que acostumbramos degustar para la época navideña, es sumamente rico, diverso, pero difícil de maridar con vinos.
La tarea de maridar nuestras comidas típicas con este líquido preciado llamado champagne, no se limita a recomendar su pareo con la morcilla, pues cada plato puertorriqueño tiene diferentes cantidades de sazón, acidez, azúcar, pique, especias, proteínas y grasas que le hacen particular a la hora de maridar.
A estos elementos en conjunto se le conoce como el cuerpo.
Comidas con cuerpo pesado o
completo necesitan un vino con ese mismo estilo de cuerpo. Para tener una idea más completa del proceso de maridaje de champagne con la comida típica puertorriqueña, debemos conocer algunos términos, estilos y atributos del reseñado vino.
Como regla general la composición de uvas en el champagne se distribuye de la siguiente manera: 60 % Chardonnay, 30% Pinot Noir, y 10% Pinot Meunier. Cada una de estas varietales juega un papel importante en la creación de los vinos. No obstante, los conocedores del champagne sostienen que las dos varietales más importantes son Chardonnay y Pinot Noir. De hecho, prestigiosos champagnes son hechos solamente con una o ambas de estas varietales, excluyendo la Pinot Meunier.
DE LA IDEA DEL MARIDAJE AL PLATO
Cómo influye la aportación de cada uva en el plato, es una guía importante; por ejemplo, la Pinot Noir le da a la mezcla, cuerpo, complejidad y estructura.
Los vinos que son dominados en todo o en su mayoría por esta varietal muestran un aroma y sabor a galletas y pan tostado. Mientras que la Pinot Meunier contribuye con aromas florales, sabor y aromas a fruta madura, lo que ayuda a que el vino se pueda consumir más tempranamente; y la Chardonnay le otorga delicadeza, acidez marcada, frescura, elegancia y los elementos necesarios para que los vinos puedan envejecer periodos más extensos, en comparación con los que no cuentan con ella en la mezcla. Estos son los atributos más importantes de las tres varietales para los vinos elegantes y delicados.
53
Blanc de Blanc es un champagne hecho exclusivamente de Chardonnay, lo que constituye una excepción a los vinos de Champagne.
El vino Blanc de Blanc es exactamente lo que su propio nombre implica, un vino blanco de uvas blancas. Estos vinos son más ligeros en cuerpo que los champagnes tradicionales, y son excelentes acompañantes de comidas ligeras, aperitivos, pescados, viandas y vegetales. Es el mejor vino para utilizarlo como apéritif —primera bebida—, debido a su cuerpo, acidez, y elegancia. Mientras que un Blanc de Noir —excepción aun más rara en Le Champagne— es un vino blanco de uvas tintas exclusivamente Pinot Noir, Pinot Meunier: una o ambas. Este estilo de vino espumoso es el mejor acompañante de comidas con cuerpo completo, tales como carnes y quesos de estilo y sabor fuerte. Lamentablemente la producción de champagnes Blanc de Noirs es bien limitada en las casas de vino que se importan a Puerto Rico.

Por otro lado, el champagne rosado o Rosé, contrario a lo que muchos puedan pensar, es seco —no dulce— y es de alta calidad. Este estilo brinda un aroma a frutas rojas, especialmente a fresa, que despierta el deseo de probarlo inmediatamente.
CAVAS: ESPUMOSOS ESPAÑOLES
No menos importante es el vino espumoso de España, que por ley se le ha designado con el nombre de Cava.
Se trata de un vino espumoso de igual calidad que la mayoría de los espumosos producidos en la región de Champagne —los únicos permitidos por ley a llevar el nombre de champagne—, obtenido mediante la realización de una segunda fermentación alcohólica en botella, del vino base, y cumpliendo el mismo método que champagne: el método tradicional.
El vino debe permanecer, al menos, nueve meses en contacto con las lías y en la misma botella en la que tuvo lugar la segunda fermentación. Podrá ser: blanco o rosado.
Debido a que como regla general es más joven que el champagne ordinario, esto le brinda una habilidad innata para limpiar y refrescar el paladar con cada bocado.
Su burbuja fina y persistente, su paladar seco y sabores cítricos, lo hace un candidato idóneo para nuestros platos,
especialmente nuestros asopaos especiados y picantes.
RECOMENDACIONES DE MARIDAJES
Así pues, tomando en consideración la versatilidad de estilos de champagnes y cavas, recomiendo las siguientes combinaciones para maridarlo con nuestra comida típica.
1Guineítos y guineítos al escabeche, con un champagne Non Vintage, de estilo y cuerpo ligero como: Baillecart Salmon,
Laurrent-Prrier, Perrier-Jouët, Taittinger, Pommery, G.H. Mumm o Ruinart.
2Viandas, solas o con aceite de oliva, con champagne Blanc de Blanc.
3Morcillas con champagne rosada, de cuerpo mediano como: Moet & Chandon rosada o Lanson rosada.
4Pernil o lechón, masitas de cerdo (fritas), mofongo —no muy grasoso— o tostones, necesitan un vino espumoso con una marcada acidez, pero de cuerpo
54 Bienestartotal | Professional Edition
mediano como: Moet & Chandon, Jacquesson, Lanson, Nicholas Feuillatte y Heidsieck & Co Monopole.
5Alcapurrias, bacalaitos y frituras de similar contenido, con champagne Brut, de cuerpo mediano, por ejemplo: NV Charles Laffitte, NV Pol Roger, NV Nicholas Feuillatte.
como por ejemplo: Pol Roger, Charles Laffitte o una de cuerpo ligero rosada como Billecart Salmon rosada.
7Arroz maspostea’o, al igual que el risotto necesita un champagne bastante seco, con cuerpo completo como: Gosset, Salon o Bollinger.
OTROS VINOS ESPUMOSOS QUE MERECEN SER MENCIONADOS
Los Espumoso de California, poseen un cuerpo más completo que los vinos regulares de Champagne, y concurren en que son producidos utilizando el método tradicional de doble fermentación originado en Le Champagne, mientras que utiliza las mismas varietales.

Australia también ha copiado exitosamente este estilo de California y produce muy buenos espumosos aplicando el método tradicional de elaboración.
En Italia tenemos a Franciacorta. Este fue el primer vino italiano producido únicamente con una segunda fermentación en botella y obtuvo su designación de DOCG — designación de calidad más alta en Italia— en 1995. Los vinos son finos, con aroma de galleta y pan tostado, secos y ligeramente amplios en boca.
En fin, cualquiera que sea tu selección para maridar esta Navidad con champagne u otro espumoso, es bueno que sepas que pocas cosas sobrepasan el placer de maridar nuestra bella cocina navideña con estos preciosos y deliciosos caldos.
Louis Roederer, Krug y Veuve Clicquot Ponsardin.
9Asopao de pollo —de los que revive muertos— acompañará muy bien con Cava Vallformosa o Agustí Torelló Mata.
6Arroz
blanco con habichuelas, arroz guisado, arroz con pollo, arroz con gandules, requieren de champagnes de cuerpo mediano y acidez más controlada,
8Platos de contenido grasosos como pasteles de yuca o plátanos, asopao de pollo o de jamón, Fabada o Caldo Gallego, maridan mejor con champagne de cuerpo completo y acidez marcada, tales como:
10Los postres típicos de Navidad como: tembleque, arroz con dulce, casquitos de guayaba con queso de hoja, parean bien con champagne dulce o semi dulce: Veuve Clicquot Ponsardin Demi Sec, Moet & Chandon Nectar Imperail o Demi Sec y Laurrent-Prrier Demi Sec.
55
Detalles de la degustación
POR AGRAEL OROZCO
Elvino es el complemento ideal para acompañar la comida dando resultados en boca verdaderamente sorprendentes. El maridaje suele ser por similitud o armonía, por contraste o por tema — historia, cultura, región vinícola, uvas, etc.— y los más realizados suelen ser los de armonía, porque como la palabra infiere, son creados para resaltar —de forma casi paralela— los atributos del vino y de la comida. Entonces, ningún sabor se sobrepone y el vino no pierde su fuerza y se expresa en boca libremente.

El Larousse de los Vinos nos recuerda que la regla general del maridaje es que los pescados, mariscos y algunas carnes blancas deben acompañarse con vino blanco, y las carnes rojas con vino tinto, porque al final de la experiencia tanto vino y comida trabajan en función de potenciar y exaltar sus cualidades y sabores.
Otra regla general es que hay que considerar seriamente los ingredientes del plato, especialmente si incluye vinagre, sabores picantes, muy dulces o mucha sal, porque afectan las cualidades del vino en boca y destruyen la experiencia. Igualmente, desde el punto de vista del vino, es preciso considerar su acidez y sus taninos, y su grado alcohólico.
Por lo general —según el Larousse de los Vinos— un plato de sabor delicado —a base de una salsa de crema— debe acompañarse con vino de sabor delicado, de lo contrario, si el vino es robusto y de sabor muy intenso, opacará los sabores sutiles del manjar.
Asimismo, el Larousse de los Vinos indica que la comida con sabores fuertes debe maridarse con vinos robustos y con cuerpo, y en muchas ocasiones se integra una salsa elaborada a base de una reducción de vino tinto para dar balance a la ecuación. Pero como todo en la vida, estas reglas, aunque buenas, tienen sus excepciones y ahí entra en función tu conocimiento sobre vinos, tu paladar y tus
56 Bienestartotal | Professional Edition
gustos. Algunas recomendaciones básicas que nos explica este diccionario sobre maridajes son:
• OSTRAS Y OTROS MOLUSCOS
Se recomienda el vino blanco, bien seco, como el Chablis o Moscatel seco francés y también un Albariño español, porque su nivel de acidez es alto y ayuda a contrarrestar el sabor salado del molusco.
• SOPAS — Aunque no suele acompañarse con vino, cuando se trata de caldos claros como el consomé, se puede maridar con vinos fortificados secos, como el Jerez, Madeira o Marsala. Incluso se pueden integrar al caldo para lograr mayor complejidad.
• CARNES BLANCAS Como regla general, la mayor parte de los pescados saben mejor cuando se les acompaña con vino blanco, porque su acidez elimina el sabor a marisco, mientras que el vino tinto acentúa su sabor metálico. Es importante destacar que según la consistencia del plato debe variar el tipo de vino blanco a servirse.
Los platos con pescado de sabor intenso como protagonista, en salsa de vino, debe degustarse con vinos más robustos como los elaborados 100% de uva Chardonnay.

Los pescados de carne y sabor delicado suelen acompañarse de vinos blancos igualmente delicados, como los franceses del Valle del Loira o Alsacia, y los vinos italianos de la varietal Pinot Grigio; mientras que el salmón —de sabor intenso— puede maridarse con un vino igualmente intenso que puede incluir un tinto liviano, un rosado seco o un blanco poderoso como los elaborados con uvas Chardonnays o Sauvignon Blanc.
Con respecto a la carne de cerdo y la ternera, se pueden acompañar con vinos blancos afrutados que no sean demasiado secos, como los Chardonnays, los vinos alsacianos de la uva Riesling o los españoles de Rioja, sin mucha madera. Asimismo, estas carnes van bien con un tinto liviano, como un Beaujolais, o un rosado seco.
En cuanto al pollo, puedes acompañarlo con prácticamente cualquier vino, desde un blanco de cuerpo medio, rosado o tinto liviano. Si el plato va a ser algo complicado, como un pollo al vino tinto, puedes acompañarlo con un vino tinto de mayor cuerpo y estructura.
• CARNES ROJAS — La de res o el cordero son carnes fuertes en sabor e imponen los vinos tintos, de buen cuerpo como los tintos franceses de Burdeos, Borgoña y el Valle del Ródano, los vinos americanos, australianos y chilenos elaborados a base de Cabernet Sauvignon y Merlot, los tintos italianos del Piemonte y los españoles de Rioja y Ribera del Duero.
• QUESOS — Suelen maridar con vinos blancos, tintos o vinos dulces. Los quesos de sabor liviano hechos a base de crema, como el Brie y el Port Salut francés combinan muy bien con vinos blancos
afrutados de Chardonnay o Sauvignon blanc; para los quesos más fuertes como el Roquefort francés, Stilton inglés y Saga Blue italiano van bien con vinos tintos con mucho cuerpo, como los elaborados en las regiones de Burdeos, en Francia; Barolo, en Italia y hasta vinos más dulces como el Sauterne francés.
• POSTRES — Lo ideal es maridarles con vinos dulces y champagne Demi-Sec. Aunque puedes hacerlo con Sauternes franceses, los extraordinarios Beerenauslese y Trockenbeerenauslese alemanes y el Oporto portugués.
57
Ácido Ribonucleico: mensajero del ADN
El ARN también lleva información genética, pero sus características y su tamaño mucho más reducido le permite pasar a través de los poros de la membrana del núcleo de la célula —donde se encuentra el ADN— y llegar hasta el compartimento celular donde se ensamblan las proteínas. Así, podemos decir que mientras el ADN “porta” la información genética, el ARN la “transporta”.
Cada
1ro de agosto se celebra el Día Mundial del Ácido Ribonucleico (ARN), con la finalidad de dar a conocer la importancia de esta molécula en la generación de proteínas en el organismo.
Este conmemoración mundial nació en 2018 por iniciativa del biólogo molecular uruguayo Juan Pablo Tosar, un investigador del Instituto Pasteur Montevideo. Este acontecimiento ha sido avalado por la RNA Society. Se eligió el 1ro de agosto como Día Mundial del ARN, debido al juego de palabras entre August 1 (1ro de agosto en inglés) y AUG 1. Es una secuencia triple del ARN — denominada codón— que da inicio a la síntesis de proteínas por parte de la célula.

FORO
POR ARACELI AGUILAR SALGADO
El ácido ribonucleico es una molécula que está formada por una cadena simple de ribonucleótidos, compuesta a su vez por ribosa, un fosfato y una base nitrogenada —adenina, guanina, citosina y uracilo. Más recientemente, se han encontrado algunos ARN de pequeño tamaño que están involucrados en la regulación de la expresión génica.
2ARN transferencia (ARNt): Tienen una estructura peculiar con forma de trébol. Su función es transportar aminoácidos específicos hasta los ribosomas para conseguir completar el proceso de traducción —de ARNm a aminoácidos que se unen para formar proteínas— del que hablábamos anteriormente.
3ARN ribosómico (ARNr):
Es el más abundante y el ARNr unido a proteínas forma los ribosomas, orgánulos encargados de la traducción.
4ARN nucleolar (ARNn):
Se origina a partir de diferentes segmentos de ADN denominados región organizadora nucleolar. Una vez formado el ARNn, se fragmenta y da lugar a los diferentes ARNr.
El ARN es un ácido nucleico similar en estructura al ADN, pero con algunas diferencias sutiles. La célula utiliza el ácido ribonucleico para una serie de tareas diferentes, una de estas moléculas se llama ARN mensajero o ARNm. Es la molécula de ácido nucleico cuya traducción transfiere información del genoma a las proteínas. Otra forma de ácido ribonucleico o ARN, es el ARNt o ARN de transferencia, y moléculas de ARN nocodificantes de proteínas, que físicamente llevan los aminoácidos al sitio dónde se lleva a cabo la traducción y permiten que sean ensamblados en las cadenas de proteínas en dicho proceso.
El ácido ribonucleico está presente en todas las células vivas que presentan similitudes estructurales con el ADN. Contiene la información copiada del ADN, necesaria para la fabricación de proteínas que son vitales para todos los procesos de la vida.
El ARN permite la síntesis de proteínas, una conexión esencial para la información genética entre el ADN y las células.
Las moléculas del ácido ribonucleico cumplen funciones regulatorias y enzimáticas. Los tipos de ARN presentes en las células son:
• ARN mensajero (ARNm)
• ARN de transferencia (ARNt)
• ARN ribosómico (ARNr)
Dependiendo de la estructura y función específica que realice cada ARN, se encontrarán distintos tipos de ARN:
Además, existen los ARN implicados en la regulación de la expresión génica, es decir, ARNs que controlan, qué parte del ADN se expresa en forma de proteína y cuales no, gracias a que son complementarios a regiones específicas de ARNm o de ADN.
Si un fragmento de ARN se une al ADN o al ARNm, habrá un obstáculo que impedirá que se lea correctamente y por tanto que pase a la proteína. Podríamos decir que la unión de ese fragmento de ARN hace que esa región del ácido nucleico quede oculta y no se traduzca por la célula.
Este tipo de ARN es conocido como ARN de interferencia (iRNA). En esta clase de ARN, nos encontramos con dos subcategorías en base a la longitud del mismo:
1ARN largo no codificante (lncRNA): ARN de 200 nucleótidos. Regula la modificación epigenética principalmente en el núcleo, regulando la transcripción de genes a nivel transcripcional mediante la modulación de la modificación de histonas o ADN, principalmente metilación y acetilación.
2Small RNA: Longitud inferior a 200 nucleótidos. Desempeña funciones importantes en procesos celulares como la diferenciación celular, proliferación, migración, apoptosis… Dentro de este último tenemos:
• Micro ARN (miRNA): Contiene alrededor de 22 nucleótidos.
1
ARN mensajero (ARNm): Estructura lineal con alguna horquilla. Se sintetiza en el núcleo de la célula a partir del ADN. Es el resultado del proceso de la transcripción. Su función es copiar fragmentos del ADN para sacar dicha información del núcleo y llevarlo a los ribosomas donde la información genética pasará a proteínas.
• ARN asociados a Piwi (piRNA): Implicado en el desarrollo embrionario, mantenimiento de la integridad del ADN de la línea germinal, silenciamiento de la transcripción de transposones, supresión de la traducción, formación de heterocromatina y regulación epigenética de la determinación del sexo.
• ARN interferente pequeño o ‘small interfering’ RNA (siRNA): No es codificado por el ADN. Se introduce artificialmente.
También existen los ARN con actividad catalítica conocidos
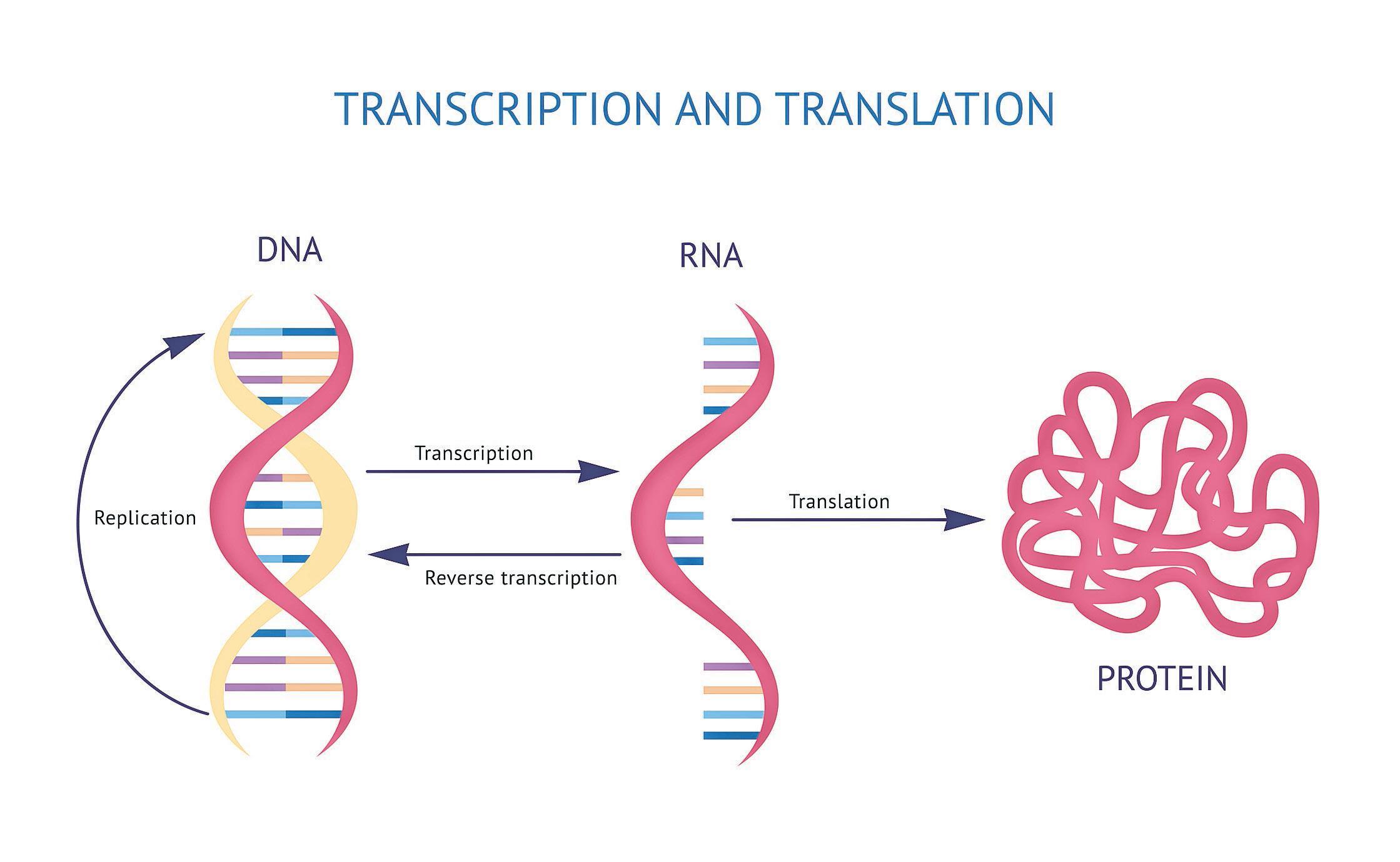
60 Bienestartotal | Professional Edition
como ribozimas, que son ARN con actividad catalítica. La palabra es el resultado de unificar “ácido ribonucleico” (ARN) con “enzima”. Son capaces de llevar a cabo reacciones bioquímicas.
El ácido nucleído es considerado como el ácido del material o código genético, por lo que tenemos que tener presente que el código genético cumple con las características básicas de:
• Es universal para virus, células eucariotas y células procariotas.
• Se organiza en codones o tripletes, cada tres nucleótido se escribe la secuencia necesaria para codificar un aminoácido
• Cada aminoácido puede ser codificado por más de un triplete, esto se denomina código degenerado.
• Existen codones que señalan el comienzo y el final de la traducción.
Hay dos tipos distintos de ácido nucleico: ADN y ARN. El ácido nucleico del ADN es desoxirribosa, mientras que el ácido nucleico del ARN es la ribosa. Como lo explican sus nombres, la desoxirribosa de ADN carece de una molécula de oxígeno en comparación con el azúcar de ribosa de ARN. Los nucleótidos que comprenden el ADN incluyen adenina (a), guanina (G), citosina (c) y timinas (t), mientras que los nucleótidos de ARN incluyen A, G, C y uracilo (NSC).
Si bien la estructura del ADN es una doble hélice en las células eucariotas, el ARN es generalmente monocatenario y se presenta en varias formas. La estructura monocatenaria del ARN permite que esta molécula se pliegue sobre sí misma y forme varias estructuras secundarias estables, según sea necesario.
Conociendo ya como está compuesto el ácido ribonucleico o ARN podemos distinguir las diferencias o los conceptos claves sobre las estructuras entre el ADN y el ARN para una mejor comprensión: ADN
• Es de doble cadena.
• Es estable.
• Es la forma de almacenar y transmitir la información genética
• Tiene complementariedad de bases adenina-tiamina, guaninacitosina
ARN
• Es de cadena sencilla.
• Es inestable.
• Implicado en los procesos de expresión y regulación de los genes.
• Tiene complementariedad de bases adenina-uracilo, guaninacitosina.
Todas las células somáticas de nuestro organismo contienen la misma información genética —genotipo—, sin embargo, el conjunto de los genes que expresan —fenotipo— son diferentes entre ellas, dando lugar a células de extirpes y funciones totalmente distintas. Incluso una misma célula puede expresar genes diferentes en función de múltiples factores.
UTILIZAR ARN SINTÉTICO COMO TERAPIA EN ENFERMEDADES GENÉTICAS
La ciencia se fija en el funcionamiento del cuerpo humano continuamente, lo ha hecho en muchos avances en el campo de la ingeniería, diseño ergonómico y por supuesto de la ciencia y la salud. En los últimos años se han aprobado diversas terapias basadas en el uso del ARN para tratar enfermedades hereditarias causadas por defectos en genes.
Estas terapias no modifican en ningún momento el ADN del paciente, sino que modulan o cambian la expresión del gen defectuoso. Algunos ejemplos son las terapias basadas en ARN por la atrofia muscular espinal, la distrofia muscular de Duchenne o la distrofia macular asociada a la edad.
Estos medicamentos utilizan moléculas sintéticas de ARN que reconocen de forma específica el ARN del propio paciente, el cual está defectuoso debido a una variante o mutación genética, y lo reprimen para silenciar la producción de proteínas perjudiciales para la célula.
Como podemos ver la vida nació hace unos 4000 millones de años, cuando una molécula atrapada entre membranas empezó a ser capaz de gestionar su entorno y sacar copias antes de colapsar y desaparecer. Esa molécula tenía la facultad de portar órdenes en una secuencia que albergaba un código. Muchos expertos piensan que antes que nada se desarrollaron moléculas similares al ARN, que tiempo después dieron lugar a variantes como el ADN.
Quizá todo comenzó con un mensaje más sencillo y lábil antes de surgir la sutil complejidad del ácido desoxirribonucleico, o tal vez fue de otra manera. Lo que resulta indudable es que estas grandes moléculas, cada una a su modo, representan lo más fascinante de la vida, la capacidad de albergar mensajes para manejar la materia, lo cual supone mantener la impetuosa carrera de relevos de los seres vivos.
La autora es periodista, abogada, ingeniera y presidenta del Congreso Hispanoamericano de Prensa, Analista y comentarista mexicana; e-mail periodistaaaguilar@gmail.com
61
Innovador mapa interactivo de apoyo para diabéticos
REDACCIÓN BTP
LaAsociación Puertorriqueña de Diabetes (APD) anunció el nuevo mapa interactivo disponible en su página diabetespr.org, que proveerá acceso a la información de apoyo para pacientes que viven con diabetes, sus familiares y la comunidad, con el fin de empoderarlos y fortalecer el alcance con aliados de servicio y cuidado.

Además de proveer un mayor alcance y visibilidad de recursos los cercanos a los pacientes, cuidadores y profesionales de la salud, este mapa permite el registro de los pacientes por área geográfica, lo que permite personalizar los recursos a disposición.
“Nuestro enfoque es llegar a todos los que viven con diabetes mediante nuevas tendencias y tecnologías accesibles a través de la plataforma. También nos permite estar peraparados antes, durante y después de emergencias, ya que contamos en la plataforma con múltiples especialistas y centros de cuidado, que será fácil identificar para una ágil atención de cada necesidad que busque el usuario”, informó Brenda Padilla, directora ejecutiva de la Asociación Puertorriqueña de Diabetes.
Esta nueva herramienta tiene entre sus objetivos brindar opciones de acceso a los servicios necesarios a la población con diabetes y acceso a múltiples fuentes de datos como registros de coordenadas GPS para todos los centros de tratamiento dirigidos por endocrinólogos, Centro de Salud Primaria (FQHC) 330 y principales proveedores de
atención primaria/IPA en todos los segmentos de atención médica en la Isla. De manera visualmente atractiva y fácil de entender, el paciente podrá conocer la disponibilidad de instalaciones de capacitación activas que incorporan diabetes.
A través del mapa interactivo los usuarios podrán identificar las localidades más cercanas a ellos y obtener información para cuidar de la diabetes. Los pacientes, sus cuidadores y comunidad en general, tendrán acceso a las opciones de servicios cerca de su comunidad, lo que fortalece la base de su atención primaria.
Varios de los participantes de servicio en el mapa interactivo son: los Centros de Salud Primaria 330, Endocrinólogos, Podriatras, Centros de úlceras, Nutricionistas, Centros de Diálisis, entre otros.
Los especialistas que quieran formar parte de los proveedores de servicios médicos en el mapa interactivo lo pueden hacer directamente en la página web: www. diabetespr.org. En la pestaña podrán acceder a un cuestionario para completar la solicitud o actualizar los datos existentes. Una vez evaluada la solicitud, se incorpora al mapa.
La Asociación Puertorriqueña de Diabetes promueve desde el 1988, servicios educativos para el control de esta condición y sus complicaciones. Para más información sobre servicios educativos y de apoyo, visite www.diabetespr. org o llame al 787-729-2210.
62 Bienestartotal | Professional Edition BTP-NEWS
REDACCIÓN BTP
Lossiete médicos residentes graduados este año 2022 del Programa de Residencia de Medicina Interna del Hospital Damas, Inc. aprobaron el examen de certificación del American Board of Internal Medicine (ABIM). Este es el cuarto año consecutivo que todos los residentes egresados del programa aprueban el examen.
El Programa de Residencia en Medicina Interna del Hospital Damas fue establecido en el 1978. Actualmente es dirigido por el Dr. Miguel Magraner Suárez, director del Departamento de Medicina Interna del Hospital y profesor de la Ponce Health & Sciences (PHSU). Este Programa está debidamente acreditado a nivel nacional por el Accreditation Council for Graduate Medical Education (ACGME).
“Estamos muy orgullosos de nuestros residentes, de su calidad como médicos y futuros servidores para la salud de nuestro País. Un gran por ciento de los
residentes que egresaron de esta clase se quedarán en Puerto Rico para proveer servicios de salud a los puertorriqueños. Agradecemos al Hospital Damas y a Ponce Health Sciences University por su apoyo y compromiso por el logro de nuestros médicos residentes”, declaró el Dr. Magraner Suárez.


La noticia surge precisamente cuando se discute en la Isla, la urgencia de fortalecer los programas de residencia para facilitar la integración de los nuevos médicos al mundo laboral y evitar la acelerada migración de estos, lo que redunda en menos servicios de salud para nuestra población en general.
REDACCIÓN BTP
Ellicenciado Víctor T. Adorno Badillo fue nombrado presidente del Colegio de Químicos de Puerto Rico (CQPR), organización fundada en 1941, y que funge como ente principal que agrupa a los profesionales de la química en el País.
“Agradezco la confianza que han depositado en este humilde servidor para dirigir los destinos de nuestro colegio. Tengo el compromiso de no defraudarlos y la certeza de que, durante esta gesta, juntos continuaremos fortaleciendo nuestro compromiso con la salud, el desarrollo y bienestar de nuestros colegiados y de todos los que habitamos en esta bella Isla del Encanto”, expresó Adorno Badillo.
A lo largo de su trayectoria
profesional, el Lcdo. Adorno Badillo se ha desempeñado en importantes roles en los ámbitos comerciales, educativos y de la química, entre ellos destacan: dirigir el Departamento de Análisis de la Autoridad de Acueductos y Alcantarillados; científico de Control de Calidad en Fujisawa; especialista en cromatografía de gas en PerkinElmer; científico de desarrollo de métodos para la industria farmacéutica en Ricons; y director ejecutivo de Caribbean University.
El Colegio de Químicos ha participado y auspiciado congresos científicos internacionales como los auspiciados por la Federación Latinoamericana de Asociaciones Químicas y del American Chemical Society. El Colegio es también el ente fundador del Congreso Panamericano de Química.
63
Egresados del Programa de Medicina Interna aprueban Board por cuarto año consecutivo
Nuevo presidente en el Colegio de Químicos de Puerto Rico
REDACCIÓN BTP
ElPuerto Rico Sexual Wellness Clinic anunció que la oficina del Dr. José Antonio Saavedra ha sido designado como Centro de Excelencia para el tratamiento con terapia de vapor de agua Rezūm™, un procedimiento mínimamente invasivo realizado en la oficina médica para hombres que buscan tratar su hiperplasia prostática benigna (HPB; BPH por sus siglas en inglés), y no solo los síntomas.

La terapia Rezūm utiliza vapor de agua natural para reducir el tamaño de la próstata y proporcionar alivio duradero de los síntomas de BPH sin cirugía invasiva, ni algunos de los posibles efectos secundarios de los medicamentos recetados.
BPH es una afección en la que la próstata del hombre se agranda y aprieta la uretra, provocando síntomas frustrantes como: necesidad de orinar frecuente o urgente, presentar un chorro de orina débil o interrumpido, y la necesidad de levantarse varias veces por la noche para orinar.
El BPH afecta aproximadamente al 50% de los hombres al cumplir los 60 años y hasta al 90 % al llegar a los 85 años.
Durante la terapia Rezūm, que se lleva a cabo durante una breve visita a la oficina del médico, se libera vapor de agua natural en todo el tejido prostático obstructivo.
Cuando el vapor entra en contacto con el tejido y vuelve a convertirse en agua, libera energía y mata el exceso de células de la próstata que aprietan la uretra. La respuesta curativa natural del cuerpo elimina las células muertas y encoge la próstata. Con el exceso de tejido eliminado, la uretra abre, aliviando los síntomas de BPH mientras preserva la función eréctil y urinaria. El procedimiento ambulatorio no requiere anestesia general y se realiza bajo sedación oral o anestesia local.
Este tipo de terapia ha sido sometida a extensos ensayos clínicos para evaluar su seguridad y eficacia. Ahora está incluida en las guías de tratamiento de BPH de la Asociación Americana de Urología y tiene datos de seguimiento de cuatro años, que muestran su capacidad para tratar las próstatas con hiperplasia de la región central, lóbulo lateral y lóbulo medio.
Más de 55 mil pacientes en todo el mundo han sido tratados con éxito con esta terapia.
Obtienen aprobación del examen del Joint Commission on Dental Examination
REDACCIÓN BTP
LaEscuela de Medicina Dental de la Universidad de Puerto Rico anunció que el 93% de los estudiantes que componen la clase de 2019 del Programa de Doctorado de Medicina Dental obtuvo la aprobación del nuevo examen Integrated National Dental Board Examination del Joint Commission on Dental Examination, en su primer intento. La prueba evalúa y aborda los componentes de ciencias básicas y las ciencias clínicas de este programa.

A su vez, la Escuela de Medicina Dental anunció que la clase entrante
del 2021 del Programa de Ubicación Avanzada obtuvo la aprobación de todos los exámenes nacionales.
“Reconocemos la excelencia de estos
estudiantes y les felicitamos por este logro. Estamos seguros de que serán pioneros en su carrera profesional al servicio de la salud oral. Les deseamos que continúen cosechando éxitos”, expuso el profesor Carlos Ortiz, rector interino del RCM.
Por su parte, el Dr. José R. Matos Pérez, decano interino de la Escuela de Medicina Dental del RCM, expuso que “estos resultados posicionan a nuestros estudiantes entre los mejores de la nación, lo cual nos enorgullece como escuela y como institución. Agradezco a la facultad y al personal no docente por su dedicación y compromiso en beneficio de la educación de nuestros estudiantes”.
64 Bienestartotal | Professional Edition
Reconocen centro para el tratamiento de terapia de vapor de agua
La oficina del Dr. José Antonio Saavedra ha sido designada como Centro de Excelencia para el tratamiento con la Terapia de Vapor de Agua Rezūm™. >Suministrada

It's your
moment to
shine. www.elvocero.com/revistas/mirame













































 POR MARCIA CRUZ-CORREA, MD, PHD, AGAF, FASGE Investigadora PanOncology Trials Catedrática Medicina & Bioquímica Universidad de Puerto Rico, Recinto de Ciencias Médicas
POR MARCIA CRUZ-CORREA, MD, PHD, AGAF, FASGE Investigadora PanOncology Trials Catedrática Medicina & Bioquímica Universidad de Puerto Rico, Recinto de Ciencias Médicas






 Actor portrayals
Actor portrayals




 POR ALANA MARRERO GONZÁLEZ, MHSN, LND
POR ALANA MARRERO GONZÁLEZ, MHSN, LND























