








Prof. Univ.
Dr. Marcel Tanțău
UMF „Iuliu Hațieganu” din Cluj-Napoca, Președintele Congresului Național de Gastroenterologie
Prof. Univ.
Dr. Cristian Gheorghe
UMF „Carol Davila” din București, Președintele Congresului Național de Coloproctologie
Prof. Univ.
Dr. Anca Trifan
UMF „Grigore T. Popa” din Iași
Prof. Univ.
Dr. Carol Stanciu
UMF „Grigore T. Popa” din Iași
Prof. Univ.
Dan Dumitrașcu
UMF „Iuliu Hațieganu“ din Cluj-Napoca
Prof. Univ.
Dr. Lucian Negreanu
UMF „Carol Davila” din București



Prof. Univ.
Dr. Cătălina Mihai
UMF „Grigore T. Popa” din Iași
Prof. Univ.
Dr. Cristina Cijevschi
UMF „Grigore T. Popa” din Iași
Prof. Univ.
Dr. Elena Toader
UMF „Grigore T. Popa” din Iași








Citește mai mult







Revista profesioniștilor din Sănătate • 2024 - 2025 • Publicație creditată B+ conform
Gastroenterologie
Noninvasive Medical diagnosticul hepatic neinvaziv prin biomarkerii serici


Corectează disbioza prin modularea microbiotei intestinale!

Acest material promoţional este destinat profesioniştilor din domeniul sănătăţii. Pentru informaţii suplimentare vă rugăm să consultaţi Rezumatul caracteristicilor produsului complet. Medicament eliberat pe bază de prescripţie medicală-PRF Administrare orală. Profesioniștii din domeniul sănătăţii sunt rugaţi să rapor teze orice reacţie adversă suspectată sau reclamaţie cu privire la acest medicament la adresa de e -mail: Drugsafety.alfasigma@addenda.ro sau la Agenţia Naţională a Medicamentului și a Dispozitivelor Medicale din România https://adr.anm.ro/ DAPP Alfasigma S.p.A.
Alfasigma România S.R.L. str. Cluceru Udricani, nr. 18, parter și etaj 1, sector 3, București tel.: 031.805.35.26, 031.805.35.27; fax: 031.805.35.28. e-mail: info.ro@alfasigma.com


SUFERI DE ALERGII?
Simptome frecvente cum ar fi strănut, prurit, rinoree, dificultăți de respirație, tuse, sau erupții cutanate pot fi reacții alergice.
LISTĂ ALERGENI
Polen
Polen graminee
Pir gros
Iarbă de gazon
Iarba de Bahia
Timoftică
Trestie
Secară
Polen de arbori
Salcâm
Cenușer(Alianthus)
Arin negru
Mesteacăn argintiu
Dud japonez (de hârtie)
Polen de alun
Criptomeria
Chiparos de Arizona
Chiparos
Fag
Frasin comun
Polen de nuc
Ienupăr
Dud
Măslin
Curmal
Platan englezesc
Plop negru
Ulm
Polen de ierburi
Știr
Ambrozie
Pelin negru
Cânepă
Spanac sălbatic
Trepădătoare
Paracherniţă
Patlagină
Ciulin rusesc
Urzică
Acarieni
Acarieni
Dermatophagoides farinae
Dermatophagoides pteronyssinus
Acarian de alimente
Acarian de făină
Blomia tropicalis
Glycyphagus domesticus
Lepidoglyphus destructor
Tyrophagus putrescentiae
Fungi
Drojdii
Malassezia sympodialis
Drojdie de panificație
Ciuperci
Alternaria alternata
Aspergillus fumigatus
Cladosporium herbarum
Penicilium chrysogenum
Alimentele din plante
Leguminoase
Arahidă
Năut
Soia boabe
Linte
Fasole
Mazăre
Cereale
Ovăz
Quinoa
Hrișcă
Orz
Semințe de lupin
Orez
Mei
Secară
Grâu
Grâu speltă
Porumb
Condimente
Boia de ardei
Chimen Oregano
Pătrunjel
Anason
Muștar
Fructe
Kiwi
Papaya
Portocală
Pepene
Smochină
Căpșună
Măr
Mango
Banană
Cireașă
Piersică
Pară
Afină
Struguri
Legume
Ceapă
Usturoi
Țelină
Morcov
Avocado
Cartof
Roșie
Nuci
Caju
Nucă braziliană
Nucă de pecan
Alună
Nucă
Macadamia
Fistic
Migdală
Semințe
Semințe de dovleac
Semințe de floarea-soarelui
Mac
Semințe de susan
Semințe de schinduf (molotru)
Alimente de origine animală
Lapte
Lapte de vacă
Lapte de cămilă
Lapte de capră
Lapte de iapă
Lapte de oaie
Ou
Albuș de ou
Gălbenuș de ou
Pește și fructe de mare
Vierme parazit din pește
Crab
Hering
Crevete de nisip
Crap
Cod de Atlantic
Homar
Crevete
Calamar
Midie
Stridie
Crevete nordic
Scoică
Crevete Black Tiger
Pisică de mare
Somon
Scrumbia albastră
Ton
Pește-spadă
Carne
Greiere
Carne de vită
Carne de cal
Carne de pui
Lăcustă
Carne de curcan
Carne de iepure
Carne de miel
Carne de porc
Larvă de făină
Venin insecte
Venin furnică de foc
Furnică de foc
Venin albină
Albină
Venin de viespe
Viespe americană
Viespe de hârtie
Viespe comună
Gândac de bucătărie
Gândac roșu de bucatarie
german
Gândac de bucătărie american
Alergeni de origine animală
Epiteliul animalelor de companie
Urină de câine (incl. Can f 5)
Câine
Porcușor de Guineea
Pisică
Șoarece
Iepure
Hamster siberian
Șobolan
Animale de fermă
Vacă
Epiteliu de capră
Cal
Epiteliu de oaie
Epiteliu de porc
Altele
Latex
Ficus
Ficus plângător
CCD
Hom s Lactoferrin
Parazit
Căpușa porumbeilor


Copierea fără acordul scris al editurii a oricăror elemente de grafică sau conținut editorial apărute în revistele editurii sunt considerate furt de proprietate intelectuală și intră sub incidența legii.









Șef de lucrări Dr. Oana Timofte
Ş. L., Dep. Medicale I- Semiologie Medicală-Gastroenterologie, UMF „Grigore T.Popa” Iași
As. Univ. Dr. Adriana Cojocaru
UMF „Victor Babeș” din Timișioara; Președinte al Societății de Neurologie și Psihiatrie a Copilului și Adolescentului din România
As. Univ. Dr. Ana Maria Ghiuchici
UMF „Victor Babeș” din Timișoara
As. Univ. Dr. Laura Huiban
UMF „Grigore T. Popa” din Iași
As. Univ. Dr. Raluca Ioana Avram
UMF „Grigore T. Popa” din Iași
As. Univ. Dr. Petrică Popa
Medic specialist Gastroenterologie, Universitatea de Medicină și Farmacie din Craiova
Dr. Răzvan-Cristian Statie
Medic rezident Gastroenterologie, Universitatea de Medicină și Farmacie din Craiova
Dr. Josan Jennifer
Clinica de Psihiatrie Copii și Adolescenţi, Timișoara; Secretar General al Societății de Neurologie și Psihiatrie a Copilului și Adolescentului din România
Dr. Marina Cozma
Clinica de Gastroenterologie, Spitalul Universitar de Urgență, UMF „Carol Davila” București
Trimite email pe adresa redactie@finwatch.ro, solicită un abonament la revista Medical Market
și primești 10 puncte EMC.

Sumar „Un concept deosebit - Gastroenterologia Verde - Green Gastroenterology!“ Interviu cu Prof. Univ. Dr. Marcel Tanțău 6 Programul ROCCAS de „Prevenție, depistare precoce, diagnostic şi tratament precoce al leziunilor precanceroase colorectale!“ Interviu cu Prof. Univ. Dr. Cristian Gheorghe 10 „Obezitatea - una dintre epidemiile silențioase!“ Interviu cu Prof. Univ. Dr. Anca Trifan 16 Un mesaj pe care mai ales medicii tineri trebuie să-l aibă în vedere! Prof. Univ. Dr. Dan Dumitrașcu 18 Este necesară colonoscopia la pacienții cu sindrom de intestin iritabil? Prof. Univ. Dr. Elena Toader 20 Cum putem preveni decompensarea cirozei hepatice? Prof. Univ. Dr. Anca Trifan, Prof. Univ. Dr. Carol Stanciu, As. Univ. Dr. Laura Huiban, As. Univ. Dr. Raluca Ioana Avram 24 Noi perspective în pregătirea intestinului Conf. Univ. Dr. Laura Carina Tribuș 30 Screeningul şi pregătirea adecvată pentru colonoscopie - pilonii în prevenția cancerului colo-rectal Prof. Dr. Lucian Negreanu, Dr. Marina Cozma 36 Sindromul de intestin iritabil Prof. Dr. Cătălina Mihai, Prof. Dr. Cristina Cijevschi 40 Controlează efectele refluxului gastroesofagian 43 Rezecțiile intestinale: dincolo de actul chirurgical Dr. Oana Timofte, Dr. Elena Gologan 44 Carcinoamele ampulare As. Univ. Dr. Petrică Popa, Dr. Răzvan-Cristian Statie 46 Tulburări ale dispoziției – anxietatea şi depresia la copiii cu boli inflamatorii intestinale Asist. Univ. Dr. Adriana Cojocaru, Dr. Josan Jennifer 48 Cum refacem deficitul nutrițional? Soluția oferită de familia de produse Resource© Prof. Dan L. Dumitrașcu 54 Rectocolita ulcero-hemoragică în sarcină As. Univ. Dr. Ana-Maria Ghiuchici 56
Consultant medical:
medic primar Medicină de familie Editor Calea
Sector 5, București, Electromagnetica Business
Corp 01, et. 1, cam. 4 Tel: 021.321.61.23 e-mail: redactie@finwatch.ro ISSN 2286 - 3443 4 www.revistamedicalmarket.ro Gastroenterologie
Dr. Aurora Bulbuc,
Rahovei, nr. 266-268,
Park,

„Un concept
deosebit
- Gastroenterologia Verde Green Gastroenterology!“
Interviu realizat cu Domnul Prof. Univ. Dr. Marcel Tanțău, UMF „Iuliu Hațieganu” din Cluj-Napoca, Medic primar Medicină internă și Gastroenterologie
Stimate Domnule Prof. Marcel TANȚĂU, anul acesta cel deal 43-lea Congres Național de Gastroenterologie, Hepatologie și Endoscopie Digestivă va avea loc în perioada 27 - 29 iunie 2024 la Cluj Napoca. În calitatea dvs. de Președinte al Congresului, vă rog, să specificați care va fi viziunea programului științific?
Organizarea Congresului Național de Gastroenterologie, Hepatologie și Endoscopie Digestivă este o mare provocare și o mare responsabilitate.
Din fericire, am reușit să ne mobilizăm și să îl organizăm în cadrul Sălii Polivalente din Cluj-Napoca, ce oferă un spațiu mult mai generos de organizare a unui congres de această talie în care dorim să adunăm peste 1000 de participanți.
Am invitat să ni se alăture și celelalte specialități: medicină generală, medicină internă, chirurgia digestivă, gastroenterologia pediatrică, pentru a avea cât mai multe prezentări interactive.
Dorim neapărat să implicăm cât mai mult și spitalale nonuniversitare, deoarece acestea, de multe ori vin la astfel de congrese pentru a audia, dar acum vrem să le oferim un cadru de a-și prezenta experința și dificultățile pe care le au în zonele unde își desfășoară ei activitatea. Dorim ca mulți dintre ei să poată progresa astfel încât să poată realiza intervenții la nivelul spitalelor universitare.
La acest congres vom acorda o atenție deosebită tinerilor gastroenterologi, aceștia vor avea sesiuni speciale dedicate lor, unde își vor putea prezenta cazuri deosebite și vor putea interacționa cu experții,

vor putea pune întrebări persoanelor cu cea mai mare experiență din domeniul gastroenterologiei românești.
Un concept deosebit la care ținem foarte mult este Gastroenterologia Verde-Green Gastroenterology prin care dorim să promovăm practici sănătoase, să reeducăm populația pentru a avea un comportament sănătos, în sensul de a avea o alimentație diversificată, un stil de viață sănătos, care, printre altele, este și un stil de viață ecologic, care protejează planeta noastră.
Din acest motiv, am lansat o inițiativă unică în societățile noastre de gastroenterologie, aceea de a realiza o ascensiune ecologică între Bâlea Cascadă și Bâlea Lac în data de 9 iunie, pentru a sublinia importanța activității fizice.
Gastroenterologia mondială realizează progrese foarte importante în toate domeniile. Desigur, ce ne interesează cel mai mult este, din păcate, creșterea accelerată a numărului de cancere digestive
și aici notăm cancerul de colon care, cel puțin în România, în ultimii treizeci de ani s-a triplat ca și incidență, ceea ce denotă clar, impactul factorilor de mediu, a modului în care ne alimentăm, de aceea și noi, încercăm să subliniem prin ințiativa noastră de gastroenterologie verde, să atragem atenția că un comportament corect este principalul pion în prevenția cancerelor digestive.
În domeniul acesta, o altă problemă majoră este creștea rapidă a greutății populației românești. Din păcate, în ultimii ani asistăm la o creștere a numărului de obezi în societatea noastră. Practic, dacă stăm să ne uităm după standarde, undeva la 30%, maxim 40% dintre adulți mai sunt normoponderali, 20%-30% sunt obezi în diferite stadii de obezitate. De aceea, în momentul de față avem o explozie de activități care să substituie voința noastră, fie prin metode endoscopice sau chirurgicale de modificare a tubului digestiv pentru a scădea greutatea corporală, care duce la complicații importante în timp, dacă nu este controlată. În cadrul congresului național, avem și o masă rotundă vis-à-vis de obezitate și managementul acesteia.
Dezvoltări ale intervențiilor endoscopice?
Desigur, s-au făcut progrese în special în domeniul endoscopiei, dezvoltarea celui de-al treilea spațiu, în sensul că există intervenții endoscopice care se realizează sub stratul mucos, după ce acesta se incizează printr-o incizură a mucoasei, se pot realiza miotomii, în special pentru achalazie, fiind una dintre cele mai cunoscute, se poate realiza secționarea pilorului, a diverticulului Zenker, a extirpării unor
6 www.revistamedicalmarket.ro Gastroenterologie Interviu






tumori submucoase și foarte important în momentul de față este o dezvoltare impetuoasă a rezecțiilor endoscopice agresive care concurează rezecțiile chirurgicale.
Aici vorbim pentru polipii de mari dimensiuni și plați, de disecția submucosală endoscopică care defapt este un procedeu prin care tumora este scalpată pas cu pas de pe stratul muscular și îndepărtată într-un singur fragment corect, complet, după care este înmânată histopatologului care poate să facă o evaluare post rezecție extrem de exactă.
Tehnica de POEM (Peroral Endoscopic Myotomy) este introdusă în România din 2013, la cinci ani după ce a fost introdusă la nivel mondial și ne apropiem de 300 de proceduri realizate, cu o îmbunătățire importantă a calității vieții celor cărora le-am efectuat.
De asemenea, să nu uităm dezvoltarea impetuoasă a ecoendoscopiei intervenționale care permite drenaje atât a colecțiilor peripancreatice cât și drenaje biliare sau intervenții biliopancreatice complexe, gastroenteroanastomoze realizate ecoendoscopic.
O altă revoluție tehnologică este dezvoltarea unui mini endoscop care se introduce prin duodenoscop, cu care putem investiga interiorul căilor biliare până în porțiunea distală, putem prelua biopsii, putem sparge calculi care nu erau accesibili altfel, sau pe căile pancreatice, unde putem să recoltăm biopsii din formațiuni, din stenozele pancreatice, să spargem sub control endoscopic calculi pancreatici și să tratăm patologiile pancreatice benigne, cum ar fi pancreatita cronică, o patologie care din păcate în țara noastră este frecventă din cauza etilo-tabacismului care este un viciu constant în societatea noastră.
Să nu uităm, din punct de vedere al hepatologiei, patologia legată de obezitate, care este încărcarea grasă a ficatului, +/- afectarea alcoolică care în momentul de față își caută o abordare cât mai complexă și din păcate, odată cu creșterea patologiei hepatice cronice, hepatocarcinomul reprezintă și el o patologie malignă extrem de frecventă care are abordări complexe și din acest motiv, unii pacienți pot beneficia de transplant hepatic, o realitate pe care o dorim și la Cluj, să devenim al treilea centru național de transplant hepatic, care va aduce o rază de speranță pentru pacienții care necesită schimbarea ficatului.
Proiecte viitoare?
Unul dintre proiectele noastre importante din domeniul gastroenterologiei este proiectul de educație continuă a pacienților noștri pentru a-și preveni prin schimbarea modului de viață, o repetăm din nou, dar este unul dintre pilonii importanți în a preveni patologiile digestive care sunt într-o creștere exponențială, astfel că se apropie de cele cardiovasculare.
Un comportament corect vis-à-vis de corpul nostru, este un comportament corect și față de planeta noastră, lucrurile sunt atât de legate încât trebuie doar să le privim atent și să le vedem. De exemplu, dacă noi consumăm un steak de vită și o farfurie de cereale, suprafața agricolă pentru steak-ul de vită este de douăzeci de ori mai mare. Trebuie să ne gândim cât steak de vită putem consuma ca să nu distrugem planeta.
Dat fiind faptul că au crescut leziunile premaligne digestive pe care le vedem la endoscopie, am dezvoltat un proiect corect de aliniere a endoscopiștilor români la tehnicile actuale de disecție și am demarat proiectul Romanian ESD Taskforce în care încercăm să instruim și
să atragem cât mai mulți gastroenterologi și endoscopiști în a efectua aceste disecții corecte, care au recidivă foarte redusă și care pot salva organul și pot îmbunătăți foarte mult prognosticul pacienților.
O nouă astfel de sesiune de hands-on pe stomace de porc se va derula vineri, 12 aprilie 2024, în cadrul celui de-al 12lea Congres Național de Coloproctologie care va avea loc tot la Cluj-Napoca. Ce mesaje/sfaturi aveți pentru tinerii care vor să aleagă această ramură a medicinei și anume Gastroenterologia?
După cum vedeți, Gastroenterologia este o specialitate extrem de dinamică, cu dezvoltări importante în ultimul timp, iar gastroenterologul român poate să realizeze că are la îndemână atât o activitate de integrare clinică, de studiu clinic, de patologie clinică, dar și o activitate intervențională cu o dezvoltare foarte susținută, dar care necesită multă implicare.
Din acest punct de vedere, Gastroenterologia are un viitor important și mulți dintre tinerii care vor îmbrățișa această specialitate vor fi fascinați de posibilitățile de diagnostic și de tratament.


8 www.revistamedicalmarket.ro Gastroenterologie Interviu

Luaţi decizii de tratament informate pentru binele pacienţilor
QuikRead go® iFOB
• Testare imunochimică cantitativă realizată în imediata proximitate a pacientului (test FIT)
• Decizii optime privind tratamentul potrivit fiecărui pacient
• Gestionare optimă a resurselor în colonoscopii
Rezultate fiabile
• Reducerea potenţialului de eroare umană
• Trasabilitatea rezultatelor datorită funcţiilor de conectivitate și memorare a rezultatelor
• Performanţă a testării dovedită și fiabilă
Cu setul de recoltoare QuikRead iFOB obţineţi rezultate de screening îmbunătăţite
• Procedura igienică de recoltare îmbunătăţeste conformitatea probelor
• Volumele de probă sunt ușor de recoltat datorită recoltorului furnizat
• Rezultatele sunt aliniate la recomandările naţionale privind testele de screening
QuikRead go® este marcă înregistrată Aidian Oy (Finlanda). Aidian dezvoltă, produce şi comercializează sisteme de diagnostic pentru profesioniştii din sănătate, cu peste 40 de ani de experienţă în domeniu.
Distribuitor pe teritoriul României:
Pentru informaţii suplimentare, vă rugăm accesaţi adresa: www.aidian.eu Jensen Pharma SRL, Tel +40 771 464 977 www.jensenmed.ro, office@jensenmed.ro
Programul
ROCCAS
de „Prevenție, depistare precoce, diagnostic şi tratament precoce al leziunilor precanceroase colorectale!“
Interviu realizat cu Domnul Prof. Univ. Dr. Cristian Gheorghe, Medic Primar
Gastroenterologie și Medicină Internă, Șef Secția 1 Gastroenterologie, Centrul pentru Boli
Digestive și Transplant Hepatic, Institutul Clinic Fundeni, Coordonator al Laboratorului de endoscopie digestivă diagnostică și intervențională, Institutul Clinic Fundeni
Stimate Domnule Profesor, în calitate de Președinte în exercițiu al Societății Române de Coloproctologie (SRCP), vă rog să descrieți, care sunt atributele și obiectivele acestei Societăți?
Societatea Română de Coloproctologie (SRCP) este o societate multidisciplinară în care însă ponderea membrilor este reprezentată de chirurgi cu interes în patologia coloproctologică și gastroenterologi-endoscopiști cu preocupări de asemenea în patologia colorectală organică și funcțională; particularitatea Societății este schimbarea alternativă a Președintelui la doi ani prin alegerea succesivă a unui chirurg și ulterior a unui gastroenterolog -endoscopist cu experiență recunoscută național și internațional în domeniul coloproctologiei. Unul dintre obiectivele majore ale SRCP este educația. În acest sens, în timpul Congresului Societății care se desfășoară bianual, în afara meselor rotunde în care se discută tot ceea ce este nou în tematica congresului, sunt multiple sesiuni educaționale, prezentări video pentru tehnici de bază și tehnici noi endoscopice și chirurgicale; de asemenea sunt discuții pe baza prezentărilor de cazuri în același scop educațional. Tinerii pot lua contact cu liderii de opinie și oraganizatorii programelor naționale și internaționale pentru accesarea cursurilor și stagiilor de pregătire în coloproctologie. De asemenea, SRCP are un rol important în realizarea echi-

pelor complexe pentru terapia optimă a pacienților cu asemenea afecțiuni, pentru creșterea adresabilității și accesibilității pacienților. Pentru un tratament optim ne dorim concentrarea cazurilor dificile în Centre de excelență iar organizarea acestora și recunoaștera lor este esențială. În aceste condiții, medicii implicați în îngrijirea pacienților vor ști care sunt indicațiile și contraindicațiile celor mai noi abordări pentru o anumită patologie coloproctologică și de asemenea, cu cine să colaboreze pentru managementul optim al pacienților. Societatea își are de asemenea ca obiectiv și realizarea contactelor cu Societățile Europene, cea de Coloproctologie (ESCP) și cea de Endoscopie digestivă (ESGE).
Anul acesta, cel de-al 12lea Congres National de Coloproctologie, va avea loc în perioada 11-13 Aprilie 2024 la Cluj Napoca iar cel de-al 43-lea Congres Național de Gastroenterologie, Hepatologie și Endoscopie Digestivă, va avea loc în perioada 27 – 29 iunie 2024 tot la Cluj-Napoca. Ce tematici cu noutate științifică vor fi prezentate, vor fi și speakeri străini și la ce participare fizică respectiv online vă așteptați?
În 2024 într-adevăr la Cluj-Napoca vor fi cele 2 congrese naționale în care vor fi implicați gastroenterologii și chirurgii. La ambele congrese vor fi atât speakeri români cât și străini cu participare fizică și on line.
Congresul Național de Coloproctologie va avea tematicile clasice discutate la toate congresele de coloproctologie internaționale: cancerul colonic, cancerul rectal, urgențele în coloproctologie, bolile inflamatorii intestinale, patologia funcțională și aici ca noutate este secțiunea de tulburări motorii de planșeu pelvin, patologia proctologică benignă care este extrem de variată; vor fi prezentări video cu tehnici endoscopice și chirurgicale; de asemenea, în ultima zi vor fi cursuri dedicate tehnicilor chirurgicale, ecografie de tub digestiv, curs de manometrie anorectală, de polipectomie și disecție endoscopică.
10 www.revistamedicalmarket.ro Gastroenterologie Interviu
O atenție specială am acordat anul acesta tehnicilor minim invazive. În acest sens, intervențiile laparoscopice și robotice pentru cancerele colonice sau rectale, cu indicații foarte clar conturate în prezent, ocupă un loc prioritar în tematica congresului. De asemenea, intervențiile minim invazive transanale pentru leziuni neoplazice și tehnicile noi endoscopice de rezecție și disecție pentru leziuni polipoide colorectale. Legat de aceste teme, diagnosticul complex efectuat de imagiști, endoscopiști și anatomopatologie este esențial. Calitatea rezecției endoscopice și chirurgicale ne preocupă foarte mult și de aceea am inclus în cadrul tematicii prezentări ale unor anatomopatologi recunoscuți dedicați acestei patologii.
Un subiect mai puțin discutat în cadrul altor congrese de coloproctologie este cel al afecțiunilor genetice (sindromul de polipoză colonică familială și sindromul Lynch). Geneticienii, gastroenterologii și chirurgii vor discuta abordarea acestor pacienți conform noilor ghiduri europene. Intervențiile chirurgicale ale acestor pacienți ridică probleme deosebit de complexe iar recunoașterea cazurilor și îndrumarea către centre specializate pentru managemnet sunt esențiale. Bolile inflamatorii intestinale (Boala Crohn și rectocolita ulcerohemoragică) aflate în creștere, ridică probleme deosebite de management, iar necunoaștera lor are efecte dezastruoase, mai ales datorită faptului că pacienții sunt de regulă tineri în plină activitate, iar aceste boli sunt incurabile; păstrarea remisiunii prin tratamente medico-chirurgicale în echipe complexe este esențială pentru o bună calitate a vieții pe termen lung. Atunci când este nevoie, intervențiile chirurgicale trebuie efectuate minim invaziv la acești pacienți; intervențiile chirurgicale sunt dificile, laborioase și necesită o pregătire specială.
Patologia de planșeu pelvin care afectează un număr mare de pacienți și implică tehnici de diagnostic laborioase a fost de asemenea mai puțin discutată în alte congrese de coloproctologie; tehnici cum sunt manometria anorectală, ecoendoscopia și rezonanța magnetică pentru sfincter anal ca și defecografia sunt puțin cunoscute din
nefericire. Din acest motiv cu ocazia congresului în afara mesei rotunde dedicate acestei patologii, am oraganizat în Clinica medicală și un curs practic de manometrie anorectală susținut de cei mai experimentați medici în acest domeniu și cu cel mai nou echipament pentru demonstrații.
Un alt curs teoretic și practic este dedicat ecografiei abdominale pentru afecțiuni de tub digestiv. Tehnica de ecografie abdominală cu aparatură dedicată și medic antrenat pentru această explorare (curba de învățare presupune efectuarea a cel puțin 200 de proceduri sub supravegherea unui expert) este considerat în momentul actual la nivel european o tehnică indispensabilă deoarece este puțin costisitoare, neinvazivă și frecvent repetabilă dacă afecțiunea de tub digestiv necesită acest lucru. Tehnica este utilizată pentru diagnosticul și urmărirea pacienților cu boli inflamatorii intestinale, diverticuloză/diverticulită, colită ischemică și obstrucție intestinală indiferent de cauză. În cadrul meselor rotunde de urgențe și boli inflamatorii intestinale, vor fi conferințe care vor evidenția rolul major al ecografiei de tub digestiv ca „point of care” pentru aceste afecțiuni.
În condițiile extensiei la nivelul întregii țări a programului de screening pentru cancerul colorectal, cursul teoretic și practic dedicat polipectomiei endoscopice și de asemenea mesele rotunde cu prezentări ce au ca temă polipectomia endoscopică vor fi extrem de utile pentru participanți. Echipa medico chirurgicală are un rol din ce în ce mai important în rezolvarea minim invazivă a pacienților cu polipi rectocolonici malignizați.
Chirurgii beneficiază de 2 cursuri unul de anastomoze laparoscopice și deschise și celălalt de rezecții transanale. O altă sesiune nouă în acest an este cea dedicată stomelor cu îngrijiri, tehnici chirurgicale și management al complicațiilor; vor fi implicați în această sesiune atât chirurgii cât și asistentele din cadrul Societății stoma care.
În legătură cu Congresul Național de Gastroenterologie și Hepatologie care se va desfășura la Cluj Napoca în iunie 2024, programul este complex,
cuprinde patologia digestivă în totalitate, afecțiuni de tub digestiv superior, inferior, intestin subțire, afecțiuni hepatice și pancreatice. Congresul se adresează în special medicului gastroenterolog care se confruntă cu o patologie complexă și variată atât de tub digestiv cât și hepato-bilio-pancreatică. Pentru specialistul gastroenterolog dedicat unei patologii restrânse, Societățile savante de gastroenterologie organizează și alte congrese dedicate, cum este cel de coloproctologie, cel de afecțiuni pancreatice (Bucharest PanacreticFest) cel de Boli inflamatorii intestinale (Congresul clubului român de Crohn și colită, RCCC) cel de hepatologie (Up to date in hepatology), cel de tulburări motorii (Congresul de neurogastroenterologie).
Care este situația programelor de profilaxie, supraveghere și de screening în cazul cancerelor digestive și colorectale în România?
Dintre cancerele digestive singurul care are un program de screening dedicat este cel colorectal.
Programul de „Prevenție, depistare precoce, diagnostic și tratament precoce al leziunilor precanceroase colorectale” sub acronimul ROCCAS, a început, așa cum se știe deja, ca un program pilot finanțat de Uniunea Europeană în 2019 (și s-a încheiat în decembrie 2023) în județele din sudul țării cu 4 centre coordonatoare ale screeningului (București cu 2 centre, Institutul Clinic Fundeni și Spitalul Militar Central, Craiova cu Universitate de Medicină și Farmacie și Constanța cu Spitalul Clinic Județean). Au fost incluse în screening persoane între 50 și 74 de ani asimptomatice și fără risc crescut în afara vârstei, și de asemenea persoane simptomatice și cu risc crescut familial sau personal; au fost testate prin teste imunochimice fecale (FIT) 50.000 persoane din cele 4 regiuni arondate (aproximativ 200.000 de persoane) și au fost trimise pentru colonoscopie persoanele FIT pozitive. La acești pacienți pozitivi au fost descoperite leziuni neoplazice la peste 50% (polipi adenomatoși și cancere în cea mai mare parte în stadii precoce); polipii au fost rezecați în momentul
11 Gastroenterologie 2024 - 2025 Interviu
colonoscopiei, în aceeași zi în peste 90% din cazuri.
În momentul actual suntem în faza de pregătire a programului pentru extensie la nivelul întregii țări și continuare în județele din sudul țării. Ca și în primul proiect, desfășurat între 2019 și 2023 vor fi oraganizate 2 etape; una educațională coordonată ca și în 2019 de Institutul Clinic Fundeni, în care se vor organiza cursuri pentru medicii de medicină generală, medicii specialiști gastroenterologi/ endoscopiști și anatomopatologi din întreaga țară (estimăm 800 de participanți) și o etapă/proiect de screening efectiv, cu centre dedicate de colonoscopie. Screeningul va fi coordonat de celelalte centre universitare din țară care nu au fost implicate în proiectul pilot inițial: Iași, Târgu Mureș, Cluj, Timișoara și va începe în județele arondate acestor centre universitare, foarte probabil în a doua parte a anului 2024.
Care sunt factorii de risc în apariția diverticulozei colonice?
În diverticuloza colonică factorii de risc sunt vârsta (la 60 de ani de exemplu aproximativ 60% din persoane au diverticuli), factorul genetic și evident alimentația. Legat de alimentație este cunoscut faptul că alimentația săracă în fibre vegetale (legume și fructe) predispune la apariția diverticulozei
colonice. Recomandarea este de a consuma zilnic începând din copilărie cel puțin cinci porții de legume și fructe. De asemenea este recomandată combaterea sedentarismului și a obezității. Pentru o evoluție nefavorabilă este indicată oprirea fumatului și tratamentul diabetului zaharat.
Managementul perioperator în IBD?
Managementul perioperator în bolile inflamatorii intestinale este esențial pentru succesul intervenției chirurgicale. Este necesar suportul psihologului pentru acceptarea intervenției și pentru atitudinea pozitivă și de asemenea pentru oprirea fumatului. Echipa multidisciplinară din cadrul Centrului de excelență în care trebuie admiși acești pacienți, stabilește managementul perioperator. În această etapă a afecțiunii în care se ia decizia intervenției chirurgicale rolul esențial îl au gastroenterologul, chirurgul și terapeutul intensiv și radiologul intervenționist. Trebuie să avem în vedere că mortalitatea corelată cu intervenția este pentru intervenția de urgență de 4-5% și 1% pentru intervenția electivă atât pentru boala Crohn cât și pentru rectocolita ulcerohemoragică. Morbiditatea postoperatorie poate fi datorată complicațiilor infecțioase (sepsis abdominal, abcese, fistule, infecții ale plăgii) sau non-in-
fecțioase (ileus, ocluzie, complicații ale stomei, incontinența fecală) sau inflamație a rezervorului - „pouchita” la cei cu proctocolectomie totală restaurativă pentru rectocolita ulcerohemoragică. Abcesele abdominale necesită drenaj preoperator sub ghidaj radiologic.
Pentru a evita/minimaliza aceste complicații este esențială cunoașterea indicațiilor ghidurilor de bună practică medicală: evaluarea statusului nutrițional și administrarea nutriției enterale și parenterale atunci când este necesar, administrarea de albumină la pacienții denutriți, cu valori scăzute ale abuminei service, administrarea de fier injectabil pentru pacienții anemici cu sideremie mică, oprirea administrării de cortizon cu cel puțin 4 săptămâni înainte. Este obligatorie administrarea de anticoagulante (heparina fracționată) înainte și după intervenția chirurgicală pentru profilaxia tromembolismului, complicație redutabilă la pacienții cu boli inflamatorii intestinale nespecifice moderat severe, în puseu de activitate datorită statusului procoagulant. Unele publicații extind perioada de administrare la 2 luni post operator pentru minimalizarea riscului tromboembolic. Deși au existat controverse legate de administrarea medicației biologice preoperator, în momentul actual, ghidurile permit această medicație până în apropierea actului chirurgical.

12 www.revistamedicalmarket.ro Gastroenterologie Interviu

Livrăm Sănătate. Oriunde.
www.ringdoc.ro





Consultații Video-Audio Securizate
Fără Abonament
Program Flexibil
Acoperire Malpraxis
Peste 11.000 de conturi de pacienți
Pla ormă de Telemedicină
care respectă 100% normele GDPR și Legea Telemedicinei din România cu normele sale






Tarife stabilite exclusiv de medic
Tarif diferențiat: consultație și control
Dosar Medical Electronic Pacient
Se pot înrola medici cu sau fără cabinet
Se pot înrola clinici și spitale
Accesilibilă de pe PC, iOS și Android

Înscrie-te Acum: contact@ringdoc.ro 0752 043 777





„Obezitatea
- una dintre epidemiile silențioase!“
Interviu realizat cu Doamna Prof. Univ.
Dr. Anca Trifan - Universitatea de Medicină și Farmacie „Grigore T. Popa“ din Iași, membru titular al Academiei de Științe Medicale

În peisajul manifestărilor științifice de anul acesta, vor avea loc Congresul Național de Coloproctologie 11-13 Aprilie 2024 la Cluj-Napoca și cel de-al 43-lea Congres Naţional de Gastroenterologie, Hepatologie și Endoscopie Digestivă 27-29 Iunie 2024 tot la Cluj-Napoca. Ce teme cu titlu de noutate veți prezenta?
Clujul este capitala gastroenterologiei în acest an. Programul este imaginat să ofere sprijin medicului specialist pentru managementul problemelor frecvent întâlnite dar și pentru a prezenta perspectivele care se deschid prin noile terapii și noile metode de diagnostic. Hepatita D, Bolile inflamatorii, urgențele, terapiile endoscopice moderne, problematica bolii hepatice cronice avansate de diferite etiologii, obezitatea sunt doar câteva din preocupările din acest an... Pe lângă informare, congresele medicale încearcă să atragă medicii specialiști în efortul pe care societățile profesionale îl fac pentru sensibilizarea decidenților din sănătate și a populației în general în privința
factorilor de risc care pot fi îndepărtați prin eforturi comune: consumul de alcool, alimente înalt procesate, sedentarismul. Am dori să creăm un mediu social favorabil sănătății.
Virusul Delta? Detaliați, vă rog.
În ultima decadă hepatologii au fost norocoși să poată trata eficient hepatita C și B. Sperăm că din acest an o nouă opțiune terapeutică va fi disponibilă și pentru hepatita D în România. Am vorbit puțin despre hepatita D până acum pentru că opțiunile terapeutice erau destul de limitate. Hepatita D afectează circa 8% dintre pacienții cu infecție virală B în România. Hepatita D este tipul de hepatită virală cu cel mai infaust prognostic, rata de progresie de la fibroză ușoară la ciroză cea mai rapidă, riscul de hepatocarcinom cel mai mare. De altfel, pacienții cu virus D sunt cel mai frecvent transplantați. Bulevirtida, un medicament antiviral nou, are șansa să producă un răspuns susținut biochimic și virusologic pe durata tratamentului, cu efecte foarte probabile pe evoluția bolii. Cu alte cuvinte riscul de ciroză, decompensare a cirozei și cancer hepatic va fi ameliorat. Mecanismul de acțiune este foarte interesant, bulevirtida împiedică pătrunderea virusului D în celula hepatică, prin blocarea receptorului, porții de intrare. Acest tratament a putut fi inventat datorită cunoașterii precise a replicării virale D. Existența acestui tratament și a altor antivirale care țintesc virusul D oferă șansa să tratăm eficient toate tipurile de hepa-
16 www.revistamedicalmarket.ro Gastroenterologie Interviu
tite cronice virale și să îndeplinim într-adevăr obiectivele OMS.
Care este situația cirozei hepatice în România raportat la Europa?
Într-un articol manifest publicat de Societatea Europeană de studiu al Ficatului (EASL) împreună cu Lancet, care are ca menire conștientizarea necesității unei schimbări de paradigmă în hepatologie, de la tratamentul complicațiilor bolii avansate de ficat (când opțiunile sunt limitate) la prevenție, diagnostic precoce și implicarea în societate pentru schimbări structurale care să transforme mediul în care trăim în unul care să promoveze sănătatea, este prezentată situația României de acum și prognoza pe viitorii ani; prevalența cirozei, mortalitatea prin ciroză este foarte înaltă și va continua să crească, la un nivel care depășește majoritatea țărilor europene. În rapoartele Hepahealth 1 și 2 (produse tot de EASL) România este pe primele 2 locuri prin mortalitate și pierdere de ani de viață activă din cauza cirozei. Intervenția activă este obligatorie. Prin programele LiveRO1 și 2 desfășurate în Sud sub coordonarea dnei Prof. Liana Gheorghe și în Nord de către mine, am influențat cu mare probabilitate prevalența bolii hepatice virale. Rămâne să lărgim câmpul de acțiune pentru alte etiologii și să ne alăturăm acțiunii propuse de EASL.
Va fi medicina personalizată, medicina viitorului?
Așa ar trebui. Așa și este de la Hipocrat. Nu există boli, ci bolnavi. Medicina modernă oferă deja posibilități de personalizare a tratamentului în cancere, când schemele terapeutice sunt modulate în funcție de receptori sau alte profiluri. Cred că omics-urile și inteligența artificială vor sprijini individualizarea medicinei. Momentan, medicul curant integrează datele furnizate de medicina prezentului și orientează managementul. Viitorul probabil va fi altfel. Sigur, scopul suprem va fi același, anume ameliorarea, vindecarea omului din fața noastră cu utilizarea tuturor resurselor posibile, fără alt fel de calcul! Așa ar fi ideal! Pe de altă parte, în boli frecvente este cost-efi-
cient să avem un tratament standard pentru toți și să obținem vindecarea. Acest fel de abordare este posibil în hepatita C unde una-trei pastile pe zi, 8-12 săptămâni pot vindeca aproape fiecare pacient, permițând eliminarea virusului prin tratament.
Frecvența bolilor inflamatorii intestinale este în creștere. Cum pot fi prevenite aceste boli și ce recomandări aveţi pentru pacienţii care suferă de boli inflamatorii intestinale?
Greu de răspuns la această întrebare. Pentru a preveni trebuie să știi cauza exactă. BII sunt afecțiuni multifactoriale a căror patogeneză nu este pe deplin elucidată; se consideră că sunt implicați factori imuni, microbiota intestinală, modificatori endogeni care inițiază și întrețin inflamația. De asemenea, rolul factorilor de mediu este susținut de creșterea incidenței patologiei în regiuni cu incidență scăzută, condiții predispozante precum dieta săracă în fructe, legume și fibre, bogată în grăsimi saturate, alimente semipreparate și preparate tip fast-food fiind condiții predispozante documentate.
Pacienții cu BII trebuie să ia conducerea în monitorizarea bolii, deoarece PRO (patient reported outcomes) sunt cele mai precoce și importante ținte terapeutice și nicio modificare a planului terapeutic nu se poate face fără ca aceștia să fie implicați. Trebuie să fie informați, să înțeleagă principiile de bază ale tratamentului și să-și asume alături de medici ceea ce este puțin controlabil. Consider că pacienții trebuie să fie îngrijiți de medici dedicați, capabili de angajament pe termen lung, care să aibă abilitatea de a însoți bolnavii pe un drum nu întotdeauna ușor, cu posibile acutizări, complicații, chirurgie. Sfătuiesc pacienții să-și aleagă un astfel de medic cu care să poată comunica. Sunt sigură că numeroasele terapii noi, inovatoare, fiecare cu alt mecanism de interferare a inflamației, vor putea în cele din urmă să ofere fiecărui pacient în parte șansa vindecării profunde și poate și a clearence-ului bolii.
Cum aţi descrie evaluarea hemoragiei digestive de cauză intestinală?
Dacă vă referiți la hemoragia digestivă care-și are originea în intestinul subțire, numită și intermediară, este mai dificil de diagnosticat. Astăzi avem însă videocapsula endoscopică, angio CT-ul, scintigrafia cu eritrocite marcate și enteroscopia care reușesc să identifice și uneori chiar să trateze leziunea sângerândă. Când metodele clasice (endoscopia bidirecțională, adică superioară și inferioară) nu reușesc să identifice originea unei hemoragii trebuie rapid trimis pacientul către centre ce pot efectua celelalte tehnici. Nu cred că răspunsul nu putem, nu avem poate fi acceptat. Sistemul medical românesc de stat este unul articulat, ierarhizat, unde trimiterea către centrul de competență superioară se poate face imediat dacă interesul pacientului o cere. Deși căutarea cauzei unei hemoragii intermediare poate fi frustrantă uneori, identificarea cauzei și eventuala vindecare a pacientului aduce satisfacții profesionale medicului curant.
Cum este reflectată obezitatea în România și ce terapii contra obezităţii puteţi enumera?
Una din epidemiile silențioase la care omenirea trebuie să facă față este obezitatea. Dacă mergem pe stradă sau vedem copii care ies din școli vedem o creștere a obezității care va aduce probleme viitoare. Obezitatea este factor de risc pentru boli cardio-vasculare, diabet zaharat, steatohepatita cu risc de ciroză, cancere cu diverse localizări (sân, colon, pancreas, ficat, esofag etc.). Obișnuiam să punem pe umerii pacienților terapia obezității. Recomandam dieta și așteptam rezultatele sau eșecul de care pacientul era vinovat. S-a produs o schimbare de concept în tratamentul obezității și s-a luat de pe umerii pacientului întreaga responsabilitate. Astăzi, obezitatea este considerată o boală cronică cu tratament permanent. Sunt soluții terapeutice medicamentoase și există și metodele de chirurgie bariatrică. Alegerea metodei adecvate necesită o judicioasă cântărire a riscurilor și beneficiilor și asigurarea că pacientul este compliant. Medicina obezității s-a schimbat radical în ultimii ani și medicii trebuie să cunoască și să ofere pacienților toate opțiunile disponibile.
17 Gastroenterologie 2024 - 2025 Interviu
Un mesaj pe care mai ales medicii
tineri trebuie să-l aibă în vedere!
Este important ca medicii să-şi păstreze abilitățile clinice chiar şi în condițiile unei avalanşe de mijloace de investigații moderne. Chiar şi în țări mult mai tehnologizate ca noi, cum este SUA, competențele şi abilitățile clinice sunt la mare cinste, nu se pierd din vedere şi nu se pune niciodată un diagnostic doar pe baza unor analize. Medicina este profesia care leagă pacientul de medic şi nu ar trebui pusă nicio barieră în comunicarea dintre aceştia.

Prof. Univ.
Dr. Dan Dumitrașcu
(UMF Iuliu Hațieganu Cluj-Napoca, șef secție Interne III-Medicala 2, Spitalul Clinic Județean de Urgență, Cluj Napoca, Societatea Română de Neurogastroenterologie (președinte de onoare), Societatea de Medicină Biopsihosocială (președinte), Academia de Ştiințe Medicale (membru titular), Past-Chairman al Comitetutului
Societăților Național al Uniunii Europene de Gastroenterologie, Director-at-large al Comitetului
Exectiv al Organizaţiei Mondiale de Gastroenterologie
Am solicitat doctorului Dan Dumitrașcu o opinie referitoare la o chestiune care frământă comunitatea medicilor gastroenterologi din România.
Prof. univ. dr. Dan Dumitrașcu: Una dintre preocupările importante ale colegilor practicieni gastroenterologi este accesul la noile tehnici și proceduri de investigație. Într-adevăr, în ceea ce privește gastroenterologia și hepatologia am asistat în ultimii ani la o explozie de posibilități de investigare, care conduc către microcosmos capacitatea de a cunoaște structura și funcțiile aparatului digestiv și patogeneza multora dintre boli. În aceste condiții, există dorința justificată de a apela în activitatea practică la cele mai noi posibilități de investigație. Și atunci, problema care se ridică este următoarea: se pierde cumva relația dintre clinician și pacient atunci când tentația investigațiilor moderne este atât de mare?
Noi, la facultate învățăm pe studenți și pe rezidenți că niciodată diagnosticul și apoi indicațiile terapeutice nu se fac fără o bună evaluare clinică a cazului, și care înseamnă anamneză, urmată de examenul clinic general, specific pentru aparatul afectat al pacientului.
Din păcate, în ultimii ani asistăm la o diluare a rigurozității examenului clinic. Pe de o parte, fiind mulți studenți, accesul la practică pe pacienți se îngreunează, există secții inundate de studenți și rezidenți, masteranzi și doctoranzi, dar pe de altă parte există și un oarecare dezinteres față de medicina clasică, în care contactul cu pacientul era primordial. Sigur, trebuie să fim realiști, așa cum toată societatea evoluează, medicina evoluează și ea. Nu mai învățăm simptomele pe care le mai întâlnim doar în cărțile medicale folosite cu generații în urmă. Pe vremea aceea, capacitatea de cunoaștere a organismului era mai restrânsă și atunci semnificația care se dădea manifestărilor clinice, subiective sau obiective era mult mai mare. Iată motivul pentru care în manuale medicale de acum 50-70-100 de ani vom întâlni tot felul de semne și de manifestări ale unor boli cărora acum abia dacă le mai dăm o semnificație. Pot să înțeleg că ponderea examenului clinic în ziua de astăzi s-a redus, pentru că noi beneficiem azi de posibilități pe care înaintașii noștri nu le aveau, dar pot de asemenea să afirm că examenul clinic este în prezent subutilizat. Atunci când nu aveai la îndemână posibilitățile de investigații de azi, trebuia să ai un simț clinic mult mai dezvoltat și să ai un contact prelungit cu pacientul. Când eu am început activitatea medicală abia se introducea ecografia, erau foarte puține centre în care se practica endoscopia, pasajul cu bariu era sfânt iar arborele biliar se investiga cu substanță iodată de contrast. Azi nu se mai face medicină în acest fel, spre norocul nostru! Pe de altă parte însă, pacienții discutau mai mult cu medicii curanți, care aveau două ore de contravizită după-amiaza și 5 ore de consult dimineața, deci expunerea directă a pacientului în fața medicului era mult mai mare. Marele chirurg german Christian Albert Theodor Billroth spunea recent glumind că ”pacientul așteaptă pentru vizita zilnică a medicului, pentru că aceasta a ajuns să
fie evenimentul la care se concentrează toate gândurile și emoțiile sale”.
Deci, unde este problema? Având mulți studenți, multe serii iar numărul de pacienți în paturile de spital același, contactul studentului viitor clinician cu pacientul se reduce. Așa se face că accesul la cunoașterea și deprinderea tacticilor de examen clinic se alterează și în acest fel, generațiile mai noi de medici pun tot mai puțin accentul pe examenul clinic. Totodată, se reduce din ce în ce mai mult gândirea clinică și se insistă mai mult pe investigații, care pot fi din produse biologice, investigații imagistice, inclusiv de medicină nucleară și investigații endoscopice. Progresele tehnologice sunt importante însă ajungem la un paradox. Căutarea bolii, cauzelor sale, în vederea stabilirii unui tratament corect se face fără a se mai trece prin filtrul examenului clinic și al gâmdirii clinice. Observăm o mulțime de analize care se fac în mare abundență și care au rezultat negativ. Pentru că analizele nu se mai fac cu scopul de a îți confirma sau infirma o suspiciune clinică ci se fac ca un fel de screening la cererea pacientului. S-a ajuns să se ofere pacienților ”pachete de markeri tumorali” la ofertă! Păi unde suntem, la Supermarket? Totodată, s-a schimbat și mentalitatea pacienților, care merg uneori să-și facă analize ”la ofertă” cu care apoi merg la medic și-l întreabă ce părere are.Mie nu o dată foști pacienți sau cunoștințe sau prieteni îmi trimit pe whatsapp analize nesolicitate, pentru care au plătit niște bani și îmi solicită consultații pe baza acestora, fără să-i consult. Sunt pus să interpretez niște analize pe care nu i le-am cerut pacientului și nu știu de ce și le-a făcut. Sunt exemple nenumărate de cazuri pe care le văd zilnic,în care pornind de la un rezultat al unei explorări nesolicitate de medic și ruptă de contextul clinic, se declanșează o avalanță de alte investigații imagistice, radiologice, endoscopice, biochimice, imunologice care nu duc la nicio concluzie.
18 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
Elite InGenius® este o soluție ușor de utilizat, de la probă la rezultat, dedicată diagnosticului molecular, care integrează extracția, amplificarea și interpretarea rezultatelor cu o flexibilitate fără precedent și o posibilitate de meniu de analiză.
Elite InGenius® proceseză 1 până la 12 probe în canale paralele și independente
Elite InGenius® oferă laboratoarelor o capacitate de meniu nelimitată, combinând cel mai mare meniu de boli infecțioase CE-IVD disponibil pe un instrument de la probă la rezultat.

Infecțiile gastrointestinale (GI) pot fi cauzate de o mare varietate de virusuri, bacterii sau paraziți. Cazurile acute de diaree reprezintă o cauză majoră de morbiditate și mortalitate la nivel mondial, în principal la copiii mici (mai ales dacă sunt malnutriți), la vârstnici și la imunocompromiși. Metodele convenționale de diagnosticare prezintă numeroase provocări, inclusiv inconsecvențe notabile, sensibilitate inadecvată, procese laborioase și timpi de execuție îndelungați. Mai recent, s-a pus din ce în ce mai mult accentul pe diagnosticele multiplex bazate pe PCR în timp real, datorită numeroaselor sale avantaje, cum ar fi detectarea simultană a unei game largi de agenți patogeni ai infecțiilor gastrointestinale, rezultate rapide și fiabilitate sporită atunci când sunt amalgamate cu platforme automatizate.
Panel teste
Kit 1 Kit 2 Kit 3 Kit 4 GI Bacterial PLUS GI Viral PLUS GI Norovirus PLUS GI Parasitic PLUS
Este necesară colonoscopia la pacienții cu sindrom de intestin iritabil?
Sindromul de intestin iritabil afectează semnificativ calitatea vieții pacienților, care deja sunt împovărați de teste multiple, majoritatea inutile, de pierderea timpului cu pregătirea pentru investigații, de efectele semnificative legate de sedare şi de costurile financiare directe. Cu toate acestea, sunt mulți pacienți cu sindrom de intestin iritabil care, în loc să se concentreze pe controlul simptomelor reale, continuă să fie preocupați de condiția medicală, pe care o consideră potențial gravă, sau chiar fatală. În prezentările clinice, asemănările cu o serie de boli organice precum boala Crohn, colita ulcerativă, boala celiacă dar mai ales teama de cancer care nu poate fi depăşită, mulți pacienți dar şi medici, apelează la teste invazive pentru a exclude o boală organică, înainte de a confirma un diagnostic de sindrom de intestin iritabil. În lipsa unor teste diagnostice noninvazive, care să ofere un diagnostic fiabil şi reproductibil al sindromului de intestin iritabil, cu un raport de probabilitate pozitiv suficient de mare şi o valoare de probabilitate negativă suficient de scăzută, colonoscopia rămâne una dintre explorările cele mai solicitate.

Opinia pacienților despre colonoscopie în sindromul de intestin iritabil
Raportat la explorarea colonoscopică, atitudinea pacienților cu sindrom de intestin iritabil este mult influențată de rezultatul investigației. Pentru un pacient o colonoscopie negativă, fără evidența unei afecțiuni organice, pe lângă certificarea diagnosticului de sindrom de intestin iritabil generează și un impact pozitiv asupra calității vieții și a gradului de satisfacție. În plus, contribuie la evitarea expunerii la investigații și riscuri suplimentare, precum și la economisirea resurselor corespunzătoare cerințelor standard de management non-invaziv al sindromului de intestin iritabil. Pentru un pacient o colonoscopie pozitivă pentru diferite tipuri de leziuni nonmaligne asociate sindromului de intestin iritabil, precum polipii sau diverticulii, generează neîncredere în certitudinea diagnosticului și insatisfacție față de serviciile medicale. Opinia medicală despre colonoscopie în sindromul de intestin iritabil
În mod tradițional, diagnosticul unei boli este realizat prin obiectivarea anomaliilor anatomice sau funcționale. Sindromul de intestin iritabil este o condiţie medicală în care se încearcă să se schimbe paradigma diagnosticului de la una de diagnostic prin excludere, la un proces de diagnostic proactiv, bazat pe un sistem de încadrare a simptomelor. În absența unor markeri biologici specifici, sindromul de intestin iritabil este confirmat ca o tulburare funcțională numai după ce bolile organice gastro-intestinale au fost excluse printr-o serie exhaustivă de teste diagnostice. În multe cazuri, aceaste evaluări includ colonoscopia, care este una dintre cele mai costisitoare investigații diagnostice.
În practica clinică curentă, majoritatea doctorilor tind să stabilească diagnosticul de sindrom de intestin iritabil după experiența
personală, conturată pe o serie de teorii informale și opinii despre ce este această afecțiune și nu după definițiile științifice de manual sau preluate din ghiduri. Acest tip de experiență clinică nu generează o atitudine unitară a medicilor implicați în managementul pacienților cu sindrom de intestin iritabil. Spre exemplu, un medic generalist care are nevoie de un suport informațional în conformitate cu standardele de diagnostic pentru sindromul de intestin iritabil, recomandă frecvent colonoscopia, în timp ce un clinician este înclinat să considere că simptomele pacientului sunt previzibile sau foarte probabile pentru un diagnostic cauzat de schimbări anatomice și nu de o tulburare funcțională. Specialistul în gastroenterologie pare a fi mai prudent și reflectează mai mult cu privire la orientarea asupra tipului de management invaziv sau noninvaziv la caz. Pro și contra colonoscopiei în sindromul de intestin iritabil
Susţinătorii investigației afirmă că o colonoscopie normală, fără leziuni, poate oferi asigurări de certitudine pentru diagnosticul de sindrom de intestin iritabil, contribuind ulterior la scăderea utilizării resurselor sau extinderea investigațiilor diagnostice, precum și la îmbunătăţirea satisfacţiei și calității vieții pacienților.
Oponenții investigației, pornesc de la considerentul că pre-testarea prin colonoscopie pentru simptome asemănătoare cancerului colorectal, bolilor inflamatorii intestinale, diareei infecțioase este cu o probabilitatea mai mică de 1% pentru diagnostice alternative. De altfel, colonoscopia în foarte puține cazuri modifică diagnosticul inițial, iar un diagnostic cert de sindrom de intestin iritabil este rareori revizuit în timp.
Având în vedere că explorarea rareori se dovește a fi utilă, recomandarea de a efectua colonoscopia în sindromul de intestin iritabil la un minim necesar ar trebui contrabalansată de eforturile de transfer a resurselor (financiare, profesionale) în zone unde este mai multă nevoie, cum ar fi screeningul pentru cancerul colo-rectal.
Colonoscopia modelează profilul de complianță și aderență a pacienților cu sindrom de intestin iritabil?
Pacientul cu sindrom de intestin iritabil este cu un profil de complianță și aderență care se raportează la impactul pe care boala îl are asupra calității vieții. Pacienţii complianți sunt cei care își acceptă diagnosticul de sindrom de intestin iritabil, respectă recomandările stabilite de medicii lor, nu sunt tentați de a solicita investigaţii suplimentare, colonoscopia nu reprezintă o preocupare sau o prioritate, au un grad de satisfacție bun și acceptă faptul că vor fi zile bune și zile rele.
Pacienţii mai puțin complianți, percep sindromul de intestin iritabil ca o boală cu impact negativ asupra calităţii vieţii, sunt nemulțumiți de persistența simptomatologiei și de eficiența suboptimală a tratamentului, încât sunt tentați spre investigații suplimentare. În ceea ce privește colonoscopia, în multe situații investigația devine o prioritate, în special pentru pacienții care nu acceptă ideea că nu este nimic rău sau că nu sunt în dezavantaj.
În concluzie, dacă la colonoscopie este puțin probabil să se descopere diagnostice alternative, să se detecteze leziuni incidente importante din punct de vedere clinic sau să liniștească pacientul, atunci se pare că nu există niciun motiv științific pentru o recomandare curentă de a efectua această procedură, în special la pacienții tineri, care prezintă simptome tipice de sindrom de intestin iritabil.
Bibliografie
1. Mahadeva S. Improving adherence towards bowel preparation for colonoscopy. JGH Open. 2023 Sep 23;7(9):597-598.
2. Amber J. Tresca, Colonoscopy and Irritable Bowel Syndrome (IBS): What to Know. Updated on February 28, 2024 https://www.verywellhealth.com/colonoscopy-irritable-bowel-syndrome-8558879
3. Black CJ, Ford AC. Rational investigations in irritable bowel syndrome. Frontline Gastroenterol. 2019 Jun 6;11(2):140-147.
4. Du X, Allwood G, Webberley KM, Inderjeeth AJ, Osseiran A, Marshall BJ. Noninvasive Diagnosis of Irritable Bowel Syndrome via Bowel Sound Features: Proof of Concept. Clin Transl Gastroenterol. 2019 Mar;10(3):e00017.
5. Otto S. Lin, Colonoscopy in irritable bowel syndrome: whom are we reassuring? Gastrointestinal Endoscopy Volume 62, No. 6 : 2005:900-902.
6. Spiegel BM, Gralnek IM, Bolus R, Chang L, Dulai GS, Naliboff B, Mayer EA. Is a negative colonoscopy associated with reassurance or improved health-related quality of life in irritable bowel syndrome? Gastrointest Endosc. 2005 Dec;62(6):892-9.
20 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
Prof. Univ. Dr. Elena Toader
Medic primar gastroenterologie și medicină internă, UMF„Grigore T. Popa” Iași, Institutul de Gastroenterologie și Hepatologie, Spitalul Clinic Județean de Urgență„Sfântul Spiridon”
Polibioticul cel mai puternic din lume
miliarde de bacterii


· Un amestec concentrat de 90 de miliarde de bacterii vii într-o singură doză
Aceleași 8 tulpini bacteriene într-o combinație echilibrată
· Un plus de eficiență prin vitamina D, care contribuie la funcționarea normală a sistemului imunitar
30 de capsule - pentru 30 de zile!
H I L I B R U L M I C R O B I O T E I D I G E S T I V E
E N Ț I N E E C H I L I B R U L microbiotei și C O N S O L I D E A Z Ă rezultatele!
(450
vii provenind din 8 tulpini) R E S TA B I L EȘT E E C
NOU! M
Poate fi comandat online la w www.diamondlily.ro

8 tulpini bacteriene:
B. animalis subsp. lactis B L 03, S. thermophilus B T 01, B. animalis subsp. lactis B I 04, L. plantarum B P 06, L. acidophilus B A 05, L. paracasei B P 07, L. helveticus B D 08, B. breve B B 02.
Ingrediente: amestec de bacterii lactice liofilizate și bifidobacterii, amidon de porumb, capsulă vegetală (hidroxipropilmetilceluloză), colecalciferol (vitamina D3), agent antiaglomerant: E470b
Doza zilnică recomandată: 1 capsulă pe zi! Nu depășiți doza zilnică recomandată!
A nu se utiliza dacă capsula este deteriorată A nu se lăsa la vederea și îndemâna copiilor mici Dacă sunteți însărcinată, alăptați, aveți alte probleme medicale sau luați medicamente, consultați-vă cu medicul înainte de utilizare
Depozitare: A se păstra la loc uscat și răcoros, la temperatura camerei (până la 25°C)
Doza zilnică recomandată: 1 - 2 plicuri (adică 4,4 – 8,8 g) pe zi! A se dizolva conținutul plicului în apă, iaurt, suc de mere sau altă băutură rece necarbogazoasă și a se consuma imediat A nu se depăși doza recomandată pentru consumul zilnic În unele cazuri, este posibil să apară balonarea intestinală în primele zile de utilizare a V S L#3, acesta fiind un fenomen normal Nu este destinat copiilor sub 3 ani A nu se lăsa la vederea și îndemâna copiilor
Depozitare: V S L#3 păstrat la frigider (2 până la 8°C) poate fi utilizat până la data indicată pe ambalaj. Poate fi păstrat la temperatura camerei (< 25°C) timp de 7 zile fără ca proprietățile sale să fie afectate.
V S L#3 și V S L# Balance sunt suplimente alimentare și nu înlocuiesc o dietă variată și echilibrată și un stil de viață sănătos. Nu conțin gluten sau lactoză.
Certificate de Notificare:
V S L#3: A A 10499 / 2017
Ingrediente: maltoză, bacterii lactice liofilizate și bifidobacterii, amidon de porumb, agent antiaglomerant: silice Notificate în Romania de ADEXILIS srl, Calea Moșilor 199/25, București
V S L#Balance: A D 3591 / 2022
VSL#3 și VSL#Balance sunt produse în Italia, fiind mărci comerciale înregistrate ale Actial Farmaceutica srl

www.diamondlily.ro



Microgranule cu eliberare prelungită, 80% acționând la nivelul colonului5,6,7
Pentasa 500 mg, 1 g, comprimate cu eliberare prelungită. Pentasa 2g granule cu eliberare prelungită. Indicații terapeutice: Colita ulceroasă, Boala Crohn.
Pentasa supozitoare 1000 mg. Indicație terapeutică: Proctita ulceroasă8
Efect terapeutic independent d e n ivel u l p H -u l u i 4 • De Lungă Durată2 • Rapidă1 • Susținută1 Administrare UNICĂ pe zi în cazul pacienților cu BII1,3 Remisiune Referințe: 1. Flourie B et al. Aliment Pharmacol Ther. 2013; 2. Dignass AU et al. Clin Gastroenterol Hepatol. 2009; 3. Pentasa 500 mg comprimate cu eliberare prelungită - Rezumatul caracteristicilor produsului, Septembrie 2019; Pentasa 1g comprimate cu eliberare prelungită - Rezumatul caracteristicilor produsului, Septembrie 2019; Pentasa 2g granule cu eliberare prelungităRezumatul caracteristic lor produsului, Septembrie 2019. 4. Hardy JG, et al. J Clin Pharmacol 1993;33:712-718. 5. Layer PH, et al. Gastroenterology 1995;108:1427-1433. 6. Rasmusse SN, et al. Gastroenterol 1982;83:1062-1070. 7. Christensen LA, et al. Aliment Pharmacol Ther 1990;4:523-533. 8. Pentasa supoz toare 1000 mg - Rezumatul caracteristicilor produsului, Februarie 2016. Acest material promoțional este destinat profesioniștilor din domeniul sănătății Pentru informații suplimentare, consultați Rezumatul Caracteristicilor Produsului disponibil la cerere sau pe website-ul www.anm.ro Aceste medicamente se eliberează pe bază de prescripție medicală P6L Ferring Pharmaceuticals România S.R.L. Str. Independenței nr. 2, camera 3, 300207 - Timișoara, jud. Timiș Tel: +40 356 113 270, Fax: +40 356 113 278 www.ferring.ro RO-GAS-2200002
Cum putem preveni decompensarea cirozei hepatice?
Prevalența și mortalitatea asociate cu ciroza hepatică (CH) continuă să crească în ciuda îmbunătățirii cunoștințelor și a îngrijirii medicale. Conform datelor din Statele Unite, numărul anual de decese legate de CH a crescut cu 65%, în timp ce numărul de spitalizări pentru CH aproape s-a dublat într-un deceniu (1). Conform ultimelor date ale OMS publicate în 2020, decesele în România atribuite bolilor hepatice au ajuns la un număr de 8.920 sau 3,82% din numărul total al deceselor. În țara noastră, ciroza hepatică este a 4-a cauză de deces la bărbați (61/100.000) și a 6-a cauză de deces la femei (31/100.000) (2) .




CProf. Univ.
Dr. Anca Trifan
UMF ,,Grigore T. Popa” din Iași, membru titular al Academiei de Ştiințe Medicale
Prof. Univ.
Dr. Carol Stanciu
Universitatea
de Medicină și Farmacie
„Grigore T. Popa” din Iași
As. Univ.
Dr. Laura Huiban
Universitatea de Medicină și Farmacie
„Grigore T. Popa” din Iași
As. Univ. Dr. Raluca
Ioana Avram
Universitatea de Medicină și Farmacie
„Grigore T. Popa” din Iași
iroza hepatică a fost în mod tradițional privită ca o entitate cu un continuum de grade crescânde de severitate până la moarte sau transplant hepatic. Recent, aceste paradigme s-au schimbat, ducând la recunoașterea CH ca o afecțiune eterogenă cu prognostic diferit în diferitele stadii (3). Indiferent de etiologie, cel mai important factor de prognostic pentru supraviețuire este prezența sau absența decompensării hepatice, definită prin apariția ascitei,
hemoragiei variceale, encefalopatiei hepatice și/sau icterului (4). Deși pacienții cu ciroză hepatică pot rămâne în stadiul compensat pentru o perioadă lungă de timp, mai ales dacă factorii de risc subiacenți sunt atenuați, aproximativ 11% dintre cei cu boală compensată experimentează noi decompensări în fiecare an (5), iar progresia de la ciroza compensată la ciroza decompensată este considerată un punct de cotitură semnificativ în progresia cirozei, deoarece semnalează o scădere drastică a ratelor medii de supraviețuire de la 1012 ani la doar 1-2 ani (5)
Ciroza hepatică a fost mult timp văzută ca stadiul final al bolii hepatice cronice. Cu toate acestea, această percepție a început să se schimbe în ultimele două decenii. Wanless et al. (6) au fost primii care au descris inversarea CH, iar de atunci numeroase serii de pacienți cirotici cu diverse etiologii au demonstrat același lucru (6). În ciuda faptului că sunt asimptomatici, între o treime și jumătate dintre pacienții cu CH compensată au varice și hipertensiune portală semnificativă clinic (CSPH) la momentul diagnosticului (7) De-a lungul timpului, pacienții cu CH compensată dezvoltă mai mulți factori de risc care le cresc susceptibilitatea la decompensarea clinică, cum ar fi creșterea presiunii la nivelul venei porte, inflamația sistemică și modificările hemodinamice. În plus, anumiți factori declanșatori, inclusiv infecția bacteriană, medicamentele sau alcoolul, pot precipita în mod acut decompensarea. Atunci când cauza de bază a CH
compensate este eliminată devreme, o proporție semnificativă de pacienți experimentează regresia cirozei (8) .
Dincolo de povara pe care o are asupra sănătății pacienților și a calității vieții, ciroza hepatică reprezintă, de asemenea, o provocare în domeniul sănătății. Costurile sunt suportate în mod disproporționat în managementul complicațiilor în rândul celor cu boală decompensată. Recent, strategiile de management au evoluat de la concentrarea în primul rând pe modificarea factorilor de risc și tratamentul complicațiilor, către prevenirea decompensării hepatice la pacienții cu risc ridicat de decompensare (9) .
Istoria naturală a pacienților cu ciroză hepatică compensată
Progresia naturală a cirozei este caracterizată printr-un continuum de la o fază compensată asimptomatică la o fază de decompensare simptomatică. Rata de trecere de la o etapă compensată la una decompensată este de aproximativ 5%-7% în fiecare an (10). Rata mortalității la 5 ani în ciroza compensată fără sau cu varice este de 5%, respectiv 10% (11). Există mai mulți factori cunoscuți asociați cu decompensarea, cum ar fi presiunea portală ridicată, leziunea etiologică persistentă, inflamația sistemică și modificările hemodinamice. În plus, mai multe
24 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
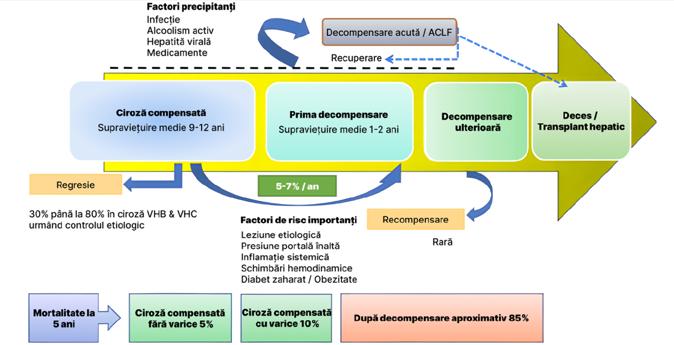
tipuri de evenimente declanșatoare, cum ar fi infecția bacteriană, alcoolul, hepatita virală sau medicamentele, pot provoca decompensare acută și insuficiență hepatică acută pe cronică (ACLF) (11). Controlul prompt și eficient al factorilor etiologici este asociat nu numai cu regresia cirozei compensate, ci și cu recompensarea cirozei decompensate (12)
Factorii asociați cu decompensarea cirozei hepatice compensate
Tranziția de la stadiul compensat la cel decompensat al cirozei hepatice are loc ca urmare a unei interacțiuni complexe între factorii predispozanți și cei precipitanți (Tabel 1). Hipertensiunea portală (HTP) este principalul determinant al progresiei cirozei hepatice către decompensarea clinică.
Pe măsură ce gradientul de presiune venoasă hepatică (HVPG) crește peste 10 mmHg, ceea ce înseamnă „hipertensiune portală semnificativă clinic” (CSPH), riscul de decompensare începe să crească.
Strategii de prevenire a decompensării cirozei hepatice
Tot mai multe dovezi sugerează că abordarea cauzei de bază a cirozei hepatice și reducerea HTP de către BBNS au impact pozitiv asupra istoriei naturale a pacienților cu CH compensată. Strategiile eficiente de tratament care modifică boala ar putea include: (1) Eliminarea factorilor etiologici; (2) Terapie orientată pe fiziopatologia cirozei; (3) Managementul factorilor agresivi precum obezitatea, DZ, dislipidemia și alcoolismul; (4) Terapii antifibrotice
Tabel 1. Factori asociați cu decompensarea cirozei hepatice compensate
Factori de risc pentru decompensarea non-acută
Septuri fibroase groase și micronodularitate la biopsie hepatică
Leziuni hepatice persistente prin factor etiologic
Hipertensiune portală
Inflamație sistemică și modificări hemodinamice
Factori de risc metabolici: DZ, obezitate și dislipidemie
Factori genetici de risc: genotipul PNPLA3 G/G
și regenerative; (5) Eliminarea factorilor precipitanți care conduc la decompensarea acută/ACLF.
Eliminarea factorilor etiologici. Principala condiție prealabilă pentru regresia fibrozei este încetarea agresiunii la nivel hepatic, care se realizează prin controlul terapeutic al factorilor cauzali. Într-o revizuire sistematică a 463 de pacienți cu ciroză VHB, regresia cirozei hepatice a fost observată la 33% până la 80% dintre pacienți după supresia virală susținută (13). Între timp, CH a regresat la 33% până la 100% din 58 de pacienți cu ciroză VHC după RVS (14). Acest lucru sugerează că, odată ce elementul cauzal este îndepărtat precoce în stadiul compensat al cirozei, progresia este oprită și regresia cirozei apare la un număr semnificativ de pacienți.
Pierderea în greutate prin modificări ale stilului de viață îmbunătățește fibroza la pacienții cu steatohepatită nonalcoolică (NASH), dar efectele acesteia asupra cirozei NASH în sine sunt încă puțin înțelese. Într-un studiu publicat recent, care a implicat 709 pacienți cu ciroză NASH compensată privind simtuzumab și selonsertib față de placebo, regresia CH a fost observată la 135 de pacienți în timpul unei urmăriri mediane de 16,6 luni (15). În special, impactul medicamentului nu a fost mai bun decât placebo, indicând influența modificării stilului de viață (15). Un alt studiu care a evaluat efectele pe termen lung ale chirurgiei bariatrice la 180 de pacienți obezi cu NASH a constatat o regresie semnificativă a fibrozei la 5 ani după operație. Fibroza a scăzut la 70,2% dintre pacienți, a dispărut la 42,0% dintre pacienți și 33,0%
Factori precipitanți pentru decompensarea acută
Infecții bacteriene
Consumul persistent de alcool
Hemoragie gastrointestinală
Consumul de medicamente hepatotoxice
Suprainfecție sau apariție a hepatitei virale
Chirurgie majoră și anestezie generală
26 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie

dintre pacienții cu CH inițial au devenit non-cirotici (16)
Abstinența de la alcool îmbunătățește prognosticul în toate etapele CH legate de alcool. Într-un studiu, pacienții care au fost abstinenți au prezentat o probabilitate de decompensare pe 3 ani de 32,4% față de 60,0% pentru cei care au continuat să consume alcool (17). Abstinența precoce la alcool după diagnosticul de CH s-a dovedit a fi un predictor semnificativ în supraviețuire, pacienții abstinenți având o rată de supraviețuire de 72% la 7 ani, comparativ cu 44% la pacienții care au continuat să consume alcool (18). Reversibilitatea fibrozei hepatice a fost documentată și la pacienții cu hepatită autoimună. Un studiu asupra hepatitei autoimune tratate cu corticosteroizi a evidențiat regresia CH histologică de la 16% la 11% (19). Tratamentul cu acid ursodeoxicolic poate opri progresia bolii și poate îmbunătăți supraviețuirea pacienților cu colangită biliară primară, dar pare a fi mai puțin eficient în promovarea regresiei fibrozei (20). Într-o analiză retrospectivă a pacienților cu hemocromatoză tratați cu venesecție, regresia CH a fost observată la 15 din 66 (23%) pe o perioadă mediană de 9,5 ani (21)
Terapie orientată pe fiziopatologia cirozei. La pacienții cirotici, CSPH este un factor fiziopatologic important al primului eveniment de decompensare. Conform recomandărilor actuale, pacienții cu varice cu risc ridicat ar trebui să aibă BBNS sau ligatura variceală endoscopică (LVE) ca profilaxie primară pentru hemoragia variceală. Atunci când trebuie optat între BBNS și LVE, trebuie luate în considerare preferințele pacientului, toleranța, profilul efectelor secundare și contraindicațiile (22) Important, BBNS, pe lângă faptul că este la fel de eficient ca LVE în prevenirea hemoragiei variceale, are avantajul suplimentar de a reduce riscul de decompensare și mortalitate conform rezultatelor studiului PREDESCI (23) Dintre BBNS utilizate în mod obișnuit, propranololul și nadololul reduc presiunea portală prin reducerea fluxului venos portal prin blocarea receptorilor adrenergici β1 și β2, în timp ce carvedilolul are activitate vasodilatatoare intrinsecă suplimentară datorită activității sale anti-α-adrenergice și ca-
pacității sale de a crește eliberarea de oxid nitric (23). Mai mult, s-a observat că carvedilolul provoacă o reducere mai mare a HVPG în comparație cu propranolol sau nadolol (24). Carvedilolul poate fi util în special pentru pacienții cu CH compensată, unde o rezistență vasculară hepatică mai mare este cauza principală a HTP (24) .
În ultimii ani au fost publicate mai multe studii privind efectele benefice ale statinelor la pacienții cu CH. Beneficiile includ o scădere a presiunii portale, efecte favorabile asupra funcției endoteliale sinusoidale, microcirculației și fibrozei hepatice prin creșterea generării de NO în sinusoidele hepatice și reducerea rezistenței vasculare intrahepatice (25). Mai mult, s-a constatat că simvastatina a avut un efect aditiv cu BBNS asupra reducerii HVPG (26) . Într-o revizuire sistematică recentă, statinele au fost asociate cu un risc redus cu 46% de decompensare hepatică și un risc cu 46% mai mic de mortalitate la pacienții cirotici (26). Pacienții cu CH care beneficiază de statine sunt în principal cei cu clase Child-Pugh A sau B, dar nu cei cu clasa Child C. În CH decompensată, simvastatina poate provoca chiar rabdomioliză și hepatotoxicitate (26). Prin urmare, în ciuda faptului că statinele sunt utile pentru pacienții cirotici, sunt necesare mai multe dovezi înainte de a putea fi recomandate în mod regulat pacienților cu ciroză hepatică.
Managementul factorilor agresivi. Pacienții obezi cu CH au niveluri mai ridicate de citokine inflamatorii, crescând riscul de decompensare printr-un răspuns inflamator sistemic [94]. Prin urmare, pierderea în greutate poate fi o strategie terapeutică eficientă pentru pacienții obezi cu ciroză (27). Chirurgia bariatrică nu este recomandată în general pacienților cu CH compensată și este contraindicată în ciroza decompensată. Pacienților cu CH li se poate recomanda în siguranță să-și schimbe stilul de viață sub îngrijirea unui dietetician, cu scopul de a reduce greutatea corporală. În cazul ciroticilor care asociază DZ tip 2, menținerea unui control glicemic adecvat poate aduce beneficii cursului bolii. Cu toate acestea, managementul standardizat al diabetului pentru pacienții cu CH
nu a fost încă stabilit. Pe lângă modificarea stilului de viață, pot fi utilizați agenții hipoglicemici orali până la clasa Child-Pugh B, în timp ce insulina este recomandată pentru CH în toate etapele (28). Abstinența de la alcool reduce riscul de decompensare și îmbunătățește rezultatele în toate etapele CH legate de alcool (29). Conform unei meta-analize a șapte studii de cohortă care au implicat 1235 de pacienți cu ciroză alcoolică, este necesar cel puțin 1,5 ani de abstinență înainte de a putea fi observată o diferență semnificativă statistic în supraviețuire între grupul abstinent și cel consumator de alcool (29). Intervențiile dietetice ar trebui să includă un aport de proteine țintă de 1,2-1,5 g/kg/zi și exerciții aerobice regulate pentru a preveni sau ameliora sarcopenia, care este asociată cu rezultate slabe la pacienții cirotici (30)
Terapii antifibrotice și regenerative. Evoluțiile recente ale căilor fiziopatologice importante legate de HTP în CH au dezvăluit o serie de noi ținte posibile de tratament. Acestea includ anomalii intrahepatice asociate cu inflamație, fibrogeneza și modificări microvasculare. Unele medicamente, inclusiv inhibitorii fosfodiesterazei-5, agoniștii receptorilor farnesoid X, antagoniștii receptorului endotelinei-A și taurina acidului amino sulfonic, s-au dovedit că reduc HTP, ceea ce poate fi util în reducerea decompensării la pacienţii cu CH compensată (31). Cu toate acestea, sunt necesare dovezi mai solide și consecvente cu privire la siguranța și eficacitatea acestor medicamente. În prezent, nu există farmacoterapii pentru fibroză care au fost autorizate, dar cercetările privind medicamentele antifibroză au făcut progrese semnificative în ultimii ani, în special în ceea ce privește medicamentele pentru fibroza asociată bolii hepatice grase nonalcoolice.
Eliminarea factorilor precipitanți. Mai multe evenimente precipitante pot duce la agravarea bruscă a stării clinice a pacienților cu CH prin cauzarea ACLF. Astfel, controlul unor astfel de variabile precipitante poate reduce semnificativ morbiditatea și mortalitatea asociate cirozei. Profilaxia cu antibiotice și tratamentul cu antibiotice prompt și judicios pot ajuta la preveni-
28 www.revistamedicalmarket.ro
de specialitate Gastroenterologie
Articole
rea ACLF declanșată de infecție (32). De asemenea, antibioticele profilactice în combinație cu gestionarea eficientă a sângerării gastrointestinale pot preveni precipitarea ACLF. O altă strategie preventivă importantă este vaccinarea împotriva hepatitei virale. Pentru toți pacienții cu CH, se recomandă vaccinul împotriva hepatitei B. Cu toate acestea, în comparație cu subiecții normali, pacienții cu ciroză ating rate de seroprotecție mai scăzute după vaccinarea VHB (rata medie de răspuns de 47%) (33)
În concluzie, dezvoltarea decompensării hepatice reprezintă cel mai important factor de prognostic din istoria naturală a cirozei hepatice. Tratamentele care ameliorează acest risc au un rol important în managementul pacienților cu CSPH. În lumina dezvoltării instrumentelor neinvazive care permit stratificarea în timp util și precisă a riscului pacienților cu ciroză, aplicarea chimioprevenției devine din ce în ce mai fezabilă. BBNS sunt în prezent pilonii de bază ai tratamentului în acest sens, dar terapiile emergente, cum ar fi statinele, rifaximina, pot oferi speranță pentru strategii multimodale personalizate în viitor. Această schimbare de paradigmă poate reduce în cele din urmă morbiditatea și mortalitatea legată de ficat, poate îmbunătăți calitatea vieții și poate limita sarcina socio-economică a cirozei hepatice, indiferent de factorii etiologici implicați.
Bibliografie:
1. Lee S, Saffo S. Evolution of care in cirrhosis: Preventing hepatic decompensation through pharmacotherapy. World J Gastroenterol. 2023 Jan 7; 29(1):61-74. doi: 10.3748/wjg.v29.i1.61.
2. https://data.who.int/countries/642. Ultima accesare 17 august 2023
3. GBD 2017 Cirrhosis Collaborators. The global, regional, and national burden of cirrhosis by cause in 195 countries and territories, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet Gastroenterol Hepatol. 2020;5:245–266.
4. D’Amico G, Bernardi M, Angeli P. Towards a new definition of decompensated cirrhosis. J Hepatol. 2022; 76:202–207.
5. Trebicka J, Hernaez R, Shawcross DL, Gerbes AL. Recent advances in the prevention and treatment of decompensated cirrhosis and acute-on-chronic liver failure (ACLF) and the role of biomarkers. Gut. 2024.gutjnl-2023-330584. doi: 10.1136/gutjnl-2023-330584.
6. Schulz MS, Angeli P, Trebicka J. Acute and non-acute decompensation of liver cirrhosis (47/130). Liver Int. 2024 Mar 1. doi: 10.1111/liv.15861.
7. D’Amico G, Morabito A, D’Amico M, et al. New concepts on the clinical course and stratification of compensated and decompensated cirrhosis. Hepatol Int. 2018; 12:34–43.
8. Hytiroglou P, Theise ND. Regression of human cirrhosis: an update, 18 years after the pioneering article by Wanless et al. Virchows Arch. 2018; 473:15–22.
9. D’Amico G, Garcia-Tsao G, Pagliaro L. Natural history and prognostic indicators of survival in cirrhosis: a systematic review of 118 studies. J Hepatol. 2006; 44:217–231.
10. Samonakis DN, Koulentaki M, Coucoutsi C, et al. Clinical outcomes of compensated and decompensated cirrhosis: A long term study. World J Hepatol. 2014; 6:504–512.
11. Damodaran A, Zachariah SM, Nair SC. Novel therapeutic approaches for the management of hepatitis infections. Ther Deliv. 2024 Mar; 15(3):211-232. doi: 10.4155/tde-2023-0074.
12. Tapper EB, Ufere NN, Huang DQ, Loomba R. Review article: current and emerging therapies for the management of cirrhosis and its complications. Aliment Pharmacol Ther. 2022; 55:1099–1115.
13. Manne V, Akhtar E, Saab S. Cirrhosis regression in patients with viral hepatitis B and C: a systematic review. J Clin Gastroenterol. 2014; 48:e76–e84.
14. Xu M, Chen Y, Artru F. Acute decompensation of cirrhosis versus acute-on-chronic liver failure: What are the clinical implications? United European Gastroenterol J. 2024 Mar; 12(2):194-202. doi: 10.1002/ueg2.12538.
15. Sanyal AJ, Anstee QM, Trauner M, et al. Cirrhosis regression is associated with improved clinical outcomes in patients with nonalcoholic steatohepatitis. Hepatology. 2022; 75:1235–1246.
16. Lassailly G, Caiazzo R, Ntandja-Wandji LC, et al. Bariatric Surgery Provides Long-term Resolution of Nonalcoholic Steatohepatitis and Regression of Fibrosis. Gastroenterology. 2020; 159:1290–1301.e5.
17. Hofer BS, Simbrunner B, Hartl L, et al. Alcohol Abstinence Improves Prognosis Across All Stages of Portal Hypertension in Alcohol-Related Cirrhosis. Clin Gastroenterol Hepatol. 2022.
18. Lim WH, Tay P, Ng CH, et al. Meta-analysis: Prevalence and impact of alcohol abstinence in alcohol-associated cirrhosis. Aliment Pharmacol Ther. 2024 Mar; 59(6):730-741. doi: 10.1111/apt.17888.
19. Shiffman ML. Autoimmune Hepatitis: Epidemiology, Subtypes, and Presentation. Clin Liver Dis. 2024 Feb; 28(1):1-14. doi: 10.1016/j. cld.2023.06.002.
20. Sohal A, Kayani S, Kowdley KV. Primary Sclerosing Cholangitis: Epidemiology, Diagnosis, and Presentation. Clin Liver Dis. 2024 Feb; 28(1):129141. doi: 10.1016/j.cld.2023.07.005.
21. Bardou-Jacquet E, Morandeau E, Anderson GJ, et al. Regression of Fibrosis Stage With Treatment Reduces Long-Term Risk of Liver Cancer in Patients With Hemochromatosis Caused by Mutation in HFE. Clin Gastroenterol Hepatol. 2020; 18:1851–1857.
22. Cromer M, Wilcox CM, Shoreibah M. Beta-blockers and cirrhosis: Striking the right balance. Am J Med Sci. 2024 Apr; 367(4):228-234. doi: 10.1016/j.amjms.2024.01.009.
23. Villanueva C, Albillos A, Genescà J, et al. β blockers to prevent decompensation of cirrhosis in patients with clinically significant portal hypertension (PREDESCI): a randomised, double-blind, placebo-controlled, multicentre trial. Lancet. 2019; 393:1597–1608.
24. Møller S, Danielsen KV, Nabilou P, et al. Beta-adrenergic blockade in cirrhosis - harmful or helpful? Expert Rev Gastroenterol Hepatol. 2023 Jan-Jun; 17(6):519-529. doi: 10.1080/17474124.2023.2215428.
25. Muñoz AE, Pollarsky F, Marino M, et al. Baseline Severity and Inflammation Would Influence the Effect of Simvastatin on Clinical Outcomes in Cirrhosis Patients. Dig Dis Sci. 2023 Aug; 68(8):34423450. doi: 10.1007/s10620-023-07969-3.
26. Pose E, Solà E, Lozano JJ, et al; investigators of the LIVERHOPE Consortium. Treatment With Simvastatin and Rifaximin Restores the Plasma Metabolomic Profile in Patients With Decompensated Cirrhosis. Hepatol Commun. 2022 May; 6(5):1100-1112. doi: 10.1002/hep4.1881.
27. Miñambres I, Rubio MA, de Hollanda A, et al. Outcomes of Bariatric Surgery in Patients with Cirrhosis. Obes Surg. 2019; 29:585–592.
28. Kumar R, García-Compeán D, Maji T. Hepatogenous diabetes: Knowledge, evidence, and skepticism. World J Hepatol. 2022; 14:1291–1306.
29. Hofer BS, Simbrunner B, Hartl L, et al. Alcohol Abstinence Improves Prognosis Across All Stages of Portal Hypertension in Alcohol-Related Cirrhosis. Clin Gastroenterol Hepatol. 2022.
30. Bischoff SC, Bernal W, Dasarathy S, et al. ESPEN practical guideline: Clinical nutrition in liver disease. Clin Nutr. 2020; 39:3533–3562.
31. Zhao J, Li B, Zhang K, Zhu Z. The effect and safety of obeticholic acid for patients with nonalcoholic steatohepatitis: A systematic review and meta-analysis of randomized controlled trials. Medicine (Baltimore). 2024 Feb 16; 103(7):e37271. doi: 10.1097/MD.0000000000037271.
32. Garcia-Tsao G. Prophylactic Antibiotics in Cirrhosis: Are They Promoting or Preventing Infections? Clin Liver Dis (Hoboken) 2019; 14:98–102.
33. Zhao Q, Liu H, Tang L, et al. Mechanism of interferon alpha therapy for chronic hepatitis B and potential approaches to improve its therapeutic efficacy. Antiviral Res. 2024 Jan; 221:105782. doi: 10.1016/j.antiviral.2023.105782. Epub 2023 Dec 17. PMID: 38110058.
29 Articole de specialitate Gastroenterologie 2024 - 2025
Noi perspective în pregătirea intestinului
Colonoscopia este o investigație esențială în diagnosticul și, uneori, chiar în tratamentul bolilor colonice. Deasemeni, joacă un rol important în diagnosticul precoce al cancerului colorectal și oferă oportunitatea unui tratament în stadiile incipiente ale bolii, crescând, astfel, durata supraviețuirii și calitatea vieții pacienților.
Conf. Univ. Dr. Laura Carina Tribuș
Medic primar Medicină Internă, Medic primar Gastroenterologie, UMF „Carol Davila”
Pregătirea colonului pentru investigațiile colonoscopice este o etapă foarte importantă în care comunicarea medic-pacient este esențială, nu doar pentru explicarea pregătirii, ci și pentru informarea pacientului cu privire la indicațiile colonoscopiei, la ce presupune această procedură, care sunt beneficiile și riscurile și ce complicații pot apărea în timpul acesteia.
Preparatele pe bază de PEG (polietilenglicol) pentru pregătirea în vederea investigațiilor colonoscopice
Preparatele pe baza de PEG sunt o clasa de medicamente cu efect laxativ, care acționează prin formarea de legături de hidrogen cu moleculele de apă, ducând astfel la scăderea absorbției acesteia în intestin și creșterea motilității intestinale. Ele sunt totodată recomandate și de ESGE în pregatirea intestinală de elecție.
Formula Plenvu
Plenvu este un preparat pe bază de PEG de ultimă generație, cu volum redus, doar 1 l de substanță de administrat. Este indicat la persoane peste 18 ani pentru pregătirea intestinului înainte de intervențiile la acest nivel (colonoscopie, enteroscopie, intervenții chirurgicale). Fiind o cantitate redusă de substanță ce trebuie ingerată, cresc tolerabilitatea și complianța, maximizând șansele unei pregătiri eficiente. Substanțele constitutive ale produsului sunt Macrogol 3350 (PEG), acid ascorbic, sulfatul de sodiu (substanțe cu acțiune laxative osmotică) și electroliți, precum clorura de sodiu și de potasiu special combinate în ambele doze de administrare, astfel încât să faciliteze eficiența pregătirii intestinale, printr-o curățare de înaltă calitate, cu cel mai mic volum de administrare.
În zilele anterioare procedurii este necesar a se urmări un ghid alimentar pentru o
pregătire eficientă. Pregătirea începe cu treicinci zile înaintea intervenției, când trebuie sistat consumul alimentelor ce conțin semințe, cu o zi înainte de procedură sunt permise un mic dejun ușor și un prânz bazat pe alimente sărace în fibre (cu trei ore înaintea administrării primei doze) și se recomandă a se evita băuturile colorate, sucurile cu pulpă, lapte, bulion, băuturi carbogazoase și alcool. Cu două ore înainte de investigație nu se va mai administra niciun fel de lichid(1)
Modul flexibil de administrare a Plenvu permite adaptarea administrării în funcție de programarea procedurii
Procedură programată dimineața în intervalul 9:00-13:00 – schema divizată în două zile (seara/dimineața). În seara anterioară procedurii, în jurul orei 18:00, se începe administrarea primei doze de preparat (primul preparat dizolvat în 500 ml de apă sau lichid limpede) împreună cu înca 500 ml de apă sau lichid limpede. În dimineața procedurii, ora 6:00, se administrează a doua doză de produs (plicurile A+B dizolvate în 500 ml de apă sau lichid clar) împreună cu încă 500 ml de apă sau lichid limpede(2).
Procedură programată la începutul după-amiezii, începând cu ora 14:00. Administrarea într-o singură zi (dimineața). Schema de administrare numai dimineața, cu ambele doze administrate în dimineața zilei procedurii clinice (ora 5.00); a doua doză trebuie să fie administrată la un interval de cel puțin 2 ore de la începutul administrării primei doze (ora 7.00). Plicurile A+B dizolvate în 500 ml de lichid clar. După fiecare doză de preparat se vor consuma încă 500 ml de lichide limpezi(3)
Procedură programată dimineața devreme, 6:00 - 9:00. Administrarea într-o singură zi (seara). Ambele doze luate în seara de dinaintea procedurii clinice, prima doză începând cu ora 18:00; a doua doză trebuie să fie administrate la un interval de cel puțin 2 ore de la începutul administrării primei doze. Dizolvarea ambelor doze necesită 500 ml de apă, fiecare. După fiecare doză de preparat se vor consuma câte 500 ml de lichid clar(4).
Plenvu are contraindicații similare tuturor preparatelor utilizate în această categorie de pregătire intestinală înaintea procedurilor, printre care se numără hipersensibilitatea la substanțele componente, ocluzia intestinală, ileusul, perforația tubului digestiv, megacolonul toxic, perturbările evacuării gastrice, defcitul de glucoză-6-fosfat dehidrogenază și fenilcetonuria. Se recomandă prudență la pacienții cu risc de aspirație, deshidratați, la cei cu valoarea clearence-ului creatininei mai mic de 30 ml/minut, cu insufciență cardiacă stadii avansate, cu risc de a dezvolta aritmii cardiace sau în bolile inflamatorii intestinale acute, formele severe. Este foarte important a se observa (și atenționa pacientul) care sunt medicamentele cronice pe care pacientul le are în tratament curent, având în vedere posibila influență în absorbția medicamentelor orale administrate concomitent(5)
S-au efectuat numeroase studii care au comparat eficiența și tolerabilitatea Plenvu cu ale altor produse utilizate pentru pregătirea pentru colonoscopie. Plenvu a probat clinic rezultate de o calitate înaltă în pregătirea colonului, tolerabilitate superioară și complianță bună în grupurile la care s-a administrat comparativ cu alte preparate PEG, cât și non-PEG.
Majoritatea pacienților care au urmat pregătirea cu Plenvu au fost mulțumiți de volumul mic de lichide ce trebuie administrat în cadrul pregătirii și de pregătirea bună ce a permis o vizualizare corespunzătoare a colonului, timp mai scurt și un grad de confort mai mare în timpul procedurii.
Bibliografie
1. PLENVU® Summary of Product Characteristics. Rezumatul Caracteristicilor Produsului. Data revizuirii textului: ianuarie 2023.
2. DeMicco MP, et al. Gastrointest Endosc. 2018;87(3):677-687.e3.
3. Bisschops R, et al. Endoscopy. 2019 Jan;51(1):60-72.
4. Schreiber S, et al. Endoscopy. 2019;51(01):73-84.
5. Norgine Limited. PLENVU® powder for oral solution UK summary of product characteristics. Rezumatul Caracteristicilor Produsului. Data: septembrie 2023. PM-RO-2023-10-5268 din 25/10/2023
30 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
PM-RO-2023-11-5588 din 8.11.2023
Pulbere pentr u soluție or ală
Macrogol 3350, A scor bat de sodiu, Sulfat de sodiu anhidr u, Acid ascor bic , C lor ur ă de sodiu și c lor ur ă de potasiu
Primul produs de 1 L itru pentru pregătirea colonului pe bază de PEG*
Îmbunăt ățeș te efic ac itatea cur ăț ăr ii colonului cu cel mai mic volum total** de adminis trare

PLENVU® oferă în mod constant o curățare de calitate înaltă cu cel mai mic volum total de administrare


PLENVU® oferă dozare divizată, facilă și adaptabilă în funcție de programarea procedurii

PLENVU® oferă o complianță bună – volum redus de administrare, dietă permisivă*** și arome diferite
PEG* – preparate intestinale ce conțin polietilen glicol (macrogol 3350) - consacrate datorită siguranței și eficacității lor pentru pregătirea de rutină a intestinului - Saltzman et al. Gastrointestinal Endoscopy 2015; 81(4):781-795; Volum total** este format din soluție reconstituită + lichid de hidratare; Dietă permisivă*** este permis mic dejun ușor, urmat de un prânz ușor în ziua înaintea procedurii; 1.Bisschops R, et al. Endoscopy 2019; 51(1): 60-72. 2. Schreiber S, et al. Endoscopy 2019; 51(1): 73-84. 3. DeMicco MP, et al. Gastrointest Endosc 2018; 87(3): 677-687
Produsului. Data, ultimei reînnoiri a autorizației: Ianuarie 202 3 Reac țiile adverse se pot rapor ta și către reprezentanța locală a deținătorului autorizației de punere pe piață la următoarele date de contac t: medinfo romania@swix xbiopharma com; + 40 37 1 530 850
Produs distribuit sub licență de Swix x BioPharma PLENVU, NORGINE și logo-ul pânzei sunt mărci înregistrate ale grupului de companii Norgine
Pentru aspec te legate de distribuția medicamentului în România vă rugăm să contac tați Swix x Biopharma SRL , tel + 037 1 530 850; romania info@swix xbiopharma com
EFICACITATE TOLERABILITATE FLEXIBILITATE
Acest material promoţional este destinat profesioniş tilor din domeniul sănătăţii Acest medicament se eliberează pe bază de prescripție medicală, PRF Pentru informații complete, vă rugăm să consultați Rezumatul C arac teristicilor


















CEL MAI RAPID DE A LUPTA ÎMPOTRIVA ANEMIEI FERIPRIVE
Fe + Mn + Cu.5
Asorbabil imediat + Bine tolerat.1, 4
Până în ziua 30, normalizarea nivelului de hemoglobină
la toate tipurile de pacienți.1, 2, 3
1
2 S.Y Anmouth, O.B. Saneeva and A.V Tchouprova. Les nouveautés dans le traitement de l’anémie sidéropénique chez les enfants. Le journal des « Maladies des Nouveaux Nés et des Enfants ». 2001. 1 : 68-70
3 -
with other liquid or solid formultaions containing bivalent or trivalent iron. Minerva ginecologica. 1996. 48 : 511-518
4 Raport ul din anul 2017 privind siguranța, actualizat periodic (1 Iulie 2010 - 30 Iunie 2017)
5 Rezumatul caracteristicilor produsului pentru Tot’héma®. Rezumatul caracteristicilor produsului pentru Tot’héma® este disponibil la stand la cerere.
M O DU L N OST R U
Acest material este destinat profesioniştilor din domeniul sănătății.
INNOTECH INTERNATIONAL
Avenue Aristide Briand
Arcueil - France
5
LABORATOIRE
22
94110
TOTEM_INNO_TOTH_RO_06-2022-3455_V2
Noninvasive Medical
Indicații
• Hepatite cronice cu virus B și C, coinfecție VHB-Delta, VHB/VHC-HIV
• Consum excesiv de alcool
• Sindrom metabolic: insulinorezistență, obezitate, dislipidemie, HTA, diabet zaharat
• Bilanț hepatic perturbat
• Tranzaminaze normale, dar factori de risc metabolic prezenți
• Steatoză sau ficat gras depistate ecografic
FibroMax cuprinde 5 teste: FibroTest, ActiTest, SteatoTest, NashTest și AshTest
Rolul evaluării fibrozei hepatice în hepatita cronică cu VHC
FibroMax este un instrument de valuare a fibrozei hepatice la începutul tratamentului fără interferon, ce ghidează medicul în alegerea schemei și a duratei de tratament, dar și în privința monitorizării ulterioare a pacientului.
(Aliment Pharmacol Ther. 2016)
FibroMax este un test pentru identificarea cirozei sau a unui stadiu de fibroză avansat în cazul pacienților recent diagnosticați, fără evaluări anterioare și fără semne clinice (pacienți la risc).
(BMJ Open 2015)
FibroMax este un instrument de evaluare a regresiei fibrozei sau a riscului de a progresa. Chiar și după vindecarea virusologică a VHC, pacientul poate rămâne cu un risc de evoluție a fibrozei în prezența comorbidităților.
(Aliment Pharmacol Ther. 2018)
FibroMax este util în screeningul populației generale. La persoanele de 40 de ani, fără factori de risc identificați, prevalența observată a fibrozei hepatice avansate este de aproximativ 3%.
(Lancet Gastroenterol. Hepatol 2017)
Pacienții de sex masculin, cu ALD (boală hepatică alcoolică) sau NAFLD (ficat gras de cauză non-alcoolică), vârsta peste 30 ani, cu sau fără alte comorbidități, prezintă un risc crescut de progresie a fibrozei hepatice.
(J. Hepatol 2012)
A l t e r n a ti v a s igu r ă l a p u n cț i a-b io p s i e he p a ti c ă
BioPredictive | NONINVASIVE MEDICAL | o ce@noninvasive.ro | noninvasive.ro
FibroTes t FibroMax
diagnosticul hepatic neinvaziv prin biomarkerii serici
Noninvasive Medical
FibroMax la inițierea tratamentului fără interferon permite:
Trierea pacienților cu VHC în vederea alegerii schemei terapeutice adecvate și a duratei tratamentului (stadiu F3F4 vs F0F1F2).
Identificarea pacienților cu fibroză avansată care necesită monitorizare post RVS.
Identificarea pacienților cu steatoză metabolică care vor necesita monitorizare ulterioară cu FibroMax.
FibroMax pentru monitorizarea pacienților cu fibroză avansată:
Scopul principal al terapiei fără interferon este vindecarea infecției, respectiv obținerea unui răspuns virusologic susținut (RVS).
Un RVS este în general asociat cu normalizarea rapidă a enzimelor hepatice, îmbunătățirea sau dispariția activității necrotico-inflamatorii hepatice (evaluată cu ActiTest) și regresia fibrozei (evaluată cu FibroTest).
Pacienții cu fibroză severă (scorul METAVIR F3) sau ciroză (F4) rămân cu risc de complicații majore, în principal cancerul primitiv hepatic, chiar și după RVS.
(Aliment Pharmacol Ther. 2018)
În comparație cu pacienții netratați sau non-responderi, riscul de cancer primitiv hepatic și mortalitatea hepatică sunt reduse în mod semnificativ după obținerea RVS, dar nu complet eliminate pentru pacienții cu RVS la stadiul de ciroză. (FibroTest stadiu F4 METAVIR).
Cofactorii de morbiditate hepatică cum ar fi sindromul metabolic, consumul excesiv de alcool și/sau infecția concomitentă cu virusul hepatitei B (HBV), adaugă un risc de persistență a fibrozei severe care poate fi reevaluată prin FibroMax.
A l t e r n a ti v a s igu r ă l a p u n cț i a-b io p s i e he p a ti c ă
FibroMax BioPredictive | NONINVASIVE MEDICAL | o ce@noninvasive.ro | noninvasive.ro
FibroTes t
diagnosticul hepatic neinvaziv prin biomarkerii serici
Screeningul şi pregătirea adecvată pentru colonoscopie - pilonii în prevenția cancerului colo-rectal
Cancerul colo-rectal (CCR) este una dintre cele mai comune forme de cancer la nivel mondial și are un impact semnificativ asupra sănătății publice. Conform datelor Organizației Mondiale a SănătățiiAgenția Internațională pentru Studiul Cancerului, CCR este al patrulea cancer ca incidență după cancerele de sân, prostată și plămân și al treilea ca mortalitate, după cancerul pulmonar și cel de sân1,2.


CNegreanu
Clinica de Gastroenterologie, Spitalul Universitar de Urgență, UMF „Carol Davila” București
Dr. Marina Cozma
Clinica de Gastroenterologie, Spitalul Universitar de Urgență, UMF „Carol Davila” București
onform programului SEER (Surveillance, Epidemiology and End Results) al Institutului Național de Cancer din SUA, s-a observat o scădere în incidența și mortalitatea CCR printre adulții peste 50 de ani. Aceste îmbunătățiri sunt datorate cel mai probabil screeningului, îmbunătățirii tratamentului în cancerul colorectal și identificării factorilor de risc.
În schimb, incidența CCR cu debut precoce a crescut, motivele fiind încă necunoscute. Deși istoricul familial și sindroamele ereditare sunt responsabile de o parte din cancerele cu debut precoce, factorii de mediu și stilul de viață sunt de asemenea contributori3
În România, în anul 2022 s-au înregistrat 13.541 noi cazuri de CCR, fiind cel mai frecvent tip de cancer (12,9% dintre cancere), clasându-se al doilea ca rată de mortalitate, fiind responsabil pentru 13,1% dintre decese4. Prin comparație, în Franța, unde există un program național de screening mai bine organizat, CCR a fost al treilea cel mai frecvent cancer si al doilea ca mortalitate4. Astfel, putem deduce că acest tip de cancer este unul ce poate fi prevenit, iar un program eficient de screening ar îmbunătăți statisticile la nivel național.
Conceptul de screening în CCR a început să se creioneze în mai 1927, când Lockhart-Mummery și Dukes au publicat un articol in revista Surgery, Gynecology and Obsetrics denumit “Modificarile precanceroase în rect și colon”5
Colonoscopia de screening a fost introdusă în ghiduri în anii 1990. A fost recomandat inițial ca intervalul între examinările colonoscopice de screening să fie în jur de 10 ani în populația cu risc mediu. Acest interval s-a bazat pe durata de 10-15 ani, necesară ca un polip sa crească și să se transforme în CCR6 Ulterior, pe măsură ce au fost disponibile date științifice noi, recomandările au devenit extrem de individualizate in funcție de situația pacienților.
În stadiu incipient, CCR este asimptomatic sau prezintă doar simptome vagi. Polipii reprezintă leziuni precanceroase bine determinate. Îmbătrânirea este un factor de risc important. Populația a fost împărțită în două categorii în funcție de nivelul de risc de a dezvolta CCR: populația cu risc mediu și populația cu risc înalt și foarte înalt. Se consideră că populația peste 50 de ani prezintă un risc mediu de a dezvolta CCR, în timp ce populațiile cu risc înalt și foarte înalt includ persoane cu antecedente familiale de adenom sau de CCR, persoane cu boli inflamatorii intestinale, acromegalie și sindroame familiale –PAF (polipoza adenomatoasă familială) și Sindromul Lynch7,8.
Ghidurile europene recomandă colonoscopia completă ca metodă gold-standard de screening pentru CCR în populația cu risc mediu, având o sensibilitate și specificitate mai mari decât toate celelalte tipuri de teste. Intervalul optim de testare este între vârstele de 50-74 de ani, cu repetarea colonoscopiei la 5 sau 10 ani. Sigmoidoscopia flexibi-
lă efectuată la fiecare 5-10 ani poate fi o alternativă pentru cei care refuză colonoscopia în unele sisteme de sănătate. Alte teste, mai puțin invazive, dar care nu pot îndepărta polipii vizualizați, includ capsula endoscopică sau colonografia CT.
Testele non-invazive, non-colonoscopice, sunt recomandate persoanelor cu risc mediu de dezvoltare a CCR, începând cu vârsta de 50 de ani, care încă nu au fost incluse în programe de screening prin colonoscopie. Combinarea colonoscopiei cu un test anual FOBT (Testul Hemoragiei Oculte Fecale) sau, mai nou, cu mai performantul test FIT (Fecal Immunochemical Test) este opțiunea recomandă acum în majoritatea programelor de screening. Testele trebuie efectuate în mod optim anual și este recomandat ca intervalul între acestea să nu depășească 3 ani. În cazul în care testele sunt pozitive, o colonoscopie trebuie efectuată cât mai devreme posibil. Alte metode includ teste bazate pe ADN folosind markeri precum M2-PK, însă datele cu privire la performanța lor nu sunt suficiente7,8,9
Conform recomandărilor ESGE (Societatea Europeană de Endoscopie Gastrointestinală), pentru persoanele cu sindromul Lynch, care fac parte din populația la risc foarte înalt de a dezvolta CCR, screeningul prin colonoscopie debutează la vârsta de 25 de ani și este repetat la fiecare 2 ani. Vârsta de debut a screeningului este de 25 de ani în cazul purtătorilor MLH1 și MSH2 și la 35 de ani pentru purtătorii MSH6 și PMS2.
În cazul persoanelor cu boli inflamatorii intestinale (populație cu risc înalt), screeeningul se realizează la 8-10 ani de la debutul bolii și este repetat anual. ESGE definește populația cu risc familial de dezvoltare a CCR ca având cel puțin două rude de gradul I diagnosticate
36 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
Prof. Dr. Lucian
COMPLIANŢA PACIENŢILOR
în REAL-LIFE
>90% la administarea de soluţie salină preparată și lichide limpezi5
Recomandat de ghidul
Când complianţa devine eficacitate în practica medicală
Complianţă optimă a pacienţilor, dovedită în practica medicală, 1 de până la 96,8%
Eficacitate dovedită inclusiv la nivelul colonului drept, mai dificil 1-3 de investigat
Profil de siguranţă dovedit în practica medicală, inclusiv la 1-5 pacienţii vârstnici
1
UȘOR DE ADMINISTRAT

EFICACITATE
în REAL-LIFE
la 9 din 10 pacienţi curăţarea colonului a fost bună și excelentă5
2 flacoane al cărui conţinut se diluează cu apă Conţine sulfat de sodiu, magneziu și potasiu

Kit complet de pregătire intestinală, ce include pahar dozator pentru o pregătire corectă
1L de soluţie reconstituită - preparat LOW VOLUME
2L de lichide limpezi
Gust placut de cocktail de fructe
1.ENCEPP 2019. Data on file and available at http://www.encepp.eu/ encepp/viewResource.htm?id=30186 accesat iulie 2019; 2.Di Palma et al. Am J Gastroenterol 2009;104:2275-84; 3.Rex et al. Gastrointest Endosc 2010;72:328-36; 4.EZICLEN® RCP 2023; 5.Regula Endoscopy International Open 2020; 08: E247–E256. Acest material promoţional este destinat profesioniștilor din domeniul sănătăţii. Este important să raportaţi orice reacţie adversă suspectată la Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale din România, Str. Aviator Sănătescu nr. 48, sector 1, Bucureşti 011478- RO, e-mail: adr@anm.ro Website: www.anm.ro. Totodată, reacţiile adverse suspectate se pot raporta și către reprezentanţa locală a deţinătorului autorizaţiei de punere pe piaţă, la Mayoly Romania SRL, Str. Mihai Eminescu, Nr. 108-112, București, Sector 2. Telefon: +40 371 575 757, e-mail: vigilance.ROU@mayoly.com

Pentru informaţii complete de prescriere, vă rugăm să scanaţi codul QR
kit pentru pregatirea colonoscopiei ) VEZI TOT CE AI NEVOIE SA VEZI! )
RO-EZC-2024180302
Principalele recomandări ale Societății Europene de Endoscopie Gastrointestinală (ESGE) cu privire la pregătirea pentru colonoscopie
1 ESGE recomandă dieta săracă în fibre în ziua ce precede colonoscopia.
2 ESGE recomandă furnizarea de informații detaliate pacienților cu privire la pregătirea pentru colonoscopie.
3 ESGE recomandă adăugarea Simeticonei orale la pregătirea pentru colonoscopie.
4 ESGE recomandă pregătirea în doze fracționate pentru colonoscopia electivă.
5 Conform ESGE, pentru pacienții ce efectuează colonoscopie în a doua parte a zilei, pregătirea în aceeași zi este acceptată ca alternativă la pregătirea în doze fracționate.
6 ESGE recomandă începerea ultimei doze de substanță de pregătire în ultimele 5 ore ce preced colonoscopia, iar aceasta să fie finalizată la cel puțin la 2 ore înainte de debutul procedurii.
7 Conform ESGE, regimurile bazate pe PEG cu volum mic și PEG cu volum mare, cât și pe agenți non-PEG au fost validate clinic pentru pregătirea de rutină. La pacienții la risc de dezechilibre hidroelectrolitice, alegerea substanței trebuie să fie individualizată.
8 ESGE nu recomandă utilizarea prokineticelor pentru pregătire.
9 ESGE nu recomandă utilizarea de rutină a clismelor pentru pregătire.
cu CCR înaintea vârstei de 50 de ani. În cazul acestei populații, este recomandat ca screeningul prin colonoscopie să înceapă la vârsta de 40 de ani10,11
Pregătirea adecvată a colonului este, pobabil, unul din cele mai importante aspecte in programul de screening. Pentru a optimiza calitatea procedurilor colonoscopice, ESGE a elaborat o serie de recomandări: timpul dedicat colonoscopiei 30-45 de minute, timpul de observare a mucoasei la coborâre 6-10 minute, rată satisfăcătoare de detecție a adenoamelor sau a polipilor la nivelul centrului, necesitatea intubației cecale, tehnica adecvată de polipectomie, pregătirea adecvată12,13. În aproximativ 28-33% dintre colonoscopii, pregătirea intestinală este nesatisfăcătoare, acest fapt ducând la costuri ascunse precum rata de decese prevenibile sau tratabile a CCR. Pregătirea pentru colonoscopie este astfel esențială pentru obținerea unor rezultate precise și pentru minimizarea riscurilor asociate procedurii. Atât ESGE, cât și UEG (United European Gastroenterology) recomandă o pregătire adecvată în cel puțin 90% din cazuri, calculate atât la nivel de centru, cât și pentru fiecare endoscopist în parte14-16
Tabelul I. include principalele recomandări ale Societății Europene de En-
doscopie Gastrointestinală (ESGE) cu privire la pregătirea pentru colonoscopie17
Pentru a crește calitatea colonoscopiei foarte importante sunt campaniile de conștientizare și educare a pacienților, comunicarea cu aceștia și furnizarea de instrucțiuni (protocolul de pregătire a colonoscopiei) care să explice clar și în detaliu importanța și pașii de urmat pentru o cât mai bună pregătire intestinală.
Produsele administrate pentru pregătirea intestinului în colonoscopia diagnostică sau terapeutică, conform Ghidului ESGE17, sunt de tipul high-volume, respectiv soluția PEG (polietilen glicol) cu electroliți (PEG-E sau PEG 4 L), sau low-volume, respectiv soluții PEG cu electorliți și adjuvanți, sau soluții saline de tipul sulfat sau picosulfat.
Un exemplu de produs low-volume pentru pregătirea colonoscopiei este soluția orală de sulfați (OSS, oral salt solution). Aceasta conține sulfați de sodiu, de magneziu și de potasiu. Pregătirea colonului cu acest produs presupune administrarea a 1 L de produs preparat urmat de 2 L de lichide limpezi. Acest preparat a fost comparat cu PEG-E în trei studii clinice randomizate17 în care s-au arătat non-nferioritatea OSS în doză divizată față de PEG-E în ceea ce privește eficacitatea, un profil de
siguranță ridicat și o tolerabilitate mai bună. Un alt studiul clinic randomizat a comparat OSS cu picosulfat, cele două produse fiind administrate în doză divizată. S-a demonstrat că rata de succes a colonoscopiei (curățare intestinală bună și excelentă) a fost mai bună în grupul OSS17. Alte avantaje ale produsului sunt ușurința în administrare și palatabilitatea sa.
În concluzie, screeningul pentru cancerul colo-rectal reprezintă un aspect vital în prevenția și combaterea acestei afecțiuni, oferind oportunitatea de detectare precoce a leziunilor precanceroase sau a cancerului în stadii incipiente, când tratamentul este mai eficient și șansele de supraviețuire sunt mai mari.
În plus, screeningul oferă posibilitatea de a identifica grupurile de risc și de a le oferi îndrumare suplimentară și supraveghere medicală adecvată, contribuind la gestionarea și reducerea factorilor de risc asociați acestei patologii.
Pregătirea adecvată pentru colonoscopie crește calitatea procedurii de colonoscopie, o pregătire corespunzătoare a pacientului fiind esențială pentru obținerea unei vizualizări optime a mucoasei intestinale.
Implicarea în screeningul regulat pentru CCR și pregătirea adecvată pentru colonoscopie reprezintă piloni fundamentali în lupta împotriva acestei afecțiuni.
Bibliografie
1.The Global Cancer Observatory 2020, accesat sept 2023; 2.Sung et al. CA Cancer J Clin. 2021;71(3):2099; 3.Saraiva et al. World J Gastroenterol. 2023;29(8):1289-3; 4. The Global Cancer Observatory 2022, accesat feb 2024; 5.Lockhart-Mummery JP. Surg Gyn Obs 1928;46:591-6; 6.Ransohoff DF., Lang CA. N Engl J Med. 1991;325:37–41; 7.Atkin et al. Endoscopy 2012;44:E151-E163; 8.Lin et al. JAMA 2016;315:2576-94; 9.Bretthauer et al. JAMA Intern Med 2016;176:894-902; 10.Stjepanovic et al. Ann Oncol 2019;30:1558-71; 11.Van Leerdam et al. Endoscopy 2019; 51(11):1082-93; 12.Rembacken et al. Endoscopy. 2012;44(10):957-68; 13.Kaminski et al. Endoscopy [Internet]. 2017;49(4):378-97; 14.Negreanu et al. Journal of International Medical Research 2020;48(4):1-8; 15.Hassan et al. Clinical Gastroenterology and Hepatology 2012;10(5):501–506; 16.Pahomeanu MR., Negreanu L. Modern Medicine 2020;27(3):139-144; 17.Hassan et al. Endoscopy 2019;51:775-94.
38 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie

DEZINFECȚIE
AER & SUPRAFEȚE
cu lumină UVC
Roboți mobili și autonomi | Dispozitive smart
Servicii Abonament "DAaaS" | Platformă integrată
Consultanță proiectare | Sesiuni Demo

Wolf-e Robotics S.R.L.
Jud. Prahova, România
+40 733 263 259
offic e@w olf e.r o
CoBOT-Ultra
WolfBOT
WolfBOT-Mini
CoBOT-Lite AER
Breez Beam Lift AER 500+
Wolf-SENSE AER S
www.wolfe.ro
Sindromul de intestin iritabil
– de la simptome la soluții terapeutice
Sindromul de intestin iritabil (SII) este una din cele mai frecvente patologii digestive (ocupă 20-50% din consultațiile gastroenterologice), prevalența fiind cuprinsă între 5 și 10% din populația generală1. Afectează predominant femeile și populația tânără. Caracterul cronic, recidivant, asocierea cu alte tulburări funcționale, afectarea calității vieții, costurile individuale la nivel de sisteme medicale (costuri directe de până la 10 bilioane anual în Statele Unite) și sociale (concendii medicale, absenteism la locul de muncă) fac din SII o adevărată problemă de sănătate publică2.


PProf. Dr. Cătălina Mihai
UMF ”Grigore T. Popa”, Institutul de Gastroenterologie
și Hepatologie Iași
Prof. Dr. Cristina Cijevschi
UMF „Grigore T. Popa”, Institutul de Gastroenterologie
și Hepatologie Iași
atogenia SII este incomplet elucidată, dar pertubarea axei creier-intestin pare a fi mecanismul principal. Au fost descrise modificări multiple: perturbări ale microbiotei intestinale, anomalii ale celulelor endocrine ale tractului digestiv, hipersenzitivitate viscerală, tulburări de motilitate, creșterea permeabilității mucoasei intestinale.
Factorii etiologici incriminați sunt cei alimentari, genetici, psihologici, precum și infecțiile tractului digestiv sau consumul de antibiotice3. Unul din 10 pacienți cu SII au în antecedente o infecție enterică (bacteriană, virală, parazitară), alcătuind grupul pacienților cu SII post-infecțios4. Există studii care indică prezența SII la până la 11,6% din pacienții post - COVID 19, factorii de risc fiind sexul feminin, severitatea episodului respirator, prezența simptomelor digestive în timpul infecției SARS-CoV-2, anxietatea și depresia5.
Microbiota intestinală a fost intens studiată în SII. Există o scădere a diversității speciilor bacteriene, cu o creștere a enterobacteriilor și o scădere de bifidobacterii și lactobacilli; Veillonella este asociată cu constipația din SII. În ciuda modificărilor constatate, nu s-a identificat o „semnătură microbiană” în diferitele tipuri de SII6. Mecanismele prin care disbioza intestinală intervine în patogeneza SII sunt multiple: pierderea integrității barieri intestinale cu translocare bacteriană și declanșarea răspunsului inflamator, răspuns imun abe-
rant cu creșterea hipersenzitivității viscerale, mimetism molecular între antigenele bacteriene și proteinele gazdei7. Studii actuale se concentrează asupra metaboliților microbiotei (acizi biliari, butirat, neurotransmițători) ca potențiali biomarkeri sau ținte terapeutice în SII8. Sindromul de suprapopulare bacteriană (SIBO), caracterizat prin creșterea excesivă a numărului de bacterii în intestinul subțire, este present la 15% din pacienții cu SII7.
Statusul inflamator din mucoasa pacienților cu SII este documentat prin creșterea numărului de mastocite, limfocite și citokine proinflamatorii. Perturbările imune, endocrine și neuronale afectează în ambele direcții axa creier-intestin și induc modificările caracteristice SII.
Simptomele clinice în SII sunt reprezentate de durere abdominală în asociere cu o modificare în frecvența și/sau consistența scaunului. Meteorismul abdominal este un simptom frecvent întâlnit dar prezența sa nu este obligatorie pentru diagnosticul de SII. Pot apărea tenesme rectale, defecație dificilă sau incompletă, scaune cu mucus. Frecvent se asociază și alte patologii: dispepsie funcțională, boală de reflux gastroesofagian, sensibilitate la gluten non-celiacă, endometrioză, fibromialgie, migrene, oboseală, tulburări psihiatrice1,9
Strategia de diagnostic recomandată converge spre un diagnostic pozitiv bazat pe simptome și nu pe un diagnostic de excludere. Criteriile de diagnostic sunt cele

Fig. 1. Scala Bristol de apreciere a formei scaunului în SII.
stabilite de experți prin consensul ROMA IV10. Acestea presupun existența durerii abdominale (cel puțin un episod pe sâptămână în ultimele 3 luni) în asociere cu modificări în forma și/sau frecvența scaunelor și/sau cu modificarea caracterului durerii în relație cu defecația. Debutul simptomelor să fie de cel puțin 6 luni10
Consistența scaunelor se apreciază conform scalei Bristol10 (Fig. 1). În funcție de această scală SII poate fi clasificat în mai multe subtipuri (Tabel I)10.
În cazul paciențor cu SII – D, Colegiul American de Gastroenterologie recomandă testarea de rutină a serologiei pentru boală celiacă și a markerilor inflamatori (proteina C reactivă, calprotectina fecală) pentru excluderea bolii celiace și a bolii Crohn11. În schimb, același ghid nu recomandă testarea de rutină a agenților patogeni în scaun sau a alergiilor alimentare. Testele fiziologice ano-rectale sunt indicate în caz de simptome sugestive pentru disfuncții ale planșeului pelvin, incontinență anală, pentru selectarea pacienților ce vor beneficia de tehnici de biofeedback. În plus, ghidul britanic recomandă teste de identificare a malabsorbșiei acizilor biliari la pacienții colecistectomizați sau cu diaree nocturnă12
Colonoscopia este recomandată pacienților cu simptome „de alarmă” (hemoragie digestivă, anemie, scădere ponderală, debutul simptomelor la vârstă înaintată, febră, frisoane, simptome nocturne, istoric familial de cancer colorectal, boală inflamatorie intestinală, boală celiacă) sau celor cu vârstă peste 45-50 de ani (fără screening colonoscopic prealabil).
Diagnosticul difernțial al SII trebuie făcut atât cu afecțiuni organice (cancer colo-rectal, boală inflamatorie intestinală, boală celiacă, colită microscopică, insuficiență pancreatică exocrină, tumori neuroendocrine, hipertiroidie, afecțiuni genitale, urinare) cât și cu afecțiuni funcționale: constipația funcțională, diareea funcțională, durerea abdominală funcțională, meteorismul funcțional, tulburările intestinale funcționale nespecifice.

40 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
Citrat de alverină Simeticonă
Capsule moi


Citrat de alverină
Simeticonă


Ameliorează
durerea abdominală
și balonarea1,2
Singurul medicament pe bază de citrat de alverină*3
Cea mai mare concentrație de simeticonă disponibilă pe unitate terapeutică*3
Combinația unică - tratamentul de primă intenție pentru ameliorarea durerii abdominale în SII, prin alverină
și tratamentul balonării asociate, prin simeticonă 1,2,4,5
Acțiune țintită asupra durerii abdominale, spasmului și balonării 4,6
Ameliorează simptomatologia clinică și îmbunătațește calitatea vieții 1,2,4
Dovedit clinic - îmbunătățește gradul de satisfacție al pacientului 1,2
Pentru informații complete de prescriere, vă rugăm să scanați codul QR.

MeteoSpasmyl® este indicat adulţilor pentru ameliorarea simptomatologiei gastro-intestinale, indusă de acumularea excesivă de gaze în intestin, de exemplu, flatulenţa. Simptomatologia determinată de acumularea de gaze în tractul gastro-intestinal poate fi un semn al tulburărilor funcţionale de la acest nivel, manifestându-se ca presiune sau balonare, plenitudine, eructaţie, mişcări peristaltice intestinale şi flatulenţă.7 1. Wittmann et al. Aliment Pharmacol Ther 2010;31(6):615–624; 2. Ducrotte et al. Int J Clin Pract 2014;68(2):245–254; 3. Raport Cegedim – PHR Data Octombrie 2023. 4. Quigley et al. WGO Global Guidelines IBS 2015; 5. Annaházi et al. World J Gastroenterol. 2014;20(20):6031-6043; 6. Coelho et al. JPP 2001;53:1419-1426; 7. RCP MeteoSpasmyl® 2023 *În România
Acest material promoţional este destinat profesioniștilor din domeniul sănătăţii. Este important să raportaţi orice reacţie adversă suspectată la Agenţia Naţională a Medicamentului şi a Dispozitivelor Medicale din România, Str. Aviator Sănătescu nr. 48, sector 1, Bucureşti 011478- RO, e-mail: adr@anm. ro, Website: www.anm.ro. Totodată, reacţiile adverse suspectate se pot raporta și către reprezentanţa locală a deţinătorului autorizaţiei de punere pe piaţă, la Mayoly Romania SRL, Str. Mihai Eminescu, Nr. 108-112, București, Sector 2. Telefon: +40 371 575 757, e-mail: vigilance.ROU@mayoly.com.
RO-MTO-2024200301
Tabel I. Subtipurile de SII conform clasificării ROMA IV; tipurile de scaun 1-7 sunt definite conform scalei Bristol Subtipul de SII Caracterizare
SII cu constipație (SII-C)
SII cu diaree (SII-D)
SII mixt (SII – M)
Peste 25% din defecații se asociază cu tipul 1 sau 2; tipurile 6 și 7 sunt prezente la mai puțin de 25% din defecații
Peste 25% din defecații se asociază cu tipul 6 sau 7; tipurile 1 și 2 sunt prezente la mai puțin de 25% din defecații
Peste 25% din defecații sunt asociatecu tipul 1 sau 2 și peste 25% din defecații se asociază cu tipul 6 sau 7
SII neclasificabil Nu poate fi încadrat în nici unul din subtipurile precedente
Abordarea terapeutică este complexă, de la dietă, medicamente până la suport psihologic și terapii complementare.
Modificarea stilului de viață este prima linie de tratament. Se recomandă activitate fizică, evitarea stressului, dietă adecvată. Pornind de la constatarea că anumite alimente exacerbează simptomele SII, multiple diete par a avea eficiență în ameliorarea clinică: recomandările dietetice tradiționale (mese mici și repetate, limitarea consumului de alcool, cafea, evitarea alimentelor trigger), dieta fără gluten, dieta mediteraneeană. Cea mai utilizată dietă în SII este dieta cu conținut redus FODMAP (oligozaharide, dizaharide, monozaharide fermentabile și polioli). Acesta se realizează în 3 etape (excludere – 6 săptămâni, reintroducere treptată, dietă personalizată), preferabil sub supravegherea unui dietetician. Dieta cu conținut redus FODMAP și-a dovedit superioritatea comparativ cu alte tipuri de dietă în ameliorarea simptomelor din SII13 Suplimentarea cu fibre solubile, în cantități progressive, ameliorează simptomele globale ale pacienților cu SII, în special în cazul constipației; fibrele insolubile nu sunt recomandate.
Terapiile comportamentale cognitive (hipnoza, psihoterapia, terapiile de relaxare) îmbunătățeșc simptomatologia digestivă, reduc simptomele psihiatrice și cresc calitatea vieții la pacienții cu SII9. Efectele favorabile se datorează acțiunii asupra mecanismelor centrale și periferice (scăderea percepției dureroase, ameliorarea hipersenzitivității viscerale și a tulburărilor de motilitate). O metaanaliză ce a inclus 36 de trialuri randomizate a demonstrat eficacitatea superioară a terapiilor psihotrope în SII comparativ cu grupul de control14.
Realitatea virtuală pare a fi o alternativă terapeutică promițătoare la pacienții cu afecțiuni ale axei creier-intestin15. De asemenea, inteligența artificială pare a câștiga teren în diagnosticul, monitorizarea și abordarea terapeutică personalizată a pacienților cu SII16.
Tratamentul medicamentos. În absența unei etiologii și patogenii certe, tratamentul medicamentos se adresează principalelor simptome din SII.
Pentru durere se administrează antispastice, cu acțiune de relaxare a musculaturii netede, anticolinergice, blocante ale receptorilor muscarinici sau ale canalelor de calciu: pinaverină, trimebutină, mebeverină, bromură de otiloniu, hyoscină, alverină. Uleiul de mentă și-a dovedit de asemenea utilitatea în ameliorarea simptomatologiei dureroase. Deși evidențele privind terapiile antispastice sunt dificil de evaluat datorită heterogenității studiilor și preparatelor folosite, s-a demonstrat superioritatea acestora comparativ cu placebo în ceea ce privește ameliorarea durerii abdominale și a simptomelor globale din SII17. La pacienții care asociază simptome polimorfe combinațiile medicamentoase pot fi o soluție (combinația citrat de alverină-simeticonă în caz de meteorism abdominal asociat). Antispasticele au efecte favorabile nu numai în ameliorarea durerii abdominale dar și a tulburărilor de tranzit asociate.
În caz de diaree se recomandă agoniști opioizi (eluxadoline, loperamid), antibiotic (rifaximină), antagoniști ai receptorilor 5-HT3 (alosetron). Chelatorii acizilor biliari (colestiramină, colestipol) pot avea efecte favorbile la unii pacienți.
Pentru constipație medicamentele folosite sunt laxativele osmotice (polietilen glycol), derivați de prostaglandine (lubiprostonă), agoniști de receptori 5-HT4 (tegaserod, prucaloprid), agoniști de guanilat-ciclază (linaclotid, plecanatid) sau inhibitori ai antiportului de sodiu/hidrogen 3 (tenapanor).
Probioticele, prebioticele, sinbioticele și postbioticile și-au dovedit eficiența în ameliorarea simptomelor din SII în unele studii, dar dovezile sunt insuficiente pentru a recomanda o anumită tulpină sau combinații de tulpini. O metaanaliză recentă ce a inclus 82 de studii
și peste 10 000 de pacienți, a demonstrat evidențe modeste privind eficiența probioticelor (Escherichia, Saccaromyces, Lactobacillus, Bifidobacterium) în tratamentul SII18
Transplantul de materii fecale, cu rezultate încă controversate privind eficiența în SII, necesită cercetări viitoare înainte de a fi recomandat în practica clinică curentă19
Medicația psihotropă (antidepresive triciclice, inhibitori selectevi de recaptare ai serotoninei) este utilizată în caz de eșec al medicației de primă linie sau atunci când simptomele psihiatrice asociate o impun.
Tratamentul SII trebuie abordat în trepte și personalizat. Într-o primă etapă sunt recomandate modificările dietetice, antispastice, laxative, antidiareice, probiotice. Medicația psihotropă, rifaximina, eluxadolina, alosetronul, odansetronul, linaclotida, lubiprostona, plecanatida, tegaserod, tenapanor sunt considerate medicamente de linia a doua, recomandate de medicul specialist.
În concluzie, SII este o afecțiune frecventă, ce afectează calitatea vieții individului și impactează sistemele de sănătate. Etiopatogenia este incomplet înțeleasă, centrată pe interacțiunile bidirecționale ale axei creier-intestin. Criteriile de diagnostic sunt stabilite prin consens – ROMA IV. Abordarea terapeutică este complexă, de la dietă și modificarea stilului de viață, la medicamente simptomatice, probiotice, psihotrope. Construirea unei relații de încredere medic-pacient, abordarea multidisciplinară, explicarea caracterului benign al bolii, implicarea pacientului în decizia terapeutică sunt factorii – cheie ai succesului în tratamentul SII. O înțelegere mai bună a mecanismelor de producere ale bolii va duce în viitor la abordare și terapie individualizată, personalizată în SII.
Bibliografie
1.Ford et al. Lancet 2020;396:1675-88; 2.Canavan et al. Aliment Pharmacol Ther 2014;40:1023–34; 3.Jayasinghe et al. Cureus 2024;16(2):e54244; 4.Card et al. United European Gastroenterol J 2018;6:1245-53; 5.Silva JTC, Fonseca Neto OCLD. Rev Col Bras Cir. 2023;50:e20233618; 6.Pittayanon et al. Gastroenterology 2019;157:97-108; 7.Napolitano et al. Microorganisms 2023;11(10):2369; 8.Xiao et al. Front Cell Infect Microbiol 2021;11:729346; 9.Huang et al. World J Gastroenterol 2023;29(26):4120-4135; 10.Lacy et al. Gastroenterology 2016;150:1393-1407; 11.Lacy et al. Am J Gastroenterol 2021;116(1):17-44; 12.Vasant et al. Gut 2021;70(7):12141240; 13.Black et al. Gut. 2022;71(6):1117–1126; 14.Ford et al. Am J Gastroenterol 2019;114:21-39; 15.Travers et al. Curr Opin Gastroenterol 2024;40(1):27-33; 16.Vulpoi et al. Diagnostics (Basel) 2023;13(21):3336; 17.Ruepert et al. Cochrane Database Syst Rev. 2011;(8):CD003460; 18.Goodoory et al. Gastroenterology 2023;165(5):1206-1218; 19.Ianiro et al. Aliment Pharmacol Ther 2019;50(3):240–248.
42 www.revistamedicalmarket.ro
de specialitate Gastroenterologie
Articole
Controlează efectele refluxului gastroesofagian
GASTROTUSS DE LA DMG ITALIA (cu variantele baby și light)
UN PRODUS UNIC PE PIAȚA ROMÂNEASCĂ
Dispozitiv medical cu acțiune mecanică indicat pentru tratamentul refluxului gastroesofagian la sugari și copii. Reduce simptomele legate de aceasta, de exemplu: regurgitare, tuse, pirozis, esofagită, disfonie, flogoză rinofaringiană și în orice caz de boală fiind cauzată în principal sau secundar de refluxul gastroesofagian. Este destinat utilizării pe cale orală.
Este un produs sigur care poate fi administrat timp îndelungat: 3 luni sau după nevoile pacientului, la 2 luni reduce cu 90% simptomele. Gust plăcut, Gastrotuss Baby se administrează la nou născuți şi copiii până în 12 ani Hipocaloric, Gastrotuss light se administrează copiilor peste 12 ani, la gravide, persoanelor cu obezitate şi celor care țin dietă, persoanelor cu diabet zaharat, şi celor care au restricție de sodiu, celor cu HTA sau litiaza renală.
Are în plus şi Simeticona, D-panthenol şi zinc: elimina gazele şi asigura vindecarea mucoasei esofagiene
PepsinO spray este SINGURUL SPRAY pentru răgușeală, tuse, corp străin din refluxul laringofaringian
PepsinO Oral Reflux Spray 30ml este un spray pentru reflux gastro-esofagian care contracarează simptomele refluxului şi lubrifiază mucoasa faringiană.
Util în cazul simptomelor de reflux faringian, cum ar fi: globus hipofaringian (senzație de corp străin în gât), tuse, nevoia de a drege vocea, uscăciune sau iritație faringiană
• Asociat cu Gastrotuss light sirop combate tusea asociată refluxului gastroesofagian

Produsele noastre le găsiţi în farmacii sau, la preţ de importator, cu un singur click pe farmaciile3f.ro
43 Articole de specialitate Gastroenterologie 2024 - 2025
Rezecțiile intestinale: dincolo de actul chirurgical
Rezecțiile intestinale reprezintă intervenții frecvente în chirurgie și se realizează pentru un spectru foarte larg de situații patologie, unele în regim electiv altele in regim de urgență. Cele mai frecvente indicații ale rezecțiilor intestinale sunt reprezentate de: neoplazii intestinale (cel mai frecvent de colon și rect), neoplazii de vecinătate cu invazie intestinală ce impun uneori rezecții de necesitate, ocluzii cu ansă compromisă (prin hernii strangulate, eventrații , bride aderențiale, torsiuni etc), sindroame de ischemie acută intestinală, endometrioza peritoneală, leziuni traumatice intestinale, boli inflamatorii intestinale necontrolabile cu tratament medical, chirurgie bariatrică.


IDr. Oana Timofte
Ş. L., Dep. Medicale I- Semiologie Medicală-Gastroenterologie, UMF „Grigore T.Popa” Iași
Dr. Elena Gologan
Ş. L., Dep. Medicale I- Semiologie Medicală-Gastroenterologie, UMF „Grigore T.Popa” Iași
ntervențiile sunt de amploare diferită de la rezecții minime până la rezecții întinse, unele la limita cu posibilitățile de compensare a funcțiilor segmentelor afectate. Este esențială lungimea segmentului intestinal restant, mai degrabă decât lungimea celui excizat de aceea se recomandă ca chirurgul să măsoare ceea ce rămâne din intestin și nu ceea ce rezecă.
Medicul gastroenterolog se confruntă adesea cu complicații postoperatorii la distanță de aceste intervenții, unele cu soluții eficiente, altele doar limitate; în rare cazuri rezecția, efectuată eroic este urmată de consecințe metabolic-nutriționale incompatibile cu supraviețuirea (insuficiență intestinală).
Sindromul de intestin scurt reprezintă o anomalie secundară unei rezecții intestinale cu manifestări clinice și consecințe metabolic-nutriționale. Factorii de care depinde tipul și amploarea simptomelor sunt: localizarea segmentului excizat, boala pentru care s-a efectuat rezecția, lungimea segmentului rezecat, boala reziduală, tipul anastomozei, calitatea adaptativă a segmentului rămas.
Totuși, intestinul are o capacitate de adaptare la lipsa unui segment, lucru care se realizează lent, în 1-2 ani, prin creșterea în lungime și grosime a vilozităților intestinale (astfel mărindu-se suprafața de absorbție), creșterea calibrului intestinal, creșterea timpului de tranzit intestinal (pentru un
mai bun timp de contact pentru absorbție). Dacă segmentul rămas este de peste 2 m de intestin subțire este posibilă adaptarea.
Diareea post rezecție intestinală este de așteptat în rezecțiile largi de intestin subțire, de colon drept. Este secundară cel mai frecvent diminuării absorbției apei (în plus și a nutrienților și electroliților) din intestin rămânând un bol fecal voluminos, fetid, uneori cu steatoree, de consistență scăzută sau diareic; dacă segmentele rămase au modificări inflamatorii diareea este secundară și acestora.
Dacă a fost excizată și valva ileo-cecală este de așteptat să apară un sindrom de suprapopulare bacteriană intestinală prin migrarea microbiotei specifice colonului ascendent, în intestinul subțire. Aceasta antrenează apoi deconjugarea acizilor biliari generând malabsorbția lipidelor cu steatoree.
În rezecțiile rectale, mai ales în cele cu anastomoze joase, colo-anale efectuate în scopul prezervării continuității de pasaj digestiv natural pacienții acuză adesea diaree cu incontinență anală pentru gaze și materii fecale ceea generează o calitate a vieții alterată, unii preferând efectuarea într-un timp ulterior a unei colostome/ileostome definitive.
Malabsorbția de principii nutriționale aduce malnutriție cu scădere ponderală, uneori severă, cu sarcopenie, uneori chiar marasm nutrițional dar deopotrivă carențe se pot înregistra și pentru vitamine și minerale; cele mai frecvente sunt: carența de vitamina B12 (cu pancitopenie, afectare neurologică și digestivă globală) și folați (vitamina B9) în rezecțiile ileale, carența de vitamina K, A, E, D și calciu în rezecțiile ileale, carența de fier în rezecțiile duodenale și jejunale (cu anemie feriprivă secundară). Uneori asociază malabsorbție pentru zinc, magneziu și vitamina C. Dacă malnutriția este proteino-calorică poate să apară retenția de lichide în corp prin scăderea presiunii coloid-osmotice a plasmei secundară hipoproteinemiei și având ca manifestare clinică edemul, iniți-
al decliv dar în stadii avansate, dacă nu este compensat terapeutic, chiar anasarcă.
Astenia este frecvent întâlnită la pacienții cu rezecții intestinale fiind secundară deshidratării prin diaree cronică dar și prin dezechilibre hidro-electrolitice.
Sindroamele dispeptice manifeste prin meteorism, borborisme, flatulență, greață, disconfort abdominal sunt expresia anomaliilor de digestie secundare pasajului prea rapid cu timp scurt de digestie și implicit de absorbție; în plan secundar apar modificări consistente ale microbiotei ce necesită corectare orală.
Osteoporoza apare frecvent la pacienții cu sindrom de intestin scurt datorită carențelor de vitamina D, calciu, proteine dar și secundar unei mai reduse expuneri la lumină naturală datorită dizabilității induse de starea nutrițională precară. Investigațiile utile unui pacient cu sindrom de intestin scurt trebuie efectuate în echipă multidisciplinară cu gastroenterolog, endoscopist, chirurg, oncolog, nutriționist, psiholog, medic de familie și includ:
1. investigații referitoare la starea segmentelor intestinale restante și posibile complicații: endoscopie digestivă superioară, colonoscopie, endoscopie cu videocapsulă, enteroscopie, biopsii multiple, scintigrafie de tranzit, laparoscopie second-look, osteodensitometrie, teste de disbioză intestinală, acizi biliari fecali etc.
2. investigații referitoare la statusul nutrițional (proteine totale, albumină, glicemie, lipide, colesterol, trigliceride, teste de coagulare, Ca, Mg, Zn, Se, Fe, feritină, vitamine (A, D, E , K, B12, B9, C)
3. investigații referitoare la boala de bază pentru care s-a efectuat rezecția: computer-tomografie cu contrast , imagistică prin rezonanță magnetică, tomografie cu emisie de pozitroni, scintigrafie etc.
Tratamentul bolii se face în funcție de simptome, segmentul rezecat, impactul nutrițional, boala de bază.
44 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
Special dezvoltat pentru
colonoscopia de calitate superioară!
2 Gust de lime a a a a
Volum redus (2L)
1,2
1 Curăţare excelentă
Mai puţine bule
1,2

Clensia® 1-3 conţine Macrogol 4000, sulfat de sodiu anhidru, simeticonă și electroliţi.
este indicat în golirea intestinului înaintea oricăror proceduri clinice care Clensia® necesită un intestin curat, de exemplu endoscopie intestinală sau examen radiologic.
este indicat la adulţi. Clensia®

Acest material promoţional este destinat profesioniştilor din domeniul sănătăţii. Pentru informaţii suplimentare vă rugăm să co nsultaţi R ezumatul carac te r isticilor produsului co mplet. M edicament eliberat pe bază de prescr ipţie medicală-PRF. Administrare orală. Profesioniștii din domeniul sănătăţii sunt rugaţi să rapor teze orice reac ţie adversă suspec tată sau reclamaţie c u p r i v i r e l a a c e s t m e d i c a m e n t l a a d r e s a d e e - m a i l : D r u g s a fe t y. a l f a s i g m a @ a d d e n d a . r o s a u l a A g e n ţ i a N a ţ i o n a l ă a Medicamentului și a Dispozitivelor Medicale din România https://adr.anm.ro/ DAPP Addenda Pharmaceuticals S.R.L.
Adaptat după: 1. Spada C. et al. Dig Liver Dis. 2017; 49(6): 651-656. 2. Rezumatul carac teristicilor produsului.
Alfasigma România S.R.L. str. Cluceru Udricani, nr. 18, parter și etaj 1, sector 3, București tel.: 031.805.35.26, 031.805.35.27; fax: 031.805.35.28. e-mail: info.ro@alfasigma.com
Carcinoamele ampulare
Carcinoamele ampulare (ACs, ampullary carcinomas) sau carcinoamele ampulei lui Vater sunt tumori rare, reprezentând doar 0.2% dintre cancerele tractului digestiv și aproximativ 7% dintre carcinoamele periampulare [1]. Din punct de vedere anatomic, aceste carcinoame se dezvoltă la nivelul complexului ampular, distal de confluența dintre calea biliară principală și ductul pancreatic [2]. ACs apar mai frecvent la sexul bărbătesc și pot surveni la orice vârstă, constatându-se o incidență mai mare după decada a 5a de viață [3]. Având în vedere frecvența redusă a ACs, la momentul actual nu există recomandări ferme în ceea ce privește management-ul terapeutic al acestor tumori. Datele existente în registrele internaționale demonstrează existența unei incidențe relativ scăzută a ACs în cazul țărilor occidentale, de 0.5 cazuri la 100,000 locuitori, dar, cu toate acestea, studii recente sugerează un trend crescător a ratei de incidență a ACs de-a lungul ultimelor decenii, cel mai probabil în contextul facilitării accesului la serviciile de endoscopie digestivă și îmbunătățirii screening-ului indivizilor cu risc crescut, cum este cazul pacienților cu polipoză adenomatoasă familială (FAP, familiar adenomatous polyposis) [4]. Astfel, acest articol își propune să ofere o imagine de ansamblu în ceea ce privește datele existente în literatura de specialitate despre etiopatogenia și opțiunile terapeutice ale ACs.


ÎAs. Univ. Dr. Petrică Popa
Medic specialist Gastroenterologie, Universitatea de Medicină și Farmacie din Craiova
Dr. Răzvan-Cristian Statie
Medic rezident Gastroenterologie, Universitatea de Medicină și Farmacie din Craiova
n funcție de localizare, ACs pot fi împărțite în trei categorii: (1) neoplasme intraampulare, se disting printr-o dezvoltare intraluminală, fără a depăși sfincterul Oddi; (2) neoplasme periampulare, prezintă o importantă componentă protruzivă, care proemină în lumenul duodenal, de obicei, de natură adenomatoasă, neinvazivă și asociază frecvent, o zonă ulcerată ce corespunde componentei invazive; (3) neoplasme mixte, caracterizate printr-o dezvoltare atât intraampulară, cât și spre lumenul duodenal. În toate cele trei situații, macroscopic, se constată mărirea de volum a regiunii ampulare [5]
Majoritatea ACs sunt adenocarcinoame. Organizația Mondială a Sănătății (WHO, World Health Organization), a revizuit în anul 2010, criteriile pentru diagnosticul histopatologic al ACs, descriind trei subtipuri distincte pe baza caracteristicilor morfologice și imunohistochimice: (1) tipul intestinal; (2) tipul pancreatobiliar; și (3) tipul mixt [6]. Tipul
intestinal asociază frecvent o componentă neinvazivă, corespunzătoare adenomului duodenal. Microscopic, se caracterizează printr-o arhitectură similară cancerului colorectal (CRC, colorectal cancer), cu prezența de glande tubulare sau cribriforme și necroză centrală. Componenta invazivă este, de obicei, mai redusă comparativ cu tipul pancreatobiliar și prezintă mai rar invazie limfovasculară și perineurală. Acest subtip al ACs, poate fi însoțit de prezența unor imunomarkeri intestinali, precum CK20 (cytokeratin 20), MUC2 (mucin2) și CDX2 (caudal-related homeodomain transcription factor 2) [5, 7-10]. Tipul pancreatobiliar este asemănător, din punct de vedere morfologic, cu adenocarcinomul ductal pancreatic sau colangiocarcinomul distal, datorită prezenței unor glande tubulare complexe compuse din celule atipice, asociate cu o stromă desmoplastică abundentă [5]. Imunohistochimic, aceste celule exprimă CK7, MUC1 și MUC5AC [10]. Între 1840% dintre ACs, prezintă un fenotip hibrid, caracterizat prin suprapunerea trăsăturilor celor două subtipuri principale, instestinal și pancreatobiliar, adesea, cu rezultate neconcludente ale testelor imunohistochimice [11, 12]. Aceste aspecte sugerează variabilitatea interobservator ridicată în rândul medicilor anatomopatologi, în clasificarea subtipurilor de ACs [5, 11]. Semnificația clinică majoră a clasificării histologice se reflectă asupra aprecierii prognosticului bolii: supraviețuirea în carcinomul pancreatobiliar este semnificativ mai mică (mediana 33-41 luni), comparativ cu subtipul intestinal (72-80 luni) [11, 13] .
ACs sunt în general neoplasme sporadice, dar similar CRC, acestea pot asocia o componentă neinvazivă ce corespunde secvenței adenom-carcinom la nivelul papilei [14]. Pe de altă parte ACs se pot dezvolta și în contextul unor sindroame familiale. În mod particular, FAP evoluează frecvent cu apariția de adenoame duodenale și prezintă un risc de 100 până la 200 de ori mai mare pentru dezvoltarea ACs [15, 16]. Este sugerată prezența unor mutații somatice diferite la nivelul genei APC, sugerând astfel, existența unor căi distincte referitor la patogenia moleculară a ACs sporadice și cele care apar în contextul FAP [17]. Prin utilizarea unor teste genetice precum secvențierea întregului exom (WES, whole exom sequencing), studii recente au identificat alterări ale genelor asociate ACs, incluzând genele APC, SMAD4, KRAS și TP53 [18, 19]. Mai mult de atât, s-a identificat o nouă genă „conducătoare” (driver gene) pentru ACs, reprezentată de gena supresor tumorală ELF3 [19]. De asemenea, a fost studiată relația dintre subtipurile histologice și mutațiile genice. Similar CRC, subtipul intestinal prezintă o incidență mai mare a mutațiilor genelor APC, KRAS și TP53. Pe de altă parte, în cazul subtipului pancreatobiliar predomină mutațiile genelor „conducătoare” pancreatice SMAD4, KRAS și TP53, cu incidențe asemănătoare celor întâlnite în cazul adenocarcinomului ductal pancreatic [18, 20, 21]. Heterogenitatea semnăturilor genetice corespunzătoare subtipurilor histologice, indică diversitatea tumorală a ACs [14, 18, 19]. Astfel, ar putea fi necesară o revizuire a clasificării histologice, având în vedere absența
46 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
unei relații specifice între subtipul morfologic și caracteristicile moleculare [14]
Cunoașterea profilului molecular al ACs este deosebit de importantă, întrucât a fost demonstrată o acuratețe superioară asupra prognosticului bolii, comparativ cu clasificarea histologică. Mutațiile TP53 și KRAS sunt considerate predictori independenți ai prognosticului nefavorabil în ceea ce privește supraviețuirea, indiferent de subtipul histologic [22]. Caracteristicile moleculare comune între diferitele subtipuri, precum mutațiile KRAS și TP53, pot reprezenta factori determinanți ai progresiei tumorii, aflată într-un stadiu incipient al bolii. În schimb, alte modificări genetice, precum cele caracteristice tipului pancreatobiliar (SMAD4, CDKN2A) sau cele ce aparțin căii de semnalizare moleculară Wnt, pot apărea în cadrul etapelor ulterioare ale creșterii tumorale [5, 14, 18, 19]. Regimurile terapeutice actuale nu separă pacienții pe baza subtipurilor histologice, profilul molecular putând fi astfel utilizat în identificarea unor posibili candidați pentru diverse scheme chimioterapeutice, indiferent de existența unei diferențieri histologice clare [5, 18, 23, 24]. Identificarea alterărilor moleculare caracteristice etapelor avansate ale progresiei tumorale, ar putea susține utilizarea rezecției chirurgicale radicale asociată cu limfadenectomia, în pofida aplicării unor metode de tratament mai conservatoare. Aceste date subliniază importanța analizei genetice și necesitatea integrării acesteia în rapoartele examenelor histopatologice convenționale [5] Tabloul clinic al ACs este asemănător cu cel întâlnit în neoplasmul de cap de pancreas. Simptomul dominant este reprezentat de icterul obstructiv, motiv pentru care ACs asociază o rată crescută de rezecabilitate la momentul diagnosticului [5, 25]. Spre deosebire de icterul din cancerul de cap de pancreas, care are caracter progresiv, în ACs întâlnim un icter de intensitate variabilă, fluctuant. Alte simptome asociate pot include scădere ponderală involuntară, inapetență, greață și vagi dureri abdominale (rareori cu caracter colicativ). Pruritul, urinile hipercrome și scaunele acolice sunt secundare obstrucției biliare. Cu toate acestea, în majoritatea cazurilor pacienții se prezintă cu icter nedureros [26]. În evoluție pot apărea pusee de colangită acută sau episoade de hemoragie digestivă în cantitate mică, care produc anemie, sau importante cantitativ, urmate de emisia de scaune melenice [5]. Examenul obiectiv poate constata în cazul unor pacienți palparea veziculei biliare destinse, nedureroasă (semnul Courvoisier-Terrier). Cu toate acestea, niciuna dintre manifestările cli-
nice enumerate anterior nu sunt sensibile sau specifice pentru tumorile ampulare, putând fi observate, de asemenea, în cazul pseudochisturilor și tumorilor capului de pancreas, litiazei coledociene sau colangiocarcinomului [26]
Algoritmul diagnostic presupune de obicei utilizarea unor investigații imagistice ale abdomenului precum ultrasonografia, tomografia computerizată și/sau rezonanța magnetică, cu scopul de a exclude alte cauze ale icterului și de a realiza stadializarea bolii. Ca urmare a localizării anatomice și a dimensiunilor frecvent reduse ale tumorii, este adesea dificilă vizualizarea unei mase tumorale ampulare, dar semne indirecte precum dilatarea ductului pancreatic și/sau a căilor biliare pot fi observate [5]. Endoscopia deține un rol major pentru diagnosticul diferențial al unei papile modificate macroscopic (fie că este mărită de volum sau ulcerată), precum și pentru evaluarea extensiei loco-regionale a bolii. Biopsiile endoscopice pot asocia rate ridicate ale rezultatelor fals negative pentru adenocarcinom, adesea subestimând patologia reală, în timp ce biopsiile ghidate ecoendoscopic (EUS) îmbunătățesc acuratețea diagnosticului până la o valoare de aproximativ 90% [27-29]. De asemenea, EUS joacă un rol esențial pentru stadializarea locală a tumorilor ampulare, datorită capacității sale de a estima invazia tumorală în profunzimea peretelui duodenal și de a evalua prezența metastazelor la nivelul ganglionilor regionali.
Singura opțiune terapeutică cu potențial curativ este reprezentată, la momentul actual, de rezecția chirurgicală radicală (duodenopancreatectomia), în timp ce papilectomia endoscopică este rezervată tumorilor non-invazive. Rezecția radicală asociată cu limfadenectomie este de obicei recomandată pentru tumorile invazive, chiar și de dimensiuni mici, datorită riscului semnificativ de metastazare ganglionară sau de rezecție incompletă a tumorii. Stadializarea corectă este esențială pentru a ghida deciziile ulterioare privind tratamentul [5]
Papilectomia endoscopică este tratamentul de elecție pentru tumorile benigne sau non-invazive ale ampulei. Dacă EUS identifică o leziune limitată la mucoasă, iar examenul histopatologic nu evidențiază caracteristici sugestive pentru displazie de grad înalt sau invazie, poate fi recomandată ampulectomia endoscopică [30]. Examinarea histologică ulterioară a piesei rezecate endoscopic trebuie să evalueze marginile de rezecție și să ia în considerare eventuala prezență a unei componente invazive [31]. Este sugerat faptul că ampulectomia endoscopică ar trebui inclusă în algorit-
mul diagnostic și considerată a avea potențial curativ în cazul prezenței displazie de grad înalt, dar cu margini de rezecție indemne la evaluarea histopatologică definitivă [5]. Având în vedere morbiditatea și mortalitatea semnificative asociate intervenției chirurgicale, a fost propusă, de asemenea, utilizarea rezecției endoscopice pentru ACs incipiente [32-34] Această afirmație rămâne totuși controversată, în principal datorită riscului semnificativ pentru metastaze ganglionare și a ratei ridicate a marginilor de rezecție pozitive, această opțiune terapeutică fiind rezervată pacienților ce nu pot tolera intervenția chirurgicală [35] Rata complicațiilor postprocedurale asociate ampulectomiei endoscopice este relativ scăzută (aproximativ 10%), cea mai frecvent întâlnită fiind pancreatita acută, urmată de stenoza papilară și colangită. Majoritatea acestor complicații pot fi prevenite prin plasarea unor stenturi pancreatice și/sau biliare temporare [5]
Râmâne încă un subiect controversat dacă terapia oncologică adjuvantă oferă un beneficiu în ceea ce privește supraviețuirea pacienților care beneficiază de rezecția ACs. Relația dintre subtipul histologic și răspunsul la chimioterapie reprezintă un subiect de larg interes. Este sugerat faptul că subtipul intestinal ar trebui să beneficienze de tratament asemănător celui pentru CRC, iar subtipul pancreatobiliar ar trebui tratat similar cancerului de pancreas [5, 14]. Cu toate acestea, nu a fost observat vreun beneficiu al supraviețuirii pacienților cu subtip intestinal ce au urmat chimioterapie adjuvantă. Pacienții cu adenocarcinom ampular de tip pancreatobiliar și/sau mixt ce a fost rezecat, ar putea beneficia de chimioterapie adjuvantă pe bază de gemcitabină, deși rezultatele unui studiu retrospectiv au arătat că terapia adjuvantă a fost administrată mai frecvent pacienților cu factori de prognostic nefavorabil, însă nu a fost constatată o supraviețuire mai bună, indiferent de subtipul histologic al tumorii [36]
În ciuda faptului că în ultimii ani am asistat la dezvoltarea unor noi opțiuni terapeutice destinate diverselor tipuri de neoplazii, tratamentul malignităților rare, inclusiv al ACs, rămâne provocator ca urmare a inexistenței de suficiente date bazate pe dovezi. Astfel, sunt necesare eforturi suplimentare pentru a realiza o clasificare superioară a subgrupurilor de pacienți cu ACs și pentru a îmbunătăți cunoștințele referitoare la evoluția și prognosticul acestei afecțiuni gastrointestinale rare, ce ridică încă numeroase probleme la care uneori există dificultăți în furnizarea unei soluții adecvate.
Bibliografie pe: revistamedicalmarket.ro
47 Articole de specialitate Gastroenterologie 2024 - 2025
Tulburări ale dispoziției
– anxietatea şi depresia la copiii cu boli inflamatorii intestinale
„Toate bolile încep în intestine.”- Hipocrate, sec. III î.Hr.
Chiar dacă acum câțiva ani ar fi fost mai dificil de crezut că există o corelație între microbiota intestinală și creier, acum se vorbește tot mai des despre acest lucru și se fac tot mai multe studii care evidențiază necesitatea alegerii unei alimentații, în concordanță cu coabitarea bacteriilor microbiene bune de la nivelul intestinului, pentru a combate tulburările afective (1, 3) .

Asist. Univ.
Dr. Adriana Cojocaru
UMF „Victor Babeș” Timișioara, Clinica de Psihiatrie
Copii și Adolescenţi, Timișoara, Președinte al Societății de Neurologie și Psihiatrie a Copilului și Adolescentului din România

Dr. Josan Jennifer
Clinica de Psihiatrie Copii și Adolescenţi, Timișoara Secretar General al Societății de Neurologie și Psihiatrie a Copilului și Adolescentului din România
Etiologia bolii Crohn și a colitei ulcerative nu este bine delimitată, dar în prezent se înțelege că se referă la interacțiunea complexă dintre variabilele genetice și de mediu, care rezultă într-un răspuns inflamator intestinal inadecvat și exagerat la indivizii vulnerabili (1, 2) .
Microbiota cuprinde microorganisme simbiotice comensale și patogene, cu rol principal în reglarea imunității. Astfel, toate acestea depind de factori precum nașterea, alăptarea, predispoziție genetică, factori de mediu, utilizarea antibioti-
celor, stresul emoțional și fiziologic etc. (2,4). Microbiota intestinală comunică cu Sistemul Nervos Central (SNC) prin căile neuroimune, neuroendocrine și căile neuronale formând acest supranumit ax de reglaj. Sistemul nervos enteric și sistemul nervos central iau naștere din același țesut embrionar. Studiile recente au constatat rolul important al microbiotei în neuroplasticitate, atât la nivelul SNC cât și la nivelul SNE. Pentru fiecare 1 mesaj transmis prin nervul vag, de la SNC către intestin, există 6 mesaje de la intestin către SNC. Mai mult microbiota poate modifica echilibrul triptofanului cu formarea de serotonină (2, 4, 5, 7)
Serotonina, o moleculă de semnalizare critică în axa intestin-mircobiotă-creier, este produsă majoritar de celulele enterocromatofine din intestin.S-a demonstrat că unele componente ale microbiotei intestinale au efecte benefice în tulburările psihice prin secreția deneurotransmițători(7).Astfel tot mai multe sudii susțin că prezența unei afecțiuni medicale cronice, precum bolile inflamatorii intestinale, este adesea asociată cu rate mai mari de anxietate și depresie în comparație cu populația generală, mai mult, simptomele acestor afecțiuni sunt mai severe în perioadele de boală activă cu evoluție mai gravă la pacienții depresivi(6, 8, 9, 10) .
La pacienții cu Boala Chron (BC), anxietatea sau depresia apare de 5 ori mai frecvent decât în populația generală, iar la pacienții cu Colită ulcerativă (CU), anxietatea apare de aproape 4 ori mai des și depresia de 2 ori mai des decât la lotul de
control.Alte studii au arată că două treimi dintre cei cu o tulburare de anxietate (65%) și peste jumătate dintre cei cu o tulburare de dispoziție (54%) au avut primul debut cu 2 ani sau mai mult înainte de diagnosticul Boală inflamtorie intestinală (BII) (11,12, 17, 25)
Experienţa BII este suficient de stresantă pentru a declanșa sau intensifica starea psihică, dar, totodată anxietatea sau depresia pot fi suficiente pentru a declanșa sau exacerba BII(12, 13) .
Mecanismele din spatele relației BII – depresie/anxietate includ creșterea citokinelor proinflamatorii, semnalizarea nervului vag, disbioza intestinală și modificările funcționării și morfologiei creierului(14).
La copil și adolescent bolile inflamatorii intestinale pot perturba dezvoltarea psihomotorie și fizică. În plusmedicamentele administrate pentru controlul afecţiunii sau intervenţiile chirurgicalepot afecta dezvoltarea fizică și pot conduce la dezechilibre psihologice și scăderea performanţelor școlare. Este importantă alianța terapeutică, colaborarea dintre gastroenterolog-familie-psiholog-psihiatru-școală și alte specialități (15) .
Un studiu calitativ care evaluează utilizarea medicamentelor antidepresive pentru pacienții cu BII în cabinetele de gastroenterologie a constatat că majoritatea specialiștilor gastroenterologi (78%) și-au tratat pacienții cu antidepresive ca terapie adjuvantă, în special pentru durere sau dificultăți de somn. Jumătate au tratat în mod specific depresia sau anxie-
48 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie

tatea la pacienții lor, în timp ce restul, au trimis pacienții cu depresie la un specialist în sănătate mintală sau la medicul de familie. Majoritatea nu credeau că medicamentele antidepresive au influențat în mod direct BII, dar au observat că tratamentul tulburării comorbide a îmbunătățit calitatea vieții pacientului și a îmbunătățit capacitatea acestora de a gestiona BII(15, 16, 17)
Literatura clinică despre antidepresive sugerează că acestea sunt sigure și sunt la fel de eficiente atât pentru tulburările de anxietate, cât și pentru tulburările depresive. Mulți dintre pacienți, întrerup tratamentul în primele săptămâni sau luni, adesea din cauza efectelor secundare, limitând eficacitatea tratamentului, în special având în vedere recomandările ca tratamentul medicamentos să continue cel puțin un an(15, 16, 17) .
Pacienții pot fi mai capabili să gestioneze efectele secundare sau să le tolereze în timpul inițierii tratamentului dacă sunt conștienți de ele, precum și de potențialele beneficii de a persista până când s-au adaptat la medicament.Efectele secundare gastrointestinale pot fi de îngrijorare deosebită pentru pacientul cu BII.Aceste reacții adverse sunt în general legate de doză și tind să scadă în primele săptămâni de tratament. Diareea a fost raportată mai des la Sertralină decât la celelalte SSRI, iar creșterea în greutatelaParoxetină și Mirtazapină. În unele cazuri, poate exista o scădere în greutate la începutul tratamentului și o creștere în greutate mai târziu(18, 20) .
Psihoeducația cu accent pe efectele secundare poate ajuta ca pacienții să fie complianți la medicamentele antidepresive. Se cunosc puține date în ceea ce privește factorii de risc pentru distresul psihologic și în special factorii socio-economici asociați cu suferința psihologică din BII.Antidepresivele și terapiile comportamentale arată nu numai eficacitate în tratamentul depresiei și anxietății, dar pot să atenueze simptomele BII sau să scadă riscul de recidivă, deși dovezile sunt încă limitate(19, 21, 22)
Literatură de specialitate susține eficacitatea terapiilor cognitiv-comportamentale pentru anxietate și depresie. Terapia cognitiv-comportamentală a fost evaluată într-un studiu cu adolescenți cu depresie majoră (n = 11) și un studiu controlat randomizat la adolescenți cu de-
presie subsindromală (n = 41). În ambele studii, tratamentul a redus semnificativ depresia și a îmbunătățit funcționarea globală. Pentru cei care au avut și o tulburare de anxietate comorbidă, a existat și o reducere semnificativă a anxietății. Îmbunătățirile simptomelor psihiatrice au fost menținute la 12 luni de urmărire atât în probele pentru adolescenți, cât și pentru adulți, sugerând o bună durabilitate a efectului(9, 10, 23, 24)
În concluzie tulburările de dispoziție sunt comorbidități comune în boala inflamatorie intestinală (BII).Relația dintre BII-depresie și anxietate pare să fie bidirecțională. Tratamentul eficient al anxietății sau depresiei poate reduce suferința și poate duce la îmbunătățirea funcționării și a calității vieții. Sunt necesare cercetări suplimentare pentru a evalua cele mai eficiente abordări ale tratamentului anxietății și depresiei în contextul BII.
Microorganismele care ne colonizează ne controlează și funcţia cerebrală, având un rol important în modularea funcției neuronale și a comportamentului.
Bibliografie
1. Chandra S, Alam MT, Dey J, et.al, HealthyBrain: The GutMicrobiome in NeurodegenerativeDisorders. Curr Top Med Chem. 2020;20(13):1142-1153. doi: 10.2174/15680266206662004 13091101. PMID: 32282304
2. Cenit MC, Sanz Y, Codoñer-Franch P. Influence of gutmicrobiota on neuropsychiatricdisorders. World J Gastroenterol. 2017 Aug 14;23(30):5486-5498. doi: 10.3748/wjg.v23.i30.5486. PMID: 28852308; PMCID: PMC5558112
3. Cryan JF, O’Riordan KJ, Cowan CSM, Sandhu KV, et.al, The Microbiota-Gut-Brain Axis. Physiol Rev. 2019 Oct 1;99(4):18772013. doi: 10.1152/physrev.00018.2018. PMID: 31460832
4. The foodconnection – dr. UmaNaidoo
5. Brainmaker – dr. David Perlmutter
6. Mohajeri MH, La Fata G, Steinert RE, Weber P. Relationship between the gut microbiome and brain function.Nutr Rev. 2018 Jul 1;76(7):481-496. doi: 10.1093/nutrit/nuy009. PMID: 29701810
7. Kelly JR, Clarke G, Cryan JF, Dinan TG. Brain-gut-microbiota axis: challenges for translation in psychiatry. Ann Epidemiol. 2016 May;26(5):366-72. doi: 10.1016/j.annepidem.2016.02.008. Epub 2016 Mar 8. PMID: 27005587.
8. Petra AI, Panagiotidou S, Hatziagelaki E, Stewart JM, Conti P, Theoharides TC. Gut-Microbiota-Brain Axis and Its Effect on Neuropsychiatric Disorders With Suspected Immune Dysregulation.ClinTher. 2015 May 1;37(5):984-95. doi: 10.1016/j.clinthera.2015.04.002. PMID: 26046241; PMCID: PMC4458706.
9. Firth J, Gangwisch JE, Borisini A, Wootton RE, Mayer EA. Food and mood: how do diet and nutrition affect mental wellbeing? BMJ. 2020 Jun 29;369:m2382. doi: 10.1136/bmj.m2382. Erratum in: BMJ. 2020 Nov 9;371:m4269. PMID: 32601102; PMCID: PMC7322666
10. Scott KM, Bruffaerts R, Tsang A, et al. Depression-anxietyre-
lationshipswithchronicphysicalconditions: resultsfromthe World Mental Healthsurveys. J AffectDisord. 2007; 103: 113–120. DOI: 10.1016/j.jad.2007.01.015
11. Leue C, van Os J, Neeleman J, et al. Bidirectionalassociationsbetweendepression/anxietyandboweldisease in a populationbasedcohort. J EpidemiolCommunityHealth. 2005; 59: 434–435
12. L M Kurina, M J Goldacre, D Yeates, L E Gill, Depressionandanxiety in peoplewithinflammatoryboweldisease, J EpidemiolCommunityHealth 2001;55:716–720
13. StéphaneNahon, MD, Pierre Lahmek, MD, ChristelleDurance, Alain Olympie, et al., RiskFactors of AnxietyandDepression in InflammatoryBowelDisease, InflammatoryBowelDiseases, Volume 18, Issue 11, 1 November 2012, Pages 2086–2091, https://doi.org/10.1002/ibd.22888
14. Tania H. Bisgaard, Kristine H. Allin, LaurieKeefer, Ashwin N. Ananthakrishnan, Depressionandanxiety in inflammatoryboweldisease: epidemiology, mechanismsandtreatment,NatureReviewsGastroenterology&Hepatology volume 19, pages717–726 (2022)
15. GlynisByrne, GregRosenfeld, YvetteLeung, et al., Prevalence of AnxietyandDepression in PatientswithInflammatoryBowelDisease, Volume 2017 | Article ID 6496727 | https://doi. org/10.1155/2017/6496727
16. Ruth Ann Marrie MD, PhD a b, John R. Walker PhD c d, Lesley A. GraffPhD , et al., Performance of administrative case definitions for depressionandanxiety in inflammatoryboweldisease, Journal of PsychosomaticResearch, Volume 89, October 2016, Pages 107-113
17. AntoninaMikocka-Walus, Valerie Pittet ‖, Jean-BenoîtRossel ‖, Roland von Känel, Symptoms of DepressionandAnxiety Are Independently Associated WithClinicalRecurrence of InflammatoryBowelDisease, ClinicalGastroenterologyandHepatology, Volume 14, Issue 6, June 2016, Pages 829-835.e1
18. David J. GracieBSc, MBChB, MRCP, Alexander C. Ford MBChB, MD, PsychologicalComorbidityandInflammatoryBowelDiseaseActivity: Cause or Effect?, ClinicalGastroenterologyandHepatology, Volume 14, Issue 7, July 2016, Pages 1061-1062
19. Keefer, L., Kane, S.V., Document details - Consideringthebidirectionalpathwaysbetweendepressionand IBD: Recommendations for comprehensive IBD care, GastroenterologyandHepatology, Volume 13, Issue 3, March 2017, Pages 164-169
20. www.nhs.uk/conditions/inflammatory-bowel-disease/
21. https://www.hopkinsmedicine.org/health/conditions-and-diseases/inflammatory-bowel-disease
22. AntoninaMikocka-Walus, Simon R. Knowles, LaurieKeefer, LesleyGraffPhD, ControversiesRevisited: A Systematic Review of theComorbidity of DepressionandAnxietywithInflammatoryBowelDiseases, InflammatoryBowelDiseases, Volume 22, Issue 3, 1 March 2016, Pages 752–762, https:// doi.org/10.1097/MIB.0000000000000620, Published: 03 February 2016
23. Lesley A. Graff, PhD, John R. Walker, PhD, Charles N. Bernstein, MD, DepressionandAnxiety in InflammatoryBowelDisease:A Review of Comorbidityand Management, InflammatoryBowelDiseases, Volume 15, Issue 7, 1 July 2009, Pages 1105–1118, https://doi.org/10.1002/ibd.20873, Published: 22 January 2009
24. Podolsky DK. Inflammatoryboweldisease. N Engl J Med. 2002; 347: 417–429 2002 Aug 8;347(6):417-29. doi: 10.1056/ NEJMra020831
25. 16. Graff LA, Walker JR, Lix L, et al. The Manitoba IBD CohortStudy: therelationship of diseasetypeandactivitytopsychologicalfunctioningand quality of life. Clin Gastroenterol Hepatol.2006; 4:1491–1501.DOI: 10.1016/j.cgh.2006.09.027
50 www.revistamedicalmarket.ro
de specialitate Gastroenterologie
Articole












Str. Nisipari, nr. 27, sector 1, București; tel/fax 021.317.91.88/89, e-mail: office@vavian.ro

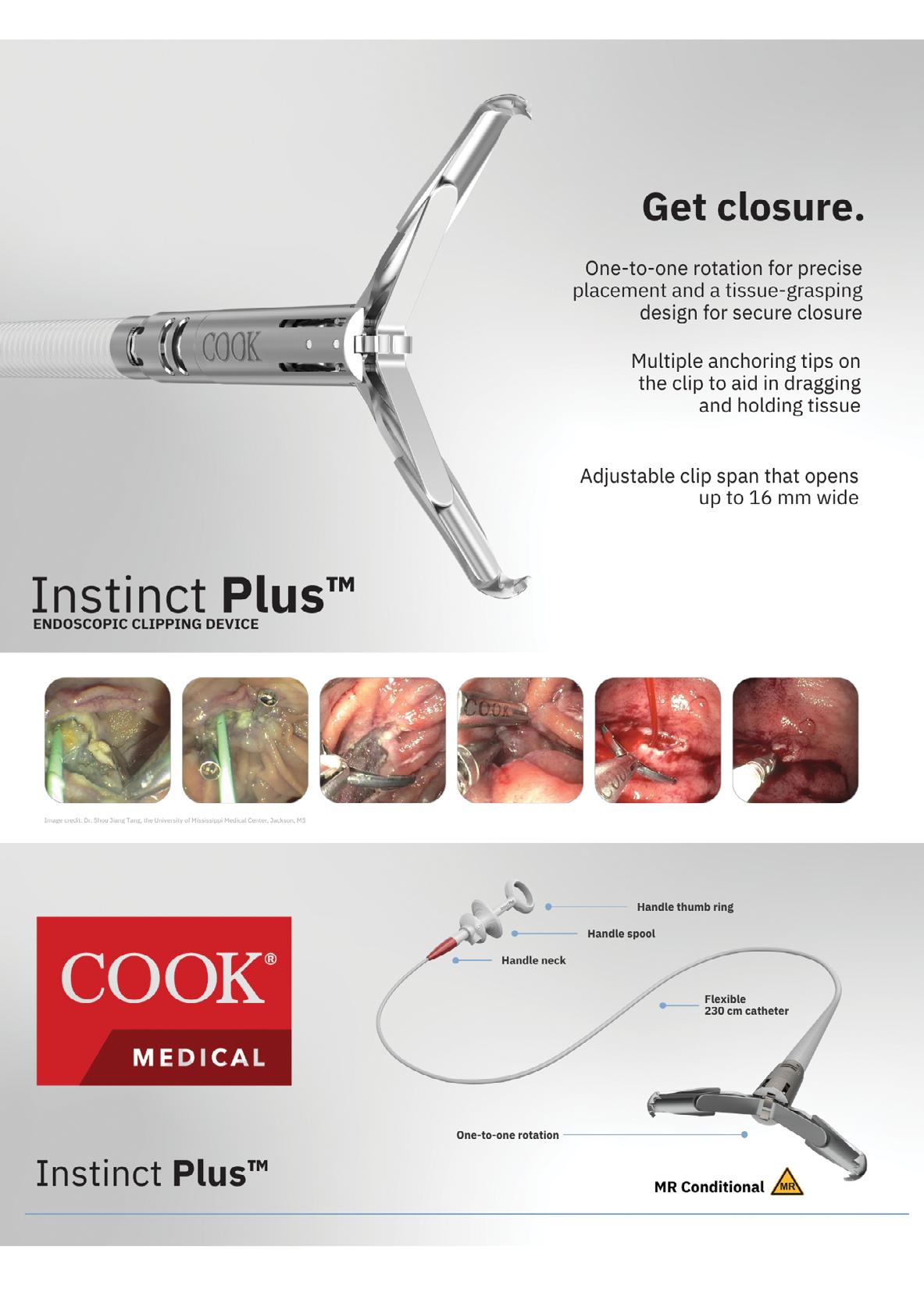

Str. Nisipari, nr. 27, sector 1, București; tel/fax 021.317.91.88/89, e-mail: office@vavian.ro
Cum refacem deficitul nutrițional?
Soluția oferită de familia de produseResource©
Nutriția este una dintre funcțiile esențiale ale organismului uman. Ea este descrisă în sens mai larg şi polisemantic, conform Agenției ONU pentru Alimentație şi Agricultură (Food and Agriculture Organization, FAO) ca „ştiința modului în care organismul foloseşte componentele alimentelor pentru a creşte, a se dezvolta şi a funcționa corect. Nutriția este un domeniu multidisciplinar care cuprinde diverse aspecte ale ştiinței alimentare, biologiei şi sănătății şi joacă un rol fundamental în sănătatea generală şi calitatea vieții indivizilor şi comunităților“. Sub aspect clinic, nutriția este procesul prin care substanțele preluate prin alimente din mediu sunt transformate în structuri specializate ale organismului, spre a furniza energie pentru toate funcțiile şi activitățile fizice şi psihice din viața curentă. Buna desfăşurare a funcției de nutriție determină starea de nutriție a unei persoane.

UMF Iuliu Hațieganu, SCJU Cluj, Past-chairman EAGEN (Asociația Europeană de Gastroenterologie, Endoscopie și Nutriție)
Nutriția fiziologică
Starea normală de nutriție este considerată cea care corespunde indicelui de masă corporală cuprins între 18,5 și 24,9. Abaterile în sus, sau în jos de la acest index reflectă a stare de nutriție globală alterată (deficit ponderal, respectiv suprapondere și obezitate). Dar, variațiile de la normal ale nutriției se pot manifesta și sub aspect calitativ. Acest aspect reprezintă tulburările de nutriție cauzate de deficite alimentare sau de aport insuficient în condiții de solicitări crescute (gravide, eforturi fizice, boli consumptive).
Din punct de vedere calitativ, există mai multe categorii de nutrienți, mulți indispensabili organismului: hidrații de carbon, proteinele, lipidele, vitaminele, sărurile minerale, fibrele alimentare și apa. Unii se găsesc în cantități mici și sunt denumiți micronutrienți. Spre deosebire de nutrienți, vorbim si de nutrimente, adică de produși finiți ai digestiei sau de substanțe care se absorb fără a trece prin procesele fizico-chimice ale digestiei. Exemple de nutrimente sunt glucoza și alte oligozaharide, acizii aminati, acizii grași, minerale, vitamine și apa.
Malnutriția
Aspectele patologice legate de starea de nutriție sunt malnutriția și formele ei. Malnutriția se referă la denutriție sau supranutriție, adică la nutriție deficitară, respectiv în exces. Mai nou, se includ în cadrul malnutriției și riscurile produse de diete excesive (ortorexie, anorexie, diete neștiințifice). În sens mai larg, malnutriția se referă la denutriție, care ea însăși are multe cauze: deficit de aport, malabsorbție, maldigestie, tulburări psihice etc. Malnutriția poate fi prin deficit proteo-caloric, dar prin deficit de micronutrienți, cauzat de malabsorbții selective, aport redus, lipsa elementelor din mediu, necesități
crescute în momente fiziologice, condiții patologice sau eforturi fizice.
Pe plan global, o treime din populație este afectată de subnutriție, mai ales în emisfera sudică. În România, conforma datelor World Bank, 2,5% din populație suferă de denutriție, iar rata de deces ajustată la vârstă este de 0.38%. Deficitele selective, cauzate de sarcină, boli consumptive (1), supraactivitate fizică sunt însă mai frecvente și trebuie recunoscute spre a fi tratate. Două forme particulare și severe de denutriție sunt: cașexia și sarcopenia (2, 3) .
Cașexia se definește ca pierderea extremă în greutate și pierderea masei musculare. Deși frecvent este asociată cu cancerul, de fapt cașexia apare și în alte boli consumptive, de exemplu HIV, insuficiență cardiacă congestivă foarte avansată, cordul pulmonar sever etc. În cașexie apare pierdere ponderală, atrofie musculară, epuizarea rezervelor adipoase. Debutează prin precașexie și evoluează spre cașexie refractară.
Sarcopenia reprezintă o suferință asemănătoare, asociată sau nu cașexiei. Se caracterizează pin pierderea masei musculare și a funcției locomotorii. Apare la vârstnici și în caz de imobilizare, de asemenea în boli cronice precum ciroza hepatică sau bolile inflamatorii intestinale, Se asociază cu fragilitate, tulburări cognitive progresive și căderi, declin funcțional, mortalitate crescută. Tratamentul denutriției
Este evident că denutriția neselectivă și cea selectivă se tratează prin substituție și atunci când se poate, etiologic sau patogenetic. Un grup major de tratamente este reprezentat de suplimentarea nutrițională orală. De această suplimentare au mare nevoie persoanele cu denutriție, cu cașexie sau sarcopenie, dar și persoanele sănătoase cu necesități sporite de suplimentare a nutriției. În contextul multitudinii de cazuri care necesită nutriție orală suplimentară, este necesară practicarea medicinei bazate pe dovezi. Două publicații demonstrează eficiența acestora, deși, desigur, suplimentarea nutrițională orală nu este panaceu. Totuși concluziile sunt încurajante (4, 5)
Dieta elementală în tratamentul denutriției și a necesarului de suplimente.
Este evidentă necesitatea de a corecta pe cale orală (și la nevoie pe sondă naso-enterală) deficitele globale și selective din denutriție. Ingestia de flacoane de alimentație elementală este recomandată, iar dieta polimerică este considerată a fi mai bine tolerată pentru gustul său. Printre alternative, proba timpului a trecut-o gama produselor Nestlé denumită Resource (6). Acest grup include produse care oferă nutriție suplimentară sau unică atât pentru copii, cât și pentru adulți. Sunt suplimente nutritive orale sau pentru alimentație enterală compuse în mod special pentru cerințe nutriționale speciale, inclusiv denutriție, diabet, pacienți cu escare și imobilizați. Conțin produse de așa-numită dietă polimerică, special adecvate pacienților cu boli inflamatorii intestinale. Dar produsele se adresează și pacienților oncologici, cu cașexie, cu sarcopenie, a celor cu necesități sporite de micronutrienți. Având ocazia să le folosesc în străinătate, m-am convins de valoarea produselor din gama Resource și de acceptabilitatea mare din partea pacienților (produsele sunt palatabile și oferite în șase variante de gusturi).
Bibliografie
1. Sabo CM, Simiras C, Ismaiel A, Dumitrascu DL. Diet and Gut Inflammation: The Effect of Diet on Inflammatory Markers in Inflammatory Bowel Disease - A Scoping Review. J Gastrointestin Liver Dis. 2023;32(3):402-410.
2. Iacob S, Beckebaum S, Dumitrascu DL, Gheorghe L. Editorial: Sarcopenia, Frailty and Nutrition in Liver Diseases. Front Nutr. 2022;9:929459.
3. Ismaiel A, Bucsa C, Farcas A, Leucuta DC, Popa SL, Dumitrascu DL. Effects of Branched-Chain Amino Acids on Parameters Evaluating Sarcopenia in Liver Cirrhosis: Systematic Review and Meta-Analysis. Front Nutr. 2022; 9:749969.
4. Stratton RJ, Elia M. A review of reviews: a new look at the evidence for oral nutritional supplements in clinical practice. Clin Nutr Supplements. 2007;2(1):5–23
5. Baldwin C, Smith R, Gibbs M, Weekes CE, Emery PW. Quality of the Evidence Supporting the Role of Oral Nutritional Supplements in the Management of Malnutrition: An Overview of Systematic Reviews and Meta-Analyses. Adv Nutr. 2021 31;12(2):503-522.
6. https://www.nestlehealthscience.com.au/brands/resource

54 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
Prof. Dan L. Dumitrașcu

CARACTERISTICI RESOURCE
kcal
Dietă completă nutriţional
Hipercalorică (Resource 2.0, Resource 2.0 cu fibre, Resource Protein), aport sporit de proteine (Resource Protein)
Aport de antioxidanţi: vitaminele A, C, E, Seleniu, Zinc
Fără gluten






Dietă lichidă polimerică gata preparată pentru consum
CUI SE RECOMANDĂ
6 arome disponibile: Caise, Vanilie, Ananas-Mango, Căpșune, Cacao și Cafea
RESOURCE?

Adulţi şi copii cu vârsta peste 3 ani
TĂU ÎN GESTIONAREA MALNUTRIȚIEI
PARTENERUL
www.nestlehealthscience.ro
Rectocolita ulcero-hemoragică în sarcină
Prezentare de caz
Introducere. Rectocolita ulcero-hemoragică (RCUH) şi boala Crohn (BC) sunt formele majore de boală inflamatorie intestinală (BII), ce prezintă caracteristici particulare şi necesită abordare terapeutică distinctă. RCUH reprezintă o afecțiune inflamatorie cronică a tractului digestiv caracterizată prin perioade de activitate şi remisiune, a cărei etiopatogenie este incomplet explicată. Cea mai frecventă ipoteză are la bază interacțiunea dintre substratul patogenic imun, microbiota şi factorii de mediu la subiecții cu predispoziție genetică. În RCUH inflamația interesează rectul şi se poate extinde proximal la nivelul colonului fără a depăşi valva ileo-cecală. Tabloul clinic este determinat de extensia şi severitatea inflamației, simptomele cele mai sugestive sunt diareea sanguinolentă şi rectoragia care pot fi însoțite de tenesme rectale, dureri abdominale difuze/crampe, proctalgii, senzația de defecație imperioasă. Diagnosticul pozitiv se stabileşte în baza unui ansablu de argumente clinice, endoscopice, imagistice şi histologice.

RAs. Univ.
Dr. Ana-Maria Ghiuchici
Clinica de Gastroenterologie
și Hepatologie, UMF
„Victor Babeș” din Timișoara
CUH poate afecta femeile tinere aflate în perioada reproductivă, cu implicații asupra fertilității, sarcinii și alăptării. Managementul bolii active în timpul sarcinii poate fi o provocare, iar remisiunea poate fi dificil de obținut.
Prezentare caz clinic. Pacientă în vârstă de 31 de ani, fără antecedente personale patologice, cu istoric familial negativ, prezintă în primul trimestru de sarcină 1-2 scaune moi/zi și rectoragie minimă motiv pentru care efectuează un consult gastroenterologic. Examenul clinic obiectiv este normal, teste de laborator în limite normale cu excepția calprotectinei fecale -260 ng/g fecale, rectoscopia relevă eritem, granularitate, diminuarea desenului vascular și friabilitate la nivelul mucoasei rectale. Se stabilește diagnosticul de proctită formă ușoară scor Mayo 1 și se decide inițierea tratamentului cu Mesalazină supozitoare 1g/zi cu evoluție favorabilă și normalizarea scaunelor. În săptămâna 34 de sarcină pacienta se prezintă în serviciul de urgență al Clinicii de Obstetrică-Ginecologie acuzând contracții uterine dureroase nesistematizate, scaune diareeice multiple cu sânge proaspăt și dureri abdominale localizate în pelvis. S-a evaluat și monitorizat starea mater-
no-fetală ecografic și cardiotocografic, rezultatele menținându-se în parametrii fiziologici. S-a administrat tratament antispastic și tocolitic, s-a efectuat profilaxia detresei respiratorii fetale cu corticoterapie (Dexametazonă 6 mg/12 ore, 4 doze) și reechilibrare hidroelectrolitică. Pacienta este referată către Clinica de Gastroenterologie SCJUPBT cu stare generală ușor influențată, sarcină în evoluție, activitate cardiacă fetală prezentă, fără semne de suferință fetală acută.
Examenul obiectiv la prezentare relevă paloare sclero-tegumentară, abdomen destins prin uterul gravid, dureros la palpare în etajul abdominal inferior, scaune diareice cu sânge multiple >10/24 h, sindrom emetic.Testele de laborator evidențiază leucocitoză (20000/m3↑), trombocitopenie ușoară (275 000/m3 ↓), anemie moderată (Hb = 9.1 g/dl ↓), sindrom inflamator (PCR= 125 mg/l ↑; Fibrinogen= 286 mg/dl ↑;VSH= 45 mm/1h ↑), hipoproteinemie cu hipoalbuminemie (Proteine totale= 6,1g/dl ↓; Albumina = 2.2 g/dl ↓) și valori ridicate ale Calprotectinei fecale (1601ng/g fecale). Examen coproparazitologic, Toxina A și B Clostridium difficile, Coprocultura, Urocultura, Hemoculturi - negative. Ecografia abdominală (Figura 1) evidențiază colon cu perete bine vizibil, cu perete îngroșat până la 10 mm, cu ștergerea stratificării și ascită minimă.
Diagnostic pozitiv: Rectocolită ulcero-hemoragică formă pancolică în puseu acut scor parțial Mayo 8 puncte Anemie normocromă normocitară formă moderată. Sarcină 34 săptămâni, făt unic
viu, membrane intacte, prezentare cefalică, amenințare de naștere prematură.
Tratamentul pe parcursul internării a inclus soluții de reechilibrare hidroelectrolitică, antiemetice, antalgice, Mesalazină cp 1g, 3 x 1 cp/zi și supozitoare 1g/zi, Albumina 20% 100 ml/zi și inițierea corticoterapiei sistemică cu Hemisuccinat de Hidrocortizon i.v. 200 mg/zi.
Evoluția sub tratament la 48h este staționară, fără remiterea simptomatologiei, însă cu accentuarea durerilor abdominale și apariția contracțiilor uterine. După reevaluarea ginecologică, pacienta naște prin operație cezariană, făt viu, unic, de sex feminin, Scor APGAR 8, G=2600 g pentru indicația RCUH în puseu acut. După 2 zile postoperator pacienta revine în Clinica de Gastroenterologie când se decide escaladarea terapiei prin inițierea tratamentului biologic cu agenți anti-TNF-α - Infliximab 300 mg (a doua perfuzie a fost administrată după 2 săptămâni). După prima perfuzie de Infliximab evoluția pacientei este lent favorabilă cu remiterea parțială a simptomelor și îmbunătățirea constantelor biologice; dar cu persistența a 7-8 scaune sanguinolente/zi.
Pacienta este consiliată psihologic și evaluată chirurgical având în vedere răspunsul slab la tratamentul conservator. La 7 zile după administrarea perfuziei 2 de Infliximab pacienta prezintă mai mult de 10 scaune/zi cu crampe severe, rectoragie, sensibilitate abdominală la palpare, hipotensiune arterială, tahicardie și paloare. Teste de laborator: Hb= 6,2 g/dL, CRP= 171 mg/L. Se efectuează RMN abdominal care descrie modificări infla
56 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie
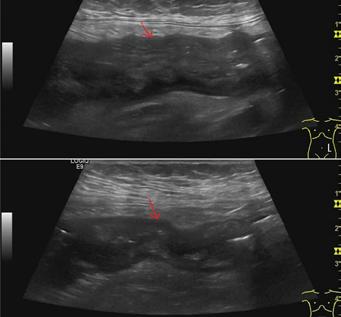
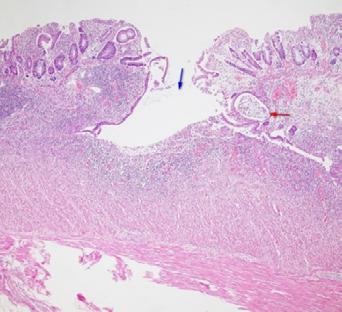
matorii difuze ce interesează colonul și la nivelul grăsimi pericolice, se exclude megacolonul toxic (Figurile 2A, 2B). Se decide reevaluare chirurgicală având în vedere lipsa răspunsului la tratamentul conservator și necesitatea transfuziilor sanguine zilnice, însă pacienta refuză intervenția chirurgicală. În 48 h pacienta este conștientă, cooperantă, dar cu stare generală sever influențată, prezentând hematochezie severă și semne de șoc hemoragic (hipotensiune ce nu răspunde la corecția volemică, tahicardie, paloare, timp de umplere capilară prelungit) Hb= 4,2 g/dL post-administrare II unități CER - se decide intervenția chirurgicală de urgență. Intraoperator se descrie aspect de pancolită, cantitate importantă de sânge proaspăt la nivelul colonului, mucoasa colonică edemațiată, friabilă cu sângerare difuză în pânză. Se practică colectomie totală cu prezervarea rectului mediu și inferior cu ileostomă terminală iliacă dreaptă. Piesa de exereză este evaluată histopatologic - mucoasă colonică subțire cu anomalii arhitecturale glandulare, ulcerații, abcese criptice, infiltrat inflamator polimorf bogat, vase hiperemice, extravazate hematice (Figurile 3A, 3B).
Evoluția postoperatorie este favora-
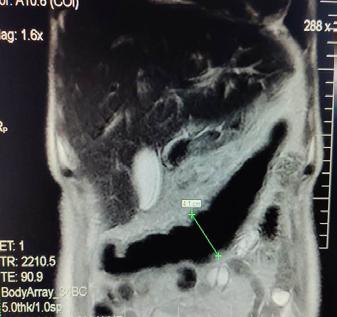
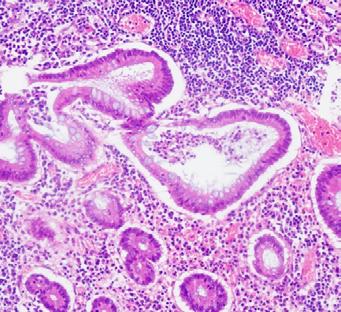
bilă cu parametrii respiratori, cardiaci și hemo-dinamici stabili, afebrilă, cu tranzit prezent pe ileostomă și toleranță bună la reluarea alimentației pe cale enterală, cu îmbunătățirea stării generale și a parametrilor biologici, pacienta fiind externată după 2 săptămâni cu recomadarea de a continua tratamentul cu Mesalazină supozitoare 1g/zi.
Discuții. Evoluția RCUH în timpul sarcinii se corelează cu nivelul activității bolii în momentul concepției. Dacă, concepția are loc într-o perioadă de remisiune clinică, boala va continua probabil să fie inactivă pe tot parcursul sarcinii; în timp ce RCUH activă la concepție se poate agrava progresiv în timpul sarcinii cu creșterea riscului de naștere prematură și greutate mică la naștere. Debutul RCUH în sarcină este mai puțin frecvent și este asociat cu un prognostic nefavorabil.
Conform ghidului ECCO, majoritatea medicamentelor utilizate în tratamentul BII sunt considerate a fi sigure atât pentru mamă, cât și pentru făt. Corticoterapia convențională și preparatele nonsulfatate de 5-ASA (Mesalazina) nu cresc riscul de anomalii congenitale. Intervenția chirurgicală de urgență este indicată în prezența complicațiilor acute precum colita acută
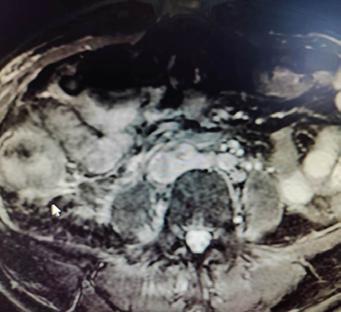
Figura 1. Ecografie abdominală – colon cu perete bine vizibil, îngroşat până la 10 mm.
Figura 2A. RMN abdomen- excludere megacolon toxic.
Figura 2B. RMN abdomen -modificări inflamatorii difuze parietale şi în grăsimea pericolică.
Figura 3A. Examen histopatologic - perete colonic subțire, mucoasă cu anomalii arhitecturale glandulare, ulcerație (săgeata albastră) şi abces criptic (săgeata roşie). Colorația HE, x4.
Figura 3B. Examen histopatologic - mucoasă colonică cu anomalii arhitecturale glandulare, infiltrat inflamator polimorf bogat, vase hiperemice, extravazate hematice, abcese criptice. Colorația HE, x40.
fulminantă refractară la tratament conservator, megacolon toxic, perforație sau hemoragie digestivă severă.
Concluzii. Managementul sarcinii asociate RCUH este complex și necesită implicarea unei echipe multidisciplinare. La pacientele cu BII este importantă planificarea sarcinii în perioada de remisiune a bolii cu menținerea acestui status pe toată perioada sarcinii. Medicația uzuală din RCUH (excepție Metotrexat și Tofacitinib) nu reprezintă un risc pentru mamă, făt sau alăptare. Complicațiile acute necesită intervenție chirurgicală de urgență.
Particularitățile cazului: pacienta prezintă debutul bolii în cursul sarcinii cu evoluție fulminantă refractară la tratamentul conservator intensiv.
Bibliografie:
1. Torres J, Chaparro M., Julsgaard M., et. al. European Crohn’s and Colitis Guidelines on Sexuality, Fertility, Pregnancy, and Lactation, Journal of Crohn’s and Colitis, Volume 17, Issue 1, January 2023, Pages 1–27, https://doi.org/10.1093/ecco-jcc/jjac115.
2. Kapasi R, Glatter J, Lamb CA, et al. Consensus standards of healthcare for adults and children with inflammatory bowel disease in the UK. Frontline Gastroenterol. 2019; 11(3):178-187.
3. Andersson P, Söderholm JD. Surgery in ulcerative colitis: indication and timing. Dig Dis. 2009;27(3):335-340.
57 Articole de specialitate Gastroenterologie 2024 - 2025
Figura 1
Figura 3A
Figura 2A
Figura 3B
Noi perspective în pregătirea intestinului
Colonoscopia este o investigație esențială în diagnosticul și, uneori, chiar în tratamentul bolilor colonice. Pentru acuratețea diagnosticului și minimizarea erorilor, colonul trebuie, în prealabil, pregătit corespunzător. O pregătire bună a colonului anterior efectuării procedurii nu permite leziunilor să rămână neobservate din cauza prezenței reziduurilor. Astfel, atât înaintea colonoscopiei, cât și în cazul intervențiilor chirurgicale la nivelul tubului digestiv inferior, se recomandă administrarea unor preparate cu rol de a elimina conținutul intestinal și de a pregăti colonul, scăzând riscul de erori de diagnostic sau de complicații ce pot pune în pericol viața pacienților.
Conf. Univ. Dr. Laura Carina Tribuș
Medic primar Medicină Internă, Medic primar Gastroenterologie, UMF „Carol Davila”
Colonoscopia joacă un rol important în diagnosticul precoce al cancerului colorectal și oferă oportunitatea unui tratament în stadiile incipiente ale bolii, crescând, astfel, durata supraviețuirii și calitatea vieții pacienților. De-a lungul timpului, s-au implementat programe de screening colonoscopic al cancerului colorectal în tot mai multe regiuni ale lumii. Vârsta de debut la care se recomandă începerea screeningului diferă ușor de la ghid la ghid în funcție de regiunea vizată, dar vârsta medie recomandată este 45-50 de ani, investigația urmând a fi repetată periodic(1).
Cancerul colorectal este unul dintre cele mai frecvente cancere întâlnite în populația generală, fiind a doua cauză neoplazică de deces după cancerul pulmonar. Este mai frecvent întâlnit la sexul masculin(2). În ultimii ani s-a observat o scădere a mortalității prin cancer colorectal în rândul pacienților de peste 50 de ani. Acest fapt se datorează atât terapiilor actuale moderne, mult mai efciente decât în trecut, cât și programelor de screening ce permit diagnosticul precoce și, astfel, creșterea speranței și calității vieții. Majoritatea cazurilor de cancer colorectal sunt diagnosticate în urma investigațiilor efectuate pacienților simptomatici. Principalele simptome ce impugn efectuarea investigațiilor colonoscopice pentru a confirma sau infirma un proces neoplazic sunt: hemoragia digestive inferioară, sindroamele anemice și durerile abdominale. Pacienții pot beneficia inițial de investigații radiologice precum computer tomograf (CT) sau clismele cu bariu, dar colonoscopia rămâne investigația de elecție, având o sensibilitate de aproximativ 95% și permițând
diagnosticul macroscopic și histopatologic deoarece oferă posibilitatea recoltării de biopsii. Cu toate acestea, în aproximativ 25% din cazuri, adică 1 din 4 colonoscopii, eșuează* din cauza intestinului pregătit insuficient (*vizibilitate improprie).
Programele de screening au, de asemenea, o importanță semnificativă prin efectuarea colonoscopiei la pacienții asimptomatici, 11% din cazurile de neoplasm colorectal precoce fiind diagnosticate în acest mod. În plus, colonoscopia de screening oferă posibilitatea diagnosticării leziunilor premaligne, acestea putând fi îndepărtate anterior transformării maligne. Dar pentru aceasta colonul trebuie pregătit corespunzător, pentru a nu permite omiterea acestor leziuni care, de cele mai multe ori, sunt mici, plate și pot fi ușor ratate din cauza prezenței reziduurilor.
Colonoscopia poate, de asemenea, diagnostica diverse alte patologii colonice, precum bolile inflamatorii intestinale, diverticuloza colonică, angiodisplazia colonică, leziunile de ischemie mezenterică și patologia hemoroidală(3)
Pregătirea colonului
Pregătirea colonului este o condiție esențială pentru vizualizarea optimă a mucoasei colorectale. Aceasta își găsește utilitatea și în cazul altor proceduri precum intervențiile chirurgicale ce interesează regiunea abdominală. Un intestine incomplet curățat poate avea consecințe precum: vizualizarea incompletă a intestinului în timpul intervențiilor colonoscopice (cu compromiterea consecutivă a investigației și necesitatea repetării acesteia sau chiar omiterea anumitor elemente patologice), creșterea dificultății și a timpului necesar realizării colonoscopiei, creșterea riscului de reacții adverse și a riscului de complicații infecțioase post-colonoscopie, precum și creșterea mortalității postoperatorii atunci când se
efectuează în contextul intervențiilor chirurgicale abdominale.
În practică se utilizează scalele Boston și Harefield – ele evaluează gradele de pregătire intestinală. În cazul ambelor scale de evaluare, o curățare adecvată este considerată atunci când se obține un scor 2, 3 (scala Harefield) sau 2 (scala Boston) pe fiecare segment și pentru o curățare de înaltă calitate 3, 4 Harefield și 3 (scala Boston)(5,6), afirmă unii specialiști în gastroenterologie.
Comunicarea medic-pacient
Pregătirea colonului pentru investigațiile colonoscopice este o etapă foarte importantă în care comunicarea medic-pacient este esențială. Fiind, de obicei, un proces destul de laborios, pregătirea trebuie explicată în detaliu pacientului folosind toate ustensilele disponibile pentru a asigura o bună înțelegere și o bună complianță, maximizând, astfel, beneficiile procedurii ce va avea loc. S-a observat că furnizarea unor instrucțiuni detaliate, sub formă vizuală sau în format video, folosirea de aplicații sau mesaje telefonice, are efect benefic în ceea ce privește complianța la administrarea preparatelor pentru pregătirea colonului(7). Pe lângă explicarea etapelor de pregătire pentru colonoscopie prin consumul substanțelor destinate acestui scop, este importantă și expunerea detaliată a dietei și a consumului de lichide în perioada de pregătire, acestea având un rol esențial în calitatea procesului. Transmiterea acestor informații și în format scris, vizual sau video poate îmbunătăți complianța pacientului. În plus, anterior efectuării colonoscopiei, comunicarea medic-pacient este esențială nu doar pentru explicarea pregătirii, ci și pentru informarea pacientului cu privire la indicațiile colonoscopiei, la ce presupune această procedură, care sunt beneficiile și riscurile și ce complicații pot apărea în timpul acesteia.
58 www.revistamedicalmarket.ro Articole de specialitate Gastroenterologie







































































































































































