3.3 carga neta +1
L o s a m i n o á c i d o s p u e d e n a c tua r co m o á c i d o s y co m o b a s e s
carga neta 0
carga neta –1
neutro
forma iónica
forma catiónica
67
Zwitterion isoeléctrico COOH +
H 3N
C
H
H+ +
pKa = 2.34
H+
COO– H 3N
C
R
H
pKa = 9.69
COO– H2N
R
C
H
R
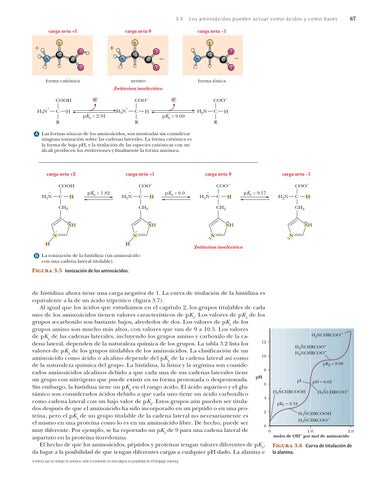
A Las formas iónicas de los aminoácidos, son mostradas sin considerar ninguna ionización sobre las cadenas laterales. La forma catiónica es la forma de bajo pH, y la titulación de las especies catiónicas con un álcali producen los zwitteriones y finalmente la forma aniónica.
carga neta +2
carga neta +1
COOH +
C
H3N
H
COO
COO pKa = 1.82
+
C
H3N
CH2
H
pKa = 6.0
C
NH
carga neta –1
–
+
H3N
CH2
H
COO– pKa = 9.17
C
H2N
CH2
NH
+
H
CH2
NH
NH
+
N H
carga neta 0
–
N H
N
N
Zwitterion isoeléctrico
B La ionización de la histidina (un aminoácido con una cadena lateral titulable).
Figura 3.5 Ionización de los aminoácidos.
de histidina ahora tiene una carga negativa de 1. La curva de titulación de la histidina es equivalente a la de un ácido triprótico (figura 3.7). Al igual que los ácidos que estudiamos en el capítulo 2, los grupos titulables de cada uno de los aminoácidos tienen valores característicos de pKa. Los valores de pKa de los grupos a-carboxilo son bastante bajos, alrededor de dos. Los valores de pKa de los grupos amino son mucho más altos, con valores que van de 9 a 10.5. Los valores de pKa de las cadenas laterales, incluyendo los grupos amino y carboxilo de la ca12 dena lateral, dependen de la naturaleza química de los grupos. La tabla 3.2 lista los valores de pKa de los grupos titulables de los aminoácidos. La clasificación de un 10 aminoácido como ácido o alcalino depende del pKa de la cadena lateral así como de la naturaleza química del grupo. La histidina, la lisina y la arginina son conside8 rados aminoácidos alcalinos debido a que cada una de sus cadenas laterales tiene pH un grupo con nitrógeno que puede existir en su forma protonada o desprotonada. 6 Sin embargo, la histidina tiene un pKa en el rango ácido. El ácido aspártico y el glutámico son considerados ácidos debido a que cada uno tiene un ácido carboxílico 4 como cadena lateral con un bajo valor de pKa. Estos grupos aún pueden ser titulados después de que el aminoácido ha sido incorporado en un péptido o en una pro2 teína, pero el pKa de un grupo titulable de la cadena lateral no necesariamente es el mismo en una proteína como lo es en un aminoácido libre. De hecho, puede ser 0 muy diferente. Por ejemplo, se ha reportado un pKa de 9 para una cadena lateral de aspartato en la proteína tioredoxina. El hecho de que los aminoácidos, péptidos y proteínas tengan valores diferentes de pKa, da lugar a la posibilidad de que tengan diferentes cargas a cualquier pH dado. La alanina e A menos que se indique lo contrario, todo el contenido en esta página es propiedad de ©Cengage Learning.
H2NCHRCOO– + H3NCHRCOO– H2NCHRCOO–
pK2 = 9.69
pI
pH = 6.02
+
H3NCHRCOOH
+
H3NCHRCOO–
pK1 = 2.34 +
H3NCHRCOOH + H3NCHRCOO– 0
1.0 2.0 moles de OH– por mol de aminoácido
Figura 3.6 Curva de titulación de la alanina.