Cap. 1 Estrutura e Ligação 13
H H H C C H H H
H
H
H
C
C
H
H
H
CH3CH3
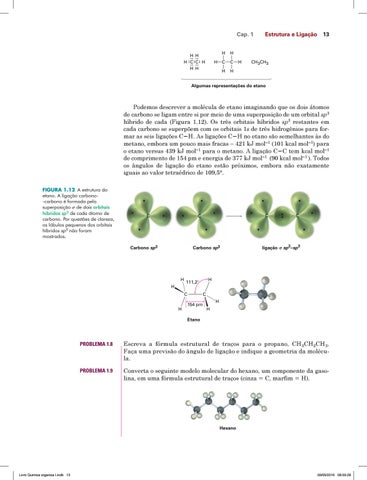
Algumas representações do etano
Podemos descrever a molécula de etano imaginando que os dois átomos de carbono se ligam entre si por meio de uma superposição de um orbital sp3 híbrido de cada (Figura 1.12). Os três orbitais híbridos sp3 restantes em cada carbono se superpõem com os orbitais 1s de três hidrogênios para formar as seis ligações CH. As ligações CH no etano são semelhantes às do metano, embora um pouco mais fracas – 421 kJ mol–1 (101 kcal mol–1) para o etano versus 439 kJ mol–1 para o metano. A ligação CC tem kcal mol–1 de comprimento de 154 pm e energia de 377 kJ mol–1 (90 kcal mol–1 ). Todos os ângulos de ligação do etano estão próximos, embora não exatamente iguais ao valor tetraédrico de 109,5°. FIGURA 1.12 A estrutura do etano. A ligação carbono-carbono é formada pela superposição de dois orbitais híbridos sp3 de cada átomo de carbono. Por questões de clareza, os lóbulos pequenos dos orbitais híbridos sp3 não foram mostrados.
C
C
C
Carbono sp3
Carbono sp3
H H
H
sp3–sp3
H
111,2 C
ligação
C
C
154 pm
H H
Etano
PROBLEMA 1.8
Escreva a fórmula estrutural de traços para o propano, CH3CH2CH3. Faça uma previsão do ângulo de ligação e indique a geometria da molécula.
PROBLEMA 1.9
Converta o seguinte modelo molecular do hexano, um componente da gasolina, em uma fórmula estrutural de traços (cinza 5 C, marfim 5 H).
Hexano
Livro Quimica organica I.indb 13
09/05/2016 08:59:28