

ХЕМИЈА
ОПШТУ И ГИМНАЗИЈУ ПРИРОДНО-МАТЕМАТИЧКОГ СМЕРА, МЕДИЦИНСКУ
санитарно-еколошки техничар, педијатријска сестра–техничар, гинеколошко-акушерска сестра, медицинска сестра–васпитач и осталe делатности личних услуга
Хемија
Рецензенти
доцент др Јелена Пољаревић, Хемијског
Јасна Петровић, професор Прве
Слађана Басуровић, професор Медицинске
Манојле Шалипуровић, професор у
Уредник
др Иван Живадиновић
Одговорни уредник
Главни уредник др Милорад Марјановић
За издавача
ISBN 978-86-17-20290-1
8.4. Изједначавање
8.5. Лимитирајући
8.7.
8.8.
1.
Хемија објашњава појаве које се свакодневно дешавају око нас. Примера је безброј, од хемијски једноставних, на пример рђања гвожђа, па до сложе-
нијих, рецимо, зашто лишће жути или како се храном одржавамо у животу.
Хемија утиче на све аспекте нашег живота и свакодневно се срећемо са хемијским производима, од лекова,
намештаја, ђубрива, па до хемијског оружја и експлозива. У једној реченици – хемија изучава структуру и својства супстанце (облика материје) и промене кроз које она пролази. Учећи основне хемијске принципе, трудићемо се да их приметимо
објашњење експерименталних података,
уколико
речима

1.1. Meрења


броја цифара. Број цифара мора да одговара поузданости датог мерења, односно прецизност диктира број значајних
(6,0±0,1) cm3
6,1 cm3 . Ако меримо масу неке супстанце на аналитичкој ваги, њена маса ће бити изражена у грамима, бројем који садржи четири децимале јер је толика поузданост мерења на аналитичкој
маса
супстанце износи 2,2360 g, њу ћемо написати у облику (2,2360±0,0001) g.
Мерења се могу унапређивати коришћењем бољих прибора, уређаја
инструмената, а непоузданост увек
инструмента, док је последња цифра увек непоуздана.
1.3.
3.
5.
цифре.
Такође, постоји група правила која се односи
1. Приликом одузимања и сабирања одговор
цифара
2.
41,9.
Питања и задаци
1. Претворити следеће вредности: 0,076 l у cm3; 5,0∙10–8 m у nm; 5,66∙10–3 s у ms; 1,55 kg/m3 у g/dm3 . (Решење: 76 cm3; 0,5 nm; 5,66 ms; 1,55 g/dm3)
2. Која је просечна маса три предмета ако су појединачне масе 10,3 g, 9,334 g и 9,25 g?
(Решење: 9,6 g)
3. Која је запремина тела изражена у cm3 ако су његове димензије 22,86 cm x 38,0 cm x 76 cm?
(Решење: 66 020 cm3)
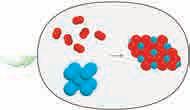
2. ВРСТЕ
Универзум, односно целокупна природа, сачињен је од материје. Материја, то јест све што нас окружује, организована је на различите начине, а може постојати у два облика: као супстанца коју карактерише физичка величина маса и која заузима простор и као поље сила које карактерише енергија. Изучавање хемије почећемо класификацијом супстанци. Два су принципа класификовања супстанце: у
2.1. Агрегатна стања
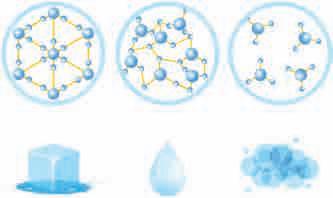
чисте.
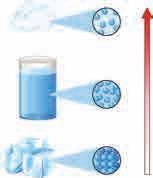
Хомогене смеше често називамо растворима.
2.1.2. Раздвајање смеша на чисте компоненте
Смеша, било хомогена било хетерогена, може да се разложи на саставне компоненте физичким методама. Избор методе за разлагање смеша на компоненте, најпре, зависи од физичких и хемијских својстава компоненти смеше. Тако, на пример, смешу

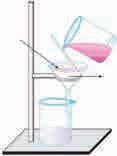
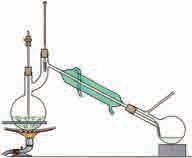

на Земљи, док су други производ нуклеарних реакција у лабораторијама. За означавање елемената хемичари користе хемијске симболе. Прво слово хемијског елемента је увек велико, а друго је мало (уколико га има). На пример, Cо је симбол кобалта, а CО угљеник (II)оксида. Симболи неких елемената су изведени из латинских имена, каo на пример Au од речи aurum (злато), Fe од ferrum (гвожђе), док је већина симбола изведена из енглеских имена. Атоми елемената могу да реагују градећи једињења. Гасовити водоник
бурно реагују дајући воду, чија се својства значајно разликују од својстава

опет добити лед. Према томе, температура топљења је физичко својство. Међутим, ако водоник и кисеоник реагују
воду, то је њихово хемијско својство. Након хемијске промене, настала је нова супстанца, другачијих хемијских и физичких својстава,
можемо добити водоник и кисеоник неком физичком променом, на пример
хлађењем или загревањем.
Мерљива својства супстанци припадају
екстензивна и интензивна својства. Екстензивна својства зависе
количине посматране супстанце. Таква су, на пример, маса и запремина. За разлику од њих измерене вредности интензивних величина не зависе од количине узорка. То су, на пример, температура или
ности се не могу сабирати. Замислимо да у две чаше имамо исту запремину воде исте температуре. Након мешања ових течности, укупна запремина ће бити једнака збиру првобитних запремина, али ће температура бити иста као у појединачним узорцима.
Питања и задаци
1. Супстанце: пудинг, морску воду, магнезијум, бензин, ваздух, сок од парадајза, кристале јода и песак сврстајте у чисте супстанце или смеше. Уколико је смеша, наведите
хетерогена.
2. Који су симболи следећих елемената: сумпора, магнезијума, угљеника, азота, јода, калијума, бакра, злата?
3. Како бисте раздвојили на компоненте следеће смеше: шећер и песак; гвожђе и сумпор?
4. Наведите имена следећих елемената: F, Ni, Al, Ag, H, O, Pb, Sn.
5. Бела чврста супстанца означена са А загревана
3.
Још од древних времена људи су покушавали да проникну у структуру материје (супстанце). Данашње модерно схватање структуре материје почиње да се обликује почетком XIX века, појавом Далтонове атомске теорије.
Знамо да су све супстанце сачињене од атома, молекула и јона и да се све гране хемије (неорганска, органска, биохемија) баве овим честицама. У V веку п. н. е. грчки филозоф Демокрит је сматрао да се материја састоји од веома малих недељивих честица које је назвао атомима (грч аtomos = недељив). Иако Демокритове ставове нису прихватили многи његови савременици, а нарочито
модерним дефиницијама елемената и једињења. Године 1808.
1.
2.
и хемијским својствима. Атоми једног елемента се
елемента.
3. Једињења се састоје од атома различитих елемената, односно једињења настају сједињавањем атома различитих елемената.
4. Приликом хемијске реакције атоми се сједињавају или раздвајају, при чему не долази до стварања нових или уништавања постојећих атома.
3.1. Структура атома На основу Далтонове
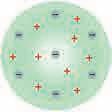
чине протони, концентрисано је у језгру,
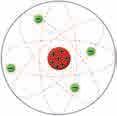
Rutherford, 1871–1937)
протона.
Chadwick, 1891–1972)
Хемија
називамо једноставно водоник, садржи један протон у језгру. Деутеријум садржи један протон и један неутрон, док трицијум садржи један протон и два неутрона. Сва три изотопа садрже један електрон у електронском омотачу.
Атоме елемента уобичајено приказујемо
атомским бомбама, док други
за ту примену. Хемијска својства
3.3. Молекули
елементи
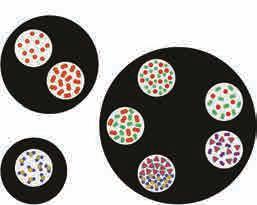
једињења
смеше

OH–, CN–, NH4 + и многи, многи други.
N2O3
Молекулска формула нам, међутим, не указује на структуру молекула, односно на начин на који су атоми повезани. За то служе структурне формуле и у њима су атоми представљени својим симболима,
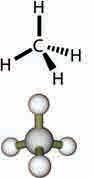
1.
са 39
(Решење: А = 9, А = 48, А = 70)
2. Одредите
40Ca, 119Sn, 244Pu. (Решење: Ca: 20, 20, 20; Sn: 50, 69, 50; Pu: 94, 150, 94)
3. Напишите
5.
6. Попуните
Покушаји научника да објасне структуру
у XIX
нису били потпуно успешни. Требало је времена да научници схвате да се атоми и молекули не понашају по законима који важе у макроскопском свету. Дански физичар Нилс Бор 1 је уочио да Радерфордов модел, који претпоставља да електрони
сурвао” у језгро. Атоми су, међутим, стабилни (са изузетком радиоактивних атома) и могу да зраче само ако им се довeде енергија у облику топлоте или светлости, и тада зраче светлост

је
атому квантификована, међутим, и даље није било потпуно јасно понашање електрона у атому.
4.2. Таласно-механички модел атома
Данашње модерно објашњење структуре атома, подразумева
облику таласа.
Шредингер1 је 1926. године, користећи сложене математичке операције, формулисао једначину
субмикроскопских честица. Ова једначина обухвата
нашање честица.
разумевање као
Schrödinger, 1887–1961)
исте вредности орбиталног квантног броја су поднивои. Магнетни квантни број – ml описује просторну оријентацију
је l = 0, ml je 0, кada je l = 1, ml може бити –1, 0 или 1, а када је l = 2, ml има вредности –1, –2, 0, 1, 2. Укупан број магнетних квантних бројева говори о броју орбитала датог поднивоа. Главни, орбитални









4.4. Електронска
За приказивање распореда електрона у омотачу атома,
називамо електронска конфигурација, важно нам је да знамо енергију (релативну) орбитала. Код атома водоника који садржи један електрон, енергија је одређена само главним квантним
имају исту енергију: За вишеелектронске атоме енергетски
орбиталног
је конфигурација
применићемо Паулијев принцип искључења. Овај принцип каже да два електрона у атому не могу имати иста сва четири квантна броја. Ако два електрона имају исти главни квантни број, орбитални квантни
и
квантни број, другим речима, ако се налазе у
орбитали, разликоваће се по четвртом квантном броју – спину. Дакле, у једној орбитали се
само два електрона, али ће они имати супротне спинове. Атом хелијума који садржи два електрона
електронске конфигурације представљамо писањем племенитог
а затим распоређивањем преосталих електрона у поднивое последњег нивоа. Тако ћемо, на пример, конфигурацију флуора написати [He]2s22p5 Раније је поменуто да се 4s-подниво
је
електронска конфигурација аргона, конфигурацију калијума ћемо представити као [Ar]4s1, где [Ar] означава конфигурацију аргона. Електрони који се налазе у последњем непопуњеном
. Елементи од скандијума (Z = 21) до бакра (Z = 29) су прелазни метали. Прелазни метали имају делимично
конфигурација кобалта, чији je редни број 27, гласи
Лантаниди
тала, укључујући лантан и хафнијум (Z = 72), протеже се
(
n-поднивоа. На пример, ако је n = 2, постоје два поднивоа (две вредности) орбиталних квантних бројева 0 и 1;
2. сваки подниво квантног броја садржи 2l + 1 орбитала. На пример, ако је l = 1, постоје три орбитале, и то су три p-
3. у орбитали се могу наћи
4.
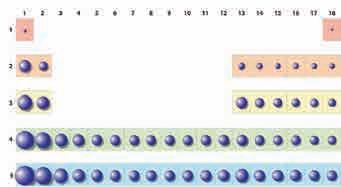
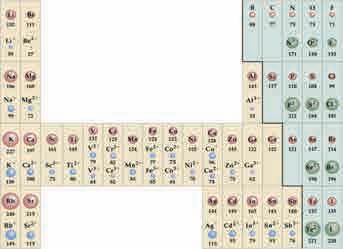
физичким својствима. У савременом
периодама,
систематично класификовани према својим својствима и која
њиховог хемијског понашања.
Многа хемијска својства елемената могу бити објашњена њиховом електронском конфигурацијом. У зависности од поднивоа који се последњи попуњава, елементе ћемо поделити на елементе главних група, племените гасове, прелазне елементе (метале), лантаниде и актиниде (слика 4.9). Елементи главних група имају непопуњене s или pподнивое највећег главног квантног броја своје конфигурације. Са изузетком хелијума (1s2), племенити гасови имају потпуно попуњени p-подниво. Прелазни метали (атоми или јони) имају непопуњене dподнивое, а лантаниди и актиниди (атоми или јони) fподнивое. Zn, Cd
својства. То је нарочито изражено код алкалних метала (елементи прве групе, конфигурације
ns1), земноалкалних метала (елементи друге групе, конфигурације валентног нивоа ns2), племенитих гасова (елементи осамнаесте групе, конфигурације валентног нивоа ns2np6). Видети демонстрациони оглед 4.1 на страни 44. Елементи неких група се, међутим, значајно разликују у својим хемијским својствима – на пример четрнаесте групе, конфигурације ns2np2. У случају прелазних метала, електронска конфигурација се не може уопштено приказати, али је сличност хемијског понашања
сваког осмог елемента јављају сличне хемијске особине. Ову правилност је формулисао као Закон о октавама. Међутим, испоставило се да ова законитост не важи за елементе теже од калцијума, те је због тога овај закон научна заједница брзо одбацила. Неколико година касније, тачније 1869. године, руски хемичар Мендељејев и немачки хемичар Мајер,
предлажу много
класификацију елемената, такође засновану на периодичном понављању својстава елемената са повећањем атомских маса. Мендељејева класификација је била прецизнија у груписању елемената, а он је, такође претпоставио и постојање до тада неоткривених елемената, нпр. екаалуминијума (ekaпрви, што је значило први испод алуминијума у групи).
редних
у предвиђању физичких, а нарочито хемијских својстава елемената. Значај периодног система, између осталог,
4.5.1. Енергија јонизације
је
(у kJ/mol) потребна за издвајање електрона из основног стања атома
наелектрисан јон. X(g) + енергија → X+(g) + e–Вредност енергије
везан у атому.
(Dmitri Ivanovich Mendeleev,
(John Alexander Reina Newlands, 1838–1898)
(Julius Lothar Meyer, 1830–1895)
6

само валентне електроне. Једноставно, унутрашњи електрони су сувише чврсто
предао другом атому, па чак и делио са другим атомима.
4.5.2. Афинитет према електрону
Афинитет према електрону је топлотни ефекат
Хемија
и електрицитета од метала. У периодама слева надесно опада метални, а расте неметални карактер елемената. У Периодном систему групе су означене бројевима од 1 до 18, а веома често се елементи прве групе називају алкални, друге земноалкални, шеснаесте халкогени, седамнаесте халогени, а осамнаесте племенити гасови.
4.5.3. Атомски
могу бити невезивни и везивни. Невезивни полупречници су растојање до кога
(Решење: l = 0, 1, 2, 3)
2.
3. Које бројчане
(Решење: m e = –2, –1, 0, 1, 2; dорбитале)
3p, 2s, 4f, 5d
n = 3, l = 2; n = 2, l = 0; n = 4, l = 3; n = 5, l = 2) 4.
5.1. Луисови симболи Познавање
2
дођу у контакт, спољашњи, валентни
електрон атома литијума прелази на атом флуора. Користећи Луисове симболе (симбол
елемента и тачкица за сваки валентни
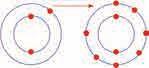
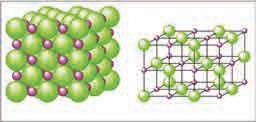
електрона као племенити гас неон. Једињење магнезијумоксид
оксидни анјон: 2Li + O ⟶ 2Li+ + O 2− . 1s22s1 1s22s22p4 [He] [Ne] Kaда на повишеној температури
магнезијумнитрид (Mg3N2).
3 Mg(s) + N2(g) → Mg3N2
5.3.
јонских супстанци. Све до почетка XIX века
истих елемената као и елемената блиских вредности енергија јонизације
водоник у елементарном стању јавља у облику двоатомног молекула. Како оба атома имају исту
енергију јонизације
Примери су молекули кисеоника и азота. N N N≡N
Ковалентна веза настаје и између атома различитих елемената. Луисовом структуром је приказан молекул воде: H O H H−O−H H O H .
Настајање ових молекула илуструје октетно правило, односно тежњу атома (свих сем водоника) да у свом валентном нивоу имају осам електрона. Овом правилу подлежу атоми елемената друге периоде, док се за остале веома често при формирању везе јавља одступање од октетног правила.
5.3.1. Правила писања Луисових структура
Луисове
позиције. На пример, CO3 2– NF3 пракажемо на следећи начин:
Затим се саберу сви
одреди њихов укупан број. Притом се води рачуна о наелектрисању, уколико се ради о јону. Тако је, на пример, код CO3 2– број валентних електрона: 4 (валентни електрони угљеника) + 3 × 6 (по шест
кисеоника) + 2 (наелектрисање анјона) = 24 eлектрона.
3. Централни атом са околним
4.
6. Уколико нема довољно електрона да се
5.3.2 Oдступање од октетног правила Неки атоми приликом формирања
односно у свом валентном нивоу немају осам електрона. Примери су молекули са непарним бројем електрона, NO, NO2, ClO2, молекули у којима атоми имају
1.
3.
електричну струју. У таблици 5.1 дато је поређење физичких својстава NaCl (типично
ним растварачима, а када јесу, не
5.3.4. Електронегативност
Карактеристика ковалентне везе јесте образовање заједничких електронских парова. Код молекула водоника, који се састоји од идентичних атома водоника, електрони су једнако расподељени између
како је у
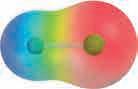
и великог афинитета ка електрону (лако прима електрон) имаће велику електронегативност, док ће, на пример, натријум имати
7
својства ковалентних
Елементи изразито различите електронегативности, као на пример неметали (горњи десни угао периодног система) и метали (доњи леви угао периодног система) градиће јонску везу. На пример, када реагује најелектронегативнији елемент флуор (4,0) са елементом најмање електронегативности − цезијумом (0,8), због велике разлике у електронегативности, наградиће се јонско једињење које
фосфора у молекулу фосфина.
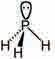
поларне ковалентне и јонске везе, али је усвојено правило по коме атоми
је разлика електронегативности већа од 1,9 образују јонску везу. Када је разлика мања од 1,9, настаје поларна ковалентна веза.
5.3.5. Геометрија молекула
Геометрија молекула је тродимензионални распоред атома у молекулу. Распоред атома у молекулу утиче на физичка и хемијска својства, као што су температура топљења, температура кључања, густина, као и реакције којима подлеже. Дужина и углови веза се одређују експериментално,
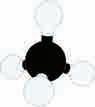


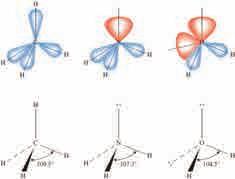
немају диполни момент услед геометрије код које долази до потирања диполних момената. Узмимо, на пример, угљеник(IV)оксид (угљендиоксид). Свака од веза је поларна, али, како је молекул линеаран, долази до потирања диполних момената и молекул је неполаран.
О=C=O
линеарни молекул (без диполног момента)
Молекул воде (H2O) такође има две поларне О−H
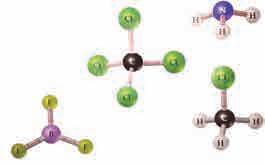

(CH
неспарена електрона, гради две једноструке везе
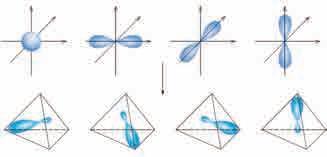
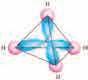

тале угљениковог
хибридних
преклапање
са
Код етина се јавља трострука
угљеникових атома учествују s
једна p, док две p орбитале остају нехибридизоване и задржавају свој облик. Преклапањем sp хибридне орбитале угљениковог атома са s орбиталом
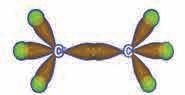
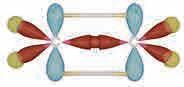
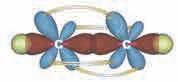
5.5. Метална веза
Највећи број елемената у периодном систему су
Осим живе (температура топљења –39°C), галијума (температура топљења 29,8°C) и цезијума (температура топљења 28,4°C) сви остали
температури и атмосферском притиску,

да се лако деформишу, на пример извлаче у жице и фолије.
3. Користећи Луисове симболе представите реакцију између Ca и F.
4. Које једињење настаје реакцијом
трисања
5. Користећи Луисове симболе
SiCl4 из Si и Cl.
6. Напишите Луисову структуру HCN.
7. Користећи само Периодни систем, у свакој групи, изаберите најелектронегативнији атом: а) Se, Rb, O, In; б) Al, Ca, C, Si; в) Ge, As, P, Sn; г) Li, Rb, Be, Sr.
8. Помоћу ОВЕП теорије, објасните разлике у угловима H−N−H веза: NH2 –105°, NH3 107°, NH4 + 109°.
9. Прикажите преклапање а) две sорбитале; б) s и pорбитале; в) две pz-орбитале претпостављајући да се оба језгра налазе на zоси; д) две py орбитале претпостављајући да се оба језгра налазе на zоси.




6.4. Водонична веза
Температура кључања често
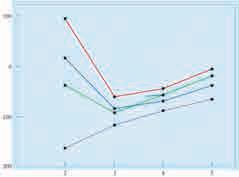
Наиме, између ових молекула, амонијака, воде и флуороводоника, јавља се посебан тип међумолекулских диполдипол интеракција које називамо водонична веза. Водонична веза је интеракција између водоника из поларне везе (N˗H, О˗H, F˗H) и слободног електронског пара на малом електронегативном атому или јону (обично F, O
је приказујемо тачкицама, односно испрекиданим линијама:
A−H···A. Да би дошло до ове интеракције, атом водоника треба да буде везан за изразито електронегативни атом, као што су флуор, кисеоник и азот. Услед везе са јако електронегативним атомом, атом водоника постаје практично
огољени протон и може да оствари блиску и јаку електростатичку интеракцију са електронегативним атомом, флуором,

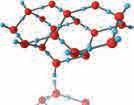
атоми нису фиксирани на сталним положајима, остварују се
6.5. Aгрегатна стања
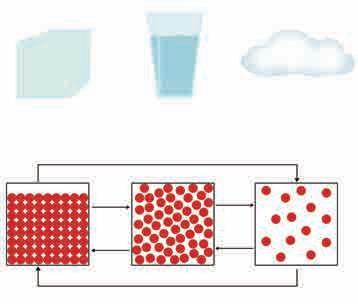
може лако предвидети. Другим речима, гасови се понашају веома слично, без обзира на то из којих честица се састоје.

1/P (1/Pa)
(Robert Boyle, 1627–1691)
The Skeptical Chymist, 1661)
1
6.5.3. Својства чврстих супстанци Чврста супстанца
јединице, атоми, молекули, јони, налазе на тачно одређеним

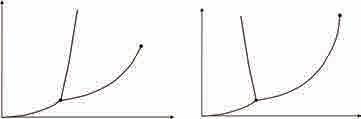
6.5.4. Фазни прелази Веома често се једна супстанца може јавита у два агрегатна стања, једно поред другог. На пример, коцке леда у чаши воде. Тада се каже да се у систему налазе различите фазе. Дакле, фаза је хомогени део система у додиру са другим деловима система, али одвојен добро дефинисаном границом. Промене агрегатних стања се називају фазне промене. Слика 6.11.
потребно уложити више енергије за раздвајање честица (молекула, јона, атома), односно за прелаз из уређенијег у неуређеније стање. Агрегатна стања се, такође, могу мењати променом притиска јер већи примењени притисак фаворузује кондензованије стање, течно над гасовитим, а чврсто
агрегатним стањем. Фазни дијаграми су
Питања и задаци
1. Три агрегатна стања поређајте по: а) порасту међумолекулских сила; б) повећању неуређености; в) томе које је агрегатно стање најлакше сабити на мању запремину.
2. Наведите нека својства идеалних гасова.
3. Објасните везу између јачине међумолекулских интеракција и температуре кључања течности.
4. A) Боца за роњење садржи 0,29 kg кисеоника у запремини од 2,3 dm3 . Израчунати притисак гаса на 9° C. Б) Коју запремину заузима ова количина кисеоника на 100 kPa и 26° C? (Решење: 9,24 MPa; 225 dm3)
5. Колики је притисак у тениској лоптици ако садржи 0,33 g N2 у запремини од 144 cm3 на температури од 24° C? (Решење: 202,1 kPa)
6. Које међумолекулске силе је потребно превазићи да би се следеће супстанце
а) I2; б) CH3CH2OH; в) H2Se?
7. Супстаце: BaCl2, H2, CO, HF и Ne
кључања.
8. У којој од следећих супстанци
CH4, H2NNH2, CH3F, H2S?
Демонстрациони огледи
6.1. Сублимација јода
Јод је на нормалним условима чврста супстанца.
7. ДИСПЕРЗНИ СИСТЕМИ
До сада смо изучавали структуру и својства чистих супстанци у гасовитом, течном или чврстом агрегатном стању. Међутим, у свакодневном животу смо окружени смешама, као што су ваздух који дишемо, вода коју користимо или храна коју једемо. У овом поглављу ћемо изучавати смеше, а ограничићемо
7.1. Раствори Раствори
јаче од интеракција које постоје између самих
молекула растворене супстанце и самих молекула растварача, растварање ће бити фаворизовано, а поред растварања биће примећено и ослобађање топлоте, односно загревање раствора. Уколико су пак слабије, приметиће се везивање топлоте, односно хлађење раствора. Видети демонстрациони оглед 7.1 на страни 87. О топлотним
више речи у поглављу 8.7. Да бисмо
хемијских реакција
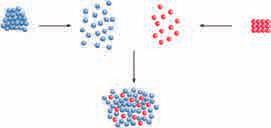
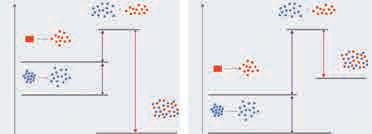

управо, неуређеност. Чиста растворена супстанца и чист растварач
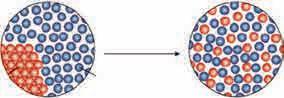
јер је, привлачење, на пример, између молекула угљентетрахлорида
упоредиво са интеракцијама између самих молекула угљентетрахлорида и самих молекула бензена. Јонске супстанце, попут натријумхлорида, лако ће се растварати у поларним супстанцама, као што је вода, јер ће доћи до јондипол интеракција које нису могуће између јона и
растварача, као што је, рецимо,
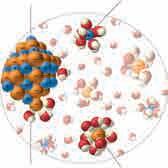
је, на пример, растварање CaCl2
праћено ослобађањем топло-
те, а NH4NO3 везивањем топло-
те, али се растворљивост обе
соли ипак повећава са порас-
том температуре. Зависност се
зато одређује екпериментално
и на слици 7.6 је приказана за-
висност растворљивости неких
соли од температуре. Ова зависност се користи за раздвајање
смеше раствора појединих соли.
Та техника се назива фрак
циона кристализација.

Засићени
од количине растворене супстанце

7.5. Квантитативни састав раствора – изражавање концентрације раствора
За квантитивно проучавање раствора, потребно је знати количину супстанце, односно количину реактаната, када изучавамо хемијске реакције у раствору. У општем смислу, концентрација раствора је количина растворене супстанце у одређеној количини растварача и она се
изразити на више начина од којих сваки има одређене предности и недостатке.
Процентни састав (или масени део) је однос масе растворене супстанце и масе раствора помножен са 100, или, другим речима, број грама растворене супстанце у 100 грама раствора.
На пример 20% раствор NaCl садржи
80 грама воде. У 200 грама
рида и 160 грама
у 1 dm3 раствора.
Задатак: Колико грама NaOH је потребно за припремање 100 cm3 NaOH раствора концентрације 0,1 mol/dm3?
0,01 мол NaOH, а то је 0,4 грама
Такође, подсетимо се да је густина дата изразом:
7.6. Kолигативна својства
Колигативна својства су она која зависе само од броја честица растворене супстанце, а не и од својстава тих честица. Дакле, на ова својства не утиче природа растворене супстанце, тако да је небитно да ли су у питању молекули, атоми или јони. Колигативна својства су снижење напона паре, повишење температуре кључања, снижење температуре
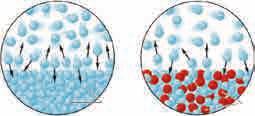
Marie Raoult,
Ако
трансформисати
Тако
растворене супстанце. Повишење
Taчка кључања раствора јесте температура на којој се
температуре кључања раствора једнако је разлици температуре кључања раствора и температуре кључања растварача, ΔТк = Тк – Тк°. ΔТк је пропорционално снижењу напона паре, па је стога пропорционално концентрацији раствора, у
концентрације,
Тк = Кe · c m где Ke представља
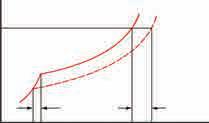


Након извесног времена уочава се да се ниво течности у једном одељку постепено смањивао, а у другом повећавао. Процес се одвијао до успостављања равнотеже, односно изједначавања концентрација. Oсмотски притисак је притисак који треба применити да би се процес осмозе зауставио. Његова вредност је дата изразом Π = cRT,
где је c моларна концентрација раствора, R универзална гасна константа, а T
апсолутна температура. Уколико два раствора имају исти осмотски притисак, онда су изотонични. Тада је раствор већег притиска хипертоничан, а нижег осмотског притискa хипотоничан. Практичну примену осмотског притиска налазимо код
Дисперзни
фаза, распоређена у другој, коју називамо дисперзно средство. Према величини дисперзне фазе раствори се
1. Грубо
честице су видљиве голим оком. To су суспензије код којих је чврста супстанца диспергована у течности, на пример глина у води, и емулзије код којих су ситне капљице
масти у млеку.
2. Колоиди, код којих је величина честица
3.


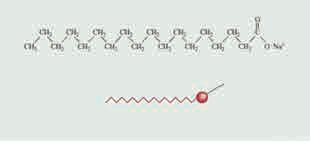
колоидима. Хидрофилни су, на пример, раствори протеина у води, као што је хемоглобин. Молекули хемоглобина су организовани тако да групе као карбоксилна или аминогрупа могу да остваре интеракције са молекулима воде (на пример водоничну везу). Уопштено, ови колоиди су релативно стабилни, за разлику од хидрофобних колоида у којима се честице дисперговане фазе групишу, што доводи до нарушавања колоида (на пример формирања талога или филма на површини колоида). Хидрофобни колоиди се могу стабилизовати додатком соли које формирају слој око честице чиме је, практично, онемогућено њихово приближавање и груписање. Хидрофобни колоиди, такође, могу бити стабилизовани присуством хидрофилних група на њиховој површини. Пример за то су

1.
2. Попунити следећу
3.
(Решење: 194 mol/kg; 17,85 mol/dm3)
4. Објасните израз: слично се у сличном раствара.
5. Антифриз за аутомобиле садржи неиспарљиви етиленгликол (Mr = 62). Израчунајте снижење температуре мржњења и повишење температуре кључања 25,0% етиленгликола у води. (Кe = 0,51° C; Кk = 1,86° C). (Решење: 2,74° C; 10° C)
Демонстрациони огледи
8.1.
8. ХЕМИЈСКЕ
Користећи знање о хемијској структури и хемијским формулама, у овом поглављу ћемо изучавати односе маса атома и молекула, те ћемо објашњавати састав једињења и проучавати промене хемијског састава једињења, односно хемијске промене. Користићемо формуле да прикажемо хемијску реакцију,
је
једног атома изражена у атомским јединицама масе (amu) или u унифицирана атомска јединица масе. Једна
вивалентна маси једне дванаестине угљениковог изотопа C12 а то је 1,000 amu. Овај изотоп угљеникa, C12, садржи
12 ∙ 8,40/100 и износи 1,008 amu . Слично томе, маса кисеониковог атома
вредности маса нису целобројне вредности. То је због тога
изотопа. На пример, природна заступљеност C12 је 98,90% а C13 је 1,10%,
C13 је 13.00335 amu. Просечну масу угљеника израчунавамо: (0,9890)(12,00000 amu) + (0,0110) (13,00335 amu) = 12,01 amu (проценте смо
маси израженој у amu. Другим речима, ако знамо атомску масу, знаћемо и моларну масу. Такође, ако знамо да један мол атома садржи Авогадров број атома, можемо израчунати масу појединачног атома тако што ћемо, када је у питању на пример C12, број 12 поделити са 6,022 · 1023 и добити број 1,992 · 10–23g.
којих се молекул састоји, могуће је израчунати масу
удео водоника у води добијамо дељењем 2,02 са 18,02 и множењем са 100, а кисеоника количником 16 и 18,02 и множењем са 100. Поступак је обрнут уколико на основу процентног састава желимо да сазнамо формулу једињења. На пример, елементалном анализом је утврђено да је процентни састав аскорбинске киселине (витамина C) 40,92% угљеника, 4,58% водоника и 54,50% кисеоника и, ако желимо да одредимо формулу витамина C, то ћемо урадити
40,92 / 12,01; 4,58
Добићемо
C 3,407 / 3,407 = 1,000
H 4,54 / 3,407 = 1,33
O 3,406 / 3,407 =1,000. Број 1,33 је превише
добијeна је емпиријска формула
не мора увек бити иста као молекулска формула. Да бисмо добили молекулску формулу, потребно је да знамо моларну масу једињења. Ево примера: узорак једињења садржи 1,52 g азота и 3,47 g кисеоника. Моларна маса једињења је између 90 и 95. Потребно је одредити молекулску формулу и тачну моларну масу. Најпре ћемо
од њих чиме добијамо да је
једињења била 46,01. Како нам је у задатку речено да је маса између 90 и 95, јасно је да ћемо молекулску формулу траженог једињења добити множењем индекса у емпиријској формули са
гласити N2O4, док релативна молекулска маса износи 92,02.
8.3. Хемијске једначине и стехиометријски
реакција ће гласити 2H2 + O2 → 2H2О
и значиће да два молекула водоника реагују са молекулом кисеоника (oни су реактанти) дајући два молекула воде (производ реакције), а то истовремено значи и да два мола водоника реагују са једним молом кисеоника и да настају два
једињења, реакција ће истовремено значити да реагују
9,01 g воде. Евентуални вишак
2HgO(s) → 2Hg(l) + O2(g)
NaCl(aq) + AgNO3(aq) → NaNO3
Једно од основних питања у хемијској лабораторији се односи на количину производа који је добијен у некој хемијској реакцији или на количину реактаната коју је потребно применити за добијање
израчунавање приноса реакције. Оваква и слична израчунавања се називају стехиометрија. Било да је количина реактаната и производа задата у моловима, грамима, cm3, или неким другим јединицама, за ова израчунавања је најподесније те јединице превести у молове. Тада коефицијенте у једначинама хемијских реакција представљамо као бројеве молова супстанци. Погледајмо једначину реакције настајања амонијака:
N2(g) + 3H2(g) → 2NH3(g)
Стехиометријски коефицијенти нам кажу да један молекул азота реагује са три молекула водоника и да
N2(g) + 3H2(g) → 2NH3(g)
Затим треба израчунати масу једног мола калцијумкарбоната. Она износи 100 g/mol, те задатих 200 g представља 2 мола. Из једначине се види да се разлагањем једног мола калцијумкарбоната
цијумоксида, па ће се загревањем 2 мола добити 2 мола калцијумоксида. Како је његова моларна маса 56 g/mol, у реакцији ће се добити 112 грама калцијумоксида.
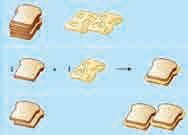
8.5. Лимитирајући (ограничавајући) реактант
Када се изводи хемијска реакција, реактанти обично нису присутни у тачним стехиометријским односима. Реакција се зауставља чим се потроши један од реактаната остављајући вишак другог реактанта. Тај реактант, кога има мање, назива се лимитирајући (ограничавајући) реактант. Претпоставимо, на пример, да нам је
и 7 молова кисеоника који ће међусобно реаговати у реакцији: 2H2(g) + O2(g) → 2H2O(l) Пошто 2 мола H2 реагују са једним
Питања и задаци
1. Природни узорак галијума се састоји од изотопа масе 68,95 и изотопа масе 70,95 чија је природна заступљеност 60,16% и 39,84%. Колико износи просечна релативна маса галијума? (Решење: 69,75)
2. Израчунајте број молова у: а) 127,08 грама бакра; б) 20,0 грама калцијума; в) 0,012 грама калијума; г) 5,0 милиграма америцијума.
(Решење: а) 2 мола; б) 0,5 молова; в) 3 · 10–4 мола; г) 2,06 · 10–5 молова)
3. Израчунајте број грама у: а) 0,1 мола гвожђа; б) 2,31 мола силицијума; в) 0,023 мола угљеника; г) 6,03 мола злата.
(Решење: а) 5,6 g; б) 64,9 g; в) 0,28 g; г) 1187,9 g)
4. Израчунајте број атома у сваком од примера у задацима 2 и 3. (Решење: 2а) 1,2 · 1024; 2б) 3 · 1023; 2в) 1,8 · 1020; 2г) 1,2 · 1019; 3а) 6 · 1022; 3б) 1,4 · 1024; 3в) 1,4 · 1022; 3г) 3,6 · 1024)
5. Израчунајте масу једног атома бакра. (Решење: 1,06 · 10–20 g)
6. Једна таблета AlkaSeltzer садржи 324 mg аспирина (C9H8O4), 1904 mg NaHCO3 и 1000 mg лимунске киселине (C6H8O7). A) Израчунајте број молова сваке супстанце у таблети; Б) Колико молекула аспирина има у једној таблети? (Решење: a) 1,8 · 10–3 C9H8O4, 2,3 · 10–2 NaHCO3, 5,2 · 10–3 C6H8O7; б) 1,08 · 1021)
7. Никотин,
8.
B2H6)
9. Витамин C је једињење које се састоји од угљеника, водоника и кисеоника. Одредити емпиријску формулу ако се сагоравањем 4,00 mg витамина C у кисеонику добија 6,00 mg CO2 и 1,632 mg H2O. (Решење: C3H4O3)
10. Смешљивац, N2O, је гас који се добија термичким разлагањем амонијумнитрата: NH4NO3 → N2O + 2H2O. Ако се има на располагању 1,00 · 103 g амонијумнитрата, колики је теоријски принос смешљивца?
(Решење: 550 g)
11. N2F4 се добија следећом реакцијом: 2NH3 + 5F2 → N2F4 + 6HF. Ако се помеша 4,0 грама амонијака и 14,0 грама флуора, који реактант је у вишку и колико производа се добија? (Решење: NH3, 7,7 g N2F4)
8.7. Енталпија хемијске реакције
енергије. Та енергија се назива унутрашњом енергијом
Област термодинамике
(грчки endon = унутра). Топлота која се
(ослобођене или апсорбоване) енергије
тивни предзнак:
ΔU = Q(p=const) – pΔV односно Q(p=const) = ΔU + pΔV
Ова промена топлоте реакције при константном
Топлота хемијске реакције је разлика енталпије производа и реактаната. Дакле, за егзотермне реакције током
Тако је, на пример, промена енталпије реакције настајања воде у гасовитом агрегатном стању при стандардним условима дата термохемијском реакцијом: H2(g) + ½О2(g) → H2О(g) ΔH° = − 241,8 kJ/mol
А за настајање воде у течном
стању,
има другу вредност: H2(g) + ½О2(g) → H2О(l) ΔH° = − 285,8 kJ/mol
Међутим, за испаравање два мола је
топлоте.
Најзад, треба
2H2О(l) → 2H2О(g) ΔH° = 88 kJ
има исту бројчану вредност, а различит предзнак
директне реакције.
2H2(g) + O2(g) → 2H2O(g) ∆H° = − 483,6 kJ
2H2O(g) → 2H2(g) + O2(g) ∆H° = + 483,6 kJ
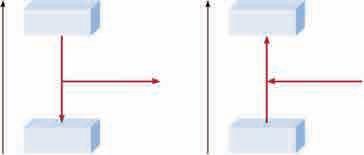
2H2(g) + O2(g)
(g) + O2(g)
2H2O(g) 2H2O(g)
H2(g) + ½О2(g) →
= − 285,8 kJ/mol
Применом овог закона доћи ћемо до
сагоравања угљеника до угљеник(II)окисида. Ову енталпију је тешко експериментално одредити јер се оксидација увек делимично одвија до угљеник(IV)оксида. C(s) + ½O2(g) → CO(g) ΔH° = ?
Али, оно што се може одредити, и одређено је, јесу промене енталпије реакција:
C(s) + O2(g) → CO2(g) ∆H°= − 393,5 kJ
CO(g) + ½O2(g) → CO2(g) ∆H°= − 283,0 kJ
Како је по Хесовом
реакција оксидације C у CO и оксидације CO у CO2 једнака енталпији директне реакције C у CO2, очигледно је
C у CO2 и CO у CO2.
C(s) + O2(g) − CO(g) − ½O2(g) → CO2(g) − CO2(g) Након скраћивања се добија реакција:
C(s) + ½O2(g) → CO(g)
C(s) + ½O2(g) → CO(g) ΔH° = −111 kЈ C(графит) + О2(g)
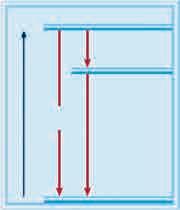
Хемија
Промена енталпије хемијске реакције једнака је разлици збира енталпија производа и збира енталпија реактаната: ΔH°реакције = ΣΔH° производа − ΣΔH° реактаната
За општу рекацију
аA + bB → cC + dD,
промена енталпије ће износити:
ΔH°реакције = aΔH°A + bΔH°B − (cΔH°C + dΔH°D).
Конкретан пример јесте реакција сагоревања пропана
C3H8(g) + 5O2(g) → 3CO2(g) + 4H2O(l),
чија промена енталпије износи:
ΔH°реакције = 3ΔH°CO2 + 4ΔH°H2O − (ΔH°C3H8 + 5ΔH°O2).
Енталпије настајања, односно енталпије формирања супстанци, можемо експериментално одредити као енталпије реакције у којима то једињење настаје из елемената у стандардном стању. Наиме, према договору, енталпије елемената у свом стандардном стабилном стању једнаке су нули. На пример, приликом реакције стварања угљеник(IV)оксида из угљеника у облику графита и кисеоника ослобађа се 393,5 kJ. C(s) + O2(g) → CO2(g) ΔH° = − 393,5 kJ, ΔHреакције = ΔHCO2 − (ΔHC + ΔHO2)= − 393,5 kJ. Како су према договору ΔH°C и ΔH°O2 једнаке нули, добијамо да је ΔH°реакције = ΔH°CO2 ,
тело – нису спонтани.
Претпоставком да су спонтани процеси, који су праћени смањењем енергије, објаснићемо спонтаност већине егзотермних реакција (производи реакције имају мању енталпију од реактаната).
Примери су сагоревање метана или реакција неутрализације:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(l) ΔH° = − 890,4 kJ/mol, H+(aq) + OH–(aq) → H2O(l) ΔH° = − 56,2 kJ/mol.
Међутим, спонтано се одвијају и многе ендотермне хемијске реакције. Како код таквих процеса производи
садржај енергије од реактаната, поставља се питање зашто се они дешавају.
Примери ендотермних спонтаних реакција јесу топљење леда на температурама изнад нула степени или растварање амонијумнитрата. H2O(s) → H2O(l) ΔH° = 6,01 kJ/mol, NH4NO3(s) → NH4(aq)+ + NO3 –(aq) ΔH° = 25 kJ/mol.
Другим речима, само на основу промене енталпије
претпоставити, потребно је да се упознамо са још једном термодинамичком величином
а сваки систем, при одређеним условима, притиску и температури, има одређени степен неуређености, који се бројчано изражава вредношћу ентропије, а обележава словом S. Приликом хемијске или физичке промене, та вредност се мења. Примера ради, при испаравању течности слабе међумолекулске силе и молекули су много покретљивији због чега неуређеност,
Спонтане су хемијске реакције код којих је ΔG < 0, на датој температури. Оне реакције код којих је ΔG > 0
нису спонтане, док су оне код којих је ΔG = 0 у равнотежи. На нижим температурама спонтаност реакција ће зависити од промене енталпије (ΔH), док ће на вишим бити условљена вредношћу промене ентропије (ΔS).
У природи ће се, међутим, одвијати и рекације које нису спонтане, попут реакције у атмосфери
представља препреку.
Питања и задаци
1. Сагоревањем сирћетне киселине, CH3COOH(l), добија се H2O(l) и CO2(g) и ослобађа 871,7 kJ топлоте по молу CH3COOH(l). Написати изједначену термохемијску једначину ове реакције.
(Решење: CH3COOH(l) + 2O2(g) → 2CO2(g) + 2H2O(l) ΔH° = −871,7 kJ/mol)
2. За хипотетичке реакције A → B ΔH = + 30 kJ B → C ΔH = + 60 kJ а)

ΔHAl2O3 = − 1674,1 kJ/mol ΔHFe2O3 = −821,4 kJ/mol. (Решење: −852,7 kJ)
4. Како се мења ентропија ако се: а) чврста супстанца топи; б) гас кондензује у течност; в) чврста супстанца сублимује (прелази у гасовито агрегатно стање)?
5. За неку реакцију ΔH° = −19,5 kJ и ΔS° = −19,5 kJ/K. а) Да ли је ова реакција егзотермна или ендотермна? б) Да ли реакција доводи до повећања или смањења неуређености система? в) Одредите промену слободне енергије при стандардним условима. г) Да ли је ова реакција
8.1. Реакција разлагања
епрувету
нику. Уочити промене.
8.2. Реакција између баријум-хидроксида
и баријум-хидроксида и енергично
циљева, до, на пример, праћења брзине настајања и трошења
8.9.1. Фактори који утичу на брзину
веза, брзина реакције
агрегатном стању. Када је један, или сви реактанти, у чврстом стању,
је
на њихову додирну површину. Другим речима, већина таквих реакција се брже
лек у облику прашка ће се брже растворити у желуцу од лека који је узет у виду таблете.
2. Концентрација реактаната.
брзина реакције.
3. Температура. Повећање температуре
4.
Размотрићемо општу реакцију: реактант → производ, или А → B.
реактаната (слика 8.5).
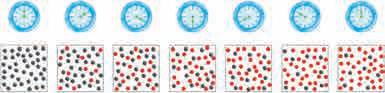
= – Δ[A]/Δt = Δ[B]/Δt
где су Δ[A] и Δ[B] промене концентрације
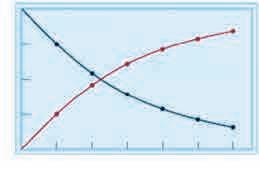
= – ½ Δ[A]/Δt = Δ[B]/Δt.
= – 1/a Δ[A]/Δt = –1/b Δ[B]/Δt = 1/c Δ[C]/Δt = 1/d Δ[D]/Δt.
8.9.2. Закон
8.9.3. Теорија судaра
Теорија судара подразумева да се молекули, који се налазе у непрекидном кретању, сударају и
судара.
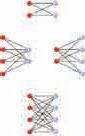
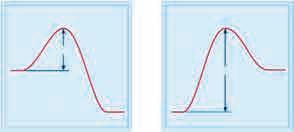
ка настајању производа.
Детаљан опис процеса којим се реакција
реакције. Ево примера за реакцију која се одиграва у једном ступњу.
NO(g) + O3(g) → NO2(g) + O2(g)
Међутим, има и реакција које се одвијају у више ступњева. Сваки појединачни ступањ тих реакција
ступњу назива се молекуларност.
судар три молекула. На пример, реакција испод:
NO2(g) + CO(g) → NO(g) + CO2(g), се одвија у два елементарна ступња, оба бимолекулска. NO3(g) у овој реакцији представља интермедијер, производ једног елементарног ступња, који ће бити реактант у другом елементарном ступњу.
Ступањ 1: NO2(g) + NO2(g) → NO(g) + NO3(g)
Ступањ 2: NO3(g) + CO(g) → NO2(g) + CO2(g)
Укупна реакција: NO2(g) + NO2(g) + NO3(g) + CO(g) → NO(g) + NO3(g) + NO2(g) + CO2(g)
односно NO2(g) + CO(g) → NO(g) + CO2(g) Збир елементарних ступњева мултиступњевитих
8.9.4. Катализатори
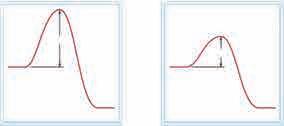
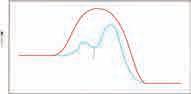
Битно је уочити да катализатори не утичу на енергију, односно енталпију реактаната и производа, већ само снижавају енергију активације и то како за директну, тако и за повратну реакцију.
Питања и задаци
1. Наведите четири фактора која утичу на брзину хемијске реакције.
2. Шта је интермедијер, а шта прелазно стање?
3. Процес разлагања озона одвија се у два ступња: O3(g) → O2(g) + O(g), O3(g) + O(g) → 2O2(g).
а) Која је молекуларност сваког од ступњева?
б) Напишите укупну реакцију разлагања озона.
(Решење: 2O3(g) → 3O2(g))
в) Шта је (су) интермедијер(и)?
(Решење: O.)
4. Ако се реакција A + 2B → C одвија у два ступња: А + B → АB (споро) и АB + B → C (брзо), написати израз за брзину реакције.
(Решење: V=k[А][B])
Демонстрациони оглед
8.4. Реакција између хлороводоника и амонијака У једну епрувету до 2/3 запремине сипати концентровани амонијак, а у другу исту запремину концентроване хлороводоничне киселине. Приближите отворе једне другој. Обратити
Директна реакција: SO2(g) + O2(g) → SO3(g).
Повратна реакција: SO3(g) → SO2(g) + O2(g)
Збирна реакција: SO2(g) + O2(g) → → SO3(g). У
a A + b B → → c C + d D. Израз
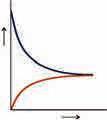

да умањи спољашњи утицај


то је на страну мањег броја молова који врше мањи

Утицај катализатора
Катализатор
смеше.
Питања и задаци
1. Написати изразе за константу равнотеже реакција: PCl3(g) + Cl2(g) → → PCl5(g), 2H2O2(g) → → H2O(g) + O2(g).
2. За повратну реакцију H2(g) + Br2(g) → → 2HBr(g) ∆H = + 68 kJ размотрити утицај следећих промена.
ПРОМЕНА [Br2] [HBr] Kc Додатак водоника
Повећање температуре
Повећање притиска HBr
Повећање запремине балона
3. Како ће промене утицати на равнотежну реакцију 2SO2(g) + O2(g) → →
(g) ∆H < 0 и то: а) додатак O2(g); б) загревање реакционе смеше; в) двоструко повећање запремине реакционе смеше; г) додатак катализатора; д) уклањање SO3(g) из реакционе смеше?
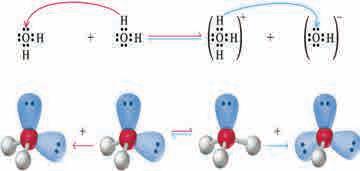
Киселине и базе су значајне у бројним хемијским процесима, од биолошких до инддустријских, у хемијским реакцијама које изводимо у лабораторији до оних у нашој животној средини. Карбонати из стена и CO2 (угљеник(IV)оксид, угљендиоксид) су присутни у природним водама. Вулкани и топли извори образују јако киселе средине, услед присуства HCl и SO2 (сумпор(IV)оксид, сумпордиоксид). Биолошки процеси, као што су фотосинтеза или респирација преко реакција трошења или настајања CO2 утичу на концентрацију хидронијум јона (H3O+). Све ове реакције, које су веома важне у живим организмима, многим индустријским процесима, неким поступцима лечења, али и у свакодневном животу, јесу реакције
јоне
утицајем поларних молекула воде. Због постојања јона ови раствори
9.2. Теорије о киселинама и базама
на оне супстанце
у свом молекулу не садрже H+
базну реакцију. Поред поменуте реакције у води, киселине
или винско сирће које свој кисео укус дугује сирћетној киселини. Киселине
реагују
хлороводоничне киселине
2HCl(aq) + Mg(s) → MgCl2(aq) + H2(g).
Киселине реагују са карбонатима
угљеник(IV)оксида.
2HCl(aq) + CaCO3(s) → CaCl2(aq) + H2O(l)+ CO2(g) HCl(aq) + NaHCO3(s) → NaCl(aq) + H2O(l)+ CO2(g)
(Johannes Nicolaus Brønsted. 1879–1947)
(Thomas Martin Lowry, 1874–1936)
изгубио електрон и као такав је изузетно мали, те
постоји као слободан већ у хидратисаном облику (H3O+). Хидратисани протон, H3O+(aq), назива се хидронијум јон. (Експериментални подаци указују на то да је хидронијум јон окружен додатним молекулима воде, односно додатно хидратисан,
да може садржати неколико молекула воде, при чему то не утиче на његова кисела својства.)
је јача уколико има већу тежњу за примањем протона.
У лабораторији се најчешће налазе киселине као што су хлороводонична (хлоридна), азотна (нитратна), сумпорна (сулфатна), фосфорна (фосфатна), сирћетна (ацетатна) киселина.
HNO3(aq) + H2O(l) → H3O+(aq) + NO3 –(aq) Хлороводонична
H2SO4(aq) + H2O(l) → H3O+(aq) + HSO4 –(aq), HSO4 –(aq) + H2O(l) → → H3O+(aq) + SO4 2–(aq). У првом ступњу сумпорна киселина је јака киселина,
је HSO4
киселина због непотпуне јонизације. Трипротичне киселине се јонизују у три ступња. Пример је фосфорна киселина:
H3PO4(aq) + H2O(l) → H3O+(aq) + H2PO4 –(aq), H2PO4 –(aq) + H2O(l) → → H3O+(aq) + HPO4 2–(aq), HPO4 2–(aq) + H2O(l) → → H3O+(aq) + PO4 3–(aq).
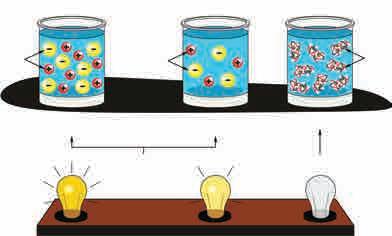
Киселина
Ацетатна (сирћетна) киселина
Карбонатна (угљена) киселина
Цијановодонична кислеина
Флуороводонична кислеина
Сумпорводонична кислеина
Хипохлораста (хипохлоритна)
Азотаста (нитритна) киселина
10–5
9,5 · 10–8 1 · 10–19

Peer Lauritz Sorensen,


CH3COONa(aq) → Na+(aq) + CH3COO (aq)
CH3COO (aq) + H2O(l) → → CH3COOH(aq) + OH–(aq)
стога слаба киселина. Након растварања амонијумхлорида долази до следећих реакција:
NH4Cl(aq) → NH4+(aq) + Cl (aq),
NH4 +(aq) + H2O(l) → → NH3(aq) + H3O+(aq).
NH4 +(aq) реагује са водом јер је катјон слабе
нијака, па према томе јака киселина, јача
Након предавања протона води, настаће хидронијум јон, услед чега водени раствор ове амонијумове соли реагује кисело.
NaCl(aq) → Na+ (aq) + Cl (aq)
Натријумхлорид дисосује на Na+ и Cl јоне. Na+ је, како је поменуто, слаба киселина (катјон јаке базе), а Cl анјон јаке хлороводоничне киселине, зато слаба база, па ни један ни други не реагују са водом. Дакле, водени раствор натријумхлорида
(амонијум катјон) и јаку базу (нитритни анјон). Водени раствор ове
реагује
неутрално. NH4NO2(aq) → NH4+(aq) + NO2 (aq) NH4 +(aq) + H2O(l) → → NH3(aq) + H3O+(aq)
2AgNO3(aq) + Na2CrO4(aq) → Ag2CrO4(s) + 2NaNO3(aq)
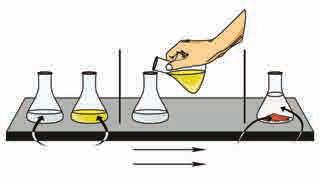
у раствору у следећим случајевима:
1. када настаје нерастворна чврста супстанца, односно талог;
2. када настаје слаб
3.
Ag+(aq) + NO3 –(aq) + K+(aq) + Cl–(aq)
AgCl(s) + K+(aq) + NO3 –(aq)
Ag+(aq) + Cl–(aq ) → AgCl(s). Реакција
NaNO2(aq) + HCl(aq) → HNO2 + NaCl(aq)
Na+(aq) + NO2 –(aq) + H+ (aq) + Cl– (aq
HNO2 + Na+ (aq) + Cl– (aq)
H+ (aq) + NO2 –(aq) → HNO2.
NaОH(aq) + HBr(aq) → NaBr(aq) + H2O(l)
Na+(aq) + OH–(aq) + H+ (aq) + Br–(aq) → Na+ (aq) + Br– (aq) + H2O(l) H+ (aq) + OH–(aq) → H2O(l)
NaHCO3(aq) + HBr(aq) → NaBr(aq) + CO2(g) + H2O(l)
Na+(aq) + HCO3 –(aq) + H+ (aq) + Br–(aq) → Na+ (aq) + CO2(g)
Питања и задаци
1. А) Напишите коњуговане базе следећих киселина: HClO4, H2S, PH4 +, HCO3 –Б) Напишите коњуговане киселине следећих база: CN–, SO4 2–, H2O, HCO3 –.
2. HSO3 – је амфипротична супстанца. а) Напишите реакцију HSO3 – са водом, у којој се понаша као киселина, и одредите коњуговане киселинскобазне парове. б) Напишите реакцију HSO3 – са водом, у којој се понаша као база, и одредите коњуговане киселинскобазне парове.
3. Израчунајте pH раствора ако су концентрације водоничних и хидроксидних јона: a) [H+] = 2,0∙10–2 mol/dm3; б) [H+] = 4,0∙10–9 mol/dm3; в) [OH–] = 1,0∙10–7 mol/dm3; г) [OH–] = 7,0∙10–13 mol/dm3. Који раствори су кисели, који базни, а који неутрални?
(Решење: а) 1,70; б) 8,40; в) 7,00; г) 1,84)
4. На температури мржњења воде, на 0° C, jонски производ воде – KW износи 1,2∙10–15. Израчунајте [H+] и [OH-] за неутрални раствор на тој температури.
(Решење: 3,4∙10–8 mol/dm3)
5. Израчунати pH раствора који садржи: a) раствор KOH, концентрације 0,080 mol/dm3; б) 1,065 g KOH у 500 cm3 раствора; в) раствора добијеног разблаживањем 100 cm3 0,01 mol/dm3 Ca(OH)2 до 500 cm3 . (Решење: а) 12,90; б) 12,58; в) 11,60)
6. Ако је pH раствора NaOH 11,5, колика је концентрација тог раствора? (Решење: 3,16∙10–3 mol/dm3).
7. Напишите производе следећих киселобазних реакција и предвидите да ли
8.
Демонстрациони оглед
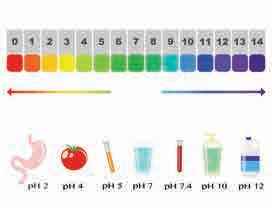
9.1. Испитивање pH вредности водених раствора електролита универзалном индикаторском хартијом
У епрувете сипати 1 до 2 cm3 раствора HCl, CH3COOH, NaOH, NH3, NaCl, FeCl3, NaNO2 познате концентрације или
полагању. Одредити pH вредност помоћу универзалне индикаторске хартије. Рачунским путем проверити тачност експеримента.

2Mg0 + O2 0 → 2Mg2+ + 2O2–,
је реакција: 2Mg + O2 →

настајања
Хемија
ментални подаци показују да приликом настајања хлороводоника долази до делимичног преноса електрона са водоника на хлор, односно са сумпора на кисеоник приликом настајања сумпор(IV)оксида, хемичари су пронашли начин да се у оксидоредукционим реакцијама прати ток електрона. У томе
нам помаже оксидациони број или оксидационо стање. У поменутим реакцијама H2(g) + Cl2(g) → 2HCl(g) или S(s) + O2(g) → SO2(g),
елементи, тј. водоник, хлор, сумпор и кисеоник имају оксидациони
тронски пар из везе припишемо електронегативнијем атому.
омогућава да лако одредимо који су се елементи оксидовали, а који редуковали. Елементи којима се оксидациони
реакција, док су се они којима се оксидациони број смањује редуковали. Постоје правила код
1. Оксидациони број атома у елементарном стању је нула. Примери су
C, Ag, H2, P4, S8 и тако даље.
2. Оксидациони број јона који се састоје од само једног атома, односно моноатомских јона, једнак је наелектрисању јона. Елементи прве групе (алкални метали) имају оксидациони број +1, друге групе (земноалкални метали) +2, алуминијум +3.
3. Оксидациони број кисеоника у већини једињења је –2 (у поменутим магнезијумоксиду или сумпор(IV)оксиду). У пероксидима (водоникпероксид, H2O2, или његове соли) оксидациони број кисеоника је –1. У супероксидима, О2 –, оксидациони број кисеоника није цео број већ има вредност –½.
4. Оксидациони број водоника је +1, осим у једињењима у којима је водоник везан за метал (хидридима, LiH, NaH, CaH2) када му је оксидациони број –1.
5. Оксидациони број флуора је у свим једињењима –1. Остали халогени елементи имају оксидациони број –1, у халогеноводоничним кисе-

2. Одредити оксидациона
отпуштених електрона:
3. Написати
2КMnO4(aq) + HCl(aq) → KCl(aq) + 2MnCl2(aq) + 5Cl2(g) + H2O(l).
4. На крају
кисеоник, воду:
2КMnO4(aq) +16HCl(aq) → 2KCl(aq) + 2MnCl2(aq) + 5Cl2(g) + 8H2O(g) Исти
реакције: Cu(s) + HNO3(aq) → Cu(NO3)2(aq) + NO(g) + H2O(g), ,
3Cu(s) + HNO3(aq) → 3Cu(NO3)2(aq) + 2NO(g) + H2O(l), 3Cu(s) + 8HNO3(aq) → 3Cu(NO3)2(aq) + 2NO(g) + 4H2O(l).
сле-
Реакције сједињавања
4Na(s) + O2(g) → 2Na2O(s) или N2(g) + 2O2(g) → 2NO2(g),
2Al(s) + 3Br2(l) → 2AlBr3(s). Реакције
+ 2HCl(aq) → ZnCl2(aq) + H2(g
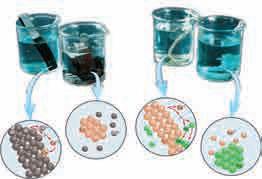

Спонтане
Супротне
сне цинк
Zn(s) + CuCl2(aq) → ZnCl2(aq) + Cu(s), Cu(s) + 2АgNO3(aq) → Cu(NO3)2(aq) + 2Аg(s).
његове соли и да
елементарни цинк, као ни да сребро истисне бакар. Једноставан начин да се предвиди смер одигравања редо-
ксреакција јесте увид у електрохемијски низ, или, како се још назива, напонски низ. У овом низу метали су поређани према способности да замене водоник у води или киселини. Литијум је најреактивнији метал, а злато најмање реактиван метал. Другим речима, метал може да истисне други метал који се налази „испод” њега у
Реакције замене укључују и реакције
ционо средство.
Cl2(g) + 2KBr (aq) → 2KCl(aq) + Br2(l)
Оксидациона моћ ових елемената опада у групи, што значи да
истисне само јод.
Cl2(g) + 2KI (aq) → 2KCl(aq) + I2(s)
Br2(l) + 2KI (aq) → 2KBr (aq) + I2(s) Аутооксидо-редукционе реакције
редукује до –1 у хлориду.
Б) Могуће су и реакције када исти елемент из два различита оксидациона стања даје производ у ком елемент има једно оксидационо стање.
2H2S(g) + SO2(g) → 3S(s) + 2H2O(l).
Питања и задаци
1. У свакој од следећих реакција, одредите супстанцу која се редукује
и редукционо средство:
2Al (s)+ 3Cl2(g) → 2AlCl3(s);
8H+(aq) + MnO4 –(aq) + 5Fe2+(aq) → 5Fe3+(aq) + Mn2+(aq) + 4H2O(l);
FeS(s) + 3NO3 –(aq) + 4H+(aq) → 3NO(g) + SO42–(aq) + Fe3+(aq) + 2H2O.
2.
уређајима, а за производњу
Cd(s) + NiO2(s) + 2H2O(l) → Cd(OH)2(s) + Ni(OH)2(s).
Одредити која се супстанца у овој реакцији
Постоје многи недостаци употребе никалкадмијумских батерија. Кадмијум је
Oксидо-редукционе
3. Oдредите коефицијенте у следећим оксидоредукционим реакцијама (агрегатна стања су, ради једноставности, изостављена): MnO2 + HCl → MnCl2 + Cl2 + H2O, KMnO4 + Na2SO3 + H2SO4 → K2SO4 + MnSO4 + Na2SO4 + H2O, S + HNO3 → H2SO3 + N2O, FeCl3 + KBr → FeCl2 + Br2 + KCl.
4. На основу напонског низа одредите да ли се следеће реакције спонтано одвијају: Fe(s) + Sn2+(aq) → Fe2+(aq) + Sn(s), Ag(s) + Ni2+(aq) → Ag+(aq) + Ni(s).
5. Четири метала – A, B, C, D испољавају следећа својства: а) A и C реагују са хлороводоничном киселином, концентрације 1,0 mol/dm3, притом ослобађајући водоник (H2); б) када се C дода у растворе соли других метала, издвајају се ти метали, тј. A, B и D; в) метал D редукује
средини
епрувету сипати 1 до 2 cm3 раствора калијумпермангата (0,5 mol/dm3), додати пар капи разблажене сумпорне киселине (0,1 mol/dm3) и 1 cm3 гвожђе(II)сулфата. Пратити промене.
У другу епрувету сипати 1 до 2 cm3 раствора калијумпермангата (0,5 mol/dm3), додати пар капи разблаженог натријумхидроксида (0,1 mol/dm3) и 1 cm3 гвожђе(II)сулфата. Пратити промене. На основу запажања написати једначине изведених хемијских реакција.
10.2. Haпонски
(0,1 mol/dm3). У
Литература
1. Raymond Chang, Chemistry, 10th Edition, McgrawHill, 2010.
2. Theodore L. Brown, H. Eugene Lemay Jr., Bruce E. Bursten, Catherine J. Murphy, Patrick M. Woodward, Mathew W. Stoltzfus, Chemistry: The Central Science, Pearson Higher Ed USA, 2017.
3. John C. Kotz, Keith F. Purcell, Chemistry & Chemical Reactivity, Saunders College Publishing, 1987.
4. Зоран Тодоровић, Срећко Трифуновић, Тибор Сабо, Општа хемија, Универзитет у Београду, Хемијски факултет, 2014.
ШИПКА
ХЕМИЈА за I разред
гимназије општег типа и природноматематичког смера и средње стручне школе у подручјима рада: пољопривреда, производња и прерада хране за образовне профиле: зоотехничар и техничар хортикултуре; текстилство и кожарство, за образовне профиле: текстилни техничар, конфекцијски техничар, техничар моделар коже; здравство и социјална заштита за образовне профиле: санитарноеколошки техничар, педијатријска сестра–техничар, гинеколошкоакушерска сестра, медицинска сестра–васпитач и осталe делатности личних услуга
Издавач ЗАВОД ЗА УЏБЕНИКЕ Београд, Обилићев венац 5 www.zavod.co.rs
Лектор САЊА ДАКИЋ
Графички уредник СТЕВАН ПАКОВИЋ
Коректори
Обим: 9 штампарских табака Формат: 16,5 × 23,5 cm
Тираж: 7 000 примерака
Рукопис предат у штампу јуна 2020. године. Штампање завршено јула 2020. године. Штампа „Планета принт”, Београд
CIP - Каталогизација у публикацији Народна библиотека Србије, Београд
37.016:54(075.3)
ГРГУРИЋ-Шипка, Сања, 1971Хемија : за I разред гимназије општег типа и природноматематичког смера и средње стручне школе у подручјима рада: пољопривреда, производња и прерада хране за образовне профиле: зоотехничар и техничар хортикултуре; текстилство и кожарство, за образовне профиле: текстилни техничар, конфекцијски техничар, техничар моделар коже; здравство и социјална заштита за образовне профиле: санитарно-еколошки техничар, педијатријска сестра-техничар, гинеколошко-акушерска сестра, медицинска сестра-васпитач и осталe делатности личних услуга / Сања Гргурић Шипка. - 1. изд. - Београд : Завод за уџбенике, 2020 (Београд : Планета принт). - 142 стр. : илустр. ; 24 cm
Тираж 7.000. - Напомене уз текст. - Библиографија: стр. 142. ISBN 978-86-17-20290-1
COBISS.SR-ID 16805129

