

KATALYS
Magnus Ehinger KEMI 2
A. Varför
B.
A5.
A6.
B5.
D.
D1.
D2.
D3.
E. Fördjupad organisk kemi .........................................................................................................
E1. Oxidation av alkoholer
E2. Aldehyder och ketoner .......................................................................................................................................
E3. Tioler och disulfider
E4. Etrar .............................................................................................................................................................................
E5. Aminer ........................................................................................................................................................................
E6. Nitroföreningar och organiska nitrater
E7. Karboxylsyror...........................................................................................................................................................
E8. Aromatiska karboxylsyror, dikarboxylsyror och hydroxisyror
E9. Optisk isomeri (spegelbildsisomeri)
E10. Estrar ...........................................................................................................................................................................
E11. Det organiska stamträdet
F. Biomolekyler ............................................................................................................................
F1. Fetter och andra lipider
F2. Mono-, oligo- och polysackarider .................................................................................................................
F3. Aminosyror och peptider
F4.
G. Biokemi.....................................................................................................................................
G2.
G3.
G4.
G7.
G8. Citronsyracykeln
G9.
H. Analytisk
H1.
H2. Kromatografiska
H3. Spektrofotometri
H4. IR-spektroskopi .......................................................................................................................................................
H5. NMR-spektroskopi
H6. Masspektrometri
H6.
- A -
Varför sker kemiska reaktioner?

Centralt innehåll
• Materiens och energins oförstörbarhet i kemiska reaktioner, däribland beräkning av entalpiändringar. Gibbs fria energi.
• Reaktionshastighet och olika faktorers inverkan på den.
• Jämvikter och jämviktskonstanter samt faktorer som påverkar dessa. Jämviktssystem i olika miljöer.
Mål
Målet är att du ska lära dig följande begrepp:
• Förbränningsentalpi, Δ H c 0
• Bildningsentalpi, ΔH f 0
• Hess lag
• Bindningsentalpi
• Gibbs fria energi, ∆G
• Reaktionshastighet
• Katalysator
• Enzym
• Aktiveringsenergi
• Aktiverat komplex
Dessutom ska du förstå:
• Endoterm reaktion
• Exoterm reaktion
• Jämviktsläge
• Dynamisk jämvikt
• Heterogen jämvikt
• Massverkans lag (Guldberg–Waages lag)
• Jämviktskonstanten K
• Koncentrationskvoten Q
• Le Chateliers princip
• hur man beräknar entalpiförändringen för en viss reaktion med hjälp av bildningsentalpier eller bindningsentalpier.
• hur olika faktorer (ämnenas natur, temperatur, koncentration och katalysator) påverkar hastigheten på en reaktion.
• hur en katalysator påverkar en reaktions aktiveringsenergi och förändring i entalpi.
• hur man beräknar jämviktskonstanten för ett system i jämvikt.
• hur man beräknar och använder sig av koncentrationskvoten i olika sammanhang.
• hur ett jämviktsläge förskjuts vid olika förändringar av koncentration, tryck och temperatur, samt vad som händer vid tillsats av en katalysator i ett system.
A1. Förbränningsentalpi och
bildningsentalpi
I kemi nivå 1 fick du lära dig en hel del om kemiska reaktioner. Vi har till exempel fällningar, som när silverjoner och kloridjoner går samman och bildar fast silverklorid. Men vi har också redoxreaktioner, som till exempel sker i batterier eller i förbränningar. Samt syrabasreaktioner, där protoner (vätejoner) avges eller tas upp.
Du fick helt enkelt lära dig att reaktioner sker. Men har du någonsin funderat på varför reaktionerna sker?

Exoterma och endoterma reaktioner
I kemi nivå 1 tittade vi på vad som händer med energin när olika reaktioner sker. Vi konstaterade att det vid en del reaktioner avges energi. Sådana reaktioner kallas för exoterma. Ett klassiskt exempel är förbränningen av kol i närvaro av syre. Då bildas det koldioxid samtidigt som det avges energi i form av värme. Vi kan skriva det med en reaktionsformel på det här sättet:
C(s) + O2(g) CO2(g) + energi
Koldioxidens energiinnehåll (entalpi, H) är lägre än kolets och syrets. Därför blir ΔH för den här reaktionen (och alla andra exoterma reaktioner) negativt, det vill säga ΔH < 0.
I endoterma reaktioner tas det istället upp energi från omgivningen. Då får produkterna högre entalpi än reaktanterna. Det sker till exempel när fast ammoniumnitrat löses upp i vatten:
NH��NO��(s) + energi NH 4 + (aq) + NO 3 (aq)
Eftersom energi tillförs i reaktionen blir ΔH för den endoterma reaktionen positivt, det vill säga ΔH > 0.
Förbränningsentalpi
Vid förbränningar reagerar något ämne med syrgas. Då reduceras syrgasen samtidigt som bränslet oxideras. I reaktionen avger bränslet elektroner som istället tas upp av syreatomerna. Förbränningar är alltid exoterma.
Den här typen av reaktioner är så pass viktiga att den förändring av entalpi som sker vid en förbränning fått ett eget namn: Förbränningsentalpi, Δ H c 0 (av engelskans combustion = förbränning). Nollan i Δ H c 0 anger att entalpin anges för ämnena vid standardtryck och temperatur, vanligen 101,�� kPa och 298 K (25 °C), det vill säga ”normala” väderförhållanden på ett laboratorium. Förbränningsentalpin är alltid negativ, eftersom förbränningar alltid är exoterma.

Ammoniumnitrat är ett vitt pulver. När detta löses i vatten sker en endoterm reaktion. Om reaktionen sker i en bägare kan du känna på bägaren att det blir kallt.

Gasol består huvudsakligen av kolvätena propan och butan. När dessa förbränns bildas koldioxid och vatten. Hur mycket energi som frigörs kan beräknas med hjälp av förbränningsentalpin för respektive ämne.
Förbränningsentalpin anger hur stor förändringen i entalpi är vid förbränning av en mol av ett ämne. Därför ska det ämne som förbränns alltid ha en etta som koefficient i en reaktionsformel där förbränningsentalpin anges. Då kan det hända att de andra ämnena i formeln till exempel får koefficienter med decimaler. Så är det till exempel om man vill ange förbränningsentalpin för butan, C��H10:
C��H10(g) + 6,5O2(g) ��CO2(g) + 5H2O(l)
För denna förbränning är förbränningsentalpin
Δ H c 0 = –2 878 kJ/mol. Vi kan skriva det direkt i reaktionsformeln på det här viset:
C��H10(g) + 6,5O2(g) ��CO2(g) + 5H2O(l) + 2 878 kJ
Förändringen i entalpi (ΔH) för en viss reaktion beror också på vilket aggregationstillstånd ämnena i reaktionen har. Eftersom förbränningsentalpin anges för ämnena i standardtillståndet ska till exempel koldioxiden vara i gasform, CO2(g), medan vattnet ska vara i flytande form, H2O(l).
Bildningsentalpi
Bildningsentalpi fungerar ungefär som förbränningsentalpin. Bildningsentalpin anger förändringen i entalpi när 1 mol av ett ämne bildas från sina grundämnen. Man kan till exempel bilda metangas, CH��(g), ur kol och vätgas enligt den här reaktionsformeln:
C(s) + 2H2(g) CH��(g)
Lägg märke till att kol är i fast form medan både vätgas och metangas är i gasfas vid standardtryck och temperatur. Bildningsentalpin tecknas ΔH f 0 (från engelskans formation = bildning). För reaktionen ovan har man mätt upp att bildningsentalpin ΔH f 0 = –7��,9 kJ/mol. Vi kan skriva in det direkt i reaktionsformeln på det här viset:
C(s) + 2H2(g) CH��(g) + 7��,9 kJ
Eftersom bildningsentalpin anger förändringen i entalpi när ett ämne bildas ur grundämnena i standardtillstånd kommer alltid
bildningsentalpin för rena grundämnen i standardtillstånd att vara 0 kJ/mol. Därför blir till exempel
Δ H f,C 0 = 0 kJ/mol och Δ H f, H 0 = 0 kJ/mol.
Fysikaliska kemister har ägnat stor möda åt att mäta upp bildningsentalpier för en mängd olika ämnen. Dessa bildningsentalpier kan man använda för att beräkna den totala entalpiförändringen för olika reaktioner. Det gör man genom att lägga samman bildningsentalpierna för alla produkterna i en reaktion och sedan dra ifrån bildningsentalpierna för reaktanterna.
Rent matematiskt kan man då teckna entalpiförändringen för en viss reaktion, ΔH, såhär:
H H H =–∑∑f,produkterf,reaktanter 00
Tecknet ∑ betyder ”summan av” och ΔH f 0 är bildningsentalpierna för produkterna och reaktanterna.
EXEMPEL 1
När bensen, C6H6, förbränns bildas koldioxid och vatten enligt nedanstående reaktionsformel:
C6H6(g) + 7,5O2(g) 6CO2(g) + 3H2O(l)
Beräkna förbränningsentalpin för bensen. Följande bildningsentalpier är kända:
ΔH H fCkJ/mol , 6 6 0 49 =
ΔH fOkJ/mol , 2 0 0 =
Lösning
ΔH fHOkJ/mol , 2 0 2 =–86 ΔH f CO kJ/mol , 2 0 394 =–
För att beräkna den totala förändringen i entalpi ska vi addera alla bildningsentalpierna för produkterna och dra ifrån alla bildningsentalpierna för reaktanterna. Vi tecknar ∆H så här: Δ Δ ΔΔ Δ HH HH H =–=+. ( fprodukterfreaktanterfC ,,OfHO ,, 00 630022 ) –+ ( ) Δ Δ H H fCHfO ,, 66 2 0 0 ∑ ∑ =. –() +. –() () – + () kJ/molkJ 6/ 394 3 286 49 0 mo lkJ/mo =l –3 271
Svar: Förbränningsentalpin för bensen är –3 271 kJ/mol.
ÖVNINGSUPPGIFTER
Öva begreppen
1. Ange för var och en av reaktionerna nedan om de är endoterma eller exoterma.
a. CH4(g) + 2O2(g) CO2(g) + 2H2O(l)
b. H2O(s) H2O(l)
c. 6CO2(g) + 6H2O(l) C6H12O6(s) + 6O2(g) ∆H = +2 803 kJ/mol
d. HCl(aq) + NaOH(aq) NaCl(aq) + H2O(l) + 57,1 kJ
2. Vilka av nedanstående påståenden om bildningsentalpi är riktiga?
a. Bildningsentalpin är alltid negativ.
b. Bildningsentalpin anges oftast för grundämnenas aggregationstillstånd vid standardtemperatur och standardtryck.
c. Eftersom ∆H = –394 kJ för reaktionen C(s) + O2(g) CO2(g) kan vi också säga att bildningsentalpin för koldioxid är ΔH fC,OkJ 2 0 394 =–
Öva förståelsen
3. Använd tabellen med bildningsentalpier på sida 415 för att beräkna förändringen i entalpi, ∆H, för följande reaktioner:
a. C3H8(g) + 5O2(g) 3CO2(g) + 4H2O(l)
b. Fe2O3(s) + 2Al(s) Al2O3 + 2Fe(s)
c. N2(g) + 3H2(g) 2NH3(g)
d. CaCO3(s) CaO(s) + CO2(g)
4. För kvävetrifluorid NF3 gäller att bildningsentalpin är ΔH fNFkJ/mol , 3 0 114=– . För kvävetriklorid
NCl₃ är bildningsentalpin ΔH fNClkJ/mol , 3 0 115 =+ . Ett av ämnena är explosivt. Vilket då, och hur kan man se det?
5. Ammoniak framställs industriellt genom att man låter vätgas reagera med kvävgas enligt nedanstående reaktionsformel:
N2(g) + 3H2(g) 2NH3(g)
För reaktionen gäller att ∆H = −92 kJ. Hur stor är bildningsentalpin för ammoniak, ΔH f,NH 3 0 ?
Analysera och diskutera
• Vad innebär det för ett ämnes kemiska egenskaper om det har en hög eller en låg bildningsentalpi, eller om den är positiv eller negativ?
A2. Hess lag
Om du har försökt cykla uppför en lång backe någon gång, har det kanske hänt att du har tröttnat, klivit av cykeln och istället lett cykeln upp till backens krön. Men vilket är egentligen jobbigast? Att gå uppför hela backen (vilket tar längre tid) eller att cykla uppför den?

Vägen spelar ingen roll för energiförändringen
Om du promenerar uppför en kulle eller ett berg, så kommer din lägesenergi att öka. När du har nått toppen kommer du att ha fått en viss lägesenergi oavsett om du tog helikopter upp till toppen eller om du vandrade längs snirkliga serpentinvägar. På samma sätt förlorar du exakt lika mycket i lägesenergi när du tar dig ner igen, oavsett om du åker störtlopp rakt ner, eller om du tar samma slingriga vägar som du vandrade upp.
Din förändring i (läges-)energi blir samma oavsett vilken väg du tar
Oavsett vilken väg du tar upp till toppen, så kommer du att ha samma lägesenergi när du väl är där.

Det är på exakt samma sätt med kemiska reaktioner och med förändringen i entalpi. Det spelar ingen roll vilken reaktionsväg man tar – förändringen i entalpi, ΔH, blir alltid densamma, hur reaktionen än sker.
Förbränning av kol i ett eller två steg
Vi tittar på förbränning av kol i två steg för att visa hur det går till. Om man förbränner kol med dålig syretillförsel bildas kolmonoxid, CO(g) enligt den här reaktionsformeln:
C(s) + ½O2(g) CO(g) + 111 kJ
Man har alltså mätt upp att för denna reaktion gäller att ΔH = −111 kJ, för varje mol CO som bildas. Kolmonoxid kan reagera vidare med ytterligare syrgas och bilda koldioxid. För den reaktionen har man mätt upp att det frigörs 28�� kJ för varje mol bildad koldioxid enligt den här reaktionsformeln:
CO(g) + ½O2(g) CO2(g) + 28�� kJ
För den reaktionen gäller alltså att ΔH = −28�� kJ/mol bildad CO2
I de två reaktionerna frigörs först 111 kJ och sedan 28�� kJ, alltså sammantaget ��9�� kJ. Detta är exakt lika mycket som frigörs i reaktionen där kol förbränns till koldioxid enligt den här reaktionsformeln:
C(s) + O2(g) CO2(g) + ��9�� kJ
Vi ser här att oavsett om reaktionen sker i två steg eller bara i ett, så blir det samma förändring i entalpi, ΔH. Detta kallas för Hess lag, och den innebär att oavsett reaktionsväg, så är den totala förändringen i entalpi, ΔH, densamma.
C(s) + O2(g)
Entalpi, H
CO(g) + ½O2(g)
CO2(g) ∆H1 = –111 kJ
∆H2 = –283 kJ ∆H tot = –394 kJ
Den totala förändringen i entalpi ( Htot) är lika stor som entalpiförändringen i de två delreaktionerna ( H1 och H2).
EXEMPEL 2
Beräkna ∆H för följande reaktion:
2FeO(s) + ½O2(g) Fe2O3(s)
Följande två reaktioners förändringar i entalpi är kända:
2FeO(s) 2Fe(s) + O2(g) H = +556 kJ
2Fe(s) + 1½O2(g) Fe2O3(s) H = –826 kJ
Lösning
Om vi adderar delreaktionerna kommer vi att få en nettoreaktion som är exakt den reaktion vi är ute efter:
Delreaktion 1 2FeO(s) 2Fe(s) + O2(g) H = +556 kJ + Delreaktion 2 2Fe(s) + 1½O2(g) Fe2O3(s) H = –826 kJ
Totalreaktion 2FeO(s) 2Fe(s) + O2(g) 2Fe(s) + 1½O2(g) Fe2O3(s) H = –270 kJ
Vi kan förkorta bort 2Fe(s) och 1O₂(g) både till höger och vänster om reaktionspilen. Då får vi följande nettoreaktion:
2FeO(s) + ½O2(g) Fe2O3(s) H = –270 kJ
ÖVNINGSUPPGIFTER
Öva begreppen
6. Vad är den grundläggande innebörden av Hess lag?
a. Den totala entalpiförändringen för en reaktion är densamma oavsett om reaktionen sker i ett eller flera steg.
b. Alla kemiska reaktioner är exoterma om de sker spontant vid rumstemperatur.
c. Endast reaktioner som involverar gaser kan analyseras med hjälp av entalpiförändringar.
d. Entalpiförändringen för en reaktion beror på den väg reaktionen tar från reaktanter till produkter.
7. Bildningsentalpin för kolmonoxid, CO(g), är svår att mäta direkt. Entalpierna för följande reaktioner är dock kända:
C(s) + O2(g) CO2(g) Δ H = –394 kJ/mol
CO(g) + ½O2(g) CO2(g) Δ H = –111 kJ/mol
Använd dem för att beräkna entalpiförändringen, H, för nedanstående reaktion:
C(s) + ½O2(g) CO(g)
Öva förståelsen
8. Följande tre reaktioner är kända:
Na+(g) + Cl (g) Na(g) + Cl(g) + 147 kJ
Na(g) + Cl(g) Na(s) + ½Cl₂(g) + 230 kJ
Na(s) + ½Cl2(g) NaCl(s) + 411 kJ
Använd dem för att beräkna H för reaktionen Na⁺(g) + Cl⁻(g) NaCl(s)
9. Följande två bildningentalpier är kända: H f,FeCl 2 kJ/mol 0 341 8 =–, och H f,F eCl 3 kJ/mol 0 399 5 =–, .
a. Skriv reaktionsformler för bildning av FeCl2 och FeCl3 ur grundämnena. Sätt också in rätt energimängd till höger eller vänster om reaktionspilarna.
b. Utnyttja reaktionsformlerna i fråga a) för att beräkna H för reaktionen 2FeCl2(s) + Cl2(g) 2FeCl3(s).
Analysera och diskutera
• Diamant bildas genom att kol (grafit) pressas samman under värme och högt tryck. Bildningen kan beskrivas med följande reaktionsformel:
C(grafit) C(diamant)
Hur skulle man kunna bära sig åt för att mäta entalpiförändringen, H, för bildningen av diamant?
A3. Bindningsentalpi
När vi tittade på kemisk bindning i kemi nivå 1 fick du lära dig att olika bindningar är olika starka. Vätebindningar är till exempel starkare än van der Waals-bindningar, men de är betydligt svagare än kovalenta bindningar. Men hur mycket? Finns det något sätt som man kan använda för att sätta en siffra på hur stark en bindning är?

H2, universums enklaste (och vanligaste) molekyl.
Att bryta bindningar kräver energi
Vätemolekylen, H2, är universums enklaste molekyl. Den består av två väteatomer som sitter ihop med en elektronparbindning. För att bryta bindningen mellan två atomer (eller två ämnen) måste man alltid tillföra energi. Mellan två väteatomer i en vätemolekyl behöver man tillsätta ����6 kJ för att bryta bindningen så att det bildas två fria väteatomer istället:
H2(g) H(g) + H(g) ∆H = +����6 kJ/mol
Den mängd energi som krävs för att bryta en viss bindning kallas för bindningsentalpi. Eftersom det krävs energi för att bryta en bindning är bindningsentalpin alltid positiv.
Hur man beräknar entalpiändring med bindningsentalpier
Eten, C2H��(g), och vätebromid, HBr(g) kan reagera med varandra i en slags reaktion som kallas för additionsreaktion. Då bildas brometen enligt den här reaktionsformeln:
C2H��(g) + HBr(g) C2H5Br(g) ∆H = –105,7 kJ/mol
För denna reaktion har man mätt upp att det avges 105,7 kJ för varje mol C2H��(g) som reagerar. Man kan också skriva reaktionen med strukturformler:
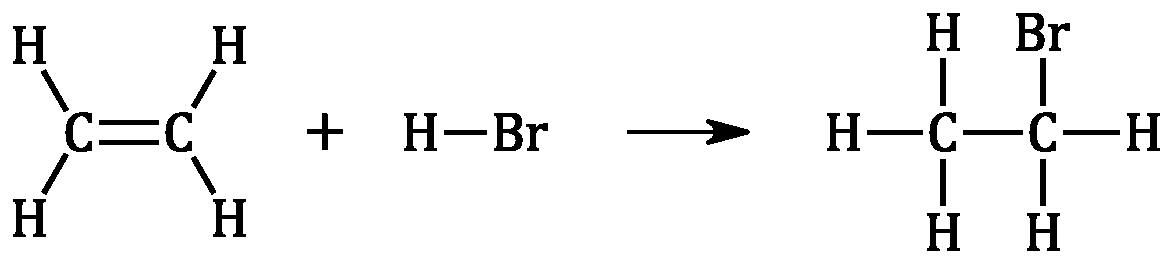
När den här reaktionen sker kan man lite förenklat se det som att den ena av bindningarna i dubbelbindningen mellan kolatomerna öppnas upp. Det gör att väteatomen från HBr kan binda till den ena kolatomen och bromatomen från HBr kan binda till den andra kolatomen.
Men vi vet ju också från Hess lag att för ∆H spelar det ingen roll vilket sätt reaktionen sker på, så länge slutresultatet blir detsamma. Därför kan vi lika gärna tänka oss att i reaktionen bryts först samtliga bindningar mellan reaktanterna så att det finns två fria kolatomer, fem fria väteatomer och en bromatom. Sedan uppstår det nya bindningar mellan alla åtta atomerna så att det bildas brometan. Om vi då vet bindningsentalpierna för de olika bindningar som bryts och uppstår i reaktionen kan vi beräkna det teoretiska värdet på ∆H för reaktionen. Det blir summan av alla bindningsentalpier (BE) för bindningar som bryts minus summan av bindningsentalpierna som bildas, vilket vi kan beskriva matematiskt såhär:
Fysikaliska kemister har redan mätt upp bindningsentalpier för en mängd olika bindningar. Därför kan man hämta värden ur tabellsamlingen och till exempel se att bindningsentalpin för en enkelbindning mellan C–H är +��1�� kJ/mol och bindningsentalpin för en dubbelbindning mellan C=C är +61�� kJ/mol.
Med flera värden ur tabellsamlingen kan vi se att följande bindningsentalpier gäller för när bindningarna i reaktionen mellan eten och vätebromid bryts och bildas:
Bindningar bryts:
• 4 st. C–H (414 kJ/mol)
• 1 st. C=C (614 kJ/mol)
• 1 st. H–Br (366 kJ/mol)
Bindningar uppstår:
• 5 st. C–H (414 kJ/mol)
• 1 st. C–C (346 kJ/mol)
• 1 st. C–Br (285 kJ/mol)
Med hjälp av de värdena kan vi beräkna det teoretiska värdet på ΔH för reaktionen:
∆H = (�� · ��1�� + 61�� + ��66) kJ/mol – (5 · ��2�� + ����6 + 285) kJ/mol = –65 kJ/mol
Det teoretiska värdet på ΔH (–65 kJ/mol) skiljer sig dock avsevärt från det uppmätta värdet (–105,7 kJ/mol). Vad kan det bero på?
Kvävgasens trippelbindning är mycket starkare än vätgasens enkelbindning. Det kan du se på bindningsentalpierna för respektive bindning.
Bindningsentalpierna är medelvärden
Bindningsentalpin är den energimängd som krävs för att bryta en kemisk bindning. Även för identiska bindningar i en och samma molekyl, som C– H i eten, är inte bindningsentalpin konstant. När en C– H bindning bryts förändras molekylen, vilket påverkar energin som behövs för att bryta nästa C–H-bindning.
De värden för bindningsentalpi som man hittar i tabeller är därför medelvärden från mätningar på många olika ämnen. Det gör att teoretiska beräkningar av en reaktions entalpiändring (ΔH) blir en uppskattning som kan skilja sig från det verkliga, uppmätta värdet.
Bindningsentalpier och bindningars styrka
Bindningsentalpins storlek är ett direkt mått på bindningens styrka. Ju högre bindningsentalpi, desto starkare bindning. Detta förklarar varför vissa ämnen är mer reaktiva än andra.
Till exempel har kvävgas (N2) en mycket stark trippelbindning med en bindningsentalpi på 9��5 kJ/mol. Denna höga energikostnad för att bryta bindningen gör kvävgas väldigt stabil och reaktionströg (inert). Vätgas (H2), å andra sidan, har en svagare enkelbindning med en bindningsentalpi på ����6 kJ/mol. Eftersom det krävs mindre än hälften så mycket energi för att bryta H–Hbindningen är vätgas betydligt mer reaktivt än kvävgas. Detta kan jämföras med intermolekylära krafter, som väte- och van der Waalsbindningar, som är mycket svagare, med entalpier på endast cirka 2�� kJ/mol mellan två vattenmolekyler (vätebindning) respektive under 10 kJ/mol mellan två kvävemolekyler (van der Waalsbindning).


ÖVNINGSUPPGIFTER
Öva begreppen
10. Hur definieras bindningsentalpin för en specifik kovalent bindning, till exempel en O–H-bindning i en vattenmolekyl?
a. Bindningsentalpin är den totala summan av all kinetisk och potentiell energi som finns lagrad i hela den molekyl som innehåller den specifika bindningen.
b. Bindningsentalpin är den aktiveringsenergi som måste övervinnas för att molekylen ska kunna delta i en förbränningsreaktion med syrgas.
c. Bindningsentalpin är energi som frigörs när en mol av bindningen bildas från fria atomer i gasfas; denna process är alltid starkt exoterm.
d. Bindningsentalpin är den energi som krävs för att bryta en mol av bindningen i gasfas.
11. Varför är värdena för bindningsentalpi som man hittar i tabeller ofta angivna som genomsnittliga värden? Ge ett exempel med C–H-bindningen.
Öva förståelsen
12. I luften finns både kvävgas (N2) och syrgas (O2). I kvävgasen sitter atomerna ihop med en trippelbindning och i syrgas sitter atomerna ihop med en dubbelbindning. Vilken av bindningarna har högst bindningsentalpi, och varför?
13. Vätgas och syrgas reagerar med varandra och bildar vatten i den klassiska knallgasreaktionen:
2H2(g) + O2(g) 2H2O(g)
Beräkna H för reaktionen när följande bindningsentalpier är kända:
H–H: 436 kJ/mol
O=O: 498 kJ/mol
14. Metangas förbränns enligt nedanstående reaktionsformel:
CH4(g) + 2O2(g) CO2(g) + 2H2O(g)
Beräkna H för reaktionen när följande bindningsentalpier är kända:
C–H: 413 kJ/mol
O=O: 498 kJ/mol
Analysera och diskutera
C=O: 804 kJ/mol
O–H: 464 kJ/mol
O–H: 464 kJ/mol
• Starka bindningar ger stabila material, men ibland behövs istället material som lätt kan brytas ner eller förändras. På vilket sätt skulle kunskap om bindningsentalpier kunna påverka hur vi designar nya material, från plaster till läkemedel?
A4. Entropi och Gibbs fria energi
Ta och titta en stund på ditt eget rum (eller varför inte toaletterna på skolan)! Om inte någon lägger lite energi på att hålla ordning, kommer det att bli stökigare och stökigare. Det är nästan som om det vore någon slags naturlag. Kan det vara det?

Från ordning till oordning
Om man släpper en droppe bläck i en bägare med vatten, så kommer droppen med bläck först att sjunka mot botten. Men efterhand som tiden går kommer färgen att sprida sig mer och mer i vattnet, även om man inte rör om det allra minsta i det. Detta kallas för diffusion. Till slut kommer bläcket att ha diffunderat ut i hela bägaren, så att bläckkoncentrationen är lika hög oavsett var i bägaren man tittar.

När bläcket är samlat i droppröret är det betydlig mer ordnat än vad det är när det har diffunderat ut helt i vattnet i bägaren. Av detta kan vi dra slutsatsen att oordningen i systemet hela tiden ökar. Det beror på att sannolikheten hela tiden är större att färgämnena i bläcket rör sig utåt, mot lösningen, än inåt, för att samlas i en enda sammanhållen bläckdroppe igen.
Men det här gäller inte bara en droppe bläck i en bägare med vatten, utan i alla slutna system: De strävar hela tiden efter en större oordning. Oordningen kallas för entropi och tecknas S. Den har enheten joule per kelvin (J/K). Om oordningen ökar i en reaktion blir ΔS > 0 och om den minskar blir ΔS < 0.
Det allra största slutna systemet vi känner till, det är hela universum. Vi har observerat att oordningen i universum hela tiden ökar, alltså att universums entropi hela tiden ökar. Detta kallas för termodynamikens andra huvudsats, och är egentligen bara ett så kallat postulat. Det innebär att vi har kunnat konstatera att det är så, men egentligen aldrig kunnat förklara varför.
En droppe av bläck diffunderar spontant ut i vattnet även om man inte rör om i bägaren.
Oordningen ökar hela tiden om man inte tillför energi för att upprätthålla ordningen.

Entropin i en iskristall är låg medan entropin är högre i flytande vatten. I vattenånga är entropin allra högst.
Ett och samma ämne kan ha olika entropi beroende på vilket aggregationstillstånd det befinner sig. Fasta ämnen har låg entropi, eftersom de ingående atomerna är samlade på ett (mer eller mindre) regelbundet sätt i det fasta ämnet. I ett flytande ämne är entropin högre och i gasform är entropin allra högst.
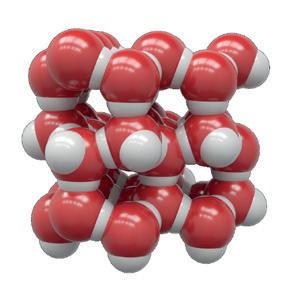
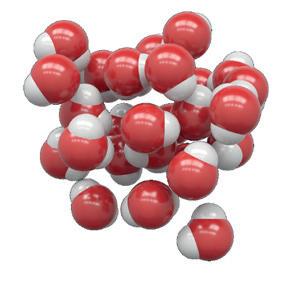
Flytande vatten
Is H2O(s) H2O(g)
H2O(l)
Låg entropi
När sker en kemisk reaktion?
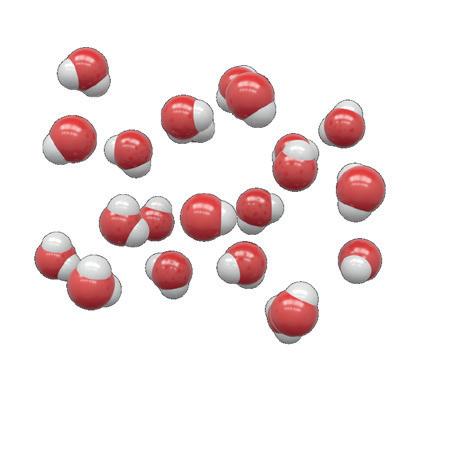
Hög entropi
Om du placerar en boll på en kulle är sannolikheten hög att bollen rullar ner. Då förlorar bollen i energi. Om du har bollen nere vid kullens fot är däremot sannolikheten mycket låg att den rullar uppåt igen. Ungefär likadant är det med kemiska reaktioner. Om man har ett ämne med hög entalpi är det stor sannolikhet att det reagerar och omvandlas till ett ämne med låg entalpi. Det som sker då är en exoterm reaktion, där ΔH < 0. Exoterma reaktioner är ofta spontana, det vill säga man behöver inte tillföra någon ytterligare energi för att de ska ske.
En sådan reaktion är den som inträffar när ammoniumnitrat, NH��NO�� (s), exploderar. Vi kan skriva den reaktionen med följande reaktionsformel:
NH��NO�� (s) N2 (g) + 2H2O(g) + ½O2 (g) + energi ΔH < 0
I det här fallet går vi också från ett system med låg entropi (den fasta ammoniumnitraten, NH��NO��(s)) till ett system med hög entropi (alla gaspartiklarna som bildas i reaktionen). Eftersom oordningen ökar i reaktionen blir ΔS > 0.
Men det finns också tillfällen då en endoterm reaktion sker spontant (och bollen så att säga rullar uppför kullen igen)! Det inträffar om oordningen samtidigt ökar tillräckligt mycket. Vi tar samma ämne igen, ammoniumnitrat, och ser vad som händer när den löses i vatten. Det som händer då är att den fasta ammoniumnitraten omvandlas till vattenlösta ammonium- och nitratjoner, samtidigt som temperaturen sjunker och det blir kallt:
NH��NO��(s) + energi NH 4 + (aq) + NO 3 (aq) ΔH > 0
I den fasta ammoniumnitraten är entropin låg, precis som innan. När ammoniumnitraten löses och bildar vattenlösta joner ökar oordningen och därmed entropin markant. Även i den här reaktionen blir alltså ΔS > 0.
Spontana och icke-spontana reaktioner
Att en reaktion är spontan betyder att den kan ske utan att ytterligare energi tillförs (förutom aktiveringsenergin). En icke-spontan reaktion kan bara ske om det tillförs energi kontinuerligt till den. För att utvärdera om en viss reaktion är spontan eller inte kan man titta på förändringen i Gibbs fria energi, ΔG för reaktionen.
Gibbs fria energi är ett samband mellan entalpi, temperatur och entropi hos ett system. Det sambandet ser ut såhär:
ΔG = ΔH – T∆S
där ΔH är förändringen i entalpi, T är systemets temperatur i K och ΔS är förändringen i entropi. Om ΔG < 0 finns det tillräckligt mycket fri energi i systemet för att underhålla reaktionen, som då blir spontan. Om ΔG > 0 är reaktionen inte spontan.
Av alla icke-spontana reaktioner är kanske fotosyntesen den allra viktigaste. I den fogas koldioxid och vatten samman till glukos med hjälp av energin i solljuset:
6CO2(g) + H2O(l) + energi C6H12O6(aq) + 6O2(g)
Vi ska nu titta på fyra exempel för att utvärdera om reaktionen är spontan eller inte.

Fotosyntesen är en icke-spontan reaktion eftersom den är beroende av en ständig tillförsel av solenergi för att fortgå.
EXEMPEL 3
Blyazid, Pb(N3)2, är ett ämne som mycket lätt sönderfaller till fast bly och kvävgas. I princip exploderar det, samtidigt som det frigörs en hel del energi:
Pb(N3)2(s) Pb(s) + 3N2(g) + energi
Vi kan konstatera att H < 0 eftersom det är en exoterm reaktion. Vi kan också konstatera att S > 0 eftersom oordningen ökar i reaktionen. Vad betyder detta för G?
G H T S =–
För det första kan vi se att eftersom temperaturen aldrig kan bli lägre än 0K och S > 0, kommer T S alltid att bli större än noll, oavsett temperatur. Eftersom reaktionen är exoterm är H < 0 kommer uttrycket H – T S också alltid att var mindre än noll. Vi får då att för den här reaktionen är alltid G < 0, och den är alltid spontan.
EXEMPEL 4
I knallgasexplosionen reagerar vätgas och syrgas med varandra, och bildar vatten samtidigt som det avges energi:
2H2(g) + O2(g) 2H2O(g) + energi
Vi ser att H < 0 eftersom reaktionen är exoterm. Vi ser också att entropin minskar i och med att det är tre gaspartiklar till vänster om reaktionspilen, men bara två till höger om den. Det betyder att S < 0 för reaktionen. Vad betyder det för tecknet på G, och om reaktionen är spontan eller inte?
G H T S =–
> < 0 0
0 förlåga T
> 0 förhöga T >
För det första har vi redan konstaterat att H < 0 för den här reaktionen. I det här fallet kommer T S alltid att bli mindre än noll, eftersom S < 0. Om temperaturen T är låg kommer inte heller värdet på – T S att vara så stort, och hela uttrycket H – T S kommer att fortsätta vara mindre än noll. Det betyder att vid låga temperaturer är G < 0, och reaktionen är spontan.
Vi högre temperatur T blir dock värdet på –T S så stort att uttrycket H – T S blir positivt. Det betyder att vid höga temperaturer blir G > 0, och reaktionen är inte längre spontan. Detta stämmer också med vad som händer om vatten upphettas. Om temperaturen är tillräckligt hög sönderdelas vatten till vätgas och syrgas enligt nedanstående reaktionsformel:
H2O(g) + energi 2H2(g) + O2(g)
EXEMPEL 5
Upplösning av ammoniumnitrat, NH4NO3(s), i vatten är en endoterm process, vilket vi har konstaterat tidigare i avsnittet:
NH4NO3(s) + energi NH 4 +(aq) + NO3 (aq)
Eftersom reaktionen är endoterm är H > 0. Vi ser också att entropin ökar i reaktionen, och därför också att S > 0. Vad gäller nu för G och om reaktionen är spontan eller ej?
G H T S =–
> < < 0 0 0 förhöga T
0 förlåga T >
För att reaktionen ska vara spontan (och G < 0) måste T S vara större än H. Eftersom S > 0 sker detta om temperaturen T är tillräckligt hög. Om T är för låg finns det inte tillräckligt mycket energi i systemet för att ammoniumnitraten ska kunna lösas upp, utan den stannar kvar i fast form.
EXEMPEL 6
Hydrazin, N2H4, är ett mycket energirikt ämne som bland annat används som raketbränsle. Det kan bildas ur kvävgas och vätgas enligt nedanstående reaktionsformel:
N2(g) + 2H2(g) + energi N2H4(l)
Vad gäller för G för den här reaktionen?
G H T S =–
> < 0 0 0 föralla T
För den här reaktionen gäller att H > 0 eftersom det är en endoterm process, och att S < 0 eftersom entropin minskar i reaktionen. För att reaktionen ska vara spontan måste T∆S vara större än H. Det kommer dock aldrig att bli eftersom S < 0. Därför är G > 0 för den här reaktionen, oavsett vad temperaturen är. Därför är denna reaktion aldrig spontan, utan man måste hela tiden tillföra energi till den för att den ska kunna ske.
ÖVNINGSUPPGIFTER
Öva begreppen
15. För var och en av processerna nedan, ange om entropin ökar ( S > 0) eller minskar ( S < 0).
a. Vatten avdunstar från en sjö: H2O(l) H2O(g)
b. Socker löses upp i en kopp hett te.
c. Koldioxid fryser till kolsyreis (torris): CO2(g) CO2(s)
d. Vätgas och syrgas reagerar och bildar flytande vatten: 2H2(g) + O2(g) 2H2O(l)
16. Förbränning av metangas är en exoterm reaktion: CH4(g) + 2O2(g) CO2(g) + 2H2O(l).
För denna reaktion gäller att
H = –890 kJ/mol
S = –242 J/(mol·K)
a. Använd sambandet G = H – T S för att beräkna förändringen av Gibbs fria energi vid 25 °C (298 K).
b. Är reaktionen spontan eller inte vid 25 °C?
Öva förståelsen
17. Vid kalkbränning sönderdelas kalciumkarbonat enligt nedanstående reaktionsformel:
CaCO3(s) + energi CaO(s) + CO2(g)
a. Är värdet på H positivt eller negativt?
b. Är värdet på S positivt eller negativt?
c. Använd sambandet Δ G = H – T S för att utvärdera om reaktionen blir mer eller mindre spontan med stigande temperatur.
18. Använd sambandet G = H – T S för att utvärdera när och om följande reaktioner är spontana:
a. 2Na(s) + 2H2O(l) 2Na+(aq) + H2(g) + OH–(aq) + energi
b. 6CO2(g) + 6H2O(g) C6H12O6 (s) + 6O2(g) H = 2 816 kJ/mol
c. NH4NO3(s) + energi NH 4 + (aq)+ NO3 (aq)
Analysera och diskutera
• Termodynamikens andra huvudsats säger att universums totala entropi hela tiden ökar. Något som är levande är dock extremt välordnat och komplext. Hur är livets existens och evolutionen mot mer komplexa organismer möjlig i ett universum som enligt fysikens lagar strävar mot maximal oordning? Är levande organismer ett undantag från termodynamikens andra huvudsats?
A5. Reaktionshastighet
Tänk dig tillbaka till en varm dag på sommarlovet. Om du häller upp ett glas mjölk och låter det stå framme en timme, så är det en stor risk att mjölken har blivit dålig. I kylskåpet håller sig dock mjölken fräsch i flera dagar, kanske till och med en hel vecka. Du förstår såklart att det är för att det är kallt i kylskåpet. Men varför gör det att mjölken håller sig bättre?


Reaktioner sker långsamt i låga temperaturer. Därför kan man spara känsliga prover i flytande kväve i flera år utan att de bryts ner.
Faktorer som påverkar reaktionshastigheten
Att mjölken blir sur beror förstås på att det sker kemiska reaktioner i den som frigör sura ämnen. Reaktionerna går relativt fort i sommarvärmen, men mycket långsammare i kylskåpet.
Kemiska reaktioner kan alltså gå olika fort.
En del reaktioner går rasande fort, som explosioner till exempel. Andra, som när järn rostar, tar betydligt längre tid på sig. Vi kan konstatera dels att reaktioner kan ske med olika hastighet, och dels att det finns några olika faktorer som påverkar hur fort en reaktion går. Dessa faktorer är:
• Ämnenas inneboende egenskaper
• Temperatur
• Koncentrationen
• Närvaro av en katalysator
Ämnenas
inneboende egenskaper
Redan i kemi nivå 1 fick du lära dig att olika grundämnen reagerar olika kraftigt. Om man tittar på exempelvis alkalimetallerna (grupp 1) kommer man kanske ihåg att francium är den mest reaktiva av alla alkalimetallerna. Det beror på att joniseringsenergin för francium är så pass låg, vilket i sin tur beror på att franciumatomens enda valenselektron är så långt ifrån atomkärnan att den känner av kärnladdningen så svagt att det bara behövs lite energi för att avlägsna den helt från atomen.
Grundämnena i det periodiska systemet är olika reaktiva, bland annat beroende på atomernas storlek och antal valenselektroner.
Om man släpper ner en bit litium i en bägare med vatten kommer det att ske en rätt så kraftig reaktion, där det bildas vätgas, litiumjoner och hydroxidjoner. Om man släpper ner en bit rubidium kommer samma typ av reaktion att ske, men den kommer att vara mycket kraftigare. Att reaktionen går fortare med rubidium än med litium beror på rubidiumets och litiumets inneboende egenskaper.
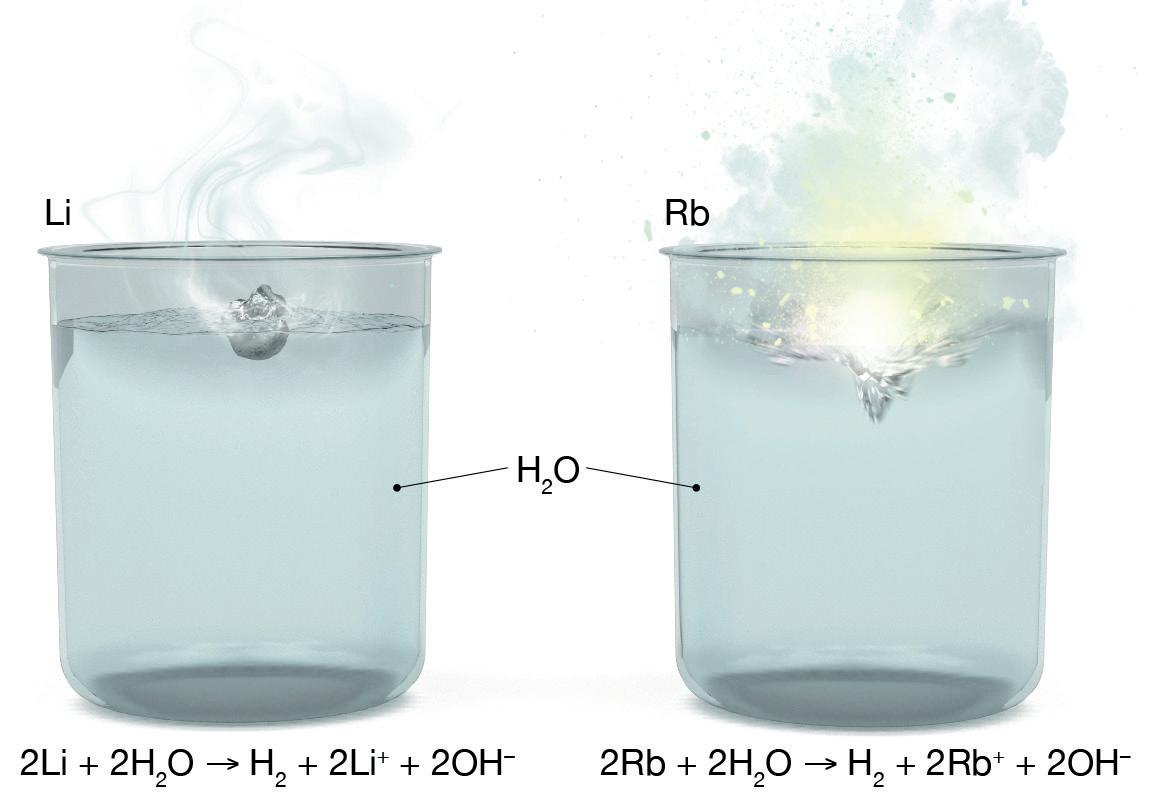
Även ett ämnes fysikaliska egenskaper spelar roll för hur fort reaktionen sker. Om du jämför hur fort det går att lösa grovt salt i vatten med hur fort det går att lösa finsalt, kommer du att se att det grova saltet tar mycket längre tid att lösa upp. Eftersom finsaltet har större angreppsyta, det vill säga större yta som är exponerad mot vattnet, går det fortare för jonerna att lösa sig i vattnet.
I en järnspik sitter järnatomerna mycket tätt packade, och bara de som är allra ytterst är exponerade mot syret och vattnet i omgivningen. Om man istället filar ner spiken till järnfilspån blir den sammanlagda ytan mycket större, och järnet reagerar mycket fortare med luftens syre. Det är därför som det är ganska lätt att sätta fyr på ett tomtebloss, men omöjligt att sätta fyr på en järnspik med bara en tändsticka.
Både när litium och rubidium reagerar med vatten bildas vätgas H2, hydroxidjoner OH och metalljoner. Reaktionen med rubidium är dock mycket kraftigare, vilket är ett annat sätt att säga att den sker med högre hastighet.
Temperatur
Vi har redan konstaterat att mjölken lättare blir dålig en varm sommardag, i 25 °C värme, än om man låter den vara i kylskåpet. Det beror på att reaktioner går fortare ju högre temperaturen är.
För att kunna förklara varför reaktioner sker fortare ju högre temperaturen är, måste vi titta på varför reaktioner sker. För att en reaktion ska kunna ske mellan två ämnen, måste de ämnenas atomer kollidera med varandra. Det räcker dock inte med att de krockar in i varandra, utan kollisionen måste både ske på rätt sätt, och med tillräckligt hög energi.
Vi tittar på reaktionen mellan kvävedioxid NO2 och kolmonoxid
CO som exempel. Vid reaktionen bildas kvävemonoxid NO och koldioxid CO2 enligt följande reaktionsformel:
NO2 + CO NO + CO2
För att reaktionen ska kunna ske, måste kollisionen inträffa så att kolatomen stöter ihop med en av syreatomerna hos kvävedioxiden. Om kolatomen krockar med kväveatomen sker det ingen reaktion, utan det är bara när kolatomen krockar med en av syreatomerna i kvävedioxiden som det kan ske någon reaktion.
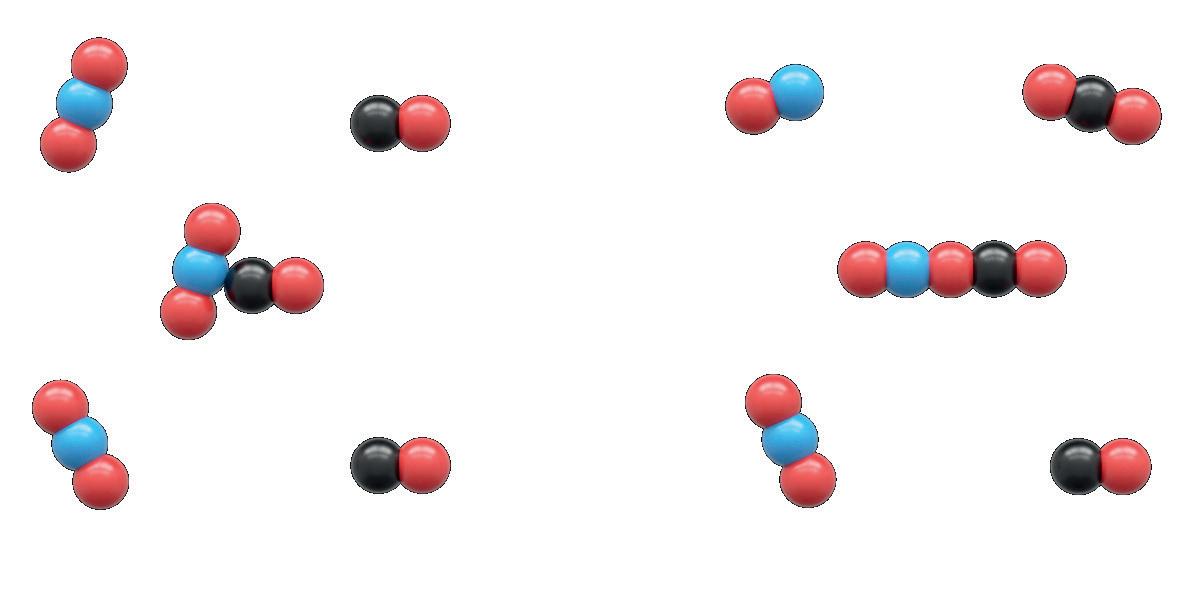
I bilden till vänster sker ingen reaktion eftersom kolatomen krockar med kväveatomen. I bilden till höger krockar kolatomen med en av syreatomerna i kvävedioxiden, och det bildas koldioxid och kvävemonoxid.
Det räcker dock inte med att kollisionen sker på rätt sätt, den måste som sagt också ske med tillräckligt hög energi. Från kemi nivå 1 kommer du ihåg att den energi som krävs för att en reaktion ska sätta igång kallas för aktiveringsenergin. Temperaturen hos ett ämne är ett mått på hur hög rörelseenergi partiklarna (atomerna/jonerna/ molekylerna) i ämnet har. Ju högre temperatur, desto högre energi har också partiklarna.
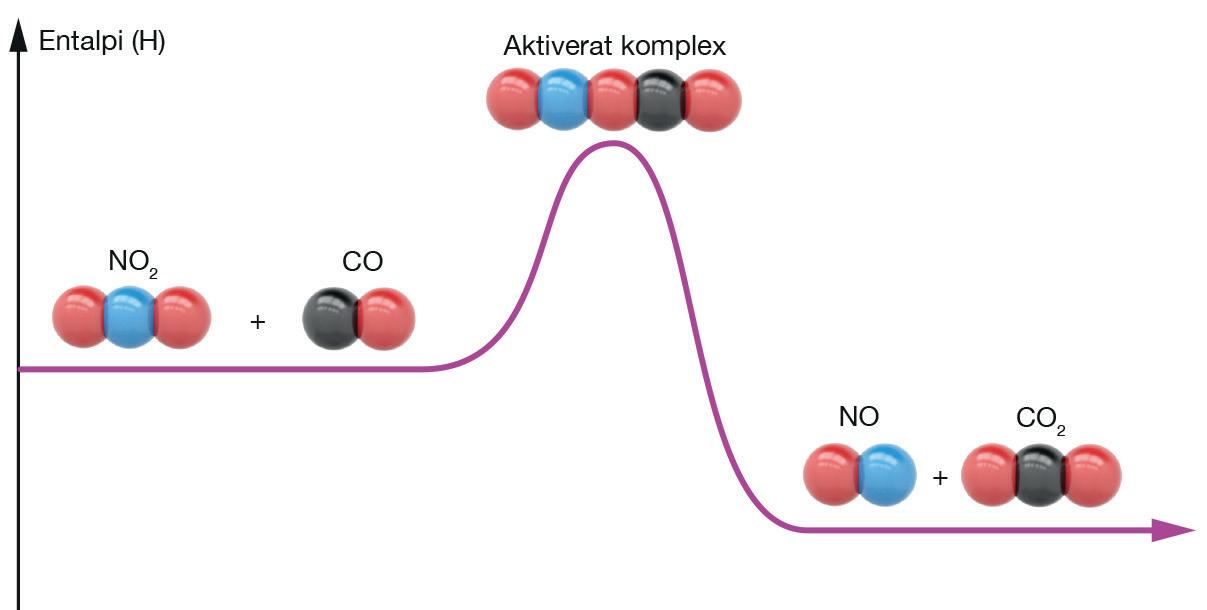
Om partiklarna har tillräckligt hög energi, och de kolliderar på ett korrekt sätt, så uppnår de ett tillfälligt stadium som kallas för aktiverat komplex. Det aktiverade komplexet är en övergångsform eller intermediär som mycket snabbt sönderfaller till produkterna. En hög temperatur leder alltså till att det sker fler energirika kollisioner mellan reaktanterna varje sekund. Därför blir reaktionshastigheten högre, ju högre temperaturen är.
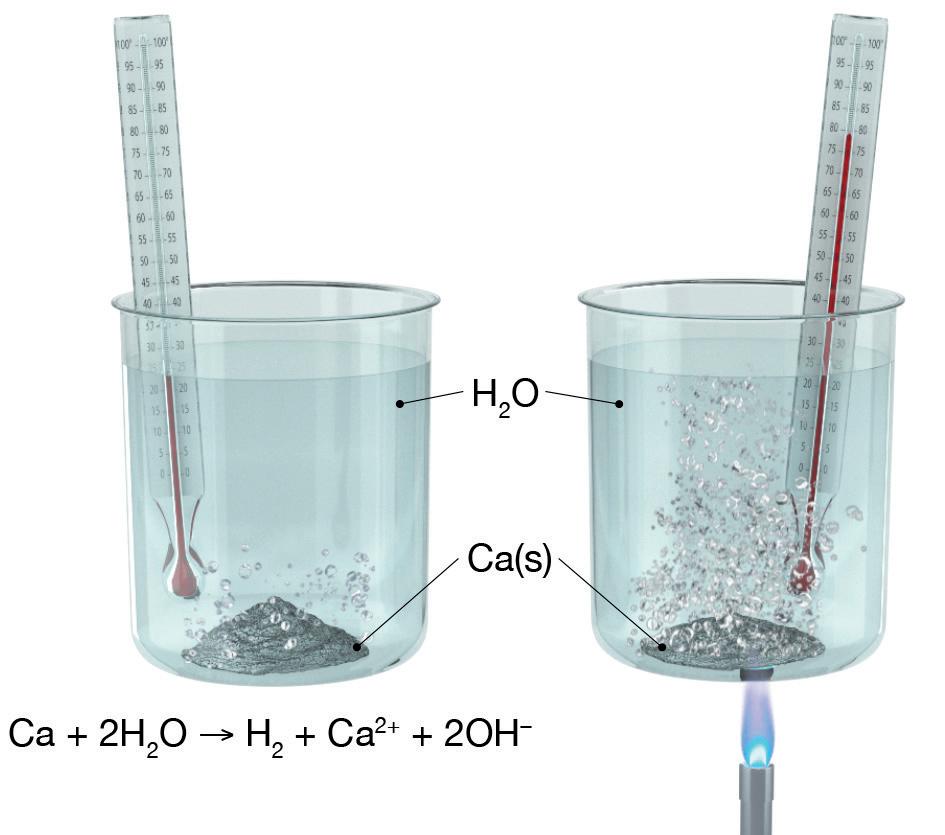
Om NO2- och CO-molekylerna har tillräckligt hög energi kan de bilda ett aktiverat komplex när de kolliderar. Det aktiverade komplexet sönderfaller mycket fort till produkterna NO och CO2.
Kalcium reagerar med vatten och oxideras till kalciumjoner Ca2+ Samtidigt reduceras vattnet till vätgas H2 och hydroxidjoner OH I varmt vatten sker reaktionen fortare än i kallt.
Koncentration
Om man stoppar ner en bit magnesium i saltsyra sker följande reaktion:
Mg(s) + 2HCl(aq) MgCl2(aq) + H2(g)
Upplösningen sker mycket fortare om man använder koncentrerad saltsyra än om man använder utspädd saltsyra. Det beror på två saker.
Vid högre koncentration finns det förstås fler partiklar i reaktionsblandningen. Det gör att det är större sannolikhet att två reaktanter träffar på varandra, det vill säga att det oftare sker kollisioner mellan reaktanterna.
Men vi vet ju redan att det inte räcker med att det sker kollisioner, de måste dessutom ske med tillräckligt hög energi. Temperaturen på ett ämne är ett genomsnitt av alla atomernas temperatur eller rörelseenergi. Det betyder att det finns några atomer som har lägre rörelseenergi än genomsnittet, men också att det finns de som har högre temperatur än genomsnittet. Med högre koncentration ökar det totala antalet atomer, och därmed också det totala antalet atomer med tillräckligt hög energi för att det ska kunna ske en reaktion. Därför ökar reaktionshastigheten med ökad koncentration.
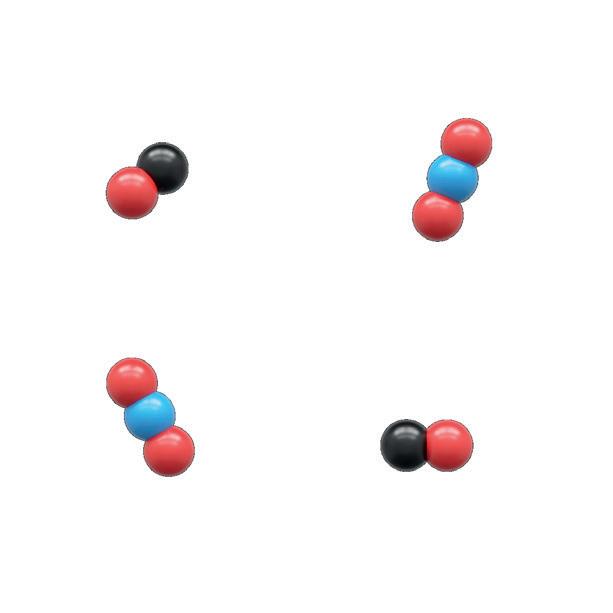
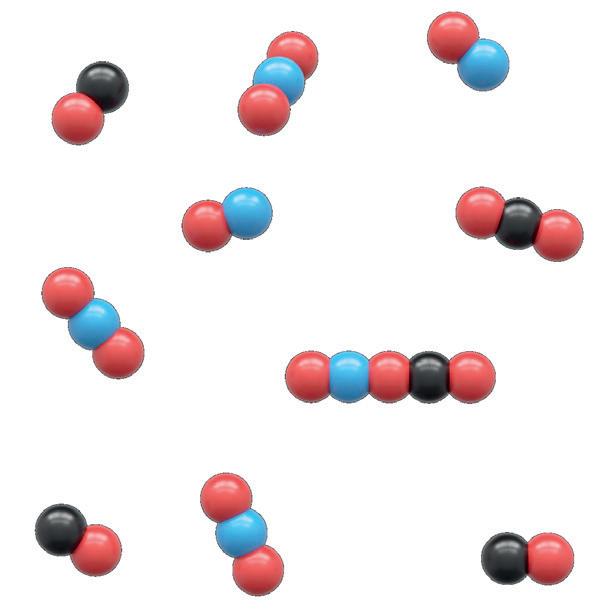
Eftersom koncentrationen är högre i reaktionskärlet till höger ökar sannolikheten att två molekyler med rätt energi kolliderar med varandra och reagerar.
Katalysator
När bensinen förbränns i en bilmotor sker det vid så hög temperatur att även en del kvävemolekyler oxideras. Det bildas en blandning av framför allt kvävemonoxid NO och kvävedioxid NO2, en blandning som ofta skrivs NOx. Kväveoxiderna är skadliga eftersom de snabbt reagerar med luftens vattenånga och syre och bildar salpetersyra HNO��.
I bilens avgassystem sitter det en katalysator. Den har till uppgift att göra så att kväveoxiderna omvandlas till syre och kvävgas igen (samt att förbränna kvarvarande bränslerester i avgaserna). Avgaskatalysatorn består vanligen av platina eller av en legering av palladium och rodium.
En katalysator är ett ämne som påskyndar en viss reaktion utan att själv förbrukas. Det kan katalysatorn göra genom att öppna upp en ny reaktionsväg, en reaktionsväg som inte kräver lika hög aktiveringsenergi som den okatalyserade reaktionen. I avgaskatalysatorn går katalysen mycket förenklat till så att kväveoxiderna gärna binder till ädelmetallerna. På det sättet kommer kväveoxidmolekylerna närmare varandra, och kan då också lättare reagera med varandra.
Ett enzym är ett protein som fungerar som en katalysator. Enzymerna styr nästan allt som sker i dina celler. Det kan de göra för det första tack vare att de är mycket specifika, det vill säga de katalyserar bara en enda reaktion. För det andra sänker de aktiveringsenergin för reaktionen de katalyserar flera miljoner, och ibland många miljarder gånger. Vi kommer att titta noggrannare på hur enzymer fungerar längre fram i kursen, i avsnittet om biokemi.

Vid bilbesiktningen kontrollerar man att katalysatorn fungerar som den ska, och att halterna av kväveoxider inte är för höga.
Tack vare katalysatorn öppnas en ny reaktionsväg med lägre aktiveringsenergi upp.
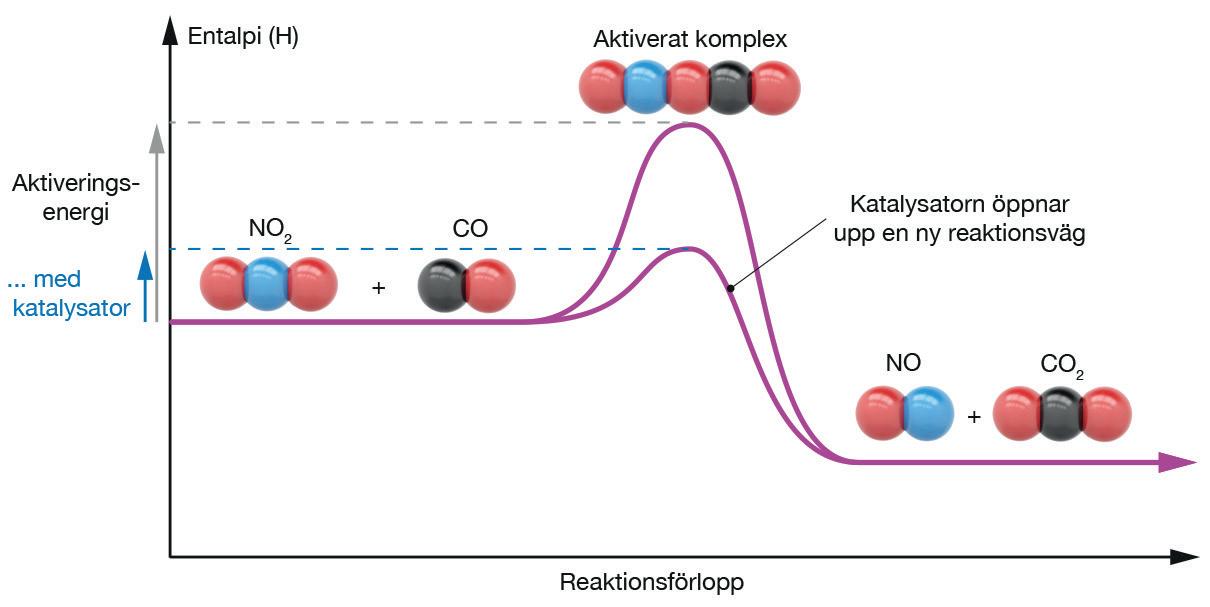
ÖVNINGSUPPGIFTER
Öva begreppen
19. Vilka av nedanstående processer går fort, och vilka går långsamt?
a. När man kokar ett ägg.
b. När deg jäser i ett varmt rum.
c. När äppeljuice omvandlas till cider.
d. När bensin förbränns i en bilmotor.
Öva förståelsen
20. I ett försök löste man upp en liten bit tavelkrita i 50 ml 2 M saltsyra för att beräkna halten kalciumkarbonat i tavelkritan. Vilket av påståendena a–e nedan är felaktigt?
För att få reaktionen att gå fortare kan man
a. finfördela kritan
b. använda 4 M saltsyra istället för 2 M saltsyra
c. höja temperaturen
d. tillsätta någon form av katalysator
e. Inget av påståendena ovan är felaktigt.
21. Varför går en reaktion fortare om man höjer temperaturen?
Analysera och diskutera
• Katalys är viktig och helt nödvändig i väldigt många kemiska reaktioner, inte minst biokemiska processer. Varför tror du att det är så?
A6. Jämviktsreaktioner
och jämviktsekvationen
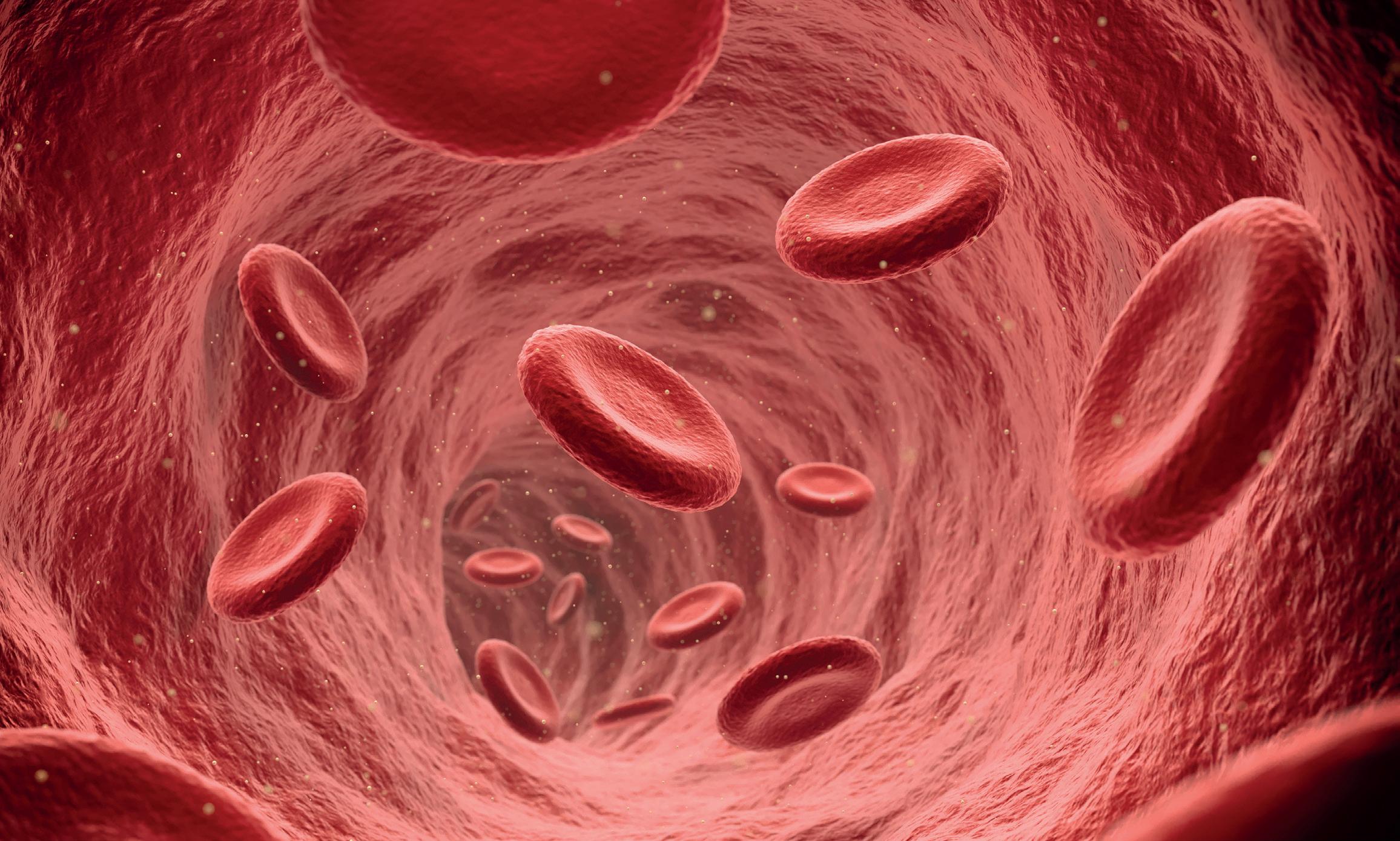
Ta ett djupt andetag. Luften och syret strömmar ner i dina lungor. Där kommer syret i kontakt med ett protein i de röda blodkropparna som heter hemoglobin. Hemoglobinet fungerar som en ”syretaxi” som hämtar syret i lungorna och lämnar av det ute i kroppen där det förbrukas. Men hur ”vet” hemoglobinet om det ska plocka upp eller lämna av syret?
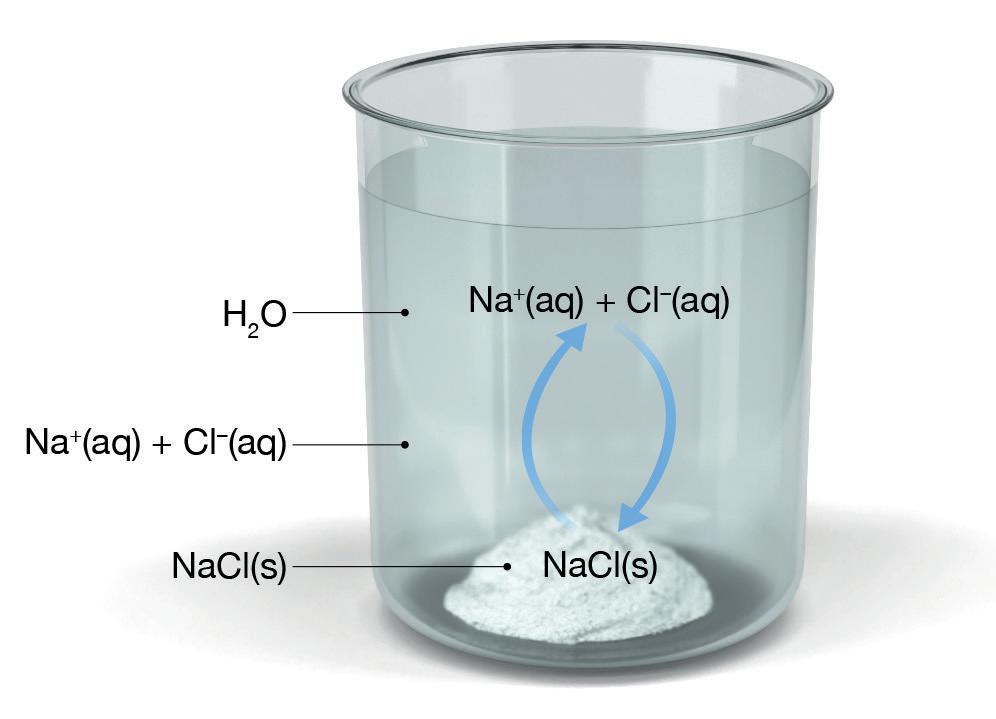
I bägaren med en mättad saltlösning uppstår det en jämvikt mellan det fasta saltet och jonerna i lösningen.
Reaktioner kan gå åt båda hållen
De allra flesta reaktioner som vi studerade i kemi nivå 1 gick fullständigt åt höger. Det betyder att alla reaktanter omvandlades till produkter tills reaktanterna helt enkelt tog slut, och det inte kunde bildas mer produkter.
Så är det ofta med till exempel förbränningar. När vi sätter fyr på bunsenbrännaren eldar vi upp propangas C��H8 som får reagera med luftens syre och bilda koldioxid och vatten enligt nedanstående reaktionsformel:
C��H8 + 5O2 ��CO2 + ��H2O
I reaktionen omvandlas allt propan till koldioxid och vatten. I många reaktioner, framför allt i biologiska system, går dock inte reaktionen bara åt höger, som i förbränningen ovan, utan samtidigt även åt motsatt håll, det vill säga åt vänster. Sådana reaktioner kallas för jämviktsreaktioner.
Vi kan titta på hur det ser ut i en mättad saltlösning. En mättad saltlösning är en lösning med så hög saltkoncentration att det inte går att lösa mer salt i den. Det betyder att om man tillsätter mera fast salt till lösningen, så kommer det bara att lägga sig i en hög på botten av bägaren.
Med blotta ögat ser det ut som att det inte händer något med saltet i bägaren, men på nano-nivå gör det faktiskt det! Ett litet antal natrium- och kloridjoner kan nämligen frigöra sig från den fasta fasen och gå ut i lösningen. Det kan vi skriva på det här sättet:
NaCl(s) Na+(aq) + Cl–(aq)
Exakt lika fort som det bildas natrium- och kloridjoner i vattenlösning kommer dock andra natrium- och kloridjoner att gå samman och bilda fast natriumklorid igen. Det sker enligt den här reaktionen:
Na+(aq) + Cl–(aq) NaCl(s)
Båda de här reaktionerna sker exakt lika fort. Det betyder att de balanserar varandra, och systemet är i jämvikt (dynamisk jämvikt).
Vi kan skriva det i en jämviktreaktion med en dubbelharpun ”⇌” som visar att reaktionen går åt både höger och vänster:
NaCl(s) ⇌ Na+(aq) + Cl–(aq)
Vad händer när en reaktion når jämvikt?
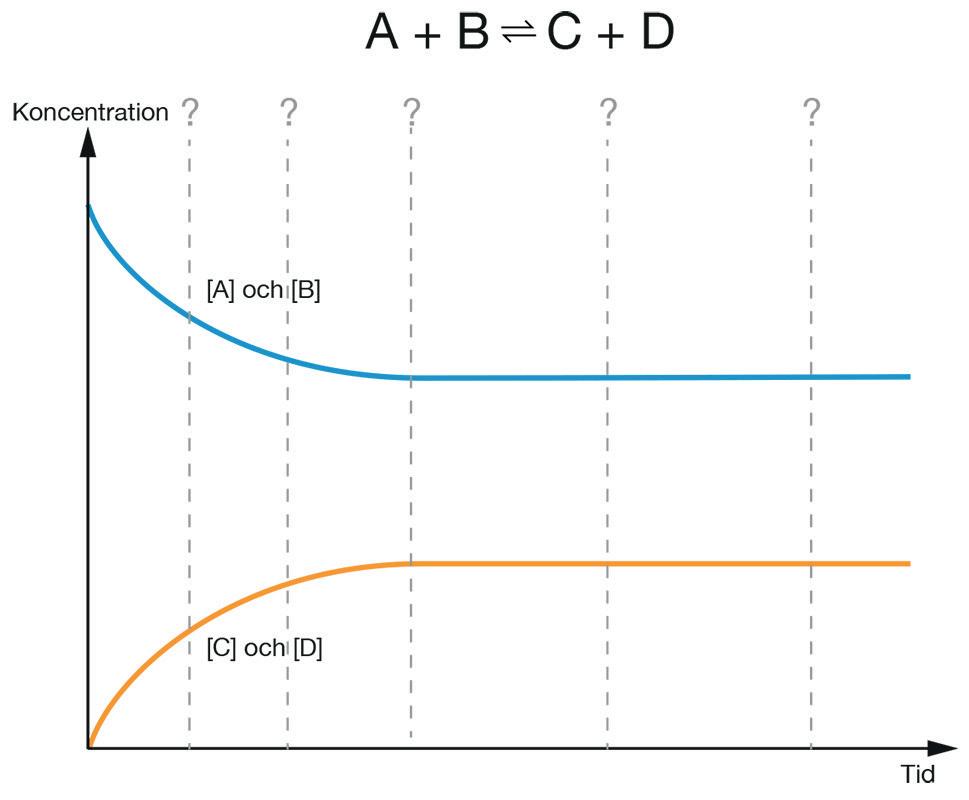
För att förklara vad som händer när en reaktion når jämvikt ska vi titta på en tänkt reaktion, där två ämnen som vi kallar för A och B får reagera med varandra och bilda C och D. Det sker enligt följande reaktionsformel: A + B ⇌ C + D
Om vi börjar med att blanda samman A med B, så kommer de ursprungliga koncentrationerna [A] och [B] att vara ganska höga. Koncentrationerna [C] och [D] kommer dock att vara lika med noll. Därför kommer reaktionshastigheten åt höger till en början att vara ganska stor, medan reaktionshastigheten åt vänster är noll.
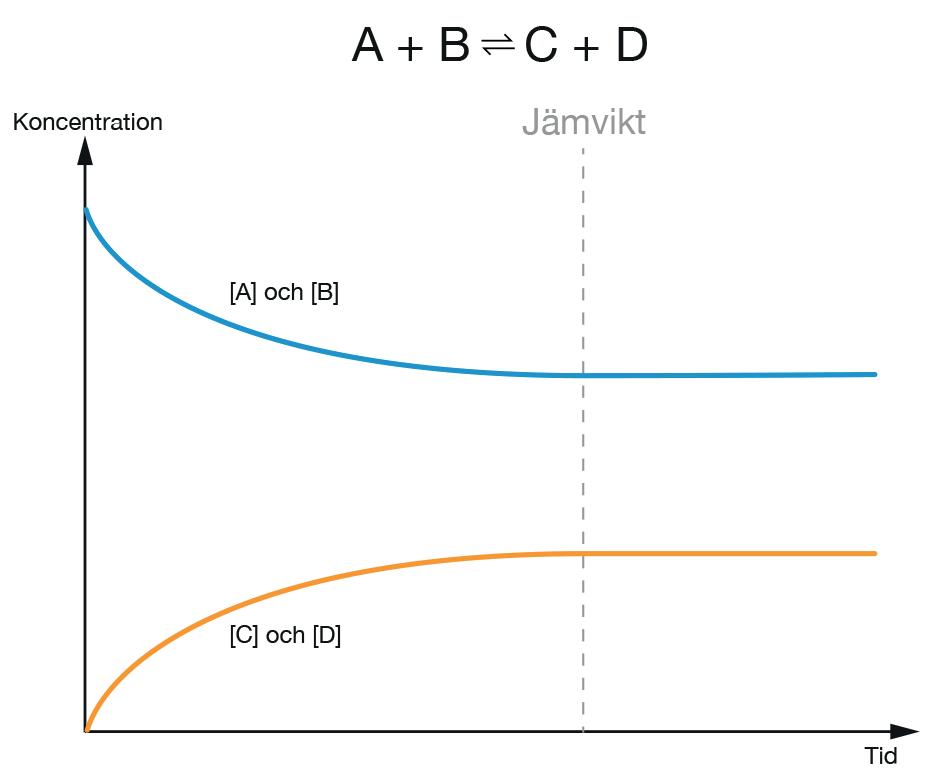
Två ämnen, A och B, får reagera med varandra och bilda C och D. Efter en tid förändras inte koncentrationerna [A], [B], [C] eller [D] mer. Det är för att reaktionen åt höger då går exakt lika fort som reaktionen åt vänster. Då är systemet i jämvikt.
I och med att det bildas C och D i reaktionen, så sjunker koncentrationerna [A] och [B]. Eftersom koncentrationen är en av de saker som bestämmer reaktionshastigheten, betyder det också att reaktionshastigheten åt höger minskar.
Men i och med att det bildas just C och D i reaktionen, och koncentrationerna [C] och [D] ökar, så betyder det också att reaktionen åt vänster sätter igång och ökar i hastighet. Från och med ett visst tillfälle är reaktionshastigheten åt höger exakt lika hög som reaktionshastigheten åt vänster. Då är systemet i jämvikt, ett jämviktsläge har uppnåtts, och koncentrationerna [A], [B], [C] och [D] ändras inte mer.
Ett annat sätt att betrakta jämvikten är ur Gibbs fria energi ΔG. Du har tidigare fått lära dig att när ΔG < 0 är reaktionen åt höger spontan, och när ΔG > 0 är reaktionen åt höger icke-spontan. När en jämviktsreaktion uppnår jämvikt blir ΔG = 0, vilket innebär att reaktionerna åt höger och vänster balanserar varandra, så att varken reaktanternas eller produkternas koncentrationer förändras något mer.
Jämviktskonstanten
Eftersom koncentrationerna [A], [B], [C] och [D] i vår tänkta reaktion ovan inte ändras mer när systemet har uppnått jämvikt, kan man säga att de är konstanta. Det betyder att förhållandet mellan produkternas och reaktanternas koncentration också är konstant, något som man kan uttrycka matematiskt: K = [][] [][] CD AB eller förenklat K = [] [] produkter reaktanter
Sambandet kallas för jämviktsekvationen (eller ibland massverkans lag eller Guldberg–Waages lag) och K kallas för jämviktskonstanten. Det enda som påverkar värdet på jämviktskonstanten K för en viss reaktion är temperaturen. Varken vilka koncentrationer man har från början eller om det finns med någon katalysator påverkar jämviktskonstantens värde, utan endast temperaturen. Vad det betyder ska vi titta närmare på i de kommande avsnitten.
ÖVNINGSUPPGIFTER
Öva begreppen
22. En viss reaktion har nått jämvikt. Vilket eller vilka av påståendena nedan är korrekta?
a. Koncentrationerna på produkter och reaktanter är lika stora.
b. Koncentrationerna på produkter och reaktanter ändras inte mer.
c. Reaktionshastigheterna ändras inte mer.
d. Temperaturen sjunker.
e. Temperaturen ökar.
f. Ingenting händer mer när reaktionen har nått jämvikt.
Öva förståelsen
23. Hur kan man avgöra att följande reaktioner har uppnått jämvikt?
a. H2(g) + I2(g)⇌ 2HI(g) färglös violett färglös
b. Fast socker + vatten ⇌ sockerlösning
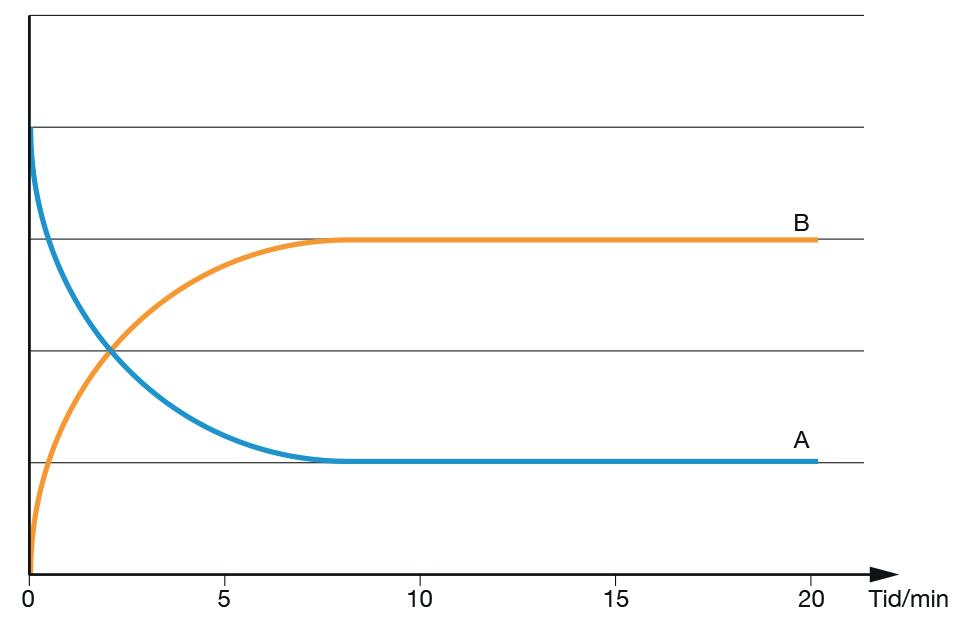
24. I ett försök mätte man hur ämnet A övergick till ämnet B för att till slut nå följande jämvikt:
A ⇌ B
Koncentrationerna [A] och [B] sattes av mot tiden i nedanstående diagram.
a. Vid vilken tidpunkt uppnådde reaktionen jämvikt?
b. Är värdet på jämviktskonstanten K större än, lika med eller mindre än 1?
25. Titta på nedanstående jämviktskonstanter. Ange för var och en om koncentrationen produkter är större än, mindre än eller lika stor som koncentrationen reaktanter vid jämvikt.
a. K = 1,5 · 10–5
b. K = 5,1 · 108
c. K = 0,000048
Analysera och diskutera
• Ordet ”jämvikt” kan också användas i vardagliga sammanhang, och inte bara i kemiska.
Vad skulle du säga är skillnaden mellan ”vardaglig” jämvikt och kemisk jämvikt?
A7. Beräkningar på jämviktssystem
I alla beräkningar som du har gjort i kemi nivå 1 har du fått lära dig att vara noggrann med storhet, mätetal och enhet. Alla konstanter, inklusive jämviktskonstanten K bär också på en enhet. Men som du ska få se har jämviktskonstanten inte alltid samma enhet. Hur kan det vara så?

Jämviktskonstantens enhet
När kväve N2 reagerar med vätgas H2 bildas ammoniak NH�� enligt följande reaktionsformel:
N2 + ��H2 ⇌ 2NH��
Reaktionen är en jämvikt, och kanske en av världens viktigaste industriella processer. Det är nämligen så att den ammoniak som bildas används till att göra konstgödsel, och är alltså en reaktion som ger oss mat på bordet! Processen kallas för Haber–Boschprocessen efter sina uppfinnare Fritz Haber och Carl Bosch. För sin metod för framställning av ammoniak fick de 1918 års nobelpris i kemi. Vi ska nu använda Haber–Bosch-processen för att studera vilka typer av beräkningar man kan utföra på kemiska jämvikter. Vi börjar med att teckna jämviktskonstanten för reaktionen.
I reaktionen reagerar en kvävemolekyl med tre vätemolekyler för att bilda två ammoniakmolekyler. Vi kan (lite omständligt) skriva det på det här sättet:
N2 + H2 + H2 + H2 ⇌ NH�� + NH��
När vi tecknar jämviktskonstanten för reaktionen tar vi koncentrationerna av produkterna delat med koncentrationerna av reaktanterna. Då får vi följande uttryck:

Haber–Bosch-processen används för att framställa ammoniak som finns i konstgödsel. Utan konstgödsel hade vi inte kunnat odla mat i den skala vi gör idag.
Lägg alltså märke till att koefficienterna i reaktionsformeln
N2 + ��H2 ⇌ 2NH�� blir till potenser i uttrycket för jämviktskonstanten K. Vi kan då också titta på vad enheten för jämviktsekvationen blir. Enheten för koncentration är mol/dm��, något som man också kan förenkla och bara skriva M (molar). Vi gör det nu, och ersätter storheterna i jämviktskonstanten för Haber–Bosch-processen med endast enheten M. Vi får då följande uttryck: MM MMMM M M M · == 2 4 2
För just Haber–Bosch-processen, med reaktionsformeln
N2 + ��H2 ⇌ 2NH��, får alltså jämviktskonstanten K enheten M−2.
EXEMPEL 7
Teckna jämviktskonstanten för nedanstående jämviktsreaktion och ange vilken enhet jämviktskonstanten K får.
H2 + I2 ⇌ 2HI
Lösning
K = [] [][] HI HI 2 2 2
Jämviktskonstantens enhet beräknas:
M MM 2 · = 1
I det här fallet blir alltså jämviktskonstanten K enhetslös!
Clara Immerwahr: Vetenskapens samvete i skuggan av kriget
Clara Immerwahr var en pionjär och en kvinna djupt trogen sina ideal. År 1900 blev hon den första kvinnan i Tyskland att erhålla en doktorstitel i kemi, en enastående prestation i en tid då kvinnor sällan tilläts högre utbildning. Hennes passion var kemins potential att förbättra människors liv. Hon var en övertygad pacifist och ansåg att vetenskapen endast skulle tjäna fredliga och konstruktiva syften.

Året därpå gifte hon sig med Fritz Haber, en av tidens mest framstående kemister. Deras äktenskap kom att symbolisera en av vetenskapshistoriens djupaste moraliska konflikter. Haber fick nobelpriset för Haber–Bosch-processen, som katalyserar reaktionen N2(g) + 3H2(g)⇌ 2NH3(g). Men samma katalytiska process gör det även möjligt att framställa sprängämnen på industriell skala.
När första världskriget bröt ut ställde Haber sin expertis till den tyska krigsmaktens tjänst. Han blev arkitekten bakom Tysklands program för kemisk krigföring och ledde personligen den första storskaliga klorgasattacken vid Ypres 1915. För Clara var detta ett oerhört svek mot vetenskapens sanna syfte. Hon såg sin makes arbete som en ”perversion av vetenskapen” och vädjade till honom att sluta, men förgäves.
Konfrontationen mellan hennes pacifistiska ideal och hans militära ambitioner blev total. Några dagar efter en middag där Haber firade sin ”framgång” vid fronten, tog Clara Immerwahr sitt liv med hans tjänstepistol. Hennes död står som en tragisk protest och en evig påminnelse om det personliga ansvar som följer med vetenskaplig kunskap.
kemins historia
Clara Immerwahr.
Jämviktskonstanten kan användas för att beräkna hur mycket produkter som bildas i en viss reaktion, eller hur mycket reaktanter som är kvar när jämvikten har ställt in sig. Vi börjar dock med att titta på hur man beräknar jämviktskonstanten för några olika jämviktsreaktioner.
EXEMPEL 8
Fosgen, COCl2, är en otrevlig gas som användes som stridsgas under första världskriget. Den framställs genom att man låter kolmonoxid reagera med klorgas enligt följande jämviktsreaktion:
CO(g) + Cl2(g)⇌ COCl2(g)
I en behållare på 10 dm3 hade man vid jämvikt 0,28 mol CO, 0,21 mol Cl2 och 0,81 mol COCl2. Använd detta för att beräkna värdet på jämviktskonstanten K
Lösning
Vi börjar med att teckna jämviktskonstanten:
K = [] [][] COCl COCl 2 2
Därefter utnyttjar vi sambandet c = n V för att beräkna jämviktskoncentrationerna:
[CO]mol dm = 028 10 3 , = 0,028 mol/dm3 = 0,028 M
[], Clmol dm 2 3 021 10 = = 0,021 mol/dm3 = 0,021 M
[], COClmol dm 2 3 081 10 = = 0,081 mol/dm3 = 0,081 M
Med hjälp av koncentrationerna kan vi nu beräkna jämviktskonstanten:
K = 0 081 0 028 0 021 , , , M MM · = 137,755102 M–1≈1,4 · 10 2 M–1
Man kan också använda stökiometriska resonemang (som vi gjorde i kemi nivå 1) för att beräkna jämviktskonstanten. Vi betraktar sönderdelningen av svaveltrioxid, SO��, till svaveldioxid och syrgas för att undersöka det.
EXEMPEL 9
Svaveltrioxid sönderfaller spontant till svaveldioxid och syrgas enligt följande jämvikt:
2SO3(g) ⇌ 2SO2(g) + O2(g)
I ett experiment fyllde man en behållare på 50 dm3 med 1,0 mol svaveltrioxid. Vid jämvikt hade det bildats 0,58 mol svaveldioxid. Beräkna jämviktskonstanten K!
Lösning
För att kunna lösa uppgiften måste vi ta reda på hur stor substansmängd syrgas som har bildats, och hur stor substansmängd svaveltrioxid som är kvar. Det gör vi enklast genom att ställa upp en tabell med de ämnen som ingår i reaktionen. I översta raden vid 1 skriver vi in vilka substansmängder vi hade vid starten, nstart
⇌
cjämvikt
8
042 50 , = 0,0084
Nu vet vi från uppgiften att det vid jämvikt fanns 0,58 mol SO2 i reaktionskärlet. Det fyller vi i vid 2 . Då vet vi också att substansmängden SO2 ökade med +0,58 mol under reaktionen 3
I reaktionsformeln ser vi att n n SOO 2 2 2 1 :: = . Det betyder att samtidigt som substansmängden SO2 ökar med 0,58 mol, kommer substansmängden O2 att öka med 0,29 mol 4 . Det betyder att substansmängden O2 vid jämvikt 5 kommer att vara 0,29 mol.
I reaktionsformeln ser vi också att n n SOSO 3 2 11:: = . Det betyder att det gick åt 0,58 mol SO3 i reaktionen 6 . Det betyder att vid jämvikt fanns det kvar (1,0 − 0,58)mol = 0,42 mol svaveltrioxid 7 .
Alla dessa substansmängder måste delas med 50 dm3 för att vi ska få koncentrationerna, som vi sedan kan använda för att beräkna jämviktskonstanten. Vi skriver in koncentrationerna i raden vid 8
Nu ställer vi upp uttrycket för jämviktskonstanten K, och beräknar den med hjälp av koncentrationerna vi fick fram i tabellen:
K == [][] [] (,), () SOO SO MM 0,0084 M
2 2 2 2 2 2 2 0 0116 0 0058 · = 0,011060771 M ≈ 0,011 M
Nu kan vi också titta på ett exempel där vi vet vad jämviktskonstanten för en viss reaktion är. Det ska vi använda för att beräkna hur mycket det är kvar av reaktanterna när reaktionen har uppnått jämvikt.
EXEMPEL 10
Kolmonoxid och vatten reagerar med varandra och bildar koldioxid och vätgas enligt följande jämviktsreaktion:
CO(g) + H2O(g) ⇌ CO2(g) + H2(g)
I ett visst experiment mätte man upp följande koncentrationer vid jämvikt: [CO2] = 0,060 M, [H2] = 0,090 M och [H2O] = 0,030 M. Vid temperaturen som rådde vid experimentet var jämviktskonstanten
K = 5,0. Hur stor var halten kolmonoxid?
Lösning
Vi börjar med att teckna jämviktskonstanten för reaktionen:
K = [][] [] [] COH COHO 2 2 2
Eftersom vi inte känner [CO] kan vi kalla den x. Vi skriver in de övriga värden som vi känner i uppgiften, och löser ut x.
50 0 060 0 090 0 030 , ,, , = MM M x · ·
x = 0 060 0 090 0 030 ,, , MM M · 5 0 , = 0,036 M
Svar: Vid jämvikt var [CO] = 0,036 M.

Fällningar av från vänster silverklorid
AgCl(s), silverbromid AgBr(s) och silverjodid AgI(s). Lägg märke till att de har lite olika färg; silverjodiden längst till höger är gulaktig medan silverkloriden är helt vit.
Mättade lösningar blir heterogena jämvikter
I kemi nivå 1 tittade vi på några klassiska fällningsreaktioner. En sådan är där silverjoner reagerar med kloridjoner och bildar en fällning av fast silverklorid, AgCl(s). Faktum är att silverjoner bildar fällningar även med bromidjoner och jodidjoner, och alltså bildar fast silverbromid AgBr(s) och fast silverjodid AgI(s).
Även om silverjodid, silverbromid och silverklorid är mycket svårlösliga, så kommer det alltid att finnas små mängder lösta joner i vattnet. Det beror på att det uppstår en jämvikt mellan den fasta jonföreningen och de lösta jonerna. Eftersom jonerna befinner sig i olika faser – fast och löst i vatten – kallas denna typ av jämvikt för en heterogen jämvikt.
När en fällning av silverklorid bildas, inställer sig följande jämvikt:
AgCl(s) ⇌ Ag+(aq) + Cl (aq)
För denna jämvikt kan vi ställa upp en jämviktsekvation, precis som för alla andra jämvikter. Den ser ut så här:
K = [+–()][()] [] AgaqClaq AgCl(s)
Den fasta silverkloriden är dock lite speciell. Eftersom den består av ett rent, fast ämne, ändras dess koncentration inte alls när lite av Ag+- och Cl -jonerna går ut i lösning. Eftersom den är konstant, kan den bakas samman med K, och vi får istället en konstant som kallas för löslighetsprodukt, Ks. Vi tecknar löslighetsprodukten för silverklorid så här:
Ks, AgCl = [Ag+(aq)][Cl-(aq)]
EXEMPEL 11
Löslighetsprodukten för fast silverklorid i vatten är Ks, AgCl = 1,77 · 10–10 M2. Beräkna [Ag+] i en mättad lösning av AgCl.
Lösning
I den mättade lösningen av AgCl ställer följande jämvikt in sig:
AgCl(s) ⇌ Ag+(aq) + Cl–(aq)
Vi tecknar löslighetsprodukten för silverklorid:
Ks, AgCl = [Ag+(aq)][Cl–(aq)]
I reaktionsformeln kan vi se att nAg+:nCl– =1:1. Därför kommer [Cl (aq)] och [Ag+(aq)] att vara lika stora, och vi kan skriva så här:
[Cl (aq)] = [Ag+(aq)]
Ks, AgCl = [Ag+(aq)]2
Vi drar roten ur båda sidor och får att
[()] Agaqs,AgCl + K
Eftersom det är orimligt med en negativ koncentration kan vi bortse från den och beräkna [Ag+(aq)]: [ ( Ag)],+aqM = 1 7710 10 2 · – =1,3304134
EXEMPEL 12
Man kan lösa upp till maximalt 358,9 g natriumklorid i vatten med temperaturen 20 °C. Beräkna löslighetsprodukten för natriumklorid vid 20 °C.
Lösning
I en mättad lösning av natriumklorid ställer följande jämvikt in sig: NaCl(s) ⇌ Na+(aq) + Cl–(aq)
Vi tecknar också löslighetsprodukten för natriumklorid:
Ks, NaCl = [Na+(aq)][Cl–(aq)]
I reaktionsformeln kan vi se att nNaCI:nNa+: nCI– = 1:1:1. Därför kan vi konstatera att i lösningen kommer [Na+] = [Cl–] = cNaCl. För att beräkna cNaCl måste vi först beräkna nNaCl:
n m M NaCl NaCl NaCl g g/mol =mol = + = 358 9 22 99 35 45 6 14134155 , (,,),
c n V NaCl NaClmol dm mol/ ==dm = 6 14134155 1 6 14134155 3 3 , ,
Eftersom [Na+] = [Cl–] = cNaCl kan vi nu beräkna löslighetsprodukten:
Ks, NaCl = 6,14134155 M · 6,14134155 M = 37,7160759955 M2 ≈ 37,7 M2
ÖVNINGSUPPGIFTER
Öva begreppen
26. Teckna jämviktskonstanten K för nedanstående reaktioner, och ange vilken enhet den får. a. PCl5 ⇌ PCl3 + Cl2 b. 2CO + O2 ⇌ 2CO2 c. 4NH3 + 3O2 ⇌ 2N2 + 6H2O
27. Skriv jämviktsreaktionen för de reaktioner som ger upphov till följande jämviktskonstanter:
a. K = [][] [][] HOCO HCO 2 2 2 b. K = [] [] O O 3 2 2 3 c. K = [][] [][] PHF HFPF 3 2 3 3 3
Öva förståelsen
28. I ett experiment förde man in BrCl(g) i en lufttät behållare och lät följande jämvikt ställa in sig vid 25 °C:
2BrCl(g) ⇌ Br2(g)+ Cl2(g)
Man uppmätte då följande koncentrationer: [BrCl] = 0,22 M; [Br2] = 0,15 M; [Cl2] = 0,15 M.
Beräkna jämviktskonstanten K.
29. Löslighetsprodukten för magnesiumhydroxid Mg(OH)2 är 5,6 · 10–12 M3 vid 25 °C. Är magnesiumhydroxid en svårlöslig eller lättlöslig förening?
30. I ett experiment förde man in lite kvävedioxid NO2 i en lufttät behållare. Man hettade upp behållaren till 100 °C, då följande jämvikt ställde in sig:
2NO2(g) ⇌ N2O4(g)
Man mätte då koncentrationen [N2O4] och fann att den var 0,040 M. För den här reaktionen är jämviktskonstanten K = 2,8 M–1 vid 100 °C. Beräkna koncentrationen [NO2] vid jämvikt.
31. För Haber-Bosch-processen, N2(g) + 3H2(g)⇌ 2NH3(g), fann man vid jämvikt i en behållare att [N2] = 0,5M, [H2] = 1,0 M och [NH3] = 0,5 M vid en viss temperatur. Beräkna värdet på jämviktskonstanten K vid denna temperatur.
32. För silverklorid är löslighetsprodukten i vatten Ks, AgCl = 1,77 · 10−10 M2 vid 25 °C. Beräkna hur stor massa silverklorid som maximalt kan lösas i 1,0 dm3 vatten vid denna temperatur.
Analysera och diskutera
• En jämviktsreaktion, till exempel A + B ⇌ C + D kan lika gärna skrivas ”tvärtom”, det vill säga C + D A + B. Vad får detta för betydelse för jämviktskonstanten K, och varför tror du att man väljer att skriva en jämviktsreaktion på ena eller andra hållet?
A8. Koncentrationskvoten Q
Många jämvikter ställer in sig mycket fort, nästan omedelbart när reaktanterna blandas. Andra jämvikter skulle ta mycket lång tid på sig för att nå jämvikt (om de inte skyndas på av någon katalysator). Hur kan man då veta om en reaktion uppnått jämvikt eller inte?

Om man mäter reaktanternas och produkternas koncentrationer i reaktionen A + B ⇌ C + D vid olika tidpunkter, hur vet man när jämviktsläget har uppnåtts?
Hur man tar reda på om ett system är i jämvikt
För att ta reda på om ett system har uppnått jämvikt eller inte kan man göra mätningar av reaktanternas och produkternas koncentrationer under tiden som jämvikten ställer in sig. Med hjälp av mätningarna kan man beräkna en koncentrationskvot Q och jämföra den med jämviktskonstanten K.
För att kunna jämföra koncentrationskvoten Q med jämviktskonstanten K måste vi beräkna dem på exakt samma sätt. För reaktionen A + B C + D tecknas därför koncentrationskvoten Q så här: Q = [][] [][] CD AB
Om Q = K vet vi att systemet är i jämvikt. Men i vilken riktning håller reaktionen på att gå för att uppnå jämvikt? Kommer den att gå åt höger (så att det bildas mer av produkterna) eller kommer den att gå åt vänster (så att det bildas mer av reaktanterna)? Vi vet inte än, men tar ett exempel för att förklara.
EXEMPEL 13
Vid 425 °C är jämviktskonstanten K = 54 för reaktionen H2(g) + I2(g)⇌ 2HI(g). Vid ett visst tillfälle är koncentrationerna på alla ingående ämnen 1 · 10−3 M.
a. Är systemet i jämvikt?
b. Om systemet inte är i jämvikt, vilket håll kommer reaktionen att gå åt?
Lösning
a. För att ta reda på om systemet är i jämvikt beräknar vi koncentrationskvoten Q och jämför med jämviktskonstanten K.
Q = [] [][] HI HI 2 2 2
Vi sätter in koncentrationerna i uttrycket för Q och beräknar koncentrationskvoten:
Q = –––() 110 110 1 10 3 2 3 3 M MM · · · · = 1
Vi kan se att Q < K eftersom 1 < 54. Eftersom Q ≠ K är systemet inte i jämvikt än.
b. För att systemet ska nå jämvikt måste Q öka tills det är lika stort som K. Q kan bara öka om täljaren ökar, samtidigt som nämnaren minskar. Det betyder i det här fallet att koncentrationen av produkten, det vill säga [HI], måste öka, samtidigt som koncentrationen av reaktanterna, det vill säga [H2] och [I2], minskar.
Q = ↑ ↓ [] [][] HI HI 2 2 2
Om koncentrationen av produkterna ökar samtidigt som koncentrationen av reaktanterna minskar, betyder det att reaktionen H2(g) + I2(g)⇌ 2HI(g) går åt höger ända tills jämviktsläget har uppnåtts.
Vi kan nu sammanfatta vad som gäller för koncentrationskvoten
Q och jämviktskonstanten K.
• Om Q = K har systemet uppnått jämvikt, och koncentrationerna ändras inte mer.
• Om Q < K är systemet inte i jämvikt, och kommer att gå åt höger ända tills jämviktsläget har uppnåtts.
• Om Q > K är systemet inte i jämvikt, och kommer att gå åt vänster ända tills jämviktsläget har uppnåtts.
ÖVNINGSUPPGIFTER
Öva begreppen
33. Beräkna koncentrationskvoten Q för vart och ett av nedanstående reaktionssystem, och avgör om systemet är i jämvikt, går åt höger eller går åt vänster.
a. N2(g) + O2(g) ⇌ 2NO(g)
[N2] = 0,92 M [O2] = 0,86 M [NO] = 0,041M
K = 0,0025 (vid 2130 °C)
b. 2HF(g) ⇌ H2(g) + F2(g)
[HF] = 12 M [H2] = 0,43 M [F2] = 0,27 M
K = 1,0 · 10−13 (vid 1000 °C)
c. 2SO2(g) + O2(g) ⇌ 2SO3(g)
[SO2] = 0,344 M [O2] = 0,172 M [SO3] = 0,056 M
K = 0,15 M–1 (vid 1 227 °C)
Öva förståelsen
34. Förklara med egna ord vad skillnaden mellan koncentrationskvoten Q och jämviktskonstanten K är.
35. Vid 450 °C är jämviktskonstanten K = 50 för nedanstående jämvikt
H2(g) + I2(g)⇌ 2HI(g)
I ett experiment blandar man 1,01 g H2, 127 g I2 och 512 g HI i en 5,0-liters behållare vid 450 °C. Är reaktionen i jämvikt? Motivera med beräkning.
36. Om man upphettar fast kol tillsammans med vattenånga ställer följande heterogena jämvikt in sig: C(s) + H2O(g) ⇌ CO(g) + H2(g)
I ett experiment upphettade man kol och vattenånga i en 2,0-liters behållare till 900 K och mätte att det fanns 6,0 g kol, 3,6 g vattenånga, 2,8 g kolmonoxid och 0,10 g vätgas.
Vid denna temperatur är reaktionens jämviktskonstant K = 0,11 M. Hade systemet nått jämvikt?
Om inte, åt vilket håll gick reaktionen?
Analysera och diskutera
• I början av kapitlet påstods att förbränningar ofta går helt åt höger, och omvandlas helt till produkter. Finns det några förbränningar som inte går helt åt höger, utan istället är jämvikter?
Vad skulle det kunna vara i så fall?
A9. När koncentrationen rubbas
När ett system nått jämvikt förändras inte dess koncentrationer längre, utan de är konstanta över tid. Men låt oss säga att vi rubbar jämvikten genom att föra in mer av någon reaktant. Vad händer då med den reaktantens koncentration, och vad händer med hela jämviktssystemet?

Vätejodidjämvikten
I exempel 1�� var systemet H2(g) + I2(g) ⇌ 2HI(g) inte i jämvikt, så reaktionen gick åt höger. Nu ska vi beräkna vad koncentrationerna blir när jämvikt uppnås.
EXEMPEL 14
Vid 425 °C är jämviktskonstanten K = 54 för reaktionen H2(g) + I2(g)⇌ 2HI(g). I ett experiment förde man in 0,100 mol H2 och 0,100 mol I2 i ett kärl på 1,00 dm3, och höjde temperaturen till 425 °C. Vilka blev koncentrationerna [H2], [I2] och [HI] vid jämvikt?
Lösning
Vi behöver jämviktskonstanten K för att beräkna de olika jämviktskoncentrationerna.
K = [] [][] HI HI 2 22
En tabell hjälper oss att hålla redan på vilka koncentrationer vi har vid reaktionens början, hur de ändras och vilka det är vid jämvikt. Vid 1 fyller vi i koncentrationerna vid start.
[H2] [I2] [HI]
nstart 1 0,100 0,100 0 M
ändring 2 –x 3 –x 4 +2x M
cjämvikt 5 0,100
Vid reaktionen kommer det att gå åt en okänd mängd vätgas och jodgas. Vi kan därför skriva att koncentrationerna [H2] och [I2] minskar med x M vid 2 och 3 . Reaktionsformeln visar att n n n HIHI 2 2 :: =1:1:2. Därför ökar koncentrationen [HI] med 2x, vilket vi skriver in vid 4 . Nu kan vi summera varje kolumn i tabellen, och skriver in alla jämviktskoncentrationerna i raden vid 5 . Vi sätter in jämviktskoncentrationerna i uttrycket för K och beräknar x. När vi känner x kan vi sedan beräkna alla jämviktskoncentrationerna.
54 2 0 100 0 100 2 0 100 22 2 = ––= –() (, )(,) () (, ) x xx x x
Vi kan dra roten ur båda leden (vi kan bortse från rötternas negativa lösningar, eftersom det skulle ge ett orimligt resultat) och lösa ut x.
54 2 0 100 2 0 100 2 2 = –= –() (, ), x x x x vilket ger x = 0,0786061
Nu kan vi beräkna koncentrationerna vid jämvikt:
[H2] = [I₂] = (0,100 – x) M = (0,1 – 0,0786061) M = 0,0213939 M ≈ 0,0214 M [HI] = 2x M = 2 · 0,0786061 M = 0,1572122 M ≈ 0,157 M
Vi kan visa vad som händer när jämvikten i föregående exempel ställer in sig med hjälp av ett diagram. I diagrammet sätter vi ut koncentrationerna [H2] och [I2] tillsammans med koncentrationen [HI]. Efter att jämvikten väl har uppnåtts kan den rubbas igen genom att man tillsätter mer eller tar bort av något ämne som ingår i reaktionen. I jämvikten H2(g) + I2(g) ⇌ 2HI(g) kan vi alltså rubba jämvikten genom att ta bort eller sätta till mer vätgas, jodgas eller vätejodidgas. Vi ska nu studera hur man tar reda på vad som händer med jämvikten då.
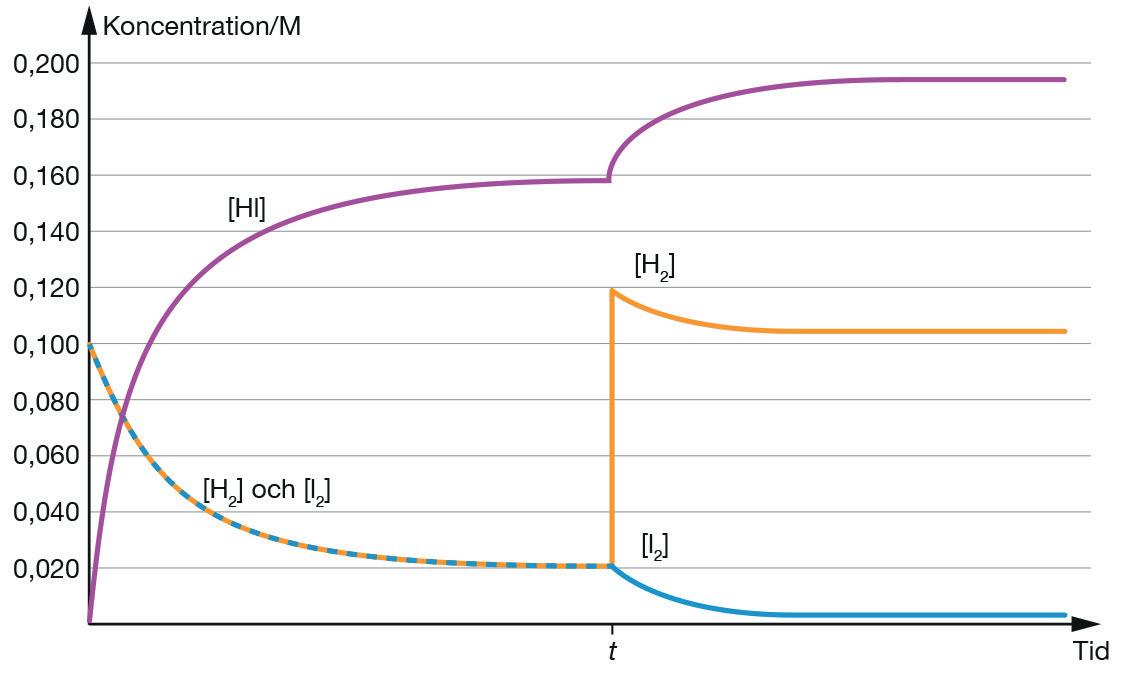
Koncentrationerna [HI], [H2] och [I2] förändras tills de når jämvikt. Vid tiden t rubbas jämvikten genom att ytterligare vätgas tillsätts. Koncentrationen vätgas ökas med 0,100 M till 0,1214 M. Då börjar jämvikten H2(g) + I2(g) gå åt höger igen, ända tills ett nytt jämviktsläge uppnåtts.
EXEMPEL 15
I ett experiment med jämvikten H2(g) + I2(g)⇌ 2HI(g) hade man följande jämviktskoncentrationer: [H2] = [I2] = 0,0214 M och [HI] = 0,157 M. Jämviktskonstanten för reaktionen var K = 54. Man rubbade jämvikten genom att tillsätta extra vätgas, så att koncentrationen [H2] ökade till 0,1214 M.
a. Är systemet fortfarande i jämvikt?
b. Om systemet inte längre är i jämvikt, vilket håll kommer reaktionen att gå åt?
Lösning
a. För att ta reda på om systemet är i jämvikt eller inte, måste vi beräkna koncentrationskvoten Q och jämföra den med jämviktskonstanten K.
Q == [] [][] (, , HI HI M) M 0,0214 M 2 2 2 2 0 157 0 1214 · = 9,48782891 ≈ 9,5
Q ≠ K. Systemet är inte i jämvikt.
b. Eftersom K = 54 och Q = 9,5 kan vi konstatera att Q < K, och att reaktionen därför kommer att gå åt höger. För jämvikten H2(g) + I2(g) ⇌ 2HI(g) betyder det att koncentrationerna [H2] och [I2] kommer att minska samtidigt som koncentrationen [HI] kommer att öka ända tills Q = K och systemet återigen är i jämvikt.
Att jämvikten förskjuts åt höger när man tillsätter mer av reaktanterna kan vi även förstå med hjälp av reaktionshastigheter. En av de saker som påverkar reaktionshastigheten är ju koncentrationen. När vi ökar koncentrationen av någon av reaktanterna kommer sannolikheten för kollisioner mellan reaktanterna att öka, och då ökar också reaktionshastigheten åt höger, vilket gör att jämviktsläget förskjuts åt höger.
Hur ett jämviktssystem reagerar när det rubbas sammanfattas i en princip som först formulerades av den franske kemisten Henry Louis Le Chatelier (Le Chateliers princip). Den säger att om man gör en förändring av ett jämviktssystem sker en nettoreaktion så att ändringen motverkas.
Det betyder att om man tillsätter mer av någon reaktant till ett jämviktssystem, så kommer reaktionen att gå åt höger, så att reaktanterna minskar i koncentration ända tills jämviktsläget har uppnåtts igen. Man kan också säga att om man istället tillsätter mer produkt till ett system som är i jämvikt, så kommer reaktionen att gå åt vänster, så att koncentrationen av produkterna minskar.
Men ändringarna gäller också om man tar bort någon av reaktanterna eller produkterna. I jämvikten H2(g) + I2(g) 2HI(g) gäller till exempel att om man minskar koncentrationen [HI] (genom att helt enkelt ta bort det), så kommer reaktionen att gå åt höger. Då ökar koncentrationen [HI] igen, samtidigt som koncentrationerna [H2] och [I2] minskar ända tills jämviktstillståndet uppnåtts igen.
Jämviktsreaktioner som är i gasform kan också rubbas om trycket ändras, något vi kommer att titta närmare på i nästa avsnitt.
ÖVNINGSUPPGIFTER
Öva begreppen
37. Vid 2 130 °C är jämviktskonstanten K = 0,0025 för nedanstående reaktion:
N2(g) + O2(g)⇌ 2NO(g)
Vid ett visst tillfälle mätte man att [N2] = 0,810 M, [O2] = 0,750 M och [NO] = 0,0300 M.
a. Visa att systemet inte är i jämvikt.
b. Vilket håller kommer reaktionen att gå åt?
c. Beräkna [N2], [O2] och [NO] när jämvikten åter fått ställa in sig.
38. När syrgas O2 och svaveldioxid SO2 reagerar bildas svaveltrioxid SO3. Då ställer nedanstående jämvikt in sig:
O2(g) + 2SO2(g) ⇌ 2SO3(g)
Använd Le Chateliers princip för att avgöra vad som händer med jämviktsreaktionen om man …
a. tillsätter en katalysator till reaktionsblandningen.
b. ökar [O2] genom att tillsätta mer O2 till reaktionsblandningen.
c. ökar [SO3] genom att tillsätta mer SO3 till reaktionsblandningen.
d. minskar [SO2] genom att avlägsna SO2 från reaktionsblandningen.
e. minskar [O2] genom att låta det reagera med kol, så att det istället bildas koldioxid.
Öva förståelsen
39. Vid 100 °C är jämviktskonstanten K = 0,36 M för nedanstående reaktion:
N2O4(g)⇌ 2NO2(g)
I ett försök förde man in en viss substansmängd dikvävetetraoxid N2O4 i en behållare med volymen
1,0 dm3 och lät jämvikten ställa in sig vid 100 °C. Då kunde man mäta att [N2O4] = 0,040 M.
a. Beräkna [NO2] vid jämvikt.
b. Hur stor substansmängd N2O4 hade man fört in från början?
40. Kobolt(II)joner bildar ett blått färgkomplex med kloridjoner enligt nedanstående jämviktsreaktion:
Co2+(aq) + 4Cl (aq) ⇌ CoCl 4 2 –
rosa färglöst blått
Vad händer med reaktionsblandningens färg när en lösning av natriumklorid NaCl(aq) sätts till reaktionsblandningen?
Analysera och diskutera
• I början av kapitlet påstods att förbränningar ofta går helt åt höger, och omvandlas helt till produkter. Finns det några förbränningar som inte går helt åt höger, utan istället är jämvikter?
Vad skulle det kunna vara i så fall?
A10. Spädning och komprimering
Le Chateliers princip säger oss att om en jämvikt rubbas, så kommer jämviktsreaktionen att gå antingen åt höger eller åt vänster för att kompensera för rubbningen. Men vid en spädning är det både reaktanternas och produkternas koncentrationer som minskas, inte bara den ena. Hur påverkas jämviktssystemet då?

Spädning av järntiocyanatjämvikten
När man blandar vattenlösningar av järn(III)joner Fe ��+ med tiocyanatjoner SCN bildas järntiocyanat FeSCN2+ i en jämvikt som mycket snabbt ställer in sig:
Fe��+ + SCN ⇌ FeSCN2+
För denna reaktion kan vi förstås teckna en jämviktskonstant:
K = + +–[] [][] FeSCN FeSCN 2 2
För att göra det enkelt för oss kan vi anta att koncentrationerna vid jämvikt är så här:
[FeSCN2+] = a
[Fe��+] = b
[SCN ] = c
Vid jämvikt gäller då att jämviktskonstanten K a bc = . Men vad händer om vi späder jämviktsblandningen till dubbla volymen? Då kommer ämnenas koncentrationer att halveras och bli följande:
[] FeSCN22 + = a
[] Fe 3 2 + = b
[]SCN–= c 2
Om vi beräknar koncentrationskvoten Q med de nya koncentrationerna och jämför med jämviktskonstanten K, kan vi se vad som händer vid spädningen.
Q a bc a bc a bc a bc K ====== + +–[]
Eftersom Q a bc =2 och K a bc = kan vi konstatera att Q > K, och jäm-
vikten Fe��+ + SCN FeSCN2+ kommer att gå åt vänster när den späds. I den här jämvikten kan vi konstatera att det är två partiklar till vänster om jämviktspilen (Fe��+ och SCN–) men bara en partikel till höger (FeSCN2+). Vid spädningar är det alltid så att jämvikten förskjuts åt det håll där det är flest partiklar, i det här fallet åt vänster.

Järn(III)tiocyanatlösningar i olika koncentrationer.






















Kvävgas
Vätgas Ammoniak
När en gasblandning komprimeras kommer jämvikten att förskjutas åt det håll där det är lägst antal partiklar. I Haber-Bosch- processen bildas således mer ammoniak när reaktionen får ske under ett högre tryck (gaserna komprimeras).
Komprimering av Haber–Bosch-processen
Ett sätt att öka koncentrationerna om man har en gasblandning är att trycka ihop den. Då ökar också trycket. I Haber–Bosch-processen framställs ammoniak ur kvävgas och vätgas enligt nedanstående jämviktsreaktion:
N2(g) + ��H2(g) ⇌ 2NH��(g)
Jämviktskonstanten K för reaktionen tecknas
För att undersöka vad som händer med jämvikten när vi ökar koncentrationerna gör vi som ovan, vi antar att de olika jämviktskoncentrationerna är a, b och c på det här sättet:
[NH��] = a
[N2] = b
[H2] = c
Vid jämvikt gäller då att
Om gasblandningen komprimeras till halva volymen, kommer samtidigt alla koncentrationer att fördubblas. De nya koncentrationerna kommer då att bli så här:
[NH��] = 2a
[N2] = 2b
[H2] = 2c
Med hjälp av koncentrationskvoten Q kan vi avgöra åt vilket håll reaktionen kommer att förskjutas för att återigen uppnå jämvikt.
Vi ser att Q < K, eftersom Q bara är ¼ så stort som K. Det betyder att reaktionen N2(g) + ��H2(g) ⇌ 2NH��(g) kommer att gå åt höger om den komprimeras. I Haber–Bosch-jämvikten kan vi konstatera att det är fyra partiklar till vänster om jämviktspilen (en N2-molekyl och tre H2-molekyler) men bara två partiklar till höger (två NH��-molekyler).
Vid komprimeringar är det alltid så att jämvikten förskjuts åt det håll där det är lägst antal partiklar, i det här fallet åt höger.
Varför det är bra att kunna kemisk jämvikt om man ska borra tunnlar

Projektet med att bygga en tågtunnel genom Hallandsåsen, som inleddes av Banverket 1992, kantades av stora problem. Målet var att förbättra tågförbindelserna mellan Malmö, Göteborg och Oslo. Tunneln skulle enligt den ursprungliga planen stå klar 1997.
Bygget stötte tidigt på motgångar. En specialinköpt tunnelborrmaskin körde fast efter bara 13 meter på grund av åsens oväntat mjuka berggrund, vilket tvingade fram en övergång till traditionell sprängteknik. Därefter uppstod massiva vattenläckage från sprickor i berget.
För att täta läckorna användes tätningsmedlet Rhoca-Gil, som består av polyakrylamid. Polyakrylamiden tillverkas ur nervgiftet akrylamid enligt nedanstående jämvikt:
Problemet är bara att när en jämvikt späds, så förskjuts den åt sidan med flest partiklar –i det här fallet den giftiga polyakrylamiden, som läckte ut i stora mängder i grundvattnet med död fisk, förlamade kor och förorenat dricksvatten som följd.
Efter stora förseningar och kostnadsökningar kunde tunneln slutligen öppnas för trafik i december 2015, nästan 20 år senare än planerat. Slutnotan blev cirka elva gånger högre än den ursprungliga budgeten. Om den som ansvarade för tätningen med Rhoca-Gil hade kunnat sin kemiska jämvikt hade mycket pengar och lidande sparats!
Bild på tunneln genom Hallandsåsen
ÖVNINGSUPPGIFTER
Öva begreppen
41. Åt vilket håll förskjuts reaktionen om man ökar trycket (till exempel genom att halvera volymen) i nedanstående jämviktsreaktioner?
a. N2(g) + 3H2(g) ⇌ 2NH3(g)
b. 2CO2(g) ⇌ 2CO(g) + O2(g)
c. H2(g) + Cl2(g) ⇌ 2HCl(g)
Öva förståelsen
42. I ett experiment förde man in kolmonoxid och klorgas i en behållare på 1,0 dm3 och upphettade till 600 °C. Då bildades COCl2 enligt följande jämviktsreaktion:
CO(g) + Cl2(g) ⇌ COCl2(g)
Vid jämvikt uppmätte man följande koncentrationer:
[CO] = 0,25 M, [Cl2] = 0,15 M och [COCl2] = 0,54 M.
a. Beräkna jämviktskonstanten K för reaktionen.
b. Man sänkte därefter trycket genom att expandera behållarens volym till 2,0 dm3. Åt vilket håll försköts jämvikten då?
c. Vad blev [CO] efter att man expanderat behållarens volym och en ny jämvikt fått ställa in sig?
Analysera och diskutera
• Vid bygget av tunneln genom Hallandsåsen var det uppenbart att man behövde kunna något om vad som händer när jämvikter späds (eller komprimeras). Läs vidare och se om du kan finna andra tillfällen i vardagen, inom biologin, medicin eller inom kemiindustrin då det är nödvändigt att ha koll på kemisk jämvikt!
A11. När temperaturen förändras
När vi har diskuterat jämvikter hittills har vi hela tiden varit noga med att ange att de sker vid en viss temperatur. Du har också fått lära dig att temperaturen är det enda som påverkar jämviktskonstantens värde för en viss reaktion. Men varför är det på det sättet, och vad händer om man ändrar på temperaturen på ett visst jämviktssystem?

Hur jämviktskonstanten förändras i en exoterm reaktion
Vi tänker oss en exoterm jämvikt där ämnena A och B reagerar och bildar C och D. Eftersom det är en exoterm reaktion avges det energi i form av värme i reaktionen. Vi kan skriva reaktionsformeln så här:
Jämviktskonstanten tecknas: K = [][] [][] CD AB
Om vi skulle öka koncentrationerna [A] eller [B] i den här jämvikten, så säger oss Le Chateliers princip att reaktionen skulle gå åt höger, så att mera C och D skulle bildas. Men det är inte bara koncentrationerna [C] och [D] som skulle öka – även den avgivna energin skulle öka, eftersom den står till höger om jämviktspilen.
Om man istället skulle tillsätta mera C eller D till reaktionsblandningen, skulle reaktionen gå åt vänster så att [A] och [B] ökar, samtidigt som [C] och [D] minskar ända tills jämvikten har uppnåtts igen. Samtidigt skulle dock även den avgivna energin minska, eller rättare sagt, systemet skulle ta upp energi för att kunna gå åt vänster.
Vad skulle då hända om vi upphettar reaktionsblandningen, det vill säga vi tillför energi till den? Enligt Le Chateliers princip kan vi se att reaktionen skulle gå åt vänster, det vill säga koncentrationerna [A] och [B] kommer att öka, samtidigt som koncentrationerna [C] och [D] minskar. Det betyder att vid den nya jämvikten, vid den högre temperaturen, kommer vi att få andra jämviktskoncentrationer än vad vi hade vid den lägre temperaturen.
Om vi tittar på hur man tecknar jämviktskonstanten för reaktionen kan man se vad som händer med jämviktskonstanten K när den nya jämvikten ställer in sig.
Eftersom [C] och [D] minskar samtidigt som [A] och [B] ökar när vi ökar temperaturen i en exoterm jämvikt, kommer värdet på K att minska. På samma sätt kommer värdet på K istället att öka om energi leds bort från systemet, det vill säga temperaturen sänks.
A + B ⇌ C + D + värme
Hur jämviktskonstanten
förändras i en endoterm reaktion
Vi tänker oss en annan reaktion för att visa vad som händer i en endoterm reaktion när värme tillförs eller leds bort. I denna reaktion tillförs värme till reaktanterna E och F, vilket gör att produkterna G och H bildas enligt nedanstående jämviktsreaktion:
E + F + värme ⇌ G + H
Jämviktskonstanten för denna reaktion blir så här:
K =[][] [][] GH EF
Med hjälp av Le Chateliers princip kan vi direkt avgöra vad som händer om vi tillsätter mer värme, det vill säga höjer temperaturen på reaktionsblandningen. Då kommer jämvikten att förskjutas åt höger, så att de nya koncentrationerna [G] och [H] ökar samtidigt som koncentrationerna [E] och [F] minskar. Om vi ritar in ett par pilar i uttrycket för jämviktskonstanten blir det lite lättare att se vad som händer med K:
K = [][] [][] GH EF ↑ ↓
Det betyder alltså att om man ökar temperaturen i en endoterm jämvikt, så kommer produkternas koncentrationer att öka samtidigt som reaktanternas koncentrationer minskar – vilket leder till att värdet på jämviktskonstanten K ökar. Om man istället minskar temperaturen kommer värdet på jämviktskonstanten K att minska.
I det här läget är det ingen idé att du försöker lära dig utantill vad som händer med jämviktskonstantens värde om man tillför eller avlägsnar värme, och om reaktionen är exo- eller endoterm. Försök istället att lära dig att resonera kring vad som händer i de olika typerna av reaktioner med hjälp av Le Chateliers princip. Då lär du dig mycket bättre hur kemiska jämvikter fungerar!


Bilderna visar jämviktsreaktionen
Co(H O) (aq) + 4C lv ä rm (aq) + 6H O CoCl 2 6 2+ –2 4 2–+ e ⇌
I rumstemperatur är blandningen lila. Om vi kyler blandningen blir den röd och om vi värmer den blir den blå.
ÖVNINGSUPPGIFTER
Öva begreppen
43. Bly(II)klorid PbCl2 är en relativt svårlöslig jonförening. I en mättad lösning av bly(II)klorid
ställer följande jämvikt in sig:
Pb2+(aq) + 2Cl–(aq) ⇌ PbCl2(s) + värme
färglös färglös vit fällning
Vad händer med jämvikten om reaktionsblandningen upphettas?
44. Kobolt(II)joner bildar ett blått färgkomplex med kloridjoner enligt nedanstående jämviktsreaktion:
energi + Co2+(aq) + 4Cl (aq)⇌ CoCl 4 2 –
röd färglöst blått
Vad händer med reaktionsblandningens färg om reaktionsblandningen kyls av?
Öva förståelsen
45. Eten C2H4 reagerar med jodgas och följande jämvikt ställer in sig:
C2H4(g)+ I2(g) ⇌ C2H4I2(g)
färglös violett färglös
För reaktionen åt höger är H < 0. Vad händer med färgen på reaktionsblandningen om den upphettas?
46. Kolmonoxid och vattenånga bildar koldioxid och väte enligt nedanstående reaktionsformel:
CO(g) + H2O(g)⇌ CO2(g) + H2(g)
Vid 600 °C är jämviktskonstanten K = 3,2 och vid 1000 °C är K = 0,72. I ett experiment låter man jämvikten ställa in sig vid 600 °C.
a. Ökar eller minskar masshalten vatten i blandningen om man höjer temperaturen till 1000 °C?
b. Är reaktionen åt höger exoterm eller endoterm?
Analysera och diskutera
• Vid framställning av ammoniak enligt Haber–Bosch-processen körs reaktionen vanligen vid en hög temperatur (450 °C). Reaktionen mellan kväve och vätgas är dock exoterm, vilket betyder att den gynnas av en låg temperatur. Varför väljer man ändå att köra reaktionen vid en högre temperatur, tror du?
Sammanfattning
Kemiska reaktioner drivs av energi och strävan mot oordning. I en exoterm reaktion avges det energi och ∆H < 0, medan det upptas energi i en endoterm reaktion och ∆H > 0. Specifika entalpiförändringar inkluderar förbränningsentalpi, ∆Hc0, som är den energi som frigörs vid förbränning av en mol av ett ämne, och bildningsentalpi, ∆Hf0, energin som åtgår eller frigörs när en mol av ett ämne bildas från sina grundämnen i standardtillstånd.
Hess lag fastställer att den totala entalpiförändringen för en reaktion är oberoende av reaktionsvägen, vilket möjliggör beräkningar via kända delreaktioner. På molekylär nivå kan entalpiförändringar uppskattas med bindningsentalpi, det vill säga den energi som krävs för att bryta en bindning.
För att avgöra om en reaktion sker spontant används Gibbs fria energi, ∆G, som kombinerar entalpi (∆H) med entropi (∆S), ett mått på oordning. Spontana processer, som diffusion, leder till ökad oordning. Om ∆G är negativt kommer reaktionen att vara spontan.
Reaktionshastighet beskriver hur snabbt en reaktion sker. Hastigheten påverkas av ämnenas egenskaper, temperatur, koncentration och närvaron av katalysator.
En katalysator, till exempel enzym i biologiska system, ökar hastigheten genom att sänka reaktionens aktiveringsenergi via en alternativ reaktionsväg, ofta genom ett instabilt aktiverat komplex.
Många reaktioner är reversibla, det vill säga går både åt höger och åt vänster (framåt och bakåt). De når ett jämviktsläge, en dynamisk jämvikt där hastigheten för den framåtgående reaktionen är lika stor som för den bakåtgående. Förhållandet mellan produkters och reaktanters koncentrationer vid jämvikt beskrivs av massverkans lag (Guldberg–Waages lag) och uttrycks med jämviktskonstanten K. I en heterogen jämvikt befinner sig ämnena i olika faser.
För att avgöra om ett system är i jämvikt beräknas koncentrationskvoten Q
Om Q < K går reaktionen åt höger, om Q > K går den åt vänster, och om Q = K är systemet i jämvikt.
Le Chateliers princip förklarar hur ett jämviktssystem svarar på störningar. Om koncentration, tryck eller temperatur ändras, förskjuts jämvikten för att motverka förändringen och uppnå ett nytt jämviktsläge.
Grundämnenas periodiska system
KATALYS KEMI
2
Katalys Kemi 2 är ett basläromedel i ämnet kemi på nivå 2, 100 poäng.
Katalys innehåller ett helt unikt material av filmatiserade genomgångar via QR-koder av hela innehållet som tillsammans med traditionellt skrivna faktatexter underlättar elevens lärande. Läromedlet bygger på en genomtänkt pedagogik som följer en logisk struktur och låter eleverna bygga ny kunskap på redan kända fakta.
Varje avsnitt i kapitlen följs av ett antal övningsuppgifter av olika karaktär och svårighetsgrad: ”Öva begreppen”, ”Öva förståelsen” och ”Analysera och diskutera”.
Boken har följande kapitelindelning:
A Varför sker kemiska reaktioner?
B. Hur sker syrabas-reaktioner?
C. Kolväten och deras närmaste släktingar
D. Hur sker organiska reaktioner?

E. Fördjupad organisk kemi
F. Biomolekyler
G. Biokemi
H. Analytisk kemi
Magnus Ehinger är gymnasielektor i kemi och biologi med många års erfarenhet av undervisning. Magnus är mycket engagerad i att använda flippat klassrum som pedagogisk modell i sin undervisning. Magnus Ehinger har fått Beijerstiftelsens lärarpris till Ingvar Lindqvists minne för sina pedagogiska, egenproducerade genomgångar på Youtube.
