Avaliação in vitro da atividade citotóxica do
sobrenadante proveniente de bactérias probióticas em culturas de células de câncer
In vitro evaluation of the cytotoxic activity of supernatant from probiotic bacteria in cancer cell cultures
RESUMO
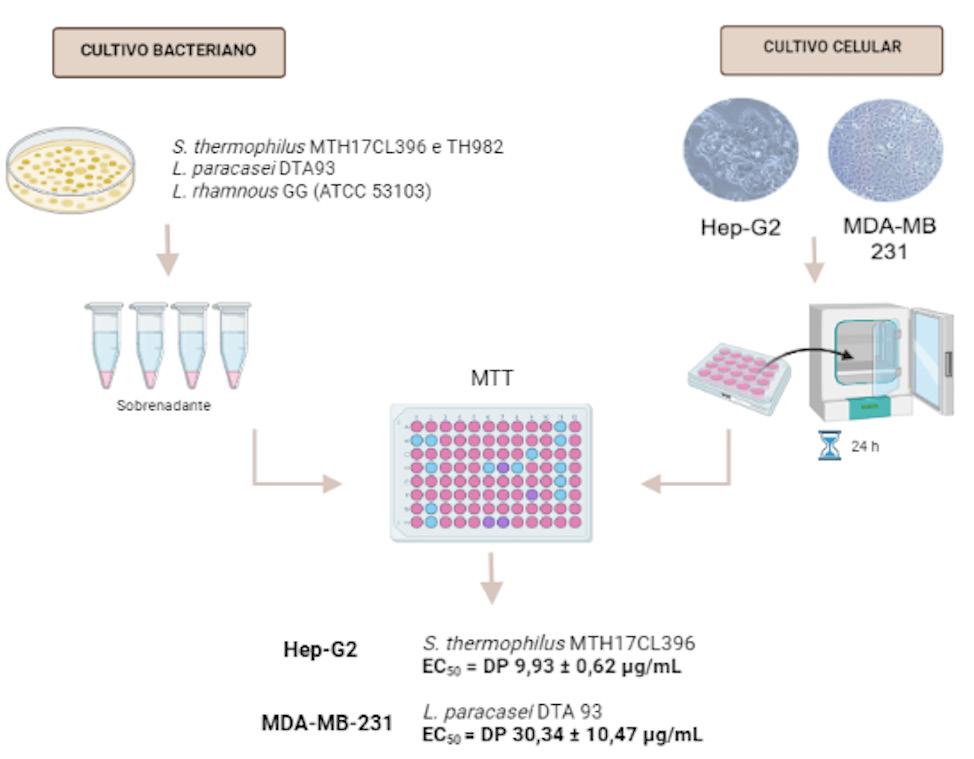
Estudos têm demonstrado resultados promissores quanto às propriedades anticancerígenas dos probióticos, correlacionando a microbiota intestinal disbiótica com diversas doenças, incluindo neoplasias malignas. Para realização do presente estudo, cepas probióticas foram cultivadas por 24 horas para obtenção do sobrenadante. Na sequência foram adicionadas concentrações de 10 a 80 µg/mL nas culturas de células tumorais para avaliação citotóxica pelo método MTT ({brometo de (brometo de 3- [4,5-dimetiltiazol-2-il]-2,5-difeniltetrazólio). Os resultados demonstraram que as cepas Streptococcus thermophilus MTH17CL396 e Lactobacillus paracasei DTA 93 apresentaram uma boa atividade citotóxica in vitro sobre as células Hep-G2 e MDA-MB-231, respectivamente. Entretanto, são necessários estudos adicionais para um melhor entendimento da atuação das bactérias intestinais sobre a saúde.
APLICABILIDADE
Palavras-chave: Citotoxicidade; câncer; probióticos; anticancerígeno; microbiota
A literatura tem demonstrado que os componentes da dieta e nutrição afetam a incidência, progressão e prevenção de neoplasias malignas. Dessa forma, o melhor entendimento da atuação de cepas probióticas intestinais interligadas ao câncer, é necessário para que se desenvolvam tratamentos adjuvantes, diminuindo os efeitos colaterais deletérios e potencializando as terapias convencionais.
RESUMO GRÁFICO
[1] Introdução
Ocâncer é uma patologia caracterizada por danos e acúmulos de mutações no material genético, mecanismo que culmina em multiplicações desordenadas das células teciduais. Segundo a Organização Mundial da Saúde (OPAS/OMS) em 2020 ocorreram, aproximadamente, 10 milhões de mortes em decorrência de neoplasias malignas. Projeções para 2040 indicam que o número de novos casos poderá aumentar 29.5 milhões em comparação com 2020 (NIH National Cancer Institute, 2020). Estima-se que no Brasil o número de novos casos por ano, entre o período de 2020 e 2022, seja de 625 mil (INCA, 2020).
O intestino humano abriga cerca de 100 trilhões de espécies de microrganismos, as quais integram a microbiota intestinal. Atualmente, sabe-se sobre a existência de uma relação simbiótica entre a microbiota e seu hospedeiro, que atua na manutenção de funções metabólicas, imunológicas e hormonais, quando em equilíbrio (BLASER, 2014; GOULET, 2015; SHARMA, 2019). A disparidade entre as populações colonizadoras, conhecida como disbiose, vem sendo associada a sintomatologia, ao metabolismo de quimioterápicos e aos processos carcinogênicos (GARRETT, 2015; KELLY et al., 2016; SHARMA, 2019).
Estudos clínicos e experimentais desenvolvidos com microrganismos vivos, probióticos, demonstram ter efeitos promotores de saúde, principalmente no tratamento e prevenção de diferentes doenças, incluindo alguns tipos de cânceres (DE LEBLANC, 2014; PESSIONE; CIRRINCIONE, 2016; QIN et al., 2012; SHARMA, 2019; SUEZ et al., 2018; WU et al., 2013; ZMORA et al., 2018). Portanto, o presente estudo tem por objetivo inves-
tigar a atividade citotóxica de diferentes sobrenadantes de bactérias probióticas em culturas de células tumorais de diferentes linhagens
[2] Metodologia
[2.1] Obtenção das cepas probióticas
Neste trabalho foram utilizadas cepas de Streptococcus thermophilus MTH17CL396 e TH982 e de Lactobacillus paracasei DTA 93, que foram gentilmente fornecidos pela Universidade de Pádua (Università degli Studi di Padova – UNIPD, Itália). As cepas de S. thermophilus MTH17CL396 e TH982 foram originalmente isoladas de queijo Tipo Fontina (Itália) e do queijo Mozzarella di Bufala (Itália), respectivamente. (TARRAH et al., 2018). A cepa de Lactobacillus paracasei DTA 93 foi isolada de fezes de crianças entre 7 e 21 dias, assistidas pelo Banco de Leite Humano (BLH), pela Unidade de Terapia Intensiva Neonatal (UTIN) do Instituto Fernandes Figueira da FIOCRUZ e pelo HMB do Hospital Estadual da Rocha Faria do Rio de Janeiro. Todas estas cepas já foram previamente descritas como cepas bacterianas com propriedades probióticas (GUERRA et al., 2018; TARRAH et al., 2018). A cepa Lactobacillus rhamnosus GG (ATCC 53103) foi incluída em todos os testes como cepa de referência para propriedades probióticas (TARRAH et al., 2018).
[2.2] Obtenção do sobrenadante das bactérias probióticas
Foi realizado o cultivo das bactérias em meio ágar M17 (Difco, Estados Unidos) contendo 0,5% de lactose, sendo
incubadas a 37ºC por 24 horas. Para armazenar as cepas foi preparado uma solução do cultivo com 20% (v/v) de glicerol, fracionadas em tubos criogênicos e armazenadas a - 80ºC. Cada cepa foi subcultivada três vezes no caldo M17 antes de seu uso para promover seu crescimento. Para a obtenção do sobrenadante das cepas probióticas, foi transferido assepticamente 1 mL da cultura descongelada, devidamente homogeneizada, para tubos de ensaio contendo 9 mL de caldo MRS (HiMedia, Estados Unidos) para L.paracasei DTA 93 e 9 mL de caldo M17 para L. rhamnosus GG e para as cepas de S. thermophilus. Posteriormente, as culturas foram incubadas a 37ºC por um período de 24 h a 48 h, sendo a viabilidade estimada pela contagem de colônias características de cada bactéria. Após esse período de incubação, o caldo foi centrifugado a 12.000 r.p.m. por 10 minutos e o sobrenadante foi coletado.
[2.3] Liofilização do sobrenadante livre de células
Após centrifugação e coleta, o pH do sobrenadante foi ajustado com uma solução de hidróxido de sódio (NaOH, Sigma, Brasil) 1N até que atingisse a faixa de 6,2 a 6,8. Os sobrenadantes foram filtrados por meio de membranas filtrantes em éster de celulose com 0,22 mm de poro e 25 mm de diâmetro (Millipore). Esse filtrado constitui o sobrenadante livre de células não concentrado, que foi então concentrado 20 vezes por liofilização (LIOTOP) e ressuspenso em solução tampão-fosfato de potássio 4mM (pH 7,0).
[2.4] Cultura das células de câncer
As linhagens células tumorais utilizadas neste estudo foram de adenocarcinoma de mama MDA-MB-231 (ATCC® HTB-26™) e carcinoma hepatocelular Hep-G2 [HEPG2] (ATCC® HB-8065™). As células MDA-MB-231 e Hep-G2 foram cultivadas em meio DMEM (Dulbecco’s Modified Eagle Medium; Sigma-Aldrich, Estados Unidos), suplementado com 10% de soro bovino fetal inativado (Gibco BRL, Estados Unidos) e 1% de penicilina (10.000 UI/mL) e estreptomicina (10 mg/mL; Gibco BRL, Estados Unidos). Todas as culturas foram mantidas a 37 °C e com 5% de CO2. O monitoramento do crescimento celular foi realizado a cada 24 horas e, quando a monocamada celular atingia 90% de confluência, era realizada a manutenção da cultura celular com lavagem em tampão HBSS (Sigma-Aldrich) e solução de tripsina-EDTA (0,25%) (Gibco BRL, Estados Unidos).
[2.5] Ensaios de viabilidade e citotoxidade celular
O teste para avaliação da atividade antitumoral foi
realizado pelo método de MTT ({brometo de (brometo de 3- [4,5-dimetiltiazol-2-il]-2,5-difeniltetrazólio) que é um teste colorimétrico utilizado para avaliar a viabilidade celular e o estado metabólico da célula. A viabilidade mitocondrial, e consequentemente, a viabilidade celular, é quantificada pela redução do MTT (que é um sal de coloração amarela e solúvel em água) à formazan (um sal de coloração arroxeada e insolúvel em água) pela atividade enzimática. Dessa maneira, a quantidade de formazan que foi formada, medida por espectrofotometria, é diretamente proporcional à atividade mitocondrial e ao número de células viáveis.
As células Hep-G2 e MDA-MB-231 foram cultivadas separadamente em placas de 96 poços na concentração de 1x105 células/mL e incubadas por 24h a 37 °C em ambiente controlado de 5% de CO2. Após esse período, as culturas de células de câncer receberam diferentes concentrações do sobrenadante (10 – 80 µg/mL) e foram novamente incubadas, por 24h a 37°C e em 5% de CO2. O controle utilizado para evidenciar a morte celular foi uma solução de dimetilsulfóxido (DMSO) (Sigma-Aldrich, Estados Unidos) na concentração de 3% (controle positivo) e para o controle de crescimento foi empregado apenas meio de cultivo (controle negativo). Ambos os controles, positivo e negativo, foram incluídos em cada placa em todos os experimentos. Após esse período de 24h, foi adicionado 20 µL de uma solução de MTT (5 mg/mL) em cada poço, sendo as placas incubadas, nas mesmas condições, por mais 2 h. Sucessivamente, foi retirado o meio de cultura das placas e adicionado 100 µL de DMSO (Sigma-Aldrich, Estados Unidos) em cada poço para dissolver os cristais de formazan. Após as placas foram colocadas em incubação a 37°C por mais 20 min e a absorvância do resíduo de MTT foi medida a um comprimento de onda de 570 nm, utilizando um leitor de microplacas (SpectraMax M5, Molecular Devices, Estados Unidos), contra o branco. Os valores de EC50, que se refere à concentração na qual uma droga, anticorpo ou toxina induz uma resposta na metade entre a taxa inicial e a máxima após um tempo especificado de exposição, foram calculados a partir do gráfico de absorvância contra diferentes concentrações do sobrenadante. Todos os experimentos foram realizados em triplicata.
[2.6] Análise estatística
Todos os dados obtidos foram submetidos a análise de variância de uma via (ANOVA), seguida pelo teste post hoc de Dunnet, quando necessário, com intervalo de confiança de 95%. Os dados foram analisados pelo programa estatístico GraphPad Prism (versão 9.0) e o nível de significância foi estabelecido em P < 0,05.
[3] Resultados e interpretações
O objetivo do estudo foi de avaliar a atividade citotóxica do sobrenadantes de diferentes cepas de bactérias
com propriedades probióticas em linhagens de células cancerígenas. As cepas utilizadas no presente estudo têm potencial tecnológico de acordo com estudos anteriores (TARRAH et al., 2018; VENDRAMIN et al., 2017). Sendo assim, estas cepas foram testadas para atividade citotóxica contra células de adenocarcinoma de mama MDA-MB-231 e carcinoma hepatocelular Hep-G2 usando Lactobacillus rhamnosus GG como cepa de referência. Os resultados demonstraram que alguns sobrenadantes das cepas probióticas utilizadas, foram significativamente citotóxicas para as células Hep-G2 [F(3,9) = 595,7], P < 0,0001. O sobrenadante de Streptococcus thermophilus MTH17CL396 teve um efeito citotóxico significativo (EC50 = 9,93 ± 0,62 μg/mL;) sobre o crescimento de células Hep-G2 em comparação com as mesmas células tratadas com o controle Lactobacillus rhamnosus GG (EC50 = 60,01 ± 0,24 µg/mL; P = 0,0006). Porém, quando comparamos as células tratadas com o sobrenadante de Streptococcus thermophilus TH982 com o controle, não observamos diferenças significativas na citotoxicidade (EC50 = 61,56 ± 2,90 µg/mL; P = 0,99). Além disso, neste presente estudo, o sobrenadante de Lactobacillus paracasei DTA 93 foi o que menos apresentou atividade citotóxica contra a linhagens de células Hep-G2 (EC50 = 350,5 ± 23,35 µg/mL; Tabela 1).
126 μg/mL; Tabela 1).
apresentou atividade citotóxica contra a linhagens de células Hep-G2 (EC50 = 350,5 ± 23,35
127
128
Na linhagem de células cancerígenas MDA-MB-231, apenas o sobrenadante de
Streptococcus thermophilus MTH17CL396 apresentou diferença significativa quando
ao controle (EC50 = 35,17 ± 5,35 µg/mL), é necessária uma dose muito maior do sobrenadante de Streptococcus thermophilus MTH17CL396 para causar citotoxicidade celular (EC50 = 81,74 ± 0,13 µg/mL). Já quando comparamos o controle de Lactobacillus rhamnosus GG com os sobrenadantes das outras cepas probióticas, como Streptococcus thermophilus TH982 (EC50 = 43,61 ± 15,3 µg/mL; P = 0,586) e Lactobacillus paracasei DTA 93 (EC50 = 30,34 ± 10,47 µg/mL; P = 0,586), não obtivemos resultado estatisticamente significativo, porém mesmo assim, estas duas cepas probióticas apresentaram atividade citotóxica, sendo que a cepa de Lactobacillus paracasei DTA 93 apresenta maior citotoxicidade quando comparada as demais. (Tabela 1).
129 comparado ao controle [F(3,8) = 10,47], P = 0,0038. Apesar desse dado ser significativo, isso
130 não significa que o sobrenadante tem potencial citotóxico, pois comparado ao controle (EC50 =
131 35,17 ± 5,35 μg/mL), é necessária uma dose muito maior do sobrenadante de Streptococcus
133
132 thermophilus MTH17CL396 para causar citotoxicidade celular (EC50 = 81,74 ± 0,13 μg/mL).
Já quando comparamos o controle de Lactobacillus rhamnosus GG com os sobrenadantes das
outras cepas probióticas, como Streptococcus thermophilus TH982 (EC50 = 43,61 ± 15,3
μg/mL; P = 0,586) e Lactobacillus paracasei DTA 93 (EC50 = 30,34 ± 10,47 μg/mL; P = 0,586),
Na linhagem de células cancerígenas MDA-MB-231, apenas o sobrenadante de Streptococcus thermophilus MTH17CL396 apresentou diferença significativa quando comparado ao controle [F(3,8) = 10,47], P = 0,0038. Apesar desse dado ser significativo, isso não significa que o sobrenadante tem potencial citotóxico, pois comparado
Os resultados do presente estudo também revelaram que o efeito antiproliferativo é dependente da dose, conforme já descrito por Plessas e cols. (2017), que também usou Lactobacillus rhamnosus GG como referência. Além disso, o tratamento de células de adenocarcinoma colorretal Caco-2 com L. paracasei K5 inibiu a proliferação celular de uma maneira dependente do tempo e da dose, sendo que os efeitos antiproliferativos parecem ser mediados através da indução de apoptose via modulação da expressão de proteínas da família Bcl-2 (PLESSAS et al., 2017).
não obtivemos resultado estatisticamente significativo, porém mesmo assim, estas duas cepas
139
137 probióticas apresentaram atividade citotóxica, sendo que a cepa de Lactobacillus paracasei 138 DTA 93 apresenta maior citotoxicidade quando comparada as demais. (Tabela 1).
Nosso estudo comparou duas dessas cepas de S. thermophilus (MTH17CL396 e TH982) isoladas por Tarrah e cols. (2018), provenientes de queijos produzidos na Itália e demonstrou que é necessária uma quantidade bem inferior do sobrenadante da cepa isolada do queijo Tipo Fontina (Streptococcus thermophilus MTH17CL396) para
Tabela 1 - EC50 dos sobrenadantes de diferentes cepas probióticas contra as células Hep-G2 e 140 MDA-MB-231 utilizando o ensaio MTT
TABELA 1
EC50 dos sobrenadantes de diferentes cepas probióticas contra as células Hep-G2 e MDA-MB-231 utilizando o ensaio MTT
Streptococcus thermophilus TH982 61,56 ± 2,9
Streptococcus thermophilus MTH17CL396 9,93 ± 0,62*
Lactobacillus paracasei DTA 93 350,5 ± 23,35
Lactobacillus rhamnosus GG 60,01 ± 0,25
Streptococcus thermophilus TH982 43,61 ± 15,3
MDA-MB231
Streptococcus thermophilus MTH17CL396 81,74 ± 0,13
Lactobacillus paracasei DTA 93 30,34 ± 10,47*
Lactobacillus rhamnosus GG 35,17 ± 5,35
LEGENDA: DP = desvio padrão, MDA-MB-231 = células de adenocarcinoma de mama, Hep-G2 = células de carcinoma hepatocelular. *P < 0,05 quando comparado ao controle
Legenda: DP = desvio padrão, MDA-MB-231 = células de adenocarcinoma de mama, Hep-G2 =
células de carcinoma hepatocelular. *P < 0,05 quando comparado ao controle
apresentar atividade citotóxica in vitro em carcinoma hepatocelular quando comparado aos outros sobrenadantes. Já o sobrenadante da cepa isolada da Mozzarella di Bufala (Streptococcus thermophilus TH982) é mais citotóxico para a linhagem celular de adenocarcinoma de mama, embora não tenha havido uma diferença estatisticamente significativa quando comparado ao grupo controle. Isso pode ser explicado devido ao fato de as condições de maturação e conservação dos dois queijos seja totalmente diferente, e portanto, suas bactérias podem apresentar diferentes metabolismos.
No estudo de Escamilla, Lane e Maitin (2012) os sobrenadantes de Lactobacillus casei e Lactobacillus rhamnosus GG demonstraram prevenir a invasão das células de câncer de cólon, sugerindo que o sobrenadante probiótico tem substâncias bioativas anti-metastáticas que podem participar na diminuição da atividade celular in vitro (ESCAMILLA; LANE; MAITIN, 2012). Além disso, sobrenadantes de Lactobacillus rhamnosus e Lactobacillus crispatus também possuem efeito citotóxico em células tumorais do tipo HeLa, no entanto, apenas o tratamento com o sobrenadante de Lactobacillus rhamnosus é relativamente efetivo em células HT-29 (NOURI et al., 2016). Ademais, o mesmo trabalho demonstrou que essas bactérias poderiam afetar apenas as células tumorais de HeLa, mas não as células não tumorais do tipo MRC-5, pois o mesmo sobrenadante não teve efeitos adversos quando testados nestas células normais. Os pesquisadores sugerem a presença de uma substância diferente de lactato nos sobrenadantes das cepas de L. rhamnosus que pode ter como alvo específico as células cancerígenas HT-29 e HeLa, mas não as células normais (NOURI et al., 2016). Sendo assim, as cepas de Lactobacillus e Streptococcus podem estimular respostas positivas para a saúde, pois ambas possuem propriedades anticarcinogênicas envolvidas na produção de células natural killer (NK) para regular a progressão de tumores. Além disso, as secreções metabólicas produzidas por Streptococcus thermophilus estão ligados à diminuição do dano ao DNA e, portanto, ao câncer (KUMAR et al., 2010).
Sadegui-Aliabadi e cols. (2014) observaram a influência dos sobrenadantes de Lactobacillus plantarum A7 e Lactobacillus rhamnosus GG em três diferentes concentrações (2,5, 5 e 10 mg/mL) na viabilidade de células de adenocarcinoma de cólon humano (HT-29). A concentração de 10 mg/mL demonstrou uma diferença significativa na viabilidade das células HT-29 entre os grupos de sobrenadantes de L. plantarum A7 e L. rhamnosus GG quando comparados com o grupo controle (SADEGHI-ALIABADI et al., 2014). Em um outro estudo, a administração de Lactobacillus rhamnosus GG em células de câncer gástrico e de cólon apresentou efeito antiproliferativo em altas concentrações e reduziu pela metade a viabilidade celular nas linhas celulares de câncer de colorretal (DLD-1) e câncer gás-
trico (HGC-27) (ORLANDO et al., 2009). Além disso, o uso do probiótico Lactobacillus rhamnosus GG induz a ativação de macrófagos, a produção de óxido nítrico por macrófagos e aumenta significativamente a produção do fator de necrose tumoral alfa (TNF-α), que pode ser citotóxico ou citostático para células tumorais (BERTKOVA et al., 2010; SWITZER et al., 2011). Em um outro estudo, Gammalat e cols. (2016) demonstraram que o Lactobacillus rhamnosus GG induziu a apoptose e reduziu a expressão de várias proteínas angiogênicas e inflamatórias em ratos com câncer de cólon, demonstrando que a administração de L. rhamnosus GG pode desempenhar um papel na prevenção da tumorigênese por meio de inibição da angiogênese e da inflamação (GAMALLAT et al., 2016).
As pesquisas também se estendem a outros tipos de neoplasias além do trato gastrointestinal (TGI), como por exemplo, Aghazadeh et al. (2017) demonstrando que a toxicidade celular foi significativa a partir dos metabólitos secretados de Acidobacter syzygii em linhagens de células de câncer bucal em comparação aos resultados com as cepas de Lactobacillus acidophilus. Para os L. acidophilus, a indução de apoptose nas células cancerígenas de câncer bucal foi superior a 89% e em células normais foram menores que 7%. Interessantemente, a indução de apoptose tardia por A. syzygii foi maior do que por L. acidophilus (63,7% e 2,4% respectivamente) (AGHAZADEH; POURALIBABA; YARI KHOSROUSHAHI, 2017).
[4] Considerações finais
É importante reconhecer que medidas dietéticas e comportamentais têm influência direta na diminuição do risco de desenvolvimento do câncer. Certamente, múltiplas razões, a saber, dietas desequilibradas, consumo de tabaco e álcool, diminuição da atividade física e exposição a tóxicos ambientais, baixa escolaridade, baixa renda e status socioeconômico, são consideradas para a incidência e progressão do câncer. Ferramentas de intervenção dietética podem ser uma estratégia emergente e segura na prevenção do câncer. O manejo da microbiota intestinal pela alteração da dieta parece ser a maneira mais eficaz e econômica de reduzir o risco de câncer, e, portando, o uso de probióticos e seus sobrenadantes pode ser uma alternativa bastante promissora na interferência da oncogênese e progressão tumoral. No entanto, essa área do conhecimento ainda está nos estágios iniciais e mais pesquisas são necessárias para melhor desenvolver este conhecimento.
REFERÊNCIAS
AGHAZADEH, Z.; POURALIBABA, F.; YARI KHOSROUSHAHI, A. The prophylactic effect of Acetobacter syzygii probiotic species against squamous cell carcinoma. Journal of dental research, dental clinics, dental prospects, v. 11, n. 4, p. 208–214, 2017. Disponível em: <http:// www.ncbi.nlm.nih.gov/pubmed/29354246>.
BERTKOVA, I. et al. The effect of probiotic microorganisms and bioactive compounds on chemically induced carcinogenesis in rats. Neoplasma, v. 57, n. 5, p. 422–428, 2010. Disponível em: <http://www.elis.sk/index. php?page=shop.product_details&flypage=flypage. tpl&product_id=1995&category_id=59&option=com_virtuemart&Itemid=1>.
BLASER, Martin J. The microbiome revolution. Journal of Clinical Investigation, v. 124, n. 10, p. 4162–4165, 1 out. 2014. Disponível em: <http://www.jci.org/articles/ view/78366>.
DE LEBLANC, Moreno. The Administration of Probiotics and Fermented Products Containing Lactic Acid Bacteria Exert Beneficial Effects Against Intestinal and NonIntestinal Cancers. Journal of Food & Nutritional Disorders, v. s1, n. 01, 2014.
ESCAMILLA, Juanita; LANE, Michelle A.; MAITIN, Vatsala. Cell-Free Supernatants from Probiotic Lactobacillus casei and Lactobacillus rhamnosus GG Decrease Colon Cancer Cell Invasion In Vitro. Nutrition and Cancer, v. 64, n. 6, p. 871–878, ago. 2012. Disponível em: <http:// www.tandfonline.com/doi/abs/10.1080/01635581.20 12.700758>.
GAMALLAT, Yaser et al. Lactobacillus rhamnosus induced epithelial cell apoptosis, ameliorates inflammation and prevents colon cancer development in an animal model. Biomedicine & Pharmacotherapy, v. 83, p. 536–541, out. 2016. Disponível em: <https://linkinghub.elsevier. com/retrieve/pii/S0753332216305820>.
GARRETT, Wendy S. Cancer and the microbiota. Science, v. 348, n. 6230, p. 80–86, 3 abr. 2015. Disponível em: < https://www.science.org/doi/10.1126/science. aaa4972>.
GOULET, Olivier. Potential role of the intestinal microbiota in programming health and disease: Figure 1. Nutrition Reviews, v. 73, n. suppl 1, p. 32–40, 14 ago. 2015. Disponível em: <https://academic.oup.com/nutritionreviews/article-lookup/doi/10.1093/nutrit/nuv039>.
GUERRA, André Fioravante et al. Lactobacillus paracasei probiotic properties and survivability under stress-induced by processing and storage of ice cream bar or ice-lolly. Ciência Rural, v. 48, n. 9, 27 ago. 2018. Disponível em: <http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0103-84782018000900751&lng=en&tlng=en>.
INCA, Instituto Nacional de Câncer. Brasil terá 625 mil novos casos de câncer a cada ano do triênio 2020-2022. Brasil, 04 de fevereiro, 2020. Disponível em: https:// www.inca.gov.br/noticias/brasil-tera-625-mil-novos-casos-de-cancer-cada-ano-do-trienio-2020-2022 Acesso em: 30/03/2022
KELLY, Debra Lynch et al. The Microbiome and Cancer. Cancer Nursing, v. 39, n. 3, p. E56–E62, maio 2016.
KUMAR, Manoj et al. Cancer-preventing attributes of probiotics: an update. International Journal of Food Sciences and Nutrition, v. 61, n. 5, p. 473–496, 26 ago. 2010. Disponível em: <http://www.tandfonline.com/ doi/full/10.3109/09637480903455971>.
NIH, US National Cancer Institute. Cancer Statistics. Estados Unidos, 25 setembro, 2020. Disponível em: https://www. cancer.gov/about-cancer/understanding/statistics Acesso: 30/03/2022
NOURI, Zahra et al. Dual Anti-Metastatic and Anti-Proliferative Activity Assessment of Two Probiotics on HeLa and HT-29 Cell Lines. Cell journal, v. 18, n. 2, p. 127–34, 2016. Disponível em: <http://www.ncbi.nlm.nih.gov/ pubmed/27551673>.
OPAS/OMS, Organização Pan-Americana da Saúde. Câncer. Outubro, 2020. Disponível em: https://www.paho.org/ pt/topicos/cancer Acesso: 30/03/2022
ORLANDO, Antonella et al. Effects of Lactobacillus rhamnosus GG on proliferation and polyamine metabolism in HGC27 human gastric and DLD-1 colonic cancer cell lines. Immunopharmacology and immunotoxicology, v. 31, n. 1, p. 108–16, 2009. Disponível em: <http://www. ncbi.nlm.nih.gov/pubmed/19234959>.
PESSIONE, Enrica; CIRRINCIONE, Simona. Bioactive Molecules Released in Food by Lactic Acid Bacteria: Encrypted Peptides and Biogenic Amines. Frontiers in Microbiology, v. 7, 9 jun. 2016. Disponível em: <http://journal. frontiersin.org/Article/10.3389/fmicb.2016.00876/ abstract>.
PLESSAS, Stavros et al. Isolation, characterization and evaluation of the probiotic potential of a novel Lactobacillus strain isolated from Feta-type cheese. Food Chemistry, v. 226, p. 102–108, jul. 2017. Disponível em: < https://linkinghub.elsevier.com/retrieve/pii/ S0308814617300511>.
QIN, Junjie et al. A metagenome-wide association study of gut microbiota in type 2 diabetes. Nature, v. 490, n. 7418, p. 55–60, 26 out. 2012. Disponível em: <http:// www.nature.com/articles/nature11450>.
SADEGHI-ALIABADI, Hojjat et al. Effects of Lactobacillus plantarum A7 with probiotic potential on colon cancer and normal cells proliferation in comparison with a commercial strain. Iranian journal of basic medical sciences, v. 17, n. 10, p. 815–9, out. 2014. Disponível em: <http://www.ncbi.nlm.nih.gov/pubmed/25729553>.
SHARMA, Anshul. Importance of Probiotics in Cancer Prevention and Treatment. Recent Developments in Applied Microbiology and Biochemistry. [S.l.]: Elsevier, 2019. p. 33–45. Disponível em: <https://linkinghub.elsevier. com/retrieve/pii/B9780128163283000040>.
SUEZ, Jotham et al. Post-Antibiotic Gut Mucosal Microbiome Reconstitution Is Impaired by Probiotics and Improved by Autologous FMT. Cell, v. 174, n. 6, p. 1406- 1423.e16, set. 2018. Disponível em: <https://linkinghub.elsevier. com/retrieve/pii/S0092867418311085>.
SWITZER, Christopher H. et al. Nitric oxide and protein phosphatase 2A provide novel therapeutic opportunities in ER-negative breast cancer. Trends in Pharmacological Sciences, v. 32, n. 11, p. 644–651, nov. 2011. Disponível em: < https://linkinghub.elsevier.com/retrieve/pii/ S0165614711001167>.
TARRAH, Armin et al. In vitro Probiotic Potential and Anti-cancer Activity of Newly Isolated Folate-Producing Streptococcus thermophilus Strains. Frontiers in Microbiology, v. 9, 19 set. 2018. Disponível em: <https:// www.frontiersin.org/article/10.3389/fmicb.2018.02214/ full>.
VENDRAMIN, Veronica et al. Genome comparison and physiological characterization of eight Streptococcus thermophilus strains isolated from Italian dairy products. Food Microbiology, v. 63, p. 47–57, maio 2017. Disponível em: <https://linkinghub.elsevier.com/retrieve/ pii/S0740002016305512>.
WU, Na et al. Dysbiosis Signature of Fecal Microbiota in Colorectal Cancer Patients. Microbial Ecology, v. 66, n. 2, p. 462–470, 4 ago. 2013. Disponível em: <http:// link.springer.com/10.1007/s00248-013-0245-9>.
ZMORA, Niv et al. Personalized Gut Mucosal Colonization Resistance to Empiric Probiotics Is Associated with Unique Host and Microbiome Features. Cell, v. 174, n. 6, p. 1388- 1405.e21, set. 2018.