Spis treści tomu III
TOM 3 Poszerzanie horyzontów: postępy i zastosowania
24 Chemia materiałów i nanomateriały 753
Synteza materiałów 754
24.1 Tworzenie materiałów o dużej masie 755
Defekty i transport jonów 757
24.2 Defekty rozszerzone 757
24.3 Dyfuzja atomów i jonów 759
24.4 Elektrolity stałe 760
Tlenki, azotki i fluorki metali 764
24.5 Monotlenki metali szeregu 3d 764
24.6 Wyższe tlenki i tlenki złożone 766
24.7 Szkła tlenkowe 778
24.8 Azotki, fluorki i fazy mieszanych anionów 780
Siarczki, związki interkalacyjne i fazy bogate w metale 782
24.9 Warstwowe związki MS2 i interkalacja 782
24.10 Fazy Chevrela i termoelektryki chalkogenkowe 786
Struktury szkieletowe i kataliza heterogeniczna w materiałach porowatych 787
24.11 Struktury oparte na tetraedrycznych oksoanionach 787
24.12 Struktury oparte na połączonych oktaedrycznych i tetraedrycznych centrach metalicznych 791
24.13 Zeolity i struktury mikroporowate w katalizie heterogenicznej 796
Wodorki i materiały magazynujące wodór 799
24.14 Wodorki metali 799
24.15 Inne nieorganiczne materiały magazynujące wodór 801
Właściwości optyczne materiałów nieorganicznych 802
24.16 Barwne ciała stałe 804
24.17 Białe i czarne pigmenty 805
24.18 Fotokatalizatory 806
Chemia półprzewodników 807
24.19 Półprzewodniki 14. grupy 807
24.20 Układy półprzewodnikowe izoelektronowe z krzemem 809
Materiały molekularne i fullerydy 809
24.21 Fullerydy 810
24.22 Chemia materiałów molekularnych 811
Nanomateriały 815
24.23 Terminologia i historia nanomateriałów 815
24.24 Synteza nanocząstek w roztworach 816
24.25 Synteza nanocząstek przez osadzanie z fazy gazowej 818
24.26 Synteza nanomateriałów z wykorzystaniem szkieletów, nośników i podłoży 819
24.27 Charakteryzowanie i tworzenie nanomateriałów przy użyciu mikroskopii 821
Nanostruktury i ich właściwości 821
24.28 Jednowymiarowa kontrola: nanorurki węglowe i nanodruty nieorganiczne 821
24.29 Dwuwymiarowa kontrola: grafen, studnie kwantowe i supersieci stałe 823
24.30 Trójwymiarowa kontrola: mezoporowate materiały i kompozyty 827
24.31 Specjalne właściwości optyczne nanomateriałów 831
Heterogeniczne katalizatory z nanocząstek 833
24.32 Natura katalizatorów heterogenicznych 834
24.33 Reakcje z udziałem heterogenicznych katalizatorów z nanocząstek 838
LITERATURA DODATKOWA 839 ZADANIA 840 ZADANIA SEMINARYJNE 842
25 Zielona chemia 845 Dwanaście zasad 846
25.1 Zapobieganie 846
25.2 Ekonomika atomowa 847
25.3 Mniej niebezpieczne specje chemiczne 848
25.4 Projektowanie bezpieczniejszych substancji chemicznych 849
25.5 Bezpieczniejsze rozpuszczalniki i środki pomocnicze 850
25.6 Projektowanie pod kątem efektywności energetycznej 851
25.7 Wykorzystanie surowców odnawialnych 853
25.8 Ograniczenie pochodnych 854
25.9 Kataliza 854
25.10 Projektowanie z myślą o degradacji 857
25.11 Analiza w czasie rzeczywistym w celu zapobiegania zanieczyszczeniom 858
25.12 Bezpieczniejsza chemia dla zapobiegania wypadkom 858
LITERATURA DODATKOWA 859 ZADANIA 859
ZADANIA SEMINARYJNE 860
26 Chemia bionieorganiczna 861
Organizacja komórek 862
26.1 Fizyczna budowa komórek 862
26.2 Skład nieorganiczny organizmów żywych 862
26.3 Biologiczne miejsca koordynacji jonów metali 865
Jony metali w komunikacji i transporcie 870
26.4 Transport sodu i potasu 870
26.5 Wapniowe białka sygnalizacyjne 872
26.6 Selektywny transport i magazynowanie żelaza 874
26.7 Transport i magazynowanie tlenu 876
26.8 Przeniesienie elektronu 880
Procesy katalityczne 886
26.9 Kataliza kwasowo-zasadowa 886
26.10 Enzymy przetwarzające H2O2 i O2 893
26.11 Enzymy przetwarzające rodniki i grupy alkilowe 903
26.12 Przeniesienie atomu tlenu przez enzymy molibdenowe i wolframowe 906
26.13 Hydrogenazy, enzymy aktywujące H2 909
26.14 Cykl azotowy 910
Metale w procesie regulacji genów 913
26.15 Czynniki transkrypcyjne i rola cynku 913
26.16 Białka zawierające żelazo jako sensory 914
26.17 Białka wykrywające poziomy miedzi i cynku 917
26.18 Biomineralizacja 918 Perspektywy 919
26.19 Udział poszczególnych pierwiastków 919
26.20 Przyszłe kierunki rozwoju 921 LITERATURA
924
27 Chemia nieorganiczna w medycynie 925 Chemia pierwiastków w medycynie 925
27.1 Kompleksy nieorganiczne w leczeniu nowotworów 927
27.2 Leki przeciw zapaleniu stawów 931
27.3 Bizmut w leczeniu wrzodów żołądka 931
27.4 Lit w leczeniu choroby afektywnej dwubiegunowej 932
27.5 Leki metaloorganiczne w leczeniu malarii 933
27.6 Kompleksy metali jako leki przeciwwirusowe 934
27.7 Leki zawierające kompleksy metali, które powoli uwalniają CO: środek przeciw stresowi pooperacyjnemu 935
27.8 Terapia chelatacyjna 935
27.9 Substancje obrazujące 936
27.10 Nanocząstki w celowanym dostarczaniu leków 939
27.11 Perspektywy 940
LITERATURA DODATKOWA 940 ZADANIA 940
ZADANIA SEMINARYJNE 941
Dodatek 1: Wybrane promienie jonowe 943
Dodatek 2: Właściwości elektronowe pierwiastków 945
Dodatek 3: Potencjały standardowe 948
Dodatek 4: Tablice charakterów 961
Dodatek 5: Orbitale SALC 965
Dodatek 6: Wykresy Tanabe–Sugano 969
Skorowidz S-1
24.4 Elektrolity stałe
Każde ogniwo elektrochemiczne, takie jak bateria, ogniwo paliwowe, wyświetlacz elektrochromowy lub czujnik elektrochemiczny, wymaga elektrolitu. W wielu zastosowaniach roztwór jonowy (np. rozcieńczony kwas siarkowy w akumulatorze kwasowo-ołowiowym) jest akceptowalnym elektrolitem, ale ponieważ często pożądane jest unikanie fazy ciekłej ze względu na możliwość rozlania, istnieje duże zainteresowanie rozwojem elektrolitów stałych. Dwa ważne i dokładnie zbadane elektrolity stałe z mobilnymi kationami to tetrajodortęcian(II) srebra, Ag2HgI4 i β-tlenek glinu sodu o składzie Na1+xAl11O17+x/2. Inne ważne przewodniki o szybko poruszających się kationach obejmują NASICON (nazwa utworzona z liter w nazwie angielskiej „Na superionic conductor”) o składzie Na1+xZr2P3–x Si xO12, granaty litowe, takie jak Li7–xLa3Zr2–x Ta xO12, oraz szereg przewodników protonowych, które działają w temperaturze pokojowej lub umiarkowanie wyższej, takich jak CsHSO4 w temp. powyżej 160 °C.
Ciała stałe o dużej ruchliwości anionów są rzadsze niż przewodniki kationowe i generalnie wykazują duże przewodnictwo tylko w podwyższonych temperaturach: aniony są zazwyczaj większe niż kationy, a zatem bariera energetyczna dla dyfuzji przez ciało stałe jest wysoka. W konsekwencji szybkie przewodzenie przez aniony w ciałach stałych jest ograniczone do F– i O2– (o promieniach jonowych odpowiednio 133 pm i 140 pm). Pomimo tych ograniczeń anionowe przewodniki jonowe odgrywają ważną rolę w czujnikach i ogniwach paliwowych, w których typowym materiałem jest stabilizowany itrem tlenek cyrkonu (YSZ – ang. yttria-stabilized zirconia) o składzie Y xZr1–xO2–x/2. W tabeli 24.1 podsumowano niektóre typowe wartości przewodnictwa jonowego elektrolitów stałych i innych mediów o przewodnictwie jonowym.
TABELA 24.1 Wartości przewodnictwa jonowego i elektronowego
Materiał Przewodnictwo*/(S m 1)
Przewodniki jonowe
Kryształy jonowe 10 16–10 2
Przykład: LiI w temp. 298°C 10 4
Elektrolity stałe 10 1–103
Przykład: YSZ w temp. 600°C 1
Przykład: AgI w temp. 500°C 102
Elektrolity mocne (ciekłe) 10 1–103
Przykład: 1 mol dm–3 NaCl(aq) 102
Przewodniki elektronowe
Metale 103–106
Półprzewodniki 10 3–102
Izolatory >10 7
*Symbol S oznacza siemens; 1 S = 1 Ω 1
(a) Stałe elektrolity kationowe
KLUCZOWE PUNKTY Stałe elektrolity nieorganiczne często mają strukturę niskotemperaturową, w której jony są uporządkowane w podzbiorze miejsc; w wyższych temperaturach jony zajmują miejsca w sposób nieuporządkowany, a przewodnictwo jonowe wzrasta.
Chociaż istnieje szybko rosnąca liczba różnych składów i struktur, które wykazują dużą ruchliwość kationów w pobliżu lub tuż powyżej temperatury pokojowej, podstawę tej właściwości można łatwo zilustrować na przykładzie dwóch dobrze zbadanych materiałów, Ag2HgI4 i β-tlenku glinu sodu.
Poniżej temperatury 50 °C Ag2HgI4 ma uporządkowaną strukturę krystaliczną, w której jony Ag+ i Hg2+ są koordynowane tetraedrycznie przez jony I– i występują niezajęte luki tetraedryczne (rys. 24.6a), a jego przewodnictwo jonowe jest małe. Jednak powyżej temperatury 50 °C jony
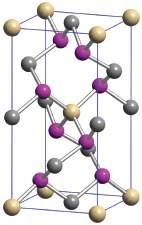




Hg, lub
RYSUNEK 24.6 (a) Niskotemperaturowa uporządkowana struktura Ag2HgI4. (b) Wysokotemperaturowa nieuporządkowana struktura, pokazująca nieuporządkowanie kationów. W postaci wysokotemperaturowej Ag2HgI4 jony Ag+ są przewodnikiem jonowym
Ag+ i Hg2+ są losowo rozmieszczone w miejscach tetraedrycznych (rys. 24.6b), w wyniku czego istnieje znacznie więcej miejsc, które jony Ag+ mogą zajmować w strukturze, niż jest obecnych jonów Ag+. W tej temperaturze materiał jest dobrym przewodnikiem jonowym, głównie ze względu na mobilność jonów Ag+ pomiędzy różnymi dostępnymi dla nich miejscami. Układ o najgęstszym ułożeniu polaryzowalnych jonów I– łatwo ulega deformacji, co powoduje niską energię aktywacji migracji jonów Ag+ z jednego miejsca jonowego do następnego wolnego. Istnieje wiele pokrewnych elektrolitów stałych o podobnych strukturach zawierających miękkie aniony, takich jak AgI i RbAg4I5, w których jony Ag+ są bardzo mobilne, tak że przewodnictwo RbAg4I5 w temperaturze pokojowej jest większe niż przewodnictwo wodnego roztworu chlorku sodu.
β-Tlenek glinu sodu jest przykładem mechanicznie twardego materiału, który jest dobrym przewodnikiem jonowym. W tym przypadku sztywne i gęste płytki Al2O3 są mostkowane przez rozproszony układ jonów O2– (rys. 24.7). Płaszczyzna zawierająca mostkujące jony tlenkowe


1,120 nm
O2–(a) (b)
płytka Al2O3

płaszczyzna przewodzenia

płytka Al2O3
Na+ mostkując y jon O2–Na+
RYSUNEK 24.7 (a) Schematyczny widok z boku β-tlenku glinu sodu, pokazujący płaszczyzny przewodzenia Na2O między płytami Al2O3. Atomy O w tych płaszczyznach łączą dwie płytki. (b) Widok płaszczyzny przewodzenia. Zwróć uwagę na obfitość ruchliwych jonów i luk, w których mogą się one poruszać
zawiera również jony Na+, które mogą przemieszczać się z miejsca na miejsce, ponieważ nie ma większych przewężeń utrudniających ich ruch. Znanych jest wiele podobnych sztywnych materiałów zawierających płaszczyzny lub kanały, przez które mogą przemieszczać się jony; nazywane są one elektrolitami szkieletowymi. W innym blisko spokrewnionym materiale, β′-tlenki glinu sodu, ruch jonów jest jeszcze mniej ograniczony niż w β-tlenku i okazało się, że możliwe jest zastąpienie jonów Na+ dwudodatnimi kationami, takimi jak Mg2+ lub Ni2+. Nawet duży kation lantanowca Eu2+ może być wprowadzony do β′-tlenku, chociaż dyfuzja takich jonów zachodzi wolniej niż w przypadku ich mniejszych odpowiedników. Materiał NASICON, wspomniany wcześniej, jest niestechiometrycznym roztworem stałym ze szkieletem zbudowanym z oktaedrów ZrO6 i tetraedrów PO4, odpowiadających fazie macierzystej o składzie NaZr2P3O12 (rys. 24.8). Stały roztwór można uzyskać przez częściowe zastąpienie atomów P atomami Si, aby otrzymać Na1+xZr2P3–x Si xO12, ze wzrostem liczby jonów Na+ w celu zrównoważenia ładunku. W tym materiale pełny zestaw możliwych miejsc Na+ jest tylko częściowo zapełniony, a miejsca te znajdują się w trójwymiarowej sieci kanałów, które umożliwiają szybką migrację pozostałych jonów Na+. Inne klasy materiałów badanych obecnie jako szybkie przewodniki kationowe obejmują Li4GeO4 domieszkowany V w miejscach Ge, Li4–x(Ge1–x V x)O4, przewodnik litowo-jonowy z lukami w podsieci jonów Li+; perowskit La0,6Li0,2TiO3 oraz krzemian itru sodu, Na5YSi4O12, przewodnik sodowo-jonowy. Jedno z najlepszych przewodnictw litowo-jonowych w temperaturze pokojowej, 1,1 ∙ 10–3 S cm–1, zostało stwierdzone w przypadku Li6,4La3Zr1,4Ta0,6O12. Ciała stałe o dużym przewodnictwie litowo-jonowym budzą zainteresowanie jako elektrolity we wszystkich stałych bateriach litowo-jonowych. W większości komercyjnych akumulatorów litowo-jonowych wykorzystuje się ciekły lub żelowy elektrolit, taki jak LiPF6 w rozpuszczalniku organicznym, z którym związane są problemy bezpieczeństwa i kompromisy konstrukcyjne (ciekłe elektrolity nie mogą być używane z metaliczną anodą litową).
kanały przewodzenia
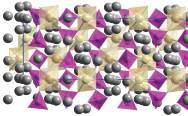

RYSUNEK 24.8 Struktura Na1+xZr2P3–x Si xO12 (NASICON) pokazana jako połączone tetraedry (P,Si)O4 i ZrO6
D3d (3m) E 2C3 3C2 i 2S6 3σd h = 12
A 1g 1 1 1 1 1 1 x2 + y2 , z2
A2g 1 1 1 1 1 1 R z
E g 2 1 0 2 1 0 (R x, R y) (x2 y2 , xy) (zx, yz)
A1u 1 1 1 1 1 1
D4d E 2S8 2C4 2S8 3 C2 4C2 ′ 4σd h = 16 A1 1 1 1 1 1 1 1 x2 + y2 , z2
A2 1 1 1 1 1 1 1 R z B1 1 1 1 1 1 1 1 B2 1 1 1 1 1 1 1 z E1 2 2 0 2 2 0 0 (x, y) E2 2 0
Grupy regularne
Td (43m) E 8C3 3C2 6S4 6σd h = 24
A1 1 1 1 1 1 x2+ y2+z2 A2 1 1 1 1 1
E 2 1 2 0 0 (2z2 x2 y2 , x2 y2) T1 3 0 1 1 1 (R x, R y, R z) T2 3 0 1 1 1 (x, y, z) (xy, yz, zx)
Oh (m3m) E 8C3 6C2 6C4 3C2 (= C42) i 6S4 8S6 3σh 6σ v h = 48
A 1g 1 1
E g 2 1 0 0 2 2 0 1 2 0 (2z2 x2 y2 , x2 y2)
T 1g 3 0 1 1 1 3 1 0 1 1 (R x, R y, R z)
T2g 3 0 1 1 1 3 1 0 1 1 (xy, yz, zx)
A1u 1 1 1 1 1 1 1 1 1 1 A2u 1 1 1 1 1 1 1 1 1 1
E u 2 1 0 0 2 2 0 1 2 0 T1u 3 0 1 1 1 3 1 0 1 1 (x, y, z)
T2u 3 0 1 1 1 3 1 0 1 1
Grupa ikosaedru
I E 12C5 12C5 2 20C3 15C2 h = 60
A1 1 1 1 1 1 x2 + y2+z2
T1 3 (1 5) 1 2 (1 5) 1 2 0 1 (x, y, z) (R x, R y, R z)
T2 3 (1 5) 1 2 (1 5) 1 2 0 1
G 4 1 1 1 0
H 5 0 0 1 1 (2z2 x2 y2 , x2 y2 , xy, yz, zx)
