Spis treści tomu II
2 Pierwiastki i ich związki
9 Zmiany w układzie okresowym 303
Właściwości okresowe pierwiastków 303
9.1 Konfiguracje elektronów walencyjnych 304
9.2 Parametry atomowe 304
9.3 Występowanie 309
9.4 Charakter metaliczny 310
9.5 Stopnie utlenienia 311
Charakterystyka okresowa związków chemicznych 314
9.6 Obecność niesparowanych elektronów 314
9.7 Liczby koordynacyjne 315
9.8 Kierunki zmian entalpii wiązań 315
9.9 Związki dwuskładnikowe 316
9.10 Szersze aspekty okresowości 319
9. 11 Nietypowy charakter pierwszego pierwiastka każdej grupy
Wodór
Proste związki
B: Szczegóły
10.3 Właściwości jądrowe
10.4 Produkcja diwodoru
10.5 Reakcje diwodoru
10.6 Związki wodoru
10.7 Podstawowe metody syntezy dwuskładnikowych związków wodoru
11 Pierwiastki 1. grupy
Nietypowe właściwości litu
11.4 Występowanie oraz otrzymywanie
11.5 Zastosowanie pierwiastków i ich związków
Tlenki i związki pokrewne
Siarczki, selenki i tellurki
Fazy Zintla zawierające litowce
Związki koordynacyjne
12.3 Nietypowe właściwości berylu
Część B: Szczegóły
12.4 Występowanie oraz otrzymywanie
12.5 Zastosowanie pierwiastków i ich związków
Wodorki
Tlenki, siarczki i wodorotlenki
Azotki i węgliki
oksokwasów
Rozpuszczalność, hydratacja i berylany
Związki koordynacyjne
12.13 Związki metaloorganiczne
12.14 Związki pierwiastków grupy 2. na niższym stopniu utlenienia
13 Pierwiastki 13. grupy
Proste związki
Klastery boru i borki
Część B: Szczegóły
13.4 Występowanie oraz odzyskiwanie
13.5 Zastosowanie pierwiastków i ich związków
13.6 Proste związki boru z wodorem
13.7 Trihalogenki boru
13.8 Związki boru z tlenem
13.9 Związki boru z azotem
13.10 Borki metali
13.11 Wyższe borany i hydrydoborany
13.12 Metalaborany i karbaborany
13.14 Trihalogenki glinu, galu, indu i talu
13.15 Halogenki glinu, galu, indu i talu na niższym stopniu utlenienia
13.16 Tlenki glinu, galu, indu i talu
13.17 Siarczki galu, indu i talu
13.18 Związki z pierwiastkami 15. grupy
13.19 Fazy Zintla
13.20 Związki metaloorganiczne
14 Pierwiastki 14. grupy
Część A: Podstawy
14.3 Związki krzemu i tlenu o rozległej sieci 438
Część B: Szczegóły 439
14.4 Występowanie i otrzymywanie 439
14.5 Diament i grafit 439
14.6 Inne odmiany alotropowe węgla 441
14.7 Wodorki 444
14.8 Związki z fluorowcami 447
14.9 Związki węgla z tlenem i siarką 450
14.10 Proste związki krzemu z tlenem 453
14.11 Tlenki germanu, cyny i ołowiu 454
14.12 Związki z azotem 455 14.13 Węgliki 456
14.14 Krzemki 458
14.15 Związki krzemu i tlenu o rozległej sieci 458
14.16 Związki krzemoorganiczne i germanoorganiczne 462
14.17 Związki metaloorganiczne 463
L ITERATURA DODATKOWA 464
ZADANIA 465
ZADANIA SEMINARYJNE 466
15 Pierwiastki 15. grupy 467
Część A: Podstawy 468
15.1 Pierwiastki 468
15.2 Proste związki 469 15.3 Tlenki i oksoaniony azotu 471
Część B: Szczegóły 472
15.4 Występowanie i otrzymywanie 472
15.5 Zastosowanie 473
15.6 Aktywacja azotu 476
15.7 Azotki i azydki 476
15.8 Fosforki 478
15.9 Arsenki, antymonki i bizmutki 478 15.10 Wodorki 478
15.11 Halogenki 481 15.12 Oksohalogenki 482
15.13 Tlenki i oksoaniony azotu 483
15.14 Tlenki fosforu, arsenu, antymonu i bizmutu 488
15.15 Oksoaniony fosforu, arsenu, antymonu i bizmutu 488
15.16 Fosforany skondensowane 490
15.17 Fosfazeny 491
15.18 Związki metaloorganiczne arsenu, antymonu i bizmutu 492
16 Pierwiastki 16. grupy 497
Część A: Podstawy 498 16.1 Pierwiastki 498
16.2 Proste związki 499
16.3 Związki pierścieniowe i klasterowe 501
Część B: Szczegóły 502 16.4 Tlen 502
16.5 Reaktywność tlenu 504
16.6 Siarka 505
16.7 Selen, tellur i polon 507
16.8 Wodorki 508
16.9 Halogenki 510 16.10 Tlenki metali 511
16.11 Siarczki, selenki, tellurki i polonki metali 512
16.12 Tlenki 513
16.12 Oksokwasy siarki 515
16.14 Polianiony siarki, selenu i telluru 520
16.15 Polikationy siarki, selenu i telluru 520
16.16 Związki siarki i azotu 521
L ITERATURA DODATKOWA 522
ZADANIA 522
ZADANIA SEMINARYJNE 523
17 Pierwiastki 17. grupy 525
CZĘŚĆ A: Podstawy 526
17.1 Pierwiastki 526
17.2 Związki proste 527
17.3 Związki międzyhalogenowe 529
CZĘŚĆ B: Szczegóły 530
17.4 Występowanie, otrzymywanie i zastosowania 530
17.5 Struktura cząsteczek i ich właściwości 534
17.6 Zmienność właściwości chemicznych 535
17.7 Związki pseudohalogenowe 536
17.8 Wyjątkowe właściwości związków fluoru 537
17.9 Cechy strukturalne 538
17.10 Związki międzyhalogenowe 539
17.11 Tlenki fluorowców 542
17.12 Oksokwasy i oksoaniony 543
17.13 Termodynamiczne aspekty reakcji redoks oksoanionów 544
17.14 Kierunki zmian szybkości reakcji redoks z udziałem oksoanionów 546
17.15 Właściwości redoks związków na poszczególnych stopniach utlenienia 546
17.16 Fluorowęglowodory 548
LITERATURA DODATKOWA 549
ZADANIA 550
ZADANIA SEMINARYJNE 551
18 Pierwiastki 18. grupy 553
Część A: Podstawy 554
18.1 Pierwiastki 554
18.2 Związki proste 554
Część B: Szczegóły 556
18.3 Występowanie i otrzymywanie 556
18.4 Zastosowania 557
18.5 Synteza i struktura fluorków ksenonu 558
18.6 Reakcje fluorków ksenonu 558
18.7 Związki ksenonu i tlenu 559
18.8 Związki insercyjne ksenonu 560
18.9 Związki organiczne ksenonu 561
18.10 Związki koordynacyjne 562
18.11 Inne związki gazów szlachetnych 562
LITERATURA DODATKOWA 563
ZADANIA 563
ZADANIA SEMINARYJNE 564
19 Pierwiastki bloku d 565
Część A: Podstawy 566
19.1 Występowanie i otrzymywanie 566
19.2 Właściwości chemiczne i fizyczne 567
Część B: Szczegóły 569
19.3 Grupa 3.: skand, itr i lantan 569
19.4 Grupa 4.: tytan, cyrkon i hafn 571
19.5 Grupa 5.: wanad, niob i tantal 573
19.6 Grupa 6.: chrom, molibden i wolfram 576
19.7 Grupa 7.: mangan, technet i ren 582
19.8 Grupa 8.: żelazo, ruten i osm 583
19.9 Grupa 9.: kobalt, rod i iryd 586
19.10 Grupa 10.: nikiel, pallad i platyna 587
19.11 Grupa 11.: miedź, srebro i złoto 589
19.12 Grupa 12.: cynk, kadm i rtęć 591
LITERATURA DODATKOWA 595
ZADANIA 595
ZADANIA SEMINARYJNE 595
20 Kompleksy metali bloku d: struktura elektronowa i właściwości 597
Struktura elektronowa 597
20.1 Teoria pola krystalicznego 598
20.2 Teoria pola ligandów 608
Widma elektronowe 613
20.3 Widma elektronowe atomów 613
20.4 Widma elektronowe kompleksów 617
20.5 Przejścia z przeniesieniem ładunku 622
20.6 Reguły wyboru i natężenie 624
20.7 Luminescencja 626
Magnetyzm 627
20.8 Magnetyzm kooperatyny 627
20.9 Kompleksy spin-crossover 629
LITERATURA DODATKOWA 630 ZADANIA 630
ZADANIA SEMINARYJNE 632
21 Chemia koordynacyjna: reakcje kompleksów 633
Reakcje substytucji ligandów 634
21.1 Szybkość reakcji substytucji ligandów 634
21.2 Klasyfikacja mechanizmów reakcji 635
Substytucja ligandów w kompleksach płaskich kwadratowych 639
21.3 Nukleofilowość grupy wchodzącej 639
21.4 Kształt stanu przejściowego 640
Substytucja ligandów w kompleksach oktaedrycznych 643
21.5 Równania kinetyczne reakcji i ich interpretacja 643
21.6 Aktywacja kompleksów oktedrycznych 645
21.7 Hydroliza zasadowa 648
21.8 Stereochemia 649
21.9 Reakcje izomeryzacji 650
Reakcje redukcji i utlenienia 651
21.10 Klasyfikacja reakcji redukcji i utlenienia 651
21.11 Mechanizm wewnętrznosferowy 651
21.12 Mechanizm zewnętrznosferowy 653
Reakcje fotochemiczne 657
21.13 Reakcje natychmiastowe i opóźnione 657
21.14 Reakcje z przejściami d–d i z przejściami z przeniesieniem ładunku 658
21.15 Przejścia w układach z wiązaniami metal–metal 659
LITERATURA DODATKOWA 660
ZADANIA SEMINARYJNE 661
22 Chemia metaloorganiczna metali bloku d 663
Sposób wiązania 665
22.1 Trwałe konfiguracje elektronowe 665
22.2 Preferencje dotyczące liczby elektronów 667
22.3 Zliczanie elektronów i stopnie utlenienia 667
22.4 Nazewnictwo 669
Ligandy 670
22.5 Tlenek węgla(II) 670
22.6 Fosfiny 672
22.7 Wodorki i kompleksy z diwodorem 674
22.8 Ligandy η1-alkilowe, -alkertlowe, -alkirylowe i -arylowe 675
22.9 η2-Alkeny i -alkiny jako ligandy 675
22.10 Niesprzężone dieny i polieny jako ligandy 676
22.11 Butadien, cyklobutadien i cyklooktatetraen 677
22.12 Benzen i inne areny 679
22.13 Ligand allilowy 680
22.14 Cyklopentadien i cykloheptatrien 681
22.15 Karbeny 682
22.16 Alkany, agostyczne wodory i gazy szlachetne 683
22.17 Diazot i tlenek azotu(II) 684
Związki 685
22.18 Karbonylki metali bloku d 685
22.19 Metaloceny 691
22.20 Wiązanie metal–metal i klastery metali 695
Reakcje 699
22.21 Substytucja ligandów 699
22.22 Oksydacyjna addycja i redukcyjna eliminacja 702
22.23 Metateza wiązań σ 703
22.24 Reakcje migracyjnej insercji 1,1 703
22.25 Insercje 1,2 i eliminacja β-wodorku 704
22.26 Eliminacje α-, γ- i δ- wodorków oraz cyklometalacje 705
Kataliza 705
22.27 Metateza alkenów 706
22.28 Uwodornienie alkenów 707
22.29 Hydroformylacja 709
22.30 Utlenianie alkenów metodą Wackera 710
22.31 Reakcje tworzenia wiązań C–C katalizowane palladem 711
22.32 Oligomeryzacja i polimeryzacja 712
LITERATURA DODATKOWA 717 ZADANIA 718
ZADANIA SEMINARYJNE 719
23 Pierwiastki bloku f 721
Pierwiastki 722
23.1 Orbitale walencyjne 722
23.2 Występowanie i otrzymywanie 723
23.3 Właściwości fizyczne i zastosowania 724
Chemia lantanowców 725
23.4 Ogólne tendencje 725
23.5 Właściwości optyczne i magnetyczne 728
23.6 Dwuskładnikowe związki jonowe 733
23.7 Trójskładnikowe i złożone tlenki 735
23.8 Związki koordynacyjne 736
23.9 Związki metaloorganiczne 738
Chemia aktynowców 742
23.10 Ogólne tendencje 742
23.11 Widma elektronowe aktynowców 745
23.12 Tor i uran 746
23.13 Neptun, pluton i ameryk 748
LITERATURA DODATKOWA 748
ZADANIA 749
ZADANIA SEMINARYJNE 749
Skorowidz S-1
TABELA 21.10 Parametry kinetyczne ataku anionu na Cr(III)*
X L = H2O L = NH3 k/ (10-8 mol 1 s 1) Δ‡H/ (kJ mol 1) Δ‡S/ (J K 1 mol 1) k/ (10 4 dm3 mol 1 s 1)
Br 0,46 122 8 3,7
Cl 1,15 126 38 0,7
NCS 48,7 105 4 4,2
* Dla reakcji [CrL5(OH2)]3+ + X → [CrL5X]2+ + H2O.
W tabeli 21.10 przedstawiono niektóre dane dotyczące tworzenia kompleksów Br–, Cl– i NCS– z [Cr(OH2)6]3+ i [Cr(NH3)5(OH2)]3+. W przeciwieństwie do silnej zależności heksaakwakompleksu od rodzaju czynnika nukleofilowego, pentaaminakompleks wykazuje jedynie słabą zależność, co sugeruje przejście od mechanizmu I a do Id Ponadto, stałe szybkości reakcji wymiany cząsteczki H2O w [Cr(OH2)6]3+ na Cl–, Br– lub NCS– są około 104 razy mniejsze niż analogicznych reakcji [Cr(NH3)5(OH2)]3+. Różnica ta sugeruje, że ligandy NH3, które są silniejszymi donorami elektronów σ niż H2O, skuteczniej promują dysocjację szóstego liganda. Jak stwierdziliśmy uprzednio, takiego zachowania należy się spodziewać w reakcjach aktywowanych dysocjacyjnie.
PRZYKŁAD 21.3 Interpretacja danych kinetycznych w odniesieniu do mechanizmu reakcji
Stałe szybkości reakcji drugiego rzędu tworzenia kompleksu [VX(OH2)5]+ z [V(OH2)6]2+ i X–, gdzie X– = Cl–, NCS–i N3–, mają się do siebie, jak 1:2:10. Co sugerują te dane w odniesieniu do etapu determinującego szybkość reakcji substytucji?
Odpowiedź Musimy wziąć pod uwagę czynniki, które mogą wpływać na szybkość reakcji. Wszystkie trzy ligandy są jednoujemnie naładowanymi anionami o podobnej wielkości, możemy więc oczekiwać, że stałe równowagi tworzenia kompleksów spotkaniowych będą podobne. Dlatego stałe szybkości reakcji drugiego rzędu są proporcjonalne do stałych szybkości reakcji substytucji pierwszego rzędu w kompleksie spotkaniowym. Stała szybkości reakcji drugiego rzędu jest równa KEk2, gdzie KE jest stałą przedrównowagi, a k2 jest stałą szybkości reakcji substytucji pierwszego rzędu w kompleksie spotkaniowym. Większe wartości stałych szybkości dla NCS– niż dla Cl–, a zwłaszcza pięciokrotnie mniejsza stała szybkości dla NCS– niż dla jego bliskiego analogu strukturalnego N3 –, sugerują pewien udział ataku nukleofilowego i mechanizmu asocjacyjnego. W przeciwieństwie do tego, nie ma takiego systematycznego wzorca dla tych samych anionów reagujących z Ni(II), dla których uważa się, że mechanizm jest dysocjacyjny.
Sprawdź, czy umiesz 21.1 Korzystając z danych z tab. 21.6, oszacuj odpowiednią wartość stałej KE i oblicz
wartość stałej k2 reakcji V(II) z Cl–, jeśli zaobserwowana stała szybkości reakcji drugiego rzędu wynosi 1,2 · 102 dm3 mol–1 s–1
21.7 Hydroliza zasadowa
KLUCZOWY PUNKT Reakcja substytucji w kompleksach oktaedrycznych może być znacznie przyspieszona przez jony OH–, gdy obecne są ligandy zawierające kwasowe jony wodorowe, w wyniku zmniejszenia ładunku reaktywnych form i zwiększonej zdolności deprotonowanego liganda do stabilizacji stanu przejściowego.
Rozważmy reakcję substytucji, w której ligandy zawierają kwasowe protony:
[CoCl(NH3)5]2+ + OH → [Co(OH)(NH3)5]2+ + Cl−
Rozszerzone badania wykazały, że podczas gdy równanie kinetyczne opisuje reakcję drugiego rzędu o szybkości = k[CoCl(NH3)52+][OH–], mechanizm nie polega na prostym bimolekularnym ataku jonu OH– na kompleks. Na przykład, wymiana Cl– na OH– jest szybka, jednak wymiana Cl– na F– jest powolna, nawet jeśli F– bardziej przypomina OH– pod względem wielkości i nukleofilowości. Istnieje duża liczba pośrednich dowodów odnoszących się do tego problemu, ale jeden reprezentatywny eksperyment pokazuje zasadniczą kwestię. Ten rozstrzygający dowód pochodzi z badania rozkładu izotopów 18O/16O w produkcie [Co(OH)(NH3)5]2+. Wiadomo, że w stanie równowagi stosunek izotopowy 18O/16O w cząsteczkach H2O i anionach OH–, jest różny, a fakt ten można wykorzystać do ustalenia, czy wchodząca grupa to H2O czy OH–. Stosunek izotopowy 18O/16O w kompleksie kobaltu odpowiada stosunkowi w cząsteczkach H2O, a nie w jonach OH–, co dowodzi, że to cząsteczka H2O jest grupą wchodzącą. W mechanizmie, który uwzględnia te obserwacje, zakłada się, że rolą jonów OH– jest działanie w charakterze zasady Brønsteda, a nie grupy wchodzącej:
H[ 23
[CoCl(NH) ]O CoCl(NH)(NH) ]H O [CoCl(NH)(NH) ][Co(NH)(NH) ]Cl (wolny, etap determinujący szybkość) [Co(NH )(NH )] HO [Co(OH)(NH) ] (szybki) 35 2 23 42 23 42 34 2 23 4 2 5 2 → →
W pierwszym etapie skoordynowany ligand NH3 działa jak kwas Brønsteda i szybko ustala się stan równowagi między wyjściowym kompleksem a sprzężoną z nim zasadą, która zawiera ligand amidowy (NH2–). Deprotonowana forma kompleksu ma mniejszy ładunek i łatwiej odłącza jon Cl–niż protonowana forma, przyspieszając w ten sposób reakcję. Ponadto ligand amidowy jest zarówno silniejszym donorem elektronów σ niż cząsteczka NH3, jak i dobrym donorem elektronów π. Te silne właściwości donorowe ligandu NH2– powodują, że ligand Cl–, zajmujący pozycję trans jest labilny i stabilizuje pięciokoordynacyjny stan
przejściowy (patrz następne Krótkie podsumowanie w celu omówienia konsekwencji stereochemicznych). Ostatnim etapem jest szybkie przyłączenie cząsteczek wody i przeniesienie protonu do amidu.
21.8 Stereochemia
KLUCZOWY PUNKT Reakcja przebiegająca z utworzeniem produktu pośredniego o strukturze piramidy kwadratowej powoduje zachowanie oryginalnej struktury, ale reakcja przebiegająca z utworzeniem produktu pośredniego o strukturze bipiramidy trygonalnej może prowadzić do izomeryzacji.
Klasycznych przykładów stereochemii reakcji substytucji w kompleksach oktaedrycznych dostarczają kompleksy Co(III). W tabeli 21.11 przedstawiono niektóre dane dotyczące hydrolizy kompleksów cis- i trans-[CoAX(en)2]+ odpowiednio (8) i (9), w których X jest grupą opuszczającą (Cl–lub Br–), a A to OH–, NO2–, NCS– lub Cl–. Stereochemiczne konsekwencje podstawienia w kompleksach oktaedrycznych są znacznie bardziej skomplikowane niż w przypad-
TABELA 21.11 Stereochemiczny przebieg reakcji hydrolizy [CoAX(en)2]+
A X Udział izomeru cis w produkcie/ % cis OH Cl 100
Cl Cl 100
NCS Cl 100
Cl Br 100 trans NO2 Cl 0
NCS Cl 50–70
Cl Cl 35
OH Cl 75
X jest grupą opuszczającą.
ku kompleksów płaskich kwadratowych. Kompleksy cis nie ulegają izomeryzacji podczas reakcji substytucji, natomiast formy trans wykazują tendencję do izomeryzacji coraz większą w kolejności A = NO2– < Cl– < NCS– < OH–
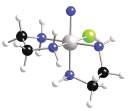
-[CoAX(en)2]
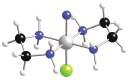
Dane te można zrozumieć, zakładając mechanizm Id i uznając, że pięciokoordynacyjny centralny jon metalu w stanie przejściowym może przypominać jedną z dwóch trwałych struktur pięciokoordynacyjnych, a mianowicie piramidę kwadratową lub bipiramidę trygonalną. Jak wynika z rys. 21.13, reakcja zachodząca przez utworzenie kompleksu o strukturze piramidy kwadratowej powoduje zachowanie oryginalnej struktury, ale reakcja zachodząca przez utworzenie kompleksu o strukturze bipiramidy trygonalnej może prowadzić do izomeryzacji. Kompleks cis
RYSUNEK 21.13 Reakcja przebiegająca przez tworzenie kompleksu o strukturze piramidy kwadratowej (górna droga) powoduje zachowanie oryginalnej struktury, ale reakcja przebiegająca przez tworzenie kompleksu o strukturze bipiramidy trygonalnej (dolna droga) może prowadzić do izomeryzacji
Część B: Szczegóły
W tej części omawiamy szczegóły chemii pierwiastków 16. grupy i obserwujemy bogate zróżnicowanie struktur tworzonych przez nie związków.
16.4 Tlen
KLUCZOWE PUNKTY Tlen ma dwie odmiany alotropowe, ditlen i ozon. Ditlen ma trypletowy stan podstawowy i utlenia węglowodory zgodnie z rodnikowym mechanizmem łańcuchowym. Reakcja z cząsteczką w stanie wzbudzonym może wytworzyć dość długożyjący stan singletowy, który może reagować jak elektrofil. Ozon jest nietrwałym i bardzo agresywnym utleniaczem.
Tlen jest gazem biogennym (tj. takim, który został utworzony w wyniku działania organizmów): prawie w całości powstaje w wyniku fotosyntezy, chociaż jego śladowe ilości są wytwarzane w górnych warstwach atmosfery w wyniku działania promieniowania nadfioletowego na parę wodną. Tlen gazowy jest bezbarwny, bezwonny i rozpuszczalny w wodzie w ilości 3,08 cm3 na 100 cm3 wody w temp. 25 °C i pod ciśnieniem atmosferycznym. Rozpuszczalność ta spada poniżej 2,0 cm3 w wodzie morskiej, ale nadal jest wystarczająca do podtrzymania tlenowego życia morskiego. Rozpuszczalność O2 w rozpuszczalnikach organicznych jest około 10 razy większa niż w wodzie. Dobra rozpuszczalność O2 sprawia, że konieczne jest oczyszczanie wszystkich rozpuszczalników stosowanych w syntezie związków wrażliwych na tlen.
Tlen jest łatwo dostępny w postaci O2 z atmosfery i jest otrzymywany na masową skalę przez skraplanie i destylację ciekłego powietrza. Głównym gospodarczym zastosowaniem jest odzyskiwanie O2 do produkcji stali, w której reaguje on egzotermicznie z koksem (węglem) w celu utworzenia tlenku węgla. Wysoka temperatura jest niezbędna do osiągnięcia szybkiej redukcji tlenków żelaza przez CO i węgiel (podrozdz. 6.16). Czysty tlen, a nie powietrze, jest korzystny w tym procesie, ponieważ energia nie jest zużywana na ogrzewanie azotu. Do wyprodukowania 1 tony stali potrzeba około 1 tony (1 t = 103 kg) tlenu. Tlen jest również potrzebny w przemyśle do produkcji białego pigmentu TiO2 w procesie chlorkowym:
TiCl (c)O (g)TiO (s)2 Cl (g) 42 22
Produkcja tlenu na niewielką skalę, np. w domach osób cierpiących na astmę, polega na procesie adsorpcji zmiennociśnieniowej, w której powietrze przepuszczane jest przez zeolit, który preferencyjnie adsorbuje azot. Tlen jest wykorzystywany w wielu procesach utleniania, na przykład w produkcji oksiranu (tlenku etylenu) z etenu. Tlen jest również dostarczany na dużą skalę do oczyszczania ścieków, odnawiania zanieczyszczonych dróg wodnych, bielenia masy papierniczej oraz jako sztuczna atmosfera w zastosowaniach medycznych i na łodziach podwod-
nych. Tlen jest również niezbędnym produktem ubocznym wytwarzania wodoru w procesie elektrochemicznego rozkładu wody (Ramka 16.2).
Ciekły tlen jest bladoniebieski i wrze w temperaturze –183 °C. Jego barwa wynika z przejść elektronowych obejmujących pary sąsiadujących cząsteczek: jeden foton z czerwonożółtozielonego obszaru widma widzialnego może wzbudzić dwie cząsteczki O2 do stanu wzbudzonego, tworząc parę molekularną. Pod wysokim ciśnieniem barwa stałego tlenu zmienia się z jasnoniebieskiej na pomarańczową, a następnie na czerwoną przy około 10 GPa. Opis orbitali molekularnych O2 sugeruje istnienie podwójnego wiązania; jednak, jak stwierdziliśmy w podrozdz. 2.8, dwa najbardziej zewnętrzne elektrony o równoległych spinach zajmują różne antywiążące orbitale π; w rezultacie cząsteczka jest paramagnetyczna (rys. 16.1). Symbolem termu stanu podstawowego trypletowego jest 3Σ–g, dlatego cząsteczka będzie oznaczana O2(3Σ–g), gdy właściwe będzie określenie stanu spinowego1. Stan singletowy, 1Σ+ g z antyrównoległymi elektronami na tych samych dwóch orbitalach π*, ma wyższą energię o 1,63 eV (158 kJ mol–1), a inny stan singletowy 1Δ g („singlet delta”), w którym oba elektrony są sparowane na jednym orbitalu π*, leży pomiędzy tymi dwoma termami, 0,98 eV (94 kJ mol–1) powyżej stanu podstawowego. Z dwóch stanów singletowych ten drugi ma znacznie dłuższy czas życia w stanie wzbudzonym, a O2(1Δg) istnieje wystarczająco długo, aby uczestniczyć w reakcjach chemicznych. Gdy jest potrzebny do reakcji, tlen w stanie O2(1Δg) może być generowany w roztworze przez transfer energii z fotowzbudzonej cząsteczki. W ten sposób [Ru(bpy)3]2+ może zostać wzbudzony przez absorpcję światła niebieskiego (452 nm)
1 Symbole Σ, Π i Δ są używane dla cząsteczek liniowych, takich jak tlen, zamiast symboli S, P i D używanych dla atomów. Litery greckie oznaczają wielkość całkowitego orbitalnego momentu pędu wokół osi międzyjądrowej. RYSUNEK 16.1 Diagram orbitali molekularnych O2
RAMKA 16.2 Czy utlenianie wody można wykorzystać do produkcji energii odnawialnej?
Tlen jest niezbędny nie tylko jako reagent w procesach spalania lub ogniwach paliwowych: jest on również podstawowym produktem ubocznym wytwarzania wodoru w procesie elektrochemicznego rozkładu wody. Produkcja H2 z wody przy użyciu energii elektrycznej wytwarzanej z energii słonecznej oferuje ważne rozwiązanie dwóch głównych wyzwań związanych z energią odnawialną, radzenia sobie z okresowym występowaniem światła słonecznego i energii wiatrowej oraz zastąpienia paliw kopalnych wykorzystywanych w transporcie. Na każde dwie cząsteczki H2 wyprodukowane na katodzie ogniwa, jedna cząsteczka O2 musi zostać uwolniona na anodzie. Wspomnieliśmy już o znaczeniu opracowania wydajnych katalizatorów do produkcji H2 (podrozdz. 10.4). Bezpośrednie utlenianie wody do tlenu cząsteczkowego (E⦵ = 1,23 V) jest znacznie trudniejsze kinetycznie, ponieważ wymaga usunięcia czterech protonów i czterech elektronów z dwóch cząsteczek wody w procesie, który obejmuje kilka nietrwałych produktów pośrednich; dlatego do aktywacji reakcji potrzebny jest duży i nieekonomiczny nadpotencjał. Istnieje zainteresowanie opracowaniem katalizatorów, które będą przeprowadzać utlenianie wody z niewielkim nadpotencjałem, ale aby były one użyteczne,
muszą być wytrzymałe i składać się z tanich, powszechnie występujących pierwiastków. Wybranymi katalizatorami są wielojądrowe akwa/oksokompleksy metali bloku d, zdolne do poddawania się kolejnym etapom utleniania przez sprzężone z protonem przeniesienie elektronu.
W biologii fotosyntetyczna przemiana O2 zachodzi w klasterze Mn–O, który może produkować ponad 100 cząsteczek O2 na sekundę (podrozdz. 26.10). Niektóre obiecujące niebiologiczne elektrokatalizatory do utleniania wody oparte są na tlenkach kobaltu. Elektrochemiczne utlenianie uwodnionych jonów Co2+ za pomocą anionów oksoboranowych lub fosforanowych powoduje osadzanie galwaniczne warstwy tlenku kobaltu, która katalizuje wydzielanie O2 przy niskim nadpotencjale. Prawdopodobny mechanizm (rys. R16.1) można zrozumieć, biorąc pod uwagę, w jaki sposób kwasowość skoordynowanej cząsteczki wody wzrasta wraz ze wzrostem stopnia utlenienia jonu metalu (podrozdz. 5.2). Jony kobaltu na powierzchni ulegają utlenieniu przez kolejne sprzężone przeniesienia proton–elektron, w wyniku czego powstaje sąsiednia para rodników oksylowych koordynowanych przez Co(III): następuje utworzenie wiązania O–O i uwalniana jest cząsteczka O2.
elektroda
RYSUNEK R16.1 Prawdopodobny mechanizm katalitycznego tworzenia O2
do elektronowego stanu wzbudzonego, oznaczonego
*[Ru(bpy)3]2+ (podrozdz. 20.7), a stan ten przekazuje energię do O2(3Σ–g):
*[ Ru(bpy)] O( )[ Ru(bpy)] O( ) 3 2 2 3 g3 2 2 1 g
Innym skutecznym sposobem wytwarzania O2(1Δg) jest rozkład termiczny ozonku:
W przeciwieństwie do rodnikowego charakteru wielu reakcji O2(3Σ–g), tlen O2(1Δg) reaguje jako elektrofil. Ten tryb reakcji jest możliwy, ponieważ O2(1Δg) ma pusty orbital π*, a nie dwa, z których każdy jest zajęty przez pojedynczy elektron. Na przykład O2(1Δg) przyłącza się do dienu, naśladując w ten sposób reakcję Dielsa–Aldera butadienu z elektrofilowym alkenem:
+ O2 (1Δg)
+ O2 (1Δg)
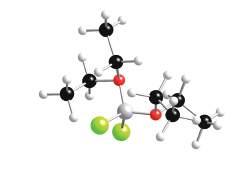
W fazie gazowej związek ma tendencję do tworzenia dimeru opartego na hybrydyzacji sp2 (3), a gdy temperatura przekracza 900 °C tworzą się liniowe monomery, co wskazuje na hybrydyzację sp (
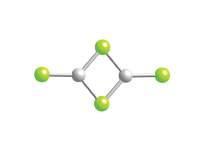

4 faza gazowa BeCl2, T > ok. 900 °C
Bezwodne halogenki magnezu można otrzymać przez bezpośrednie połączenie pierwiastków lub, w przypadku strontu i baru, przez odwodnienie uwodnionej soli halogenkowej; przygotowanie z roztworów wodnych daje sole uwodnione, które w przypadku lżejszych pierwiastków ulegają częściowej hydrolizie podczas ogrzewania. Wszystkie fluorki z wyjątkiem BeF2 są trudno rozpuszczalne, chociaż rozpuszczalność nieznacznie wzrasta w dół grupy. Wraz ze wzrostem promienia kationu od Be do Ba liczba koordynacyjna we fluorkach wzrasta od 4 do 8; BeF2 tworzy struktury analogiczne do SiO2 (takich jak kwarc, koordynacja 4:2), MgF2 przyjmuje strukturę rutylu (6:3), a CaF2, SrF2 i BaF2 przyjmują strukturę fluorytu (8:4) (podrozdz. 4.9). Pozostałe halogenki 2. grupy tworzą struktury warstwowe, odzwierciedlając rosnącą polaryzowalność jonów halogenkowych. Chlorek magnezu przyjmuje strukturę warstwową CdCl2, w której warstwy są ułożone w taki sposób, że jony Cl tworzą sieć regularną o najgęstszym ułoeniu atomów (rys. 12.4). Zarówno MgI2, jak i CaI2 przyjmują powiązaną z nią strukturę jodku kadmu, w której warstwy jonów I– należą do sieci heksagonalnej o najgęstszym ułożeniu atomów (podrozdz. 4.9, rys. 4.40). Najważniejszym fluorkiem w tej grupie jest CaF2. Jego postać mineralna, fluoryt, jest jedynym źródłem fluoru
Cd Cl
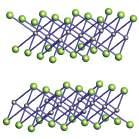
RYSUNEK 12.4 Struktura CdCl2 przyjmowana przez MgCl2
na dużą skalę. Bezwodny fluorowodór wytwarza się przez działanie stężonym kwasem siarkowym(VI) na fluoryt:
CaF(s) HSO(c) C aSO (s)2 HF(c) 22 44 → Wszystkie chlorki rozpływają się pod wpływem wilgoci powietrza i tworzą hydraty; mają niższą temperaturę topnienia niż fluorki. Chlorek magnezu jest najważniejszym chlorkiem dla przemysłu i różnych zastosowań. Wydobywa się go z wody morskiej, a następnie wykorzystywany jest do produkcji magnezu. Duże znaczenie ma także chlorek wapnia, który jest produkowany na masową skalę przemysłowo. Jego higroskopijny charakter zapewnia mu szerokie zastosowanie jako środka suszącego w laboratoriach. Zarówno MgCl2, jak i CaCl2 stosuje się do odladzania dróg, gdzie są one bardziej skuteczne niż NaCl z dwóch powodów. Po pierwsze, rozpuszczanie jest bardzo egzotermiczne: H CaCl (s)Ca(aq)2 Cl (aq 2kJmol 2 2 rozp o 1 →
Wytworzone ciepło pomaga stopić lód. Po drugie, minimalna temperatura zamarzania mieszaniny CaCl2 w wodzie wynosi –55 °C, w porównaniu z –18 °C dla NaCl w wodzie. Chlorki wapnia i magnezu są również mniej toksyczne niż NaCl dla roślin otaczających drogi i są mniej korozyjne dla żelaza i stali. Egzotermiczne rozpuszczanie chlorków prowadzi również do zastosowań w błyskawicznie nagrzewających się opakowaniach i samoogrzewających się pojemnikach na napoje.
Rad ma najmniej rozpuszczalnych halogenków ze względu na małą entalpię hydratacji dużego jonu Ra2+; rozpuszczalności RaCl2 i BaCl2 w temp. 20 °C wynoszą odpowiednio ok. 200 g dm–3 i ok. 350 g dm–3. Właściwość tę wykorzystuje się do oddzielenia Ra2+ od Ba2+ przez krystalizację frakcyjną chlorku lub bromku.
PRZYKŁAD 12.3 Przewidywanie charakteru halogenków
Wykorzystaj dane z tabeli 1.7 i rys. 2.28, aby przewidzieć, czy CaF2 jest głównie jonowy czy kowalencyjny.
Odpowiedź Jedno z podejść polega na określeniu elektroujemności dwóch pierwiastków w związku, a następ -
nie odniesienie się do trójkąta Ketelaara (podrozdz. 2.13), aby ocenić rodzaj występującego wiązania. Wartości elektroujemności Paulinga pierwiastków Ca i F wynoszą odpowiednio 1,00 i 3,98. Średnia elektroujemność wynosi zatem 2,49, a różnica 2,98. Te wartości w trójkącie Ketelaara na rys. 2.28 wskazują, że CaF2 powinien być jonowy. Sprawdź, czy umiesz 12.3 Oceń, czy (a) BeCl2 i (b) BaF2 są głównie jonowe czy kowalencyjne. Omów struktury przyjęte przez te dwa związki, odnosząc się do dokonanych przewidywań.
12.8 Tlenki, siarczki i wodorotlenki
Pierwiastki 2. grupy reagują z O2, tworząc tlenki. Wszystkie pierwiastki z wyjątkiem Be również tworzą nietrwałe nadtlenki. Tlenki od Mg do Ra reagują z wodą, tworząc zasadowe wodorotlenki; BeO i Be(OH)2 są amfoteryczne.
(a) Tlenki, nadtlenki i tlenki złożone
KLUCZOWE PUNKTY Wszystkie pierwiastki 2. grupy tworzą normalne tlenki w reakcji z tlenem, z wyjątkiem Ba, który tworzy nadtlenek; wszystkie nadtlenki rozkładają się na tlenki, a ich trwałość rośnie w dół grupy.
Tlenek berylu otrzymuje się przez spalenie metalu w tlenie. Jest to białe, nierozpuszczalne ciało stałe o strukturze wurcytu (podrozdz. 4.9). Jego wysoka temperatura topnienia (2570 °C), mała reaktywność i doskonała przewodność cieplna, która jest największa ze wszystkich tlenków, prowadzą do jego zastosowania jako materiału ogniotrwałego. Jest wysoce toksyczny przy wdychaniu, co prowadzi do przewlekłej berylozy, choroby płuc oraz raka. Problem ten pogarsza jego stosunkowo mała gęstość (3,0 g cm–3), ponieważ cząstki pyłu pozostają w powietrzu przez długi czas, ale BeO jest bezpieczny w wielu zastosowaniach, gdy jest używany jako spiekany monolit. W połączeniu z metalami elektrododatnimi beryl tworzy kompleksowe berylany, takie jak K2BeO2 i La2Be2O5, które zawierają tetraedry BeO4 i są strukturalnie analogiczne do krzemianów. Tlenki pozostałych pierwiastków 2. grupy można otrzymać przez bezpośrednie połączenie pierwiastków (z wyjątkiem Ba, który tworzy nadtlenek), ale częściej otrzymuje się je przez rozkład węglanów:
MCO(s)32MO(s)CO(g)
Wszystkie tlenki pierwiastków od Mg do Ba przyjmują strukturę typu soli kamiennej (podrozdz. 4.9). Ich temperatury topnienia zmniejszają się w dół grupy, ponieważ entalpie sieci maleją wraz ze wzrostem promienia kationu. Tlenek magnezu topi się dopiero w temp. 2852 °C i jest stosowany jako wykładzina ogniotrwała w piecach przemysłowych. Podobnie jak BeO, MgO ma duże przewodnictwo cieplne w połączeniu z małym przewodnictwem elektrycznym. Ta kombinacja właściwości prowadzi do jego zastosowania jako izolatora elektrycznego wokół
elementów grzejnych urządzeń gospodarstwa domowego oraz w kablach elektrycznych.
Tlenek wapnia (w postaci wapna lub wapna palonego) jest stosowany w dużych ilościach w przemyśle stalowym do usuwania P, Si i S. Po podgrzaniu CaO staje się termoluminescencyjny i emituje jasne, białe światło. Tlenek wapnia stosuje się również jako zmiękczacz wody w celu usunięcia jej twardości przez reakcję z rozpuszczalnymi węglanami i wodorowęglanami, w celu utworzenia nierozpuszczalnego CaCO3. Reaguje z wodą, tworząc Ca(OH)2, czasami nazywany wapnem gaszonym, i używany jest do zobojętnienia kwaśnych gleb.
Nadtlenki SrO2 i BaO2 można otrzymać na drodze bezpośredniej reakcji pierwiastków, natomiast nierozpuszczalne nadtlenki Mg i Ca otrzymuje się przez dodanie nadtlenku sodu, Na2O2 do wodnych roztworów tych metali. Wszystkie nadtlenki są silnymi utleniaczami i rozkładają się na tlenki:
MO (s)MO(s) O(g) 2 1 2 2 →
Trwałość termiczna nadtlenków wzrasta w dół grupy wraz ze wzrostem promienia kationu. Zmianę tę wyjaśnia się, biorąc pod uwagę entalpie sieci nadtlenku i tlenku oraz ich zależność od względnych promieni kationów i anionów. Ponieważ O2– jest mniejszy niż O22–, entalpia sieci tlenku jest większa niż odpowiadającego mu nadtlenku. Różnica między dwiema entalpiami sieci maleje w dół grupy, ponieważ obie wartości zmniejszają się wraz ze wzrostem promienia kationu, a więc tendencja do rozkładu maleje. W związku z tym nadtlenek magnezu, MgO2, jest najmniej trwałym nadtlenkiem i jest stosowany jako źródło tlenu in situ w wielu zastosowaniach, w tym w bioremediacji zanieczyszczonych dróg wodnych. CaO2 ma podobne zastosowania w dezynfekcji wody oraz jako środek wybielający mąkę.
PRZYKŁAD 12.4
Wyjaśnienie trwałości termicznej nadtlenków
Oszacuj różnicę między entalpiami sieci nadtlenku i tlenku Mg oraz Ba, a następnie skomentuj otrzymane wartości.
Odpowiedź Równanie Kapustinskiego [równ. (4.4) i (4.5)] może być użyte do oszacowania entalpii sieci, przy wykorzystaniu promieni jonowych z tab. 12.1 i promieni jonów tlenkowych oraz nadtlenkowych (odpowiednio 126 i 180 pm). Pamiętając, że nadtlenek jest pojedynczym anionem O22–, podstawienie wartości daje
MgO MgO2 BaO BaO2
ΔsiećH /(kJ mol−1) 4037 3315 3147 2684
Różnica /(kJ mol−1) 722 463
Obliczenia te potwierdzają, że różnica między entalpiami sieci tlenku i nadtlenku maleje w dół grupy.
Sprawdź, czy umiesz 12.4 Oblicz entalpie sieci CaO i CaO2 oraz sprawdź, czy powyższy trend został potwierdzony.
