1. Wprowadzenie
2. Krótka historia chromatografii
3. Nauki omiczne (omiki)
4. techniki biochromatograficzne
4 .2 . Chromatografia cienkowarstwowa
5 .1 . Znaczenie przygotowania próbek do analizy
5 .2 . Ogólne zasady przygotowania próbek do analizy
5 .3 . Rodzaje próbek biologicznych
5 .4 . Metody chromatograficzne w przygotowaniu próbek biologicznych
5 .4 .1 . Chromatografia wykluczania
5 4 2 Chromatografia powinowactwa
5 .5 . Wybrane procedury przygotowania próbek biologicznych
5 .5 .1 . Wstępna filtracja próbek biologicznych
5 .5 .2 . Precypitacja białek z próbek biologicznych przed oznaczaniem związków małocząsteczkowych
5 5 3 Przygotowanie próbek do analizy białek w proteomice (procedura SPEED)
5 .5 .4 . Usuwanie fosfolipidów z próbek biologicznych
5 .5 .5 . Procedura ekstrakcyjna QuEChERS
5 .6 . Klasyczne techniki ekstrakcji
5 6 1
5 .6 .2 . Klasyczna ekstrakcja do fazy stałej
.7 . Techniki mikroekstrakcyjne
.7 .1 . Mikroekstrakcja z wykorzystaniem rozpuszczalników
5 .7 .2 . Dyspersyjna mikroekstrakcja ciecz-ciecz
5 7 3 Mikroekstrakcja cieczą wspomagana ciekłą membraną
5 .7 .4 . Mikroekstrakcja z wykorzystaniem sorbentów stałych
5 7 5 Modyfikacje mikroekstrakcji do fazy stałej
5 .8 . Materiały inteligentne do przygotowania próbek do analizy
5 .9 . Trendy w przygotowaniu próbek biologicznych do analizy chromatograficznej
6. Zastosowanie chromatografii gazowej do bioanaliz
7. chromatografy cieczowe do bioanaliz
8. Spektrofotometry optyczne jako detektory w chromatografii cieczowej
9. Spektrometry mas i ruchliwości jonów jako detektory w chromatografii cieczowej
10. Kolumny do chromatografii cieczowej
11. techniki chromatografii cieczowej wykorzystywane w bioanalizie
11 .1 . Chromatografia w odwróconym układzie faz
11 .2 . Chromatografia par jonowych w odwróconym układzie faz, chromatografia par jonowych
11 .3 . Chromatografia oddziaływań hydrofobowych
11 .4 . Chromatografia w normalnym układzie faz
11 .5 . Chromatografia oddziaływań hydrofilowych
11 .6 . Chromatografia jonowa, chromatografia jonowymienna, chromatografia kationowymienna i chromatografia anionowymienna
11 .7 . Chromatografia wykluczania, chromatografia żelowa
11 .8 . Chromatografia powinowactwa
11 .9 . Chromatografia związków chiralnych
11 .10 . Chromatografia micelarna
11 .11 . Chromatografia cienkowarstwowa
12. chromatograficzne oznaczanie aktywności biologicznej substancji
12 .1 . Biomimetyczne układy chromatograficzne
12 2 Chromatograficzne oznaczanie lipofilowości związków chemicznych
12 .3 . Chromatograficzne oznaczanie parametrów farmakokinetycznych substancji
12 .4 . Chromatografia błon komórkowych
12 .5 . Badanie aktywności biologicznej substancji za pomocą chromatografii cienkowarstwowej
Skorowidz
4.2. chromatografia cienkowarstwowa
Chromatografia cienkowarstwowa (ang. thin layer chromatography – TLC) jest niedocenianą techniką chromatografii cieczowej. Jest ona znacznie mniej rozpowszechniona w laboratoriach bioanalitycznych niż chromatografia kolumnowa. Zakres jej zastosowań jest też ogólnie mniejszy. Ma ona jednak bardzo duże znaczenie w badaniach aktywności substancji biologicznie aktywnych, szczególnie pochodzenia roślinnego. Dlatego część niniejszej książki poświęciliśmy chromatografii cienkowarstwowej, mając nadzieję, że wywoła ona takie zainteresowanie, na jakie zasługuje.
4.3. chromatografia gazowa
Chromatografia gazowa (ang. gas chromatography – GC) jest stosowana do analiz substancji małocząsteczkowych, o małej i średniej polarności. Substancje polarne, np. produkty rozkładu trujących związków fosforoorganicznych, i nietrwałe termicznie przeprowadza się w substancje, które można analizować za pomocą chromatografii gazowej. Wykonuje się to w procesie derywatyzacji, przy użyciu odczynników reagujących ilościowo z analitami.
Chromatografia gazowa jest techniką, która znajduje zastosowanie głównie do rozdzielania termicznie trwałych i lotnych składników mieszanin. Umożliwia bardzo dobre rozdzielanie składników mieszanin na podstawie ich różnych właściwości retencyjnych, identyfikację oraz ilościowe oznaczenie różnych rodzajów związków chemicznych. Chromatografia gazowa odgrywa istotną rolę w analizie substancji biologicznie czynnych, choć nie aż tak ważną, jak chromatografia cieczowa.
Za pomocą chromatografii gazowej można analizować metabolity w wydychanym powietrzu. Przyrządy stosowane do takiej analizy są często mobilne, zwykle przenośne. Chromatograf jest wyposażony w krótką kolumnę wielokapilarną lub kapilarną, a spektrometr ruchliwości jonów, który stanowi jego część, jest przyrządem małym i lekkim. Dlatego takie przyrządy mogą być wykorzystywane w szpitalach, przy łóżkach pacjentów. Informacje analityczne uzyskuje się w ciągu kilku minut. Chromatografy gazowe wykorzystywane w bioanalizach w znacznej większości są łączone ze spektrometrami mas. Gdy jonizację w takich przyrządach wykonuje się za pomocą jonizacji elektronowej z energią 70 eV, to otrzymywane widma masowe można porównywać z widmami wielu tysięcy wzorców dostępnymi w bazach danych. Są to np. bazy CAS, PubChem, ChemSpider, Spectronaut.
4.4.
chromatografia preparatywna
Biochromatografia jest przede wszystkim metodą analizy, ale w przypadku chromatografii cieczowej może też mieć zastosowanie półpreparatywne i preparatywne. Polega ona na wydzieleniu z mieszaniny, w ilościach gramowych do kilogramowych, czystej substancji lub substancji zawierającej niewielką ilość zanieczyszczeń. Chromatografię w skali półpreparatywnej i preparatywnej wykonuje się w laboratoriach odpowiednio w celach badawczych i użytkowych. W pierwszym przypadku, w kolumnowej chromatografii cieczowej stosowane są kolumny o średnicach 8–10 mm wypełnione cząstkami fazy stacjonarnej o wielkości 5–10 µm. W drugim przypadku średnica kolumn wynosi co najmniej 20 mm, a wielkość cząstek wypełnienia 10–25 µm. Chromatografia preparatywna może być realizowana w skali przemysłowej w zakładach przemysłu biofarmaceutycznego, biotechnologicznego, biochemicznego i kosmetycznego. W tych zastosowaniach kolumny mogą mieć średnicę kilkudziesięciu centymetrów, np. 80 cm, i wysokość np. 2 m.
Rozdzielanie półpreparatywne jest czasem elementem przygotowania próbki do analizy lub do innych badań. Rozdzielanie w skali preparatywnej wykonuje się przy zastosowaniu chromatografów preparatywnych. Cieczowe chromatografy preparatywne, np. Nexera Prep, oprócz właściwej funkcji rozdzielania mają funkcje kontroli czystości otrzymywanych preparatów oraz ich zatężania. Za pomocą wysokosprawnej chromatografii preparatywnej otrzymuje się białka, w tym enzymy, polisacharydy, fosfolipidy, oligonukleotydy, i inne biosubstancje.
Do otrzymywania biosubstancji w dużych ilościach, w krótkim czasie i niekonieczne o dużej czystości, wykorzystuje się chromatografię nazywaną po angielsku flash. Często służy ona do pozbycia się zanieczyszczeń jakiegoś preparatu, a nie do rozdzielenia wszystkich składników mieszaniny. Szybkość rozdzielania w tej technice chromatograficznej jest związana z wielkością cząstek fazy stacjonarnej, która może wynosić 40–60 µm. Nie wszystkie są przy tym kuliste. Kolumny do chromatografii flash są zwykle wykonane z tworzywa sztucznego i mają średnice 40–80 mm. Przepływ fazy ruchomej może wynosić do 250 mL/min pod ciśnieniem kilkudziesięciu barów. Rozdzielenie składników mieszanin i czystość otrzymywanych preparatów nie są tak dobre jak w chromatografii preparatywnej, ale w wielu przypadkach zupełnie wystarczające. W chromatografii flash wykorzystuje się często mechanizm powinowactwa do wydzielania oczyszczonych biozwiązków. Na rycinie 4.4 pokazano kolumny do chromatografii flash
Cholesterol
Biwarstwa fosfolipidowa
Fosfolipid:
Fosfatydylocholina
Fosfatydyloetanoloamina
S ngomielina
Monowarstwa fosfolipidowa
r Yc. 12.1. Biomimetyczne fazy stacjonarne zbudowane ze składników błon komórkowych
Fazy stacjonarne zbudowane z fragmentów rzeczywistych błon komórkowych zawierających receptory błonowe (ang. cell membrane stationary phase – CMSP) są opisane w rozdziale 12.4.
Dużą rolę w aktywności farmakologicznej substancji odgrywa jej działanie z białkami. Wiązanie leku z białkami wpływa na objętość jego dystrybucji, na jego absorpcję i czas działania. Dlatego jedną z grup biomimetycznych faz stacjonarnych stanowią fazy z immobilizowanymi białkami. Najpopularniejszymi białkowymi fazami stacjonarnymi są fazy stacjonarne z immobilizowanymi albuminami ludzkimi – HSA i bydlęcymi – BSA oraz globulinami. W takich fazach stacjonarnych białka zachowują swoje najważniejsze właściwości, w tym właściwości sorpcyjne, które decydują o oddziaływaniu substancji aktywnych biologicznie z białkami. Podczas stosowania kolumn z immobilizowanymi białkami należy sprawdzić, czy w czasie prowadzenia eksperymentu nie doszło do dezaktywacji białek. Na przykład podczas pracy z kolumną HSA zaleca się przed każdym eksperymentem wstrzykiwanie racemicznej mieszaniny warfaryny w celu sprawdzenia dostępności głównego miejsca wiązania HSA. Jeżeli racematy się rozdzielają, oznacza to, że miejsca wiązania warfaryny są aktywne.
Fazy ruchome w biomimetycznych układach chromatograficznych Skład faz ruchomych w biomimetycznych układach chromatograficznych zależy od rodzaju fazy stacjonarnej oraz właściwości badanych substancji Należy jednak przy ich wyborze brać również pod uwagę możliwie najlepsze odwzorowanie środowiska działania substancji.
Chromatografia z fazami stacjonarnymi C18, IAM i cholesterolowymi jest chromatografią w odwróconym układzie faz. Fazami ruchomymi w tych układach są mieszaniny wodno-organiczne. W badaniach aktywności biologicznej substancji należy uwzględniać to, że „wodna” część fazy ruchomej ma odzwierciedlać fizjologiczne warunki działania leku. Dlatego w badaniach aktywności biologicznej substancji często używa się faz ruchomych, w których woda zastępowana jest roztworem buforowym o fizjologicznym pH osocza – 7,4. Jeśli chromatograficznie ma być badana dystrybucja lub absorpcja substancji w konkretnej tkance, należy uwzględnić pH tej tkanki. Zamiast wody można stosować roztwór symulujący skład osocza krwi – SBF (ang. Simulated Body Fluid).
W układach chromatograficznych z fazami biomimetycznymi RPC stosowane są najczęściej następujące fazy ruchome:
• woda – modyfikator organiczny,
• bufor (pH 7,4) – modyfikator organiczny,
• SBF – modyfikator organiczny.
Jeżeli fazy stałe zawierają immobilizowane białka lub błony komórkowe (rozdz. 12.4), należy w miarę możliwości stosować fazy ruchome symulujące środowisko działania substancji oraz takie, które nie powodują degradacji biocząsteczek. Szczególnym rodzajem faz ruchomych w układach biomimetycznych są micelarne fazy ruchome (rozdz. 11.10). Są one wodnymi roztworami surfaktantów powyżej krytycznego stężenia micelizacji. W takim roztworze oprócz monomerów surfaktantu znajdują się micele, które swoją strukturą przypominają błony komórkowe (ryc. 12.2).
Błona komórkowa Micela r Yc. 12.2. Schemat błony komórkowej i miceli
Do faz ruchomych w chromatografii micelarnej można używać różnych surfaktantów – kationowych, anionowych oraz obojętnych. Na podstawie znajomości budowy błon komórkowych oraz składu płynów fizjologicznych stwierdzono, że najlepszym modelowym micelarnym układem biomimetycznym jest układ z niejonowym surfaktantem – eterem laurynowym polioksyetylenu (BRIJ 35) – ryc. 12.3.
Komórk i, tkanki, bakterie...
r Yc. 5.4. Schemat usuwania białek w procedurze SPEED
Istotą procedury SPEED jest rozpuszczenie badanego materiału, np. tkanek, za pomocą czystego kwasu trifluorooctowego (TFA, pK a = 0,20). Rozpuszczanie trwa kilka minut i prowadzi do otrzymania czystego roztworu. Roztwór ten neutralizuje się słabą zasadą, np. tris(hydroksymetylo)aminometanem (pK a = 8,1). W wyniku tego roztwór lekko mętnieje z powodu wytrącenia się małych cząstek białek. Białka są równocześnie redukowane i alkilowane przy użyciu chloroacetamidu i tris-(2-karboksyetylo)fosfiny. Reakcje te zachodzą w temp. 70–80 °C w ciągu ok. 5 min. Następnie przeprowadza się trawienie białek, które może trwać od 1 godz. do 20 godz. Analizę tak przygotowanej próbki wykonuje się za pomocą LC-MS. Stosując technikę SPEED, zidentyfikowano odpowiednio ~2700 i ~1900 białek w bakteriach Escherichia coli i Staphylococcus aureus. Procedura SPEED jest odtwarzalna, zapewnia mniejsze straty niż starsze procedury, umożliwia szybkie analizowanie próbek i jest skuteczniejsza od procedur, w których wykorzystuje się detergenty i substancje chaotropowe. Jest szczególnie przydatna do analizy złożonych, wieloskładnikowych materiałów biologicznych.
5.5.4. usuwanie fosfolipidów z próbek biologicznych
Fosfolipidy są jednym z głównych składników błon komórkowych otaczających komórki wszystkich żywych organizmów. Dlatego są obecne we wszystkich matrycach próbek biologicznych, włączając serum, osocze i krew całkowitą. Obecność fosfolipidów w analizie małych cząsteczek metodą LC-MS ze względu na koelucję i ewentualną jonizację może powodować efekt supresji jonów, a tym samym wpływać na dokładność analizy.
W większości badań klinicznych i biologicznych przed analizą stosuje się tradycyjne metody wytrącania białek i ekstrakcję ciecz-ciecz. Chociaż metody te są niedrogie i umożliwiają szybkie usuwanie białka, to nie zdają egzaminu w przypadku fosfolipidów. Niedokładnie usunięte fosfolipidy podczas chromatografowania mogą się akumulować w kolumnie analitycznej, a następnie, wymywane strumieniem fazy ruchomej, wpływać na kolejne analizy. Aby uniknąć efektu supresji jonów, można stosować klasyczną technikę SPE, która jest czasochłonna i pracochłonna.
Wiele handlowych produktów jest przeznaczonych do usuwania zarówno białek, jak i fosfolipidów. Są wśród nich płytki i kolumienki działające w technologii HybridSPE®. Technologia ta jest prosta, szybka i łatwa w wykonaniu. Podstawą oddzielenia fosfolipidów od analizowanych składników jest mechanizm hydrofobowej retencji. Problem pojawia się, jeżeli badany analit jest również hydrofobowy, ponieważ będzie także zatrzymywany z hydrofobowymi fosfolipidami. W efekcie spada odzysk analitu i następuje pogorszenie wyników analizy. Do całkowitego usuwania białek i fosfolipidów służy HybridSPE®Phospholipid Technology. Technologia ta polega na zatrzymywaniu tych substancji na sorbentach krzemionkowych modyfikowanych jonami cyrkonu (ryc. 5.5). Substancje hydrofobowe nie są zatrzymywane na tych sorbentach. Atom cyrkonu oddziałuje z grupą fosforanową fosfolipidów, zachowując się jak kwas Lewisa. Pozostaje natomiast nieaktywny w stosunku do dużej grupy związków zasadowych, neutralnych i kwasowych. Umożliwia to zachowanie w próbce nawet bardzo hydrofobowych analitów, takich jak witaminy, które często są zatrzymywane razem z fosfolipidami.
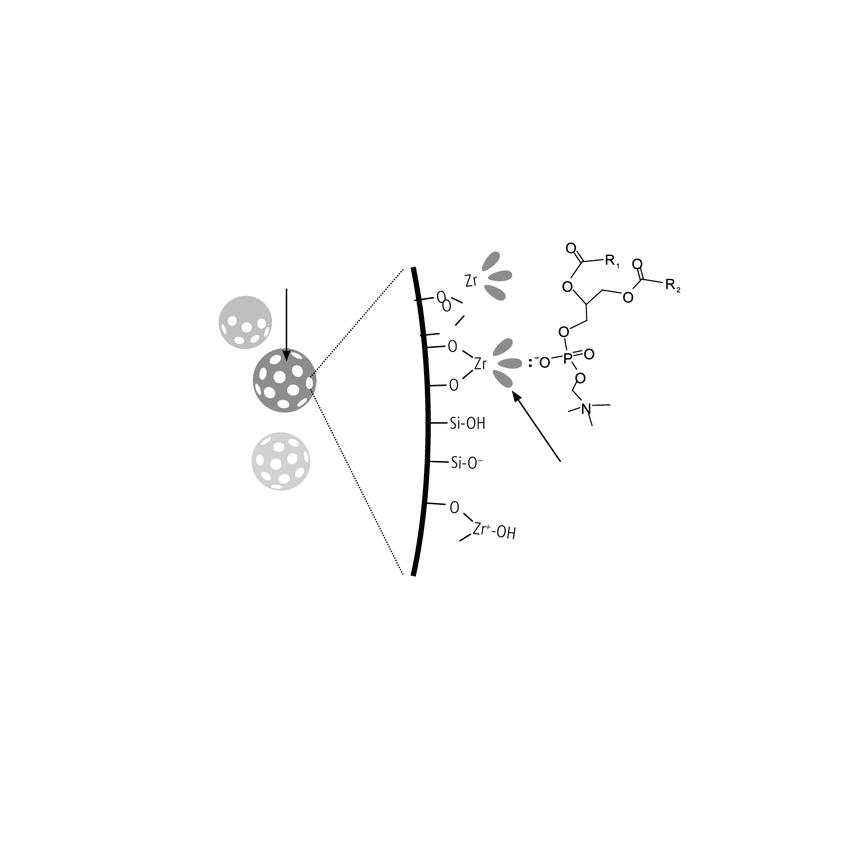
r Yc. 5.5. Mechanizm selektywnego oddziaływania jonów cyrkonu, osadzonych na żelu krzemionkowym, z fosfolipidami
Na przykłado analizy leków i ich metabolitów w technologii HybridSPE®Phospholipid stosuje się zestaw 96-dołkowej płytki i 96 pipet. Na płytkę dodaje się


