dr
n. med. Katarzyna
Holcman
prof. dr hab. n. med. Magdalena Kostkiewicz


dr
n. med. Katarzyna
Holcman
prof. dr hab. n. med. Magdalena Kostkiewicz

Copyright © 2025 by hematoonkologia.pl
Wszelkie prawa zastrzeżone. Broszura jest chroniona prawem autorskim. Przedruk i reprodukcja w jakiejkolwiek postaci całości lub części broszury bez pisemnej zgody wydawcy są zabronione.
Procedury i praktyki przedstawione w tej broszurze powinny być stosowane zgodnie z zasadami i standardami obowiązującymi w określonej sytuacji. Dołożono wszelkich starań, aby potwierdzić dokładność zamieszczonych tu informacji oraz aby rzetelnie przedstawić ogólnie przyjęte zasady praktyki klinicznej. Zarówno autor, jak i wydawca nie ponoszą żadnej odpowiedzialności za pominięcia, niedopatrzenia ani za efekty wykorzystania prezentowanego tu materiału. Broszura nie udziela żadnych gwarancji na wykorzystanie zawartych w niej informacji.
Wydawca: eorta.pl
Korekta: Justyna Łysiak
Projekt graficzny, DTP: Aleksandra Rodak-Jachymek
Drukarnia: Printika
Publikacja powstała dzięki wsparciu finansowemu firmy




dr n. med. Katarzyna Holcman, FESC
Przewodnicząca Zarządu Sekcji Kardiologii Nuklearnej
Polskiego Towarzystwa Kardiologicznego
Klinika Chorób Serca i Naczyń
Uniwersytet Jagielloński - Collegium Medicum
Zakład Medycyny Nuklearnej
Krakowski Szpital Specjalistyczny im. św. Jana Pawła II
ul. Prądnicka 80, 31- 202 Kraków
prof. dr hab. n. med. Magdalena Kostkiewicz
Założycielka Sekcji Kardiologii Nuklearnej
Polskiego Towarzystwa Kardiologicznego
Klinika Chorób Serca i Naczyń
Uniwersytet Jagielloński - Collegium Medicum
Zakład Medycyny Nuklearnej
Krakowski Szpital Specjalistyczny im. św. Jana Pawła II
ul. Prądnicka 80, 31- 202 Kraków
Pod patronatem Sekcji Kardiologii Nuklearnej
Polskiego Towarzystwa Kardiologicznego
https://kardio.nuklearna.pl/

Amyloidoza serca typu transtyretynowego (ATTR) jest chorobą postępującą, prowadzącą do niewydolności serca, zaburzeń rytmu i zgonu. Przez lata pozostawała rozpoznawana zbyt późno lub wcale – ze względu na niespecyficzne objawy i brak dostępu do nieinwazyjnych metod diagnostycznych.
Przełomem w rozpoznaniu ATTR była scyntygrafia z użyciem znaczników fosfonianowych, która umożliwia wykrycie złogów amyloidu bez konieczności biopsji – pod warunkiem wykluczenia amyloidozy łańcuchów lekkich (AL). W badaniu wykorzystywane są radioizotop Technetu 99m oraz znaczniki klasycznie używane w badaniu kośćca: kwas 3,3-difosfono-1,2-propanodikarboksylowy (DPD), kwas metylenodifosfoniowy (HMDP), pirofosforan (PYP). Ta metoda całkowicie zmieniła podejście do diagnostyki, dając pacjentom realną szansę na szybsze rozpoznanie i wdrożenie skutecznego leczenia. Dzięki scyntygrafii możliwe jest nie tylko wykrywanie choroby na wczesnym etapie, ale też różnicowanie jej podtypów, co ma bezpośrednie przełożenie na wybór terapii. Scyntygrafia stała się nieodłącznym elementem współczesnego algorytmu diagnostycznego ATTR – zgodnie z wytycznymi
Polskiego Towarzystwa Kardiologicznego (PTK), Polskiego Towarzystwa Medycyny Nuklearnej (PTMN),
Europejskiego Towarzystwa Kardiologicznego (ESC) i Europejskiego Towarzystwa Medycyny Nuklearnej (EANM). Badania populacyjne pokazują, że częstość
ATTR w populacji >75 r.ż. z niewydolnością serca i zachowaną frakcją wyrzutową (HFpEF) może sięgać
10-15%. Podobne odsetki obserwuje się u pacjentów z ciężką stenozą aortalną lub niejasną hipertrofią lewej komory, co sugeruje znacznie wyższą częstość występowania w populacji niż przypuszczano.
Amyloidoza to grupa chorób naciekowych, w których dochodzi do pozakomórkowego odkładania się nierozpuszczalnych złogów białkowych (amyloidu) w tkankach i narządach. W przypadku zajęcia serca mówimy o kardiomiopatii amyloidowej (CA) – postaci szczególnie groźnej ze względu na progresywny charakter i wpływ na funkcję skurczową i rozkurczową
komór. Wyróżniamy kilka podtypów CA, m.in. AL, ATTR dziedziczną (ATTRv) oraz ATTR dziką (ATTRwt).
Każdy z nich charakteryzuje się odmienną etiologią, przebiegiem klinicznym oraz rokowaniem. Zrozumienie różnic pomiędzy tymi postaciami jest kluczowe dla właściwego prowadzenia pacjenta i wyboru odpowiedniej strategii diagnostyczno-terapeutycznej.

Tabela 1. Główne typy amyloidozy serca
Typ Mechanizm Cechy kliniczne
AL Produkcja patologicznych immunoglobulin (szpiczak)
ATTRv Patogenny wariant genu TTR (np. Val30Met, Thr60Ala)
ATTRwt Depozyty TTR związane z wiekiem
Znaczenie dla diagnostyki
Szybki przebieg, zajęcie wielu narządów i nerek Wymaga pilnego wykluczenia – inne podejście terapeutyczne
Objawy neurologiczne, dysfunkcja autonomiczna Wymaga badań genetycznych, diagnostyka rodziny
Mężczyźni >70 r.ż., zespół cieśni nadgarstka
AL – amyloidoza łańcuchów lekkich;
Najczęstszy typ – typowy kandydat do scyntygrafii izotopowej
ATTRv – dziedziczna amyloidoza transtyretynowa;
ATTRwt – amyloidoza transtyretynowa typu dzikiego; TTR – transtyretyna.

Scyntygrafia serca z użyciem znaczników fosfonianowych [99mTc] Tc -PYP/DPD/HMDP jest unikalnym badaniem umożliwiającym bezpośrednią wizualizację CA. Właściwe wykorzystanie tej techniki w codziennej praktyce klinicznej zwiększa szansę na wczesne rozpoznanie choroby i poprawia rokowanie pacjentów.
Dzięki niej możliwe są:
• Nieinwazyjne potwierdzenie ATTR – bez potrzeby biopsji endomiokardialnej, pod warunkiem wykluczenia AL.
• Ocena stopnia zaawansowania (klasyfikacja Perugini).
• Wczesna diagnostyka chorych z rodzin.
• Monitorowanie skuteczności leczenia.
Tabela 2. Najczęściej stosowane znaczniki rekomendowane przez EANM i PTK
Radioznacznik Zastosowanie
[99mTc]Tc - PYP Główny radioznacznik w USA
[99mTc]Tc - DPD Europa, w tym Polska
[99mTc]Tc - HMDP Dostępny na całym świecie
DPD – kwas 3,3-difosfono-1,2-propanodikarboksylowy; HMDP – difosfonian hydroksymetylenu; PYP – pirofosforan; 99mTc – technet 99m.
Tabela 3. Porównanie metod obrazowych
Echokardiografia
Rezonans magnetyczny serca
Szeroko dostępna, możliwa ocena wstępna i referencyjna metoda do monitorowania leczenia Mała swoistość
Dokładna ocena morfologii i tkankowa, ocena objętości pozakomórkowej, ocena wstępna i do monitorowania leczenia
Ograniczona dostępność, przeciwwska zania
Scyntygrafia Wysoka swoistość dla ATTRv oraz ATTRwt, nieinwazyjna, ocena wstępna Wymaga wykluczenia AL

SPECT, SPECT/CT
PET/CT
Wartość prognostyczna, potencjalne zastosowanie oceny ilościowej w odpowiedzi na leczenie
Swoistość do podtypów amyloidozy, potencjalne zastosowanie oceny ilościowej w odpowiedzi na leczenie
Biopsja Potwierdzenie histologiczne
AL – amyloidoza łańcuchów lekkich;
Ograniczona dostępność
Ograniczona dostępność
Inwazyjna, ograniczona dostępność
ATTRv – dziedziczna amyloidoza transtyretynowa;
ATTRwt – amyloidoza transtyretynowa typu dzikiego;
DPD – kwas 3,3-difosfono-1,2-propanodikarboksylowy;
HMDP – difosfonian hydroksymetylenu;
PET – badanie pozytronowej tomografii emisyjne;

PYP – pirofosforan;
SPECT – tomografia emisyjna pojedynczego fotonu; 99mTc – technet 99m.
Rozpoznanie ATTR powinno być brane pod uwagę u pacjentów z objawami niewydolności serca, zwłaszcza
HFpEF czy kardiomiopatii restrykcyjnej i przerostowej, u których występują dodatkowe cechy fenotypowe.
Wskazaniem do badania są także nieprawidłowości w obrazowaniu echokardiograficznym lub rezonansie magnetycznym serca, sugerujące infiltracyjny charakter kardiomiopatii. Wczesne skierowanie na badanie może istotnie skrócić czas do rozpoznania i wdrożenia terapii.


Wskazania kliniczne:
• W celu rozpoznania u pacjentów z podejrzeniem CA związanej z ATTR.
• Diagnostyka różnicowa fenokopii kardiomiopatii przerostowej i restrykcyjnej.
• Niewyjaśniona hipertrofia lewej komory (IVSd ≥12 mm) z czerwonymi flagami (np. bez nadciśnienia tętniczego, zespół cieśni nadgarstka, zwężenie kanału kręgowego, zerwania ścięgien, pacjenci po TAVI bez poprawy hemodynamicznej, dysfunkcja autonomiczna, polineuropatia obwodowa, białkomocz, zasinienie skóry, nieprawidłowości w echokardiogragrafii i rezonansie magnetycznym).
• Diagnostyka ATTR CA w populacji nosicieli ATTRv.
Rycina 1. Algorytm diagnostyki amyloidozy serca (w oparciu o [3, 7])
prezentacje kliniczne: przerost mięśnia sercowego o nieustalonej przyczynie, kardiomiopatia przerostowa, kardiomiopatia restrykcyjna, objaw, apical sparing, zespół cieśni nadgarstka, dysfunkcja autonomiczna, zerwanie mięśnia dwugłowego ramienia, polineuropatia, dodatni wywiad rodzinny
badania diagnostyczne: EKG, badanie echokardiograficzne/rezonans magnetyczny serca
ocena obecności białka monoklonalnego w krwi i moczu badanie scyntygraficzne z 99mTcPYP/DPD/HMDP
scyntygrafia - stopień 2-3 oraz wolne
łańcuchy lekkie - brak
scyntygrafia
stopień 1 lub scyntygrafia stopień 2-3 oraz wolne
łańcuchy lekkie - obecne
scyntygrafia - stopień 0 oraz wolne
łańcuchy lekkie - brak
scyntygrafia - stopień 0 oraz wolne
łańcuchy lekkie - obecne
badanie genetyczne ATTRv vs. ATTRwt
ocena specjalistyczna hematologiczna/ onkologiczna, ocena histopatologiczna, rezonans magnetyczny
rezonans magnetyczny w wątpliwych przypadkach
ATTR
ATTR vs. AL. vs. ATTR + MGUS
ATTR oraz AL mało prawdopodobne
ocena histopatologiczna rezonans magnetyczny
AL
AL – amyloidoza łańcuchów lekkich;
ATTR – amyloidoza transtyretynowa;
ATTRv – dziedziczna amyloidoza transtyretynowa;
ATTRwt – amyloidoza transtyretynowa typu dzikiego;
EKG – elektrokardiogram;
MGUS – gammapatia monolonalna;
DPD – kwas 3,3-difosfono-1,2-propanodikarboksylowy; HMDP – difosfonian hydroksymetylenu;
PYP – pirofosforan; 99mTc – technet 99m.


Aby uzyskać wiarygodny wynik, konieczne jest przestrzeganie standardowego protokołu badania zgodnego z rekomendacjami PTK, PTMN, EANM i ESC. Dotyczy to zarówno rodzaju znacznika radiofarmaceutycznego, jak i czasu oraz sposobu akwizycji obrazów. Właściwe przygotowanie pacjenta, odpowiedni czas od podania znacznika do rozpoczęcia obrazowania, a także wykorzystanie technik, takich jak tomografia emisyjna pojedynczego fotonu (SPECT) czy SPECT/CT mają bezpośredni wpływ na jakość i interpretację wyników.
1. Znacznik radiofarmaceutyczny:
- [99mTc]Tc - DPD (preferowany w Europie), - Alternatywnie: [99mTc]Tc HMDP lub [99mTc]Tc PYP.
2. Przygotowanie pacjenta:
- Brak szczególnych zaleceń dietetycznych lub farmakologicznych, - Wykluczenie obecności monoklonalnego białka (FLC, immunofiksacja) powinno być równoległe lub wcześniejsze.
3. Podanie radioznacznika: - Aktywność: 370–740 MBq, - Droga podania: dożylna.
4. Akwizycja obrazów: - Czas: 2-3 godziny po iniekcji, - Obrazowanie planarne + obowiązkowo SPECT (ew. SPECT/CT).
5. Ocena Perugini.
6. Uzupełnieniem jest analiza półilościowa: - Wskaźnik serce/tło (Heart-to-Contralateral ratio – H/CL): obliczany na obrazach planarnych, stosunek aktywności w lewej komorze serca do aktywności w symetrycznym obszarze prawej klatki piersiowej.
Rycina 2. Scyntygrafia z zastosowaniem znacznika [99mTc]Tc DPD przykłady wychwytu znacznika wg 4-stopniowej skali Perugini

Materiał Zakładu Medycyny Nuklearnej Krakowskiego Szpitala Specjalistycznego im. św. Jana Pawła II. 1 2 3 4
Ocena scyntygrafii w kierunku ATTR opiera się na porównaniu intensywności wychwytu znacznika przez mięsień sercowy w stosunku do kości. W tym celu stosuje się klasyfikację Perugini, która dzieli wyniki na cztery stopnie od 0 do 3. Stopień 0 oznacza brak wychwytu w sercu i prawidłowy wychwyt w kościach – jest to wynik ujemny. Stopień 1 sugeruje minimalny wychwyt sercowy, mniejszy niż kostny – wynik wątpliwy. Stopień 2 i 3 oznaczają wyraźny wychwyt znacznika w mięśniu sercowym i są uważane za wyniki pozytywne, charakterystyczne dla ATTR. Przy jednoczesnym wykluczeniu białka monoklonalnego można wówczas postawić rozpoznanie bez konieczności wykonywania biopsji. W praktyce klinicznej szczególną uwagę należy zwrócić na przypadki graniczne – interpretacja powinna być zawsze wsparta obrazami SPECT i doświadczeniem zespołu medycyny nuklearnej.

Tabela 4. Klasyfikacja Perugini
Stopień Obraz
0 Brak wychwytu w sercu, prawidłowy wychwyt kostny
1 Słaby wychwyt sercowy, mniejszy niż kostny
2
3
Wychwyt sercowy równy kostnemu
Wychwyt sercowy wyraźnie większy niż kostny / brak wychwytu w kościach
ATTR – amyloidoza transtyretynowa.
Interpretacja
Ujemny
Wątpliwy / Niespecyficzny
Pozytywny – możliwe ATTR
Pozytywny – ATTR bardzo prawdopodobna
Tabela 5. Ocena i interpretacja wskaźnika H/CL
Ocena współczynnika wychwytu serca/przeciwległego płuca (H/CL) (ułamek średniej liczby w obszarze zainteresowania serca (ROI) w stosunku do średniej liczby w obszarze zainteresowania płuca przeciwległego)
H/CL ≥1.5 Pozytywny (z potwierdzeniem SPECT)
H/CL 1-1.5 Neutralny
H/L<1 Negatywny
H/CL – współczynnik wychwytu serce/przeciwległe płuco; ROI – obszar zainteresowania; SPECT – tomografia emisyjna pojedynczego fotonu.

Materiał Zakładu Medycyny Nuklearnej Krakowskiego Szpitala Specjalistycznego im. św. Jana Pawła II.

Scyntygrafia z użyciem znaczników fosfonianowych cechuje się wysoką swoistością dla ATTR, ale jej prawidłowa interpretacja wymaga znajomości potencjalnych pułapek, które mogą prowadzić do nieprawidłowej interpretacji wyników. Najczęstsze błędy to niewłaściwe przygotowanie pacjenta, nieprawidłowe ustawienia aparatu, zbyt wczesna akwizycja obrazów lub brak wykonania SPECT.
1. Obecność AL:
- Pacjenci z AL mogą wykazywać dodatni wychwyt (Perugini 1-3),
- Zawsze należy wykonać wykluczenie AL – FLC i immunofiksację surowicy i moczu,
2. Nieprawidłowy protokół obrazowania:
- Zbyt wczesna lub późna akwizycja,
- Brak SPECT → trudności w lokalizacji wychwytu,
- Zalecane stosowanie standaryzowanych szablonów opisu.
3. Artefakty i fizjologiczny wychwyt:
- Fałszywa interpretacja bez potwierdzenia w SPECT, różnicowanie z wychwytem krwi, - Wyniki fałszywie dodatnie po zawale mięśnia sercowego i w przypadku kardiotoksyczności.
4. Różna awidoność radioznacnzików:
- Wyniki fałszywie ujemne w rzadkich postaciach genetycznych.
Rycina 4. Ocena techniką SPECT/CT (badanie po korekcji pochłaniania) – widoczne zaawansowane lewokomorowe zmiany chorobowe oraz objęcie przez proces chorobowy wolnej ściany prawej komory
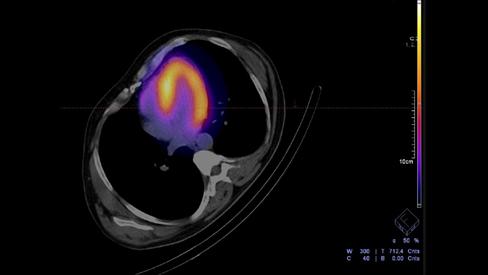
Materiał Zakładu Medycyny Nuklearnej Krakowskiego Szpitala
Specjalistycznego im. św. Jana Pawła II.
Wczesne rozpoznanie amyloidozy daje szansę na skuteczne leczenie i poprawę przeżycia.
Znaczenie scyntygrafii ATTR:
- Rozpoznanie na etapie bezobjawowym, w populacji z cechami ryzyka oraz rodzinach pacjentów z ATTRv,
- Uniknięcie biopsji w większości przypadków (Perugini 2-3 + brak białka monoklonalnego),
- Rozpoczęcie terapii i kwalifikacja do Programu Lekowego NFZ,
- Diagnostyka rodzinna i genetyczna.
Zastosowania w populacjach klinicznych:
- HFpEF u osób starszych,
- Po TAVI bez poprawy,
- Przerost lewej komory o niejasnej etiologii,
- Polineuropatia z objawami sercowymi,
- Fenotyp kardiomiopatii restrykcyjnej z czerwonymi flagami,
- Osoby z dodatnim wywiadem rodzinnym w kierunku ATTRv.
Scyntygrafia jest metodą, która zrewolucjonizowała podejście do diagnostyki ATTR. Umożliwia wczesne, nieinwazyjne i skuteczne rozpoznanie choroby, która jeszcze niedawno pozostawała niewykrywalna aż do późnych, nieodwracalnych stadiów. Dzięki niej możliwe jest włączenie terapii poprawiającej przeżycie pacjentów i kwalifikacja do programu lekowego. Aby w pełni wykorzystać potencjał tej techniki, niezwykle istotne jest przestrzeganie wytycznych oraz zastosowanie właściwego protokołu obrazowania. Włączenie scyntygrafii do codziennej praktyki diagnostycznej pozwala zmienić historię tej choroby i poprawić rokowania.
Źródła, w tym najważniejsze wytyczne PTK, PTMN, ESC, EANM:
1. Perugini E, Guidalotti PL, Salvi F, et al. Noninvasive etiologic diagnosis of cardiac amyloidosis using 99mTc-3,3-diphospho¬no-1,2-propanodicarboxylic acid scintigraphy. J Am Coll Cardiol. 2005; 46(6): 1076-1084.
2. Gillmore JD, Maurer MS, Falk RH, et al. Nonbiopsy diagnosis of cardiac transthyretin amyloidosis. Circulation 2016; 133(24): 2404-2412.

3. Garcia-Pavia P, Rapezzi C, Adler Y, et al. Diagnosis and treatment of cardiac amyloidosis: a position statement of the ESC Working Group on Myocardial and Pericardial Diseases. Eur Heart J 2021;42:1554-1568.
4. Arbelo E, Protonotarios A, Gimeno JR, et al. 2023 ESC Guidelines for the management of cardiomyopathies. Eur Heart J 2023;44:3503-3626.
5. Dorbala S, Ando Y, Bokhari Set al. ASNC/AHA/ASE/ EANM/HFSA/ISA/SCMR/SNMMI expert consensus recommendations for multimodality imaging in cardiac amyloidosis: Part 2 of 2-Diagnostic criteria and appropriate utilization. J Nucl Cardiol. 2020;27:659-673.
6. Holcman K, Dziuk M, Grzybowski J, Teresinska A, Malkowski B, Jedrzejuk D, Brockhuis B, Czepczynski R, Tomkiewicz-Pajak L, Kostkiewicz M. The scintigraphic diagnosis of cardiac amyloidosis. An expert opinion endorsed by the Section of Nuclear Medicine of the Polish Cardiac Society and the Polish Nuclear Medicine Society. Nucl Med Rev Cent East Eur. 2022;25(2):142-147.
7. Grzybowski J, Podolec P, Holcman K, Gawor-Prokopczyk M, Jankowska E, Kostkiewicz M, Dąbrowska-Kugacka A, Lipowska M, Mazurkiewicz Ł, Rajtar-Salwa R, Rubiś P, Straburzyńska-Migaj E, Szczygieł J, Mitkowski P. Diagnosis and treatment of transthyretin amyloidosis cardiomyopathy: A position statement of the Polish Cardiac Society. Kardiol Pol. 2023;81(11):1167-1185. doi: 10.33963/v.kp.97648.
Epub 2023 Sep 28.




Sekcja
Towarzystwa Kardiologicznego