




UnprogramaexclusivodeHealCanada
"Conectando la salud con el conocimiento y la promoción de la causa"

Aspectos destacados de la 66ª Reunión Anual de la ASH:
Leucemia mieloide crónica (LMC)
Mielofibrosis (MF)
Policitemia vera (PV)
Trombocitemia esencial (TE)
Número 5 de febrero de 2025
Bienvenido
El poder de la presencia: ¿Por qué los defensores de los pacientes deben asistir a conferencias como la ASH?
Cuáles son las mejores formas de gestionar la LMC en 2025?
Es mejor tratar la mielofibrosis en 2025?
Policitemia vera: ¡surfeemos la ola!
Alguien ha oído hablar de la ET? ET para la trombocitemia esencial.
Ensayos clínicos y encuestas a pacientes
Alianzas y colaboraciones
Fogonadura
Mi equipo de sangre, mi salud
Visita Mi sangre, Mi Salud.ca o Healcanada.org para descargar este número actual

En este quinto número, nos centraremos en la ASH 2024, la reunión anual de la Sociedad Americana de Hematología. ¿Por qué la ASH? Esta conferencia, creada en 1958, se ha convertido, con el tiempo, en el evento de hematología más completo del mundo. Los datos presentados en esta conferencia influyen en la forma en que los hematólogos y oncólogos abordarán las enfermedades de la sangre Este año se han realizado alrededor de 8000 presentaciones a más de 30 000 hematólogos e investigadores orientados a la hematología.
En este número, nos centraremos en los cánceres mieloides, como la neoplasia mieloproliferativa y la leucemia mieloide crónica. La investigación y el desarrollo clínico son esenciales para los pacientes. Sin embargo, nuestra misión es analizar lo que usted puede hacer hoy para mejorar su vida Por eso, en estas páginas, encontrará algunas perlas que encontramos en ASH y que puede aplicar ahora a su vida y tomar el control de su camino. Esté atento a los números excepcionales adicionales de ASH 2024 sobre otros trastornos sanguíneos que se publicarán próximamente.
Con esta revista, nuestro objetivo es cumplir con la misión de Heal Canada de empoderar a los pacientes para que tengan acceso a servicios mejores y más equitativos Estamos profundamente agradecidos a nuestros lectores por su continuo interés y apoyo. Su compromiso nos impulsa a producir contenido perspicaz y valioso que fomente la atención médica centrada en el paciente.
¡Gracias por participar en nuestro viaje y bienvenido a este esclarecedor número!
De parte de su dedicado equipo, Brigitte y Cheryl


Cheryl Petruk, MBA B.Mgt. Director ejecutivo y fundador de Heal Canada

Brigitte Leonard, Doctora en Filosofía Director científico de Mi sangre, mi salud Director
Heal Canada es una organización sin fines de lucro registrada en Canadá. sanacanada.org
Descargo de responsabilidad: La revista digital Patient Advocacy ofrece información general y recursos para promover el empoderamiento y la concienciación de los pacientes El contenido no sustituye el asesoramiento o el tratamiento médico profesional Siempre consulte con profesionales de la salud calificados para obtener orientación personalizada sobre su condición o situación médica específica


El poder de la presencia: por qué los defensores de los pacientes debenasistiracongresoscomoeldelaSociedadEstadounidensede Hematología
Conferencias como la Reunión Anual de la Sociedad Estadounidense de Hematología (ASH) son encuentros monumentales donde se revelan los últimos avances en hematología. Para muchos, estos eventos son sinónimo de investigación de vanguardia, terapias innovadoras y la convergencia de las mejores mentes en el campo. Sin embargo, en medio de la densa concentración académica y clínica se esconde un asistente a menudo subestimado pero igualmente vital: el defensor del paciente. La importancia de que los defensores del paciente asistan a estas conferencias se extiende más allá de la representación simbólica; se trata de fomentar una asociación que eleve el impacto de la investigación hematológica y garantice resultados centrados en el paciente.
Este artículo explora por qué los defensores de los pacientes deben ser participantes activos en conferencias como ASH, enfatizando su papel en la comprensión de los ensayos clínicos, la participación en iniciativas de investigación, la identificación de brechas de investigación y la configuración del futuro de la hematología.
Desmitificando los ensayos clínicos
Los defensores de los pacientes actúan como intérpretes del ecosistema de los ensayos clínicos Su posición única, armada con una combinación de experiencia y conocimiento, les permite destilar la intrincada jerga médica y convertirla en relatos con los que se puede identificar a los pacientes En conferencias como “ASH”, los defensores de los pacientes obtienen acceso de primera mano a los últimos avances en ensayos clínicos y a la investigación actual y en curso sobre neoplasias y trastornos hematológicos, lo que les permite:

Educar a sus comunidades sobre nuevos ensayos clínicos, investigaciones y terapias emergentes.
Aliviar los temores y conceptos erróneos en torno a la participación en ensayos. Promover el acceso equitativo abordando las barreras específicas de las poblaciones marginadas.
Ampliar la voz de los pacientes en el diseño de ensayos
Los ensayos clínicos suelen fracasar debido a las bajas tasas de inscripción o retención, problemas que tienen su origen en una falta de conexión entre los diseños de los ensayos y las necesidades reales de los pacientes. Los defensores de los pacientes que asisten a conferencias pueden proporcionar comentarios fundamentales a los investigadores, garantizando que los ensayos se diseñen teniendo en cuenta las consideraciones centradas en el paciente, como:

Conveniencia de los lugares de prueba Manejo de los efectos secundarios en la vida diaria Comunicación clara de posibles beneficios y riesgos
Al fomentar este diálogo, los defensores de los pacientes ayudan a crear ensayos que no solo sean científicamente sólidos sino también amigables para los pacientes, mejorando así la participación y las tasas de éxito
La participación de los pacientes en las iniciativas de investigación en hematología: una necesidad de colaboración
Incluir a los defensores de los pacientes en las iniciativas de investigación en hematología ya no es una opción: es una necesidad. Conferencias como la ASH ofrecen una plataforma para que los defensores de los pacientes interactúen directamente con investigadores, médicos y líderes de la industria, y transmitan que los pacientes son socios, no sujetos pasivos, en el proceso de investigación.


Los defensores como puentes entre las partes interesadas
Los defensores de los pacientes se destacan por tender puentes entre los investigadores y la comunidad de pacientes Su participación garantiza que la perspectiva del paciente se integre en la estructura de las iniciativas de investigación, lo que influye en:
Prioridades de investigación: Los defensores pueden destacar las áreas que más importan a los pacientes, como la calidad de vida y el manejo de los síntomas.
Estrategias de comunicación: Los defensores pueden orientar a los investigadores para comunicar eficazmente sus hallazgos a audiencias no especializadas.
Al asistir a conferencias, los defensores pueden conectarse con investigadores y formuladores de políticas, estableciendo redes de colaboración que priorizan objetivos centrados en el paciente.
Generando confianza en el proceso de investigación
La confianza es un elemento fundamental para el avance de la investigación hematológica. Los defensores de los pacientes son fundamentales para generar confianza gracias a sus vínculos profundos con sus comunidades. Su presencia en congresos como ASH simboliza transparencia y compromiso, y les asegura a los pacientes que sus voces son escuchadas y valoradas en el proceso de investigación.
Identificación de lagunas en la investigación hematológica: la perspectiva del defensor
A pesar de los avances significativos en hematología, persisten brechas, especialmente en la atención de las necesidades de las poblaciones marginadas, las comunidades con enfermedades raras y los resultados terapéuticos no tradicionales Los defensores de los pacientes están en una posición privilegiada para identificar estas brechas y abogar por una investigación inclusiva y exhaustiva
Destacando las necesidades insatisfechas
Los defensores de los pacientes aportan una perspectiva nueva a la conversación sobre investigación Pueden arrojar luz sobre áreas que pueden no ser inmediatamente evidentes para los investigadores, como:
El impacto psicosocial de vivir con enfermedades hematológicas
La toxicidad financiera de los tratamientos y cuidados de larga duración
La falta de datos sobre trastornos hematológicos raros
Los defensores pueden ayudar a dar forma a una agenda de investigación que se alinee con las realidades de los pacientes al generar conciencia sobre estas necesidades insatisfechas

de la diversidad en la investigación
La diversidad en la investigación es fundamental para generar hallazgos que se apliquen a todas las poblaciones de pacientes. Sin embargo, muchos estudios clínicos en hematología sufren de una falta de representación. Los defensores de los pacientes pueden presionar para lograr una mayor inclusión de:

Participantesétnicamentediversos.
Pacientesdeedadavanzadayconcomorbilidades. Participantesdeentornosruralesodebajosingresos.
Su defensa garantiza que los resultados de las investigaciones sean equitativos y reflejen la poblaciónmásampliadepacientes
La defensa del paciente como un socio valioso en la investigación
Para que la hematología avance verdaderamente, el papel de los defensores de los pacientes debe evolucionar desde observadores a socios activos Conferencias como la ASH brindan el entorno perfecto para mostrar el valor de esta colaboración
Impulso de las decisiones políticas y de financiación
Los defensores de los pacientes pueden influir en las decisiones de financiación y políticas al expresar el impacto humano de la investigación hematológica Sus historias y opiniones brindan un argumento convincente para priorizar las iniciativas de investigación que brindan beneficios tangibles a los pacientes
Resultados de investigación en coautoría
Están ganando terreno los modelos colaborativos en los que los pacientes abogan por la coautoría de artículos de investigación y la contribución a presentaciones en congresos Esta práctica reconoce sus contribuciones y garantiza que la perspectiva del paciente se integre en el discurso académico


Creando una cultura de colaboración
La presencia de defensores de los pacientes en las conferencias fomenta una cultura de colaboración. Su participación alienta a los investigadores, médicos y líderes de la industria a considerar a los pacientes como aliados, allanando el camino para innovaciones con impacto científico y social.
Rompiendo barreras: superando desafíos para promover la participación
Si bien la importancia de los defensores de los pacientes en las conferencias es innegable, aún existen barreras para su participación Las limitaciones financieras, la falta de apoyo institucional y la accesibilidad limitada son algunos de los desafíos que deben abordarse



Creación de capacidad
Proporcionar apoyo financiero
Los organizadores y patrocinadores de conferencias deben reconocer el valor de los defensores de los pacientes y brindar apoyo financiero para su asistencia. Las subvenciones para viajes, las tarifas reducidas y los estipendios pueden marcar una diferencia significativa.
Los esfuerzos para mejorar la accesibilidad (como ofrecer opciones de asistencia virtual, ofrecer resúmenes de las presentaciones en lenguaje sencillo y garantizar adaptaciones físicas) son esenciales para que las conferencias sean inclusivas para todos los defensores.
Invertir en programas de capacitación para defensores de pacientes garantiza que estén preparados para contribuir de manera eficaz. Los talleres sobre alfabetización científica, oratoria y habilidades de defensa de los pacientes pueden capacitarlos para maximizar su impacto.
Los defensores de los pacientes que asisten a congresos como el de la Sociedad Estadounidense de Hematología no son meramente simbólicos, sino transformadores. Su participación enriquece el proceso de investigación, cierra brechas de comunicación, identifica necesidades críticas y garantiza que los avances en hematología tengan eco en los pacientes que más importan.
Mientras continuamos ampliando los límites de lo posible en hematología, recordemos que el verdadero progreso solo se logra cuando los pacientes no son solo participantes, sino socios. Juntos, investigadores y defensores pueden construir un futuro en el que los avances hematológicos mejoren las vidas de manera más significativa. Conferencias como la ASH son las etapas donde esta colaboración comienza y prospera.
Para los defensores de los pacientes, asistir a estas conferencias no es solo una oportunidad, sino una responsabilidad hacia sus comunidades y un testimonio del poder de las voces compartidas para impulsar el cambio. Para la comunidad científica, dar la bienvenida y empoderar a estos defensores es un paso hacia un futuro más inclusivo y de mayor impacto en la hematología.



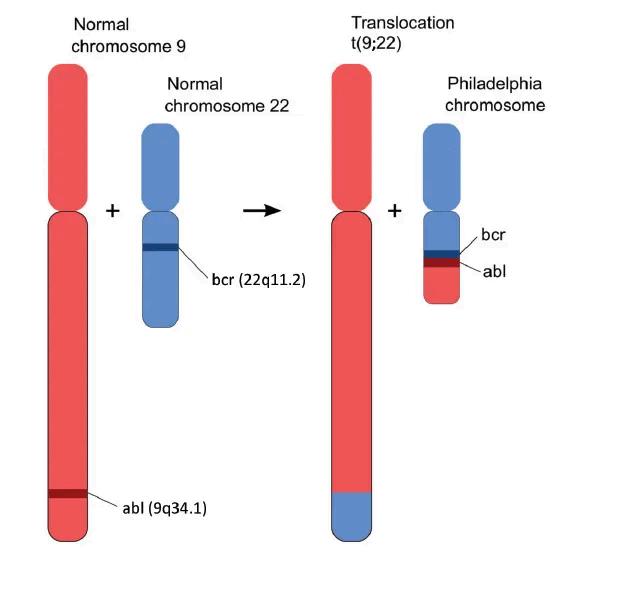
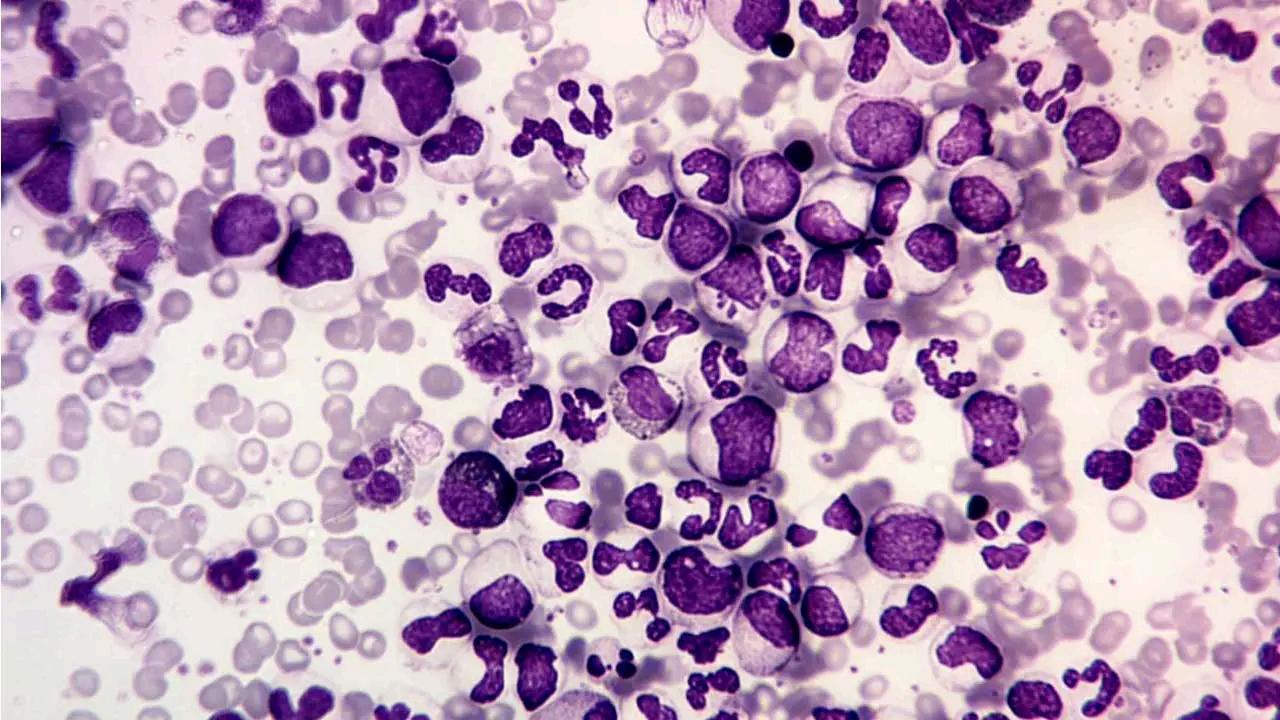
Cuáles son las mejores formas de gestionar la LMC en 2025?
Brigitte Leonard, Doctora en Filosofía
Desde la introducción de Gleevec (imatinib), un tratamiento dirigido a BCR-ABL (TKI, inhibidor de la tirosina quinasa), en el año 2000, el panorama del tratamiento de la LMC (leucemia mieloide crónica) ha evolucionado significativamente. Los pacientes con este cáncer tienen ahora una esperanza de vida casi igual a la de la población general, un marcado contraste con la esperanza de vida de 5 años anterior
Este notable progreso infunde esperanza y optimismo para futuros avances en el tratamiento de la LMC. La mayoría de las agencias regulatorias en todo el mundo han aprobado seis TKI BCR-ABL para el tratamiento de la LMC. Inicialmente se alentó el desarrollo de TKI adicionales porque no todos los pacientes responden adecuadamente al imatinib.
En 2025, los expertos en leucemia mieloide crónica aún se enfrentan a algunos desafíos. Uno de ellos es cómo seleccionar el mejor inhibidor de la tirosina quinasa en un entorno de primera línea El segundo es maximizar la posibilidad de que el paciente alcance una respuesta molecular profunda para intentar una remisión sin tratamiento, el objetivo final de la mayoría de los pacientes.
Vea lo que aprendimos en ASH con respecto a estos desafíos restantes.
La remisión sin tratamiento es el objetivo final del tratamiento.
Al principio, los médicos recetaban TKI a los pacientes con LMC hasta que el paciente dejaba de responder o moría. La comunidad médica pensaba que los TKI no podían curar a los pacientes con LMC como el trasplante.
Menos de una década después de la aprobación del primer TKI (imatinib) y con la sofisticación de la técnica de seguimiento, el equipo del Dr. Mahon

Se demostró que algunos pacientes que alcanzaron niveles indetectables de células cancerosas BCR-ABL podían suspender el tratamiento y permanecer en remisión. El fenómeno se denominó remisión sin tratamiento (TFR). El término cura no era aceptable para la comunidad de expertos en LMC porque aproximadamente la mitad de los pacientes necesitaban reiniciar el tratamiento debido al retorno de las células BCR-ABL a niveles detectables.
Los niveles indetectables de células cancerosas BCR-ABL se denominan a menudo respuesta molecular profunda (DMR). La profundidad de la respuesta es el factor principal para determinar si se puede intentar interrumpir el tratamiento de forma supervisada y permanecer en remisión. Inicialmente, la comunidad médica pensaba que solo una minoría de los pacientes podía intentar la TFR. Estos pacientes debían responder bien a la primera línea de tratamiento, alcanzar la DMR y mantener el tratamiento durante un período prolongado (de 5 a 10 años). Varios estudios clínicos han demostrado que los profesionales sanitarios pueden intentar la TFR de forma segura en pacientes que reciben varias líneas de tratamiento siempre que alcancen la DMR.
En ASH 2024, estudios adicionales del mundo real se suman a la evidencia de que los pacientes pueden intentar la TFR de manera segura en varios contextos:
Pacientes en los que fracasaron varias líneas de tratamiento (1778)
Pacientes con mutaciones adicionales como ASXL1 (3158).
Pacientes en países o ciudades de bajos ingresos (3162)
La interrupción del tratamiento debe realizarse con cautela y bajo estricto seguimiento porque la mitad de los pacientes necesitan reiniciar su tratamiento hasta que puedan intentar intentos adicionales de TFR.
El imatinib no es el mejor inhibidor de la tirosina quinasa para los pacientes que desean intentar alcanzar la tasa de recuperación total. La elección de la primera línea puede afectar significativamente las posibilidades de los pacientes de alcanzar la tasa de recuperación total y la duración de los tratamientos. Menos pacientes alcanzaron la tasa de recuperación total cuando se los trató con imatinib en comparación con los inhibidores de la tirosina quinasa de segunda generación (30 % frente a 50 %). Además, los pacientes tratados con inhibidores de la tirosina quinasa de segunda generación pueden dejar el tratamiento antes porque alcanzan la tasa de recuperación total más rápido. Algunos pacientes que responden de manera temprana pueden dejar el tratamiento después de solo tres años de tratamiento. El asciminib, el inhibidor de la tirosina quinasa más reciente, proporciona una respuesta más rápida y profunda que los inhibidores de la tirosina quinasa de segunda generación.

El mejor tratamiento de primera línea
Independientemente de la posibilidad de TFR, la elección del TKI de primera línea es crucial para los resultados del paciente. Afecta las probabilidades del paciente de adquirir mutaciones adicionales y progresar a formas más agresivas. La progresión es una sentencia de muerte para la mayoría de los pacientes con una tasa de supervivencia inferior a un año.
La mayoría de los pacientes responden bien a todos los TKI; menos del 5% progresará a una fase más agresiva si toman su medicación según lo prescrito. Por lo tanto, la elección de un TKI en lugar de otro no afecta las curvas de supervivencia. Sin embargo, las progresiones tienden a ocurrir rápidamente en los primeros meses de tratamiento. El nivel de respuesta a un TKI a los 3 meses predice las posibilidades de supervivencia de los pacientes, e incluso si se realiza un cambio de TKI, no siempre puede cambiar el destino del paciente.
Cuando analizamos los ensayos de fase III realizados en un entorno de primera línea, vimos una tendencia clara: al menos dos veces más pacientes en el grupo de imatinib (2-5%) progresaron durante el primer año en comparación con los TKI de segunda generación y asciminib (1-2,3%).
Los inhibidores de la tirosina quinasa de primera línea también pueden afectar la respuesta a largo plazo. Los ensayos de fase III en entornos de primera línea mostraron que los pacientes tratados con imatinib desarrollaron más mutaciones que los tratados con inhibidores de la tirosina quinasa de segunda generación. Estas mutaciones adicionales pueden afectar la tasa de éxito de las siguientes líneas de tratamiento.
Según varios registros y estudios en el mundo real de la ASH, el imatinib sigue siendo el TKI más prescrito en el ámbito de primera línea. ¿Por qué los pacientes siguen recibiendo un TKI inferior? El imatinib tiene un perfil de seguridad cardiovascular (CV) percibido como mejor. La comunidad médica recomienda evitar los TKI de segunda generación en pacientes con factores de riesgo CV independientemente de la gravedad de la LMC.
Para evaluar el impacto de estas recomendaciones, el equipo del Dr. Kim en el Princess Margaret Toronto analizó los resultados de la LMC en línea con una puntuación de riesgo cardiovascular validada (puntuación de riesgo de Framingham) (1768). En el momento del diagnóstico, entre el 40 y el 60 % de los pacientes con LMC tienen al menos una afección comórbida y el 30 % presenta factores de riesgo cardiovascular. Los pacientes con factores de riesgo cardiovascular tienden a recibir imatinib más que los pacientes sin riesgo (69,2 % frente a 14,9 %). En este análisis, el tipo de TKI de primera línea es el factor más crítico que influye en los resultados del tratamiento, y los TKI de segunda generación muestran resultados superiores al imatinib. Estos resultados resaltan la necesidad de tratamientos alternativos con mejor eficacia y tolerabilidad.
Es asciminib el indicado?
El asciminib se perfila como una opción prometedora de primera línea para los pacientes con LMC, lo que podría transformar el panorama de los tratamientos. El seguimiento de 96 semanas del estudio ASC4FIRST ha revelado que el asciminib ofrece una tasa de respuesta superior y presenta un perfil de mejor tolerancia en la primera línea en comparación con todos los demás inhibidores de la tirosina quinasa (imatinib y los inhibidores de la tirosina quinasa de segunda generación). Este emocionante avance allana el camino para un tratamiento más eficaz y tolerable de la LMC.

Asciminibproporcionalamejorrespuestamolecularytolerabilidad:
Respuestamolecularprofunda:segúnlosresultadosdelestudio,despuésde3a4añosdetratamiento, 3decada10pacientesseránelegiblesparaintentarTFR,frenteaunosiseiniciaconimatinibydossi seiniciaconunTKIdesegundageneración
Tolerabilidad:Lospacientestratadosconasciminibtuvierondosvecesmenosposibilidadesdeser abandonadosdelestudiodebidoaefectossecundariosquelospacientestratadosconimatiniboun TKIdesegundageneración.
Lasmejoresopcionesdesegundalínea
Aúnhayesperanzaparalospacientesenlosqueeltratamientodeprimeralíneanoda buenosresultados.LosmédicospuedenrecetarunTKIdesegundageneracióndespuésdel fracasodelimatinibodelfracasodeotroTKIdesegundageneración.Sinembargo,en esteúltimocaso,sueficaciaesmenosimpresionante.Ponatinib,unTKIdetercera generación,haproporcionadolamejorrespuestaenelcontextoposterioralasegunda generación.Ponatinibseasociaconefectossecundarioscardiovascularesgravesylos médicos están buscando una alternativa más segura. Asciminib ofrece resultados prometedoresenelestudioASC2ESCALATE,conun96%depacientesquealcanzaronsus hitosderespuestatempranaalos3mesesyun11%quealcanzaronlaDMRalos6meses. Latolerabilidadfueconsistenteconensayosanterioresenentornosdeprimeralíneayde líneaposterior(3+).
Laincorporacióndeasciminibalarsenalterapéuticogarantizaunamejorcoberturaenlo querespectaalasmutaciones.Lospacientesquedesarrollaronmutacionesenelsitiode unióndeATPdeBCR-ABLdeberíanrespondermuybienalasciminib.Porelcontrario,los pacientesquedesarrollanunamutaciónenelbolsillodemiristoilooalberganASXL1 deberíanrespondermuybienalosTKItípicosLacombinacióndeambosinhibidoresdel sitiodeunióndeATPconasciminibpuedemaximizarlarespuestaenlospacientesqueno respondenadecuadamente.
OtrositiodeunióndeATPdelinhibidordeBCR-ABL,Olverembatinib,seencuentraen desarrolloclínicoytieneunatasaderespuestayunperfildeseguridadadecuados.Un segundoinhibidordelbolsillodemiristoilo,Tgrx,tambiénseencuentraendesarrolloclínicoy tieneunatasaderespuestayunperfildeseguridadadecuados
LospacientesconLMCpuedentomarelcontroldesutrayectoriahaciendounseguimiento desusresultadosdePCR,alcanzandolaDMRycuidandosusaludgeneralreduciendosus riesgoscardiovasculares,haciendoejercicioycomiendodemanerasaludableporque, despuésdetodo,tienenunaexpectativadevidacasinormal.
Referencias:NúmerosderesumendeASH24enhttps://ashconfexcom/ash/2024/webprogram

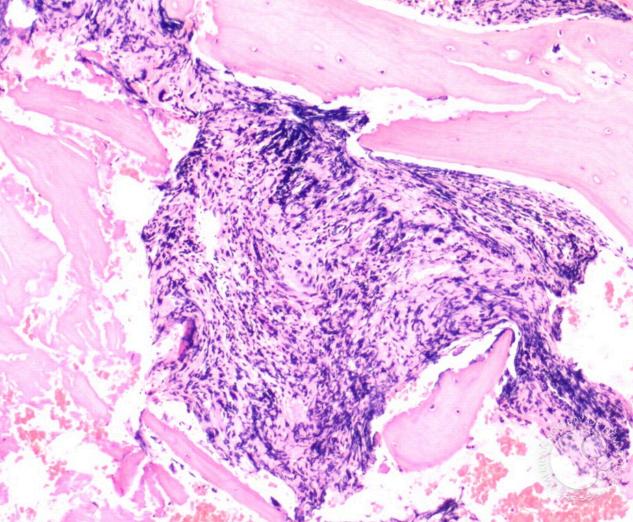
Se tratará mejor la mielofibrosis en 2025?
Brigitte Leonard, Doctora en Filosofía
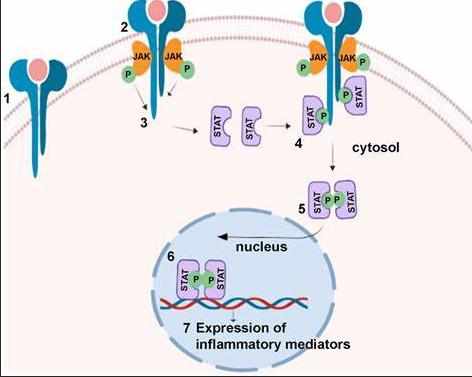
Reducir el tamaño del bazo y los síntomas es fundamental para los pacientes porque ambos factores afectan su calidad de vida y su supervivencia Desde 2010, los pacientes se han beneficiado de un tratamiento específico, ruxolitinib, un inhibidor de JAK (JAKi), para controlar estas dos características distintivas de la mielofibrosis (MF).
Desde la introducción del ruxolitinib (también conocido como JAKAFI o JAKAVI), un tipo de fármaco denominado inhibidor de la cinasa Janus (JAKi), se han aprobado tres JAKi más: fedratinib (Inrebic), momelotinib (Ojjaara) y pacritinib (Vonjo). El ruxolitinib sigue siendo el tratamiento de primera línea más utilizado para JAKi.
Mientras la comunidad de expertos en neoplasias mieloproliferativas (NMP) sigue debatiendo las categorías de riesgo y el mejor criterio de valoración de un ensayo clínico para evaluar un nuevo tratamiento en la mielofibrosis, ¿los pacientes reciben la mejor atención a diario? Existen lagunas en la práctica clínica que puedan solucionarse fácilmente?
Veamos qué aprendimos este año en ASH!
Necesidades médicas no satisfechas con ruxolitinib
El ruxolitinib sigue siendo el tratamiento de primera línea más utilizado contra los inhibidores de la enzima JAK. Se sabe que la mitad de los pacientes deben dejar de tomar ruxolitinib en un plazo de tres años debido a citopenia (anemia) o falta de respuesta. Antes de la aprobación de los nuevos inhibidores de la enzima JAK, cuando los pacientes no respondían al ruxolitinib, las opciones clínicas eran limitadas y su esperanza de vida era inferior a un año.
La anemia sigue siendo uno de los principales factores limitantes en el tratamiento de pacientes con ruxolitinib Los enfoques alternativos para el tratamiento de la anemia que incluyen terapias de apoyo tienen una eficacia limitada.
Por lo tanto, es tranquilizador para la comunidad tener acceso a momelotinib Por qué momelotinib en este contexto? El momelotinib puede restaurar de manera única la formación de glóbulos rojos al inhibir una molécula de gestión del hierro llamada ACVR1. En ASH, varios análisis de tratamientos en la vida real con momelotinib confirmaron su marcado beneficio en la mejora de la anemia, con altas tasas de pacientes que logran la independencia de las transfusiones (1790). Los niveles de hemoglobina y los recuentos de plaquetas aumentan rápidamente dentro de los 3 meses de tratamiento (2430). Más importante aún, el momelotinib reduce la mortalidad en ~ 50% en comparación con las mejores terapias disponibles anteriores en pacientes expuestos a JAKi, al tiempo que reduce el volumen del bazo y mejora los síntomas con un perfil de toxicidad aceptable (3187). Esta mejora significativa en las tasas de supervivencia debería infundir un sentido de esperanza y optimismo en la comunidad médica
Cuanto antes mejor
Por lo general, la JAKi se reserva solo para pacientes con síntomas y una forma más agresiva de MF (riesgo intermedio o alto). Esto es lamentable porque los beneficios clínicos son superiores en la etapa temprana de la enfermedad, con mejores respuestas del bazo y de los síntomas y menos efectos secundarios hematológicos y no hematológicos (1786) Esto subraya la importancia de la intervención temprana, lo que hace que la comunidad médica se sienta proactiva y responsable en su enfoque de la atención al paciente.
Además, el tratamiento con un JAKi como ruxolitinib reduce significativamente el riesgo de trombosis en pacientes con MF, que sigue siendo una causa importante de mortalidad en las NMP (3168).
Dónde están las lagunas en las prácticas clínicas actuales?
Lamentablemente, los médicos aún evalúan mal la carga de síntomas real de sus pacientes. Un análisis sólido ha demostrado que los médicos informaron una presencia de síntomas mucho menor que los pacientes, incluso en casos con una carga de síntomas grave (485). Esta observación es dramática para los pacientes porque:
Los síntomas son el principal desencadenante para iniciar el tratamiento con un inhibidor de JAK.
Algunos síntomas, como fiebre, pérdida de peso y sudores nocturnos, afectan la supervivencia. Por lo tanto, controlar los síntomas es crucial no solo para la calidad de vida, sino también para la supervivencia.

Estos hallazgos resaltan la necesidad de incluir herramientas de resultados informados por el paciente, como cuestionarios de síntomas validados, en la evaluación clínica de rutina de los pacientes con NMP Esta es una solución rápida porque ya existe un cuestionario de síntomas validado El cuestionario se llama MPN-SAF (formulario de evaluación de síntomas de NMP) o MPN10 Los pacientes pueden acceder fácilmente a este formulario (haga clic en el enlace: Formulario de evaluación de síntomas de NMP (MPN-SAF) | Jakafi com)

En ASH, un estudio que aborda el impacto de la educación continua y los programas de mejora de la calidad (QI) en la mielofibrosis pueden influir en las conductas de los médicos (3673). Los hallazgos de estos programas de educación continua y mejora de la calidad demuestran que los médicos oncólogos pueden mejorar la atención de los pacientes con mielofibrosis incorporando pruebas adecuadas y adaptando la terapia en función de las puntuaciones pronósticas y los síntomas del paciente. Después de la intervención, la evaluación de los síntomas con el formulario MPN-SAF pasó del 0 % al 80 %. La puntuación pronóstica se evaluó en el 60 % frente al 25 % al inicio. La proporción de pacientes tratados con un JAKi mejoró.

Los grupos de defensa de pacientes con MPN alientan a los pacientes a realizar un seguimiento de sus síntomas con el formulario y a utilizar los resultados durante las consultas con los médicos Esto puede tener un impacto positivo y mejorar la gestión de su atención
El futuro de la mielofibrosis
Se encuentran en desarrollo clínico varios agentes nuevos con mecanismos de acción diferentes a los JAKi Algunos agentes prometedores podrían administrarse como agente único o en combinación con un JAKi para maximizar la respuesta clínica Los más destacados son Navtemadlin y Selinexor en ensayos clínicos de fase III, que han obtenido resultados preliminares alentadores Esto debería generar entusiasmo e intriga en la comunidad médica sobre el potencial de estos nuevos agentes
Será mejor tratar la mielofibrosis en 2025?
La respuesta es sí
Los JAKi son eficaces, bien tolerados y seguros Los pacientes que toman JAKi tienen una mejor calidad de vida, un mejor control de la enfermedad y beneficios en la supervivencia
Para los pacientes con anemia y niveles bajos de plaquetas, momelotinib y pacritinib permiten un mejor control de la enfermedad frente al ruxolitinib
Sabemos que cuanto antes, mejor Si JAKi se toma en las primeras etapas del tratamiento, se amplifica el beneficio clínico y se reducen los efectos secundarios
No todos los médicos utilizan el formulario de evaluación de síntomas y la puntuación pronóstica para evaluar a sus pacientes, lo que retrasa el inicio del tratamiento con JAKi
Como paciente o cuidador, usted tiene todas las herramientas que necesita para mejorar su vida Tome el control de su proceso Evalúe sus síntomas, consulte a su médico sobre su categoría de riesgo y solicite el JAKi más adecuado para su situación También puede unirse a un grupo de pacientes como la red canadiense MPN para que lo apoyen en su proceso
Referencias:NúmerosderesumendeASH24enhttps://ashconfexcom/ash/2024/webprogram
Grupo de educación y defensa de pacientes de la Red MPN de Canadá

Brindar apoyo y educación a los pacientes con MPN Información@canadianmpnnetwork.ca

Policitemia Vera: ¡Surfeemos la ola!
Brigitte Leonard, Doctora en Filosofía
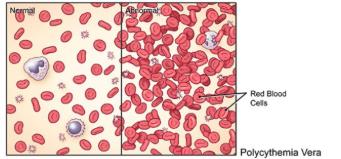
La policitemia vera (PV) es un cáncer de la sangre que se caracteriza por una producción excesiva de glóbulos rojos reflejada en niveles elevados de hematocrito (Hct). El exceso de glóbulos rojos aumenta el riesgo de desarrollar coágulos sanguíneos en venas o arterias (trombosis). La trombosis está estrechamente relacionada con niveles elevados de Hct (>45%). La intervención médica más urgente es evitar la coagulación con aspirina y controlar los niveles de Hct mediante la extracción de una gran cantidad de sangre (flebotomías) porque la mitad de los pacientes morirán por complicaciones cardiovasculares (CV). Qué pasa con los síntomas de los pacientes con PV y el riesgo de progresión a formas más agresivas de cáncer?
Un análisis reciente estimó que los pacientes con PV tratados en centros de atención especializada tienen un riesgo de mortalidad un 65 % menor (Kuykendall, 2024) Por qué? Algunas explicaciones surgieron de las presentaciones de ASH 2024. Los expertos en PV discuten la modificación de la evaluación de riesgos y la incorporación de nuevos criterios para influir en las decisiones de tratamiento.
Esta es una buena noticia para los pacientes con PV porque existen soluciones fáciles y rápidas para optimizar los tratamientos actuales. Además, se están desarrollando nuevos tratamientos para tratar a los pacientes que se quedan sin opciones.
Estás listo para una revolución? Porque nosotros sí.
Si bien los pacientes con mielofibrosis se benefician de muchas actualizaciones de la clasificación de riesgo, incluidas las mutaciones, la PV todavía se evalúa con un enfoque más simplista basado en la edad y el historial de trombosis. Los pacientes con PV se designan como de alto riesgo si tienen trombosis previa o si tienen 60 años o más. Sin embargo, ¿cómo se comparan los pacientes de bajo riesgo con la población general? La respuesta no es agradable. Los pacientes de bajo riesgo tienen entre 2,5 y 3,7 veces más trombosis que la población general. En comparación, los pacientes de alto riesgo tienen entre 3,5 y 5 veces más trombosis que la población general.
Según una revisión de historias clínicas realizada en 2020-2021, los peores resultados en los centros no especializados en PV se pueden explicar por la escasa adherencia a las recomendaciones de tratamiento actuales (Crodel, 2021):
En algunos centros oncológicos, menos del 10% de los pacientes de alto riesgo reciben tratamiento citorreductor.
A menudo, los pacientes de bajo riesgo permanecen en la categoría de bajo riesgo cuando llegan a los 60 años y su tratamiento no cambia.
Cuando reciben tratamiento, los pacientes pueden continuar con hidroxiurea (HU) a pesar de presentar signos claros de control insuficiente de la enfermedad.
Para los pacientes de bajo riesgo, las recomendaciones de tratamiento incluyen aspirina y flebotomías para mantener el hematocrito por debajo del 45 % El problema con este plan de tratamiento es que menos del 10 % de los pacientes lograron mantener con éxito su hematocrito por debajo del 45 % solo con flebotomías (Verstovsek, 2023) Seamos francos: las flebotomías frecuentes pueden ser incómodas Además, se asocian con efectos secundarios y complicaciones debido al agotamiento de hierro Los expertos en PV elaboraron una lista de signos y síntomas clínicos, identificando a los pacientes de bajo riesgo que deben considerarse de alto riesgo y recibir terapia de citorreducción La lista incluye:
Hct mayor del 53% en el momento del diagnóstico
Dificultad para controlar el hematocrito o necesidad de flebotomías frecuentes (>6 al año)
Intolerancia a la flebotomía
Los signos de progresión de la enfermedad incluyen niveles elevados de glóbulos blancos o niveles elevados de plaquetas o agrandamiento del bazo
Carga de síntomas importantes como fatiga y picazón
Factores de riesgo cardiovascular (CV) no controlados
Un análisis retrospectivo demuestra que estos signos clínicos son más predictivos que la edad para identificar a los pacientes con PV con mayor riesgo trombótico, lo que confirma que son útiles y mejoran la estratificación del riesgo Además, según la clasificación convencional, la mayoría de los pacientes de bajo riesgo requieren terapia citorreductora (242)

Qué pasa con otras mutaciones además de JAK2?
Las mutaciones de JAK2 se asocian invariablemente con la PV. Sin embargo, más del 50% de los pacientes afectados también presentan mutaciones no JAK2, algunas consideradas relevantes desde el punto de vista pronóstico. Estas mutaciones adicionales pueden estar relacionadas con la progresión de la mielofibrosis y/o la leucemia. Tres mutaciones se asocian significativamente con una menor supervivencia: SRSF2, ASXL1 e IDH2. Las mutaciones de SRSF2 y AXL1 se asocian con un mayor riesgo de progresión de la mielofibrosis y/o la leucemia (1797). Las pruebas de mutación pueden evaluar el riesgo de progresión y, en última instancia, facilitar la personalización del tratamiento. ¿Se pueden utilizar inhibidores de IDH2 en pacientes que presentan mutaciones de IDH2? ¡Solo el futuro lo sabrá!
Hablemos de la terapia de citorreducción!
A pesar de varios problemas, el primer agente y el más utilizado es la hidroxiurea (HU). Con la HU, solo el 24% de los pacientes lograron una respuesta completa. La tasa de respuesta completa es mayor en pacientes que toleran una dosis de 1 g o más al día. Sin embargo, esta dosis diaria se asocia con un aumento de la anemia y las lesiones cutáneas. De hecho, entre el 10 y el 15% de los pacientes son intolerantes a la HU. Varios médicos se muestran reacios a utilizar la HU en pacientes más jóvenes. Por lo tanto, la HU se reserva para pacientes de alto riesgo y los datos sobre pacientes de bajo riesgo son limitados.
En 2025, nuevas terapias como el interferón y JAKi pueden reemplazar a la HU. Se sabe desde hace décadas que el interferón (IFN) proporciona resultados interesantes en la PV. Sin embargo, la mala tolerabilidad de la antigua formulación afectó a su adopción en las prácticas clínicas. El RopegIFN (BESREMI) se ha estudiado en poblaciones de pacientes de bajo y alto riesgo. El RopegIFN reduce la necesidad de flebotomía y normaliza los recuentos de leucocitos y plaquetas, lo que da como resultado la ausencia de eventos trombóticos Se considera un modificador de la enfermedad El RopegIFN reduce la carga de mutación de JAK2 También mejoró la calidad de vida de los pacientes con PV, abordando las preocupaciones sobre la tolerabilidad y toxicidad del fármaco En pacientes de bajo riesgo, la dosis se puede aumentar de 100 µg cada 2 semanas a 250 → 350 → 500 µg cada dos semanas si no se observan los beneficios clínicos (1799) El RopegIFN proporciona resultados superiores en pacientes sin tratamiento previo con hidroxiurea Evitar la hiperhidrosis y comenzar a tratar a los pacientes con RopegIFN podría mejorar la atención a largo plazo Con base en estos hallazgos, la Red Nacional del Cáncer (NCCN) recomendó RopegIFN como el régimen citorreductor preferido en el entorno de primera línea para pacientes con PV de bajo riesgo y un régimen de interferón preferido en PV de alto riesgo
Qué pasa con los síntomas?
Todos los pacientes con PV y sus cuidadores saben que la carga de síntomas puede ser pesada con el tiempo y cómo afecta la calidad de vida. Síntomas como fatiga, picazón, dificultad para concentrarse, insomnio, disfunción sexual, sudores nocturnos y saciedad temprana son causados principalmente por desregulación inflamatoria y trastornos vasculares. Lamentablemente, los médicos aún evalúan mal la carga de síntomas real de sus pacientes. Un análisis sólido ha demostrado que los médicos informaron una presencia de síntomas mucho menor que los pacientes, incluso en casos con una carga de síntomas grave (485).

Esta observación es dramática para los pacientes porque los síntomas son el principal detonante para iniciar un tratamiento más eficaz, como el interferón o un inhibidor de JAK. Es una solución rápida porque ya existe un cuestionario de síntomas validado. El cuestionario se llama MPN-SAF (formulario de evaluación de síntomas de MPN) o MPN-10. Los pacientes pueden acceder fácilmente a este formulario (haga clic en el enlace: Formulario de evaluación de síntomas de MPN (MPN-SAF) | Jakafi.com). Los pacientes y los cuidadores pueden completarlo y usarlo cuando discutan las opciones de tratamiento con sus médicos.

Se han presentado varias moléculas nuevas intro Los favoritos serán: Rusfertide completó un ensayo de fase 2, en e l hematocrito a largo plazo y disminuyeron la necesidad de flebotomía Los pacientes también observaron una mejoría de los síntomas cuando recibieron tratamiento con Rusfertide El estudio aleatorizado de fase 3 VERIFY (NCT05210790) está en curso y evaluará el uso de Rusfertide frente a placebo en pacientes con PV
En un ensayo de fase 2, OB756, un inhibidor de JAK2, ha demostrado beneficios clínicos significativos en pacientes con PV, especialmente en la reducción rápida del bazo y la reducción de la alta carga de mutación de JAK2 OB756 también ha demostrado una respuesta hematológica completa y duradera y pocos efectos secundarios La fase 3 está en curso y se compara OB756 con HU en PV (3180)
Qué pueden hacer los pacientes con PV para mejorar sus probabilidades hoy?
Realice un seguimiento de sus síntomas con el formulario de evaluación de MPN Realice un seguimiento de su hematocrito y hemograma. Hable con su médico sobre las opciones de tratamiento si su enfermedad no está controlada adecuadamente. Incluso si es un paciente de bajo riesgo, es posible que necesite terapia citorreductora RopegIFN proporciona un control superior al HU. Es RopegIFN una buena opción para usted? Además, se debe alentar a los pacientes con PV a que controlen sus factores de riesgo cardiovascular: Dejar de fumar
Hacer más ejercicio
Comer sano y alcanzar un peso saludable
Dormir lo suficiente
Controlar la tensión arterial con medicación si hay hipertensión
Controlar el azúcar en sangre con medicamentos si tiene diabetes
Es mucho trabajo...pero ¡se puede!
Referencias:NúmerosderesumendeASH24en https://ashconfexcom/ash/2024/webprogram












Alguien ha oído hablar de la ET? ET para la trombocitemia esencial.
Brigitte Leonard, Doctora en Filosofía
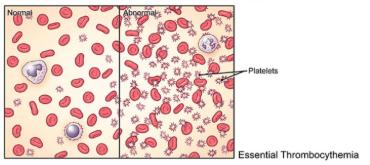
La trombocitemia esencial (TE) es un cáncer de la sangre que se caracteriza por niveles elevados de plaquetas En el caso de la policitemia vera (PV), la esperanza de vida es menor en comparación con la de la población general y las principales causas de muerte son las complicaciones vasculares y la progresión a cánceres más agresivos.
A diferencia de otras neoplasias mieloproliferativas (NMP), como la mielofibrosis (MF) y la policitemia vera, los pacientes con trombocitemia esencial (TE) no se han beneficiado mucho de los avances científicos recientes Por qué? La TE es la NMP más frecuente, por lo que debería ser la que más atención reciba, no? En realidad no, porque la TE tiene el mejor pronóstico y una expectativa de supervivencia de casi 20 años Un estudio que evalúe la eficacia de un nuevo agente tardará al menos 5 años en demostrar beneficios clínicos sustanciales contra la trombosis y 10 años contra la progresión a mielofibrosis y otras leucemias.
Por lo tanto, la mayoría de las recomendaciones de tratamiento se basan en las antiguas clasificaciones de riesgo y se centran en la aspirina infantil y en el control de los factores de riesgo cardiovascular (CV). La terapia citorreductora, principalmente hidroxiurea (HU), se recomienda solo para pacientes de alto riesgo o pacientes que muestran signos de progresión. Incluso los criterios para el cambio de tratamiento no están bien establecidos.
Existe esperanza para que los pacientes con TE tengan acceso a un plan de atención más integral?
Hemos observado algunas tendencias interesantes en ASH que pueden ser alentadoras para los pacientes con TE. También existen algunas soluciones sencillas para mejorar la experiencia de los pacientes con TE en la actualidad.
Objetivos actuales del tratamiento de ET En 2017, una encuesta reveló que los objetivos de tratamiento de los médicos se centraban en prevenir las complicaciones vasculares, mientras que los pacientes también estaban preocupados por frenar la progresión y conseguir recuentos sanguíneos saludables. Esta discrepancia puede explicar por qué, incluso en la ASH de 2024, la mayoría de los estudios se centraron en el riesgo cardiovascular y los tratamientos anticoagulantes

Los médicos se centran en el tema más urgente en la TE: las complicaciones cardiovasculares, lo cual es perfectamente lógico. Sin embargo, es justo que los pacientes deseen un enfoque más integral que aborde todos los riesgos asociados a la enfermedad.
El impacto de la mutación del conductor
La ET es un cáncer complejo. Las mutaciones impulsoras pueden ser JAK2, CALR, MPL o triple negativa (TN) en una proporción similar a la de la mielofibrosis. Es posible que todavía no sea una práctica habitual realizar pruebas de mutaciones porque no es obligatorio para confirmar el diagnóstico. Sin embargo, hallazgos recientes demostraron que el tipo de mutación afecta la evolución clínica (Abu-Zeinah, 2024). Los pacientes que presentan la mutación JAK2 o TN tienen un mayor riesgo de sufrir eventos trombóticos. Por el contrario, los pacientes que presentan la mutación CALR o MPL tienen un mayor riesgo de que la enfermedad progrese a mielofibrosis (MF).
Cómo actúa la hidroxiurea (HU) en la ET?
La HU será el principal tratamiento de primera línea ofrecido a los pacientes con TE. La HU induce el 67% de la respuesta hematológica completa (RHC), y se necesita un año completo para lograr esta respuesta. La RHC significa la normalización del recuento de plaquetas, una reducción del recuento de glóbulos blancos por debajo de 10, ausencia de síntomas de la enfermedad y un bazo normal. De los respondedores iniciales, el 20% de los pacientes desarrollaron una resistencia o intolerancia a la HU. Los pacientes que lograron la RHC tienen mejores tasas de supervivencia, menor riesgo de trombosis y una menor tasa de progresión de la enfermedad. El hecho de no lograr la RHC con HU podría considerarse un criterio elegible en la terapia de segunda línea (241). También se propone el interferón pegilado (PegIFN) o la anagrelida para la primera línea. Con base en este análisis, el 53% de los pacientes deberían estar en tratamiento de segunda línea en el segundo año de sus tratamientos. Las terapias propuestas en segunda línea después de la HU son el PegIFN, la anagrelida o el ruxolitinib (inhibidor de JAK2 utilizado en MF y PV). En un resumen de última hora en ASH24, RopegINF, una formulación de IFN mejor tolerada aprobada para PV, mostró resultados de CHR interesantes en pacientes con TE (LBA-4). RopegINF podría convertirse en una alternativa de tratamiento prometedora. Se está llevando a cabo un ensayo de fase 3 para evaluar RopegINF en pacientes con TE que son intolerantes o refractarios a los tratamientos citorreductores actuales.

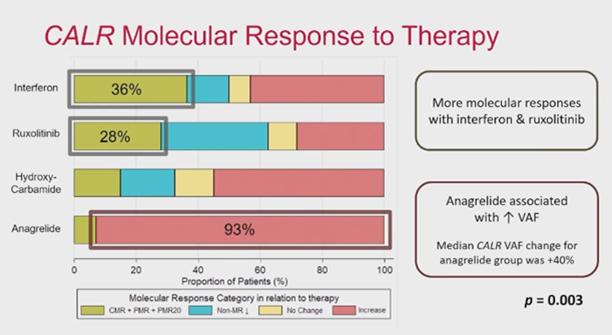
En ASH24, un análisis reciente de la carga de mutación de CALR durante el tratamiento demostró diferencias significativas entre las terapias propuestas Este análisis combinó 60 pacientes con MF y 82 pacientes con ET con CALR positivo (485) Se probaron interferón (IFN), ruxolitinib, HU y anagrelida
Casi todos los pacientes tratados con anagrelida experimentan un aumento de la frecuencia de CALR durante el tratamiento Por el contrario, alrededor del 30 % de los pacientes tratados con IFN y ruxolitinib experimentaron una disminución de la frecuencia de CALR. Un aumento de la frecuencia de CALR se correlaciona con un aumento de la fibrosis de la médula ósea La anagrelida requiere precaución y se puede utilizar en su lugar INF o ruxolitinib hasta que se generen más datos.
Qué pasa con los síntomas?
Todos los pacientes con TE y sus cuidadores saben que la carga de síntomas puede ser pesada con el tiempo y cómo afecta la calidad de vida. Los síntomas como fatiga, sudores nocturnos, mareos, depresión, entumecimiento, dolores de cabeza, cambios en la visión e insomnio son causados principalmente por desregulación inflamatoria y alteraciones vasculares.
Lamentablemente, los médicos aún evalúan de manera deficiente la carga de síntomas real de sus pacientes. Un análisis sólido ha demostrado que los médicos informaron una presencia de síntomas mucho menor que los pacientes, incluso en casos con una carga de síntomas grave (485). Esta observación es dramática para los pacientes porque los síntomas son el principal desencadenante para iniciar un tratamiento más eficaz, como el interferón o un inhibidor de JAK Es una solución rápida porque ya existe un cuestionario de síntomas validado El cuestionario se llama MPN-SAF (formulario de evaluación de síntomas de MPN) o MPN-10 Los pacientes pueden acceder fácilmente a este formulario (haga clic en el enlace: Formulario de evaluación de síntomas de MPN (MPN-SAF) | Jakafi com) Por lo tanto, los pacientes y los cuidadores pueden completarlo y usarlo cuando discutan las opciones de tratamiento con sus médicos


Qué pueden hacer hoy los pacientes o los cuidadores para mejorar su experiencia? Como paciente o cuidador, usted tiene todas las herramientas que necesita para mejorar su vida Tome el control de su camino.
1) Está seguro de que tiene TE? El agrandamiento del bazo o el nivel alto de LDL (marcador de cáncer) son poco frecuentes en la TE. En ese caso, es posible que tenga mielofibrosis en la etapa prefibrótica en lugar de TE. Estos dos tipos de cáncer de la sangre pueden confundirse fácilmente. Sin embargo, los riesgos y los tratamientos son diferentes, por lo que es mejor volver a comprobarlo
2) Conozca qué mutación provoca su cáncer y analice con su médico cómo gestionar sus riesgos personalizados
3) Evalúe sus síntomas con el formulario de evaluación de síntomas de NMP y utilice los resultados durante la conversación con su médico Una conversación franca sobre sus síntomas con su médico tratante es esencial porque están relacionados con la progresión de la enfermedad y una menor supervivencia. No se trata solo de una cuestión de calidad de vida.
4) Realice un seguimiento de sus hemogramas y analice los cambios de tratamiento si los resultados no son óptimos. ¿Puede tener acceso a RopegIFN, PegINF o un JAKi?
5) Evalúa con tu médico tus factores de riesgo cardiovascular y redúcelos al máximo:
Dejar de fumar
Hacer más ejercicio
Comer sano y alcanzar un peso saludable
Dormir lo suficiente
Controlar la tensión arterial con medicación si hay hipertensión
Controlar el azúcar en sangre con medicamentos si tiene diabetes
También puede unirse a un grupo de pacientes como la red canadiense de MPN para que lo apoyen en su proceso Le deseamos sinceramente lo mejor y esperamos que la información le resulte útil
Referencias:NúmerosderesumendeASH24en https://ashconfexcom/ash/2024/webprogram















E n s a y o s c l í n i c o s y e n c u e s t a s




¡Haz que tu voz sea escuchada!
Visite el sitio web Mi Sangre Mi Salud y participe en nuestras diversas encuestas
misangremisalud.ca monsangmasante.ca
Encuestas abiertas:
Calidad de vida (CdV) en pacientes con cáncer de sangre
Impacto de la transfusión sanguínea en la calidad de vida
Impacto de la mielofibrosis en la calidad de vida
El impacto de la leucemia mieloide aguda en la calidad de vida
































Brigitte Léonard es directora científica de My Blood, My Health, una organización sin fines de lucro registrada que promueve el acceso equitativo a una atención médica de calidad en todo Canadá. Tuvo el privilegio de trabajar en el sector farmacéutico durante más de 20 años, contribuyendo a brindar tratamientos que cambian la vida a os pacientes con los más altos estándares éticos. Ahora, quiere compartir su conocimiento y utilizar sus habilidades científicas, estratégicas y de comunicación para ayudar a la comunidad de pacientes.
Obtuvo su doctorado en Ciencias Biomédicas en la Universidad de Montreal en 2003. Su investigación doctoral se llevó a cabo bajo la supervisión del Dr. Denis-Claude Roy en el Centro de Investigación del Hospital Guy-Bernier, Maisonneuve-Rosemont. Desarrolló un ensayo de diagnóstico cuantitativo en el linfoma no Hodgkin y evaluó la relevancia de este marcador en la evolución del paciente.

Cheryl A. Petruk es una profesional multifacética cuya carrera abarca la defensa de los pacientes, los negocios y la educación postsecundaria, lo que demuestra su dedicación a lograr un impacto significativo en cada una de estas áreas.
La transición de Cheryl hacia la defensa de los pacientes fue impulsada por la pasión que le generó su situación familiar y un profundo compromiso con la garantía de los derechos de los pacientes y el acceso a la atención. Cheryl ha trabajado incansablemente para cerrar la brecha entre el sistema de atención médica, los pacientes y las partes interesadas de la industria farmacéutica, asegurándose de que se escuchen las voces de los pacientes y se satisfagan sus necesidades Su trabajo implica colaborar con las partes interesadas y las organizaciones de defensa de los pacientes, presionar para que se centren en el paciente y brindar apoyo y orientación al paciente El enfoque empático de Cheryl y su dedicación a la defensa la han convertido en una figura respetada en este campo, admirada por pacientes, profesionales de la salud y otros defensores.
Cheryl también dirige y es miembro principal del cuerpo docente de CACHeducation, Capacitación en Defensa del Paciente.