4

PROIEKTU DIGITALA
12HILEKO LIZENTZIA
J. M. Vílchez González, A. M.a Morales Cas, G. Villalobos Galdeano


J. M. Vílchez González, A. M.a Morales Cas, G. Villalobos Galdeano
Jarduera zientifikoa nolakoa den jakiteko historia
1. Ikerketa zientifikoa
2. Magnitude fisikoak eta unitateak
3. Magnitude fisikoen neurketa. Akatsak
4. Datu esperimentalen azterketa
Problemak konpontzeko orientabideak
Ikerketa-proiektua
Jolas-zientzia. Buruko esperimentuak
Lan praktikoa. Plastilinaren «dentsitatea»
Amaitzeko IKASKETA-EGOERA
Atomoaren konplexutasuna ezagutzeko historia
1. Materiaren etena
2. Atomoaren ideia eboluzionatu zuten aurkikuntzak
3. Lehen eredu atomikoak
4. Espektro atomikoak eta Bohr-en eredua
5. Atomoaren eredu kuantikoa
6. Elementu kimikoen sistema periodikoa
7. Masa atomikoak
Problemak konpontzeko orientabideak
IKT. Eredu atomikoak
Jolas-zientzia. Curie petite-ak
Lan praktikoa. Izpi katodikoak eta
deskarga-hodiak
Amaitzeko
Eranskina. Formulazio eta nomenklatura kimikoa
Lotura kimikoari buruzko istorioa
1. Lotura kimikoa
2. Lotura ionikoa
3. Lotura kobalentea
4. Molekulen arteko indarrak
5. Lotura metalikoa
6. Konposatu kimikoen propietateak
Problemak konpontzeko orientabideak
IKT. Kalkulu-orriak eta web-baliabideak
Jolas-zientzia. Substantzia motak
Lan praktikoa. Lotura-mota zehaztea
Amaitzeko
Karbonoa, komenigarria
1. Karbono atomoa
2. Karbonoaren forma alotropikoak
3. Formula eta eredu molekularrak
4. Hidrokarburoak
5. Karbono-konposatu oxigenatuak eta nitrogenatuak
6. Interes bereziko molekulak
IKT. IKTek ezagutzak finkatzen laguntzen dizute Jolas-zientzia. Eredu molekularrak
Lan praktikoa. Kortxo zuriaren disolbagarritasuna
Miraria zientzia izatera pasatu zenean
1. Aldaketa kimikoak
2. Erreakzio-abiadura
3. Substantzia kantitatea
4. Kalkulu estekiometrikoak
5. Energia erreakzio kimikoetan
Problemak konpontzeko orientabideak
IKT. Erreakzio kimikoei buruzko simulazioak
Jolas-zientzia. Burdinaren oxidazio-erreakzioak
Lan praktikoa. Erreakzio-abiadura Amaitzeko
Erreakzio kimiko bat, bi jarrera eta kimika modernoaren sorrera
1. Azidoak eta baseak
2. Errekuntza-erreakzioak
3. Errekuntza-erreakzioen garrantzia
4. Oxidazio-erreakzioak
5. Oxidazio-erreakzioen garrantzia
6. Sintesi-erreakzioak
Problemak konpontzeko orientabideak
IKT. Irudikapen grafikoak
Jolas-zientzia. Etxeko pH-adierazleak Lan praktikoa. CO2-a identifikatzea
Amaitzeko
IKASKETA-EGOERA
Itzala uzten duten erronkak: Ingeniariak aurrera 180
Erorketa librea, baina benetan librea
1. Erreferentzia-sistema
2. Mugimenduaren magnitudeak
3. Mugimendu motak
4. Mugimendu zuzenak
5. Mugimendu zirkularrak
6. Grafikoen irudikapenaren interpretazioa
Problemak konpontzeko orientabideak
IKT. Mugimenduak aztertzeko kalkulu-orriak
Jolas-zientzia. Denbora-faktorea indarretan
Lan praktikoa. Mugimendu uniformeki azeleratua da?
Amaitzeko
Bere pisuagatik erori zen sagarra
1. Indarrak
2. Eguneroko indarrak
3. Newtonen legeak
4. Newtonen legeak eguneroko mugimenduetan
Problemak konpontzeko orientabideak
IKT. Fenomeno fisikoen simulagailuak
Jolas-zientzia. Marruskadura
Lan praktikoa. Marruskadura-koefizientea irristatzeagatik
Itzala
Unibertsoa, ezezagun handia
1. Unibertsoaren azterketaren bilakaera historikoa
2. Indar grabitatorioak
3. Grabitazio unibertsalaren legearen aplikazioak
4. Satelite artifizialak orbitan
Problemak konpontzeko orientabideak
IKT. Stellarium
Jolas-zientzia. Einsteinen grabitazioaren
teoriaren simulazioa
Lan praktikoa. Astroen kokapena
Amaitzeko
Bilbilis, presio-kontzeptuaren ezagutzaren ebidentziak
1. Presioa
2. Hidrostatikaren oinarrizko legea
3. Arkimedesen printzipioa
4. Pascalen legea
5. Presio atmosferikoa
6. Kontzeptu meteorologikoak
Problemak konpontzeko orientabideak
IKT. Online aplikazio interaktiboa
Jolas-zientzia. Presio atmosferikoa
Lan praktikoa. Pascalen barrika
Amaitzeko
Vis viva-tik gaur egungo energia-kontzeptura
1. Energia
2. Lan
3. Potentzia
4. Energia zinetikoa
5. Energia potentziala
6. Energia mekanikoaren kontserbazioa
7. Energia uhin mekanikoen bidez garraiatzea
Problemak konpontzeko orientabideak
IKT. Kalkulu-orriarekin lan egitea
Jolas-zientzia. Eguzkia energia berriztagarriaren iturri gisa
Lan praktikoa. Energia mekanikoaren kontserbazioa
Beroa, materia ikusezina edo energia-transferentzia?
1. Energia termikoa. Tenperatura
2. Oreka termikoa. Beroa eta hedapena
3. Beroaren ondorioak
4. Motor termikoa
5. Energiaren degradazioa
6. Energia eta gizartea
Problemak konpontzeko orientabideak
IKT. Geogebra
Jolas-zientzia. Espektroskopioa
Lan praktikoa. Ura urtzeko bero sorra
Ardoaren ekoizpenaren eta kontsumoaren ebidentziarik zaharrena Zagros mendietan (gaur egun Iran eta Irak) aurkitutako zeramikazko ontzi bat da, K.a. 5400. urtekoa. Tradizioz, ardoa eta haren ekoizpen-prozesua misterioarekin eta jainkoarekin lotu izan dira. Hain da horrela ezen, lehenik, kultura grekoak eta, ondoren, erromatarrak ardoaren eta mahastien jainko bat baitzuten: Dioniso eta Baco,
Sineste horiek aldatuz eta desagertuz joan dira, logika eta jakinminagatik. Hala, Erdi Aroan esaten zen ardoa materia deskonposatzearen ondorioz sortzen zela (mahats-zukua edo muztioa); xix. mendean, berriz, ardoa erreakzio kimiko bati esker sortzen zela aurkitu zen: hartzidura.

Louis Pasteur kimikari frantsesak azaldu zuen hartzidura eta, ondorioz, oinarri zientifikoa eman zion ardoaren ekoizpen-prozesuari. Aldaketa kimiko hori muztioaren azukrea (glukosa) alkohol etiliko eta karbono dioxido bihurtzean datza. Erreakzio kimiko hori legamien (onddoen) jarduerari esker gerta daiteke, hala nola kandida,pichia, zygosaccharomyces edo saccharomycescerevisiae ezagunari esker. Gaur egun, bada zientzia espezializatu bat prozesu kimiko horien azterketan; badakizu zein den?
2020. urtea oso txarra izan zen Galizia, Katalunia, Gaztela-Mantxa eta Andaluziako mahastientzat, plasmoparaviticola onddoaren izurritea zela eta. Izan ere, mildiua eragiten du, eta nekazariek fungizidekin tratatu behar dituzte uzta salbatzeko.
1. Buru-hausgarriak. Bilatu mildiu gaixotasunari eta fungizidak nekazaritzan erabiltzearen ondorioei buruzko informazioa.
2. Egin nekazarientzako infografia bat, non:
– Arazo honi lotutako GJHen helburuak azaltzen diren eta horiek betetzeko beharra justifikatzen den.
– Mildiu gaixotasunari aurre egiteko tratamendu natural alternatibo bat gutxienez azaltzen den.

Unitate honetan

Miraria zientzia izatera pasatu zenean
1. Aldaketa kimikoak
2. Erreakzio-abiadura
3. Substantzia kantitatea
4. Kalkulu estekiometrikoak
5. Energia erreakzio kimikoetan
Problemak konpontzeko orientabideak
• Estekiometria-ariketa bat nola ebatzi
IKT
• Erreakzio kimikoei buruzko simulazioak
Zientzietako lantegia
• Jolas-zientzia: Burdinaren oxidazio-erreakzioak

















• Lan praktikoa: Erreakzio-abiadurari eragiten dioten faktoreak
anayaharitza.es helbidean
Motibatzeko:
• Bideoa: «Hasi aurretik».
• Dokumentua: «Energia berriztagarrien garapenarekin lotutako goi-mailako graduak».
Ideiak aldez aurretik atzemateko:
• Jarduera interaktiboa: Hasierako autoebaluazioa.
• Aurkezpena: «Zer jakin behar duzu».
Ikasteko:
• Simulazioak: «Ekuazio kimikoen doikuntza».
• Aurkezpena: «Substantzia kantitatea» eta «Ikasteko».
• Bideoa: «Erreakzio kimiko baten ebidentziak».
Zeure burua ebaluatzeko:
• Jarduera interaktiboa: Azken autoebaluazioa.
• Zenbakizko jardueren soluzioak.
Eta, gainera, proiektuaren gakoak aplikatzeko behar den dokumentazio guztia.
1.1 Erantzun galdera hauei: zer erreakzio-mota da hartzidura? Nor izan zen bere mekanismoa aztertu zuen lehena? Nola egin zuen? Koka ezazu dagokion une historikoan.
1.2 anayaharitza.es helbidean aurkituko duzuen esne jogurtaren hartzidurari buruzko artikulutik abiatuta, pentsatu nola egin dezakezuen erreakzio hori laborategian. Ondoren, grabatu bideoan prozesua erakutsiz eta nola egin duzuen azalduz.
ESPERIMENTAZIOA. ERREAKZIO-ABIADURA.
2.1 Irakurri anayaharitza.es helbidean proposatutako laborategi-praktikaren gidoia, eta, zuen irakaslearen laguntzaz, gauzatu ikastetxeko laborategian. Nola eragiten dute erreaktiboaren zatiketa-mailak eta tenperaturak erreakzio-abiaduran? Erreakzio guztietan kontserbatzen da masa? Desberdina da puxiken bolumena? Zergatik?
ESPERIMENTAZIOA. ENERGIA ERREAKZIOETAN.
3.1 Laborategian, bi hauspeakin-ontzitan, bota 50 mL ur batean eta 50 mL ozpin bestean. Neurtu horien tenperaturak. Ondoren, gehitu 1 g sodio hidroxido lehenengo ontzian eta bi koilara sodio bikarbonato bigarrenean. Erreakzioa amaitzean, neurtu ontzi bakoitzaren tenperatura. Erreakzio exotermikoak ala endotermikoak dira?
3.2 Ikastetxeko Zientzia Azokan, errepikatu esperientzia horiek eta azaldu ikaskideei ikasi duzuen oinarri kimikoa.
Jarraibide + anayaharitza.es helbidean

Erreakzio kimiko batean, aldaketaren aurretik zeuden erreaktibo izeneko substantzia batzuetatik abiatzen da, eta aldaketaren ondorioz beste batzuk lortzen dira, erreakzioaren produktu deritzenak.
Aldaketa kimikoa gertatzeko, erreaktiboek elkarrekin kontaktuan egon behar dute. Prozesuan zehar aldaketa fisikoak ere gertatzen dira, horiek agerian uzten dituztenak, ondoren azaltzen den moduan.
Erreakzio kimiko baten ondorioz substantzia berriak agertzea erreaktiboen atomoak berrantolatzean oinarritzen da. Hori gerta dadin, erreaktiboak osatzen dituzten oinarrizko entitateek elkarrekin talka egin behar dute. Talka horien ondorioz, loturak hautsi eta lotura berriak sortzen dira, substantzia berriak sortuz.
Atomoen berrantolaketa bat denez, aldaketa kimikoaren aurreko eta ondorengo substantzien masa totala ez da aldatzen; beraz, hau esan dezakegu:
Aldaketa kimiko batean, masa kontserbatu egiten da; hau da, erreaktiboen masen batura eta produktuen masen batura berdinak dira. Enuntziatu horri masaren kontserbazioaren legea esaten zaio.
2 NO O2 +
2 NO2
Nitrogeno dioxidoa emateko nitrogeno monoxidoaren oxidazio-erreakzioa agertzen da irudian.


Ikus dezakegunez, erreakzioan atomoak berrantolatu egiten dira, eta masa mantendu egiten da prozesu osoan zehar.

ULERTU, PENTSATU, IKERTU…
1 Irudiko informaziotik abiatuta, ondorioztatu zer lotura hautsi diren eta zer lotura sortu diren irudikatzen den aldaketa kimikoan.
2 1-2-4. Marraztu aurrekoaren antzeko eskema erreakzio honetarako:
CH4 + 2 O2 → CO2 + 2 H2O
Zenbat lotura hautsi dira eta zenbat eta zeintzuk eratu dira?
Aldaketa kimikoak kuantitatiboki adierazteko, ekuazio kimikoak erabiltzen ditugu.
Ekuazio kimikoek erreakzio kimiko batean ematen diren erreaktiboen eta produktuen arteko erlazioa adierazten dute, bai eta beren oinarrizko entitateen arteko proportzioa ere, koefiziente estekiometrikoen bidez.
Batzuetan, substantzien agregazio-egoeren, tenperaturaren edo presioaren berri ere ematen dute.
Ekuazio kimiko bat doitzean, koefizienteen balioak aukeratzen dira, elementu bakoitzaren atomo-kopurua berdina izan dadin erreaktiboetan eta produktuetan.
Ekuazio kimikoen adierazpena eta doikuntza
Adibide gisa, amoniakoaren eta oxigeno molekularraren (produktu gisa nitrogeno molekularra eta ura ditu) arteko erreakzioa erabiliko dugu.
1 Erreaktiboen eta produktuen formulak idazten ditugu, eta erreakzioaren noranzkoa markatzen duen gezi batez bereizten ditugu:
NH3 + O2 → N2 + H2O
2 Koefiziente estekiometrikoen balioak aukeratzen ditugu, elementu bakoitzaren atomo-kopurua berdina izan dadin erreaktiboetan eta produktuetan. Horretarako:
2.1 Lehenik, oinarrizko ez diren substantzien koefizienteak doitzen ditugu:
2 NH3 + O2 → N2 + 3 H2O
2.2 Ondoren, oinarrizko substantzienak. Beharrezkoa bada, hautatutako koefizienteak zuzenduko ditugu, tanteatuz. Zenbaki zatikiarrak erabil daitezke:
2 NH3 + 3/2 O2 → N2 + 3 H2O
Ikus ezazu nitrogeno molekularraren koefiziente estekiometrikoa 1 dela; beraz, ez da idazten.
Ekuazio kimikoa bider bi egin dezakegu, koefiziente zatikiarrik ez egoteko:
2 NH3 + 3/2 O2 → N2 + 3 H2O
3 2 6
3 Azkenik, elementuz elementu, egiaztatuko dugu erreaktiboetan agertzen den atomo kopurua eta produktuetan agertzen dena berdinak direla:
ULERTU, PENTSATU, IKERTU…
3 Adierazi aurreko ariketaren erreakzioan koefiziente estekiometrikoek zer esan nahi duten.
4 Egiazta dezagun. Doitu erreakzio kimiko hauek:
a) CO2 + H2O → H2CO3
b) NO + O2 → NO2
c) Cr2O3 + Al → Al2O3 + Cr
d) NO2 + H2O → HNO3 + NO
e) C2H2 + O2 → CO2 + H2O
Erreakzio kimiko baten abiadura erreaktibo bat desagertzeko edo produktu bat agertzeko behar den denboraren arabera definitzen da.
Batzuetan, erreakzio kimikoa gertatzen den lekuko beste propietate baten aldaketaren bidez ere zehaztu daiteke.

Ikusi dugunez, erreakzio kimiko batean loturak hausten dira eta berri batzuk eratzen dira erreaktiboen oinarrizko entitateen arteko talken ondorioz.
Talka guztiek ez dute lotura bat hausten edo eratzen; talka guztiak ez dira eraginkorrak. Energia nahikoa dutenak eta partikulek orientazio egokia dutenak baino ez dira eraginkorrak.
Zenbait faktorek eragina dute erreakzio-abiaduran, erreaktiboen agregazio-egoeraren arabera. Hauek dira:
■ Tenperatura
Likido- edo gas-egoeran dauden substantziek parte hartzen duten erreakzioetan, tenperatura igotzeak erreaktiboen oinarrizko entitateen abiadura areagotzen du. Horrek talka gehiago eragiten ditu, erreakzioak aurrera egiteko behar adinako energiarekin.
■ Erreaktiboen kontzentrazioa
Erreakzio-azalera
Demagun irudiaren karratuaren aldeak 1 cm neurtzen duela. Kalkulatu hiru kasuetan erabilgarri dagoen azalerak zenbat balioko lukeen. Lor ezazu arau orokor bat zatiketa kopuruaren arabera.
Ur-disoluzioan gertatzen diren erreakzioetan, erreaktiboen kontzentrazioa handitzeak talkak gertatzeko aukera handiagoa dakar, eta, hala, erreakzioaren abiadura handitu egiten da.
■ Erreaktiboen zatiketa maila
Erreaktiboetako bat egoera solidoan badago, haren zatien tamaina erabakigarria da aldaketa kimikoaren abiaduran (beheko irudia).
Irudian azaltzen da zergatik handitzen den erreakzio-abiadura, erreaktibo solidoaren zatien tamainaren arabera.
Erreaktibo solidoaren zatiketa-maila handitu ahala, haren eta beste erreaktiboaren (gasezkoa edo likidoa izan daiteke) arteko ukipen-azalera handitzen da. Bi erreaktiboen molekulen arteko talka eraginkorren kopurua handiagoa izango da, eta, beraz, erreakzio-abiadura handitu egingo da.
Askotan, erreakzio kimiko baten abiadura aldatu ahal izateko, zenbait faktore hainbeste aldatu behar ditugu, ezen ez den errentagarria. Kasu horretan, katalizatzaileak erabiltzen dira.
Erreakzio kimiko baten abiadura aldatzen duten substantzia kimikoak dira katalizatzaileak, erreaktiboen eta produktuen izaera aldatu gabe.
Ezaugarri horrez gain, beste bi propietate dituzte:
• Oso espezifikoak dira. Eskuarki, erreakzio kimiko bakoitzerako katalizatzaile jakin bat dago. Horien presentziak erreakzio kimiko jakin bat gertatzea eragiten du, eta ez posible den beste bat.
• Erreakzio kimikoan aldaketa iraunkorrik izan gabe parte hartzen dute. Katalizatzaile gehienak erreakzioa amaitzean berreskuratzen dira; horregatik, ekuazio kimikoan ez dira erreaktibo edo produktu gisa sartzen.
Entzimak katalizatzaile gisa
Hauek osatzen dituzte:
Ezaugarriak
Aplikazioak
Aminoazidoak (H, C, O, N, S konbinazioak) Haien egitura eta funtzioa
Hau zehazten dute:
• Erreakzio-abiadura aldatu egiten dute.
• Oso espezifikoak dira.
• pH eta T jakinetan jarduten dute.
• Digestio-sistema.
• Molekulen degradazioa.
Biologikoak
• Arnasketa zelularra.
• Energia-garraioa eta seinaleak.
• Botikak.
Industrialak
• Elikagaien ekoizpena.
• Bioerregaien garapena.
ULERTU, PENTSATU, IKERTU…
5 Azido sulfuriko kontzentratua urarekin nahastean, beti gehitu behar da, tantaz tanta, azidoa uraren gainean, eta ez alderantziz. Haien artean bortizki erreakzionatzen dutenez, azaldu zergatik hartzen dugun neurri hori. Erreakzio-abiadurari eragiten dion zer faktore fisikorekin lotuko zenuke?
6 Bilatu laktasari buruzko informazioa, eta zergatik pertsona batzuek ez duten esnea ondo digeritzen. Ezagutzen duzu beste entzima bat, funtzionatzen ez duenean elikagaien digestioan eragiten duena? Nola konpon daitezke gertaera horiek?
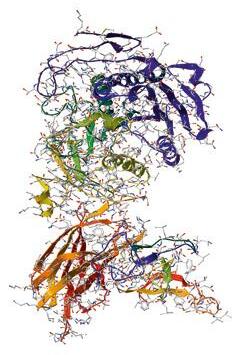
Entzimak organismoen barruan katalizatzaile gisa jarduten duten molekulak dira. Haren ekintza oso espezifikoa da; izaki bizidun baten barruan gertatzen den erreakzio kimiko bakoitzerako ia entzima bat dago.
Gizakien kasuan, haien presentzia ezinbestekoa da; izan ere, haien eragin katalitikoa behar bezala garatzen ez bada, tenperatura erregulatzeko funtzioa, presio arteriala edo DNAren eraketa kaltetu daitezke. Irudiak entzima baten hiru dimentsioko egitura erakusten du. Tamaina eta forma askotako entzimak daude.
7 Orri birakaria. Zer uste duzu gertatuko litzatekeela gure gorputzaren barruan gertatzen diren erreakzio kimikoak entzima katalitikoekin egingo ez balira?
8 Bilatu gure organismoko entzimen irudiak. Marraz itzazu zure koadernoan eta azal itzazu desberdintasunak eta antzekotasunak haien forma eta tamainetan. Zergatik uste duzu ematen direla?
9 Zergatik hondatzen da haragi xehatua xehatu ez den ezaugarri bereko haragi-puska bat baino lehen? Zer faktore fisikorekin lotzen duzu?
Erreakzio kimiko batean, komeni da jakitea substantzia bakoitzaren oinarrizko zenbat entitatek (N) parte hartzen duten. Horretarako, substantzia kantitatea izeneko magnitudea erabiltzen dugu.
Substantzia kantitatea (n) substantzia baten zati jakin batek dituen oinarrizko entitateen kopuruaren neurria da. Horren unitatea SI sisteman mol unitatea da.
Atomoen masa 10–27 kg, mailakoa denez, edozein substantziaren 1 kg-ko oinarrizko entitateen kopurua oso handia da. Karbono-12 isotopoaren masa erreferentziatzat hartuta, ezartzen da substantziaren mol batean 6,022 · 1023 oinarrizko entitate daudela. Balio hori konstantea da eta Avogadroren zenbakia número de Avogadro, (NA) deritzo.
1 mol H 2 O -ren analisia
hau du barne
18 g
6,022 · 1023 molekula bakoitzak masa hau du 18 u
Substantzia baten mol batek oinarrizko entitateen Avogadroren zenbakia du (NA = 6,022 · 1023 oinarrizko entitate/mol), eta karbono12ren 0,012 kg-tan dauden atomoak adina oinarrizko entitate dituen sistema baten substantzia-kantitatea da.
Hala, substantzia kantitatea (n) adierazpen honen bidez zehazten da:
N A =
■ Masa eta bolumen molarrak
soluto ó = horietatik horietatik
Substantzia kantitatea zeharka kuantifikatzen da, substantzia baten masa edo bolumena neurtuz eta erlazioak ezarriz:
• Substantzia baten masa molarra (M) substantzia mol baten masa (m) da, gramotan adierazia. Bere unitatea g · mol–1 da, eta bere balioa bat dator substantziaren masa molekularrarekin edo formula-unitatearekin.
() () () mol g mol g n M m –1 =

• Bolumen molarra mol batek presio- eta tenperatura-baldintza batzuetan betetzen duena da. Baldintza normaletan, b. n. (273 K eta 1 atm), edozein gasen bolumen molarra, gutxi gorabehera, 22,4 L/mol da.
Erreakzio kimiko asko ur-disoluzioan gertatzen dira, eta, beraz, komeni da erreaktiboen eta kontzentrazio molarrean dauden produktuen kontzentrazioa edo molaritatea adieraztea.
Disoluzio baten molaritatea (M) disoluzio litro bat duen solutu substantzia kantitatea da. Horren unitatea SI sisteman mol/L da.
Parametro hori ezagutzea baliagarria da disoluzioaren bolumena horrek duen substantzia-kantitatearekin zuzenean erlazionatzeko. Horrek erreakzionatzen duten substantzien kalkuluak azkar egiteko aukera emango digu. Hala, erlazio matematikoa hau da:
1 Lor ezazu Avogadroren konstantearen balioa (NA).
Mol bat C-12ren 0,012 kg-tan dauden atomoak adina oinarrizko entitate dituen sistema baten substantzia-kantitatea da, eta zenbaki hori bat dator NA-rekin:
NA = 6,022 · 1023 oinarrizko entitate/mol
C-12 isotopoak 12 u-ko masa duenez, hau da, 1,9932 · 10–26 kg (1 u = 1,661 · 10–27 kg), 0,012 kg-ko C-12-ren laginean dauden C-12 isotopoen kopurua hau izango da:
N 1 993210 0012 –26= →
,
, kg C12istop kg ooa
2 Kalkula ezazu zenbat molekula eta atomo dituen karbono dioxidoren 77 g-ko laginak. Zer bolumen hartzen du baldintza normaletan?
Datuak: M (C) = 12 g/mol; M (O) = 16 g/mol.
Lehenik, CO2-aren masa molarra kalkulatuko dugu: gmol M 12 1162 44 CO –1 2 =+ =
Hala, CO2-aren 77 g-ri dagokion substantzia kantitatea hau da:
g ,mol nM m 44 77 175 == =
CO2 molekula bakoitzean bi oxigeno atomo eta karbono atomo bat daude; beraz:
3 Kalkula ezazu sodio hidroxidoren disoluzio baten molaritatea, jakinik 500 mL-k 120 g NaOH dituela.
Datuak: M (Na) = 23 g/mol; M (O) = 16 g/mol; M (H) = 1 g/mol.
Lehenik eta behin, NaOH-aren masa molarra zein den zehaztuko dugu: gmol M 23 1161 11 40 NaOH –1 =+ +=
Masa molarretik abiatuta, dagoen substantzia kantitatea kalkulatuko dugu:
gmol g mol nM m 40 120 3 –1 == =
Disoluzioaren bolumena unitate egokietan adieraziko dugu: mL ,L V 500 05 disolución ==
Hala, sodio hidroxidoaren disoluzioaren molaritatea kalkula dezakegu: ,L mol M M 05 3 6 ==
Ikus ezazu molaritatea bere balio gisa adierazten dugula, M letra atzetik duela.
10 Kalkulatu amoniakoaren, hidrogeno kloruroaren eta kaltzio hidroxidoaren masa molarra.
11 Pentsatu eta partekatu bikotekidearekin. Aurreko ariketaren substantzietatik zeinek izango du substantzia kantitate handiena masa kilogramo batean?
12 Bilatu Avogadroren zenbakiaren zehaztapenari buruzko informazioa, eta egin txosten txiki bat.
13 Kalkula ezazu 2 M-ko NaOH-ren disoluzio baten 250 mL-ko substantzia kantitatea. Disoluzioa Ca (OH)2-koa bada, aldatu egingo da emaitza?
4
Ekuazio kimiko batean kalkulu estekiometrikoak egin ahal izateko, lehenik doitu egin behar dugu. Horretarako, koefiziente estekiometrikoak erabiltzen ditugu, bertan parte hartzen duten substantzia kantitatea, bai erreaktiboena bai produktuena, erlazionatzen dutenak. Ohartu zaitez koefiziente horiek NA-rekin biderkatzen baditugu, parte hartzen duten substantzien oinarrizko entitateen kopurua ezagut dezakegula.
4.1 Masa-masa kalkulu estekiometrikoak
Horiekin, erreakzioan parte hartzen duen substantzia baten (substantzia ezezaguna) masa kalkulatzen da, beste substantzia baten masatik abiatuta (datu-substantzia). Jarraitu beharreko urratsak hurrengo adibidean jaso dira.
ARIKETA EBATZIA
4 Potasio kloratoa, KClO3, potasio kloruroan eta oxigenoan deskonposatzen da. Kalkulatu beroaren eraginez 86,8 g potasio klorato deskonposatzean lortutako oxigeno masa.
Datuak: M (K) = 39,1 g/mol; M (Cl) = 35,5 g/mol; M (O) = 16,0 g/mol.
1 Erreakzionatzen duen eta espezie bakoitzetik sortzen den substantzia kantitatea erlazionatzeko, estekiometrikoki doitzen dugu erreakzioa:
() KClO s 2 3 → () () KClOsg23 2 +
2 Datu-substantzia eta substantzia ezezaguna identifikatzen ditugu:
() KClO s 2 3 → () () KClOsg23 2 + , g m 86 8 KClO3 =
3 Datu-substantziaren eta substantzia ezezagunaren masa molarrak kalkulatzen ditugu: ,; , g/molg/molMM 1226 32 0 KClO O 32 ==
4 Datu-substantziaren kantitatea kalkulatzen dugu bere masa molarrarekin: ,
, , gmol g mol n 1226 86 8 0 708 KClO –1 3 - =
5 Substantzia ezezagunaren kantitatea kalkulatzen dugu koefiziente estekiometrikoekin:
6 Substantzia ezezagunaren masa aurkitzen dugu bere masa molarrarekin:
,, mol32, 0g molg m 1062 33 984 O –1 2 ==

ULERTU, PENTSATU, IKERTU…
14 Kalkula ezazu adibideko erreakzioan lortzen den potasio kloruroaren masa.
15 Kalkula ezazu erreakzio honen arabera 426 g Cl2 erreakzionatzen badute lortzen den PCl3 substantzia kantitatea:
Cl2 + P4 → PCl3
16 Kalkulatu aurreko ariketaren erreakzioan behar den P4-ren substantzia kantitatea.
17 Egiazta dezagun. Kaltzio karbonatoa azido klorhidrikoarekin erreakzionarazten da, erreakzio honen arabera.
CaCO3 + 2 HCl → CaCl2 + H2O + CO2
Kalkulatu 350 g kaltzio karbonatotik lortzen den kaltzio kloruroaren masa.
18 Aurreko erreakzioan, ohiko kondizioetan, zenbat azido klorhidriko behar da?
Esan bezala, erreakzio kimiko asko ur-disoluzioan gertatzen dira, non ura disolbatzaile gisa aritzen den. Erreakzioan parte hartzen duten eta disoluzioan dauden substantzietarako (bai erreaktibo bai produktuetarako), ekuazio kimikoan substantziei (aq) laburdura erantsiz adierazten da hori.
Hala ere, urak, batzuetan, erreaktibo edo produktu gisa parte hartzen du erreakzioan. Ikus dezagun adibide bat hurrengo ariketa ebatzian, hobeto ulertzeko.
5 Kalkula ezazu zein den kaltzio hidroxidozko 0,1 M-ko disoluzio batetik 250 mL erreakzionatzeko behar den azido klorhidrikoaren 0,2 M-ko disoluzioaren bolumena. Erreakzio kimiko horren produktuak kaltzio kloruroa eta ura dira.
Aurreko orrialdeko ariketa ebatzian bezala, urrats hauei jarraituko diegu:
1 Doitutako ekuazio kimikotik abiatuko gara, eta datusubstantzia eta substantzia ezezaguna identifikatuko ditugu:
() () HClCa(OH)aqaq 2 2 + →
() HO CaCl aq 2 22 +
Kasu horretan, kaltzio hidroxidoa, Ca(OH)2, da datusubstantzia, eta substantzia ezezaguna azido klorhidrikoa, HCl, da.
Ikusi ura, disolbatzaileaz gain, erreakzioaren produktu bat dela.
2 Enuntziatuko datuak idatziko ditugu ekuazio kimikoarekin batera:
() () HClCa(OH)aqaq 2 2 + →
() HO CaCl aq 2 22 +
? V¿ HCl ; , mL L V 2500 250 Ca (OH) 2 ==
3 Molaritatearen definiziotik abiatuta, datu-substantziaren kantitatea kalkulatzen dugu:
() () L mol MV n = → () ()molLnMV =
ULERTU, PENTSATU, IKERTU…
19 Kalkulatu erreakzio honen arabera 0,2 mol zink erreakzionatzeko behar den 2,5 M-ko azido klorhidrikoaren disoluzioaren bolumena:
2 HCl + Zn → ZnCl2 + H2
20 Informa zaitez disoluzio baten kontzentrazioa adierazteko beste modu batzuei buruz. Zein abantaila du molaritatea erabiltzeak beste modu batzuen aldean kalkulu estekiometrikoak egiteko?
Gure kasuan:
,, , ML mol n 01 0250 0025 () Ca OH 2 ==
4 Ondoren, dagokion substantzia ezezagunaren kantitatea kalkulatzen dugu koefiziente estekiometrikoetatik abiatuta:
molCa(OH) molCa(OH) HCl n n
= =
0025 1 2 0050 ml de HCl o
, ,
HCl2 2 HCl
5 Azkenik, disoluzio ezezagunaren bolumena kalkulatzen dugu molaritatearen definiziotik abiatuta: () () L mol MV n = → () () L mol VM n =
Gure kasuan, datu hauek ditugu:
nHCl = 0,050 mol ; M = 0,2 mol/L
Beraz, enuntziatuaren disoluziotik 250 mL-ak guztiz erreakzionatzeko behar den azido klorhidrikoaren bolumena hau izango da:
(L) ,mol L ,(mol) ,L mL V 02 0 050 0 250 250 –1 == =
Gogoan izan urrats hauek ariketa mota horretarako egin ditugula, baina kontuan hartu behar ditugu enuntziatuak ematen dizkigun datuak, eskatutako soluzioa lortzeko.
21 A substantzia baten 2 M-ko disoluzioaren zer bolumen behar da B substantzia baten 2 M-ko beste disoluzio baten 3 mL guztiz erreakzionarazteko, A eta B-ren koefiziente estekiometrikoak berdinak badira?
22 Kalkula ezazu orrialde honetako ariketa ebatziaren azido klorhidrikoaren disoluzio-bolumena, erreaktibo horren kontzentrazioa 0,1 M bada. Zein da bi emaitzen arteko erlazioa?
Gas baten substantzia-kantitatea betetzen duen bolumenarekin erlaziona daiteke, haren presio- eta tenperatura-baldintzak ezagutzen baditugu. Magnitude horiek erlazionatzen dituen ekuazioa, gas ideala kontuan hartuta, hau da:
pVnRT =
non p presioa den; V, bolumena; n, substantzia kantitatea; T, tenperatura, eta R, gas idealen konstantea, zeinaren balioa adierazitako unitateen araberakoa den. Normalean, balio hau erabiltzen dugu:
R 0082 =
, Kmol atmL
Avogadroren legearen arabera, presio- eta tenperatura-baldintza berdinetan dauden bi gas-substantziak bolumen bera hartzen dute. Beraz:
Gasen arteko erreakzioetan, koefiziente estekiometrikoen arteko erlazioak gas-bolumenen artekoak bezalakoak dira, presio- eta tenperatura-baldintza berdinetan neurtuak.
6 Frogatu erreakzio kimiko honetako gasen bolumenen arteko erlazioa koefiziente estekiometrikoen artean lortzen dugunaren berdina dela, presioeta tenperatura-baldintza berdinetan neurtzen badira.
2 N2 (g) + 3 H2 (g) → 2 NH3 (g)
Koefiziente estekiometrikoen arteko erlazioa hau da:
2 mol N2-k 3 mol H2-rekin erreakzionatzen dira NH3-ren
2 mol lortzeko. Demagun presio- eta tenperatura-baldintzak p eta T direla.
ULERTU, PENTSATU, IKERTU…
23 Kalkula ezazu 3 litroko ontzi batean dagoen metano gasaren kantitatea p = 1,2 atm eta T = 27 °C badira. Ontzia 10 °C-raino hozten badugu, zein izango da presioaren balio berria?
24 Kalkula ezazu ateratzen den hidrogeno-bolumena (H2), 25 °C-an eta 0,98 atm-an neurtua, 41,4 g-ko sodio-lagin batek urarekin erreakzionatzen duenean, ekuazio kimiko honetan adierazten den bezala:
2 Na (s) + 2 H2O → 2 NaOH (aq) + H2 (g)
25 Egiaztatu gas idealen konstantearen balioa, SI-ko unitateetan adierazia, 8,31 J · K–1 · mol–1 dela.
26 Egiaztatu b. n.-etan neurtutako edozein gaseko mol batek (273 K eta 1 atm) 22,4 L-ko bolumena duela gutxi gorabehera.
Bolumenak ekuazio honen bidez kalkulatuko lirateke: VpnRT =
Erlazio estekiometrikoa erabiliz, hau dugu: ;; VpRTVpRTVpRT 23 2 NH NH 22 3 == =
(R · T/p) ez denez aldatzen, ondoriozta daiteke N2-ren
2 L-k H2-ren 3 L-rekin erreakzionatzen dutela NH3-ren
2 L lortzeko, koefiziente estekiometrikoen arteko erlazio bera erabiliz.
27 Kalkula ezazu kasu bakoitzean b. n.-etan askatutako CO2 bolumena, hau erretzean:
a) 5 mol propano.
b) 3 mol butano.
c) 2 mol metano.
28 Intuitzen eta deduzitzen dut. Lehenengo lau alkanoetako errekuntza-erreakzioetatik abiatuta, adierazi horietako bakoitzetik litro bat erretzean askatzen den CO2 bolumena eta masa, b. n.-etan neurtua.
CH4 + 2 O2 → CO2 + 2 H2O
C2H6 + 2 7 O4 → 2 CO2 + 3 H4O
C3H8 + 5 O2 → 3 CO2 + 4 H2O
C4H10 + 2 13 O2 → 4 CO2 + 5 H2O



Erreakzio kimiko bat gertatzen denean, beste prozesu batzuetan bezala, energia trukatzen da aldaketa gertatzen ari den sistemaren eta haren inguruaren artean.
Erreakzio kimiko batean eraldatzen den energia mota horri energia kimiko deritzo.
Energia kimikoa lotura kimikoekin eta molekulen arteko erakarpenekin lotuta dagoena da.
Erreakzionatzen duten substantzien multzoaren energia kimikoa aldatu egiten da, lotura batzuk hautsi eta berriak sortzen direlako, produktuak sortuz.
Bi egoera desberdin izan ditzakegu: bata, erreaktiboei erreakzioko produktuei baino energia gehiago dagokiena, eta, bestea, kontrakoa.
Lehenengo kasuan erreakzio exotermikoa izango da, eta bigarrenean, erreakzio endotermikoa.
Aldaketa kimiko baten energia kimikoa zenbatesteko, erreaktiboen eta produktuen energia-aldaketa erabil dezakegu: ∆E = Eproduktuak – Eerreaktiboak
Erreakzio endotermiko baterako energia-aldaketaren zeinua positiboa izango da; erreakzio exotermiko baterako, berriz, energia-aldaketaren zeinua negatiboa izango da.
Erreakzio kimiko oso exotermikoak daude; adibidez, errekuntzak. Horietan energia kimikoa askatzen da bero bidez.
Erreakzio kimiko batzuek, ordea, energia xurgatzen dute ingurunetik, eta hoztu egiten dute; erreakzio endotermikoak dira horiek.
Erreakzio exotermikoak
ERREAKTIBOAK
Erreakzio motak PRODUKTUAK
ERREAKZIOAREN AURRERAPENA
Erreakzio exotermiko batean, erreaktiboen energia handiagoa da produktuena baino, eta horregatik da negatiboa erreakzioaren energia aldaketa.
Erreakzio endotermikoak
PRODUKTUAK




ERREAKTIBOAK
ERREAKZIOAREN AURRERAPENA
Hala ere, erreakzio endotermiko batean, erreaktiboen energia txikiagoa da produktuena baino, eta erreakzioaren energiaren aldaketa positiboa da.
Sistema baten eta haren inguruen arteko edo bi sistemen arteko energia-trukea beroaren edo lanaren bidez gerta daiteke. Erreakzio kimiko bat gertatzen denean, erreakzionatzen duen sistemaren energia aldatu egiten da. Erreakzio-energiarekin edo erreakzio-beroarekin neurtzen dugu.
Erreakzio-beroa, Qr , erreakzio kimiko bat gertatzen den sistema baten eta haren inguruen artean bero gisa trukatzen den energia da.
Erreakzio-beroari esker, erreakzio endotermiko bat eta exotermiko bat bereiz ditzakegu. Horretarako, aurretik zeinu-irizpide bat definitzen dugu:
• Erreakzio endotermikoak. Erreakzio horiek gertatzen direnean, sistemaren energia handitu egiten da. Bero bidezko energia-trukea ingurunetik sistemara gertatzen da; erreakzio-beroa positiboa da.
• Erreakzio exotermikoak. Erreakzio horiek gertatzen direnean, sistemaren energia txikitu egiten da. Bero bidezko energia-trukea sistematik inguruneetara gertatzen da; erreakzio-beroa negatiboa da.
Aurreko orrian ageri diren energia-diagrametan, erreakzio kimiko baten hasierako eta bukaerako egoeren energiari buruzko informazioa baino ez da ematen. Hala ere, sistemaren bilakaera konplexuagoa da erreakzioan. Gogoratu erreaktiboen partikulen arteko talka guztiak ez direla eraginkorrak, guztiek ez baitute orientazio egokia eta energia nahikoa.
Erreakzio kimiko batean zehar, erreaktiboen eta produktuen artean energiaren trantsizio-egoera bat ematen da, biena baino energia handiagoarekin. Puntu horretan sortzen da aktibatutako konplexua.
Erreakzioa endotermikoa edo exotermikoa den kontuan hartu gabe, erreakzio kimiko guztietan energia-egoera horretatik pasatzen da.
Aktibazio-energia. Katalizatzaileak
Aktibazio-energia katalizatzailerik gabe, Ea
ERREAKTIBOAK
Katalizatu gabeko erreakzioa
Aktibazio-energia katalizatzailearekin, Ea '
Erreakzio katalizatua
ERREAKZIOAREN AURRERAPENA
PRODUKTUAK


Erreaktiboen eta trantsizio-egoeraren arteko energia-aldeari aktibazio-energia deritzo. Energia hori hesi bat da, eta nahikoa energia duten eta eraginkortasunez talka egiten duten erreaktibo-partikulek baino ez dute gaindituko.
Energia hori oso handia denean eta erreaktiboek ezin dutenean gainditu, katalizatzaileak erabiltzen dira. Substantzia horiek aktibazio-energia gutxitzen dute, eta energia-bide hobea ematen dute; hala, erreaktiboak produktu bihurtzen dira.
Ekuazio termokimiko deitzen diogu erreakzio kimiko batean parte hartzen duten substantziez gain, haien agregazio-egoerez eta zenbat energia erabiltzen den jakinarazten digun horri. Ekuazio termokimiko batean agertzen den erreakzio-beroaren balioa hauen araberakoa da:
• Erreaktiboen eta produktuen agregazio-egoera, egoera-aldaketa batek energia-aldaketa eragiten baitu.
• Erreakzionatzen duen substantzia kantitatea, beraz, erabili diren koefiziente estekiometrikoen balioetan jarri behar da arreta.
Adibidez, ekuazio termokimiko honek jakinarazten digu gas-butano mol baten errekuntzan (C4H10) 2 877 kJ askatzen direla CO2 gas-egoeran eta ur likidoa lortzen baditugu:
() ()gg 2 13 CH O 4102 + → () ()gl Q kJ 45 2 877 CO HO –r 22+= Errekuntza-erreakzioetarako, hala nola adibidekoa, erreakzio-beroari errekuntza-bero deritzo, eta erregaiaren mol bati dagokio.
Batzuetan, ekuazio kimikoan integratutako erreakzio-beroa aurkitu dezakegu; erreakzio endotermikoa bada, erreaktiboei gehituta egongo da, eta exotermikoa bada, produktuei gehituta.
7 Kalkulatu 1 kg butano erreakzionatzean askatzen den energia eta 1 kg metano erreakzionatzean askatzen dena. Datuak:
Qr (CH4) = –890 kJ/mol; Qr (C4H10) = –2 877 kJ/mol; M (C) = 12 g/mol, M (H) = 1 g/mol.
Errekuntza-beroak mol bat erregairi dagozkio. Beraz, bakoitzaren substantzia kantitatea kalkulatu behar dugu, erreaktiboei gehituta.
Aldez aurretik, masa molarrak ezagutu behar ditugu, formula molekularren bidez kalkulatuko ditugunak:
/ gmol M 12 11 416 CH4 =+ =
/ gmol M 12 41 10 58 CH410 =+ =
Erregai bakoitzaren substantzia kantitatea kalkulatuko dugu:
/ , gmol g mol n 16 1000 62 5 CH4 ==
/ , gmol g mol n 58 1000 17 2 CH410 - =
Eta, azkenik, horietako bakoitzak bere errekuntzan askatutako beroa:
29 Erreakzio endotermiko bat gertatzen ari den edalontzi bat ukitzen badugu, zer sentsazio izango dugu?
30 Bilatu erreakzio exotermiko eta endotermikoen adibideak, eta aipatu haien aplikazioak eguneroko produktuetan.
31 Zer esan dezakezu erreakzio kimiko batez, Qr = –287,9 kJ/mol bada? Eta kontrako zeinua balitz?
32 Orri birakaria. Katalizatzaile baten presentziak, Qr-en balioa aldatzen du?
33 Marraztu ezazu eskema bat, erreakzio endotermiko zein exotermikoetan gertatzen diren energia-trukeak irudikatzeko.
34 Arrazoitu erreakzio bat endotermikoa edo exotermikoa den, haren ekuazio termokimikoko erreakzio-beroa erreaktiboetan gehitutako zeinu positibokoa bada.
35 Kalkula ezazu zer energia behar den 75 g nitrogeno monoxido sortzeko, erreakzio honen arabera:
N2 (g) + O2 (g) + 181 kJ → 2 NO (g)
36 Mahai-ingurua. Azido bentzoikoaren errekuntzaberoa –26,42 kJ/g da:
a) Erreakzio endotermikoa edo exotermikoa da
b) Zenbat energia askatzen da bero gisa 3 mol azido bentzoiko (C7H6O2) erretzean?
Estekiometria-ariketa bat nola ebatzi
1. ADIBIDEAAluminio puruaren lagin batek erreakzionatu egiten du 5 M-ko kontzentrazioko azido klorhidrikoaren (HCl) disoluzio baten 150 mL-rekin. Aluminio kloruroa (AlCl3) sortzen da eta hidrogeno gaseosoa (H2). askatzen da. Zein masa zuen aluminio-laginak? Zenbateko hidrogeno-bolumena askatu da b. n.-etan neurtzen bada? Datuak: M (Al) = 27 g/mol.
ULERTU ENUNTZIATUA ETA ATERA DATUAK
Bilatu ulertzen ez dituzun eta garrantzitsutzat jotzen dituzun terminoen esanahia. Bigarren irakurketa egin ondoren, atera ematen diren datuak eta identifikatu zer eskatzen den. Gogoratu magnitudeak sinboloarekin adieraztea, eta saiatu substantzietarako azpiindizeak erabiltzen.
EGIN EGOERAREN MARRAZKI BAT
Estekiometria-problema da, erreakzionatzen duten substantziei buruzko datuak ematen baitizkigute. Ekuazio kimiko doitua idatzi behar dugu, substantzien datuekin eta masa molarrekin batera.
IDENTIFIKATU ESKU HARTZEN
DUTEN LEGE FISIKOAK
• Masa molarra, substantzia kantitatea eta masa:
() () mol g nM m =
• Gas idealen legea, P · V = n · R · T, erreaktiboak edo gas-produktuak badaude.
• Molaritatearen definizioa:
() () L mol MV n =
• Erreakzio-beroaren definizioa.
LORTU EMAITZA ETA AZTERTU HAREN BALIOZKOTASUNA
• Egin ezazu problema ebazteko zure estrategia gauzatzeko behar diren kalkuluak, eta gogoratu koherentziaz jokatu behar duzula inplikatutako magnitudeen unitateetan.
• Aztertu emaitza eta, beharrezkoa bada, egin horren iruzkina.
EBAZPENA
• Enuntziatuak erreakzio kimiko bat deskribatzen du.
• Datu-motak bereizten ditugu:
– Datu-substantzia: azido klorhidrikoa: VHCl = 150 mL; 5 M = 5 mol/L
– Substantzia ezezagunak: mAl eta VH2 eta b. n.-etan.
Ekuazio kimiko doitua hau da:
2 Al (s) + 6 HCl (aq) → 2 AlCl3 (aq) + 3 H2 (g) mAl V = 150 mL VH2 , b. n.
MAl = 27 g/mol 5 M
Beraz, 2 mol Al 6 mol HCl-rekin konbinatzen dira, eta 2 mol AlCl3 eta 3 mol H2 ematen dituzte.
Kasu honetan, sekuentzia honi jarraitu behar diogu:
1. Kalkulatu datu-substantziaren kantitatea: n (mol) = M · V (L)
2. Erlazio estekiometrikotik abiatuta, ezezagun-konposatu bakoitzaren substantzia kantitatea kalkulatzen da.
3. Kalkulatu substantzia ezezagunen masa eta bolumena, masa molarretik eta gasen ekuaziotik abiatuta, hurrenez hurren.
HCl kantitatea kalkulatzen dugu: ,, L mol Lmol n 50 15 075 HCl $ ==
Balio horrekin, Al eta H2-ren kantitatea aurkituko dugu: ,, molHCl 6mol HCl 2mol Al mol n 0750 25 Al == ,, molHCl 6mol HCl 3 mol H mol n 0750 375 H 2 2 ==
Al-ren masa eta H2-ren bolumena kalkulatzen ditugu: , , mol g/mol g m 02527 675 Al == ,, , atm mol Kmol atmL K
V 1 0 375 0 082 273 839 H2
Kalkula ezazu bero moduan askatzen den energia, 440 g propano behar adina oxigenorekin erreakzionatzen dutenean. Datua: Qr = –2 218,8 kJ/mol.
• Enuntziatuak erreakzio exotermiko bat eta bero gisa askatzen den energia deskribatzen ditu.
• Ateratzen ditugun datuak:
– Datu-substantzia: propanoa, C3H8: mg 440 CH38 =
– Erreakzio-beroa: Qr = –2 218,8 kJ/mol
Ekuazio kimiko doitua hau da:
C3H8 + 5 O2 → 3 CO2 + 4 H2O Qr = –2 218,8 kJ /g mol M 44 CH38 =
Horrek esan nahi du propano mol bat erretzean 2 218,8 kJ askatzen direla.
Kasu honetan, sekuentzia honi jarraitu behar diogu:
1. Kalkulatu datu-substantziaren kantitatea:
() () mol g nM m =
2. Kalkulatu bero moduan askatutako energia, ekuazio termokimikotik abiatuta.
37 Kalkula ezazu lehenengo adibide ebatziaren erreakzio kimikotik abiatuta sortu den aluminio kloruroaren masa. Datua: M (Cl) = 35,5 g/mol.
38 Kalkulatu lehenengo adibidetik askatutako hidrogenobolumena, 25 °C-an neurtzen bada. Adibidekoa baino handiagoa edo txikiagoa izango da?
39 Kalkula ezazu bigarren adibideko propano-kantitate osoa erretzeko zenbat oxigeno behar den.
40 Arkatzak erdira. Kaltzio hidruroak urarekin erreakzionatzen du erreakzio kimiko honen arabera:
CaH2 (s) + H20 (l ) → Ca(OH)2 (s) + H2 (g)
a) Doitu ekuazio kimikoa.
b) Kalkula ezazu zenbat kaltzio hidruro erreakzionatuko duen 3,6 mol urarekin.
c) Kalkulatu ur kantitate berarekin sortzen den kaltzio hidroxidoaren masa.
d) Zer hidrogeno-bolumen askatzen da, 300 K-etan eta 1,2 atm-tan neurtuta, erreakzionatzen duen uretatik abiatuta?
Datuak: M (Ca) = 40 g/mol; M (O) = 16 g/mol; M (H) = 1 g/mol.
41 Zer energia askatzen da C2H4O2-ren 330 g oxigeno-kantitate nahikoarekin erreakzionatzen dutenean? Erreakzioa
b. n.-etan gertatuko balitz, zer CO2-bolumen eratuko litzateke? Eta zer ur-bolumen? Qc = –875,4 kJ/mol.
Datuak: M (C) = 12 g/mol; M (O) = 16 g/mol; M (H) = 1 g/mol.
C3H8 kantitatea kalkulatzen dugu masa molarraren (M ) artean zatituz. Honela adieraz dezakegu:
44 g/mol g mol n 440 10 CH38 ==
Askatutako energia kalkulatzen dugu:
Energa – 38 38 ==
i molC H 1mol CH (–2 218,8 kJ) kJ 10 22 188
Emaitza zeinu negatiboarekin adierazten dugu, energia askatua dela adierazteko.
42 Burdin lagin bat 200 mL azido sulfurikorekin H2SO4 nahasten da, 3,5 M-ko kontzentrazioarekin. Erreakzio horretan, hauek sortzen dira: hidrogenoa gas-egoeran eta burdin sulfatoa (II). Zein masa zuen burdin laginak? Zer hidrogeno-bolumen askatzen da 30 °C-an eta 0,95 atm-an neurtuta?
Datuak: M (Fe) = 55,8 g/mol; M (S) = 32 g/mol; M (O) = 16 g/mol; M (H) = 1 g/mol.
43 Hidrogenoa lortzeko moduetako bat metanoaren erreformatzea da:
a) Doitu ekuazio kimikoa.
b) Kalkula ezazu 100 ºC-tan eta 1 atm-tan neurtutako metano-bolumena, baldintza berdinetan neurtutako 150 m3 hidrogeno ekoizteko beharrezkoa dena.
c) Zenbat CO (mol-etan) sortuko litzateke?
Unitate honetan, ekuazio kimiko batek ematen digun informazioa, desagertu eta produktu bihurtzen den erreaktibo-kantitatea, erreakzio kimiko baten oreka eta
itzulgarritasuna, eta zenbait faktorek erreakzio kimikoetan duten eragina aztertzeko aukera emango diguten simulazioak egingo ditugu.
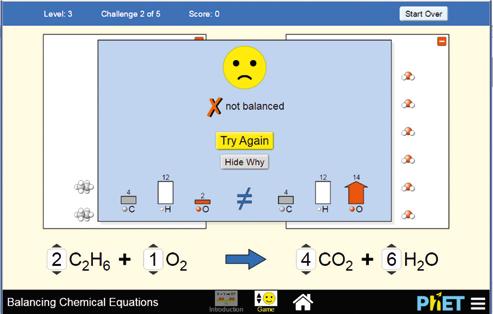
Anaya-ren webgunean eskuragarri dagoen aplikazio bat erabiliko dugu: Ekuazio kimikoen balantza. Aplikazio honek bi zati ditu: Sarrera eta jolasa.
• Aplikazio honetan, erreakzio kimikoen doikuntza modu bisual eta intuitiboan egiten da, eta erreaktiboetako eta produktuetako elementu bakoitzaren atomo-kopurua berehala kontatzen da. Hasteko, erabili Sarrera atala; aktibatu goiko eskuineko izkinan elementuen balantza bistaratzeko tresna.
• Aplikazio hau erabil dezaketen molekulen edo oinarrizko entitateen kopuruak zenbaki osoa izan behar du.
• Erabili orain jokoa zailtasun handiagoko ekuazioak doitzeko. Ariketaren bat ondo egiten ez baduzu, aplikazioak aukera ematen dizu jakiteko zergatik eta beste saio bat egiteko, hurrengo irudian erakusten den bezala.
Oraingo honetan, hemen eskuragarri dagoen aplikazio bat erabiliko dugu: https://phet.colorado. edu/es/simulations/reactions-and-rates
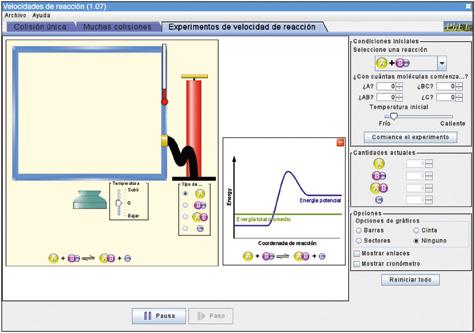
Simulazioak hiru zati ditu: Talka bakarra, Talka asko eta Erreakzio-abiadurako esperimentuak. Hiru kasuetan, erreakzio itzulgarria da, hau da, erreakzio-produktuak sortzen direnean, elkarri eragiten diote, eta erreaktiboak sortzen dira berriro. Orduan, oreka kimikoa lortu dela esaten dugu. Erreakzio kimiko askotan ematen da egoera hori.
Erreakzio itzulgarriak
Erreakzio-abiadurako esperimentuak fitxatik hasiko gara. Hemen, aplikazioak aukera ematen du erreaktiboen molekula-kopurua aldatzeko. Eskuineko aldean, esperimentua kontrolatzeko aukerak
ditugu:
Beraz, interpreta dezakegu koefiziente estekiometrikoek adierazten dutela erreakzioa abiaraztean zenbat erreaktibo-entitate dagoen eta erreakzioa bukatzean zenbat produktu-entitate egongo diren. Baina hori ez da beti horrela; erreakzioa itzulgarria den ala ez hartu beharko da kontuan, hau da, oreka kimikoko egoerara iristen den.
• Erreakzioa hautatzea. Erreakzioetako bat erabil dezakegu, edo bat diseina dezakegu, energiadiagraman oinarrituta. Erreakzio endotermikoak edo exotermikoak izateko, erreaktiboen eta produktuen energia-balioak edita daitezke, baita aktibazio-energiaren balioa ere, katalizatzaile baten presentzia simulatzeko.
• Hasieran dagoen molekula-kopurua. Erreakzioaren hasieran erreaktibo-molekulen eta produktuen molekulen kopurua aldatzeko aukera ematen digu.
• Hasierako tenperatura.
• Grafikoen aukerak. Barra-grafikoak erakusten du zenbat erreaktibo eta produktu dauden, eta zintaren grafikoa deritzonak erreakzioaren aurrerapenari buruzko ideia bat ematen du.
Erreaktibo bakoitzeko hamar molekularekin eta tenperatura-balio nahiko handiarekin egingo dugu ariketa. Gainera, barra-grafikoa agertzea markatuko dugu.
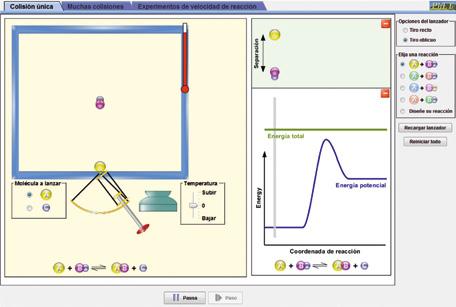
Simulazioaren atal honetan, bi erreaktibo-molekulen orientazio erlatiboak eta talkaren energiak duten eragina ikus dezakezu. Orientazio erlatiboak talka eraginkorra izatea eragiten duen edo ez ikusteko, jaurtitzailearen aukeretan (goiko eskuineko izkinan), jaurtiketa zeiharra aukeratu behar duzu, eta erreaktibo-molekula energia nahikoarekin jaurti.
Erreakzioan, barrek grafikoan duten altuera-aldaketa ikusiko dugu; hasieran, erreaktiboen kopurua gutxituz doa, eta produktuena, berriz, handituz. Gero, kontrakoa gertatzen da. Eta, azkenik, denbora pasatzen uzten dugunean, kantitateak konstante mantentzen dira eta altuerak ia-ia berdintzen dira. Puntu horretan oreka kimikoa lortzen da.
Izan den erreakzioa itzulgarria da, bi erreakzio gertatzen baitira aldi berean: zuzena, non erreaktiboek produktuak sortzen dituzten, eta alderantzizkoa, non produktuek erreakzionatu eta erreaktiboak ematen dituzten.
1 Egin esperimentuak talka bakar batekin, energia eta jaurtiketa-angelua aldatuz. Atera talka eraginkor bat gertatzeko probabilitatearen ondorioak eta adierazi zer faktoreren mende dagoen.
2 Egin ezazu erreakzio-abiaduraren esperimentu bat eskainitako lehenengo erreakzioarekin, erreaktiboen molekula kopurua aldatuz. Aktibatu kronometroa eta erreakzioa-
Talka-energiaren eragina jaurtiketak eginez ikus daiteke, jaurtitzailearen angelua gehiago edo gutxiago handituz. Jaurtiketaren energia erreakzioaren aktibazio-energia baino txikiagoa bada, ez duzu talka eraginkorrik izango. Erreakzioaren energia-diagrama bistaratzeko, energia-grafikoa aukera aktibatu behar duzu. Erreakzioaren energia-diagrama ikusi ahal izateko, aktibatu energia-grafikoa ikusteko aukera. Grafiko horretan, abzisa-ardatzak «erreakzio-koordenatua» adierazten du, hau da, erreakzioak denborarekin egiten duen aurrerapena. Koordenatu hori bi erreaktibo-molekulen arteko distantziarekin lotuta dago: elkarrengandik hurbil badaude, distantzia txikitu egiten da, eta koordenatuaren balioa handitu egiten da; izan ere, zenbat eta hurbilago egon, orduan eta aurreratuagoa dago erreakzioa, elkarrengandik hurbilago dago bien arteko talka, eta errazagoa da erreakzioaren produktua lortzea.
ren eboluzio-diagrama, erreakzioak egonkortzen zenbat denbora behar duen ikusteko. Jaso zure emaitzak taula batean, eta atera ondorioak erreaktiboen kontzentrazioaren eraginari buruz. Zergatik esaten dugu oreka kimikoa dinamikoa dela?
3 Egin esperientzia bera tenperatura aldatuz. Atera ondorioak.
Jolaszientzia
Burdinaren oxidazio-erreakzioa
Sarrera
Adibide gisa gehien erabiltzen den erreakzio kimikoetako bat burdinaren oxidazioa da; izan ere, pH neutroa dagoenean, burdin oxido(III) hidratatuaren hauspeatze bat sortzen da, kolore arre gorrixka deigarrikoa, eta, horri esker, kolore-aldaketaren ondoriozko aldaketa kimikoa ikus daiteke Oxidazio-prozesuaren abiaduran eragiten duten faktore batzuen gainean jarduteko esperientzia proposatzen dizugu. Horretarako, hauek behar dituzu: burdinazko iltzeak, ur gogorra (edo salfumana, drogerietan saltzen den azido klorhidrikoaren disoluzioa), ura, sodio kloruroa (gatz arrunta), ozpina, olioa, sodio hidroxidoa, azalera handiko eta sakonera txikiko lau ontzi.
Esperimentu batzuk egingo ditugu, modu kualitatiboan ikusteko nola eragiten dion ingurune kimikoak (pH-a eta gatzen presentzia) burdinazko iltzeen oxidazioari.
Esperimentua Ur irakina (ZURIA)
NaCl-aren disoluzioa (Itsas ingurunea)
Emaitzak alderatu ahal izateko, erreferentziako esperimentu zuri bat behar dugu, ur irakinarekin egingo duguna, disolbatutako oxigenoaren zati bat kentzeko.
Ontziak prestatzea
• 1. ontzia: iltze bat + ur irakina.
• 2. ontzia: iltze bat + sodio kloruroaren disoluzio bat.
• 3. ontzia: iltze bat + azido klorhidrikoaren disoluzio bat.
• 4. ontzia: iltze bat + ozpina.
• 5. ontzia: iltze bat + ura eta olioa.
Esperimentu horiekin, kostaldeko, pH azidoko eta leku lehorragoetako giro kimikoa erreproduzitzen dugu.
HCl-aren disoluzioa edo ozpina (pH azidoa) Ura eta olioa (Ingurune isolatua)
Behaketa 24 ordu igaro ondoren
2. ontziko oxidazioaren ondorioz, burdin oxidoa(III) sortzen da, eta uretan esekita geratzen da, hauspeatze koloidal gisa. Gainerako ontzietan hauspeatze arre gorrixka hori ikusten duzu? Hala ez bada, ez du esan behar burdina ez dela oxidatu, baizik eta burdin oxidoa(III) disolbatuta geratu dela, ingurune azidoan ez baita hauspeatzen.

Oxidaziorik badagoen edo ez egiaztatzeko, sodio hidroxidozko disoluzio-tanta batzuk gehitu; hauspeatzea sortzen bada, lehenago oxidazioa gertatu dela esan nahi du.
Jarduera amaitu ondoren, zer iritzi duzu herdoil-hondarrak azido klorhidrikoarekin garbitzeari buruz?
Prozedura
Segurtasun neurriak
Bi erreakzioetan gasak askatzen direla ikusiko da. Jaurtiketak saihesteko, erabili segurtasun-betaurrekoak.
1. esperientzia.
Erreaktibo solido baten zatiketa maila
• Jarri saio-hodi batean kareharri lainoztatuko masa ezagun bat, eta beste batean marmol zatituko masa bera. Gehitu ura hodi bakoitzari marmol-zatia murgildu arte eta, kareharri lainoztatuaren kasuan, esekidura bat lortu arte.
• Kokatu beste bi saio-hoditan azido klorhidrikoaren disoluzioaren kantitate bat, kantitate bera bietan.
• Gehitu kontu handiz azido klorhidrikoaren disoluzioak marmol-zatiak eta kareharri lainoztatua dituzten saio-hodien gainean. Idatzi zer gertatzen den.

2. esperientzia.
Erreaktibo baten kontzentrazioa
Problemaren planteamendua
Erreaktibo solido baten zatiketa-mailak, kontzentrazioak eta katalizatzaileek erreakzio-abiaduran duten eragina aztertzea.
Horretarako, bi erreakzio kimiko hauekin esperimentuak egitea proposatzen dizugu:
1. erreakzioa: CaCO3 (s) + 2 HCl (aq) → CaCl2 + CO2 (g) + H2O
2. erreakzioa: 2: Zn (s) + H2SO4 (aq) → ZnSO4 + H2 (g)
Zure proposamena
Diseinatu praktika bat, kualitatiboki egiaztatzeko nola eragiten dioten erreaktibo solidoaren kontzentrazioak eta zatiketa-mailak lehenengoaren erreakzio-abiadurari, eta katalizatzaile bat egoteak bigarrenari.
Gure proposamena
Bi erreakzioetan gas bat askatzen da. Beraz, gasaren burbuila-abiadurak erreakzioaren abiaduraren ideia bat eman dezake. Kasu bakoitzean aztertutako faktorea bakarrik aldatu behar da.
Material
• Kareharri lainoztatua • Marmol-zatiak • Azido klorhidrikoaren disoluzioa • Kobrezko eta zinkezko txirbilak • Azido sulfuriko diluituaren disoluzioa • Saio-hodiak • Tentegailua • Matraze aforatua
• Ur destilatua.
• Abiapuntuko azido klorhidrikoaren disoluziotik abiatuta, prestatu beste bi azido diluituago, kontzentrazioa hasierakoaren erdia izan arte.
• Errepikatu berriz 1. esperientzian egindakoa, baina ur destilatuan dagoen marmol-laginarekin bakarrik. Errepikatu esperientzia hiru aldiz, bat hasierako azido klorhidrikoaren disoluziorako, eta beste biak, diluituetarako.
3. esperientzia.
Katalizatzaile baten presentzia
• Saio-hodi batean, jarri zinkezko txirbilak eta estali azido sulfuriko diluituko disoluzio batekin. Behatu eta idatzi zer gertatzen den.
• Beste saio-hodi batean, jarri, zinkezko txirbilekin batera, kobrezko beste batzuk, eta bota azido sulfuriko diluitu kantitate bera. Behatu eta idatzi zer gertatzen den.
2 3.
katalizatzailea, kobrea eta azidoa soilik gehituz. Zer ikusten duzu?
abiatuta,
3 3. esperientziaren antzeko emaitzarik izango genuke kobrea erabili beharrean kobre sulfatoa bezalako konposatu bat erabiliko bagenu? Esan dezakegu kobre sulfatoak erreakzioa katalizatzen duela? Azaldu zure erantzuna.
Antolatu zure ideiak Kontzeptu-mapa sistemikoa
1 Azaldu, zure marrazkien bidez, erreakzio-abiadurari eragiten dioten faktoreak eta erreakzio endotermiko baten eta exotermiko baten arteko aldea.
2 Osatu beheko eskema kontzeptuala unitate honetan ikasi dituzun edukiekin, A, B, C, D eta E letrekin adierazitakoez gain.
Erreakzio kimiko bat
honela osatuta dago: honen bidez adierazten da: honen berri ematen digu:
A produktuak
haren loturei hau gertatzen zaie:
B hautsi egiten dira
D osagaien agregazioegoera erreakzioenergia
E negatiboa
Gogoan izan zenbakizko jarduera guztien soluzioak anayaharitza.es helbidean dituzula.
Aldaketa kimikoak
1 Ideia-biltzarra. Aipa itzazu zure eguneroko bizitzan gertatzen diren bost aldaketa kimiko, gertatzen direla dakizunak.
2 Egiazta dezagun. Doitu ekuazio hauek:
a) MgCl2 + Li2CO3 → MgCO3 + LiCl
b) P4 + O2 → P2O3
c) MgI2 + Mn(SO3)2 → MgSO3 + MnI4
d) C3H6O + O2 → CO2 + H2O
e) SeCl6 + O2 → SeO2 + Cl2
3 Egiaztatu aurreko erreakzio kimikoetan masa kontserbatzeko legea betetzen dela, horietan dauden substantziak osatzen dituzten atomoen masa kontuan hartuta.
4 1-2-4. Zer lotura hautsi eta eratzen dira aldaketa kimiko horietan?
Erreakzio-abiadura
5 Azaldu erreaktiboen kontzentrazioak erreakzio-abiadurari nola eragiten dion, horretarako talken teoria erabiliz
6 Azaldu nola eragiten dion tenperaturak erreakzio kimiko baten abiadurari, teoria zinetikoaren arabera.
7 Azaldu ezazu zein abantaila dituen muturreko presio- eta/edo tenperatura-baldintzak behar dituzten erreakzioetan katalizatzaileak erabiltzeak
8 Neurtu erreakzio kimiko batean dagoen substantzia baten kontzentrazioa eta lortu datu hauek:
13 Idatzi formula eta kalkulatu substantzia horien masa molarrak:
a) Kaltzio kloruroa. e) Dikloroa.
b) Zilarra. f) Aluminio trikloruroa.
c) Diburdin trioxidoa. g) Azido sulfhidrikoa.
d) Ozonoa. h) Azido sulfurikoa.
14 Kalkula ezazu disoluzio hauen molaritatea:
a) 200 g sodio hidroxidoren masa, guztira 500 mL-ko bolumena duena.
b) 20 g sodio nitratoren masa bat uretan, 250 mL-ko bolumena osatu arte.
a) Erreaktibo bat ala produktu bat da?
b) Adierazi kontzentrazio-datuak denborarekiko. Puntu bakoitzeko grafikoaren malda erreakzioabiaduraren neurri bat da. Erreakzioak aurrera egin ahala handitu edo txikitu egiten da erreakzioabiadura? Azaldu zure behaketa.
Substantzia kantitatea
9 Adierazi baieztapen hauek egiazkoak edo gezurrezkoak diren:
a) Mol bat uretan eta mol bat butanoan molekula kopuru bera dago.
b) Mol bat uretan eta mol bat butanoan hidrogeno atomo kopuru bera dago.
c) Mol bat uretan mol bat oxigeno atomo eta bi mol hidrogeno atomo daude.
d) Mol bat uretan 1,8066 · 1024 atomo daude.
e) Mol bat uretan 1,8066 · 1024 molekula daude.
10 Adierazi zenbat atomo dauden 360 g kobretan.
11 Kalkula ezazu gramo bateko amoniakoren, hidrogeno kloruroren eta kaltzio hidroxidoren laginek dituzten hidrogeno atomoen kopurua. Zer hidrogeno-masa du lagin bakoitzak?
12 Osatu taula 20 mol urarentzat:
c) Azido nitrikoaren disoluzioa uretan, zeinaren dentsitatea 1,12 g/cm3 den, eta % 80ko aberastasuna (% masan) duen.

d) Azido klorhidrikoaren eta uraren 2 M-ko disoluzio baten 200 mL-tik abiatuta prestatutako disoluzioa, 500 mL-ko bolumena osatu arte.
15 Kalkula ezazu aurreko ariketako (d) ataleko disoluzioak duen azido klorhidrikoaren substantzia kantitatea eta diluzio-prozesua egin aurretik zegoena; zer ikusten duzu?
16 Kalkulatu 70 g amonio kloruroren disoluzio baten molaritatea 500 mL-ko disoluzioan. Zenbat H atomo ditu?
Kalkulu estekiometrikoak
17 Kaltzio karbonatoa kaltzio oxidoaren eta karbono dioxidoaren bidez deskonposatzen da beroaren eraginez.
a) Idatzi ekuazio kimiko doitua.
b) Kalkula ezazu zenbat karbono dioxido sortzen den 150 g kaltzio karbonato erreakzionatzen badute.
18 Litio hidroxidoak hidrogeno bromuroarekin erreakzionatzen du litio bromuroa eta ura emateko.
a) Idatzi ekuazio kimiko doitua.
b) Kalkula ezazu zenbat hidrogeno bromuro behar den 5 mol litio hidroxidok erreakzionatzeko.
c) Zein masari dagozkio aurreko atalean lortutako emaitzak?
d) Kalkula ezazu 5 mol litio hidroxidotik lortzen den produktu-masa.
e) Egiaztatu, ariketako datuekin, masa kontserbatzeko legea betetzen dela.
19 3 M-ko azido sulfurikoren disoluzio baten 250 mL daude. Kalkulatu azido sulfurikoaren disoluzioak erabat erreakzionatzeko behar den 1,5 M-ko sodio hidroxidoaren disoluzio-bolumena.
20 Litopoi-zuria edo bario-zuria (ZnS + BaSO4) akuareletan erabiltzen den pigmentua da, eta bere disoluzioetatik abiatuta, gatz disolbagarriak hauspeatuz prestatzen da, erreakzio kimiko honen arabera:
BaS (aq) + ZnSO4 (aq) → ZnS (s) + BaSO4 (s)
a) Izendatu erreakzio kimiko honetan agertzen diren konposatu guztiak. Zein dira erreaktiboak eta zein produktuak?
b) Kalkula ezazu 0,2 M-ko zink sulfatozko disoluzio baten 300 mL 0,3 M-ko bario sulfuroko disoluzio baten kantitate nahikoarekin erreakzionatzean lortzen den litopoi-masa.
c) Kalkulatu bario sulfuroaren beharrezko disoluzioaren bolumena.
21 Kalkula ezazu lortzen den amoniakoaren bolumena, 68 °C-tan eta 704 mmHg-tan neurtua, baldintza beretan neurtutako 27,4 L nitrogeno erreakzionatzen badute behar adina hidrogenorekin, erreakzioaren arabera:
() () NHgg 3 22 + → () NH l 2 3
Zer hidrogeno beharko litzateke erreakzioa gertatzeko?
22 Metalek azidoekin erreakzionatzen dute hidrogenoa askatuz.
a) Idatzi zinkaren eta azido klorhidrikoaren erreakzioa.
b) Zer bolumen izan behar du 3 M-ko azido klorhidrikoak 60 g Zn-ek erreakzionatzeko?
c) Kalkula ezazu askatzen den hidrogeno-bolumena, 1 atm-tan eta 298 K-tan neurtzen badugu.
d) Kalkulatu erreakzio horretan parte hartzen duten substantzia guztien masak, eta egiaztatu masa kontserbatzeko legea betetzen dela.
Energia erreakzio kimikoetan
23 Diagraman, adierazi erreakzio katalizatuaren irudikapena zein den. Erreakzio endotermikoa ala exotermikoa da?
Trantsizio-egoera
Energia librea
Erreakzioaren aurrerapena
24 Zerk bultzatzen zaitu hori esatera? Azaldu zergatik diren egia edo gezurra baieztapen hauek:
a) Energia zinetikoa lotura kimikoei eta molekulen arteko indarrei lotutako energia da.
b) Erreakzio endotermiko batean gertatzen den energia-aldaketa positiboa da.
c) Aktibazio-energia erreaktiboen eta erreakzio kimiko bateko produktuen arteko energia-aldea da.
d) Erreakzio-beroa beti da positiboa.
e) Erreakzio guztiek energia-hesi bat gainditu behar dute hasteko.
f) Aktibatutako konplexuaren energia erreaktiboen eta produktuen energia baino handiagoa da.
25 Pentsatu eta partekatu bikotekidearekin. Idatzi erreakzio-beroa informazio honetatik abiatuta:
a) N2 (g) + O2 (g) + 181 kJ → 2 NO (g)
b) C (s) + O2 (g) → CO2 (g) + 393,5 kJ
Erreakzio endotermikoak ala exotermikoak dira?
26 Erregai baten errekuntza-beroa neurtu da eta datu hauek lortu dira:
Neurria Errekuntza-beroa/ (kJ/mol) Neurria Errekuntza-beroa/ (kJ/mol)
Kalkulatu errekuntza-beroa eta haren errore absolutua.
27 Ekuazio termokimiko hauetatik abiatuta:
a) CH3OH (g) → CH2O (g) + H2 (g)
Qr = 54,5 kJ
b) C2H6 (g) + 7/2 O2 (g) → 2 CO2 + 3 H2O (l)
Qr = –3 119,6 kJ
c) CO (g) + H2 (g) → CH2O (g)
Qr = 21,3 kJ/mol
d) HCl (g) + NH3 (g) → NH4Cl (g)
Qr = –1 75,9 kJ
Zein dira endotermikoak eta zein exotermikoak?
28 Aurreko jardueraren datuetatik abiatuta, kalkulatu
71 g HCl (g) erreakzionatzean askatzen den beroa (d) ataleko erreakzioaren arabera.
Taula honetan zenbait hidrokarburo aseren errekuntza-beroa ageri da:
IKASKETA-EGOERA
HAUSNARTU
Unitate honetan, laborategiko praktikak egin dituzu horien abiadura aztertzeko. Deskargatu anayaharitza.es helbidean eskuragarri dagoen galdera-sorta, eta hausnartu alderdi bakoitzean lortu duzun mailari buruz.
a) Kalkula ezazu hidrokarburo bakoitzaren mol baten errekuntzan askatutako karbono dioxidoaren kantitatea.
b) Kalkula ezazu hidrokarburo bakoitzaren mol baten errekuntzan askatzen den energia bero gisa, eta egin ezazu grafiko bat isuritako karbono dioxidoaren kantitatea eta askatutako energia alderatuz. Zer ikusten duzu?
c) Bilatu PC siglen esanahia, eta azaldu zergatik har dezakegun horren balioa substantzia horien errekuntza-berotzat.
Eguneroko kimika: bero eramangarria
Gaur egun, janaria eta edariak nonahi eta noiznahi kontsumitzea eguneroko kontua da. Ia berehala hartzeko prest dauden produktuak izaten ohitu gara. Berotu edo hoztu ere egin ditzakegu irentsi aurretik. Hala gertatzen da, adibidez, berez hoztu edo berotzen diren edariekin.
Berez berotzen den edari batean, ontziak tanga bat izaten du, eta, edariarekin zuzenean kontaktuan egon gabe, han gertatzen da erreakzio exotermikoa.
Ontziaren diseinuaren giltzarria da erreakzioa edaria kontsumitu behar denean has dadin, eta erreakzioa gertatzen den konpartimentuaren eta berotu behar den edariaren arteko bero-trukea nahikoa izatea edaria tenperatura optimoan kontsumitzeko.

Edaria hartzeko unean, kontsumitzaileak erreaktiboen konpartimentuen artean dagoen tartea hautsi behar du, eta, ondorioz, bere edaria berotuko duen erreakzio exotermikoa hasi egingo da eta laster kontsumitzeko prest egongo da.
Alderdiak Erabat lortua Nahiko lortua Lortua Ia lortua Ulertu erreakzioabiaduraren kontzeptua eta abiadura alda dezaketen faktoreak.
PROBATU ZURE GAITASUNAK
Egin anayaharitza.es helbidean sartuta dagoen gaitasun-autoebaluazioa.
TXOKOLATEA







Webgunean




• Erreakzio endotermiko bat erabil dezakegu berehalako hotza izateko? Bilatu amonio nitratoaren eta uraren arteko erreakzioari buruzko informazioa. Idatzi erantzuna eta esan prozesu hori maila komertzialean erabiltzen den. Jarri adibideren bat.
Jarduera
• Taldeka, antolatu kartel-erakusketa bat, ikastetxeko gainerako gelei hotz-konpresak edo berez berotzen diren edariak bezalako produktuetan ematen den berehalako hozte- eta berotze-oinarriaren berri emateko.

Bilbilis, gaur egungo Calatayudetik (Zaragoza) gertu dagoen antzinako hiri erromatarra, kultura erromatarrak presioaren kontzeptua ezagutzen zuenaren ebidentzietako bat da. Hiri horrek oso hurbil zeuden eta elkarri lotuta zeuden zisternen sare zabala zuen. Haren helburua ez zen ura biltegiratzea, baizik eta beste behar batzuk betetzea. Izan ere, ura irteteko zuloa sarrera-zuloa baino beheraxeago zegoen, eta, beraz, tanga horiek ezin ziren
Ingeniari erromatarrek zisterna-sare hori diseinatu zuten berunezko hodietako presioa murrizteko eta, hartara, akueduktuak ez hausteko. Gai izango zinateke hodien presioa arintzeko beste aukera bat pentsatzeko?
Dakigun bezala, erromatarrek presioaren ondorioak ezagutzen zituzten. Hala ere, xvii. mendearen erdialdera arte ez zitzaion azalpen fisikorik eman kontzeptu horri, hainbat faktore erlazionatuz. Aurrerapen zientifiko horren arduraduna Blaise Pascal frantsesa izan zen.

GJHEN KONPROMISOA
Duisburg-Esseneko Unibertsitatean (Alemania) 2000. urteaz geroztik egin den azterketa mediko baten arabera, airearen poluzio-mailak nabarmen handitzen du arteria-presioa. Horrek, era berean, handitu egiten du biztanleek bihotzekoak eta garun-isuriak izateko aukera.
1. Ataza prestatzea. Bilatu «presio arteriala» kontzeptuari buruzko informazioa, presio hori handitu edo murriztu dezaketen faktoreei buruzkoa eta gure zirkulazio-sisteman presio handia jasatearen ondorioei buruzkoa.

2. AGA . Lotu azterlan mediko alemaniar honek deskribatzen duen aurkikuntza
GJHen 3.4 , 3.9 , 13.3 eta 13.a xedeekin. anayaharitza.es helbidean dauden bideoak kontsulta ditzakezu.
Unitate honetan
• Bilbilis, presio-kontzeptuaren ezagutzaren ebidentziak
1. Presioa
2. Hidrostatikaren oinarrizko legea
3. Arkimedesen printzipioa
4. Pascalen legea















5. Presio atmosferikoa
6. Kontzeptu meteorologikoak
Problemak konpontzeko orientabideak
• Presioarekin eta bultzadarekin lotutako ariketak
IKT
• Online aplikazio interaktiboa
Zientzietako lantegia
• Jolas-zientzia. Presio atmosferikoa
• Lan praktikoa. Pascalen barrika
anayaharitza.es helbidean
Motibatzeko:
• Bideoa: «Hasi aurretik».
Ideiak aldez aurretik atzemateko:
• Jarduera interaktiboa: Hasierako autoebaluazioa.
• Aurkezpena: «Zer jakin behar duzu».
Ikasteko:
• Bideoa: «Arkimedesen printzipioa».




• Simulazioa: «Presiopean».
• Aurkezpena: «Ikasteko».
Zeure burua ebaluatzeko:
• Jarduera interaktiboa: Azken autoebaluazioa.
• Zenbakizko jardueren soluzioak.
Eta, gainera, proiektuaren gakoak aplikatzeko behar den dokumentazio guztia.
PRESIOPEAN.
4.1 Gizakiak jasan dezakeen presio-mugei buruzko informazioa bilatuko dugu, fluidoetako indarrekin erlazionatuko ditugun muturreko egoerak identifikatuz. Presioaren eta grabitatearen artean dagoen aldeari buruz ere hausnartuko dugu, grabitaterik gabeko egoeretan dauden astronauten adibideak erabiliz.
4.2 Lortutako emaitzak azaltzeko txostena egingo dugu. 5. ariketan bideo bat egiteko erabiliko ditugun irudi adierazgarriak izan behar ditu.
MUGAK BILATZEN.
5.1 Presio atmosferikoaren kontzeptuak Marteren kondizioetan aplikatuko ditugu, eta Lurraren eta Ilargiaren presioekin alderatuko ditugu. Presioaldaketa horiek gure egunerokoan nola eragingo luketen azalduko dugu, eta adibide zehatzak bilatuko ditugu, hala nola apnean urpean igeri egitea.
5.2 Presio-aldaketek nola eragingo liguketen azaltzen duen bideo labur bat egingo dugu. Bideo honetan, ikasketa-egoeran sortutako materiala sar dezakegu.
Jarraibide + anayaharitza.es helbidean
Ulertu presioa Irudian ikusten da nola deformatzen den buztina indarra esku-ahurrarekin edo hatz batekin aplikatzean. Eta indarra iltze bat erabiliz aplikatuko balitz?

Indarrek sortzen duten ondorioetako bat eragiten duten gorputzen deformazioa da; beste ondorioa, berriz, haien mugimendu-egoeraren aldaketa da. Horietako lehena aztertuko dugu hemen.

Dakizunez, ukipen-indarrak kontaktu fisikoaren bidez (elkar ukituz) elkarreraginean gorputzek eragiten dituzten indarrak dira. Adibidez, ukipenindarrak dira bi gorputz talka egitean elkar aplikatzen direnak, edo zoruak objektu baten gainean eragiten duen indar normala, hura zeharkatu ez dezan.
Esku-ahurrarekin buztin-zati bati indarra aplikatzen badiogu, deformatzen dela ikusiko dugu. Baina indar bera erabiliz baina hatz bakarrarekin ukituz gero, hatza buztinean hondoratzen dela ikusiko dugu, hau da, are gehiago deformatzen duela. Ikusten dugu, beraz, ukipen-indar baten eraginez objektuek jasaten duten deformazioa ez dela aplikatutako indarraren balioaren araberakoa soilik, ukipen-azaleraren araberakoa ere bada (beheko argazkiak).
Ukipen-azalera zenbat eta txikiagoa izan, orduan eta kontzentratuago dago gainazal horretan aplikatutako indarra, eta, beraz, handiagoa da indar horrek eragiten duen deformazioa. Hortik ondorioztatzen da beharrezkoa dela magnitude bat definitzea, hain zuzen ere horren berri emango diguna; magnitude hori presioa da.
Gainazal baten gainean perpendikularki eragiten duen ukipen-indar batek egiten duen presioa gainazal horren unitateko eragindako indarra da.
Matematikoki, honela adierazten da presioa:

SI-an duen unitatea Pascala (Pa) da, eta N/m2-ren baliokidea da.
Buztina indar baten bidez deformatzea
1 2 · 3 · 4 zentimetroko forma paralelepipedoa duen eta 2 g/cm3-ko dentsitatea duen objektu bat geldirik dago lurzoruaren gainean. Zehaztu lurzoruaren gainean egiten duen presioa, honako hauen gainean jartzen denean:
a) Bere aurpegi nagusia.
b) Bere aurpegi txikiena.
Objektuaren bolumena, cm3-tan adierazia, hau da:
23 424cm V 3 = =
Orain ikus dezagun zer masa duen; horretarako, dentsitatearen definizioa aplikatuko dugu, enuntziatuak ematen dituen datuen arabera:
dVm = → mdV = →
→ 2 cm g 24 cm 48 g0,048 kg m 3 3 == =
Hau da objektu horren pisua:
0, 048kg9,8 s m Pmg 2 == ≃ 0,47 N
Orekan dagoen gorputz horretan bi indar baino ez dira eragiten: pisua (P) eta normala (N), eta, beraz, elkar baliogabetzen dute: N = P ≃ 0,47 N
Indar normala lurzoruak gorputzean eragiten duen indarra da. Akzio-erreakzioaren printzipioa dela eta, gorputzak kontrako indar bat eragiten du lurzoruan, F bidez adierazten duguna:
F = N = P ≃ 0,47 N
ULERTU, PENTSATU, IKERTU…
1 Zer izango da mingarriagoa, zapata lauarekin edo takoizko zapata batekin oina zapaltzea? Azal ezazu.
2 Ideia-biltzarra. Azaldu zergatik den hobea labana ondo zorroztuta egotea ondo ebakitzeko.
3 Zehaztu presioaren dimentsioa.
4 Euro bateko txanpon batek 23,25 mm-ko diametroa eta 7,5 g-ko masa ditu. Zehaztu euro batek mahaiaren gainean egiten duen presioa.
5 Zer indar aplikatuko da 50 cm2-ko gainazal batean, presioa 10.000 Pa bada?
6 Paperezko orri batek 21,0 × 29,7 cm neurtzen badu eta 5,0 g-ko masa badu, zer presio egiten du mahai batean?
7 Egiazta dezagun. 80 kg-ko pertsona batek 170 cm2-ko euste-azalera du oin bakoitzean. Zer presio egiten du lurzoruan?
Hala, emaitza orokor hau lortu dugu: objektu orok lurzoruan eragiten duen indarra eta haren pisua berdinak dira.
Gorputzak lurzoruan egiten duen presioa zehazteko, adierazpen hau erabiltzen dugu: pS F =
a) Aurpegi nagusiaren azalera hau da: 34 12 cm 12 10 m S 2–42 1 == =
Presio hau eragiten zaio: 12 10 m 0, 47 N pS F –4 2 1 1 == ≃ 392 Pa
b) Azalera txikiena hau da: 23 6cm6 10 m S 2–42 2 == =
Aurpegi honen gaineko presioa hau da: 610m 0, 47 N pS F –4 2 2 2 == ≃ 783 Pa
8 1,2 g/cm 3-ko dentsitateko dado batek presioa egiten du 1 470 Pa-eko pisua duelako. Zehaztu kuboaren neurriak.
9 12 g-ko USB memoria batek paralelepipedo-forma du gutxi gorabehera, eta bere azalera handiena hau da: 1,6 × 5,4 cm. Zer presio egingo du zure eskuan aurpegi horren gainean jartzerakoan zure eskuan?

Fluidoa jariatzen den substantzia oro da, ez du bere forma mantentzen grabitazio-erakarpenaren azpian, eta jariatu egiten da, dagoen ontziaren formara egokitu arte. Azken batean, fluido bat egoera likidoan edo gasegoeran dagoen edozein substantzia da.
Likidoaren eta gasaren arteko alde enpiriko nagusia da likidoak ia ezin direla konprimitu eta bolumena konstante mantentzen dutela. Hala ere, gasak konprimitu egin daitezke eta, beraz, ez dute bolumen propiorik: gasak hartzen dituen ontziaren araberakoa da.
Likido batzuk beste batzuk baino errazago jariatzen dira, haien izaeraren arabera. Propietate hori biskositate-magnitudearekin neur daiteke. Zenbat eta likatsuagoa izan likidoa, orduan eta gehiago «kostatzen» zaio jariatzea, adibidez, eztiarekin gertatzen den bezala.
Azkenik, argi utzi behar da fluido bat ez dela betiko. Likido-egoeran edo gas-egoeran dagoen substantzia bati fluido esaten diogu, baina, jakina, fluido izateari utziko lioke fusio-tenperaturaren azpitik hozten denean eta solidotzen denean.
Ikertu fluidoak
Bilatu Interneten grabitaterik gabeko likidoen bideoak, zer forma hartzen dute?
Fluidoak

Zero grabitatea Grabitatearekin

Hidrostatika likidoen oreka aztertzen duen fisikaren zatia da.
Orekan dagoen likido batean indar guztien batura nulua da edozein zatitan; beraz, ez da korronterik izango barruan.
Esperimentalki, likido batek bolumen propioa du, baina ez du berezko formarik; likido hori duen ontziaren forma hartzen du grabitatearen mende dagoenean, eta, zero grabitatean forma esferikoa du.
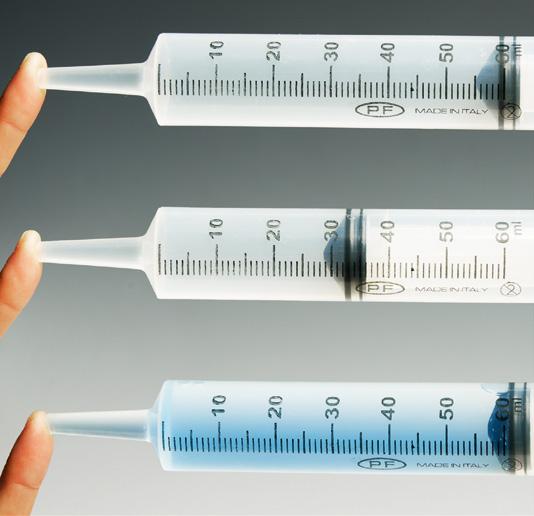
Likidoak ia ezin dira konprimitu; gasak, ordea, konprimitu egin daitezke. Horregatik, lehenengo xiringa, airez betea, konprimitu egin daiteke, eta hirugarrena, likidoz betea, ez.

Demagun likido bat orekan dugula, eta, sinpletasunagatik, paralelepipedo-formakoa dela, hala nola igerileku bateko ura. Kalkula dezagun zer presio egiten duen likidoak igerilekuaren hondoan, haren pisuaren eraginez.
Likidoak (mF masa eta V bolumena dituenak) hondoko S gainazalean eragiten duen F indarra bere pisua da, PF Dentsitatea dF bada eta h sakonera, likidoaren presioaren adierazpena hau da:
pS F S P S mg S Vdg S Shdgdgh FF FF F == == ==
Emaitza hori likidoaren edozein formatara orokortu daiteke, eta, halaber, likidoaren azpiko likido-geruzan beste edozein sakoneratan (h) eragiten duen presioa aurkitzeko ere balio du.
Hala, likido batean sakonera jakin batean dagoen presioa kalkulatzeko aukera ematen duen adierazpen matematikoa aurkitu dugu.
Adierazpen hori hidrostatikaren oinarrizko legea da:
h sakoneran dF dentsitateko orekan dagoen likido baten presioa adierazpen honen bidez adierazten da:
Likido baten barruko puntu bakoitzean haren presio hidrostatikoa aurki daiteke. Presio hori indar gisa agertzen da objektu murgildu bat sartzen denean. Presioak eragindako indarra objektuaren gainazalarekiko perpendikularra da haren puntu guztietan, eta, ondorioz, objektua konprimitzeko joera du.
Fluidoaren pisua dela eta, indar bat aplikatzen zaio fluidoaren hondoari. Baina hainbat sakoneratan ere indarra eragiten du, gainazaletik neurtuta, likido-geruzaren gainean.
Fluidoaren barruko puntu bakoitzean presio bat dago. Objektu bat likido baten barruan jartzean, horren gainazalaren puntu bakoitzeko presioa objektua konprimitzen duen indar perpendikular bihurtzen da.
ULERTU, PENTSATU, IKERTU
10 AGA. Materia osatzen duten partikulen ikuspuntutik, badakizu zergatik konprimi daitezkeen gasak eta zergatik likidoak ez? Errepasatu aurreko ikasturteetan aztertutako teoria zinetiko-molekularra.
11 Pentsatu eta partekatu bikotekidearekin. Indarrik gabeko gorputz baten egoera geldirik edo higidura zuzen uniformea da. Zergatik ezin da HZU duen korronterik egon orekan dagoen likido batean?
12 Zehaztu itsasoko uretan 20 m-ko sakoneran dagoen urpekari batek jasan beharko duen presioa. Datua: d = 1,025 g/cm3.
13 Itsaspeko batek jasan dezakeen presio maximoa 3 000 000 Pa bada, zein izango da itsas uretan murgildu ahal izango den gehieneko sakonera? Datua: d = 1,025 g/cm3
14 Urez betetako 1,8 m-ko sakonera duen ur-tanga baten hondoan, 15 cm-ko aldeak dituzten lauza karratuak daude. Zer indar jasaten du lauza bakoitzak? Datua: d = 1 g/cm3
15 Zer indar jasan egingo du 2,5 m-ko sakonerako igerileku baten hondoan dagoen 3 cm-ko diametroko txanpon baten bi aldeetako bakoitzak? Datua: d = 1 g/cm3.
Informa zaitez akueduktu erromatarrei buruz
Zertarako eraikitzen zituzten erromatarrek beren akueduktuak? Zergatik ez zuten U formako hodirik eraikitzen? Bilatu informazio hori Interneten.
Bilatu, halaber, paradoxa hidrostatikoari buruzko informazioa; horretarako, begiratu ezkerreko lehen irudia.



Hidrostatikaren oinarrizko printzipiotik ondorioztatzen da orekan dagoen eta sakonera berean dauden likido baten barruko bi puntu presio berean daudela. Hala ez balitz, likido-bolumena presio handiagoan txikiraino bultzatuko lukeen indar garbia agertuko litzateke. Hau da, presioak orekatuko lituzkeen likido-korronte bat sortuko litzateke, eta likidoa ez litzateke orekan egongo.
Horri esker, ontzi komunikatzaileen printzipioa deritzon fenomenoa ondoriozta dezakegu.
Likido bera duten eta konektatuta dauden bi ontzi edo gehiagok altuera berean izan behar dute nahitaez azalera librea.
Fenomeno horri esker, ondoriozta daiteke inguruko bi laku ezin direla lur azpitik komunikatuta egon haien azalerak altuera ezberdinetan badaude. Hala ere, altuera berean baleude, aztarna handiak izango genituzke bi lakuak konektatuta daudela susmatzeko.
U formako hodi batean isuritako likido bat adar bakoitzeko gainazalen mailekin geldituko da altuera berean. Horretan datza sifoi bat. Gure etxeetako hustubideetan, estolda-zuloaren ondoren, urez betetako sifoi bat dago. Horrela, hustubideko hodien barrualdea, usain txarra izan ohi dutenak, konketaren hustubidetik eta etxearen gainerakotik isolatzen da.
Era berean, U formako hodiak erabiltzen dira ur korrontearen horniduran oztopoak gainditzeko. Baldintza bakarra hau da: ura hornitzen duen urtegia hodiaren adarretako batean egotea, ura eraman nahi den tokietan baino altitude handiagoan.
Konektatutako ontziek gainazal librea dute altuera berean, likido-bolumena edozein dela ere.
Likido baten dentsitatea neurtzeko, U itxurako beirazko hodi bat erabil daiteke. Horretarako, dentsitate ezaguneko likido bat erabiltzen da, problema-likidoarekin nahastezina dena eta adarretako batera botako dena. Adibidez, oso erabilgarria da olio mota desberdinen dentsitatea neurtzeko, horretarako ura erabiliz, ura eta olioa ez baitira nahasten.
Irudian, E eta F puntuak, altuera berean badaude ere, ez daude presio berean, dentsitate desberdineko likidoei baitagozkie. A eta B puntuak presio berean daude, likido berekoak baitira. Muga-kasua C eta D puntuetan dago, ere presio berean daudenak; puntu hauek erabil ditzakegu olioaren dentsitatea zehazteko, dF l , baldintza hau ezarrita: ppCD = → dghdgh F F = ll → dhhd
2 U formako hodi batean ur purua isurtzen da, eta, ondoren, adarretako batean, zehaztu nahi dugun dentsitatea duen likidoa. Orekan, irudian ageri den bezala geratzen da. Zehaztu olio horren dentsitatea.
Gogora dezagun uraren dentsitatea 1 g/cm3 dela. A eta B puntuetan presioa berdina denez:
ppAB = → dghdgh FF = ll → dhhd FF = l l
Dentsitatearen neurketa
ULERTU, PENTSATU, IKERTU …
16 Herri bateko ur-biltegia 450 m-ko altitudean dago. Zein presiorekin iritsiko da ura udaletxera, 426 m-ko altitudean badago?
17 Irudiko U formako hodian bi likido nahastezin daude orekan. 1 likidoak 1,05 g/cm3-ko dentsitatea badu, zehaztu ezazu zein izango den 2 likidoaren dentsitatea.
b a
C eta D puntuetako presioa berdina da. Horregatik, sakonera desberdinak neurtuz eta uraren dentsitatea ezagutuz, gure kasuan, olioaren dentsitatea kalkula dezakegu.
a = 1 cm
b = 2,5 cm
18 Ura eraikin baten beheko solairura iristen den presioa 140 000 Pa da. Zer presiora iristen da ura laugarren solairura? Kontuan izan solairu bakoitzak 3 m-ko altuera duela.
19 Egiazta dezagun. Eraikin baten beheko solairuko uraren presioa 300 000 Pa-koa bada, zenbat solairu izan ditzake eraikin horrek ura presioz iristeko, solairu bakoitzak 3 m-ko altuera badu? Altuera handiagoko eraikin bat eraiki nahi izanez gero, zer irtenbide har liteke?
Imajina dezagun likido batean murgildutako paralelepipedo-formako gorputz bat (ezkerreko irudia). Objektuaren aurpegi bakoitzean presio hidrostatikoaren ondoriozko indar bat aplikatzen ari da. Alboetako aldeen gaineko indarrak bi-bi ezeztatzen dira, baina goiko aldearen gaineko indarra, FS, ezin da ezeztatu behekoarekin, FI, sakonera txikiagoan baitago, eta haren gaineko presioa txikiagoa baita. Ondorioz, objektua gorantz bultzatzen duen presio-diferentziak eragindako indar garbia agertzen da. Indar horri bultzada deritzo:
EFFpSpSdghSdghS –F lS lS lF S == ==

() dShhgdVg –FF lS == → Ed Vg F =
Lortutako emaitzak objektuak urperatzean kanporatutako fluidoaren pisua adierazten du, izan ere: dF · V = mF, eta mF · g = PF. Edo, beste era batera esanda, objektuak murgiltzen den likidoaz eginda balego izango lukeen pisua adierazten du. Gainera, kontuan hartu da V = S · (hI – hs) gorputz murgilduaren bolumena dela.
Emaitza hori erabat orokortu daiteke objektu solidoak duen edozein formatarako, baita fluidoa gas bat denean ere. Hala, Arkimedesen printzipioa enuntzia dezakegu:
Fluido batean murgildutako gorputz orok goranzko indar bertikala jasaten du, bultzada izenekoa (E), eta indar horren modulua kanporatutako fluidoaren pisuaren berdina da.
ARIKETA EBATZIA
3 Zehaztu uretan sartuta dagoen 1 cm-ko aldea duen dado baten gaineko bultzada.
Urez eginda egongo litzatekeen 1 cm-ko aldea duen dado baten pisua kalkulatu behar dugu, edo, bestela esanda:
EdVg F =
Gutxi gorabeherazko formak
ULERTU, PENTSATU, IKERTU
Uraren dentsitatea SI-an: 1 cm g 1000 m kg d 33 F = =
Eta dadoaren bolumena: 1cm10m V 3–63 = =
Beraz: 1000 m kg 10 m9,8 m/s E 3 –6 32 = ≃ 0,01 N
Ikus dezakezunez, emaitza guztiz independentea da dadoa eginda dagoen materialarekiko.
20 Mahai-ingurua. Zergatik uste duzu gutxiago kostatu egiten zaigula ur barruan dagoen harri bati eustea kanpoan dagoenean baino?
Grabitatearen indarrak gorputz bat erakartzen du lurrerantz, bertikalki, Lurraren azalaren gainean; indar horri pisu esaten diogu. Gainera, fluido batean sartuta badago, goranzko indar bertikal batek ere eragiten dio, bultzada deritzonak. Lurreko objektu guztiak airean murgilduta daude; aireak dentsitate txikia duenez, haren bultzada oso txikia izaten da pisuarekin alderatuta. Hala, nahiz eta gutxi izan, gorputzak zertxobait gutxiago pisatzen duela ematen du; efektu hori oso larrituta dago objektua likido batean sartuta dagoenean, hala nola uretan; kasu horretan, bultzada ez da batere baztergarria, eta askoz gutxiago pisatzen duela dirudi. Horregatik, indar gutxiago egin beharko dugu objektua eusteko (beheko eskuineko irudia), pisuaren zati bat likidoaren bultzadarekin konpentsatzen baita. Kasu honetan, itxurazko pisuaz hitz egiten da, Pap, eta modulu hau du:
PPE –ap =
Objektu bat baskula batean pisatzen denean, baskula horrek adierazten digun balioa objektuari eusteko egiten duen indarra da, hots, indar normala. Fluido batean sartuta ez balego, normala pisuaren berdina izango litzateke, baina bultzada kontuan hartzen dugunean, fluido batean sartuta dagoelako, baskularen neurria itxurazko pisua izango litzateke.
Itxurazko pisua
Baskula baten neurria gorputzari eusten dion indar normala da, eta desberdina da hutsean edo airean egiten bada; azken kasu horretan, itxurazko pisua neurtzen du.
ULERTU, PENTSATU, IKERTU …
22 Zehaztu uretan dagoen 2,7 g/cm3 eta 2,00 kg-ko masa duen arroka baten itxurazko pisua eta pisua.
4 Zehaztu lurzoruak 75,0 kg-ko pertsona bati eragiten dion indar normala; pertsona horren bolumena 79,0 litrokoa da. Datua: airearen dentsitatea, 1,19 g/L.
Airean sartuta ez balego, pisu bera izango luke normalak. Baina bulkada kontuan hartu behar dugu, pisuaren aurkakoa dena. Kalkulatzeko, lehenengo dentsitatea kg/L-tan idatziko dugu: 1, 19 L g 10 g 1kg
0,9 N
P = m · g = 75 · 9,8 = 735 N denez: 735– 0, 9734,1 N PPE –ap = ==
Pertsona horrek 734,1 N-eko indar normala izango luke, hau da, baskula batek neurtuko lukeena. Baskulen eskala ez dagoenez N-tan kalibratua, kg-tan baizik, pisua neurtzen ari den masa adierazten dute. Hala, bultzada kontuan hartuta:
Pmg ap = → 9, 8 734, 1 mg Pap == ≃ 74,9 kg
Beraz, pertsonaren benetako masa 75,0 kg-koa bada ere, eskalak 74,9 kg-rekin «engainatuko gaitu».
Haurrak indar (F ) handiagoa egin behar du bere besoekin arroka uretatik kanpo eusteko uraren barruan badago baino, uraren bultzada airearena baino askoz handiagoa baita.
23 Intuitzen eta deduzitzen dut. Noiz uste duzu gehiago markatuko lukeela baskula bat, kilo bat berunekin edo kilo bat lastorekin? Berun kilogramoak pisu handiagoa duela esatea zuzena da?
Ondorioztu eta ulertu
Batu. Noraino iritsiko da beheko irudiko globoa? Zure erantzuna arrazoitzeko, jakin behar duzu airearen dentsitatea txikituz doala altuerarekin batera.
Flotazioa
Globo bat airean
Airean murgildutako objektu bati eragiten dion bultzada haren pisua baino handiagoa bada, gorputza altxatu egingo da. Horixe gertatzen da globo aerostatikoekin edo feria-globoekin. Hori lortzeko, batez besteko dentsitatea airearena baino txikiagoa izan behar du, eta, horretarako, inguratzen dituen airea baino dentsitate txikiagoa duten gasez betetzen dira. Globoak betetzen duen gasaren dentsitatea dC bada, eta airearena, dF , eta V bada globoaren bolumena:

PE < → dVgdVg < CF → dd < CF
Era berean, likido batean (ura, adibidez) murgildutako gorputz baterako arrazoitu dezakegu. Harhen pisua bultzada baino txikiagoa bada flotatuko du, edo, bestela esanda, haren batez besteko dentsitatea likidoarena baino txikiagoa bada. Kasu horretan, gorputza gainazaleraino igoko da, eta, handik irteten hasten denean, kanporatzen duen likido-bolumena txikitzen hasiko da, eta, horrekin batera, bultzada. Bultzada berria (E' ) gorputzaren pisuaren berdina denean flotazio-oreka lortuko da:
EP = l
Bultzada berria, E’, kanporatutako likidoaren bolumenarekin bakarrik kalkulatzen da, V’, gorputzak guztira duen bolumena (V) baino txikiagoa dena.
EdVg F = ll
Likido batean
Globoa igo egiten da, bultzada pisua baino handiagoa baita.
ARIKETA EBATZIA
5 Uretan flotatzen duen 0,78 g/cm3-ko dentsitateko gorputz baten bolumenaren zer ehuneko dago urgaineratuta?
Orekan, bultzada pisuaren berdina da:
Badugu urpeko bolumena. Urpean gelditzen den bolumena, Ve , gainerakoa da:
VVVV 0780 12
Ve gorputzaren bolumen osoaren (V) % 12 da.
Objektua erabat murgilduta dagoenean, bultzada pisua baino handiagoa bada, igo egiten da. Azalean flotatzen geratzen denean, bultzada berria, E’, pisuaren berdina da, P.
ULERTU, PENTSATU, IKERTU
24 Zehaztu itsas uretan flotatzen duen iceberg baten dentsitatea, haren bolumenaren 1/9 azaleratzen bada.
Datua: d (itsasoko ura) = 1,025 g/cm3
25 Zehaztu 200 000 tonako transatlantiko batek 1,025 g/cm3-ko dentsitateko itsasoko uraren zein bolumen kanporatzen duena. Adierazi emaitza litrotan.
26 8 m-ko erradioa duen globo esferiko batek flotatu egiten du airean, bere pisua jasoz, hau da, olana (90 kg) eta pertsonak eta ekipajea dituen saskia (500 kg). Zehaztu barneko airearen dentsitatea, kanpokoa 1,23 kg/m3 bada.
A tapoiaren gainazalean indarra aplikatzean, presio bihurtzen da tapoia ukitzen duen likidoaren puntuetan. Presio-igoera hori fluidoaren puntu guztietara transmititzen da, eta, bereziki, B tapoiarekin kontaktuan dauden puntu guztietara.
Prentsa hidraulikoa
Pascalen legeak likido baten barruan presioa nola transmititzen den esaten du, edozein arrazoirengatik likidoaren puntu batean handitzen denean.
Likido baten puntu batean eragindako presioa likidoaren gainerako puntuetara transmititzen da, intentsitate bera mantenduz.
Transmisio hori likidoko soinuaren abiaduran gertatzen da. Uretan 1 500 m/s inguru da.
Lege horri esker, indarrak puntu batetik bestera transmititzea lortzen da, baita indarrak biderkatzea ere, ikusiko dugunez.
Gasetan ere transmititzen da presioa, baina, gasaren konprimigarritasuna dela eta, ez da intentsitate berarekin transmititzen, eta azkar ahultzen da hedatu ahala.

Prentsa hidrauliko bat bi enboloko likidoa (normalean, olio bat) duen andel bat da. Horietako bati, txikienari, indar bat eragiten zaio. Besteari, sekzio handiagoa duenari, indar biderkatua eragiten zaio, ezkerreko beheko irudian ikus dezakezunez.
Pascalen legearen arabera, 1. enboloan egiten dugun presioa intentsitate berean transmititzen da 2. enbolora. Hala, erlazio hauek ezar ditzakegu:
pp
Enbolo txikian indarra aplikatzean, enbolo handian indar handiagoa lortzen da.
ULERTU, PENTSATU, IKERTU …
Ikus dezakezunez, indarren arteko erlazioa enboloen gainazalen artekoaren bera da.
Prentsa hidraulikoak askotariko aplikazioak ditu. Automobilgintzako lantegietako jasogailuak, katu hidraulikoak, balazta hidraulikoak, norabide lagunduak eta abar fabrikatzeko erabiltzen da.
27 Prentsa hidrauliko batekin indarra bider 16 egin nahi badugu, zer erlazio bete beharko dute erradioek?
28 Prentsa hidrauliko bat, ibilgailu-jasogailu gisa erabiltzen dena, 2 cm-ko diametroko enbolo txiki bat eta 20 cm-ko beste handi bat ditu. Zehaztu zer indar egin behar den enbolo txikian 1 000 kg-ko masa duen ibilgailua altxatzeko.
29 Egiazta dezagun. Auto baten balazta-pedalak 0,3 cm-ko diametroko enboloa du. Ibilgailua balaztatzeko, bi enbolo daude gurpil bakoitzeko, 4 cm-ko diametroa duen balazta-diskoa pintzatzeko. Balazta 10 N-ko indarraz zapaltzen badugu, zenbat izango da zortzi zilindroen arteko balaztatze-indar totala?
30 Prentsa hidrauliko baten enbolo txikiaren azalera 2 cm2koa da. 2 N aplikatzean 90 N bihurtzen badira, zer erradio du beste enboloak?
Airean murgilduta bizi gara, eta haren dentsitatea oso txikia den arren, ikusiko dugu Lurraren azalean egiten duen presioa, pisuaren beraren eraginez, ez dela batere baztergarria.
Hori neurtzeko, pentsa dezakegu hidrostatikaren oinarrizko legea airean murgilduta gauden sakoneran aplikatu behar dela, baina lege hori ezin da aplikatu kasu horretan, airearen dentsitatea ez delako konstantea atmosfera osoan: txikiagotu egiten da altuerarekin.
Planetaren azaleko presio atmosferikoaren balioa zehazten lehena Evangelista Torricelli izan zen 1643an. Esperimentu hau egin zuen: beirazko hodi luze bat merkurioz bete zuen; hodiaren ahoa estali, buelta eman eta hodiaren ahoa merkurioa ere zuen ontzi batean sartu zuen.

Hatza hodiaren ahotik kentzean, hodia ez zela erabat husten ikusi zuen, bertan 760 mm-ko merkurio-zutabea geratzen zela. Fenomenoa azaltzeko, atmosferaren presioak merkurio-zutabearen presioa berdintzen zuela proposatu zuen; beraz, 760 mm-ko sakoneran merkurioaren presioa kalkulatuz, aireak eragiten duen presioa lortuko genuke.
Imajinatu eta arrazoitu
Zerk bultzatzen zaitu hori esatera? Torricelliren esperimentua urarekin egin izan balitz, zer hodi-luzera beharko litzateke?
Torricelliren esperimentua
Merkurioaren dentsitatea 13,6 g/cm3 dela jakinik, honako hau aurkituko dugu: ,, Pa pdgh 13 600 98 0 760 101300 Hg atm - ==
Emaitza hori gutxi gorabeherakoa da. Merkurioaren dentsitatearen eta Lurraren grabitatearen neurri zehatzagoa erabiliz gero, presio atmosferikorako balio zehatzagoa lortzen da: 101 325 Pa. Hau da baldintza meteorologiko normaletan eta itsas mailan dagoen presio atmosferikoa.
Altuerarekiko presio-aldaketa
Atmosferaren presioak merkurio-zutabea mantentzen du. Beraz, merkurio-zutabeak hura mantentzen duen aire-zutabearen presio bera egiten du. Hortik abiatuta, atmosferaren presioa kalkula daiteke.
Pertsona batek presio atmosferiko txikiagoa jasaten du mendi batean (aire gutxiago du gainean). Aldaketa, gutxi gorabehera, 1 milimetro merkurio gutxiagokoa da atmosferaren beheko geruzetan igotzen dugun 10 m bakoitzeko.
Unitate asko erabiltzen dira presioa neurtzeko. Orain arte
SI-arena baino ez dugu ikusi: Pascala, Pa.
Atmosfera (atm) izeneko presio-unitate berri bat definitzen da, honela:
1 atm = 101 325 Pa
Gogoan izan 1 atm balioa esleitzen zaiola eguraldi normaleko egun batean atmosferak itsasoaren mailan eragiten duen presioari.
Merkurioaren milimetroa, mmHg, beste presio-unitate bat da. Merkurioan murgildutako milimetro bateko sakoneran dagoen presioa da. Torricelliren esperimentutik baliokidetasun hau ondorioztatzen dugu:
1 atm = 760 mmHg
Meteorologian, milibarra, mb erabiltzen da, bar baten milaren zatia: zentimetro, gramo eta segundotan lan egiten denean erabiltzen den presio-unitatea. Atmosferarekiko duen baliokidetasuna hau da:
1 atm ≃ 1 013 mb
6 Bizikleta baten gurpilean neurtzen dugun presioa 2,5 kg/cm2 da. Adierazi presio hori ikasitako unitate ezberdinetan.
Unitate-aldaketen ariketa sinplea da hau. Konbertsiofaktoreak erabiliz, hau
Herrialde anglosaxoiek asko erabiltzen duten unitatea psi da (hazbete karratuko librak). Merezi du haien baliokidetasuna ikustea, presioak neurtzeko gailu asko baitaude eskala honekin:
1 atm ≈ 14,7 psi
Erakutsiko dugun azken presio-unitatea atmosfera teknikoa da. Erabiltzen ez den unitate bat da, baina oraindik bizikletaren edo autoaren gurpilak puztean erabiltzen dugu. Unitatea kg/cm2 da, eta kilogramo batek zentimetro karratu baten gainean duen pisuagatik egiten duen presioa adierazten du. Atmosferarekiko duen baliokidetasuna hau da:
1 atm ≃ 1,034 kg/cm2
Azken baliokidetasun horrek atentzioa eman diezazuke, gure presio atmosferikoaren intentsitatearen ideia argiagoa ematen baitigu. 1 atm-ko presioa kilogramo bat baino gehixeago suposatzen du gure azalaren zentimetro karratu bakoitzean, atmosferaren pisuaren eraginez presioa eginez.
7 Frogatu atmosferaren (atm) eta kg/cm2-aren arteko baliokidetasuna.
1 kg-ko presioa, 1 cm2-tan bermatua, hau da:
kg N 98 000 m N pS F S P S mg –4 22 = == ==
kg/cm2-ren definizioaren arabera (bere pisua dela eta, 1 kg-ko masa batek eragiten duen presioa), honako hau esan dezakegu:
98 000Pa1 cm kg 2 =
Erlazio hori honen baliokidea da:
101 325 Pa 1, 034 cm kg 2 =
Hortik ondorioztatzen da:
1atm 1, 034 cm kg 2 =
ULERTU, PENTSATU, IKERTU
31 Muino baten oinarrian neurtzen den presioa 1 014 mb da, eta gailurrean 947 mb. Zer altuera du, gutxi gorabehera, muinoak?
32 Itsasoko uretan sartzean 30 psi-ko presioa neurtzen badugu, zer sakoneratan gaude? Datua: d = 1,025 g/cm3
Presioa neurtzeko bi aparatu ditugu: barometroa, presio atmosferikoa neurtzen duena, eta manometroa, ontzi batean dauden edo likido batean sakonera jakin batean dauden gasen presioa neurtzen duena. Manometro baten neurketaren irakurketan ez da sartzen atmosferikoa; hau da, neurtzen den presioa presio atmosferikotik aurrera dagoena da.
Torricelliren esperimentuak merkurio-barometroa nola egiten den erakusten du. Presio atmosferikoak eusten dion merkurio-zutabe graduatu batean datza. Gainera, barometro mekanikoak eraiki dira, baina zehaztasun gutxiagorekin.
Gurpilen presioa neurtzeko gasolindegietan ikusten ditugun manometroak edo urpekariek erabiltzen dituztenak mekanikoak dira. Xafla bat dute, malguki bati lotua, eta, presioa egitean, orratz bat mugitzen du eskala graduatu batean. Oinarrizko manometro baten funtzionamendua interesatzen zaigu, ontzi batean itxitako gas baten presioa neurtzeko erabil daitekeena. U formako hodi bat da, non adarretako bat gas-tanga batera konektatzen den eta bestea atmosferara zabalduta geratzen den. Adar bakoitzeko gainazal libreen desoreka aztertuz, gasaren presio erlati-
ARIKETA EBATZIA
8 Goiko irudiko manometroa merkurioz eginda badago eta maila-diferentzia 420 mm-koa bada, zer presiotan dago gasa? Adieraz ezazu milibarretan.

Irudiko manometroak gasaren presio erlatiboa ematen du; absolutua aurkitzeko, kanpoko presio atmosferikoa gehitu beharko litzaioke emaitzari.
Hau da merkurioaren dentsitatea: 13,6 cm g 13 600 m kg d 33 = =
puntuko presioa A’ puntuko presioaren berdina da. A’ puntuko presioa gas itxiaren presioaren berdina da, eta -ko presioa hidrostatikaren oinarrizko legearen bidez kalkula dezakegu.
Eta hau da merkurio-zutabearen altuera: h = 420 mm = 0,420 m
Beraz, gasaren presio erlatiboak hau balio du:
Kopuru hori, milibarretan adierazita (mb), hau da:
Torricelli gai izan zen presio atmosferikoaren intentsitatea neurtzeko, eta ohartu zen merkurioak 76 cm-ko sakoneran eragiten duenaren berdina dela. Urarekin egin izan balu, 10,34 m inguruko zutabe bat lortuko zukeen, eta gutxienez luzera horretako hodi bat erabili beharko zukeen. Seguru asko, hasieran urarekin saiatuko zen, baina zer gertatu ote zitzaion urarekin eta metro bateko hodi batekin saiatu zenean?
Ura ez litzateke eroriko, eta presio atmosferikoaren eraginpean egongo litzateke erabat. Edo ur-biltegiaren ordez paper plastifikatua erabili ahal izango litzateke, eskuineko irudian ikus daitekeen moduan.


Demagun 11 m inguruko hodi bat dugula Torricelliren esperimentua egiteko. Ura 10,34 m-ko zutabe bat mantendu arte jaitsiko litzateke. Goiko espazioan zero presioko espazio hutsa egongo litzateke. Hodiaren goiko muturra zabalduz gero, lasto luzea balitz bezala, eta ura edateko xurgatzen saiatuz gero, guztiz ezinezkoa izango litzateke. Ahalik eta gehien xurgatzen denean (zero presioa), ura 10,34 m baino ez da igotzen.
Emaitza horretatik ondorioztatzen dugu ezin dela ura 10,34 m-ko sakonera baino gehiagoan duen putzu batetik ura atera, lurzoruaren arrasean xurgatze-ponpa bat erabiliz.
Jasaten ari garen presio atmosferiko handia agerian uzteko, Otto von Guericke zientzialari alemaniarrak erakusketa publikoa egin zuen Alemaniako Magdeburgo hirian, 1656an. 50 cm-ko diametroko kobrezko bi esferaerdi erabiltzen zituen esperimentuak. Bi esferaerdiak esfera bakar bat osatuz elkartzen ziren, eta balbula baten bidez airea ateratzen zen, barruan hutsa eginez. Esferak gogor elkartuta geratzen ziren, presio atmosferikoaren kanpo-presioaren eraginez. Badirudi ezin zituztela esferaerdiak banandu, alde bakoitzetik zortzi zaldiekin tiratuz ere ez.

Ura ez da erortzen
ULERTU, PENTSATU, IKERTU
33 1,15 atm-ko tanga batean itxitako gas baten presioa neurtu nahi dugu. Erabilitako likidoa merkurioa bada, zenbat desorekatuko dira gainazalak?
34 Zer indar behar da esferaerdiak banantzeko? Datua: R = 50 cm. Gogoan hartu R erradioko gainazal zirkular batean eragiten dela indarra.
Ur-biltegiaren ordez paper plastifikatua erabil daiteke, presioaren indarra gainazalarekiko perpendikularra baita eta papera gorantz bultza baitezake.
Magdeburgoko esferaerdiak

Lurreko atmosfera ez da orekan dagoen aire-masa bat. Eguzkiak atmosferako eremu desberdinetan duen eragin desorekatuaren ondorioz, aire beroko masak eta aire hotzeko masak sortzen dira, eta horrek desoreka eragiten du, eta, ondorioz, aire-mugimenduak eragiten ditu, haizea sortuz.
Ekintza-zentroak presioa ohi baino altuagoa (antizikloiak) edo ohi baino baxuagoa (depresioak) duten atmosferako eremuak dira.
Antizikloi batean goi-geruzetako aire-masak jaitsi egiten dira, bai beste aire-masa batzuek bultzatzen dituztelako, bai tenperatura baxuko airea delako, dentsoagoa dena eta horregatik jaisten da. Beheranzko aire horrek presio handiak eragiten ditu. Aire hotza denez, ur-lurrun gutxi darama; hezetasun gutxiko airea da. Egoera horrek zeru argiak eragiten ditu, euririk gabe; hau da, eguraldi egonkorra.
Aitzitik, depresio bat goranzko aire-korronteak sortzen diren atmosferako gune bat da, normalean tenperatura eta hezetasun handiagoan, igotzean hoztu egiten dena, ur-lurruna kondentsatuz eta hodeiak sortuz. Egoera horrek haize bortitzak, euriteak eta tenperatura-jaitsierak eragiten ditu.
Ikertu biraketa-noranzkoa
Bilatu Interneten nola deitzen zaien fikziozko indarrei, ibilbideak Ipar hemisferioan eskuinerantz eta Hego hemisferioan ezkerrerantz desbideratzen dituztenak.
Ikertu biraketa-noranzkoa
Antizikloia eta depresioa
Lurrazalean zehar airearen mugimendua bultzatzen den eremuak dira ekintza-zentroak. Mapa meteorologiko batean, antizikloia A letraren bidez irudikatzen da, eta depresioak, berriz, B letraren bidez. Atmosferako airea antizikloietatik hedatzen da, presio altuak direla eta, eta depresioetan konbergitzen da, behe-presioak baitira. Lurraren errotazio-mugimenduaren ondorioz, ez antizikloitik datorren airearen hedapena, ez eta depresioko airearen konbergentzia ere gertatzen dira erradialki, baizik eta ekintza-zentroaren inguruan biratuz. Ipar hemisferioan, antizikloien airea erlojuaren orratzen noranzkoan biratzen da, eta depresioetan, airea erlojuaren orratzen kontrako noranzkoan biratzen da. Hego hemisferioan alderantziz gertatzen da.
Antizikloia eta depresioa eguraldiaren mapan
Depresioan, hezetasundun aire beroa igo egiten da, hoztuz eta hodeiak sortuz. Antizikloian, aire hotza eta lehorra jaitsi egiten da, eta egun garbiak uzten ditu.
Mapa honetan antizikloi bat eta depresio bat daude. Aireak haietan duen biraketa-noranzkoa ere adierazten da (kontuan izan hori Ipar hemisferioko norabidea dela).



Mapa meteorologikoetan isobarak irudikatzen dira, presio atmosferiko bereko puntu guztiak lurrazalaren gainean lotzen dituzten lerroak, itsas mailaren altueran hainbanatuak. Presioa milibarretan adierazi ohi da (hektopascal-en baliokideak, hPa), launakako unitatetan.





Oso elkartuta badaude, presio-aldaketa handia adierazten dute distantzia txikian (fenomeno meteorologiko bortitzak haize bortitzekin), eta oso bereizita badaude, aldaketa gutxi. Aire-masek isobarei jarraitzen diete mugimenduan.
Frontea esaten zaio tenperatura desberdineko bi aire-masen arteko tarteari. Fronteak hotzak, beroak edo okluituak izan daitezke.


Aire hotza beroa baino dentsoagoa izan ahal izatea, eta azken horrek ur gehiago eduki ahal izatea disolbatuta hotza baino (uraren disolbagarritasuna tenperaturarekin batera handitzen baita), funtsezko kontzeptuak dira fronteen portaera ulertzeko.















Fronteen irudikapena eta motak
35 Bilatu Interneten airearen hezetasun erlatiboaren esanahia eta nola aldatzen den haren balioa tenperaturaren arabera.
36 Justifikatu hezetasunez betetako aire beroa hoztean hodeiak sortzen direla.
Fronte beroa desplazatzen den norabidean zirkuluerdiekin irudikatzen da, eta fronte hotza, mugitzen den alderantz triangeluekin.
Aire hotzak, dentsitate handiagokoak, aire beroa desplazatzen du, hura bultzatuz eta igo eta hoztu dadin eraginez; hodeiak sortzen ditu barruan zuen ur-lurruna kondentsatzean, eta prezipitazioak sortzen ditu.
Fronte okluitua


Aire beroak aire hotzari bultza egiten dio, haren gainetik igoz eta gora eginez. Hodeiak eta prezipitazioak sortzen dira, baina fronte hotzarekin baino intentsitate txikiagokoak.
Fronte okluitua fronte hotz bat epel batera iristen denean sortzen da. Fronte hotzaren tenperaturaren arabera, bi aukera daude; biek eragiten dituzte prezipitazioak.
Zehaztu itsasoko uretan 200 m-ko sakoneran dagoen presioa, atm, kg/cm2 eta psi-tan. Zer indar sentituko du arrain lau batek, alde bakoitzaren azalera 100 cm2-koa bada? Datua: dF = 1,025 g/cm3.
URRATSAK 1
ULERTU ENUNTZIATUA ETA ATERA DATUAK
• Enuntziatuaren kontzepturen bat ulertzen ez baduzu, egin kontsulta egokia.
• Datu bakoitzari dagokion ikurra jarri.
EGIN EGOERAREN MARRAZKI BAT
Ariketa batzuetan, marrazki on bat funtsezkoa da hura ebazteko. Beste batzuetan, iruditu liteke ez dela beharrezkoa, adibidez, ariketa honetan.
EBAZPENA 63 3 F = = • 100 cm 10 cm 1m 10 m S 2 42
hartu eta 2 –2 2 = =
F' F h S 2
IDENTIFIKATU ESKU HARTZEN DUTEN LEGE FISIKOAK
Puntu honetan ariketa honi buruz ikasi duzuna gogoratu behar duzu. Idatzi parte hartzen duten ekuazioak.
Itsasoan h sakonerako presioa indar bihurtzen da gainazal bat sakonera horretan jartzean. Indar hori beti da gainazalarekiko perpendikularra. Arrainak bi gainazal baditu, horietako bakoitzean indar bat egingo da.
Hidrostatikaren oinarrizko legearekin, likido baten presioa sakonera jakin batean aurkitzen dugu.
Eta presioak gainazal bakoitzean eragindako indarra kalkulatzeko, presioaren definizioa erabiltzen dugu.
pS F =
LORTU EMAITZA ETA AZTERTU HAREN
BALIOZKOTASUNA
Presioa SI-an adierazitako sakoneran kalkulatuko dugu.
Ondoren, adierazitako unitateetako presioa adierazteko behar diren unitate-aldaketak egingo ditugu.
pdgh F
4 1025
= ==
2009
Indarra, beraz, hau da:

2. ADIBIDEA
100 kg-ko ontzi karratu batek, 2 m-ko aldea eta 15 cm-ko lodiera duenak, harriak garraiatzen ditu ibaiaren uretan flotatzen dagoelarik. Zein arroka-masa karga daiteke gehienez?
URRATSAK
ULERTU ENUNTZIATUA ETA ATERA DATUAK
• Idatzi ariketaren enuntziatuak ematen dizkigun datuak; baliteke daturen bat ezkutatuta egotea, adibidez, uraren dentsitatea (1 g/cm3). Datu hori kontuan hartu behar dugu.
• Esleitu datu bakoitzari sinbolo egokia.
• Adierazi datuak SI-an.
EGIN EGOERAREN MARRAZKI BAT
Flotatzen ari den gorputz baten marrazkian, funtsezkoa da esku hartzen duten bi indarrak marraztea. Argi utzi behar da bolumen bat urpean dagoela eta beste bat azaleratuta.
Datuak hartu eta SI-an adieraziko ditugu:
• Ontzi karratuaren alde bakoitza: a = 2 m.
• Ontziaren lodiera: b = 15 cm = 0,15 m.
• Ontziaren masa: m = 100 kg.
• Fluidoaren dentsitatea (ura): dF = 1 g/cm3 1 cm g 10 g 1kg 1m 10 cm 1 000 m kg
Orekan dagoen ontziaren gainean bi indar jarduten dute: guztizko pisua beherantz eta bultzada gorantz. Biak berdinak dira moduluan.
4
IDENTIFIKATU ESKU HARTZEN
DUTEN LEGE FISIKOAK
Mota horretako ariketa baterako funtsezko legea Arkimedesena da. Gainera, gorputz baten pisua nola kalkulatzen den gogoratu behar dugu.
Ezinbestekoa da onartzea ezen, gorputza orekan dagoenez, bultzada pisu totalaren intentsitate berekoa dela.
LORTU EMAITZA ETA AZTERTU HAREN
BALIOZKOTASUNA
Flotatzen ari den gorputz baten edozein ariketatan ekuazio hau ebatzi behar dugu:
EP = l
Kasu honetan, dauzkagun datuekin garatu beharko da. Kontuan hartu behar dugu pisua ontziaren eta harrien ondoriozkoa dela. Eta ontziak karga dezakeen gehieneko pisua zehazteko, ahalik eta gehien hondoratuta suposatu beharko da, ahalik eta bolumen handiena ateratzeko eta bultzadak ahalik eta balio handiena izan dezan.
Arkimedesen adierazpena behar dugu:
EdVg F = ll
Gorputz baten pisua adierazpen honen bidez kalkulatzen da:
Pmg =
Gogora dezagun flotatzean gorputz batek hau betetzen duela:
EP = l
Ontzia 15 cm hondoratzen denean emango da ontziak egin dezakeen bultzada maximoa. Kasu horretan:
ll
EdVgdabg FF 2
== = =
1000 20,159,8 5 880 N
2 =
Hala, gehieneko pisua 5880 N-koa izango da, eta ontziarena gehi arrokena izango da:
PPPmgmg P roc
100 9, 8m 9, 85 880 N
roc 500kg m = =
embroc embroc += =+ =+ = = 9, 8 5880 – 100 9, 8
Hainbat web orrik aplikazio birtualak dituzte, hainbat fenomeno natural ikusteko eta haietan parte hartzen duten magnitudeen bilakaera behatzeko aukera ematen digutenak; aplikazio interaktiboak ere badaude, eta horietan erabiltzaileak manipulatu egin dezake: parametroak aldatu, neurtu, etab.
Unitate honetan, PhetInteractiveSimulations bisitatzea proposatzen dizugu; besteak beste, Coloradoko Unibertsitateak (Boulder) babesten du aplikazio hori. Orria hizkuntza askotara itzulita dago. Oso erraza da orria aurkitzea; idatzi Phet edozein bilatzailetan.
Web-orrian zaudenean, idatzi bilatzailean «hidrostatika», eta bi aplikazio agertuko zaizkizu. Guk lehenengoaren gainean egingo dugu klik: Presiopean.
INGURUNEAREKIN OHITZEA
Aplikazioa exekutatutakoan, likido bat duen tanga bat erakutsiko da. Hasierako tangaz gain, goiko ezkerreko izkinan dauden beste bi izango dituzu. Gera zaitez oraingoz lehenengo ontzi sinplearekin.
Iturriko giltzak likido gehiago botatzeko balio du, eta hustubidearenak, husteko. Likidoaren dentsitatea eta planetaren grabitatea alda ditzakezu beheko eskuineko aldean.
Neurtzeko tresna gisa, lauki-sare bat aktiba daiteke, likidoaren sakonera ikusteko; lau metroko erregela bat ere badugu nahi dugun tokian jartzeko eta altuera desberdinak neurtzeko.
Ondoren, aplikazioaren orrian sartuko gara, eta botoi bat sakatuko dugu hura gure gailuan ikusteko.
Barometro bat ere badago, eta haren neurri-unitatea kilopascalen (kPa), atmosferen (atm) edo hazbete karratuko libren (psi) artean konfigura daiteke. Barometroaren gainean klik egin eta botaz, saguaren botoia askatu gabe, nahi ditugun posizioetan nahi adina barometro jar ditzakegu.
Presio atmosferikoa
Lehenik eta behin, arrastatu barometroa airean jarri arte. Beha ezazu presioa pixka bat aldatzen dela, gorago edo beherago jartzen baduzu. Unitate honetan adierazten dugu
1 mmHg inguru aldatzen dela 10 m-ko desnibel bakoitzeko. Erabili erregela eta bi barometro hori egiaztatzeko. 10 m neurtu ezin ditugunez, altuera txikiagoarekin egin beharko dugu, eta mmHg ere ezin dugu erabili, beste unitate bat baizik. Idatzi kalkuluak zure libretan.
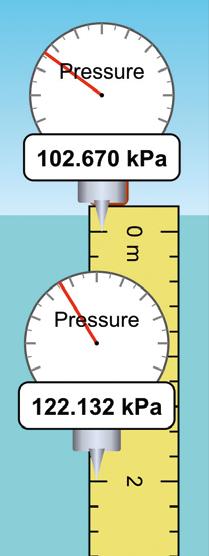
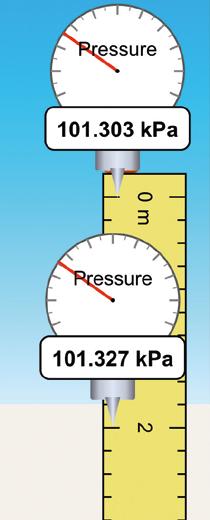
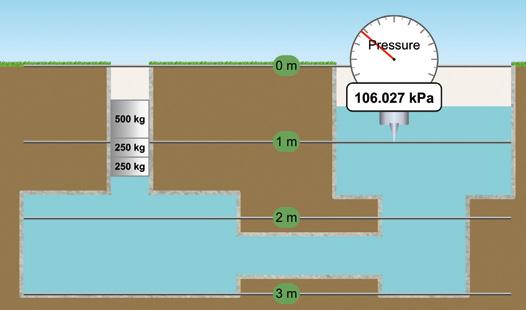
Orain atmosfera kentzen baduzu Itzalita aukera aktibatuz, barometroek zero markatzen dutela ikusiko duzu, altuera edozein dela ere.
Presio hidrostatikoa
Sakatu ResetAll esperientzia berri bati ekiteko. Barometroa likidoaren barruraino arrastatzen baduzu, ikusiko duzu presioa askoz azkarrago aldatzen dela sakonera aldatzean. Ikusi barometroa neurtzen ari den presioa presio atmosferikoa gehi presio hidrostatikoa dela. Presio hidrostatikoa bakarrik neurtu nahi baduzu, presio atmosferikoa kendu beharko zenuke, dakizunezs.
Muntaia sinple bat diseinatuko duzu, lehen airean egin duzun bezala, baina oraingoan likidoaren barruan izango da. Hori egiten duzunean, kontuan izan bi barometroen arteko presio-diferentzia finko dagoela deposituaren maila aldatzen duzunean.
Sakontasun-diferentzia da axola duena; nahiz eta atmosfera ezabatu, presioen arteko aldeak konstante dirau.
Egin zuk zeuk kalkuluak, eta egiaztatu aukeratu dituzun bi sakoneretako presio-diferentzia aplikazioak adierazten duena dela. Egin hainbat aldiz dentsitate- eta grabitate-balio desberdinekin. Idatzi kalkuluak zure libretan.
Ontzi komunikatzaileak
Bigarren tanga-motara aldatzen baduzu, ontzi komunikatzaileen adibide bat izango duzu. Ontziak betez eta hustuz, gainazal librearen mailak altuera berean mantentzen direla ikusiko duzu. Bi ontzietan barometroa jar dezakezu altuera berean, eta ontziak betetzean eta hustean presio bera egiten dutela egiaztatu. Bi ontziak komunikatzen dituen hodian barometroa jartzen baduzu, presioa dago, naiz eta puntu horren gainean ez egon likido-zutaberik gainazaleraino.
Prentsa hidraulikoa
Hirugarren tanga-motan, berriz ere bi tanga komunikatu dituzu, baina, gainera, Pascalen legea edo prentsa hidraulikoek funtzionatzen duten printzipioa ikus daitezke.
Enbolo txikian pisuak jarrita, ikusiko dugu enbolo handian likidoaren maila igotzen dela. Plataforma bat izanez gero, oso objektu astuna altxatzeko aprobetxa liteke, zeren, dakigun bezala, indarra biderkatu egiten baita.
Aplikazioaren bidez moldatzea proposatzen dizugu, enbolo txikiaren azalera kalkulatzeko. Agian beheko irudiak emango dizu hori egiteko moduaren pista bat. Idatzi kalkuluak zure libretan.
1 atm inguruko presio atmosferikoan bizi gara, hau da, gure larruazaleko cm 2 bakoitzeko 1,034 kg-ko pisuaren baliokidea. Presio hori pixka bat aldatzen da baldintza meteorologikoen eta altuera-aldaketen arabera. Seguru asko, bidaiatu duzunean, altitudea galduz edo irabaziz, presio-aldaketa nabaritu duzu inoiz, eta belarriak itxi zaizkizu.
Tinpanoa airearen bibrazioak jasotzen dituen mintza da, kanpo-belarria erdiko belarritik bereizten duena. Behar bezala entzuteko, erdiko belarriaren barneko presioak kanpoko presioaren berdina izan behar du, kanpo-belarrian dagoena dena. Erdiko belarriaren presioa kanpokoaren berdina da Eustakioren tronpa dela eta, erdiko belarria sudurraren barrualdearekin komunikatzen baitu. Hodi horrek mukiak ditu patogenoetatik babesteko. Altitudea aldatzen dugunean eta hodi horrek muki gehiegi dituenean, ezin da airerik atera edo sartu presioa berdintzeko, tinpanoa tentsio-egoeran geratzen da eta belarriak itxita sentitzen ditugu.
kanpo-belarria


barne-belarria
Esperimentua
tinpanoa
Eustakioren tronpa
Mendira edo kostara egiten duzun hurrengo bidaian
Prestatu patata-poltsa bat zure hurrengo bidaiarako. Adibidez, presioa poltsa barrukoa baino txikiagoa den mendi batera igotzen bazara, ikusiko duzu poltsa nola puzten den.
Aldiz, barnealdeko herri batetik kostara jaisten bazara, kontrakoa gertatzen dela ikusiko duzu: poltsa zimurtu egiten da.
• Zure ustez, nola eragin diezaiokete altitude-aldaketek ibilgailu baten pneumatikoen presioari?
• Bidaiari-hegazkinek 10 000 m inguruko altueran egiten dute hegaz. Altuera horretako presioa baxuegia da guk jasan ahal izateko. Horregatik, hegazkinaren kabina lurrazalekoa baino presio handiagoan presurizatzen da. Jakin ezazu zein altitudeari dagokion barne-presioa eta zergatik ez den 1 atm-an presurizatzen.
Problemaren planteamendua
Pascalen barrikaren esperimentua egin nahi dugu, baina eskala txikiagoan.
Zure proposamena
Hidrostatikaren oinarrizko legea eta Pascalen printzipioa berrikusi behar dituzu, esperimentua guztiz ulertzeko. Hori egin ondoren, saiatu esperientzia gauzatzeko modu bat asmatzen.
Gure proposamena
Barrika bat lehertu beharrean, tapoia eta lastotxoa dituen freskagarri-edalontzi batekin egingo dugu, janari lasterreko leku askotan ematen diren modukoak.
Material



• Freskagarri-edalontzi bat, urez betetako tapoiarekin.
• Metro bat eta erdi edo bi luze den mahuka edo hodia.
• Zinta itsasgarria edo silikona beroa.
• Inbutu bat.
• Botila bat urarekin.
• Errotuladorea eta zinta metrikoa.
Eskatutako ezagutzak berrikusi eta egin beharreko esperientzia egoki ulertzen duzunean, lanari ekingo diogu, urrats hauei jarraituz:
• Hodia edo mahuka lastotxorako duen tapakiaren zulora egokitu behar dugu. Horretarako, zinta itsasgarria edo silikona erabiliko dugu. Hermetikoki zigilatu behar da.
• Edalontzia urez betetzen dugu.
• Tapoia jartzen dugu urez betetako edalontziak hodia itsatsita duela.
1 Azal ezazu nola gerta daitekeen isuritako hain ur gutxiaren pisuarekin edalontzia lehertu izana. Horretarako, erabili hizkuntza zientifiko egokia eta adierazi lege edo printzipio egokiak.
2 Kalkula ezazu ur-zutabe horren ondorioz ontziari aplikatu zaion presioa, hidrostatikaren oinarrizko legea erabiliz.
• Tapoia zinta itsaskorrarekin edo silikona beroarekin zigilatzen dugu.
• Orain bakarrik falta da hodia pixkanaka urez betetzea. Horretarako, botila urarekin eta inbutuarekin erabiliko dugu. Mahuka bada, bertikalki jarri behar dugu betetzen den bitartean.
• Edalontzia lehertzen denean, egin marka bat errotuladore batekin, urez nora arte bete duzun puntua markatzeko.
• Neurtu ur-zutabearen altuera, edalontziaren tapatik markara arte.
3 Adieraz ezazu emaitza atmosfera eta hazbete karratuko libretan, eta idatzi koadernoan.
4 Esperimentu bera merkurioarekin egingo bagenu, zer altuera behar izango genuke?
5 Zer uste duzu gertatuko litzatekeela esperimentua urarekin egingo bagenu, baina mendi baten gailurrean?
Antolatu zure ideiak Kontzeptu-mapa sistemikoa
1 Marraztu gorputz bat likido batean flotatzen, haren gainean eragiten duten indarrak barne. Egin irudikapen bera likidodun depositu baten hondoan bermatuta dagoen gorputz batentzat.
Arkimedesen printzipioa
2 Osatu eskema hau zure koadernoan. Hortik abiatuta, egin ezazu kontzeptu-mapa oso bat, unitate honetan ikasi dituzun edukiak biltzen dituena.
hau da haren adierazpen matematikoa ................ ? ondorioak
Gogoan izan zenbakizko jarduera guztien soluzioak anayaharitza.es helbidean dituzula.
Presioa
1 100 N-ko indarra aplikatzen zaio 5 cm-ko diametroa duen gainazal zirkular bati. Zer presio egiten ari da?
2 Granitozko zutabe batek, 2,71 g/cm3-ko dentsitatekoak, 50 cm-ko diametroa eta 4 m-ko altuera ditu. Zehaztu bere pisuagatik bere oinarriaren gainean egiten duen presioa.
3 75 kg-ko pertsona batek 200 cm2-ko berme-azalerako bota batzuk ditu. Zehaztu zutik dagoenean elurrari egingo dion presioa. Eta eskiekin egiten duenean, bakoitza 1 800 cm2-ko azalerakoa? Eskiak daramatzanean elurra gutxiago zergatik hondoratzen den azal dezakezu?
4 20 kg-ko mahai batek 100 × 70 cm-ko taula angeluzuzena du. Lau hankak 4 × 4 cm-ko sekzio karratukoak dira. Zehaztu mahaiak lau hanken gainean bermatuta dagoenean duen pisuagatik egiten duen presioa, baita buelta eman eta taularen gainean bermatzen denekoa ere.
5 Zehaztu 7,5 cm-ko ertza duen kubo baten dentsitatea, 1 102,5 Pa-eko presioa eragiten duena bere pisuaren azpian.
6 Energia aurrerago ikasten duzunean, haren dimentsioa [E ] = M · L2 · T–2 dela ikusiko duzu. Egiaztatu presioa bolumen-unitateko energia bat dela.
Flotazioa
Pap = P – E ? ?
hau da haren adierazpen matematikoa hau da haren adierazpen matematikoa
Hidrostatikaren oinarrizko legea
7 Batu. Zero grabitateko likidoek forma esferiko bat eta ez beste bat hartzearen inguruko azalpen zientifikoa emateko gai zara?
8 Zehaztu Marianen hobiaren hondoan izango den presioa. Hori planetako puntu ezagun sakonena da, 11 012 m-koa. Demagun dentsitatea 1,025 g/cm3 dela.
d = 1 g/cm3
a = 8,5 cm
b = 4,2 cm
9 Zehaztu A puntuan dagoen presioa. a
c = 2,0 cm
bc A
10 Zer indarrekin egingo du presioa ontziko urak adarrik laburrenaren tapoian?
R = 10 cm
a = 2 cm
b = 9 cm
11 2,6 m-ko sakonera duen igerileku baten hondoan, hustubidearen tapoi zirkularra dago jarrita, 12 cm-ko diametroa eta 1,5 cm-ko lodiera duena. Bere dentsitatea 7,9 g/cm3-koa da. Zenbat pisatzen du tapoiak? Zer indar egin beharko dugu tapoia kentzeko?
d = 1 g/cm3
12 Zehaztu urak tangaren hondoan egiten duen indarra, eta esan urak duen pisua baino handiagoa edo txikiagoa den. Kontuan izan uraren bolumena adierazpen honen bidez kalkulatzen dela: V = 1/3 π · R 2 ·
· a – 1/3 π · r 2 · b
a = 10 cm
b = 4 cm
R = 6 cm
r = 3 cm
r
R
b a
13 Irudiko tangak 1 000 litro ur ditu. Hondoan 0,5 cm-ko diametroko zuloa du. Pertsona batek nahikoa indar egin dezake hatzarekin eta tanga itxi dezake hura hustu ez dadin?
Datua: h = 1 m. h
16 Zergatik uste duzu hiri-eremu batzuetan dorre altu bat dagoela, goiko aldean ur-biltegi bat duena?
17 Ikuspuntuen zirkulua. Erromatarrek akueduktu handiak egiten zituzten oztopoak gainditzeko eta ura leku batetik bestera eramateko. Zergatik guk ez ditugu eraiki behar?
18 Beheko irudiko likidoa orekan dagoela uste duzu? Justifikatu zure erantzuna
14 Gurpil logikoa. Inguruko bi lakuk altuera berean badituzte beren azalerak, ziurta dezakegu lurrazpian komunikatuta daudela?
15 Kale inklinatu batean lerro horizontal bat marraztu nahi dugun pareta bat dago; horretarako, mahuka zeharrargia dugu. Azaldu argi eta garbi nola jokatuko zenukeen hori egiteko eta zein printzipiotan oinarrituko zinatekeen.
19 Ura 20 000 Pa-ko presioan iristen bada seigarren solairura, zer presio egongo da beheko solairuan? Datua: 3 m daude solairu bakoitzeko.
20 Kantitate gutxien duen irudiko likidoa 0,8 g/cm 3ko olioa da. Zehaztu likido ezezagunaren dentsitatea.
a = 5 cm
b = 12 cm
21 U formako hodi batean hiru likido nahastezin daude. 1. likidoa ura da, eta 2. likidoaren dentsitatea 1,2 g/cm3 da. Zehaztu zein izango den 3. likidoaren dentsitatea. a
a = 3,1 cm
b = 1,3 cm
c = 0,6 cm
22 350 cm3-ko bolumena duen gorputz bat ur puruan sartuta dago. Zehaztu jasaten duen bultzada.
23 Zehaztu 3 cm-ko diametroa duen eta alkohol etilikoan sartuta dagoen esfera baten bultzada. Horren dentsitatea hau da: d = 0,79 g/cm3. Datua:
VEsfera = 4/3 · π · R3 .
24 Zehaztu 1,6 g/cm3-ko dentsitatea eta 5 cm-ko ertza duen kubo baten pisua eta itxurazko pisua uretan sartzen dugunean.
25 150 cm3-ko arroka baten itxurazko pisua, uretan sartuta dagoenean, 1,76 N da. Zehaztu arrokaren dentsitatea.
26 6 cm-ko altuera eta 2 cm-ko erradioa duen zilindro metaliko bat urez betetako ontzi batean sartzen da, irudian erakusten den bezala. Dinamometroak 1,40 N markatzen badu, zehaztu zein den zilindroaren dentsitatea. Datua: VZilindroa = π · R2 · h
31 Muntaketa hau egingo dugu. A aldean, pisuak jarri dira hagaxka orekatu arte, eta hori gertatzen da masa 4 911 g-koa denean. Muntaketaren beste aldean, B aldean, 8 cm-ko diametroko eta dentsitate ezezaguneko esfera bat jarri dugu uretan sartuta. Zehaztu ezazu esferaren dentsitatea. Datua: VEsfera = 4/3 π · R 3 . AB
32 AGA. Non uste duzu gutxiago nekatuko duela igeri egitea, ur gezatan edo gazitan? Justifikatu zure erantzuna.
33 Itsaso Hileko uraren dentsitatea 1,240 g/cm3 da. Azal dezakezu zergatik flotatzen duten pertsonek bertan?
34 Dentsimetroa gailu txiki bat da, likido batean flotatzean, urgaineratutako bolumena markatzen duena. Balio horrekin, flotatzen duen likidoaren dentsitatea zehazten da. 0,65 g/cm3-ko dentsitateko dentsimetro batek likido batean flotatzen badu eta haren bolumenaren % 35 azaleratzen bada, zer dentsitate du likidoak?
Pascalen legea
35 Azaldu prentsa hidraulikoaren funtzionamenduaren funtsa
27 Pertsona baten batez besteko dentsitatea 1,04 g/cm3koa bada, hondoratuko da edo flotatu egingo du uretan?
28 80 cm3-ko bolumena eta 0,49 g/cm3-ko dentsitatea duen gorputz bat gasolinan flotatzen ari da, zeinaren dentsitatea hau den: dF = 0,68 g/cm3. Gorputzaren zer bolumen dago azaleratuta?
29 Gehienezko karga duen itsasontzi bat itsasoko uretan nabigatzen ari bada, ibai baten bokaletik sartu ahal izango da ibaian gora nabigatuz? Arrazoitu erantzuna.
30 Mahai-ingurua. Zure ustez, zergatik jartzen dituzte urpekariek pisuak? Arrazoitu eta justifikatu zure erantzuna.
36 Prentsa hidrauliko batek 0,3 cm2-ko azalera txiki bat du, eta, handia, 40 cm2-koa. Zer indar lortuko da enbolo handienean, enbolo txikiari 100 N-ko indarra aplikatzean?
37 Prentsa hidrauliko bateko enbolo txikiaren diametroa 1,5 cm da, eta handiarena, berriz, 30,0 cm. 900 kg-ko auto bat jasota badago, zer indar aplikatzen zaio enbolo txikiari?
Presio atmosferikoa
38 Orri birakaria. Presio atmosferikoa gainean dugun airearen pisuaren ondorioa bada, zergatik ez dugu nabaritzen presioa txikitzen dela sabaiaren azpian jartzen garenean?
39 Adierazi 990 mb-ko presio-balioa ikasitako gainerako unitateetan.
40 Oso lasto luze batekin ura xurgatzen duen pertsona bat gai da bere ahoan presio atmosferikoaren hamarrena adinako hutsa egiteko. Zein altueraraino igoko da ura?





41 Urez gainezka dagoen ontzi bat kartoi mehe plastifikatu batekin estaltzen badugu eta buelta ematen badiogu, ikusiko dugu ura ez dela erortzen. Nola bultzatzen du kartoi meheak presio atmosferikoa gorantz?


42 Irudiko likidoak orekan egongo dira? Justifikatu erantzuna.
Unitate honetako jardueretan giza gorputzaren presio-mugei buruzko informazioa lortu duzu, eta presio atmosferikoaren kontzeptuak aplikatu dituzu Marteren baldintzak aztertzeko.






Deskargatu anayaharitza.es helbidean eskaintzen dizugun galdera-sorta prozesu honi buruz hausnartzeko.
formatutan
43 Bilatu Interneten gaurko mapa meteorologikoa, eta justifikatu gaurko eta biharko eguraldia
Airean murgilduta bizi gara, eta, nahiz eta horrek gutxi «pisatzen» duen, asko da gainean dugun kopurua, gure gain batere ez baztergarria den presioa eragiten duena.
Gogoratu: gutxi gorabehera kilogramo baten pisua da zentimetro karratu bakoitzean. Gure inguruan airearen presio horren frogak aurki ditzakegu.
Inoiz galdetu diozu zeure buruari zergatik itsasten diren bentosak? Gogor tiratuz gero, ez ditugu askatuko; ertz bat altxatuz gero, ordea, erraz askatzen dira.
Edo, konturatu zara nolakoa den kanario baten kaiolan dagoen edontzia? Zergatik ez da ura isurtzen?
Oso esperimentu erraz bat egitea proposatzen dizugu. Jarri egunkari-orri bat mahaiaren ertzean. Behetik erregela bat sartu, irudian ikusten den bezala.
Egin anayaharitza.es helbidean barne hartutako gaitasun-autoebaluazioa.
Erregelaren muturra leunki beherantz bultzatzen baduzu, orria altxatzen dela ikusiko duzu. Baina zer gertatzen zaio beherantz kolpe lehor bat ematen diozunean?
Bidaiatzen duzun hurrengoan, eraman plastikozko botila huts bat, hau da, airea duena barruan. Itxi ondo tapoia, eta behatu zer gertatzen zaion altitudea aldatzen denean.

© GRUPO ANAYA, S.A., 2022 - C/ Valentín Beato, 21 - 28037 Madrid.
Eskubide guztiak gordeta. Legeak lan honen edukia babestu eta espetxe-zigorrak edota isunak eta kalte-galeren ondoriozko kalte-ordainak ezartzen ditu honako hauentzat: edozein literatura-lan, artelan zein zientzia-lan, edo horren eraldaketa, interpretazioa edo gauzapena (edozein euskarritan finkatuta edo edozein eratan komunikatuta), oso-osorik edo zati batean, baimenik gabe erreproduzitu, plagiatu, banatu edo komunikatzen dutenentzat.