

MEDIA PEMBELAJARAN:
VIDEO CASE SERIES TUBERKULOSIS
Sebagai pelengkap modul ini, Dokter Muda dapat juga mengakses video pembelajaran berikut:
https://www.youtube.com/watch?v=Ma2A_u4t4vQ


KATA PENGANTAR
Puji syukur kami panjatkan ke hadirat Allah SWT atas rahmat dan karunia-Nya sehingga Modul Pembelajaran Tuberkulosis untuk Dokter Muda Stase Ilmu Penyakit Dalam ini dapat disusun dan diselesaikan.
Tuberkulosis (TB) hingga saat ini masih merupakan salah satu masalah kesehatan utama di dunia maupun di Indonesia. Beban penyakit yang tinggi, keberadaan koinfeksi dan komorbid, serta tantangan dalam tatalaksana komprehensif menjadikan TB sebagai kompetensi klinis yang wajib dikuasai oleh setiap dokter umum. Dokter muda sebagai calon dokter umum diharapkan memiliki kemampuan yang memadai dalam mengenali, menegakkan diagnosis, menatalaksana awal, serta melakukan edukasi dan upaya pencegahan TB secara terpadu.
Modul ini disusun sebagai panduan pembelajaran yang terstruktur bagi dokter muda selama menjalani stase Ilmu Penyakit Dalam, khususnya pada topik tuberkulosis. Materi di dalamnya dirancang selaras dengan Standar Kompetensi Dokter Indonesia dan kurikulum pendidikan kedokteran di Fakultas Kedokteran, Kesehatan Masyarakat dan Keperawatan Universitas Gadjah Mada, dengan penekanan pada:
1. Pemahaman dasar mengenai bakteri tuberkulosis, epidemiologi, dan faktor risiko
2. Mekanisme patogenesis TB paru dan TB ekstraparu.
3. Penegakan diagnosis berbasis gejala klinis, pemeriksaan fisik, dan penunjang sesuai pedoman terkini.
4. Prinsip tatalaksana TB secara komprehensif, rasional, dan berkesinambungan
5. Aspek pencegahan, kontrol infeksi, komunikasi efektif dengan pasien dan keluarga, serta kolaborasi interprofesional.
Kami berharap modul ini tidak hanya menjadi bahan bacaan, tetapi juga menjadi panduan praktis dalam proses pembelajaran klinis di bangsal, poliklinik, maupun layanan primer. Penyusunan modul ini tetap menyisakan ruang untuk perbaikan dan pengembangan. Oleh karena itu, kami sangat mengharapkan masukan dan saran konstruktif dari para pengajar, sejawat, dan para dokter muda pengguna modul ini, agar edisi selanjutnya dapat menjadi lebih baik dan lebih relevan dengan dinamika perkembangan ilmu pengetahuan dan pedoman klinis terkini.
Akhir kata, kami menyampaikan apresiasi dan terima kasih kepada semua pihak yang telah membantu dalam proses penyusunan modul ini, baik secara langsung maupun tidak langsung. Semoga modul ini dapat memberikan manfaat optimal dalam peningkatan kualitas pembelajaran dan turut berkontribusi pada upaya penanggulangan tuberkulosis di Indonesia.
Yogyakarta, 12 November 2025
Tim Penyusun
DAFTAR ISI

B.
B.1
B.2
B.4
C.
C.1
C.2
C.3
C.4
C.5
C.6
C.8
C.9
C.10
D. Faktor inang dan patogen yang memodulasi perjalanan penyakit
E.
E.1 Dewasa (≥15 tahun)
E.2 Anak (0–14 tahun)
E.3
F.
G.
B.1 Penatalaksanaan Efek Samping Utama
B.2 Definisi Respon dan Kegagalan Terapi
C.4
C.5
C.6

G.2
G.3
DAFTAR GAMBAR
Gambar 1 Estimasi Insidensi Tuberkulosis (WHO Global TB Report 2024) 1
Gambar 2 Gram stained M. Tuberkulosis (idm.uct.ac.za) 5
Gambar 3 Mekanisme patogenesis Tuberkulosis (Louis dan Priez, 2020) 7
Gambar 4 Gejala Tuberkulosis (Louis dan Priez, 2020) 9
Gambar 5 Patologi TB Miliar (Sharma et al., 2005)
Gambar 6 Tuberculosis Meningitis (Sharma et al., 2005)
Gambar 7 Spondilitis TB / Pott Disease (Netter et al., 2005)
Gambar 8 Peritonitis Tuberkulosis
Gambar 9 Limfadenitis Tuberkulosis
Gambar 10 Alur Penegakan Diagnosis Tuberkulosis (PNPK, 2020)
Gambar 11 Kartu Identitas Pasien TB 01 dan 02
Gambar 12 Alur Pemberian TPT pada Kontak Serumah (Kemenkes, 2025)

DAFTAR TABEL
Tabel 2 Dosis harian OAT lini pertama (dewasa, acuan mg/kgBB)
Tabel 3 Kombinasi Dosis Tetap OAT (Kemenkes, 2025) 20
Tabel 4 Panduan Terapi Pencegahan Tuberkulosis (Kemenkes, 2025) 24
Tabel 5 Panduan Terapi Pada Gagal Ginjal Kronis
BAB I
PENDAHULUAN
A. Latar Belakang dan Epidemiologi Tuberkulosis (TB)
Tuberkulosis (TB) merupakan salah satu penyebab utama mortalitas akibat penyakit infeksi di dunia. Menurut temuan terbaru (WHO Global Tuberculosis Report 2024; data hingga 2023), beban TB secara global masih tinggi dan baru pulih bertahap pasca pandemi COVID-19. Hal ini menegaskan urgensi penguatan penemuan kasus, akses diagnosis cepat berbasis molekuler, serta kesinambungan pengobatan sampai tuntas sebagai pilar eliminasi TB.
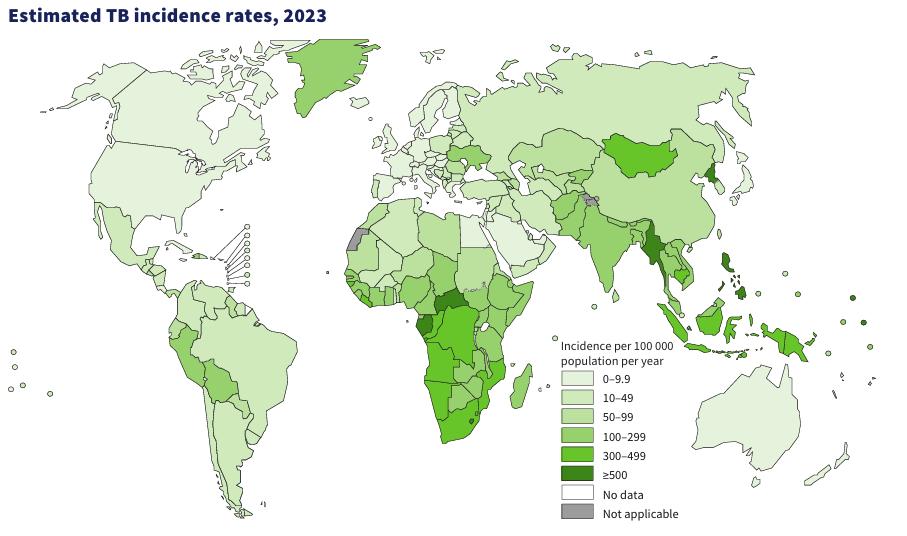

(WHO Global TB Report 2024)

Gambar 1 Estimasi Insidensi Tuberrkulosis (WHO Global TB Report 2024)
Secara global pada tahun 2023, diperkirakan sekitar 10,8 juta orang menderita TB dengan sekitar 1,25 juta kematian. Negara-negara dengan kontribusi terbesar terhadap total kasus global antara lain India, Indonesia, Tiongkok, Filipina, Pakistan, Nigeria, Bangladesh, dan Republik Demokratik Kongo. Notifikasi kasus mencapai sekitar 8,2
juta tertinggi sejak pencatatan WHO namun masih terdapat kesenjangan sekitar 2,7
juta kasus antara estimasi insidensi dan kasus yang terlapor. Beban TB resistan obat (MDR/RR-TB) diperkirakan sekitar 400 ribu kasus baru; sekitar 44% di antaranya
mendapatkan pengobatan. Proporsi MDR/RR-TB global sekitar 3,2% pada kasus baru dan 16% pada pasien dengan riwayat terapi sebelumnya. Koinfeksi TB–HIV menyumbang kira-kira 6% dari seluruh kasus TB; cakupan ART tinggi pada pasien TB yang terlapor namun masih lebih rendah bila dibanding estimasi total ODHIV yang mengalami TB, menandakan perlunya peningkatan skrining dan layanan terpadu TB–HIV.
Indonesia termasuk penyumbang beban TB terbesar kedua di dunia (sekitar 10% dari total global). Pemulihan layanan selama 2022–2023 mendorong peningkatan deteksi dan pengobatan, berkontribusi pada perbaikan tren global, namun masih terdapat kesenjangan deteksi. Indonesia menyumbang proporsi bermakna dari gap global antara insidensi estimasi dan kasus terlapor. Studi inventori nasional 2023 menunjukkan penurunan under-reporting dan konsistensi estimasi berbasis metode capture–recapture dengan model WHO, sehingga memperbaiki akurasi estimasi beban. Secara tingkat populasi, insidensi Indonesia berada pada kisaran tinggi untuk kawasan, sekitar ratusan per 100.000 penduduk (sekitar 300–400 per 100.000), menegaskan perlunya penguatan layanan primer–rujukan, perluasan tes resistansi obat, serta penanganan komorbid (HIV, DM, gizi) untuk mengurangi transmisi dan mortalitas
Konteks epidemiologis ini mempertegas kebutuhan dokter layanan primer termasuk dokter muda untuk menguasai kompetensi utama dalam penegakan dan penatalaksanaan TB. Penguasaan tersebut mencakup kemampuan klinis (diagnosis, tata laksana, pemantauan), kemampuan programatik (pencatatan–pelaporan, penelusuran kontak, edukasi kepatuhan), serta kepekaan terhadap determinannya (sosial, lingkungan, komorbiditas). Dengan begitu, pelayanan menjadi lebih komprehensif, aman, dan berorientasi pada eliminasi TB di Indonesia.

B. Pentingnya Pembelajaran TB bagi Dokter Muda (Berbasis SKDI)
Standar Kompetensi Dokter Indonesia (SKDI) menjadi acuan utama penyusunan capaian pembelajaran. Di dalam SKDI, tingkat kemampuan klinik dibagi dalam level (1–4) yang menggambarkan kemandirian dan keluasan praktik seorang dokter umum. Secara umum, level 4 (sering disebut 4A) menandakan kemampuan untuk menegakkan diagnosis dan melakukan tata laksana secara mandiri dan tuntas pada konteks layanan
primer; level 3 menekankan diagnosis klinik dan tatalaksana awal berikut keputusan rujukan yang tepat; sedangkan level 2 menekankan pengenalan masalah dan rujukan.

1. Mengacu pada daftar penyakit dalam SKDI untuk bidang respirasi dan penyakit infeksi, pembelajaran TB bagi dokter muda diarahkan pada capaian berikut:
1) Tuberkulosis paru tanpa komplikasi Level 4A: mampu menegakkan diagnosis, memulai dan memantau terapi standar, melakukan konseling kepatuhan, edukasi pencegahan penularan, serta melakukan pencatatan–pelaporan sesuai jejaring DOTS.
2) TB dengan komorbid atau kondisi khusus (mis. TB dengan HIV, TB pada anak, TB ekstraparu tertentu) Level 3A: mampu menegakkan diagnosis klinik, melakukan tatalaksana awal yang aman, menilai indikasi rujukan, dan melakukan koordinasi rujukan.
3) TB resisten obat (DR- TB/MDR-TB) Level 2: mampu mengenali kecurigaan DR-TB (riwayat pengobatan, hasil resistensi, gagal klinis), melakukan stabilisasi awal dan melakukan rujukan ke layanan rujukan DR-TB.
Dengan pendekatan berbasis SKDI, pembelajaran dokter muda berfokus pada penguasaan kompetensi klinik yang bermakna bagi layanan primer, sekaligus kompetensi programatik untuk keberhasilan pengendalian TB. Ruang lingkup kemampuan yang ditekankan antara lain:
- Anamnesis terarah dan pemeriksaan fisik sistematis pada gejala respiratorik kronik.
- Pemilihan dan interpretasi pemeriksaan awal (mikroskopis, uji cepat molekuler/NAAT, foto toraks) dan klasifikasi kasus.
- Inisiasi rejimen pengobatan standar sesuai pedoman nasional, pemantauan efek samping obat, serta penilaian keberhasilan terapi.
- Edukasi pasien dan keluarga mengenai kepatuhan minum obat, etika batuk, ventilasi, gizi, dan pencegahan penularan.
- Pencatatan–pelaporan, penelusuran kontak, dan kolaborasi layanan (puskesmas–RS rujukan–laboratorium jejaring).

- Skrining dan tata laksana awal komorbid (HIV, DM, malnutrisi), serta kewaspadaan dan rujukan pada kecurigaan DR-TB, TB anak, dan TB ekstraparu.C. Tujuan Modul
Modul ini disusun untuk memudahkan proses belajar dokter muda dengan pendekatan yang ringkas, sistematis, dan siap pakai di klinik. Tujuan khusus modul adalah sebagai berikut:
1) Menyelaraskan capaian pembelajaran dengan SKDI: TB paru tanpa komplikasi (Level 4A), kondisi khusus seperti TB dengan HIV/TB anak/TB ekstraparu (Level 3A sesuai konteks), dan DR-TB (Level 2).
2) Menyajikan ringkasan epidemiologi global dan Indonesia sebagai dasar urgensi klinik, etika profesi, dan keselamatan pasien.
3) Membekali langkah praktis layanan primer: alur diagnosis, pemilihan pemeriksaan, klasifikasi kasus, inisiasi rejimen standar, pemantauan efek samping dan kepatuhan, kriteria rujukan, serta pencatatan–pelaporan.
4) Menguatkan kemampuan komunikasi klinis untuk edukasi pasien–keluarga dan penelusuran kontak, serta kerja tim dalam jejaring DOTS.
5) Menanamkan sikap profesional, kolaboratif, dan berorientasi mutu, termasuk sensitivitas terhadap komorbid (HIV, DM) dan determinan sosial.
6) Menyediakan alat bantu belajar (ringkasan, algoritme, daftar periksa/checklist) agar dokter muda dapat melakukan tindakan sesuai kewenangan secara aman dan efektif.
BAB II
PATOGENESIS INFEKSI TUBERKULOSIS

SOAL KASUS

VIDEO: WHO's Science in 5 - Facing the TB crisis (Tuberculosis)
Pria 40 tahun dengan suspek TB tulang. Sampel histopatologi dari tulang menunjukkan granuloma tuberkulosa lengkap (kaseosa, epitelioid, limfosit). Sel mana yang menjadi penanda morfologi bahwa granuloma bersifat tuberkulosa klasik?
A. Sel Leydig
B. Sel histiosit raksasa (Langhans)
C. Sel Schwann
D. Sel penggulung (Rolled macrophage)
E. Osteoklas
A. Mycobacterium tuberculosis (MTB)
Mycobacterium tuberculosis (MTB) adalah basil aerob, tidak bergerak, tidak membentuk spora, berbentuk batang dengan dinding sel kaya lipid (asam mikolat) yang menyebabkan sifat tahan asam (acid-fast). Sifat ini mendasari penggunaan pewarnaan
Ziehl–Neelsen (ZN) atau auramin untuk deteksi Basil Tahan Asam (BTA). MTB merupakan penyebab utama tuberkulosis pada manusia dan tumbuh lambat dengan waktu generasi ±24–30 jam; pada kultur padat, koloni sering dideskripsikan kasar (‘rough, tough and buff’)
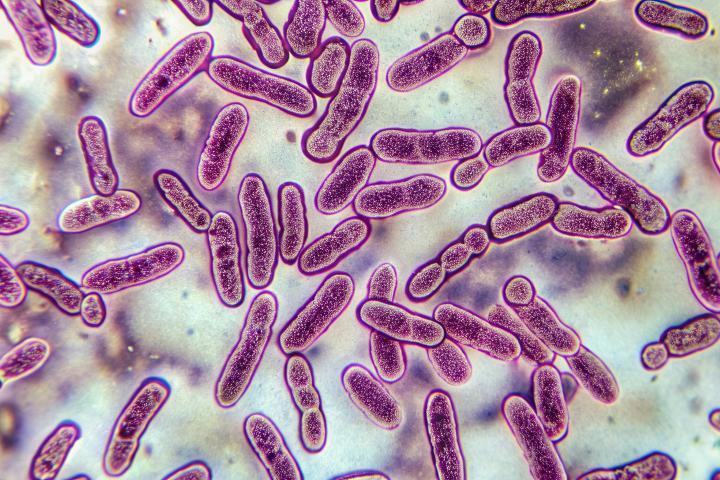
Gambar 2 Gram stained M.Tuberkulosis (idm.uct.ac.za)
Struktur dinding sel MTB terdiri atas peptidoglikan, arabinogalaktan, dan lapisan asam mikolat yang tebal, memberikan resistensi terhadap desinfektan, lingkungan yang kering, dan beberapa antibiotik. Di lingkungan, MTB dapat bertahan pada kelembapan sedang namun sensitif terhadap sinar ultraviolet dan panas.

Cara hidup di inang. MTB bersifat parasit intraseluler fakultatif. Di alveolus, basil difagositosis oleh makrofag, namun dapat menghambat fusi fagosom–lisosom, menghindari asidifikasi, dan memodulasi kematian sel sehingga bertahan hidup dan bereplikasi. Molekul patogen (mis. lipoarabinomannan, fosfatidilinositol, Hsp) dikenali
oleh PRR (TLR2/4/9) sehingga memicu produksi sitokin proinflamasi (TNF, IL-1β, IL-12)
sebagai bagian dari respon imun bawaan.
Penyebaran/Transmisi. Transmisi utama adalah melalui inhalasi droplet nuclei (1–5 μm)
yang mengandung basil hidup dari pasien TB paru aktif saat batuk/bersin/bernyanyi.
Partikel halus dapat melayang berjam-jam di udara ruangan tertutup dan terhirup individu rentan. Risiko penularan meningkat dengan beban kuman tinggi (BTA positif, kavitas), kontak erat dan lama, serta ventilasi buruk; terapi efektif menurunkan infektivitas secara cepat dan bermakna. Di antara kontak serumah, risiko infeksi rata-rata sekitar 30%.
B. Patogenesis TB Paru
B.1 Infeksi primer dan pembentukan kompleks primer
Infeksi primer lazimnya terjadi pada anak atau individu imunologis naive terhadap MTB.
Kuman berkolonisasi pada fokus parenkim (Ghon focus) dan menyebar ke kelenjar limfe regional (hilus/mediastinum), membentuk kompleks primer (kompleks Ghon/Ranke).
Limfadenopati sering menonjol pada fase primer. Sebagian besar kasus terkontrol dan menetap sebagai infeksi laten; sejumlah kecil berkembang menjadi penyakit aktif dalam bulan-bulan awal, termasuk presentasi seperti efusi pleura primer atau TB milier.

B.2 Transisi laten → reaktivasi (post- primer)
Setelah fase primer, MTB dapat bertahan lama dalam granuloma. Penurunan imunitas
sel-T (mis. karena malnutrisi, diabetes tidak terkontrol, CKD stadium lanjut, HIV, penggunaan kortikosteroid/agen imunosupresif, keganasan/kemoterapi) dapat memicu
reaktivasi. TB post-primer cenderung mengenai lobus atas/segmen posterior (kandungan oksigen relatif tinggi), disertai pembentukan kavitas. Kavitas terbentuk
akibat nekrosis kaseosa yang melikuifikasi dan terdrainase ke bronkus; dinding kavitas biasanya berkolagen. Lesi hipoksik menginduksi ekspresi MMP (mis. MMP-1) dan protease lain yang mempercepat destruksi parenkim paru.
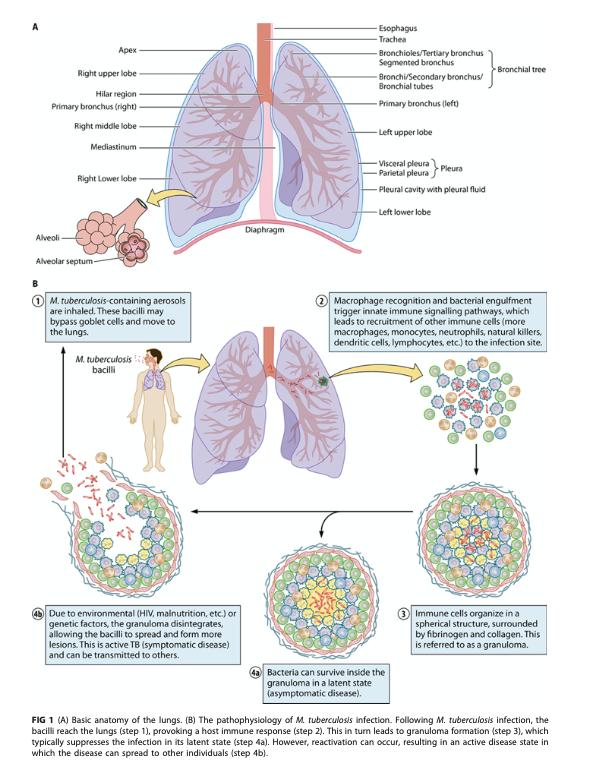
Gambar 3: Mekanisme pathogenesis Tuberkulosis (Louis and Priez,2020)

B.3 Penyebaran bronkogenik dan remodelling jaringan
Material semiliquid dari kavitas mengalir ke saluran nafas bronkial lalu menyemai fokus baru sepanjang jalan napas, menghasilkan nodul-nodul kecil (2–4 mm) dan pola bronkopneumonia TB. Secara klinis, hal ini berkorelasi dengan batuk produktif berkepanjangan, hemoptisis, dan risiko penularan yang tinggi. Dalam jangka panjang, remodelling jaringan dipengaruhi oleh keseimbangan MMP dan inhibitor-nya memicu bronkiektasis, fibrosis, serta predisposisi aspergiloma pada rongga kavitas yang menetap.
B.4 Korelasi klinis–radiologi–biologi
• TB primer: limfadenopati hiliar/mediastinal menonjol; efusi pleura dapat muncul 3– 6 bulan pascainfeksi (reaksi hipersensitivitas terhadap tuberkuloprotein; biasanya unilateral).
• TB post-primer: lesi apikal, kavitasi, diseminasi bronkogenik; gejala lebih ‘klasik’ (batuk >2–3 minggu, demam, keringat malam, penurunan BB).
• Komplikasi: bronkolitiasis (ekstrusi nodus limfe terkalsifikasi ke bronkus), hemoptisis, bronkiektasis, empyema, aspergiloma.
C. Mekanisme TB Ekstraparu (EPTB)
C.1. Prinsip umum seeding ekstra-paru
Sejak fase primer, MTB dapat memasuki sirkuit limfatik dan/atau hematogen. “Rich foci” (mikro-fokus TB laten) dapat menetap pada berbagai organ dan reaktivasi kemudian hari menghasilkan EPTB. Prinsip patogenesis EPTB tetap berpusat pada granuloma dan nekrosis kaseosa setempat, dengan tingkat destruksi jaringan yang dipengaruhi status imun host dan lingkungan mikro (hipoksia, lipid, pH, enzim proteolitik).
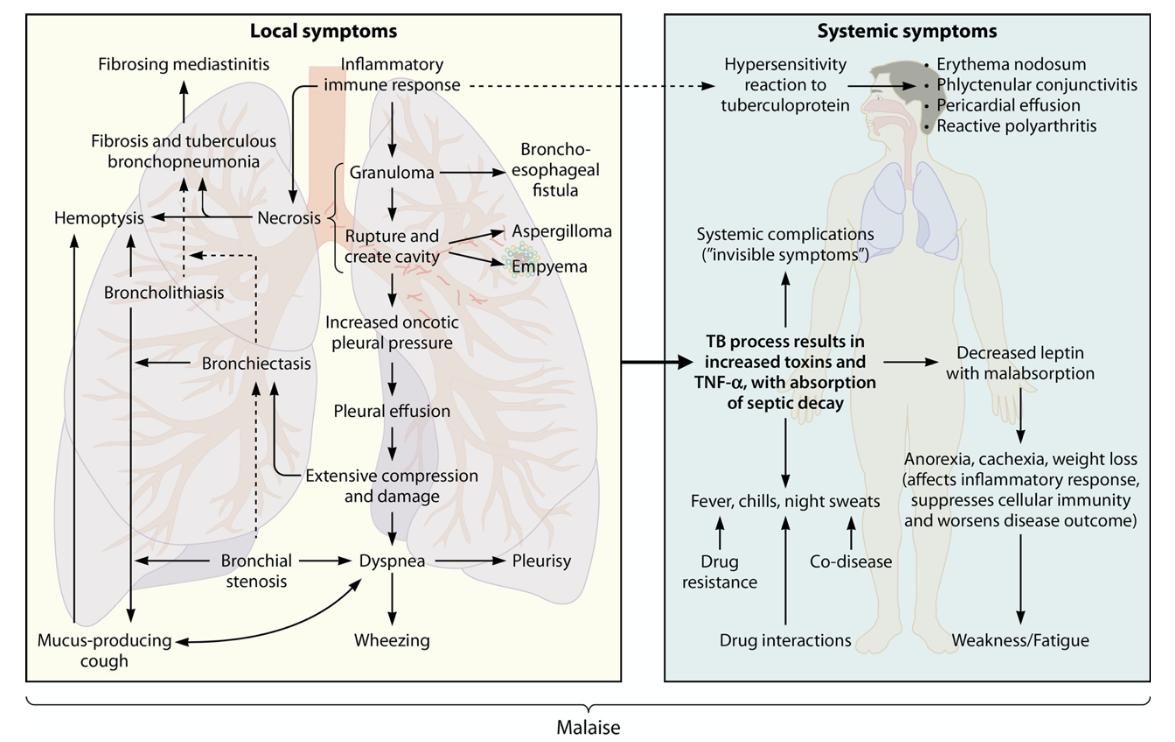
Gambar 4: Gejala Tuberkulosis (Louis and Priez,2020)

C.2. TB pleura
TB pleura primer sering terjadi 3–6 bulan pascainfeksi dan berkaitan dengan hipersensitivitas terhadap tuberkuloprotein di ruang pleura. Cairan cenderung eksudatif limfositik, dengan gambaran biokimia yang dapat menunjukkan peningkatan penanda tertentu (misal ADA—meski nilai rujukan harus ditafsirkan sesuai konteks klinis dan sumber pedoman). Efusi masif dapat menekan paru dan menyebabkan nyeri pleuritik, batuk, dan dispnea. Pada sebagian kasus, koloni MTB masuk ruang pleura melalui invasi hematogen atau ruptur fokus subpleura.
C.3. TB trakeobronkial
TB trakeobronkial dapat muncul akibat perforasi kelenjar limfe terinfeksi ke bronkus atau ekstensi dari lesi parenkim. Ulserasi dan proses penyembuhan berulang menimbulkan jaringan parut dan stenosis bronkus. Secara klinis, pasien dapat mengalami batuk menetap, mengi, wheezing monofonik, atau infeksi berulang distal dari sumbatan.

C.4. TB milier
TB milier merupakan penyebaran hematogen luas yang menimbulkan banyak nodul kecil bilateral pada paru dan keterlibatan multi-organ (hati, lien, sumsum tulang, meninges).
Biasanya berasal dari masuknya MTB ke sirkulasi melalui ruptur lesi kaseosa ke pembuluh darah atau drainase limfatik ke duktus torasikus lalu ke sistemik. Gambaran klinis dapat nonspesifik (demam panjang, penurunan BB, hepatosplenomegali) dan memerlukan kewaspadaan tinggi.
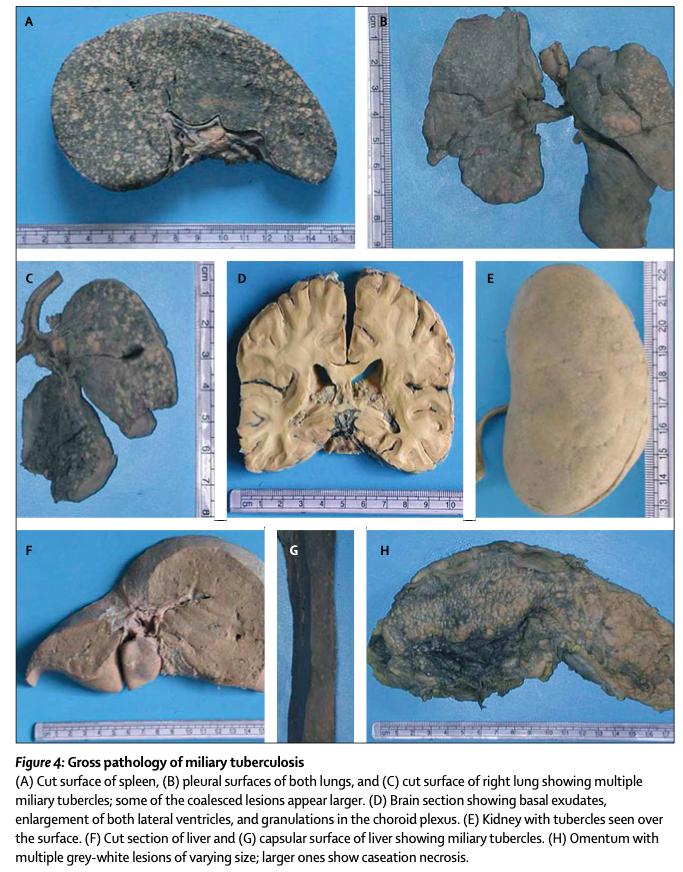
Gambar 5: Patologi TB Miliar (Sharma et al,2005)
C.5. TB meningitis
Pada TB meningitis, mikro-fokus subependim/subpial (Rich focus) mengalami ruptur ke ruang subaraknoid, memicu inflamasi luas leptomening, eksudat basal, vasculitis, dan hidrosefalus obstruktif. Keterlambatan terapi berhubungan dengan morbiditas/kematian tinggi; patogenesis ini menjelaskan dasar penggunaan kortikosteroid adjuvan pada TB meningitis (berdasar pedoman ) untuk menekan inflamasi berlebihan.

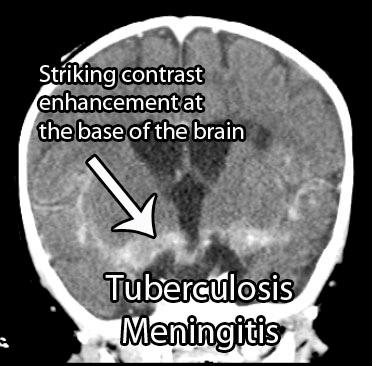
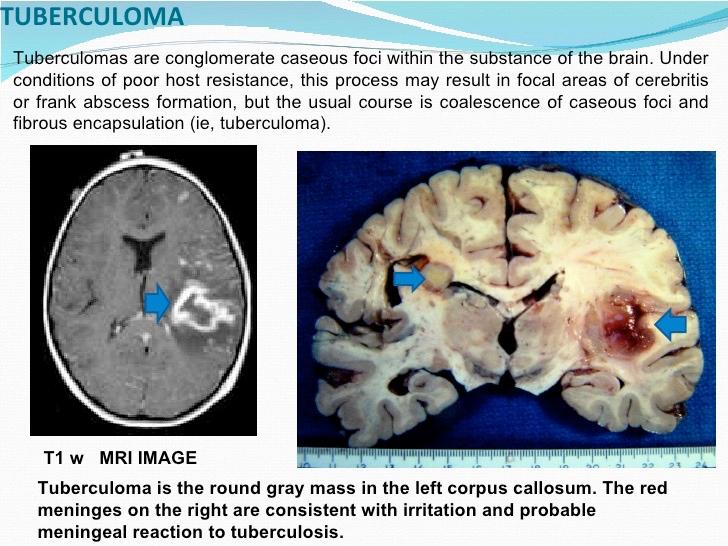
C.6. TB tulang/sendi (Pott) dan muskuloskeletal
Seeding hematogen ke korpus vertebra menimbulkan spondilitis TB (Pott disease), sering mengenai segmen torakal bawah/lumbal. Destruksi korpus dapat memicu kifosis, abses paravertebral/psoas, dan defisit neurologis akibat kompresi. Pada sendi, sinovitis granulomatosa kronik menyebabkan nyeri, pembengkakan, dan keterbatasan gerak; gambaran radiologi memperlihatkan penyempitan celah sendi progresif dan erosi marginal.
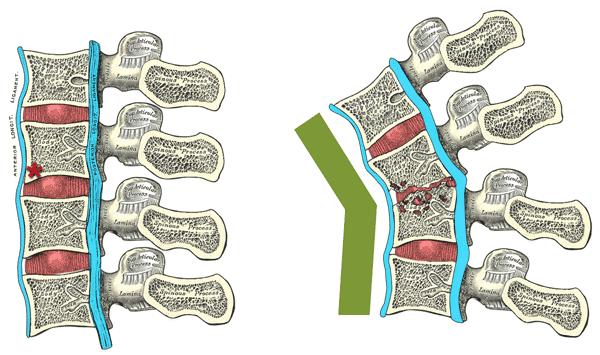
Gambar 7: Spondilitis TB/ Pott Disease (Netter et al,2005)
C.7. TB genitourinaria
Seeding ke ginjal menghasilkan granuloma kortikomeduler, yang dapat meluas ke pelvis renalis dan ureter, menimbulkan steril pyuria, hematuria mikroskopik, dan striktur ureter. Pada sistem reproduksi, TB dapat menyebabkan infertilitas (obstruksi tuba, sinekia intrauterin) atau epididimo-orkitis pada pria.
C.8 TB Gastrointestinal
Pasien dengan TB peritoneum biasanya bermanifestasi sebagai TB gastrointestinal, ditemukan pada individu berusia <40 tahun dan frekuensinya lebih besar pada perempuan. Manifestasi klinisnya tidak spesifik dan mirip dengan penyakit gastrointestinal lainnya.

C.8. TB perikardium
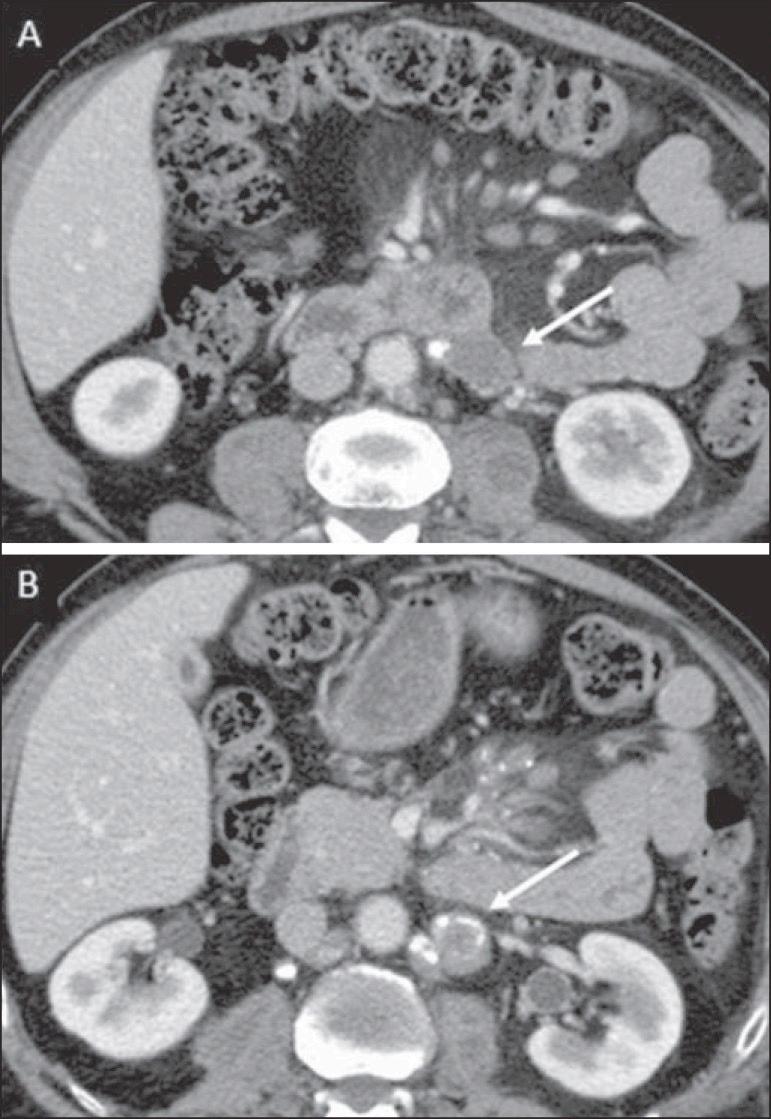
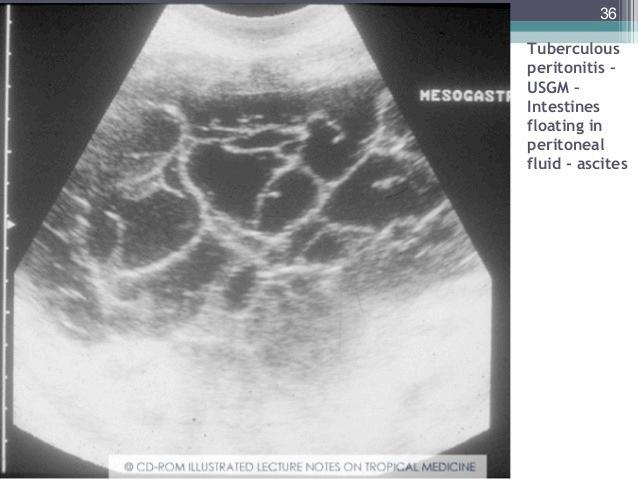
: Peritonitis Tuberkulosis
Perikarditis TB dapat terjadi melalui ekstensi dari kelenjar limfe mediastinum atau fokus paru subpleura, menghasilkan efusi perikard, perikarditis konstriktif, atau tamponade.
Patogenesis inflamasi yang berat menjadi dasar pertimbangan kortikosteroid adjuvan pada kondisi terpilih sesuai pedoman.
C.9. Limfadenitis TB ekstra- torakal.
Merupakan bentuk EPTB tersering; sering mengenai kelenjar servikal. Patogenesis mencakup perluasan dari kompleks primer, diseminasi hematogen/limfatik, reaktivasi fokus dorman, atau penjalaran langsung. Presentasi berupa massa kelenjar >2×2 cm (sering multipel) dan dapat berfistel; konfirmasi melalui FNAB/kultur/histopatologi.

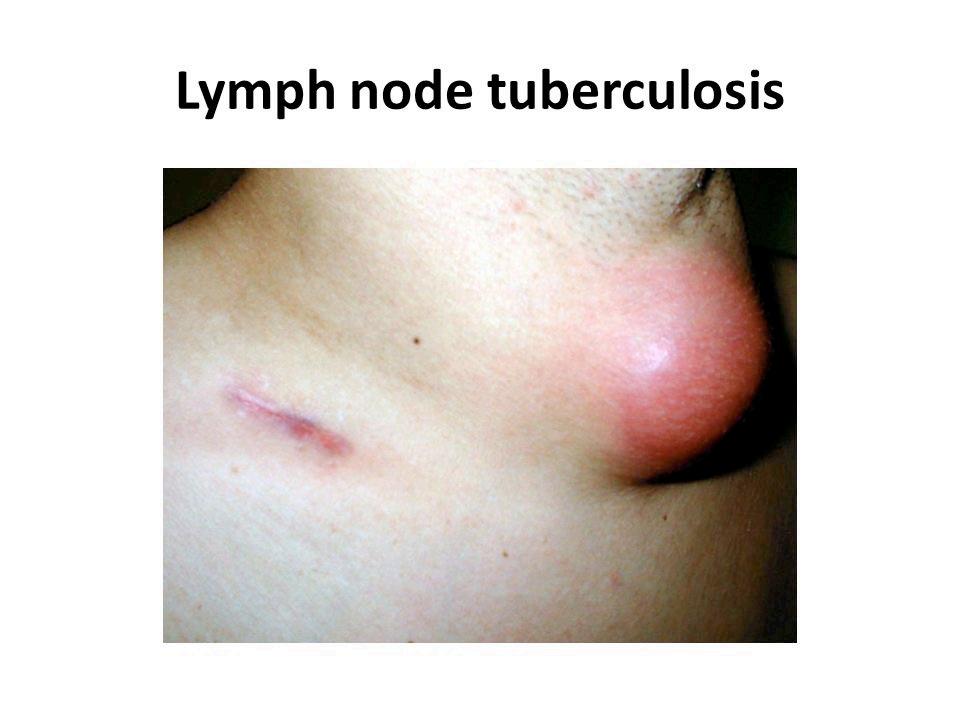
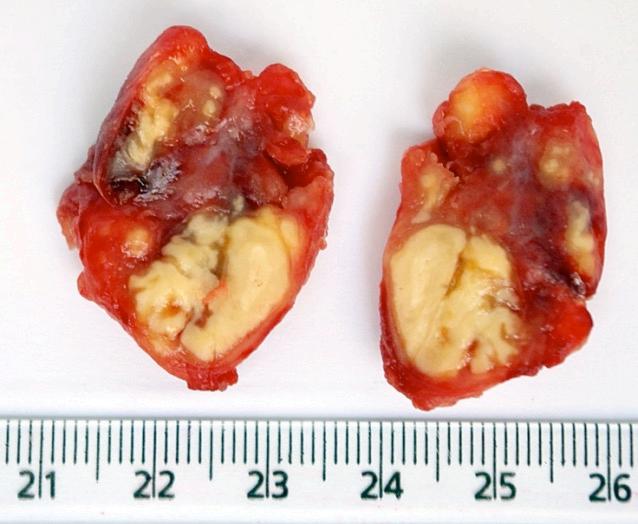
: Limfadenitis Tuberkulosis
D. Faktor inang dan patogen yang memodulasi perjalanan penyakit
- Faktor host: usia ekstrem, malnutrisi, kehamilan, diabetes mellitus (menurunkan imunitas seluler), CKD stadium lanjut (uremia), HIV, konsumsi alkohol/rokok, dan penggunaan obat imunosupresif (steroid jangka panjang, agen biologik, pascatransplantasi) meningkatkan risiko progresi dari laten ke aktif dan meningkatkan risiko EPTB.
- Faktor patogen: variasi virulensi strain, sistem sekretori ESX-1/ESAT-6 yang memengaruhi pematangan fagosom dan permeabilitas membran, serta adaptasi MTB terhadap hipoksia (regulon DosR) mempengaruhi persistensi dan pola kerusakan jaringan.
- Faktor lingkungan: ventilasi, kepadatan hunian, durasi pajanan, dan ketepatan pengobatan memengaruhi penularan serta risiko terbentuknya resistensi.
PEMBAHASAN KASUS
Sel histiosit raksasa (Langhans) terbentuk dari fusi makrofag teraktivasi (dorongan utama: IFN-γ dari sel Th1, dibantu TNF-α), dengan ciri banyak inti di tepi membentuk tapal kuda/lingkar.Menjadi penanda morfologis khas granuloma tuberkulosa bersama sel epitelioid dan nekrosis kaseosa.Berfungsi membantu membatasi kuman TB dalam granuloma, bagian dari hipersensitivitas tipe lambat (DTH) dan imunitas mediasi sel.
PENEGAKAN DIAGNOSIS TUBERKULOSIS

SOAL KASUS
Seorang laki-laki 42 tahun datang ke puskesmas dengan keluhan batuk berdahak sejak 4 minggu, kadang bercak darah. Keluhan disertai demam hilang-timbul terutama sore-malam, keringat malam, nafsu makan menurun, dan penurunan berat badan sekitar 5 kg dalam 2 bulan terakhir. Pasien tinggal di rumah kontrakan padat penghuni (6 orang, ventilasi kurang).
Rekan kerja satu ruang pernah menjalani pengobatan TB 6 bulan lalu.
Riwayat:
• Belum pernah didiagnosis TB, tidak pernah minum OAT sebelumnya.
• Riwayat merokok 10 pack-years, berhenti 2 tahun lalu. Tidak konsumsi alkohol/napza.
• 2 minggu lalu mendapat amoksisilin 5 hari dari klinik, keluhan tidak membaik.
• Tidak ada riwayat terapi steroid/kemoterapi/biologik.
• Riwayat penyakit: tidak pernah HIV diperiksa; ayah dengan diabetes melitus.
• Status imunisasi BCG masa kecil tidak ingat.
Pertanyaan 1 Dari anamnesis, sebutkan minimal 5 faktor yang meningkatkan kecurigaan TB paru pada pasien ini dan jelaskan alasannya singkat.
Pertanyaan 2 Klasifikasikan pasien ini menurut kategori kasus TB yang paling mungkin pada tahap ini (sebutkan istilah yang tepat dan alasannya).
A. Definisi Terduga TBC (Suspek)
Penegakan diagnosis TBC bertujuan menemukan kasus sedini mungkin agar penularan segera diputus dan pasien lekas mendapat terapi yang tepat hingga tuntas. Prinsip umum: deteksi aktif pada kelompok berisiko, skrining gejala, konfirmasi bakteriologis (diutamakan Tes Cepat Molekuler/TCM), serta pencatatan–pelaporan yang tepat waktu.
Setiap orang dengan batuk ≥2 minggu, atau segala bentuk batuk (berdahak/tidak) disertai gejala tambahan seperti penurunan nafsu makan/berat badan, lemah, keringat malam, demam, hemoptisis, atau sesak napas, dikategorikan sebagai terduga TBC dan perlu pemeriksaan dahak.
Kelompok Berisiko Tinggi (Prioritas Skrining)
• Kontak serumah/kontak erat dari kasus TBC (sensitif atau resisten obat).
• Orang dengan HIV, diabetes melitus, perokok, malnutrisi, atau komorbid berat lainnya.
• Bayi, anak, dan lansia yang tinggal/serumah dengan pasien TBC.
• Kelompok khusus: warga binaan pemasyarakatan, pekerja migran, tunawisma, pengungsi, komunitas padat/kumuh.

B. Alur Penegakan Diagnosis
Anamnesis dan Pemeriksaan Fisik: Tanyakan keluhan utama, gejala sistemik, riwayat kontak, pengobatan TBC sebelumnya, penyakit penyerta, dan faktor risiko. Lakukan pemeriksaan fisik menyeluruh; hasilnya menjadi dasar pemilihan penunjang yang tepat.
Pemeriksaan Bakteriologis :Tes Cepat Molekuler (TCM) adalah pemeriksaan utama untuk konfirmasi TBC dan deteksi dini resistensi rifampisin. Gunakan pada TBC paru maupun ekstra-paru, pada semua kelompok umur, termasuk ODHIV. Spesimen: dahak untuk TBC paru; spesimen non-dahak sesuai organ (misal cairan pleura, jaringan kelenjar, LCS) untuk TBC ekstra-paru. Jika akses TCM terkendala, gunakan mikroskopis
BTA sebagai alternatif dan segera rujuk spesimen/pasien ke fasilitas dengan TCM.
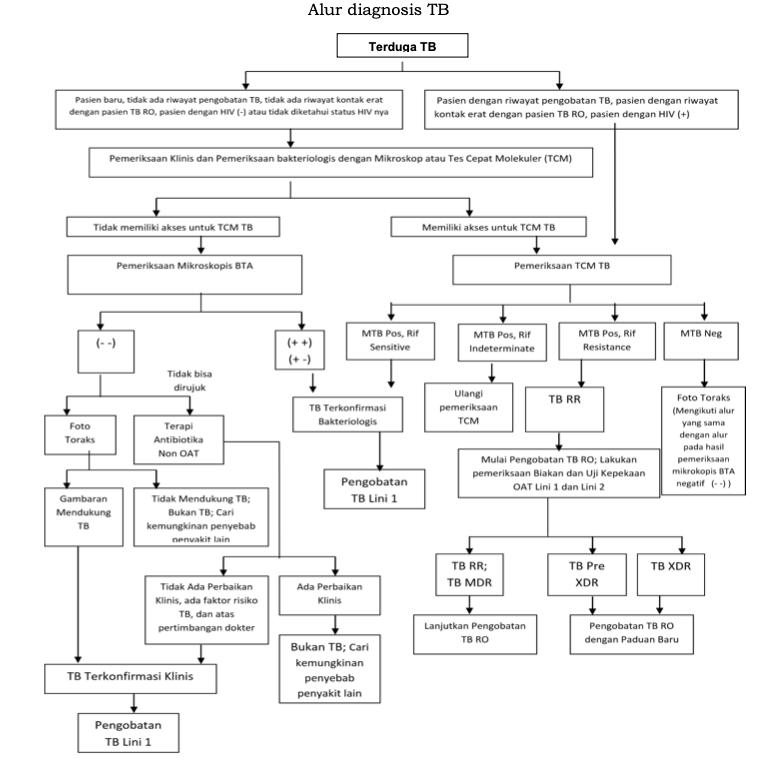
Gambar 10: Alur Penegakan Diagnosis Tuberkulosis (PNPK,2020)
Pengumpulan Spesimen Dahak
Ambil dua spesimen (Sewaktu–Sewaktu / Sewaktu–Pagi / Pagi–Sewaktu) dengan jeda ±1 jam. Pastikan kualitas: 1–4 mL, mukopurulen. Edukasi batuk efektif sebelum pengambilan.
Rujukan Spesimen/Pasien ke Fasyankes TCM
Bila fasilitas tidak memiliki TCM, rujuk segera terduga TBC atau spesimen ke fasyankes TCM terdekat untuk pemeriksaan konfirmasi.
Tabel 1: Ringkasan Algoritma Diagnostik
Populasi Langkah Utama Pemeriksaan Utama Alternatif/Back-up Catatan Penting
Dewasa (≥15 th) Skrining gejala → terduga
Anak (0–14 th) Kriteria gejala anak → rujuk evaluasi
Kontak serumah/erat Skrining gejala via formulir standar
TCM pada 2 spesimen dahak
TCM (spesimen sesuai organ)
TCM untuk kontak bergejala
C. Pemeriksaan Penunjang

Mikroskopis BTA bila TCM tidak tersedia CXR sebagai penunjang
Mikroskopis/penunjang sesuai indikasi
Rujuk ke fasyankes TCM
Pertimbangkan TBC ekstraparu
Edukasi & pengumpulan spesimen
Radiografi toraks (CXR) bermanfaat untuk skrining/penilaian luas penyakit. Pada TBC ekstra-paru, pilih spesimen sesuai organ untuk TCM; pertimbangkan USG/CT/MRI sesuai indikasi klinis.
D. Diagnostik Berbasis Investigasi Kontak (IK)
IK wajib pada seluruh kontak serumah/erat dari kasus indeks TBC terkonfirmasi (sensitif maupun resisten obat). Laksanakan sedini mungkin setelah diagnosis indeks. Skrining gejala sesuai kelompok (dewasa, anak, ODHIV). Kontak bergejala dikategorikan terduga TBC, diedukasi, dan dikumpulkan spesimen (diutamakan TCM).
5. Algoritma Praktis Penegakan Diagnosis
A. Dewasa (≥15 tahun)
1. Identifikasi gejala: batuk ≥2 minggu atau batuk apa pun + gejala sistemik → terduga TBC.

2. Kumpulkan 2 spesimen dahak berkualitas → TCM sebagai pemeriksaan utama.
3. Jika TCM tidak tersedia: mikroskopis/rujuk ke fasyankes TCM.
4. CXR sebagai penunjang sesuai kebutuhan; keputusan utama berbasis bukti bakteriologis.
B. Anak (0–14 tahun)
5. Kecurigaan bila: batuk ≥2 minggu, demam >2 minggu, BB turun/tidak naik 2 bulan, malaise/lesu → evaluasi di fasyankes.
6. Gunakan TCM pada spesimen non- dahak untuk dugaan ekstra-paru; lanjutkan evaluasi klinis-penunjang.
C. Kontak Serumah/Erat
7. Skrining gejala menggunakan formulir standar (dewasa/anak/ODHIV).
8. Jika gejala (+): edukasi, ambil dahak, lakukan TCM/rujuk.
6. Spesimen dan Kualitas
Ambil dua spesimen dahak dengan jeda ±1 jam; volume 1–4 mL, mukopurulen. Edukasi pasien dan dukungan kader dapat meningkatkan keberhasilan pengumpulan dan pengiriman spesimen.
7. Dokumentasi dan Pelaporan
Gunakan formulir standar program TBC (register terduga, permohonan pemeriksaan bakteriologis, register laboratorium, dokumen IK). Pencatatan dan pelaporan dilakukan real-time pada sistem informasi TBC setempat. Adapun pencatatan pasien TB menggunakan Kartu TB 01 dan 02 sebagai berikut


Gambar 11: Kartu Identitas Pasien TB 01 dan 02

PEMBAHASAN KASUS
1. Faktor yang meningkatkan kecurigaan TB paru
• Batuk berdahak ≥4 minggu – sesuai gejala utama terduga TB.
• Dahak bercak darah – khas kerusakan paru pada TB.
• Demam hilang-timbul sore–malam – pola demam infeksi kronik TB.
• Keringat malam + penurunan BB 5 kg & nafsu makan turun – gejala konstitusional TB.
• Kontak erat dengan rekan kerja TB – meningkatkan risiko tertular.
• Tinggal di rumah padat, ventilasi buruk – faktor lingkungan yang mendukung penularan.
• Tidak membaik dengan amoksisilin – infeksi kronik spesifik, curiga TB.
2. Klasifikasi kategori kasus TB
• Kategori: Terduga (suspek) TB paru dewasa
• Alasan: Batuk ≥2 minggu + gejala sistemik dan faktor risiko TB, tetapi belum ada konfirmasi pemeriksaan penunjang.
SOAL KASUS
Seorang laki-laki 32 tahun datang ke puskesmas dengan keluhan batuk berdahak sejak 5 minggu, kadang bercak darah. Keluhan disertai demam hilang–timbul terutama sore dan malam hari, keringat malam, nafsu makan menurun, dan penurunan berat badan ±6 kg dalam 2 bulan terakhir.
Pasien tinggal di rumah kontrakan yang padat penghuni, ventilasi kurang baik. Rekan sekamarnya sedang pengobatan TB paru 3 bulan terakhir. Riwayat pengobatan: 2 minggu lalu pasien mendapat antibiotik (amoksisilin) selama 7 hari dari klinik, namun keluhan tidak membaik. Riwayat HIV belum pernah diperiksa.
Pemeriksaan fisik:
• Keadaan umum cukup, tampak kurus
• Suhu 37,8°C, frekuensi napas 22x/menit
• Pemeriksaan toraks: suara napas vesikuler, sedikit ronki halus di regio apeks paru kanan
• Tidak ditemukan pembesaran kelenjar getah bening perifer
Foto toraks PA: infiltrat heterogen dengan kavitas di apeks paru kanan.
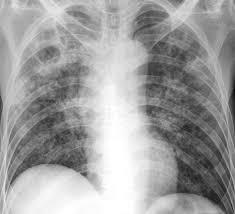
Tindakan pemeriksaan penunjang paling tepat dan utama untuk menegakkan diagnosis
TB paru pada pasien ini adalah:
A. Mengulang foto toraks 2 minggu lagi setelah terapi simptomatik
B. Pemeriksaan dahak untuk Tes Cepat Molekuler (TCM) Xpert MTB/RIF
C. Pemeriksaan IGRA (Interferon-Gamma Release Assay)
D. CT-scan toraks dengan kontras
E. Kultur Mycobacterium tuberculosis dari bronkoalveolar lavage
BAB IV
TATALAKSANA TUBERKULOSIS

SOAL KASUS

VIDEO: Cara Pengobatan Tuberkulosis (TBC)

Buku Panduan Tenaga Medis dan Tenaga Kesehatan Tuberkulosis
Laki-laki 28 tahun, BB 52 kg, keluhan batuk >3 minggu, demam sore hari, keringat malam, penurunan BB. Tidak pernah diobati TB sebelumnya. Riwayat DM, HIV, dan penyakit hati disangkal.
Foto toraks: infiltrat/apikal kanan.
Uji dahak: BTA 2+, Xpert MTB/RIF: MTB detected, RIF-resistance not detected.
Fungsi hati awal dalam batas normal.
Pertanyaan: Regimen tatalaksana farmakologis lini pertama yang paling tepat?
A. 2RHZ/4RHZ
B. 2RHZE/4RH harian (6 bulan)
C. 6HRZE harian
D. 9RH (pencegahan/LTBI)
E. 2RHZE/10HR (regimen EPTB berat)
A. Tujuan dan Prinsip Umum Terapi TB
Tujuan terapi TB adalah menyembuhkan pasien, mencegah kematian dan kekambuhan, memutus rantai penularan komunitas, serta mencegah berkembangnya resistansi obat.
Prinsip PNPK: gunakan paduan standar berbasis bukti; terapi diberikan setiap hari bukan intermiten; konsisten memantau kepatuhan, respons klinis–mikrobiologis, dan efek samping; skrining serta tata laksana komorbid (HIV, diabetes melitus/DM, penyakit ginjal/hati, malnutrisi) sejak awal; dan dokumentasikan hasil terapi dengan terminologi program.
B. Tatalaksana TB Sensitif Obat (Dewasa)
Regimen standar kasus baru (diasumsikan peka OAT): 2 bulan fase intensif RHZE (rifampisin, isoniazid, pirazinamid, etambutol) diikuti 4 bulan fase lanjutan RH. Pada sebagian TB ekstraparu dengan keterlibatan organ kritis atau beban penyakit berat, durasi dapat diperpanjang sesuai penilaian klinis pedoman.






Pemantauan yang dianjurkan:
(1) klinis (gejala respirasi/sistemik, berat badan, status fungsional);
(2) mikrobiologis pada kasus awal BTA/kultur positif (umumnya evaluasi akhir bulan ke-2, ke-5, ke-6);
(3) laboratorium sesuai risiko (fungsi hati/renal, gula darah)
(4) radiologi sesuai indikasi.
Tabel 2: Dosis harian OAT lini pertama (dewasa, acuan mg/kgBB):
Obat Dosis harian (mg/kg) Batas maksimum (mg) Dosis 3×/minggu (mg/kg) Maks 3×/minggu (mg)
Isoniazid (H) 5 (4–6) 300 10 (8–12) 900 Rifampisin (R) 10 (8–12) 600 10 (8–12) 600 Pirazinamid (Z) 25 (20–30) - 35 (30–40) -
Etambutol (E) 15 (15–20) - 30 (25–35) -
Catatan praktis: gunakan kombinasi dosis tetap (KDT/FDC) bila tersedia untuk menyederhanakan rejimen dan menurunkan risiko kesalahan. Berikan piridoksin 25–50 mg/hari pada pasien berisiko neuropati (malnutrisi, DM, HIV, hamil/menyusui, alkoholik, usia lanjut). Streptomisin umumnya dihindari pada program kasus baru; riziko ototoksik tinggi dan kontraindikasi pada kehamilan.
Dosis pemberian OAT KDT pada pasien TBC dewasa
Tabel 3: Kombinasi Dosis Tetap OAT (Kemenkes,2025)
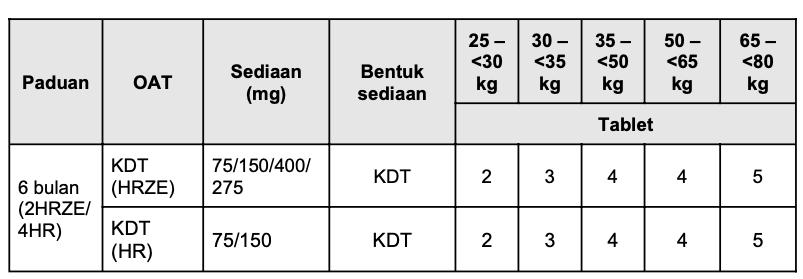

B.1 Penatalaksanaan Efek Samping Utama
Efek samping OAT seringkali dapat dikelola tanpa menghentikan semua obat. Kunci keberhasilan adalah deteksi dini, klasifikasi ringan–berat, dan pendekatan bertahap (simptomatik, substitusi, atau henti–reintroduksi). Berikut ringkasan beberapa ESO penting:
• Hepatotoksisitas (H, R, Z): curigai jika ada ikterus, mual muntah berat, nyeri perut kanan atas; evaluasi SGOT/SGPT dan bilirubin. Hentikan OAT bila SGOT/SGPT >3× nilai
normal dengan gejala, atau >5× tanpa gejala; tata laksana suportif. Setelah pulih, lakukan re-introduksi bertahap: mulai dengan obat paling penting dan relatif minim hepatotoksisitas (mis. R), kemudian H; Z dipertimbangkan terakhir atau diganti bila perlu.
• Ruam kulit: ringan–sedang dapat ditangani dengan antihistamin/topikal; ruam hebat/anafilaksis memerlukan penghentian sementara seluruh OAT dan evaluasi bertahap penyebabnya.
• Gangguan penglihatan (E): lakukan edukasi uji buta warna dan keluhan penglihatan; bila dicurigai neuritis optik, hentikan E dan rujuk ke mata.
• Hiperurisemia/nyeri sendi (Z): biasanya ringan; berikan analgesik, hidrasi; nilai ulang bila gout berat.
• Sindrom flu, trombositopenia (R): jarang namun serius; pada trombositopenia, hentikan R dan jangan diberikan kembali.
B.2 Definisi Respon dan Kegagalan Terapi
Respon baik: perbaikan gejala, kenaikan berat badan, konversi BTA/kultur pada jadwal yang diharapkan, dan perbaikan radiologis bertahap. Kegagalan dicurigai bila BTA/kultur tetap positif berkepanjangan atau re-positif setelah konversi, atau terjadi progres klinis meski kepatuhan baik. Langkah: evaluasi ulang kepatuhan, interaksi obat, komorbid, lakukan pemeriksaan uji kepekaan (TCM/LPA/kultur DST), dan pertimbangkan rujukan.
C. Tatalaksana TB Ekstraparu (EPTB)
Secara umum, paduan lini pertama sama (2RHZE/4RH). Namun beberapa lokasi organ memerlukan durasi lebih panjang dan/atau adjuvan kortikosteroid, serta intervensi bedah bila terjadi komplikasi. Prinsip utama adalah memastikan diagnosis dan menilai derajat keparahan, kemudian memulai OAT sedini mungkin.

C.1 TB Kelenjar Getah Bening
Regimen standar 6 bulan seringkali cukup. Aspirasi/biopsi diperlukan untuk diagnosis; drainase dilakukan pada abses fluktuatif atau fistula. Pembesaran KGB dapat menetap beberapa bulan meski terapi adekuat; evaluasi klinis keseluruhan lebih penting daripada ukuran tunggal kelenjar.
C.2 TB Pleura
Berikan 2RHZE/4RH. Pada efusi besar/dispnea berat, torasentesis terapeutik bermanfaat.
Kortikosteroid dapat dipertimbangkan pada efusi simtomatik tertentu berdasarkan penilaian klinis, namun tidak rutin untuk semua. Pada empiema, drainase dan tata laksana bedah dapat diperlukan.
C.3 TB Sistem Saraf Pusat (Meningitis/Tuberkuloma)
Meningitis TB adalah emergensi. Mulai OAT segera setelah kecurigaan kuat. Regimen umumnya lebih panjang (mis. 12 bulan: 2HRZ±E/S + 10HR). Kortikosteroid (prednison) direkomendasikan 4 minggu kemudian tap-off bertahap pada meningitis TB dan perikarditis TB. Kelola komplikasi (hidrosefalus shunting; kejang antiepileptik; hiponatremia) secara agresif.
C.4 TB Tulang/Sendi (termasuk Spondilitis)
Regimen berkisar 9–12 bulan sesuai berat penyakit. Imobilisasi relatif pada fase nyeri akut; fisioterapi bertahap. Indikasi bedah: defisit neurologis progresif, ketidakstabilan tulang belakang, abses besar yang tak responsif terhadap drainase konservatif.
C.5 TB Abdomen/Peritoneum
OAT lini pertama 6–9 bulan; lakukan drainase bila ada abses intraabdominal; laparoskopi diagnostik/terapeutik dipertimbangkan pada kasus tertentu.
C.6 TB Genitourinarius dan Kulit
Regimen 6 bulan umumnya cukup; pada striktur ureter atau obstruksi, intervensi urologi mungkin diperlukan. TB kulit memerlukan konfirmasi histopatologi/kultur dan OAT standar.
D. Tatalaksana TB pada Anak
Prinsip: segera memulai terapi bila diagnosis klinis/konfirmasi kuat; gunakan sediaan anak yang mudah ditelan (dispersible/larut), sesuaikan dosis terhadap berat badan dan

perbarui dosis sejalan kenaikan BB; optimalkan nutrisi dan imunisasi; edukasi keluarga dan PMO.
Contoh paduan dan durasi (ringkas): TB paru BTA( ) atau TB kelenjar: 2HRZ + 4HR; TB paru BTA(+): 2HRZE + 4HR; TB berat (miliar/kerusakan luas): 2HRZE + 7–10HR; meningitis/perikarditis/peritonitis/skeletal: 2HRZ(±E/S) + 10HR dengan kortikosteroid pada meningitis/perikarditis. Pemantauan anak lebih sering pada fase intensif (tiap 2 minggu) kemudian tiap bulan pada fase lanjutan.
Efek samping pada anak umumnya ringan; perhatikan hepatotoksisitas (terutama Z), gangguan visual (E), serta neuropati perifer (H beri piridoksin profilaksis). Kombinasi tetap anak (KDT) mempermudah pemberian dan mengurangi kesalahan dosis.
E. Koinfeksi TB–HIV
Prinsip: OAT diberikan seperti biasa (harian), dan antiretroviral (ART) dimulai sedini mungkin setelah OAT ditoleransi umumnya dalam 2–8 minggu; bila CD4 <50 sel/µL, mulai ART dalam 2 minggu pertama untuk menurunkan mortalitas. Lakukan profilaksis kotrimoksazol pada semua ODHA dengan TB. Waspadai sindrom pemulihan imun (IRIS) pada beberapa minggu pertama setelah ART dimulai; tata laksana suportif dan OAT jangan dihentikan.
Interaksi obat: rifampisin menginduksi enzim sitokrom P450 sehingga menurunkan kadar beberapa ARV dan obat komorbid lain. Koordinasi regimen ART diperlukan (mis. pilihan berbasis efavirenz atau penyesuaian pada rejimen lain); evaluasi fungsi hati lebih sering.

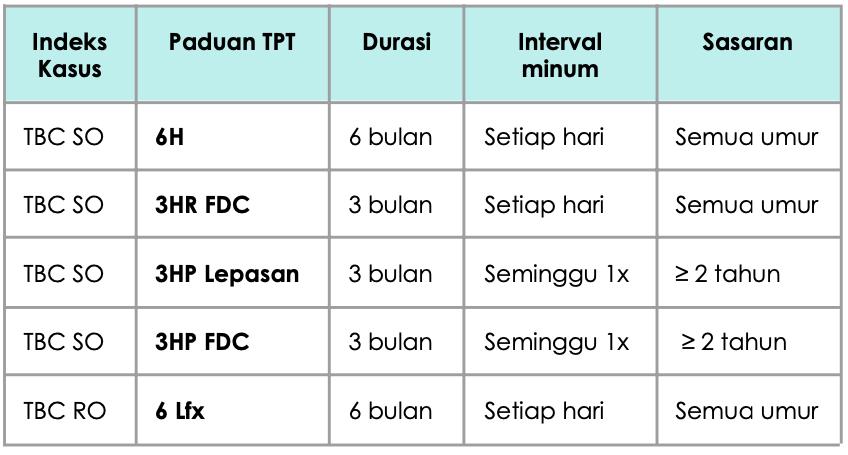
F. Terapi Pencegahan TB (TPT)
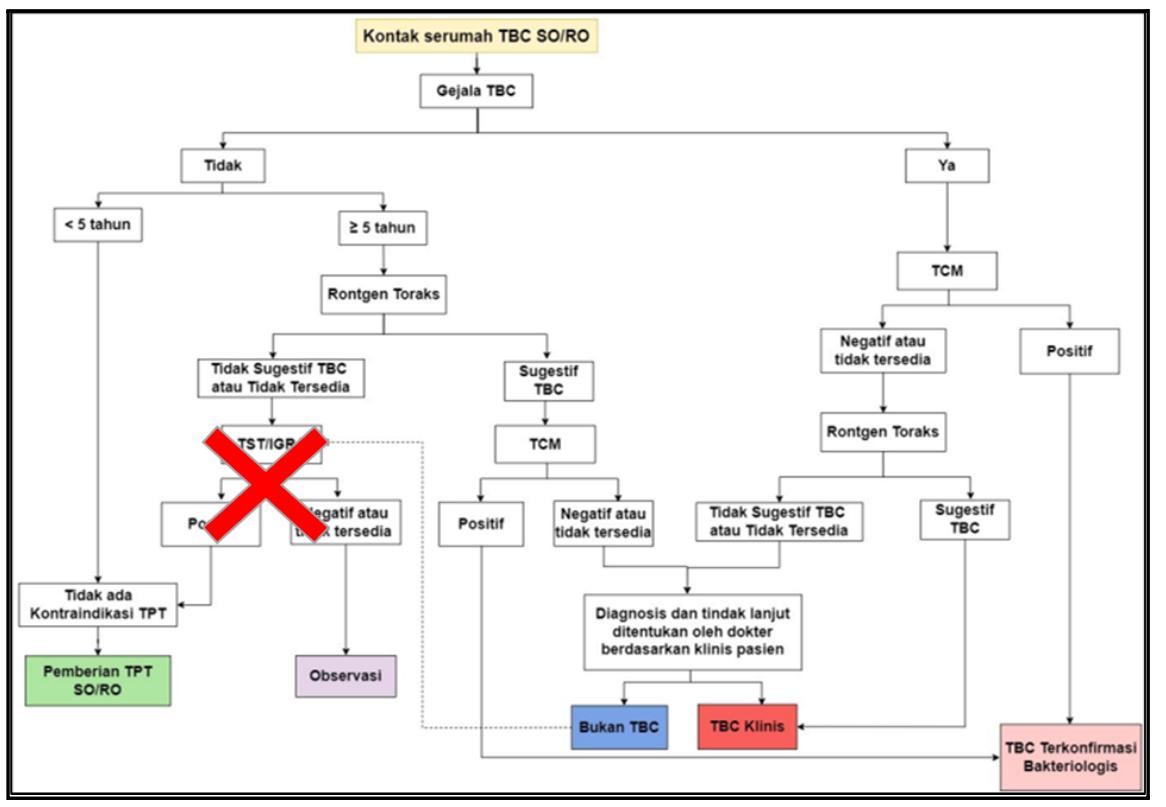
Gambar 12 Alur Pemberian TPT pada Kontak Serumah (Kemenkes,2025)
TPT ditujukan bagi individu berisiko tinggi tanpa TB aktif: kontak erat rumah tangga (terutama anak <5 tahun), ODHA, dan kelompok risiko lain sesuai program. Sebelum
TPT, pastikan tidak ada TB aktif melalui skrining gejala, pemeriksaan fisik, dan bila perlu radiologi/TCM. Rejimen yang lazim: isoniazid 6 bulan (INH 300 mg/hari + piridoksin 25 mg/hari pada dewasa), atau alternatif regimen berbasis rifapentin-isoniazid mingguan (3HP) pada usia yang memenuhi kriteria. Edukasi kepatuhan dan monitoring ESO ringan (mis. nyeri perut, ruam) tetap diperlukan.
Tabel 4: Panduan Terapi Pencegahan Tuberkulosis (Kemenkes,2025)

G. Tatalaksana TB Resistan Obat (TB- RO)
TB-RO mencakup TB resistan rifampisin (RR-TB), MDR-TB (resistan minimal H dan R), dan kategori lanjutan (pre-XDR/XDR) tergantung pola resistansi tambahan. Penegakan profil resistansi menggunakan TCM (deteksi RIF-resistan), LPA lini pertama/kedua (INH, fluorokuinolon, obat injeksi), dan uji kepekaan fenotipik. Tujuan terapi adalah menyembuhkan dengan regimen efektif, meminimalkan toksisitas, dan mencegah penularan/resistansi lebih lanjut.
G.1. Paduan Standar Jangka Pendek (±9–11 bulan)
Umumnya terdiri dari fase awal 4–6 bulan (dapat diperpanjang jika belum konversi pada bulan ke-4) yang mencakup obat injeksi (mis. kanamisin/kapreomisin) ditambah fluoroquinolone dosis penuh (moksifloksasin), clofazimine, isoniazid dosis tinggi, etambutol, pirazinamid, serta etionamid/protionamid; diikuti fase lanjutan 5 bulan: moksifloksasin + clofazimine + etambutol + pirazinamid. Pemilihan regimen mengikuti kriteria inklusi/eksklusi PNPK.
G.2. Paduan Individual (±18–20 bulan)
Pada kasus yang tidak memenuhi kriteria regimen pendek atau memiliki resistansi kompleks/ESO berat, gunakan paduan individual berbasis uji kepekaan. Pengelompokan obat (ilustratif): Kelompok A (levofloxacin/moxifloxacin; bedaquiline; linezolid), Kelompok B (clofazimine; cycloserine/terizidone), Kelompok C (ethambutol; delamanid; pirazinamid; imipenem-cilastatin/meropenem + klavulanat; amikasin/streptomisin; ethionamide/protionamide; PAS). Mulailah dengan ≥5 obat efektif pada fase awal (termasuk 3 dari kelompok A bila mungkin) lalu pertahankan ≥3 obat efektif setelah bedaquiline dihentikan. Durasi total umumnya 18–20 bulan, dengan evaluasi ketat konversi kultur dan efek samping.
G.3. Isu Keamanan dan Pemantauan TB-RO
• Bedaquiline: risiko pemanjangan QTc monitor EKG berkala, koreksi elektrolit, hindari kombinasi QT-prolonging lain bila tidak perlu.
• Linezolid: neuropati perifer/optik dan mielosupresi monitor darah lengkap; pertimbangkan penyesuaian dosis bila terapi jangka panjang.

• Aminoglikosida (amikasin/kanamisin): nefro- dan ototoksik monitor fungsi ginjal dan audiometri; hindari pada kehamilan.
• Clofazimine: kulit kemerahan/hiperpigmentasi edukasi pasien; perhatikan interaksi.
H. Populasi Khusus dan Komorbid
H.1 Kehamilan dan Menyusui
OAT lini pertama (H, R, Z, E) umumnya aman pada kehamilan; streptomisin/aminoglikosida kontraindikasi (ototoksik janin). Berikan piridoksin rutin.
Rifampisin menurunkan efektivitas kontrasepsi oral kombinasi anjurkan metode alternatif. Menyusui tidak perlu dihentikan; edukasi higiene batuk, masker, dan TPT bayi sesuai kebijakan.
H.2 Diabetes Melitus (DM)
Kontrol glikemik ketat meningkatkan hasil terapi; perhatikan interaksi rifampisin (induktor enzim) dengan obat hipoglikemik. Risiko neuropati meningkat beri piridoksin; pantau infeksi sekunder, dan lakukan edukasi nutrisi serta aktivitas fisik.
H.3 Penyakit Hati Kronik/DILI
Pertimbangkan regimen tanpa Z pada penyakit hati berat, atau pemantauan enzim hati yang lebih sering. Pada DILI, hentikan OAT sesuai kriteria, tata laksana suportif, kemudian re-introduksi bertahap (mis. R → tambah H; evaluasi kebutuhan Z).
H.4 Penyakit Ginjal Kronik/Hemodialisis
Sesuaikan dosis dan interval obat yang diekskresikan ginjal (E, Z, streptomisin/amikasin). Berikan setelah hemodialisis pada hari tindakan. Monitor ketat fungsi ginjal dan penglihatan (E).
Tabel 5: Panduan Terapi Pada Gagal Ginjal Kronis
Obat GGK St. 1–3 GGK St. 4–5 / Hemodialisis Catatan
piridoksin
Rifampisin

450 mg (<50 kg) / 600 mg (≥50 kg) qd
Dosis sama Tidak perlu penyesuaian bermakna
Pirazinamid 1,5–2 g qd (berdasar BB) 25–35 mg/kg 3×/mg Berikan setelah HD
Etambutol 15 mg/kg qd 15–25 mg/kg
3×/mg (maks 2,5 g)
Streptomisin/Amikasin Hindari bila mungkin
2–3×/mg dengan pemantauan kadar
I. Pengendalian Infeksi dan Dukungan Kepatuhan
Pantau tajam penglihatan
Ototoksik/nefrotoksik
Pengendalian infeksi: etika batuk, ventilasi baik, sinar matahari, dan penggunaan APD pada prosedur aerosol; gunakan ruang tekanan negatif bila tersedia. Isolasi relatif pada fase sangat menular hingga konversi. Edukasi pasien/keluarga mengenai etika batuk, kebersihan tangan, dan pentingnya menyelesaikan terapi.
Dukungan kepatuhan: tetapkan Pengawas Menelan Obat (PMO) dan jadwal minum obat harian; manfaatkan pengingat digital/SMS/telemedicine; sediakan konseling dan pemecahan masalah (problem-solving) bila ada efek samping atau hambatan sosial. Lakukan telusur kontak serumah dan berikan TPT sesuai kriteria.
J. Pemantauan, Rujuk Balik, dan Hasil Akhir Terapi
Jadwal kontrol: lebih sering pada fase intensif (mis. setiap 2–4 minggu) kemudian tiap bulan pada fase lanjutan. Parameter: gejala, berat badan, kepatuhan, ESO, hasil mikroskopis/kultur sesuai kategori awal, dan radiologi bila diindikasikan. Rujuk balik dari RS ke puskesmas dilaksanakan setelah kondisi stabil dengan rencana pemantauan jelas dan komunikasi dua arah.
Terminologi keluaran pengobatan program: sembuh (uji mikrobiologi akhir negatif sesuai kriteria), pengobatan selesai (tanpa bukti mikrobiologi akhir namun secara klinis menyelesaikan regimen), gagal (tidak mencapai konversi/persisten positif atau memburuk), putus berobat (interupsi ≥2 bulan), pindah (transfer out), dan meninggal. Dokumentasi harus lengkap untuk keperluan pelaporan dan evaluasi program.

PEMBAHASAN KASUS
Kunci Jawaban: B. 2RHZE/4RH harian (6 bulan)
Alasan Singkat
• Pasien kasus baru TB paru dengan uji cepat menunjukkan sensitif rifampisin dan tanpa komorbid khusus → tatalaksana standar regimen 6 bulan: fase intensif 2 bulan RHZE dilanjutkan fase lanjutan 4 bulan RH.
• Tidak ada indikasi regimen EPTB berat (meningitis tulang/sendi) atau resistensi obat.
SOAL KASUS
Seorang laki-laki 45 tahun, BB 60 kg, datang ke Puskesmas dengan keluhan batuk berdahak >1 bulan, kadang bercak darah, demam hilang-timbul sore-malam, keringat malam, dan penurunan BB 7 kg dalam 3 bulan.
Foto toraks menunjukkan infiltrat di lapang atas paru kanan. Pemeriksaan TCM sputum: MTB terdeteksi, sensitif rifampisin (TBC SO). Riwayat OAT: belum pernah minum OAT sebelumnya. Tidak ada komorbid (DM, HIV, CKD, dsb).
Pasien diklasifikasikan sebagai TB paru sensitif obat, pasien baru. Di Puskesmas tersedia OAT kombinasi dosis tetap (KDT) dewasa sesuai program nasional.
Tentukan regimen terapi TB lengkap beserta dosis OAT per hari yang paling tepat untuk pasien ini sesuai pedoman Kemenkes (berdasarkan BB pasien 60 kg).
SOAL KASUS
Seorang laki-laki 40 tahun, BB 55 kg, didiagnosis TB paru sensitif obat, pasien baru. Ia memulai pengobatan dengan regimen program 2HRZE/4HR (KDT dewasa) di puskesmas. Setelah 2 bulan terapi (fase intensif) pasien kontrol ke puskesmas. Ia mengatakan batuk sudah jauh berkurang, tidak ada demam, dan berat badan mulai naik. Pasien mengaku minum obat setiap hari, hanya sesekali lupa 1–2 kali dalam sebulan.
Sebagai dokter muda yang bertugas di puskesmas, Anda diminta untuk melakukan evaluasi follow up pengobatan TB pada kunjungan akhir fase intensif ini.
Pertanyaan:
Tindakan pemeriksaan follow up yang PALING TEPAT dan WAJIB dilakukan pada kunjungan ini untuk menilai keberhasilan pengobatan TB adalah:
A. Hanya menilai perbaikan gejala klinis (batuk, demam, nafsu makan)
B. Mengulang foto toraks dan bila membaik terapi langsung dilanjutkan tanpa pemeriksaan lain
C. Pemeriksaan dahak (BTA mikroskopis) untuk evaluasi akhir fase intensif, disertai penilaian klinis
D. Hanya menimbang berat badan dan memastikan kepatuhan minum obat
E. Melakukan kultur sputum rutin pada semua pasien TB paru pada bulan ke-2

DAFTAR PUSTAKA
1. Kementerian Kesehatan Republik Indonesia. Pedoman Nasional Pelayanan Kedokteran: Tata Laksana Tuberkulosis. Jakarta: Kemenkes RI; [tahun dokumen].
2. World Health Organization. Global tuberculosis report 2024. Geneva: WHO; 2024.
3. World Health Organization. WHO consolidated guidelines on tuberculosis. Module 3: Diagnosis Rapid diagnostics for tuberculosis detection. Geneva: WHO; 2021 (and updates).
4. World Health Organization. WHO operational handbook on tuberculosis. Module 3: Diagnosis Rapid diagnostics for tuberculosis detection. Geneva: WHO; 2021 (and updates).
5. World Health Organization. WHO consolidated guidelines on tuberculosis. Module 4: Treatment Drug-susceptible tuberculosis treatment. Geneva: WHO; 2022 (updated 2023).
6. World Health Organization. WHO operational handbook on tuberculosis. Module 4: Treatment Drug-susceptible tuberculosis treatment. Geneva: WHO; 2022 (updated 2023).
7. World Health Organization. WHO consolidated guidelines on tuberculosis. Module 4: Treatment Drug-resistant tuberculosis treatment. Geneva: WHO; 2020 (updated 2022).
8. World Health Organization. WHO operational handbook on tuberculosis. Module 4: Treatment Drug-resistant tuberculosis treatment. Geneva: WHO; 2020 (updated 2022).
9. World Health Organization. WHO consolidated guidelines on tuberculosis. Module 1: Prevention Tuberculosis preventive treatment. Geneva: WHO; 2020 (updated 2023).
10. World Health Organization. WHO operational handbook on tuberculosis. Module 1: Prevention Tuberculosis preventive treatment. Geneva: WHO; 2020 (updated 2023).
11. World Health Organization. WHO consolidated guidelines on tuberculosis. Module 5: Management of tuberculosis in children and adolescents. Geneva: WHO; 2022 (updated 2023).
12. World Health Organization. WHO operational handbook on tuberculosis. Module 5: Management of tuberculosis in children and adolescents. Geneva: WHO; 2022 (updated 2023).

13. World Health Organization. Guidelines for treatment of drug-susceptible tuberculosis and patient care, 2017 update TB/HIV considerations. Geneva: WHO; 2017 (with subsequent updates).
14. World Health Organization. Policy on collaborative TB/HIV activities: guidelines for national programmes and other stakeholders. Geneva: WHO; 2012 (and updates).
15. Boehme CC, Nabeta P, Hillemann D, Nicol MP, Shenai S, Krapp F, et al. Rapid molecular detection of tuberculosis and rifampin resistance. N Engl J Med. 2010;363(11):1005– 1015.
16. Dorman SE, Schumacher SG, Alland D, Nabeta P, Armstrong DT, King B, et al. Xpert MTB/RIF Ultra for detection of Mycobacterium tuberculosis and rifampicin resistance: A prospective multicentre diagnostic accuracy study. Lancet Infect Dis. 2018;18(1):76–84.
17. Hillemann D, Rüsch-Gerdes S, Richter E. Evaluation of the GenoType MTBDRplus assay for rifampicin and isoniazid susceptibility testing of Mycobacterium tuberculosis strains and clinical specimens. J Clin Microbiol. 2007;45(8):2635–2640.
18. Miotto P, Piana F, Cirillo DM, Migliori GB. Genotype MTBDRsl performance on detection of resistance to second-line drugs: a systematic review. Int J Tuberc Lung Dis. 2012;16(3):319– 325.
19. International Union Against Tuberculosis and Lung Disease (The Union). Technical guide: Sputum examination for tuberculosis by direct microscopy in low income countries. 5th ed. Paris: The Union; 2013.
20. Kent PT, Kubica GP. Public health mycobacteriology: A guide for the level III laboratory. Atlanta: US Department of Health and Human Services, CDC; 1985.
21. Tostmann A, Boeree MJ, Aarnoutse RE, de Lange WC, van der Ven AJ, Dekhuijzen R. Antituberculosis drug-induced hepatotoxicity: Concise up-to-date review. J Gastroenterol Hepatol. 2008;23(2):192–202.
22. Saukkonen JJ, Cohn DL, Jasmer RM, Schenker S, Jereb JA, Nolan CM, et al. An official ATS statement: hepatotoxicity of antituberculosis therapy. Am J Respir Crit Care Med. 2006;174(8):935–952.
23. Sterling TR, Njie G, Zenner D, Cohn DL, Reves R, Ahmed A, et al. Guidelines for the treatment of latent tuberculosis infection: 2020 update of the CDC and the National Tuberculosis Controllers Association. MMWR Recomm Rep. 2020;69(RR-1):1–11.
24. World Health Organization. Rapid advice: treatment of tuberculosis in children. Geneva: WHO; 2010 (superseded by Module 5 updates).

25. World Health Organization. Definitions and reporting framework for tuberculosis 2013 revision (updated 2014, 2020). Geneva: WHO; 2013.
26. Kementerian Kesehatan Republik Indonesia. Profil Kesehatan Indonesia 2023. Jakarta: Kemenkes RI; 2024.
27. World Health Organization. WHO guidelines on tuberculosis infection prevention and control, 2019 update. Geneva: WHO; 2019.
28. World Health Organization and The Union. Collaborative framework for care and control of tuberculosis and diabetes. Geneva: WHO; 2011.
29. World Health Organization. WHO consolidated guidelines on tuberculosis: module 4 treatment of drug- resistant TB: update on critical drug safety and monitoring. Geneva: WHO; 2022.
MEDIA PEMBELAJARAN TUBERKULOSIS









WHO Videos about Tuberculosis
https://www.youtube.com/watc h?v=WiQmLO -Fk-U&t=2s
