NÜTZLICHES NEUES FEATURE:
DAS BERATUNGSKENNWORT FÜR
MEHR SICHERHEIT UND SERVICE
VERTRETUNGSFALL IN DER HZV:
SO GEHT ES RICHTIG
PHARMAKOTHERAPIE-THEMA

NÜTZLICHES NEUES FEATURE:
DAS BERATUNGSKENNWORT FÜR
MEHR SICHERHEIT UND SERVICE
VERTRETUNGSFALL IN DER HZV:
SO GEHT ES RICHTIG
PHARMAKOTHERAPIE-THEMA

1 3
NÜTZLICHES
Das Beratungskennwort für mehr Sicherheit und Service
VERTRETUNGSFALL IN DER HZV
So geht es richtig
5 FORTBILDUNG
Chronische Niereninsuffizienz (DMP Diabetes)
INFORMATIONEN UND SCHULUNGEN ZUR HZV VOR ORT UND ONLINE
• Individuelle Praxisschulungen
• Infoveranstaltungen für Hausärztinnen und Hausärzte sowie MFA
• Zahlreiche unterschiedliche Online-Schulungen zur erfolgreichen Umsetzung der HZV im Praxisalltag
Schnell, einfach und unkompliziert: Jetzt online und sofort Mitglied im Hausärzteverband werden und zeitgleich die Teilnahme an den HZV-Verträgen beantragen: www.hausarztservice-online.de
Für Ihre Praxis sowie Ihre Patientinnen und Patienten: Wir bieten Ihnen Info- und Werbematerialien wie z. B. Filme für Ihr Wartezimmer, Printmaterialien und verschiedene Give-aways: www.hzv.de


Viele Hausärztinnen und Hausärzte haben in der letzten Zeit Post vom HÄVG Rechenzentrum bekommen. Der Inhalt: das so genannte Beratungskennwort. Wofür dieses neue Passwort nützlich ist und wie es sich von anderen, bereits vorhandenen Kennwörtern unterscheidet, darüber klären wir hier auf.
Neues Kennwort für noch mehr Service
Das persönliche Beratungskennwort haben in den letzten Wochen die Hausärztinnen und Hausärzte bekommen, die aktuell an mindestens einem Vertrag zur Hausarztzentrierten Versorgung (HZV) teilnehmen oder in den letzten 24 Monaten teilgenommen haben. Das Kennwort ist wichtig bei Auskünften, die personenbezogene Daten betreffen und wird seit Anfang Februar abgefragt. Es
ist nicht zu verwechseln mit dem Passwort für das Arztportal.
Grund für die Einführung des Beratungskennwortes ist eine stetige Erhöhung der Datenschutzstandards, wenn es um Personen- oder Gesundheitsdaten geht. Bei dem zugesandten Beratungskennwort handelt es sich um das Masterkennwort für die an der Hausarztzentrierten Versorgung teilnehmende Hausärztin oder den Hausarzt. Hiermit können alle Auskünfte erteilt werden.

Aber das Kennwort kann noch viel mehr, zumindest für die Nutzerinnen und Nutzer des Arztportals. Sie können dort nämlich so genannte Multikennwörter vergeben, die dann beispielsweise von den Medizinischen Fachangestellten (MFA) der Praxis genutzt werden können, um Auskünfte einzuholen. Es kann aber beispielsweise auch sinnvoll sein, dem eigenen Steuerberater ein Multikennwort zu geben, damit dieser für ihn wichtige Informationen beim Kundenservice der HÄVG erhalten kann. Jedem erstellten Multikennwort kann die Hausärztin oder der Hausarzt eine Bezugsperson oder eine Personengruppe und eine individuelle Freigabestufe zuweisen. Unterschieden wird dabei zwischen einem hohen Auskunftsgrad (Freigabestufe 1) und einem niedrigen Auskunftsgrad (Freigabestufe 2). Bei diesem werden Auskünfte zu Patienten- und Gesundheitsdaten gegeben, bei Freigabestu-
fe 1 erhält der Nachfragende zusätzlich auch Auskünfte über Honorar- und Geschäftsdaten, sowie über die Mitgliedschaft der Ärztin / des Arztes in seinem Hausärzteverband.
Kein Problem bei Verlust
Geht das Beratungskennwort verloren, hat die Nutzerin oder der Nutzer zwei Möglichkeiten, an ein neues Masterkennwort zu kommen. Es kann entweder telefonisch oder schriftlich beim Kundenservice der HÄVG angefordert werden. Die Erzeugung des neuen Beratungskennwortes erfolgt dann per Zufallsgenerator. Dieses wird anschließend per Post an die im System der HÄVG hinterlegte Anschrift versendet. Auch hier sind die Nutzer des Arztportals im Vorteil: Sie können im Arztportal nicht nur jederzeit das hinterlegte Beratungskennwort einsehen, sondern es auch auf Wunsch ändern. Anders als bei den Nutzerinnen und Nutzern, die auf den Postweg angewiesen sind, ist hier das geänderte Kennwort sofort sichtbar und kann umgehend genutzt werden.
Passwort für das Arztportal Völlig unabhängig vom Beratungskennwort haben die Nutzerinnen und Nutzer des Arztportals ein Passwort, mit dem sie Zugang dazu erhalten.
Neben den Vorteilen in Bezug auf das neue Beratungskennwort haben sie weitere Vorteile: Sie haben hier ihr elektronisches Postfach sowie eine Übersicht ihrer gesamten HZV-Verträge, sie können Dokumente und Statistiken zu ihren HZV-Verträgen einsehen, Zusatzverträge wie beispielsweise ITV oder arriba beantragen. Auch ihre Stammund Kontaktdaten können sie an dieser Stelle selbständig verwalten und auf dem neusten Stand halten.
Hausärztinnen und Hausärzte, die noch keinen Zugang zum Arztportal haben, können diesen leicht erlangen, indem sie sich unkompliziert unter arztportal.hausaerzteverband.de registrieren.
Die HÄVG-ID ist kein Kenn- oder Passwort, es ist vielmehr die persönliche Identifizie-
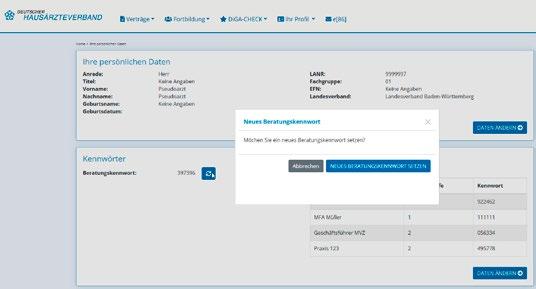
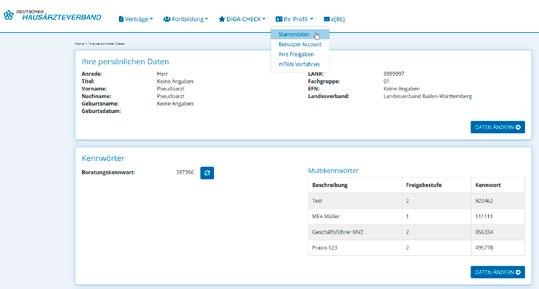
Ansicht der Profilseite im Arztportal
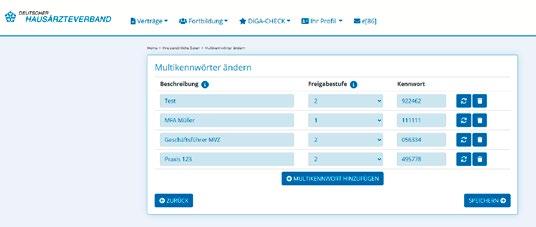
1. Beratungskennwort (Masterkennwort des Arztes. Hiermit können alle Auskünfte erteilt werden).
2. Multikennwörter (Bezugsperson und Freigabestufe kann der Arzt selbst und ausschließlich im Arztportal festlegen. Ein Multikennwort wird generiert, aber kann auch geändert werden).
3. Über das „i“ werden die Details zu den beiden Berechtigungsstufen angezeigt. (Also welche Daten, mit welcher Freigabestufe abgefragt werden können).
4. Über kann das Beratungskennwort neu generiert werden.
5. Über kann ein Multikennwort neu generiert werden.
HINWEIS: Nach allen obigen Änderungen oder neuen Generierungen muss gespeichert werden.
So vergeben Sie Multikennwörter im Arztportal
rungsnummer jeder Hausärztin oder jedes Hausarztes im System der Hausärztlichen Vertragsgemeinschaft (HÄVG). Sie gilt es, bei jedem Kontakt mit dem Kundenservice der HÄVG bereitzuhalten, da sie der ersten Identifizierung dient. Mit dieser Nummer allein kann jedoch kein Zugriff auf Personen- und Gesundheitsdaten erfolgen. Lediglich allgemeine Fragen zu den HZV-Verträgen werden damit vom Kundenservice der HÄVG beantwortet.
Noch keinen Zugang zum Arztportal?
Informationen zur Registrierung und Nutzung des Arztportals finden Sie
unter: www.hausaerzteverband.de/ arztportal
In der Hausarztzentrierten Versorgung (HZV) findet eine arztbezogene Patienteneinschreibung statt, d.h. die Patientin oder der Patient hat sich für die Hausärztin oder den Hausarzt seines Vertrauens entschieden und „bindet“ sich durch seine Teilnahme an diesen. Sollte die so genannte Betreuärztin oder der Betreuarzt nicht verfügbar sein, gibt es grundsätzlich zwei Möglichkeiten, wie ein Vertretungsfall ablaufen kann.
Um zu verstehen, wann in der HZV die Vertreterpauschale abrechenbar ist, muss man zunächst unterscheiden, ob es sich wirklich um eine Vertretung im klassischen Sinne handelt oder um eine so genannte Stellvertretung. Sprachlich nur ein kleiner Unterschied, ist dieser im Vertretungsfall aber von fundamentaler Bedeutung.
Von einer Vertretung spricht man in der Hausarztzentrierten Versorgung in dem Fall, wenn die ursprünglich gewählte Betreuärztin oder der Betreuarzt nicht verfügbar ist und
der Patient eine HZV-Vertretung in einer anderen Hausarztpraxis aufsucht.

Dabei sind Betreuärztinnen und -ärzte verpflichtet, dem Patienten geeignete HZV-Vertreterpraxen zu benennen. Geeignet bedeutet in diesem Fall, dass die Vertretung am HZVVertrag der jeweiligen Krankenkasse des Patienten teilnimmt.
Wer dafür in Frage kommt, kann man leicht unter www.hausarzt-suche.de herausfinden. Ebenfalls von einer Vertretung spricht man, wenn der Vertreterarzt mit dem eigentlichen Betreuarzt in einer Praxisgemeinschaft zusammenarbeitet, da diese über zwei Betriebsstättennummern (BSNR) verfügt. In diesem Fall empfiehlt es sich, dass beide Praxispartner an der Hausarztzentrierten Versorgung teilnehmen, damit die Patienten nicht die gewohnte Praxis verlassen und einen HZV-Arzt in einer anderen Praxis aufsuchen müssen. Ein Vertreterfall bliebe es dann dennoch, aber für die Patienten ein Service, der die Entscheidung für den gewählten HZV-Vertretungsarzt leicht macht.
Von einer Stellvertretung spricht man hingegen, wenn die Behandlung durch einen anderen Hausarzt innerhalb einer Praxis, z. B. einer Einzelpraxis mit angestellten Hausärzten, einer Berufsausübungsgemeinschaft (BAG) oder einem Medizinischen Versorgungszentrum (MVZ), erfolgt. Sowohl die hausärztlichen Praxispartner als auch angestellte Hausärzte können innerhalb der Praxis (ausgeschlossen sind hier die Praxis -
gemeinschaften) als Stellvertreter des HZVBetreuarztes behandeln und voll abrechnen, auch – und das ist wichtig zu wissen – wenn sie selbst nicht an der Hausarztzentrierten Versorgung teilnehmen. Werden bestimmte qualifikationsgebundene Leistungen, wie beispielsweise die Sonographie abgerechnet, benötigt der in Stellvertretung behandelnde Arzt selbstverständlich die erforderliche Qualifikation dazu.
Bei einem klassischen Vertretungsfall wird die Vertreterpauschale abgerechnet. Nicht
Besteht Unsicherheit, ob die Vertreterpauschale oder aber die konkret erbrachten Leistungen abgerechnet werden müssen, hilft ein Gedanke an die BSNR. Arbeiten Sie unter einer anderen Betriebsstättennummer als der zu vertretende HZV-Betreuarzt, handelt es sich um eine Vertretung und die Vertreterpauschale greift. Arbeiten Sie beide unter einer BSNR, ist es eine Stellvertretung und sie darf nicht abgerechnet werden.
vergessen: Neben der Vertreterpauschale können auch noch vertragsabhängig weitere Einzelleistungen von der vertretenden HZV-Ärztin oder dem HZV-Arzt abgerechnet werden!
Anders verhält es sich, wenn eingeschriebene HZV-Patienten im Rahmen der Stellvertretung behandelt werden. Hier erfolgt keine Abrechnung einer HZV-Vertreterpauschale, sondern die tatsächlich erbrachte Leistung wird regulär in der Vertragssoftware dokumentiert und abgerechnet. Die HZV-Vergütung der Behandlung oder diagnostischen Maßnahme durch den Stellvertreter wird laut HZV-Vertrag der Betreuärztin oder dem Betreuarzt zugeordnet. Unabhängig davon ist in der Praxis sicherzustellen, dass immer der tatsächliche Leistungserbringer, in diesem Fall also der Stellvertreter, die erbrachte Leistung in der Praxissoftware mit seiner LANR erfasst. Unabhängig von einem Stellvertreterfall können HZV-Betreuärztinnen und -ärzte übrigens Leistungen, für die sie selbst keine Qualifikation besitzen, innerhalb der eigenen Praxis durch einen Stellvertreterarzt erbringen lassen („Delegation“).

Die chronische Niereninsuffizienz (chronic kidney disease, CKD) ist oft eine Folgeerkrankung des Diabetes und gleichzeitig mit einem erhöhten Risiko für die Entwicklung einer Herzinsuffizienz verbunden. Bis zu den späten Stadien 4 oder 5 verläuft sie in der Regel asymptomatisch. Da die wesentlichen beeinflussbaren Grunderkrankungen –Hypertonie und Diabetes – in der Hausarztpraxis behandelt werden, sind Diagnostik und Therapie der Niereninsuffizienz ebenfalls eine primär hausärztliche Aufgabe. Sie stehen im Fokus dieser Fortbildung.
INHALT
• Einführung
• Verlauf und Komplikationen
• Untersuchungen in der Hausarztpraxis
– Messung der glomerulären Filtrationsrate
– Albumin-Kreatinin-Quotient im Urin
– Was tun bei reduzierter eGFR?
– Wann überweisen?
– Erste Maßnahmen bei gesicherter Diagnose
• Therapie
– Lebensstil und Ernährung
Blutdruck
– Diabetes
– Wundermittel SGLT-2-Inhibition?
• Anpassung von Pharmakotherapien bei CKD
• Monitoring
• Patienteninfo: 8 Regeln zum Nierenschutz
AUTOR
• Dr. Reinhard Merz (Interessenkonflikte: keine)
Zur Beschreibung der chronischen Niereninsuffizienz soll der Begriff chronische Nierenerkrankung (chronic kidney disease, CKD) verwendet werden. Eine CKD ist mit zahlreichen Komplikationsmöglichkeiten in verschiedenen Organsystemen verbunden und wird häufig erst beim Auftreten erster Komplikationen festgestellt.
•
Wichtigster Parameter ist die GFR. Sie kann durch die Bestimmung der Clearance von Kreatinin über die CKD-EPI-Formel geschätzt werden.
•
Die wesentlichen beinflussbaren Grunderkrankungen bei der CKD sind Hypertonie und Diabetes, die in der Hausarztpraxis behandelt werden können. Unabhängig von der Grunderkrankung führt der Verlauf über Jahre hinweg häufig progredient zur terminalen CKD.
•
Ein Screening der Nierenfunktion wird nicht empfohlen. Das diagnostische Basisrepertoire zur Abklärung einer Niereninsuffizienz ist klar definiert.
•
Bei reduzierter eGFR und akuten Symptomen eines Nierenversagens (Ödeme, Luftnot) oder schweren Elektrolytentgleisungen (Hyperkaliämie) Hospitalisierung, ansonsten eGFR Messung innerhalb von 2 Wochen kontrollieren.
•
Die Notwendigkeit einer Überweisung zum Nephrologen sollte kritisch abgewogen werden. Dabei sollte zwischen einer diagnostischen Überweisung und kontinuierlicher Mitbetreuung unterschieden werden.
•
Die Behandlung einer CKD umfasst ein Bündel von allgemeinen und medikamentösen
Maßnahmen. Sie sollen die Progression verzögern, eine terminale Niereninsuffizienz / Dialyse vermeiden und CKDbedingte Begleiterkrankungen behandeln. Zusäzlich ist die Prävention von kardiovaskulären Erkrankungen möglich..
•
Die Einstellung des Blutdrucks ist eine der wichtigsten Maßnahmen der Progressionshemmung bei chronischen Nierenerkrankungen und vermindert gleichzeitig das Risiko für kardiovaskuläre Komplikationen.
•
Studien konnten zeigen, dass SGLT-2-Hemmer eine nephroprotektive Wirkung haben und bei Menschen mit einem sehr hohen Risiko für eine terminale Niereninsuffizienz zu einer verringerten Mortalität führen. Ein blutdruckunabhängiger Effekt auf das Fortschreiten einer Niereninsuffizienz ist jedoch nicht belegt. Für Patienten, die den Kriterien der Zulassungsstudie entsprechen (Typ-2-Diabetes, höhergradige Niereninsuffizienz) scheint die Anwendung vertretbar.
•
Eine nicht oder falsch angepasste Dosierung von Medikamenten kann bei CKD-Patienten Toxizität oder eine ineffektive Behandlung verursachen.
•
Unter den Schmerzmitteln ist Paracetamol bei CKD das sicherste. NSAR sind nur bis zu einer eGFR von 30 ml/min zugelassen und sollten nach Möglichkeit ganz vermieden werden.
•
Für Monitoringintervalle und Untersuchungen gibt es keine wissenschaftliche Evidenz, daher können diese individuell mit dem Patienten abgestimmt werden. Die Leitlinie empfiehlt Intervalle basierend auf eGFR und Albuminurie.
Der Begriff der chronischen Nierenerkrankung (chronic kidney disease, CKD) wird seit 2002 von KDIGO (Kidney Disease – Improving Global Outcomes) zur Beschreibung der chronischen Niereninsuffizienz verwendet. Als Maß gilt die glomeruläre Filtrationsrate (GFR), das pro Zeiteinheit von den Nieren filtrierte Volumen (in ml / min). Die GFR kann durch die Bestimmung der Clearance von Kreatinin geschätzt werden (eGFR) und ist einer der wichtigsten Parameter zur Beurteilung der Nierenfunktion. Die Höhe der Albuminausscheidung wird als weiterer Faktor für die Klassifikation in die CKD-Stadien verwendet. Zur Abgrenzung der akuten Nierenschädigung wird eine zweite Messung der eGFR mit 3 Monaten Abstand gefordert. Nierengesunde mit einer eGFR ≥ 90 ml / min ohne Albuminurie sind keinem CKD-Stadium zu zuordnen (Tab. 1). Ab dem 40. Lebensjahr kommt es zu einem Abfall der eGFR um 1–2 ml / min pro Jahr, in Pflegeheimen haben über 50 % der Bewohner formal ein CKD Stadium ≥ 3. In der Hausarztpraxis haben bis zu 30 % der Patientinnen und Patienten eine eingeschränkte Nierenfunktion, das muss jedoch nicht pathologisch sein.
Tab.
Die chronische Niereninsuffizienz ist mit einem erhöhten Risiko für die Entwicklung einer Herzinsuffizienz verbunden (Abb. 1) Verantwortlich dafür sind Wirkmechanismen, die gleichzeitig in beiden Erkrankungen greifen. Im Vergleich von Patienten mit und ohne CKD liegt das Risiko für die Entwicklung einer Herzinsuffizienz bei 2,3. Fast 30 % der Patienten mit CKD haben eine Herzinsuffizienz, verglichen mit nur 6 % ohne CKD. Die Prävalenz einer eGFR < 60 ml / min / 1,73 m2 liegt bei 2,3 % der Bevölkerung, sie steigt im Alter. Viele der Betroffenen wissen es nicht. Patienten mit einer eingeschränkten eGFR haben eine erhöhte Gesamtmortalität. In Deutschland werden derzeit ca. 80 000 Patienten mit terminaler CKD mit Hämo- bzw. Peritonealdialyse behandelt, jährlich beginnen ca. 7500–10 000 Menschen neu und dauerhaft mit der Dialyse. Mehr als die Hälfte steht im Zusammenhang mit Diabetes mellitus oder Hypertonie (Abb. 2). Zu den möglichen Ursachen gehören auch blockierte Harnwege, Nierenanomalien (wie polyzystische Nierenerkrankung und Glomerulonephritis), Autoimmunerkrankungen (z. B. systemischer Lupus erythematodes) und die dauerhafte Anwendung von
Mehr als die Hälfte aller Dialysefälle steht im Zusammenhang mit Hypertonie und Diabetes
*G1 und G2 zählen nur zur chronischen Nierenerkrankung bei einer Albuminurie (Grad A2, A3) oder bei
Nierenstrukturveränderungen bzw. wenn eine eigenständige Nierenerkrankung vorliegt. eGFR = geschätzte glomeruläre Filtrationsrate
Unabhängig von der Grunderkrankung führt der Verlauf über Jahre hinweg häufig progredient zur terminalen CKD
nephrotoxischen Substanzen, zu denen auch die weit verbreiteten NSAR gehören. Unabhängig von der Grunderkrankung führt der Verlauf über Jahre hinweg häufig progredient zur terminalen CKD. Dabei kommt es in den verbliebenen gesunden Glomeruli im Rahmen der Aufrechterhaltung der Nierenrestfunktion zu einer intraglomerulären Drucksteigerung mit Hyperfiltration, die durch das Vorhandensein einer arteriellen Hypertonie erheblich verstärkt wird.
Über Angiotensin II werden vermehrt Zytokine und Wachstumsfaktoren produziert. Das führt zu einer glomerulären Hypertrophie / Hyperplasie sowie einer erhöhten glomerulären Permeabilität mit Verlust der glomerulären Siebfunktion (Proteinurie). Daraus können resultieren:
• Gestörte sekretorische Nierenfunktion: Anstieg der Retentionswerte im Serum, wenn mehr als 60 % des funktionstüchtigen Nierengewebes ausgefallen sind (GFR < 50 ml/min). Plasmakonzentration von
Abb. 1: PATHOPHYSIOLOGISCHE WECHSELWIRKUNGEN DES KARDIOPULMORENALEN SYNDROMS. NACH SCHWENGER ET AL.
Abnahme der Nierenfunktion
Abnahme der Herzfunktion
Abb. 2: URSACHEN EINER TERMINALEN NIERENERKRANKUNG
QUELLE: ABBOUD H ET AL 2010
urämische Kardiomyopathie, LV-Hypertrophie, VHF, HFpEF
renale Hyperfusion und renalvenöse Kongestion
gesteigerte Inflammation
Hyperventilation,PulmonalvaskukläresRemodelling
HyperkapnieRenaleVaskokonstriktion
Endotheldysfunktion
Aktivierung RAAS und SNS
Salz- und Wasserretention
Vermehrte Vasopressin Sekretion
renale Anämie
HFpEF = „heart failure with preserved ejection fraction“ (Herzinsuffizienz mit erhaltener linksventrikulärer Pumpfunktion), LV = linksventrikulär, RAAS = Renin-Angiotensin-Aldosteron-System, RV = rechtsventrikulär, SNS = sympathisches Nervensystem, TI = Trikuspidalinsuffizienz, VHF = Vorhofflimmern
Diabetes Bluthochdruck
Glomerulonephritis
chronisch interstitielle Nephritis
hereditäre Nierenerkrankung
sekundäre Glomerulonephritis
Neoplasien andere unklar
körpereigenen und körperfremden Substanzen (z. B. Medikamente) steigt an. Folge ist die Einschränkung der max. Konzentrationsfähigkeit der Nieren. Während gesunde Nieren die anfallenden osmotischen Substanzen bei max. Konzentrierung mit etwa 750 ml Endharn ausscheiden können, sind bei CKD etwa 3 l Urin notwendig.
• Störungen im Wasser-, Elektrolyt- und Säure-Basen-Haushalt: Ist die Adaptationsfähigkeit der erkrankten Nieren erschöpft, kommt es zu einer Natriumund Wasserretention (Entwicklung einer Hypertonie). Aus diesen Gründen sind Diuretika zumindest bei fortgeschrittener CKD ein unverzichtbarer Bestandteil eines jeglichen antihypertensiven Kombinationsschemas. Bei terminaler CKD muss mit einer Hyperkaliämie gerechnet werden. Bei einer Abnahme der glomerulären Filtrationsrate < 30 ml/min entwickelt sich zudem häufig eine metabolische Azidose.
RV-Belastung,TI PostkapillärepulmonaleHypertonie
• Störungen der Blutdruckregulation: Arterielle Hypertonie entsteht frühzeitig im Verlauf der CKD, ab einem CKD-Stadium 3 findet sie sich bei 70–85 % der
Patienten. Arterielle Hypotonie ist häufiger bei CKD-Stadium 4 und 5 durch intravasalen Volumenmangel.
Die CKD ist in aller Regel bis zu den späten Stadien 4 oder 5 asymptomatisch. Leichter bis mittelschwerer Verlust der Nierenfunktion führt oft nur zu leichten Symptomen, wie Nykturie und fällt erst bei einer Routinekontrolle durch erhöhtes Serum-Kreatinin und verminderte eGFR auf. Bei fortgeschrittener CKD ist die klinische Symptomatik charakterisiert durch:
• reduzierte körperliche Leistungsfähigkeit
• Ödeme
• Atemnot infolge pulmonaler Überwässerung
• Ausbildung von Pleura- und Perikardergüssen
Die wesentlichen beinflussbaren Grunderkrankungen bei der CKD sind Hypertonie und Diabetes, die in der Hausarztpraxis behandelt werden können. Die Behandlung unterscheidet sich nicht wesentlich von Patienten ohne CKD.
Komplikationen der CKD
CKD ist verbunden mit erhöhtem Risiko für Komplikationen, Hospitalisation und Tod.
Eine CKD ist mit zahlreichen Komplikationsmöglichkeiten in verschiedenen Organsystemen verbunden und wird häufig erst beim Auftreten erster Komplikationen festgestellt.
Die CKD ist ein unabhängiger kardiovaskulärer Risikofaktor. Die wichtigsten Risikofaktoren für eine CKD und kardiovaskuläre Ereignisse (Blutdruck, Diabetes und Rauchen) sind identisch und werden in den gängigen Risikokalkulatoren berücksichtigt (z. B. arriba). Rauchen ist ein Risikofaktor für CKD und CKD-Progression.
Bei Patienten im Stadium G3 besteht aufgrund kardiovaskulärer Ereignisse ein höheres Risiko für einen vorzeitigen Tod als für eine Dialysepflichtigkeit (im Stadium G3b 11-fach, im Stadium 4 21-fach erhöht).
Abb. 3: ABSOLUTES RISIKO PRO 1000 PATIENTENJAHRE / JAHR FÜR DAS AUFTRETEN EINER TERMINALEN NIERENERKRANKUNG. QUELLE: CHENOT JF ET AL. 2022
Die CKD ist lange asymptomatisch und fällt häufig erst bei Routinekontrollen auf
Bei CKD ist eine Eisenmangelanämie häufig. Sie muss adäquat behandelt werden.
Auch eine Albuminurie ist ein Prädiktor der Gesamt- und kardiovaskulären Mortalität. Das Risiko der CKD-Progression in Richtung terminale Niereninsuffizienz wird ebenfalls wesentlich durch GFR und Albuminausscheidung bestimmt (Abb. 3)
Eine renale Anämie durch verringerte Bildung von Erythropoetin ist ab einer eGFR < 45 ml/min wahrscheinlich. Am häufigsten ist bei CKD eine Eisenmangelanämie, die hausärztlich behandelt werden kann. Wird eine Anämie (Hämoglobin < 11 mg / d / 6,8 mmol / dl) festgestellt, sollten die Eisenspeicher (Ferritin, Transferrinsättigung) überprüft werden. Die Therapieentscheidung orientiert sich jedoch an der Klinik und weniger an Laborwerten. Ein Hämoglobin zwischen 10–11 g/dl (6,2–6,8 mmol/l) ist im Regelfall ausreichend. Die Entscheidung zu einer Therapie mit Erythropoetin (EPO) oder Erythropoese-stimulierenden Agenzien (ESA) wird häufig von Nephrologen getroffen. Bei Hb ≥ 10 g/dl (≥ 6,2 mmol/l) wird eine ESA-Therapie nicht empfohlen. Vor Beginn einer ESA-Therapie sollten zunächst andere korrigierbare Anämieursachen behandelt werden (z. B. Eisenmangel, Entzündung). Bei Hb ≤ 10 g / dl
(≤ 6,2 mmol / l) basiert die individuelle Entscheidung auf den Anämiesymptomen, Hb-Abfall, Ansprechen auf Eisentherapie, Risiken der ESA-Therapie.
Die CKD-Mineral and Bone Disorder (CKD-MBD) geht mit Pathologien der Laborchemie (Kalzium, Phosphat, Vitamin D, Parathormon), des Knochens (Mineralisation) sowie der Blutgefäße (Verkalkungen) einher. Im Regelfall ist ab einer eGFR < 30 ml / min eine CKD-MBD ein relevantes Risiko und sollte überprüft werden, wobei DEGAM und KDIGO ab unterschiedlichen Stadien diese erweiterte Diagnostik empfehlen (Tab. 2)
Bis CKD 3 unterscheidet sich die Therapie einer ko-existierenden Osteoporose nicht von der von Patienten ohne CKD. Ab CKD 4 sind Bisphosphonate und Teriparatid kontraindiziert, eine mögliche Alternative ist Denosumab. Es sollte keine routinemäßige Vitamin D-Substitution erfolgen. Die Entscheidung zur Notwendigkeit von Phosphatbindern (wie Calciumcarbonat und Calciumacetat, Sevelamer und Lanthancarbonat) und Vitamin D-Substitution sollte gemeinsam mit der Nephrologie getroffen werden.
Ein Screening der Nierenfunktion wird nicht empfohlen. Das diagnostische Basisrepertoire zur Abklärung einer Niereninsuffizienz sollte eingesetzt werden bei:
• neu aufgetretenen Ödemen oder Luftnot
• Diabetes mellitus
• neu diagnostiziertem Bluthochdruck
• Einnahme nephrotoxischer Medikamente
• Autoimmunerkrankungen / rheumatischen Erkrankungen
• urologischen Erkrankungen
• positiver Familienanamnese für Nierenerkrankungen, z. B. Zystennieren
• Zufallsbefunden im Labor (z. B. Proteinurie) oder Sonografie
Für die Diagnose der CKD sind mindestens zwei Messungen im Abstand von 3 Monaten notwendig.
Messung der glomerulären
Filtrationsrate
Goldstandard für wissenschaftliche Zwecke ist die exogene Messung der Clearance mithilfe zugeführter Substanzen (z. B. Inulin). Für die klinische Routine ist dies jedoch zu aufwendig. Im klinischen Alltag hat sich die leicht und kostengünstig zu messende Serum-Kreatinin-Konzentration zur Abschätzung der GFR durchgesetzt. Kreatinin wird fast ausschließlich durch glomeruläre Filtration ausgeschieden. Bei konstanter Bildungsrate / Zufuhr sowie konstanter Ausscheidung korreliert der Serum-Kreatinin-Wert umgekehrt proportional mit der GFR: Je höher der Kreatininwert, desto niedriger die GFR. Allerdings sind der Muskelstoffwechsel und die Bildung von
Kreatinin abhängig von Alter, Geschlecht und Muskelmasse. Die CKD-EPI-Formel (Chronic Kidney Disease Epidemiology Collaboration) ist die aktuell am weitesten verbreitete Näherungsformel für die GFR (siehe Kasten Seite 8). Insbesondere im Bereich leicht- bis mäßiggradig eingeschränkter GFR stimmt sie gut mit der gemessenen GFR überein.
Wie Kreatinin wird auch Cystatin C – ein ubiquitäres niedermolekulares Peptid mit stabiler Metabolisierungsrate – fast ausschließlich durch glomeruläre Filtration ausgeschieden. Der Serumspiegel korreliert daher wie die Serum-Kreatinin-Konzentration umgekehrt proportional mit der Nierenfunktion. Wenn Zweifel an der über das Kreatinin geschätzten GFR bestehen, kann eine vergleichende Bestimmung des Cystatin C zur Schweregradvalidierung einer Niereninsuffizienz sinnvoll sein.
Was tun bei reduzierter eGFR?
Bei akuten Symptomen eines Nierenversagens (Ödeme, Luftnot) oder schweren Elektrolytentgleisungen (Hyperkaliämie), Hospitalisierung, ansonsten eGFR Messung innerhalb von 2 Wochen kontrollieren. Im nächsten Schritt prüfen, ob ein Medikament als Ursache für eine erniedrigte eGFR infrage kommt, ob Medikamentendosisanpassungen notwendig sind oder ob schon bekannte Erkrankungen den Befund erklären können. Zur initialen Evaluation der Nierenfunktion bei Hinweisen auf eine nicht-altersentsprechende eGFR gehören:
• Anamnese und klinische Untersuchung
• Medikamentenreview
• Blutdruckmessung
• Sonografie der Nieren (Harnstau?)
• Urinstatus / -sediment, Albumin-Kreatinin-Ration (ACR) im Urin
• Blutbild
• Blutuntersuchung auf CRP, Elektrolyte (Na, K), Kreatinin, Harnstoff, LDH
• venöse Blutgasanalyse
Anamnese: Sollte Fragen nach aktuellen Beschwerden wie Ödembildung oder Makrohämaturie, Nykturie und weiteren Urinauffälligkeiten beinhalten. Kardiovaskuläre Begleiterkrankungen oder ein Diabetes mellitus sind in der Regel bekannt oder aus vorhandenen Unterlagen zu entnehmen. Nach Haut- oder Gelenkbeschwerden sollte gezielt gefahndet und diese sollten bei Verdacht auf eine rheumatisch entzündliche Erkrankung näher eingegrenzt werden. Auch nach Nierenvorerkrankungen sollte gezielt gefragt werden. Wirbelsäulenbeschwerden oder andere ossäre Schmerzen sollten die Aufmerksamkeit auf einen erhöhten Gebrauch von Schmerzmitteln wie NSAR lenken.
Blutbild: Eine renale Anämie ist typischerweise normochrom und normozytär. Sie ist durch Abfall des Hämoglobins (Hb) und Hämatokrits (HKT) bei unauffälligem „mean corpuscular volume“ (MCV) und „mean corpuscular hemoglobin“ (MCH) charakterisiert. Die Retikulozytenzahl ist typischerweise erniedrigt (hyporegeneratorische Anämie).
Serumelektrolyte: Eine Neigung zur Hyperkaliämie ist insbesondere bei gleichzeitig bestehender metabolischer Azidose vorhanden. Eine niedrig-normale SerumKalzium-Konzentration bei gleichzeitig hochnormalem oder erhöhtem Serum-Phos-
Die CKD-EPI-Formel ist die am weitesten verbreitete Näherungsformel für die GFR
Bei Schmerzpatienten sollte der Gebrauch von nephrotoxischen Präparaten wie NSAR erfragt werden
Besonders häufig tritt eine CKD infolge von Gefäßschäden auf
phat-Spiegel ist Hinweis auf sekundären Hyperparathyreoidismus (durch Parathormon-Messung verifizieren). Zur Beurteilung des Säure-Base-Haushaltes ist eine venöse Blutgasanalyse im Rahmen der Routineblutentnahme ausreichend.
Eine (Mikro-)Hämaturie muss immer abgeklärt werden. Der Urinstreifentest hat eine hohe Sensitivität (91–100 %) aber nur eine geringe Spezifizität (ca. 65 %). Somit eignet sich der Urinstreifentest sehr zum Ausschluss Nierenerkrankung bei vielen falsch positiven Befunden. Auf eine korrekte Durchführung der Uringewinnung ist zu achten. Die DEGAM Leitlinie „nicht-sichtbare Hämaturie“ schlägt deswegen mindestens zwei unabhängige Urinuntersuchungen vor. Das Urinsediment ist für die Zuordnung glomerulären vs. nicht-glomerulären Ursprungs einer (Mikro-)Hämaturie von wichtiger differenzialdiagnostischer Bedeutung. Je nach Befunden und Möglichkeit sollte eine nephrologische und bzw. oder urologische Abklärung erfolgen. Proteinurie und Albuminurie sind nicht identisch. Die quantitative Bestimmung einer Proteinurie hat ihre diagnostische Bedeutung bei der initialen Abklärung von Nierenerkrankungen mit größerem Eiweißverlust, z. B. bei Glomerulopathien mit nephrotischem Syndrom. Da die Albuminurie als besserer Prädiktor für Progression der meisten chronischen Nierenerkrankungen gilt, wird im Regelfall im Verlauf nur
Albumin bestimmt. Dazu dient die einfache Bestimmung von Albumin und Kreatinin im Spontanurin mit Bildung der Albumin-Kreatinin-Ratio (ACR).
Wann überweisen?
Die Notwendigkeit einer Überweisung zum Nephrologen sollte kritisch abgewogen werden. Dabei sollte zwischen einer diagnostischen Überweisung und kontinuierlicher Mitbetreuung unterschieden werden. Die DEGAM-Leitlinien empfehlen eine Überweisung in die Nephrologie:
• bei jeder erstmals festgestellten CKD mit eGFR < 30 ml/min
• bei jeder erstmals festgestellten CKD (eGFR zwischen 30 ml / min und 60 ml / min) und – persistierender nicht urologisch erklärbarer Hämaturie 2+ oder
– Albuminurie Stadium ≥ A2 oder
–refraktärer Hypertonie mit ≥ 3 Blutdruckmedikamenten
Die S3-Leitlinie formuliert offener. Bei Jüngeren mit einer nicht altersentsprechenden eGFR oder einer Albuminurie ist eine frühere Überweisung indiziert, bei Älteren kann je nach Umständen auch bei einer eGFR < 30 ml/min auf eine Überweisung verzichtet werden.
Erste Maßnahmen bei gesicherter Diagnose
Zur GFR-Abschätzung existieren etliche Näherungsformeln. Heute gebräuchlich ist die CKD-EPI-Formel (Chronic Kidney Disease Epidemiology Collaboration):
GFR (ml/min/1,73 m²) = 141 x min (SKr/κ, 1)α x max (SKr/κ, 1)-1,209 x 0,993Alter
SKr = Serumkreatinin (mg/dL); κ = geschlechtsabhängiger Faktor 0,7 (Frau) bzw. 0,9 (Mann); α = geschlechtsabhängiger Faktor -0,329 (Frau) bzw. -0,411 (Mann), min = Minimum von SKr/κ und 1, max = Maximum von SKr/κ und 1, Alter = Lebensalter (Jahre). Die Formel basiert auf einer angenommenen Körperoberfläche von 1,73 m2
Eine eingeschränkte Aussagekraft hat die Berechnung bei Kindern und Jugendlichen, sehr hohem Alter, starkem Über- oder Untergewicht, extremer Muskelmasse (Bodybuilding) sowie Skelettmuskelerkrankungen. Im Internet existieren Plattformen zur einfachen Berechnung wie www.nierenrechner.de.
Krankheiten mit einem spezifischen nephrologischen Behandlungsbedarf (z. B. Glomerulonephritis) machen nur einen kleinen Teil der CKD aus. Besonders häufig tritt eine CKD infolge von Gefäßschäden durch Diabetes und Bluthochdruck auf. Die Kontrolle dieser Grunderkrankungen ist daher einer der wichtigsten Eckpfeiler in der Prävention der CKD, die Behandlung unterscheidet sich nicht wesentlich von Patienten ohne CKD. Patienten sollten bei gesicherter Diagnose einer CKD auf jeden Fall umfassend aufgeklärt werden, weil ihre eingeschränkte Nierenfunktion Einfluss auf vorbestehende Medikationen haben kann.
Jede Medikation sollte überprüft und an die Nierenfunktion angepasst werden (Seite 13).
Die Behandlung einer CKD umfasst ein Bündel von allgemeinen und medikamentösen Maßnahmen (Abb. 4)
Therapieziele sind:
• Progression verzögern
• terminale Niereninsuffizienz / Dialyse vermeiden
• CKD-bedingte Begleiterkrankungen behandeln
• Prävention von kardiovaskulären Erkrankungen
Die Progression einer CKD wird wie das Risiko für kardiovaskuläre Erkrankungen durch den Lebensstil beeinflusst. Rauchen ist ein Risikofaktor sowohl für die Progression der CKD als auch für schwere kardiovaskuläre Ereignisse bei Patienten mit Niereninsuffizienz. Empfehlung und Unterstützung beim Rauchstopp gehören deshalb zu den hauptsächlichen Einflussfaktoren bei der nicht-medikamentösen Therapie.
Abb. 4: ÜBERSICHT DER DIAGNOSTISCH-THERAPEUTISCHEN EMPFEHLUNGEN. NACH FLEIG ET AL.
Die Progression einer CKD wird massiv durch den Lebensstil beeinflusst
Ab CKD-Stadium 4 sollte allen Patient eine Ernährungsberatung angeboten werden
Abb. 5: DIE MEDITERRANE DIÄT GILT ALS GÜNSTIGSTE ERNÄHRUNGSFORM AUCH BEI PATIENTEN MIT CKD. P = PORTIONEN
Süßigkeiten ( ≤ 1 P)
wöchentlich jeden Tag bei jeder Haupt - malhzeit
Kartoffeln ( ≤ 3 P)
weißes Fleisch (2 P) Fisch und Meeresfrüchte ( ≥ 2 P)
Milchprodukte (2 P), möglichst Magermilch
Oliven, Nüsse, Kerne (2 P)
Früchte (1–2 P), Gemüse (auf Vielfalt achten)
Regelmäßige körperliche Betätigung
Bei der Ernährung gilt generell die „westliche Diät“ mit vielen tierischen Proteinen und geringem Anteil an Ballaststoffen als ungünstig. Empfohlen wird stattdessen eine „mediterrane Diät“ (Abb. 5). Die Empfehlungen im Einzelnen (Tab. 3):
• Eiweißzufuhr: Zwar wird die früher propagierte eiweißarme Ernährung nicht mehr empfohlen, die Eiweißzufuhr in Deutschland liegt jedoch generell über der empfohlenen Menge von 0,8–1 g/kg KG /d. Bei Patienten mit einer eGFR von < 30 ml/ min/1,73 m² (Kategorie G4–G5) sollte die
rotes Fleisch (< 2 P) verarbeitetes Fleisch ( ≤ 1 P)
Eier (2–4 P) Hülsenfrüchte ( ≥ 2 P)
Kräuter und Gewürze, Zwiebeln, Knoblauch
Olivenöl, Brot, Pasta, Reis, andere Cerealien, 1–2 P
Wasser und Kräutertees
Regionale Bio Produkte der Jahreszeit
Eiweißzufuhr auf 0,8 g/kg KG/d beschränkt werden. Ab CKD-Stadium 4 sollte allen Patienten eine Ernährungsberatung angeboten werden.
• Salzzufuhr: Für die Reduktion der Natriumzufuhr wurde nachgewiesen, dass damit die Progression einer CKD verzögert werden kann (sowie kardiovaskuläre Ereignisse verhindert und die Blutdruckreduktion unterstützt). Die Aufnahme von Kochsalz sollte auf < 6 g pro Tag beschränkt werden. Die Furcht vor einer Hyperkaliämie ist wohl unbegründet,
CKD 1–3 CKD 4 CKD 5 präterminal CKD 5 Dialyse
Eiweiß 0,8–1,0 g / kg / d ≤ 0,8 g / kg / d
Energie ≤ 0,8 g / kg / d
Natrium < 100 mmol / d (3 g Na, 6 g NaCl) bei Hypertonie oder Wasserretention < 100 mmol / d
Kalium keine Einschränkung
Phosphat keine Einschränkung
Kalzium keine Einschränkung
Trinkmenge keine Mindestmenge
individuell nach Kaliumwert
10–15 g / kg / d und Phosphatbinder
1000–2000 mg / d 1000 mg / d inkl. kalziumhaltige Phosphatbinder
abhängig von Diuretikatherapie und Volumenstatus
500–800 ml plus Restdiuresevol.
einer erhöhten Kaliumzufuhr wird heute eher ein präventives Potenzial zugemessen. Eine phosphatarme Ernährung (< 1200 mg / 39 mmol) wird ab CKD4 empfohlen.
• Flüssigkeitszufuhr: Die Steuerung der Flüssigkeitszufuhr sollte individuell erfolgen unter Berücksichtigung von Grunderkrankung und Komorbiditäten. Im Allgemeinen sollte keine hohe orale Flüssigkeitszufuhr zum „Nierenspülen“ eingesetzt werden. In den meisten Fällen ist eine tägliche Trinkmenge von 1,5–2 l ausreichend. Trinkmengenbeschränkungen sind bei nicht-dialysepflichtiger CKD nur selten notwendig, z. B. bei älteren Patienten mit Herzinsuffizienz.
• Hyperurikämie: Es gibt keine Evidenz hinsichtlich der Wirkung einer harnsäuresenkenden Therapie auf die Progression der CKD (sowohl bei symptomatischen als auch asymptomatischen Patienten mit Hyperurikämie).
In der Schweizer EFFORT-Studie (Schuetz et al. 2019) wurde der Einfluss einer personalisierten Ernährungsberatung und Ernährung bei mehr als 2000 Patienten untersucht, die meisten davon mit CKD. Ernährungsziel waren die allgemein anerkannten Grundprinzipien einer „gesunden“ Ernährung (mediterrane und pflanzenbetonte Ernährung). Die positiven Effekte dieser Ernährungsform waren bei den höhergradigen CKD-Stadien am ausgeprägtesten. Da eine Ernährungsberatung nur eine fakultative Leistung der GKV ist, kann das in Deutschland schwer umsetzbar sein.
Die Einstellung des Blutdrucks ist eine der wichtigsten Maßnahmen der Progressionshemmung bei chronischen Nierenerkrankungen und vermindert gleichzeitig das Risiko für kardiovaskuläre Komplikationen. Durch eine RAS-Blockade wird nicht nur der Blutdruck eingestellt, sondern auch die progressionsfördernde Albuminurie vermindert. Der Zielblutdruck soll laut Leitlinie individuell festgelegt werden. Bei CKD-Patienten mit Albuminurie < 300 mg/
dl und ohne Diabetes mellitus liegt er bei < 140/90 mmHg. Falls tolerabel können Zielwerte um 130/80 mmHg angestrebt werden. Bei CKD- Patienten mit Diabetes mellitus und / oder Albuminurie > 300 mg/d liegt der Zielwert bei < 130/80 mmHg. Gründe für noch niedrigere Blutdruckziele können kardiovaskuläre Komorbiditäten oder jüngeres Patientenalter sein. Therapie der Wahl, insbesondere bei Vorliegen einer Albuminurie, sind ACEHemmer – bei Unverträglichkeit Angiotensin-Rezeptorblocker (ARB); hierbei soll die Therapie mit niedriger Dosis begonnen (z. B. Ramipril 1,25 mg pro Tag) und alle 2 Wochen gesteigert werden. Eine Kombination von beiden ist wegen der Gefahr einer Hyperkaliämie sowie einer akuten Nierenschädigung kontraindiziert. Es gibt keine formalen Empfehlungen für das Monitoring der Elektrolyte. Werden ACE-Hemmer neu angesetzt oder die Dosis erhöht, wird nach ca. 1–2 Wochen eine Kontrolle der eGFR und des Kaliumspiegels empfohlen.
Nur rund ein Viertel der Hochdruckpatienten kommt allein mit ACE-Hemmer oder ARB in den Zielbereich. Ggf. ist eine Kombinationstherapie mit einem anderen Antihypertensivum erforderlich, hier kommen vor allem Diuretika und Kalziumantagonisten infrage. Hydrochlorothiazid, Chlortalidon, Indapamid sind ab eGFR < 30 ml/min formal kontraindiziert. Bei einer eGFR < 30 ml/min ist das Thiazidanalogon Xipamid zu bevorzugen, da es nicht von der luminalen Seite, sondern von der Blutseite des Tubulus wirkt – aber vorsichtige Dosierung.
Die Therapie mit einem ACE-Hemmer oder einem ARB führt unabhängig von der Blutdrucksenkung zu einer Reduktion der Proteinurie von 30–45 %. Die AngiotensinHemmstoffe sollten daher möglichst ausdosiert werden, um eine optimale Senkung der Proteinurie zu erzielen und bei einer Verschlechterung der Nierenfunktion nicht abgesetzt werden.
Zu Beginn der Behandlung ist ein Absinken der eGFR um 10–20 % nicht ungewöhnlich. Dieser eGFR-Abfall ist funktionell und meist
Trinkmengenbeschränkungen sind bei nicht-dialysepflichtiger CKD nur selten notwendig
Die Einstellung des Blutdrucks vermindert die Progression der Nierenerkrankungen und gleichzeitig das Risiko für kardiovaskuläre Komplikationen
Bei Vorliegen einer Albuminurie sollten auch normotensive Patienten mit einem RAS-Blocker behandelt werden
Abb. 6: WIRKUNG VON ANGIOTENSINHEMMUNG UND NSAR AUF DEN GLOMERULÄREN FILTRATIONSDRUCK. QUELLE: CHENOT JF ET AL. 2022
Blutdruckmedikamente
Hypovolämie
Salzmangel
→ glomerulärer Druck ↓
Renin verengt efferente Arteriole
→ glomerulärer Druck ↑
ACEI / ARB erweitern die efferente Arteriole
→ glomerulärer Druck ↓
reversibel; er resultiert aus einer Erweiterung der efferenten Arteriolen der Glomeruli (Abb. 6). Bei Vorliegen einer Albuminurie sollten auch normotensive Patienten mit einem RAS-Blocker behandelt werden (mit Diabetes mellitus bei ACR ≥ 30 mg/g, ohne Diabetes bei ACR ≥ 300 mg/g).
Die Behandlungsziele zwischen DiabetesPatienten mit und ohne CKD unterscheiden sich nicht und werden individuell festgelegt.
Prostacyclin erweitert afferente Arteriole
→ glomerulärer Druck ↑
NSAR hemmt Prostacyclin-Synthese
→ glomerulärer Druck ↓
Die aktualisierte NVL schlägt an der Lebenserwartung und Patientenzielen orientierte Zielwerte vor. Der HbA1c-Wert hat bei eingeschränkter Nierenfunktion eine begrenzte Aussagekraft. Beim Vorliegen einer Makroangiopathie, die bei CKD häufig ist, können höhere Zielwerte sinnvoll sein. Der Zielkorridor des HbA1c zur Vermeidung mikrovaskulärer Komplikationen liegt bei 7–7,5 %, bei Menschen mit reduzierter Lebenserwartung sind Werte bis 8,0 % akzeptabel. Es gibt keinen nachweislichen
ml / min / 1,73m 2 verordnungsfähig
Nutzen niedrigerer Zielwerte für HbA1c bei CKD. Mittel der Wahl für die Blutzuckerkontrolle ist Metformin, das an die Nierenfunktion angepasst werden muss (Tab. 4). Seit einigen Jahren darf es bis zu einer GFR von 30 ml/min eingesetzt werden. Allerdings scheint das Risiko für eine Laktatazidose erhöht zu sein.
Wundermittel SGLT-2-Inhibition?
Mehrere Studien konnten zeigen, dass SGLT-2-Hemmer eine nephroprotektive Wirkung haben und bei Menschen mit einem sehr hohen Risiko für eine terminale Niereninsuffizienz zu einer verringerten Mortalität führen. Daraufhin wurde der NVL-Diabetes angepasst und empfiehlt
SGLT-2-Hemmer nun priorisiert als Add-on. Eine routinemäßige Verordnung von SGLT-2-Hemmern ist aber nicht indiziert. Dapagliflozin wurde 2021 zur Behandlung
der chronischen Nierenkrankheit für Patienten mit und ohne Diabetes mellitus zugelassen und kann zusätzlich zu einem ACE-Hemmer / ARB eingesetzt werden. Der Wirkmechanismus bei Niereninsuffizienz ist nicht vollständig geklärt. In der Zulassungsstudie reduzierte Dapagliflozin gegenüber Plazebo einen Kombinationsendpunkt (Verringerung eGFR, terminale Niereninsuffizienz, renal oder kardiovaskulär bedingter Tod (9,2 vs. 14,5 % nach im Median 2,4 Jahren). Aufgrund des vorzeitigen Abbruchs der Studie nach einer Zwischenanalyse wird der Effekt jedoch möglicherweise überschätzt. Ein blutdruckunabhängiger Effekt auf das Fortschreiten einer Niereninsuffizienz ist bei kritischer Sicht nicht belegt. Für Patienten mit Typ-2-Diabetes und stärkerer Niereninsuffizienz, die den Kriterien der Studie entsprechen, erscheint die Anwendung vertretbar.
Bei Patienten mit CKD (GFR < 60 ml/ min/1,73m²) soll vor der Verordnung neuer Medikamente geprüft werden, ob eine Anpassung der Dosierung notwendig ist oder eine Kontraindikation vorliegt. Müssen überwiegend renal eliminierte Arzneistoffe eingesetzt werden, muss man häufig das Dosierungsregime anpassen, um Plasmakonzentrationen zu erzielen, die dem Profil bei Nierengesunden nahekommen. Eine nicht oder falsch angepasste Dosierung von Medikamenten kann bei CKD-Patienten Toxizität oder eine ineffektive Behandlung verursachen. Grundlage der Dosisanpassung ist die Bestimmung der eGFR. Zur Dosisanpassung gibt es grundsätzlich drei Möglichkeiten:
• Vergrößerung des Abstands zwischen zwei Gaben
• Verringerung der applizierten Dosis
• Kombination aus beidem
Bei den meisten Medikamenten wird eine niedrigere Dosierung gewählt, es gibt aber
Ausnahmen: Bei Antibiotika darf die Initialdosis nicht reduziert werden, um ausreichend hohe Wirkspiegel zu erzielen, Anpassung erst im Verlauf. Schleifendiuretika müssen bei zunehmender Niereninsuffizienz höher dosiert werden. ACE-Hemmer und Sartane wirken nephroprotektiv und verlangsamen die Progression, müssen aber vorsichtig dosiert werden (Hyperkaliämierisiko), GFR berücksichtigen (www.dosing.de). Direkte orale Antikoagulanzien werden teilweise renal eliminiert. Methotrexat (MTX) wird überwiegend über die Nieren eliminiert. Bei CKD steigt das Risiko für Nebenwirkungen wie Myelotoxizität. MTX darf bei einer GFR unter 30 ml / min nicht mehr angewendet werden. Eine mögliche Alternative ist Leflunomid. Unter den Schmerzmitteln ist Paracetamol bei CKD das sicherste. NSAR sind nur bis zu einer eGFR von 30 ml/min zugelassen und sollten nach Möglichkeit ganz vermieden werden. Sie können bei vorgeschädigten
ACE-Hemmer und Sartane wirken nephroprotektiv und verlangsamen die Progression, müssen aber vorsichtig dosiert werden
www.dosing.de ist eine praktische Hilfe zur Berechnung der adäquaten Dosierung
Nieren durch Hemmung des Prostaglandinstoffwechsels die Nierendurchblutung beeinträchtigen, auch bei topischer Anwendung als Schmerzgel. Besonders riskant ist die Dreifachkombination von RAS-blockierenden Arzneimitteln, NSAR und Diuretika (engl. „triple whammy“). Patienten sollten über die möglichen Konsequenzen aufgeklärt werden, wo immer möglich sollten nichtmedikamentöse Maßnahmen angeboten werden (physikalische Therapie, Physiotherapie). Metamizol muss nicht an die eGFR angepasst werden und kann bei Wirksamkeit eine Alternative zu NSAR sein (Leberwert-
Für Monitoringintervalle und Untersuchungen gibt es keine wissenschaftliche Evidenz, daher können diese individuell mit dem Patienten abgestimmt werden. Zur Orientierung macht die Leitlinie einen Vorschlag basierend auf eGFR und Albuminurie (Abb.
8). Folgende Maßnahmen können zum Monitoring gehören:
• eGFR und Blutdruck
• Albumin-Kreatinin Quotient, wenn initial eine Albuminurie festgestellt wurde
• HbA1c bei Diabetes
• Medikamentenreview
• Blutbild ab eGFR < 30 ml / min
monitoring!). Wird eine Opioidtherapie bei CKD Grad 4 als notwendig erachtet, sind Buprenorphin, Hydromorphon und Fentanyl, die nicht nur renal eliminiert werden, gegenüber anderen Opioiden vorzuziehen (LONTS-Leitlinie).
In den meisten Fachinformationen findet man Angaben zur Dosierung bei eingeschränkter Nierenfunktion. Bei Zulassungsstudien neuer Medikamente sind Patienten mit eingeschränkter Nierenfunktion jedoch häufig ausgeschlossen. Das führt zu der verwirrenden Situation, dass zum Teil Medikamenten, die bei CKD empfohlen werden, die formale Zulassung fehlt. Entsprechend finden sich in den Fachinformationen auch keine Hinweise zur Dosisanpassung. Die extrarenale Dosisfraktion (Q0) ist eine Kennzahl für den nicht durch die Nieren ausgeschiedenen Arzneistoffanteil. Je kleiner der Q0-Wert ist, desto größer ist der Anteil der renalen Ausscheidung und umgekehrt. Ist Q0 gleich 1, ist der Anteil der renalen Elimination nahezu 0. Spielt die Niere hingegen eine große Rolle für die Ausscheidung, nimmt Q0 einen kleinen Wert an (Abb. 7).
Die Webseite www.dosing.de der Universität Heidelberg ist eine Hilfe zur Berechnung.
• Phosphat, Kalzium, Parathormon, Vitamin D ab eGFR < 30–45 ml / min erwägen
• Gewichtskontrollen. v. a. bei Ödemen
Akute Verschlechterung der Nierenfunktion wird oft durch plötzliche Ereignisse wie Dehydratation, Kontrastmittel oder nephrotoxische Medikamente ausgelöst. Daher sind anlassbezogene Kontrollen klinisch wichtiger als routinemäßige Kontrollen.
Abb. 8: EMPFEHLUNGEN FÜR DIE MONITORINGFREQUENZ (ANZAHL KONTROLLUNTERSUCHUNGEN PRO JAHR) ANHAND GFR UND ALBUMINURIESTADIEN
Wie häufig sollte Patientinnen und Patienten pro Jahr gesehen werden? (nach eGFR / Albuminurie)
Diese Regeln zum Nierenschutz eignen sich als Patienteninfo. Sie finden eine Vorlage zum Ausdrucken oder Kopieren unter www.hausarzt-bw .de:
1. Halten Sie sich fit und aktiv. Bewegen Sie sich regelmäßig.
2. Lassen Sie regelmäßig Ihren Blutzuckerspiegel überprüfen. Achten Sie bei Diabetes mellitus auf eine stabile Einstellung des Blutzuckers.
3. Halten Sie Ihren Blutdruck im Auge. Messen Sie regelmäßig ihren Blutdruck.
4. Ernähren Sie sich gesund und achten Sie auf Ihr Körpergewicht.
5. Trinken Sie ausreichend.
6. Rauchen Sie nicht.
7. Nehmen Sie nicht regelmäßig Medikamente, die frei verkäuflich sind (ohne Verschreibung).
8. Lassen Sie Ihre Nierenfunktion messen, wenn mehr als einer der „Hochrisikofaktoren“ zutrifft:
• Sie haben Diabetes.
• Sie leiden an Bluthochdruck.
• Sie sind übergewichtig.
• Ein Elternteil von Ihnen oder ein anderes Familienmitglied leidet an einer Nierenerkrankung.
IMPRESSUM
Auftraggeber:
Hausärztliche Vertragsgemeinschaft AG (HÄVG) im Auftrag des Deutschen Hausärzteverbandes e.V.
Verlag:
© mm medizin + medien
Verlag GmbH, 2023
Geschäftsführung:
Dr. Monika von Berg
Autor:
Dr. Reinhard Merz
Zertifiziert durch:
Institut für hausärztliche
Fortbildung im Deutschen
Hausärzteverband (IHF) e.V.
Für Angaben zu Dosierungen und Applikations formen übernehmen Autoren und Verlag keine Gewähr.
Abboud H, Henrich WL. Clinical practice. Stage IV chronic kidney disease. N Engl J Med 2010; 362: 56-65
Arznei-telegramm (Hrsg.). Dapagliflozin bei chronischer Niereninsuffizienz. arzneimittel-telegramm 2021, 52: 76–78
AWMF. Interdisziplinäre S2k-Leitlinie Rationelle Labordiagnostik zur Abklärung Akuter Nierenschädigungen und Progredienter Nierenerkrankungen AWMF-Register-Nr. 115/001 Erstellungsdatum:
2021
Bargetzi A et al. Admission kidney function is a strong predictor for the response to nutritional support in patients at nutritional risk. Clin Nutr 2021; 40: 2762-2771
Chenot JF et al. Langzeitbetreuung der chronische Nierenerkrankung in der Hausarztpraxis. Allgemeinmed up 2 date 2022; in print
DEGAM S3-Leitlinie Versorgung von Patienten mit chronischer nicht-dialysepflichtiger Nierenerkrankung in der Hausarztpraxis, AWMF Register-Nr. 053-048
DEGAM S3 Leitlinie Hausärztliche Risikoberatung zur kardiovaskulären Prävention. AWMF-Registernummer 053-024 (wird aktualisiert)
Dettli L. The kidney in pre-clinical and clinical pharmacokinetics. Jpn J Clin Pharmacol Ther 1984; 15: 241-254
Fleig S et bal. Chronische Niereninsuffizienz. Was ist gesichert in der Therapie. Internist 2016, 57: 1164–1171
https://deximed.de/home/klinische-themen/niere-harnwege/ krankheiten/nierenerkrankungen/nierenkrankheit-chronische https://deximed.de/home/klinische-themen/niere-harnwege/ symptome/niereninsuffizienz
Herold G. Innere Medizin. Kap. Chronische Nierenerkrankungen Krautzig S. Abklärung der Niereninsuffizienz beim geriatrischen Patienten. Z Gerontol Geriat 2021; 54: 197–204
Kuhlmann MK. Ernährung bei Nierenerkrankungen. Aktuel Ernahrungsmed 2011; 36: 367-384
Schwenger V et al. Niereninsuffizienz im Kontext der kardiopulmorenalen Pathophysiologie. Internist 2021; 62: 1153–1165
Schuetz P et al. Individualised nutritional support in medical inpatients at nutritional risk: a randomised clinical trial. Lancet 2019; 393: 2312-2321
Weckmann G, Chenot JF, Stracke S. Clinical practice guideline: The management of non-dialysis-dependent chronic kidney disease in primary care. Dtsch Arztebl Int 2020; 117: 745–751
Wintrich J et al. Therapie bei Diabetes und Niereninsuffizienz. Ein Jahresrückblick aus Sicht des Kardiologen. Kardiologe 2021; 15: 133–139
Zeisberg M et al. Herz-Nieren-Achse. Beziehung von Herz- und Niereninsuffizienz als Komorbiditäten. Internist 2018; 59: 420–427
Das HZV-Team des Deutschen Hausärzteverbandes: Sie erreichen uns von Mo-Do 8-17 Uhr, Fr 8-15 Uhr unter
Tel.: 02203 57 56-12 09 oder via E-Mail unter ptqz@hzv.de


Ihre Ansprechpartnerin Masa Maric beantwortet all Ihre Fragen zu Qualitätszirkeln in der HZV.
Impressum
QZ kompakt Q2/2023
Herausgeber:
HZV-Team des Deutschen Hausärzteverbandes. Ein Service der Hausärztlichen
Vertragsgemeinschaft AG (HÄVG) im Auftrag des Deutschen Hausärzteverbandes e. V. Edmund-Rumpler-Str. 2 51149 Köln Tel.: 02203 5756-1209 ptqz@hzv.de
Verlag: V.i.S.d.P.: Dr. Monika von Berg

Redaktion: Siv Astrid Vogeler
Redaktion Medizin: Dr. Reinhard Merz, Dr. Ulrich Scharmer
Layout: Gabi Kellner
© mm medizin+medien Verlag GmbH
Konrad-Zuse-Platz 8, 81829 München
www.hausarzt.digital
Titelfoto: stock.adobe.com/Crystal light
UnsergesamtesFortbildungsprogrammunter:
FürHausärztinnen&Hausärzte
www.ihf-fobi.de
kontakt@ihf-fortbildung.de
FürVERAH&MFA www.verah.de
verah@ihf-fortbildung.de
Weniger Bürokratie, mehr wirtschaftliche Sicherheit und eine bessere Versorgung: Profitieren auch Sie von den vielen Vorteilen der Hausarztzentrierten Versorgung (HZV). Das HZV-Team des Deutschen Hausärzteverbandes berät Sie gerne telefonisch, per E-Mail oder auch persönlich bei Ihnen in der Praxis.
Tel.: 02203/5756-1210 · info@hzv-team.de · www.hzv.de

„...meine Rolle als Hausärztin stärken und eine koordinierte Versorgung meiner Patienten sicherstellen.“