
XÂY DỰNG VÀ SỬ DỤNG HỆ THỐNG BÀI TẬP THEO ĐỊNH HƯỚNG TIẾP CẬN PISA TRONG DẠY HỌC NỘI DUNG TỐC ĐỘ PHẢN ỨNG HÓA HỌC VÀ NHÓM HALOGEN HÓA HỌC 10 CHƯƠNG TRÌNH GIÁO DỤC PHỔ THÔNG 2018 WORD VERSION | 2023 EDITION ORDER NOW / CHUYỂN GIAO QUA EMAIL TAILIEUCHUANTHAMKHAO@GMAIL.COM SÁNG KIẾN KINH NGHIỆM HÓA HỌC Ths Nguyễn Thanh Tú eBook Collection Hỗ trợ trực tuyến Fb www.facebook.com/DayKemQuyNhon Mobi/Zalo 0905779594 vectorstock com/24597468 Tài liệu chuẩn tham khảo Phát triển kênh bởi Ths Nguyễn Thanh Tú Đơn vị tài trợ / phát hành / chia sẻ học thuật : Nguyen Thanh Tu Group




DẠYKÈMQUYNHƠN OFFICIAL S¸ng kiÕn kinh nghiÖm XÂY DỰNG VÀ SỬ DỤNG HỆ THỐNG BÀI TẬP THEO ĐỊNH HƢỚNG TIẾP CẬN PISA TRONG DẠY HỌC NỘI DUNG TỐC ĐỘ PHẢN ỨNG HÓA HỌC VÀ NHÓM HALOGEN HÓA HỌC 10 CHƢƠNG TRÌNH GIÁO DỤC PHỔ THÔNG 2018 NHẰM PHÁT TRIỂN NĂNG LỰC CHO HỌC SINH LĨNH VỰC: HÓA HỌC








DẠYKÈMQUYNHƠN OFFICIAL SỞ GIÁO DỤC VÀ ĐÀO TẠO NGHỆ AN TRƢỜNG THPT NGHI LỘC 5 S¸ng kiÕn kinh nghiÖm XÂY DỰNG VÀ SỬ DỤNG HỆ THỐNG BÀI TẬP THEO ĐỊNH HƢỚNG TIẾP CẬN PISA TRONG DẠY HỌC NỘI DUNG TỐC ĐỘ PHẢN ỨNG HÓA HỌC VÀ NHÓM HALOGEN HÓA HỌC 10 CHƢƠNG TRÌNH GIÁO DỤC PHỔ THÔNG 2018 N HẰM PHÁT TRIỂN NĂNG LỰC CHO HỌC SINH LĨNH VỰC: HÓA HỌC Họ và tên : Trần Th Vân Phạm Lâm Tùng Lê Thị Phƣợng Tổ : Khoa học tự nhiên Năm thực hiện : 2021 - 2022 NĂM HỌC 2021 - 2022
HƢỚNG
CẬN PISA TRONG DẠY HỌC NỘI DUNG “TỐC ĐỘ PHẢN ỨNG HÓA HỌC VÀ NHÓM HALOGEN – HÓA HỌC 10” CHƢƠNG TRÌNH GIÁO DỤC PHỔ THÔNG 2018 NHẰM PHÁT TRIỂN NĂNG LỰC CHO HỌC SINH.................................. 3 1.1. Cơ sở lý luận....................................................................................................... 3 1.1.1. Về đổi mới phƣơng pháp dạy học................................................................... 3 1.1.2. Về việc sử dụng bài tập hóa học trong dạy học hóa học ở trƣờng THPT....... 3 1.1.3. Cơ sở lý luận về việc xây dựng bài tập hóa học mới trong dạy học hóa học ở trƣờng THPT............................................................................................................. 5 1.1.4. Tìm hiểu về chƣơng trình đánh giá học sinh quốc tế PISA........................... 6 1.2. Cơ sở thực tiễn.................................................................................................... 8 1.2.1. Thực trạng nghiên cứu..................................................................................... 8 1.2.2. Yêu cầu của việc thiết kế và sử dụng hệ thống bài tập theo định hƣớng tiếp cận PISA trong dạy học nội dung “Tốc độ phản ứng hóa học và nhóm halogen –hóa học 10” chƣơng trình giáo dục phổ thông 2018 nhằm phát triển năng lực cho học sinh
DẠYKÈMQUYNHƠN OFFICIAL MỤC LỤC PHẦN I: ĐẶT VẤN ĐỀ........................................................................................... 1 1. Lý do chọn đề tài................................................................................................... 1 2. Mục đích nghiên cứu............................................................................................. 1 3. Đối tƣợng nghiên cứu............................................................................................ 2 4. Nhiệm vụ nghiên cứu............................................................................................ 2 5. Phạm vi nghiên cứu............................................................................................... 2 6. Phƣơng pháp nghiên cứu....................................................................................... 2 PHẦN II: NỘI DUNG............................................................................................... 8 CHƢƠNG 1. CƠ SỞ LÝ LUẬN VÀ THỰC TIỄN VỀ VIỆC XÂY DỰNG VÀ SỬ DỤNG HỆ THỐNG BÀI TẬP THEO ĐỊNH
2
XÂY DỰNG VÀ SỬ DỤNG HỆ THỐNG BÀI TẬP THEO ĐỊNH HƢỚNG TIẾP CẬN PISA TRONG DẠY HỌC NỘI DUNG “ TỐC ĐỘ PHẢN ỨNG HÓA HỌC VÀ NHÓM HALOGEN - HÓA HỌC 10” CHƢƠNG TRÌNH GIÁO DỤC PHỔ THÔNG 2018 NHẰM PHÁT TRIỂN NĂNG LỰC CHO HỌC SINH........................................................................................................................ 10 2.1. Tổng quan môn hóa học 10 theo chƣơng trình GDPT 2018............................ 10 2.2. Bài tập theo hƣớng tiếp cận PISA.................................................................... 10 2.2.1. Đặc điểm của bài tập theo hƣớng tiếp cận PISA.......................................... 10 2.2.2. Các yêu cầu đối với bài tập theo hƣớng tiếp cận PISA ............................... 11 2.2.3. Nguyên tắc thiết kế bài tập theo hƣớng tiếp cận PISA................................ 12 2.2.4. Quy trình thiết kế bài tập theo hƣớng tiếp cận PISA................................... 12 2.3. Xây dựng hệ thống bài tập theo hƣớng tiếp cận PISA..................................... 14
TIẾP
...................................................................................................................... 9 CHƢƠNG
.
2.3.1. Bài tập tiếp cận PISA nội dung tốc độ phản ứng.......................................... 14 2.3.2. Bài tập tiếp cận PISA nội dung halogen và hợp chất.................................... 24 2.4. Các biện pháp sử dụng bài tập theo hƣớng tiếp cận PISA để phát triển năng lực cho học sinh............................................................................................................. 34
2.4.1. Biện pháp 1: Giúp học sinh thấy đƣợc ý nghĩa của bài tập theo hƣớng tiếp cận PISA.................................................................................................................. 34 2.4.2. Biện pháp 2: Lựa chọn bài tập phù hợp với nội dung bài học và mục tiêu dạy học .................................................................................................................... 35 2.4.3. Biện pháp 3: Kết hợp sử dụng bài tập theo hƣớng tiếp cận PISA với các phƣơng pháp dạy học tích cực ................................................................................ 35 2.4.4. Biện pháp 4: Giao nhiệm vụ, tổ chức hoạt động nhóm và cho HS trình bày trƣớc lớp.................................................................................................................. 36 2.4.5. Biện pháp 5: Hƣớng dẫn học sinh khai thác và sử dụng thông tin từ nội dung câu hỏi củabài tập,sách giáo khoa, tài liệu học tập,internet để giải bài tập...................... 36 2.4.6. Biện pháp 6: Lồng ghép bài tập theo hƣớng tiếp cận PISA với các hoạt động ngoại khóa...................................................................................................... 37 2.4.7. Biện pháp 7: Sử dụng đánh giá quá trình..................................................... 38 2.5. Giáo án thực nghiệm (phụ lục)......................................................................... 39
CHƢƠNG 3. THỰC NGHIỆM SƢ PHẠM ........................................................... 40
3.1. Mục đích và nhiệm vụ thực nghiệm................................................................. 40 3.1.1. Mục đích thực nghiệm................................................................................... 40 3.1.2. Nhiệm vụ thực nghiệm................................................................................. 40 3.2. Đối tƣợng và địa bàn thực nghiệm................................................................... 40 3.3. Thực hiện chƣơng trình thực nghiệm.............................................................. 41 3.4. Kết quả thực nghiệm và xử lí kết quả thực nghiệm.......................................... 41 3.4.1. Kết quả kiểm tra trƣớc thực nghiệm
41 3.4.2. Kết quả kiểm tra sau thực nghiệm
41 3.4.3. Kết quả tham khảo ý kiến học sinh, giáo viên
DẠYKÈMQUYNHƠN
OFFICIAL
.............................................
VÀ KIẾN
............................................................................
1. Kết luận............................................................................................................... 45 2. Kiến nghị............................................................................................................. 45 TÀI LIỆU THAM KHẢO....................................................................................... 47 PHỤ LỤC
..............................................................
.................................................................
42 C. KẾT LUẬN
NGHỊ
45
DANH MỤC TỪ VIẾT TẮT
TT Từ viết tắt
Tên đầy đủ 1 GV Giáo viên
HS Học sinh
THPT Trung học phổ thông
BTHH Bài tập hóa học
KTĐG Kiểm tra đánh giá
PPDH Phƣơng pháp dạy học
nghiệm
chứng
DẠYKÈMQUYNHƠN OFFICIAL
2
3
4
5
6
7 TN Thực
8 ĐC Đối
DANH MỤC BẢNG BIỂU
Bảng 3.1. Số học sinh đạt điểm Xi trƣớc khi thực nghiệm................................................41
Bảng 3.2. Số lƣợng HS đạt điểm Xi của trƣờng THPT X.................................................41
Bảng 3.3. Số lƣợng HS đạt điểm Xi của trƣờng THPT Y.................................................42
Bảng 3.4. Đánh giá của HS về việc sử dụng bài tập theo hƣớng tiếp cận PISA.............42
Bảng 3.5. Mức độ cần thiết của việc sử dụng bài tập theo hƣớng tiếp cận PISA đối với một số yêu cầu sƣ phạm ....................................................................................................43
Bảng 3.6. Mức độ cần thiết của những biện pháp sử dụng bài tập theo hƣớng tiếp cận PISA để phát triển năng lực học tập cho HS.....................................................................44
DẠYKÈMQUYNHƠN
OFFICIAL
PHẦN I : ĐẶT VẤN ĐỀ
1. Lý do chọn đề tài
Chƣơng trình giáo dục phổ thông mới đƣợc xây dựng định hƣớng hình thành và phát triển cho HS những năng lực chung nhƣ: năng lực tự học, năng lực giải quyết vấn đề và sáng tạo, năng lực thẩm mỹ, năng lực thể chất, năng lực giao tiếp, năng lực tính toán, năng lực hợp tác, năng lực công nghệ thông tin và truyền thông…Mỗi môn học đều đóng góp vào quá trình hình thành và phát triển các phẩm chất chủ yếu và năng lực chung.
Đổi mới để phát triển – một trong những định hƣớng lớn hiện nay của giáo dục nƣớc ta trong vấn đề đổi mới là chuyển từ truyền thụ kiến thức sang phát triển năng lực ngƣời học. Muốn vậy, ngoài đổi mới về phƣơng pháp dạy học thì đổi mới về nội dung kiến thức cũng là vấn đề quan trọng của chƣơng trình giáo dục. Chƣơng trình GDPT 2018 là minh chứng cho sự đổi mới nền giáo dục của nƣớc nhà trong thời gian sắp tới. Bài tập hóa học đƣợc xem nhƣ là một phƣơng tiện không thể thiếu đối với quá trình dạy và học môn hóa học. Chính vì thế nếu sử dụng hệ thống bài tập hợp lý thì sẽ phát huy tối đa hiệu quả trong việc phát triển năng lực đặc thù cho HS. Trƣớc xu thế hội nhập nhƣ hiện nay, việc dạy học phát triển năng lực cho HS phổ thông với các bài tập theo hƣớng tiếp cận chƣơng trình đánh giá học sinh quốc tế (PISA) đang nhận đƣợc sự quan tâm, nghiên cứu của nhiều nhà giáo dục.
Trong dạy học bộ môn Hóa học, ngoài việc truyền đạt các kiến thức lý thuyết thì việc sử dụng các bài tập có định hƣớng PISA hay có tính thực tiễn sẽ giúp HS có hứng thú, đam mê và yêu thích môn học, từ đó nâng cao chất lƣợng dạy và học, đồng thời trang bị kiến thức và kỹ năng cần thiết cho các em. Tuy nhiên việc sử dụng bài tập theo định hƣớng PISA hiện nay ở các trƣờng THPT vẫn chƣa đƣợc phổ biến. Hơn nữa chƣơng trình hóa học lớp 10 bao gồm một lƣợng kiến thức lớn cả về nội dung lý thuyết lẫn thực hành, nó là nền tảng để phát triển kiến thức hóa học và kích thích đam mê học hóa của HS lớp sau, vì thế yêu cầu GV ngoài việc giảng dạy hiệu quả còn phải có cách đánh giá phù hợp. Với mong muốn góp sức mình vào việc đổi mới và nâng cao chất lƣợng giáo dục, chúng tôi tiến hành thực hiện đề tài “Xây dựng và sử dụng hệ thống bài tập theo định hướng tiếp cận PISA trong dạy học nội dung tốc độ phản ứng hóa học và nhóm halogen hóa học 10 chương trình giáo dục phổ thông 2018 nhằm phát triển năng lực cho học sinh” .
2. Mục đích nghiên cứu
Đề tài nghiên cứu việc xây dựng và sử dụng hệ thống BTHH theo hƣớng tiếp cận PISA nhằm hình thành và phát triển một số năng lực, phẩm chất của HS góp phần nâng cao hiệu quả dạy học, đáp ứng nhiệm vụ chƣơng trình giáo dục phổ thông mới.
DẠYKÈMQUYNHƠN
1
OFFICIAL
3. Đối tƣợng nghiên cứu
Hệ thống bài tập theo hƣớng tiếp cận PISA trong dạy học nội dung “tốc độ phản ứng hóa học và nhóm halogen” hóa học 10 chƣơng trình giáo dục phổ thông mới nhằm phát triển năng lực cho HS.
4. Nhiệm vụ nghiên cứu
- Xây dựng cơ sở lí luận và thực tiễn của đề tài.
- Nghiên cứu về nội dung kiến thức, đối tƣợng HS và điều kiện dạy học.
- Nghiên cứu cách thiết kế và sử dụng hệ thống bài tập theo định hƣớng tiếp cận năng lực nội dung “tốc độ phản ứng hóa học và nhóm halogen” hóa học 10 trong chƣơng trình giáo dục phổ thông 2018 nhằm phát triển năng lực HS.
- Tiến hành thực nghiệm, đánh giá kết quả.
5. Phạm vi nghiên cứu
OFFICIAL
Xây dựng và sử dụng hệ thống bài tập hóa học 10 theo hƣớng tiếp cận PISA trong dạy học nội dung “Tốc độ phản ứng hóa học và nhóm halogen” chƣơng trình giáo dục phổ thông 2018 nhằm phát triển năng lực cho HS.
6. Phƣơng pháp nghiên cứu
- Nghiên cứu lý thuyết: Chƣơng trình tổng thể GDPT 2018 của Bộ GD & ĐT và các tài liệu có liên quan, chƣơng trình đánh giá HS quốc tế PISA, lý luận về phƣơng pháp dạy học hóa học, những vấn đề chung về đổi mới giáo dục trung học phổ thông.
- Nghiên cứu thực tiễn:
+ Phƣơng pháp điều tra sƣphạm
+ Phƣơng pháp đàm thoại.
+ Phƣơng pháp thực nghiệm sƣphạm.
DẠYKÈMQUYNHƠN
2
PHẦN II. NỘI DUNG. CHƢƠNG 1.
CƠ SỞ LÝ LUẬN VÀ THỰC TIỄN VỀ VIỆC XÂY DỰNG VÀ SỬ DỤNG HỆ THỐNG BÀI TẬP THEO ĐỊNH HƢỚNG TIẾP CẬN PISA TRONG DẠY HỌC NỘI DUNG “TỐC ĐỘ PHẢN ỨNG HÓA HỌC VÀ NHÓM HALOGEN – HÓA HỌC 10” CHƢƠNG TRÌNH GIÁO DỤC PHỔ THÔNG 2018 NHẰM PHÁT TRIỂN NĂNG LỰC CHO HỌC SINH
1.1. Cơ sở lý luận.
1.1.1. Về đổi mới phương pháp dạy học.
Nhiệm vụ trọng tâm của đổi mới PPDH là tích cực hóa hoạt động học tập ở HS, là phát huy ở HS tính tích cực, tự lực và sáng tạo. Môn hóa học cung cấp cho HS một hệ thống kiến thức phổ thông, cơ bản, vì vậy GV hóa học cần hình thành cho các em một kỹ năng cơ bản, thói quen học tập và làm việc khoa học.
Cốt lõi của đổi mới PPDH đó là:
- Đổi mới mục tiêu giáo dục.
- Đổi mới hoạt động dạy của GV.
- Đổi mới hoạt động học tập của HS.
- Đổi mới các hình thức tổ chức dạy học.
- Đổi mới hình thức sử dụng phƣơng tiện dạy học.
- Đổi mới việc kiểm tra, đánh giá.
1.1.2. Về Việc sử dụng bài tập hóa học trong dạy học hóa học ở trường THPT.
1.1.2.1. Ý nghĩa của việc sử dụng BTHH trong dạy học hóa học ở trường THPT.
Hệ thống bài tập định hƣớng năng lực chính là công cụ để HS luyện tập nhằm hình thành năng lực và là công cụ để GV và các cán bộ quản lý giáo dục KTĐG năng lực của HS và biết đƣợc mức độ đạt chuẩncủaquá trình dạy học.
BTHH vừa là mục đích, vừa là nội dung lại vừa là PPDH hiệu quả, nó không chỉ cung cấp cho HS kiến thức, con đƣờng giành lấy kiến thức mà còn mang lại niềm vui, niềm hứng thú của quá trình khám phá, tìm tòi, phát hiện cách giải quyết vấn đề. BTHH có ý nghĩa to lớn về nhiều mặt, đó là:
- Làm chính xác hoá những khái niệm hóa học; củng cố, đào sâu và mở rộng kiến thức một cách sinh động, phong phú, hấp dẫn; khi vận dụng kiến thức vào giải bài tập, HS mới nắm đƣợc kiến thức một cách sâu sắc.
- Rèn luyện các kĩ năng hóa học cho HS.
- Rèn luyện khả năng vận dụng kiến thức vào quá trình học tập và thực tiễn.
- Rèn kĩ năng sử dụng ngôn ngữ hóa học và các thao tác tƣ duy.
DẠYKÈMQUYNHƠN
3
OFFICIAL
- Là phƣơng tiện để kiểm tra đánh giá kiến thức và kĩ năng của HS.
- Giáo dục đạo đức, tính chính xác, kiên nhẫn, trung thực và lòng say mê khoa học.
- BTHH có vai trò quan trọng trong dạy học hoá học tích cực.
- BTHH nhƣ là nguồn kiến thức để HS tìm tòi phát hiện kiến thức, kĩ năng.
- BTHH mô tả một số tình huống thực của đời sống thực tế.
- BTHH đƣợc nêu lên nhƣ là tình huống có vấn đề.
- BTHH là một nhiệm vụ cần giải quyết.
1.1.2.2. Phân loại các dạng bài tập dùng trong dạy học môn hóa học ở trường THPT.
OFFICIAL
BTHH là phƣơng tiện để tích cực hoá hoạt động của HS. Có nhiều cách để phân loại BTHH, trong phạm vi đề tài này, chúng tôi tập trung phân tích bài tập theo định hƣớng năng lực và so sánh bài tập theo định hƣớng năng lực với bài tập hóa học truyền thống.
a. So sánh bài tập theo định hướng năng lực với bài tập hóa học truyền thống.
Qua thực tiễn dạy học chúng tôi rút ra những hạn chế của việc xây dựng bài tập truyền thống nhƣ sau:
- Tiếp cận một chiều, ít thay đổi trong việc xây dựng bài tập, thƣờng là nhữngbài tập đóng.
- Thiếu về tham chiếu ứng dụng, chuyển giao cái đã học sang vấn đề chƣa biết cũng nhƣ các tình huống thực tiễn cuộc sống.
- Kiểm tra thành tích, chú trọng các thành tích nhớ và hiểu ngắn hạn.
- Quáítôntậpthƣờngxuyên,bỏquasự kếtnốigiữavấnđềđãbiếtvàvấnđềmới.
- Tính tích lũy của việc học không đƣợc lƣu ý đến một cách đầy đủ…
Việc xây dựng bài tập theo hƣớng tiếp cận năng lực có những ƣu điểm nổi bật nhƣ sau:
- Trọng tâm không phải là các thành phần tri thức hay kỹ năng riêng lẻ mà là sự vận dụng có phối hợp các thành tích riêng khác nhau trên cơ sở một vấn đề mới đối với ngƣời học.
- Tiếp cận năng lực không định hƣớng theo nội dung học trừu tƣợng mà luôn theo các tình huống cuộc sống của HS. Nội dung học tập mang tính tình huống, tính bối cảnh và tính thực tiễn.
-So với dạy học định hƣớng nội dung, dạy học định hƣớng năng lực định hƣớng mạnh hơn đến HS.
b. Bài tập theo định hướng năng lực.
* Phân loại bài tập định hướng năng lực.
DẠYKÈMQUYNHƠN
4
Theo chức năng lý luận dạy học, bài tập có thể bao gồm: bài tập học và bài tập đánh giá (thi, kiểm tra).
- Bài tập học bao gồm các bài tập dùng trong bài học để lĩnh hội tri thức mới, chẳng hạn các bài tập về một tình huống mới, giải quyết bài tập này để rút ra tri thức mới, hoặc các bài tập để luyện tập, củng cố, vận dụng kiến thức đã học.
- Bài tập đánh giá là các bài kiểm tra ở lớp do GV ra đề hay các đề tập trung nhƣ kiểm tra chất lƣợng, so sánh, bài thi tốt nghiệp, thi tuyển. Thực tế hiện nay, các bài tập chủ yếu là các bài luyện tập và bài thi, kiểm tra. Bài tập học tập, lĩnh hội tri thức mới ít đƣợc quan tâm. Tuy nhiên, bài tập học tập dƣới dạng học khám phá có thể giúp HS nhiều hơn trong làm quen với việc tự lực tìm tòi và mở rộng tri thức.
Theo dạng câu trả lời của bài tập “mở” hay “đóng”, có các dạng bài tập sau:
- Bài tập đóng là các bài tập mà HS không cần tự trình bày câu trả lời mà lựa chọn từ những câu trả lời cho trƣớc.
OFFICIAL
- Bài tập mở là những bài tập mà không có lời giải cố định đối với cả GV và HS có nghĩa là kết quả bài tập là “mở”. Bài tập mở đƣợc đặc trƣng bởi sự trả lời tự do của cá nhân và không có một lời giải cố định, cho phép các cách tiếp cận khác nhau và dành không gian cho sự tự quyết định của ngƣời học. Nó đƣợc sử dụng trong việc luyện tập hoặc kiểm tra năng lực vận dụng tri thức từ các lĩnh vực khác nhau để giải quyết các vấn đề. Tính độc lập và sáng tạo của HS đƣợc chú trọng trong việc làm dạng bài tập này.
Trong thực tiễn giáo dục THPT hiện nay, các bài tập mở gắn với thực tiễn còn ít đƣợc quan tâm. Tuy nhiên, bài tập mở là hình thức bài tập có ý nghĩa quan trọng trong việc phát triển năng lực HS. Trong dạy học và kiểm tra đánh giá, GV cần kết hợp một cách thích hợp các loại bài tập để đảm bảo giúp HS nắm vững kiến thức, kỹ năng cơ bản vànăng lựcvận dụng trong các tình huống phức hợp gắn với thực tiễn.
* Các bậc trình độ trong bài tập theo định hướng năng lực. Dựa trên các mức độ nhận thức và chú ý đến đặc điểm của học tập định hƣớng năng lực, có thể xây dựng bài tập theo các dạng: Các bài tập dạng tái hiện; các bài tập vận dụng; các bài tập giải quyết vấn đề; các bài tập gắn với bối cảnh, tình huống thực tiễn.
1.1.3. Cơ sở lý luận về việc xây dựng bài tập hóa học mới trong dạy học Hóa học ở trường THPT.
1.1.3.1. Ý nghĩa của việc xây dựng các bài tập hóa học mới.
BTHH có hiệu quả sâu sắc trong việc thực hiện mục tiêu đào tạo, hình thành phƣơng pháp chung của việc tự học hợp lý, rèn luyện kỹ năng tự lực, sáng tạo.
BTHH là phƣơng tiện cơ bản để dạy HS tập vận dụng các kiến thức đã học vào thực tế đời sống, sản xuất và tập nghiên cứu khoa học.
DẠYKÈMQUYNHƠN
5
Nhằm đáp ứng với sự đổi mới PPDH theo định hƣớng năng lực thì việc xây dựng các BTHH mới, trong đó việc xây dựng bài tập theo định hƣớng năng lực là thiết yếu. Các BTHH sử dụng trong nhà trƣờng phổ thông hiện nay tuy đã đƣợc thay đổi nhƣng vẫn còn nặng về kiến thức toán học, nghèo nàn về kiến thức hóa học. Hầu hết các bài tập chƣa đánh giá nhiều về kỹ năng cơ bản môn Hoá học nhƣ: kỹ năng thực hành hóa học, kỹ năng vận dụng kiến thức hóa học vào thực tiễn,... Đồng thời, BTHH hiện nay chƣa chú trọng đến việc phát huy khả năng tƣ duy sáng tạo, lập kế hoạch, giải quyết vấn đề trong học tập và thực tiễn đời sống, chƣa chú trọng đến việc phát triển năng lực tƣ duy hóa học, năng lực phát hiện và giải quyết vấn đề của HS.
Chính vì vậy, việc xây dựng nên những BTHH mới là rất quan trọng và có ý nghĩa thiết thực.
OFFICIAL
1.1.3.2. Một số định hướng trong việc xây dựng bài tập hóa học mới - Xây dựng bài tập theo định hƣớng năng lực. Tăng cƣờng sử dụng bài tập trắc nghiệm khách quan. Xây dựng và tăng cƣờng sử dụng bài tập thực nghiệm định lƣợng.
- Loại bỏ những bài tập có nội dung hóa học nghèo nàn nhƣng lại cần đến những thuật toán phức tạp để giải. Loại bỏ những bài tập có nội dung lắt léo, giả định rắc rối, phức tạp, xa rời hoặc phi thực tiễn hóa học.
- Xây dựng bài tập mới để rèn luyện cho HS năng lực phát hiện vấn đề và giải quyết vấn đề, đặc biệt là các vấn đề liên quan đến thực tiễn trong tự nhiên và cuộc sống.
- Đa dạng hóa các loại hình bài tập nhƣ bài tập bằng hình vẽ, bài tập vẽ đồ thị, sơ đồ,… Xây dựng bài tập có nội dung hóa học phong phú, sâu sắc, phần tính toán đơn giản, nhẹ nhàng.
1.1.4. Tìm hiểu về chương trình đánh giá học sinh quốc tế PISA.
PISA là viết tắt của “Programme for International Student Assessment –Chƣơng trình quốc tế đánh giá kết quả học tập của HS” do Tổ chức hợp tác và phát triển kinh tế (OECD) khởi xƣớng và chỉ đạo.
1.1.4.1. Đặc điểm của PISA
Quy mô của PISA rất lớn và có tính toàn cầu. Qua 5 cuộc khảo sát đánh giá, ngoài các nƣớc thuộc khối OECD còn có rất nhiều quốc gia là đối tác của khối OECD đăng ký tham gia.
PISA đƣợc thực hiện đều đặn theo chu kì (3 năm/1 lần) tạo điều kiện cho các quốc gia có thể theo dõi sự tiến bộ của nền giáo dục đối với việc phấn đấu đạt đƣợc các mục tiêu giáo dục cơ bản.
Cho tới nay PISA là cuộc khảo sát giáo dục duy nhất chỉ chuyên đánh giá về
DẠYKÈMQUYNHƠN
6
năng lực phổ thông của HS ở độ tuổi 15, độ tuổi kết thúc giáo dục bắt buộc ở hầu hết các quốc gia. Độ tuổi 15 ở hầu hết các nƣớc thành viên OECD tƣơng đƣơng kết thúc lớp 9 của Việt Nam.
PISA chú trọng xem xét và đánh giá một số vấn đề sau: Chính sách công; năng lực phổ thông; học tập suốt đời.
1.1.4.2. Mục tiêu đánh giá
Mục tiêu của chƣơng trình PISA tập trung vào đánh giá năng lực của HS khi đến độ tuổi 15. Đó là những kiến thức và kỹ năng tối cần thiết cho một HS bƣớc vào cuộc sống trƣởng thành. Và đó cũng là những kỹ năng và kiến thức nền tảng không thể thiếu cho quá trình học tập suốt đời của mỗi ngƣời.
1.1.4.3. Nội dung và đối tượng đánh giá.
- Nội dung đánh giá của PISA hoàn toàn đƣợc xác định dựa trên các kiến thức, kỹ năng cần thiết cho cuộc sống tƣơng lai, không dựa vào nội dung các chƣơng trình giáo dục quốc gia. Đây chính là điều mà PISA gọi là “năng lực phổ thông” (về làm toán, về khoa học, về đọc hiểu) – những năng lực cần thiết chuẩn bị cho cuộc sống trong một xã hội hiện đại.
OFFICIAL
- Đối tƣợng đánh giá: HS trong độ tuổi 15 (đƣợc định nghĩa chính xác là từ 15 tuổi 3 tháng đến 16 tuổi 2 tháng) đang theo học ở chƣơng trình phổ thông và giáo dục thƣờng xuyên.
1.1.4.4. Những năng lực chủ yếu theo hướng tiếp cận PISA.
* Năng lực Đọc hiểu.
Là năng lực hiểu, sử dụng và phản hồi lại ý kiến của một cá nhân sau khi đọc một văn bản. Khái niệm học và đặc biệt là học suốt đời đòi hỏi phải mở rộng cách hiểu về việc biết đọc. Biết đọc không chỉ còn là yêu cầu của suốt thời kì tuổi thơ trong nhà trƣờng phổ thông, thay vào đó nó còn trở thành một nhân tố quan trọng trong việc xây dựng, mở rộng những kiến thức cá nhân, kỹ năng và chiến lƣợc của mỗi cá nhân trong suốt cuộc đời khi họ tham gia vào các tình huống khác nhau cũng nhƣ trong mối quan hệ với ngƣời xung quanh.
Các câu hỏi đƣợc đánh giá ở 3 nhóm (cấp độ) sau: Thu thập thông tin; Phân tích, lý giải văn bản; Phản hồi và đánh giá.
* Năng lực Toán học.
Là năng lực của một cá nhân để nhận biết và hiểu về vai trò của toán học trong thế giới, biết dựa vào toán học để đƣa ra những suy đoán có nền tảng vững chắc vừa đáp ứng đƣợc các nhu cầu của đời sống cá nhân, vừa nhƣ một công dân biết suy luận, có mối quan tâm và có tính xây dựng. Đó chính là năng lực phân tích, lập luận và truyền đạt ý tƣởng (trao đổi thông tin) một cách hiệu quả thông qua việc đặt ra, hình thành, giải quyết vấn đề toán học trong các tình huống và hoàn cảnh khác nhau. Các câu hỏi đƣợc đánh giá ở 3 nhóm (cấp độ) sau: Tái hiện (lặp lại); Kết nối
DẠYKÈMQUYNHƠN
7
và tích hợp; Tƣ duy toán học, khái quát hóa và nắm đƣợc những tri thức toán học ẩn dấu bên trong các tình huống và các sự kiện.
* Năng lực Khoa học.
Là năng lực của một cá nhân biết sử dụng kiến thức khoa học để xác định các câu hỏi và rút ra kết luận dựa trên chứng cứ để hiểu và đƣa ra quyết định về thế giới tự nhiên thông qua hoạt động của con ngƣời thực hiện việc thay đổi thế giới tự nhiên. Cụ thểlà:
- Có kiến thức khoa học và sử dụng kiến thức để xác định các câu hỏi, chiếmlĩnh kiến thức mới, giải thích hiện tƣợng khoa học và rút ra kết luận trên cơ sở chứng cứ về các vấn đề liên quan đến khoa học.
- Hiểu những đặc tính của khoa học nhƣ một dạng tri thức của loài ngƣời và một hoạt động tìm tòi khám phá của con ngƣời.
- Nhận thức đƣợc vai trò của khoa học và công nghệ đối với việc hình thành môi trƣờng văn hóa, tinh thần, vật chất.
OFFICIAL
- Sẵn sàng tham gia nhƣ một công dân tích cực, vận dụng hiểu biết khoa học vào giải quyết các vấn đề liên quan tới khoa học.
Các câu hỏi đƣợc đánh giá ở 3 cấp độ sau: - Nhận biết các vấn đề khoa học: HS nhận biết các vấn đề mà có thể đƣợc khám phá một cách khoa học, nhận ra những nét đặc trƣng chủ yếu của việc nghiên cứu khoa học.
- Giải thích hiện tƣợng một cách khoa học: HS có thể áp dụng kiến thức khoa học vào tình huống đã cho, mô tả, giải thích hiện tƣợng một cách khoa học và dự đoán sự thay đổi. - Sử dụng các chứng cứ khoa học, lý giải các chứng cứ để rút ra kết luận. 1.2. Cơ sở thực tiễn. 1.2.1. Thực trạng nghiên cứu. 1.2.1.1. Về giáo viên. Qua việc tiến hành khảo sát tình hình thực tế một số trƣờng THPT ở huyện
Lộc chúng tôi thấy rõ thực trạng:
không biết hoặc biết rất ít về PISA và các vấn đề về lĩnh vực khoa học trongkỳthi PISA.
- GV sử dụng bài tập PISA ở mức độ còn ít, chƣa đa dạng và hiệu quả sử dụng chƣa cao, phổ biến nhất vẫn là những câu hỏi giải thích các hiện tƣợng thực tiễn.
- Chƣa khai thác triệt để các ứng dụng của hóa học trong thực tế và các vấn đề thực tiễn có liên quan đến kiến thức hóa học vào nội dung bài tập trong KTĐG nên tính thực tiễn của môn học chƣa cao.
DẠYKÈMQUYNHƠN
8
Nghi
- Nhiều GV
- Nhiều GV tiếp cận chƣơng trình hóa học phổ thông 2018 còn mờ nhạt; tâm thế, tinh thần chƣa thể hiện rõ.
1.2.1.2. Về học sinh.
Năng lực của mỗi HS là khác nhau. Một số HS khá, giỏi rất năng động, sáng tạo, tích cực học tập, tiếp thu bài tốt, tham gia nhiệt tình vào các hoạt động học tập. Ngƣợc lại HS yếu, kém lại rất lƣời học, tiếp thu bài học một cách thụ động. Có những BTHH tạo đƣợc nhiều hứng thú cho HS khá, giỏi, nhƣng số HS yếu, kém lại không đủ khả năng tham gia tích cực, ngƣợc lại có nhiều BTHH đƣợc sự hƣởng ứng nhiệt tình của những HS yếu, kém, nhƣng lại gây nhàm chán cho số HS khá, giỏi. Nhƣ vậy, để thiết kế và sử dụng BTHH theo hƣớng tiếp cận PISA trong dạy học và KT ĐG phù hợp với các đối tƣợng HS trong lớp là việc làm cần thiết và còn nhiều sự trăn trở của mỗi GV.
OFFICIAL
1.2.2. Yêu cầu của việc thiết kế và sử dụng hệ thống bài tập theo định hướng tiếp cận PISA trong dạy học nội dung “Tốc độ phản ứng hóa học và nhóm halogen – hóa học 10” chương trình giáo dục phổ thông 2018 nhằm phát triển năng lực cho HS.
1.2.2.1. Đối với giáo viên.
Phân tích nội dung “Tốc độ phản ứng hóa học và nhóm halogen - hóa học 10” và tìm ra những mối quan hệ giữa kiến thức của 2 nội dung này với những vấn đề thực tiễn, xảy ra trong cuộc sống cá nhân và cộng đồng.
Chuẩn bị cho mình vốn kiến thức rộng trên các lĩnh vực khác nhau, nắm vững những đổi mới trong chƣơng trình GDPT 2018, thực hiện học tập suốt đời.
Lựa chọn phƣơng pháp, phƣơng tiện phù hợp để phối hợp trong quá trình tổ chức các hoạt động học tập cũng nhƣ trong KTĐG HS. Hƣớng dẫn HS biết cách vận dụng những kiến thức đã học để tiếp thu kiến thức mới.
Nhƣ vậy việc xây dựng hệ thống bài tập theo định hƣớng tiếp cận PISA trong dạy học hóa học 10 ở nội dung “ Tốc độ phản ứng hóa học và nhóm halogen” chƣơng trình GDPT 2018 nhằm phát triển năng lực cho HS đòi hỏi ngƣời GV không chỉ có những kiến thức vững chắc về bộ môn hóa học, am hiểu về những vấn đề hóa học xảy ra trong thực tiễn mà còn phải nghiên cứu nắm bắt chƣơng trình mới.
1.2.2.2. Đối với học sinh.
BTHH là phƣơng tiện hữu hiệu để rèn luyện và phát triển tƣ duy của HS, giúp HS tái tạo kiến thức cũ, tìm ra mối liên hệ bản chất giữa các sự vật và hiện tƣợng, HS phải phân tích, phán đoán, suy luận để tìm ra lời giải.
HS tích cực tham gia các hoạt động trong quá trình học tập trên lớp theo yêu cầu của GV, từ đó các em sẽ lĩnh hội đƣợc kiến thức một cách chủ động đồng thời sẽ hình thành và phát triển các phẩmchất, năng lực cần thiết cho các em.
HS phải thƣờng xuyên ôn tập, bổ sung kiến thức cho bản thân thông qua sách báo, tài liệu, internet, kiến thức thực tiễn….
DẠYKÈMQUYNHƠN
9
CHƢƠNG 2.
XÂY DỰNG VÀ SỬ DỤNG HỆ THỐNG BÀI TẬP THEO ĐỊNH HƢỚNG TIẾP CẬN PISA TRONG DẠY HỌC NỘI DUNG “TỐC ĐỘ PHẢN ỨNG
HÓA HỌC VÀ NHÓM HALOGEN - HÓA HỌC 10” CHƢƠNG TRÌNH GIÁO DỤC PHỔ THÔNG 2018 NHẰM PHÁT TRIỂN NĂNG LỰC CHO HỌC SINH
2.1. Tổng quan môn hóa học 10 theo chƣơng trình GDPT 2018. Các nội dung khái quát hóa học 10 trong chƣơng trình GDPT 2018, bao gồm:
Mạch nội dung kiến thức cốt lõi :
Kiến thức cơ sở hóa học chung:
+ Cấu tạo nguyên tử.
+ Bảng tuần hoàn các nguyên tố hoá học.
+ Liên kết hoá học.
+ Năng lƣợng hoá học.
+ Tốc độ phản ứng hoá học.
+ Phản ứng oxi hoá – khử.
Hóa học vô cơ: Nguyên tố nhóm VIIA.
Nội dung các chuyên đề học tập.
+ Chuyên đề 10.1. Cơ sở hoá học.
+ Chuyên đề 10.3. Thực hành: Hoá học và công nghệ thông tin.
+ Chuyên đề 10.2. Hoá học trong việc phòng chống cháy nổ
2.2. Bài tập theo hƣớng tiếp cận PISA.
2.2.1. Đặc điểm của bài tập theo hướng tiếp cận PISA.
- Mỗi bài tập đƣợc thiết kế dƣới dạng một chủ đề (một vấn đề liên quan đến một hoặc một vài tình huống và ngữ cảnh). Một chủ đề gồm:
+ Tiêu đề.
+ Phần dẫn các dữ kiện của câu hỏi. + Câu hỏi bao gồm: phần thân câu hỏi, mục đích câu hỏi và cách chấm (những yêu cầu HS phải trả lời đƣợc và thang điểm chấm).
- Dựa trên các tình huống của đời sống thực và không chỉ giới hạn bởi cuộc sống thƣờng ngày của các em. Các tình huống đƣợc lựa chọn không chỉ để HS thực hiện các thao tác về tƣ duy mà còn để HS ý thức về các vấn đề xã hội. - Dữ liệu đƣợc sử dụng để xây dựng bài tập rất đa dạng, chẳng hạn nhƣ: biểuđồ, tranh ảnh quảng cáo, văn bản, bài báo…
DẠYKÈMQUYNHƠN
10
OFFICIAL
- Dạng thức của câu hỏi rất đa dạng, không chỉ bao gồm các câu hỏi lựa chọnđáp án mà còn yêu cầu HS tự xây dựng nên đáp án của mình. Các kiểu câu hỏi đƣợc sử dụng trong bài tập theo hƣớng tiếp cận PISA:
+ Câu hỏi TNKQ nhiều lựa chọn kiểu đơn giản.
+ Câu hỏi Có/ Không hoặc Đúng/ Sai phức hợp.
+ Câu hỏi mở đòi hỏi trả lời ngắn.
+ Câu hỏi mở đòi hỏi trả lời dài.
+ Câu hỏi đóng đòi hỏi trả lời (dựa trên những câu trả lời có sẵn).
+ Câu hỏi yêu cầu vẽ đồ thị, biểu đồ.
+ Câu hỏi yêu cầu HS dùng lập luận để thể hiện việc đồng tình hay bác bỏ một nhận định.
+ Câu hỏi liên quan đến việc HS phải đọc và trích rút thông tin từ biểu đồ, sơ đồ, hình vẽ để trả lời câu hỏi.
OFFICIAL
- Câu trả lời của HS đƣợc quy ra các mức độ ứng với điểm số khác nhau: mức đầy đủ; mức chƣa đầy đủ và mức không tính điểm.
- Bài tập đƣợc thiết kế nhằm mục đích sử dụng để phát triển và đánh giá năng lực (Đọc hiểu, Khoa học, Toán học…) của HS.
2.2.2. Các yêu cầu đối với bài tập theo hướng tiếp cận PISA.
Câu hỏi trong bài tập theo hƣớng tiếp cận PISA cần đáp ứng các yêu cầu sau:
- Tính xác thực: nội dung câu hỏi đƣợc lấy từ thế giới thực, phù hợp với trìnhđộ HS.
- Mức độ đọc hiểu: câu hỏi ngắn gọn, rõ ràng, mạch lạc. Mức độ đọc hiểu tài liệu nên đƣợc xem xét một cách cẩn thận. Những tài liệu đề xuất dài hơn phải đƣợc phân chia một cách logic thành các mục nhỏ trong đó chứa một hoặc hai câu hỏi.
Một câu hỏi trắc nghiệmkhách quan đạt yêu cầu cần đáp ứng cáctiêu chí sau:
+ Khung hoặc cấu trúc rõ ràng (theo khung năng lực PISA). + Phần dẫn đƣợc khuyến khích đề cập đến khái niệm, kiến thức, quy trình đƣợcđánh giá (tính chất xác thực mức độ cao).
+ Các phƣơng án nhiễu phải đáng tin cậy đối với những HS “không biết”.
+ Các tuỳ chọn (câu trả lời và phƣơng án nhiễu) không đƣa ra những gợi ý không liên quan để chấp nhận hoặc từ chối.
Khi soạn câu hỏi tự luận trả lời mở cần xem xét các vấn đề sau:
+ Khái niệm khoa học, tổng hợp các khái niệm, phân tích hoặc quy trình nào mà nội dung yêu cầu?
DẠYKÈMQUYNHƠN
11
+ Có nằm trong khung năng lực của PISA hay không?
+ Có thể xây dựng câu hỏi rõ ràng, không mập mờ không?
+ Câu trả lời nào đƣợc mong đợi ở HS từ câu hỏi này?
2.2.3. Nguyên tắc thiết kế bài tập theo hướng tiếp cận PISA.
Khi thiết kế BTHH nhằm phát triển năng lực HS theo hƣớng tiếp cận PISA cần đảm bảo các nguyên tắc sau:
a. Nội dung bài tập phải bám sát mục tiêu môn học.
Khi thiết kế bài tập cần phải lấy mục tiêu môn học làm cơ sở. Bài tập còn phải phù hợp với nội dung học của HS và lứa tuổi.
Khi thiết kế bài tập cần chú ý đến khả năng sử dụng để đánh giá năng lực học tập của HS trong từng bài tập cụ thể và trong toàn hệ thống bài tập.
OFFICIAL
b. Nội dung bài tập phải đảm bảo tính chính xác, tính khoa học và hiện đại. Nguồn thông tin, nội dung kiến thức trong bài tập cần đảm bảo tính chính xác, tính khoa học và phải đƣợc cập nhật thƣờng xuyên để HS đạt đƣợc chuẩn kiến thức, kỹ năng phù hợp với thời cuộc.
Sự kiện, sự việc trong thực tế, từ báo, tạp chí, sách, internet… nhƣng phải đáng tin cậy; thích hợp với các nền văn hóa của các dân tộc và ngôn ngữ
c. Nội dung bài tập phải đảm bảo tính logic và hệ thống.
Các bài tập đƣợc thiết kế theo các mức độ từ dễ đến khó phù hợp với trình độ của HS.
d. Nội dung bài tập phải đảm bảo tính thực tiễn.
BTHH cần buộc ngƣời học phải vận dụng các kiến thức đã biết hoặc các kinh nghiệm thực tiễn, sử dụng các hành động trí tuệ hay hành động thực tiễn để giải quyết các nhiệm vụ đó nhằm chiếm lĩnh tri thức, kỹ năng một cách tích cực, hứng thú và sáng tạo.
e. Các loại hình câu hỏi cần được đa dạng hóa.
Các BTHH đƣợc thiết kế dƣới hình thức tự luận hoặc trắc nghiệm với nhiều thông tin, nhiều hình ảnh, bảng biểu, câu hỏi mở, câu hỏi đóng.
f. Nội dung bài tập phải nhằm hình thành và phát triển các năng lực Đọchiểu, Khoa học, Toán học cho HS.
Thông qua nội dung bài tập, các năng lực đặc trƣng theo hƣớng tiếp cận PISA (năng lực Đọc hiểu, năng lực Khoa học, năng lực Toán học) đƣợc hình thành và phát triển.
2.2.4. Quy trình thiết kế bài tập theo hướng tiếp cận PISA.
Bước 1: Lựa chọn đơn vị kiến thức, xác định nội dung kiến thức.
DẠYKÈMQUYNHƠN
12
Với những định hƣớng đổi mới trong dạy học cũng nhƣ trong kiểm tra đánh giámôn Hóa học ở trƣờng THPT và phát huy những điểm tích cực của PISA cần lựa chọn những đơn vị kiến thức không chỉ có ý nghĩa về mặt hóa học mà còn gắn liền với thực tiễn, với đời sống của cá nhân, cộng đồng, các vấn đề xã hội, môi trƣờng,...và phát huy đƣợc óc tƣ duy, sáng tạo,... các năng lực của HS nhƣ: năng lực khoa học, năng lực phát hiện và giải quyết vấn đề, năng lực tự học, năng lực giải bài tập PISA,... nhƣng không quá trừu tƣợng, làm mất đi bản chất hóa học.
Bước 2: Xác định các năng lực cần hình thành và phát triển cho HS.
Sau khi lựa chọn đƣợc đơn vị kiến thức, GV xác định các năng lực tƣơng ứng cần hình thành và phát triển cho HS.
Mỗi bài tập PISA cần có ngữ cảnh đi kèm. Ngữ cảnh đƣợc thiết kế theo các bối cảnh, tình huống trong cuộc sống có liên quan đến nội dung kiến thức đang học.
Bước 3: Lựa chọn các kiểu câu hỏi theo hướng tiếp cận PISA.
OFFICIAL
Tùy theo từng đơn vị kiến thức, ngữ cảnh có thể lựa chọn các kiểu câu hỏi theo hƣớng tiếp cận PISA cho phù hợp. Việc sử dụng đa dạng các dạng câu hỏi theo hƣớng tiếp cận PISA sẽ góp phần phát triển năng lực đối với mỗi HS.
Bước 4: Thiết kế hệ thống bài tập.
Từ các BTHH và các bài tập của PISA đã có, cũng nhƣ các ý tƣởng, nội dung kiến thức hóa học, thiết kế hệ thống BTHH theo các hƣớng nhƣ:
Xây dựng các bài tập tương tự các bài tập đã có.
– Giữ nguyên hiện tƣợng và chất tham gia phản ứng, chỉ thay đổi lƣợng chất.
– Giữ nguyên hiện tƣợng và thay đổi chất tham gia phản ứng.
– Thay đổi các hiện tƣợng phản ứng và chất phản ứng, chỉ giữ lại những dạng phƣơng trình hóa học cơ bản.
– Từ một bài toán ban đầu, ta có thể đảo cách hỏi giá trị của các đại lƣợng đãcho nhƣ: khối lƣợng, số mol, thể tích, nồng độ,...
– Thay các số liệu bằng chữ để tính tổng tổng quát. – Chọn những chi tiết hay ở các bài tập để phối hợp lại thành bài mới. Xây dựng bài tập hoàn toàn mới.
Thông thƣờng, có hai cách xây dựng bài tập mới là: Dựa vào tính chất hóa học và các quy luật tƣơng tác giữa các chất để đặt ra bài tập mới hay lấy những ý tƣởng, nội dung, những tình huống hay và quan trọng ở nhiều bài, thay đổi nội dung, cách hỏi, số liệu,... để phối hợp lại thành bài mới.
Bước 5: Thiết kế đáp án trả lời của bài tập.
Đáp án của bài tập theo hƣớng PISA đƣợc thiết kế ở các mức độ khác nhau: mức đầy đủ, mức chƣa đầy đủ và mức không tính điểm.
DẠYKÈMQUYNHƠN
13
Bước 6: Kiểm tra thử.

Thử nghiệm áp dụng BTHH theo hƣớng tiếp cận PISA đã thiết kế trên đối tƣợng HS thực nghiệm để kiểm tra hệ thống bài tập đã thiết kế về tính chính xác, khoa học, thực tế của kiến thức hóa học, toán học cũng nhƣ độ khó, tính ƣu việt… cũng nhƣ tính khả thi, khả năng áp dụng của bài tập.
Bước 7: Chỉnh sửa. Thay đổi, chỉnh sửa nội dung, số liệu, tình huống... trong bài tập sau khi đã cho kiểm tra thử sao cho hệ thống bài tập có tính chính xác, khoa học về mặt kiến thức, kỹ năng, có giá trị về mặt thực tế, và phù hợp với đối tƣợng HS, với mục tiêu kiểm tra – đánh giá, mục tiêu giáo dục của môn Hóa học ở trƣờng THPT.
Bước 8: Hoàn thiện hệ thống bài tập.
Các bài tập sau khi thiết kế theo các bƣớc trên sẽ đƣợc sắp xếp, hoàn thiện một cách khoa học.
OFFICIAL
2.3. Xây dựng hệ thống bài tập theo hƣớng tiếp cận PISA.
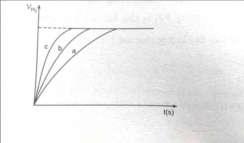
2.3.1. Bài tập tiếp cận PISA nội dung tốc độ phản ứng.
Bài tập PISA 1.
Thực hiện 3 thí nghiệm với những khối lƣợng Zn bằng nhau và với 50 cm3 dung dịch loãng H2SO4 2M. Bảng dƣới đây cho biết các điều kiện của mỗi thí nghiệm: Thí nghiệm Zn Nhiệt độ (oC) 1 Bột 30 2 Lá 20 3 Lá 30 Khí H2 thu đƣợc trong mỗi thí nghiệm đƣợc ghi lại theo những khoảng cách nhất định về thời gian cho đến khi phản ứng kết thúc, đƣợc biểu diễn bằng đồ thị sau:
DẠYKÈMQUYNHƠN
14
Câu 1: Các thí nghiệm trên đề cập đến những yếu tố ảnh hưởng đến tốc độ phản ứng nào?
A. Nồng độ, nhiệt độ, áp suất.
B. Nồng độ, nhiệt độ, diện tích tiếp xúc.
C. Nồng độ, áp suất, diện tích tiếp xúc.
D. Áp suất, nhiệt độ, diện tích tiếp xúc.
Câu 2: Dự đoán hiện tượng xảy ra khi so sánh giữa thí nghiệm 1 với 3 và thí nghiệm 2 với 3 và nêu nguyên nhân?
Câu 3: Quan sát đồ thị và cho biết các đường cong a,b,c biểu thị cho những thí nghiệm nào?
Hƣớng dẫn đánh giá bài tập PISA 1.
OFFICIAL
Câu 1: - Mức đầy đủ: HS chọn đáp án B và giải thích đƣợc sự lựa chọn: Khối lƣợng Zn lấy bằng nhau để tránh sự ảnh hƣởng về lƣợng Zn (nồng độ) trong các thí nghiệm; Zn ở các dạng bột hay lá để nói về ảnh hƣởng của diện tích tiếp xúc đối với tốc độ phản ứng; thí nghiệm ở các nhiệt độ khác nhau để nói về ảnh hƣởng của nhiệt độ đến tốc độ phản ứng. - Mức chưa đầy đủ: HS chọn các đáp án khác và giải thích đƣợc hai yếu tố đúng trong ba yếu tố nồng độ, nhiệt độ, diện tích tiếp xúc trong các đáp án đó.
- Không đạt: HS chọn sai và chỉ giải thích đƣợc một yếu tố đúng trong ba yếu tố nồng độ, nhiệt độ, diện tích tiếp xúc trong các đáp án đó hoặc giải thích sai. Câu 2: - Mức đầy đủ: HS nêu đƣợc. + Giữa thí nghiệm 1 và 3 thì khí H2 thoát ra ở thí nghiệm 1 nhanh và nhiều hơn vì tuy cùng nhiệt độ, khối lƣợng Zn nhƣng khác về hình thức của Zn. Khi Zn ở dạng bột thì diện tích bề mặt lớn hơn so với dạng lá, do đó phản ứng ở thí nghiệm 1 xảy ra nhanh hơn và khí H2 thoát ra nhanh và nhiều hơn trong cùng đơn vị thời gian so với thí nghiệm 3.
+ Giữa thí nghiệm 2 và 3 thì khí H2 thoát ra ở thí nghiệm 3 nhanh và nhiều hơn vì tuy cùng dạng bột, khối lƣợng Zn nhƣng khác về nhiệt độ của phản ứng. Khi nhiệt độ của phản ứng cao hơn thì tốc độ phản ứng sẽ lớn hơn, do đó phản ứng ở thí nghiệm 3 xảy ra nhanh hơn và khí H2 thoát ra nhanh và nhiều hơn trong cùng đơn vị thời gian so với thí nghiệm 2. - Mức chưa đầy đủ: HS chỉ nêu đƣợc.
+ So sánh đƣợc thí nghiệm 1 với 3 và 2 với 3 và nêu đƣợc nguyên nhân của 1 cặp thí nghiệm.
DẠYKÈMQUYNHƠN
15
+ Hoặc so sánh đƣợc một trong 2 cặp thí nghiệm và nêu đƣợc nguyên nhân của 2 cặp thí nghiệm.
- Không đạt: Chỉ so sánh và nêu đƣợc nguyên nhân của một cặp thí nghiệm hoặc không nêu hoặc nêu sai.
Câu 3: - Mức đầy đủ: Chỉ rõ đƣợc đƣờng cong a của thí nghiệm 2, đƣờng cong b của thí nghiệm 3, đƣờng cong c của thí nghiệm 1.

OFFICIAL
Giải thích: Giữa thí nghiệm 1 và 3 thì khí H2 thoát ra ở thí nghiệm 1 nhanh và nhiều hơn trong cùng đơn vị thời gian vì tuy cùng nhiệt độ, khối lƣợng Zn nhƣng Znở thí nghiệm 1 dạng bột có diện tích bề mặt lớn hơn so với dạng lá và giữa thí nghiệm 2 và 3 thì khí H2 thoát ra ở thí nghiệm 3 nhanh và nhiều hơn trong cùng đơn vị thời gian vì tuy cùng dạng bột, khối lƣợng Zn nhƣng nhiệt độ của phản ứng ở thí nghiệm 3 cao hơn thí nghiệm 2 thì tốc độ phản ứng sẽ lớn hơn. Vậy ta có tốc độ phản ứng của các thí nghiệm tăng dần lần lƣợt: 2 < 3 < 1 và khí H2 thoát ra trong cùng đơn vị thời gian cũng tăng tƣơng tự theo các thí nghiệm 2 < 3 < 1.
- Mức chưa đầy đủ: HS chỉ rõ đƣợc các đƣờng cong ứng với các thí nghiệm và giải thích đƣợc ít nhất một sự lựa chọn đƣờng cong.
- Không đạt:
+ HS chỉ rõ đƣợc các đƣờng cong ứng với các thí nghiệm nhƣng giải thích sai.
+ Hoặc HS chỉ chọn đƣợc một thí nghiệm với đƣờng cong và giải thích đƣợc sự lựa chọn đó.
+ Hoặc chọn sai và giải thích sai hoặc không trả lời.
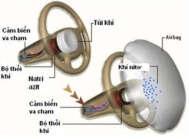
Bài tập PISA 2: TÚI KHÍ ÔTÔ
Trong xe ôtô có hệ thống bảo vệ bằng túi khí khi xe có sự va chạm, giúp bảo vệ mọi ngƣời trên xe tránh những chấn thƣơng nặng.
Khi xe bị tai nạn, những va chạm đột ngột sẽ đƣợc ghi nhận bởi 1 bộ cảm ứng, từ đó các quá trình đã diễn ra một cách cực kỳ nhanh chóng trong túi khí (car airbag). Khi đó túi khí bung ra sẽ tránh cho ngƣời lái xe những va chạm trực tiếp vào các bộ phận phía trƣớc xe và hầu hết các trƣờng hợp là giúp họ tránh khỏi những chấn thƣơng mạnh, thậm chí là cái chết thảm khốc. Trong thiết bị car airbag, hóa chất đƣợc dùng là NaN3, KNO3 và SiO2. Ban đầu, bộ cảm ứng kích thích bằng nhiệt đƣợc khơi mào khi có va chạm, NaN3 phân hủy cực nhanh tạo khí N2. Tiếp đó, nhƣ đã biết Na là kim loại hoạt động mạnh và
DẠYKÈMQUYNHƠN
16
có khả năng nổ, ngƣời ta sử dụng KNO3 và SiO2 nhƣ là chất để ngăn cản sự gây hại từ Na bằng cách tạo thành Na2O rồi tạo thành K2SiO3, Na2SiO3 và cả khí N2. Khí này bơm căng túi khí để giảm tác động lên ngƣời trên xe đồng thời ngay lập tức thoát ra ở các lỗ xả phía sau túi khí. Điều này làm giảm lực tác động lên túi khí và cũng đảm bảo cho ngƣời lái có một khoảng trống cần thiết để quan sát. Toàn bộ phản ứng tạo N2 làm căng túi khí diễn ra một cách rất nhanh và có thể mô tả bằng 3 giai đoạn:
OFFICIAL
azide (NaN3) là hợp chất ion và tan tốt trong nƣớc. Sodium azide (NaN3)còn dùng trong dù cứu hộ cho máy bay. Sodium azide(NaN3) rất độc. Ăn vào trực tiếp qua chất rắn hay qua chất lỏng có thể đƣa đến các triệu chứng sau đây chỉ sau một vài phút: thở nhanh, bồn chồn, hoa mắt, chóng mặt, ngƣời trở nên suy yếu, đau đầu, buồn nôn và nôn mửa, tim đập nhanh, mắt đỏ, chảy nƣớc mũi, ho, bỏng da (chạm trực tiếp). Phơi nhiễm một lƣợng lớn Sodium azide (NaN3) có thể gây nên các ảnh hƣởng khác nhƣ: co giật, huyết áp hạ, mất ý thức, tổn thƣơng phổi, suy hô hấp dẫn đến tử vong. Đó cũng là nguyên nhân ngộ độc khí trong một số tai nạn xe hơi gây chết ngƣời.
Câu 1: Trong nguyên lí hoạt động của túi khí đề cập tới yếu tố nào trong phản ứng?
Câu 2: Chỉ với NH3 có thể đủ tạo khí trong túi khí. Vì sao người ta còn dùng thêm chất KNO3 và SiO2? Hƣớng dẫn đánh giá bài tập PISA 2.
Câu 1: - Mức đầy đủ: HS trả lời đƣợc đề cập tới yế
DẠYKÈMQUYNHƠN
17
1.
→
+
2. 2. 2Na +
3 → K2O +
+
+ N2. 3. K2O + SiO2 → K2SiO3.
+
→
.
2NaN3
2Na
3N
2KNO
Na2O
2O2
Na2O
SiO2
Na2SiO3
Sodium
nhƣng chƣa giải
ở
- Không đạt: Không trả lời hoặc trả lờ
Câu 2: - Mức đầy đủ: + Sodium(Na)
u tố nhiệt độ. Khi có va chạm, bộ cảm ứng kích thích bằng nhiệt đƣợc khơi mào, lúc này dƣới tác dụng của nhiệt độ, Sodium azide(NaN3) phân hủy cực nhanh tạo khí N2 : 2NaN3 → 2Na + 3N2 - Mức chưa đầy đủ: HS trả lời đƣợc hoạt động của túi khí đề cập tới yếu tố nhiệt độ
thích đƣợc
giai đoạn nào.
i sai.
là chất dễ nổ, nên có Potassium nitrate (KNO3) để chuyển nó thành các oxide. Các oxide này đƣợc chuyển thành các muối Potassium siliconate (K2SiO3), Sodium siliconate (Na2SiO3) không gây hại.
+ Hạn chế đƣợc sự tồn tại của NH3 thoát ra ngoài.
- Mức chưa đầy đủ: HS nêu đƣợc 1 trong 2 ý trên.
- Không đạt: Không trả lời hoặc trả lời sai.
Bài tập PISA 3.
KHẢO SÁT CÁC YẾU TỐ ẢNH HƢỞNG TỚI TỐC ĐỘ PHẢN ỨNG.
Để tìm hiểu về các yếu tố ảnh hƣởng đến tốc độ phản ứng, ngƣời ta thực hiện thí nghiệm giữa Zn và dung dịch acid H2SO4 loãng. Bảng dƣới đây cho biết kết quả của 6 thí nghiệm xảy ra. Trong mỗi thí nghiệm, ngƣời ta dùng 0,3 gam Zn tác dụng với thể tích bằng nhau của acid, nhƣng có nồng độ khác nhau. Thí nghiệm Nồng độ acid Nhiệt độ (oC) Dạng của Zn Thời gian phản ứng (s)
OFFICIAL
Câu 1: Những thí nghiệm nào nói lên được sự ảnh hưởng của các yếu tố đến tốc độ phản ứng?
Câu 2: Từ các phản ứng trên, hãy giải thích sự ảnh hưởng của nhiệt độ tới tốc độ phản ứng?
Câu 3: Nếu song song với thí nghiệm 3, ta thực hiện một thí nghiệm 3* giống với thí nghiệm 3 nhưng chỉ thay đổi lượng acid dùng trong thí nghiệm 3* gấp đôi lượng acid dùng trong thí nghiệm 3. Nhận xét về tốc độ của 2 thí nghiệm và giải thích?
Hƣớng dẫn đánh giá bài tập PISA 3.
Câu 1: - Mức đầy đủ: HS khẳng định ởnhữ
DẠYKÈMQUYNHƠN
18
1 1M 25 Viên 220 2 1M 25 Bột 105 3 2M 25 Bột 92 4 2M 50 Viên 55 5 2M 50 Bột 30 6 3M 50 Bột 11
ta
. + Yếu tố nhiệt
+ Yếu tố
+ Yếu
- Mứ
ng thí nghiệmnày ngƣời
khảo sát 3 yếu tố
độ: Cặp thí nghiệm 3 và 5.
nồng độ: Cặp thí nghiệm 2 và 3; 5 và 6.
tố diện tích tiếp xúc: Cặp thí nghiệm 1 và 2; 4 và 5.
c chưa đầy đủ:
+ HS chỉ nêu đƣợc 2 trong 3 yếu tố, và nêu đƣợc đầy đủ các cặp thí nghiệm trong mỗi yếu tố.
+ Hoặc nêu đƣợc 3 yếu tố và có thể chỉ nêu 1 cặp thí nghiệm trong mỗi yếu tố.

- Không đạt:
+ HS chỉ nêu đƣợc 2 trong 3 yếu tố nhƣng không nêu đƣợc đầy đủ các cặp thí nghiệm trong mỗi yếu tố.
+ Hoặc HS nêu đƣợc 1 yếu tố hoặc không trả lời hoặc trả lời sai.
Câu 2:
- Mức đầy đủ: HS khẳng định đƣợc khi tăng nhiệt độ thì tốc độ phản ứng tăng. Giải thích dựa vào sự va chạm có hiệu quả của các phân tử chất phản ứng. Khi tăng nhiệt độ thì:
+ Tốc độ chuyển động của các phân tử tăng (hay động năng của các phân tử tăng) tần số va chạm giữa các phân tử chất phản ứng tăng.
OFFICIAL
+ Tần số va chạm có hiệu quả giữa các phân tử chất phản ứng tăng nhanh, tốc độ phản ứng tăng.
- Mức chưa đầy đủ: HS khẳng định đƣợc khi tăng nhiệt độ thì tốc độ phản ứng tăng và giải thích đƣợc khi tăng nhiệt độ thì các phân tử chất phản ứng hoạt động hơn làm tốc độ phản ứng tăng mà không nêu rõ đƣợc về sự va chạm có hiệu quả. - Không đạt: Chỉ khẳng định đƣợc khi tăng nhiệt độ thì tốc độ phản ứng tăng hoặc không trả lời hoặc trả lời sai.
Câu 3: - Mức đầy đủ: HS khẳng định là tốc độ ở cả 2 thí nghiệm là nhƣ nhau vì: Thể tích acid ở thí nghiệm 3* gấp đôi thể tích acid ở thí nghiệm 3 nhƣng nồng độ acid thì không thay đổi. Do đó mật độ acid trong dung dịch không thay đổi, tần số va chạm giữa các phân tử chất phản ứng không thay đổi, nên tốc độ phản ứng không thay đổi, hay tốc độ phản ứng nhƣ nhau ở 2 thí nghiệm.
DẠYKÈMQUYNHƠN
19
độ ở cả 2 thí nghiệm là nhƣ nhau nhƣng chƣa giải thích đƣợc nguyên
- Không đạt: Không trả lời hoặc trả lời sai. Bài tập PISA 4: ĐÈN XÌ OXYGEN – ACETYLENE Khí acetylene (C2H2) sinh ra khi cho Calcium carbide (CaC2) tác dụng với nƣớc đƣợc dùng làm nhiên liệu trong đèn xì oxygen – acetylene để hàn, cắt kim loại, do nhiệt độ ngọnlửa có thể lên đến 3000oC.
- Mức chưa đầy đủ: HS khẳng định là tốc
nhân.
Hàn, cắt kim loại bằng đèn xì oxygen – acetylene đƣợc sử dụng khi đóng mới hoặc sửa chữa các con tàu chạy trên sông, trên biển hay xây dựng, sửa chữa các cây cầu, các công trình xây dựng. Hay khi cần cắt, phá các con tàu bị hƣ hỏng để tận dụng sắt, thép cũ phục vụ cho ngành luyện cán thép ngƣời ta dùng đèn xì oxygen – acetylene.
Câu 1: Người ta dựa vào đâu để sử dụng đèn xì oxygen – acetylene để hàn cắt kim loại?
Câu 2: Hãy viết các phương trình biểu diễn quá trình hoạt động của đèn xì oxygen – acetylene?
Câu 3: Có thể thay đổi thành đèn xì acetylene hay không?
Hƣớng dẫn đánh giá bài tập PISA 4.
Câu 1:
- Mức đầy đủ: HS nêu đƣợc:
OFFICIAL
+ Dựa vào nhiệt độ ngọn lửa của phản ứng cháy giữa acetylene (C2H2) trong Oxygen (O2) có thể lên đến 3000oC của đèn xì oxygen - acetylene cao hơn nhiều so với cháy trong không khí.
+ Việc tạo ra khí acetylene (C2H2) đơn giản và từ những nguyên liệu phổ biến, ít tốn kém.
+ Oxygen trong phản ứng đốt cháy acetylene (C2H2) cũng là hóa chất phổ biến.
- Mức chưa đầy đủ: HS nêu đƣợc ngƣời ta dựa vào nhiệt độ ngọn lửa và một ý liên quan tới acetylene (C2H2) hoặc Oxygen (O2) đã nêu ở trên.
- Không đạt: Chỉ nêu đƣợc một ý hoặc không nêu hoặc nêu sai. Câu 2: - Mức đầy đủ: Tạo khí acetylene: CaC2 + 2H2O → C2H2 + Ca(OH)2 Khí acetylene tác dụng với Oxygen sinh nhiệt: 2C2H2+5O2 →4CO2+2H2O+ Q - Mức chưa đầy đủ: Chỉ nêu đƣợc phƣơng trình khí acetylene tác dụng với oxygen sinh ra nhiệt
DẠYKÈMQUYNHƠN
20
+
+
: 2C2H2 + 5O2 → 4CO2 + 2H2O + Q. - Không đạt:
Nêu đƣợc 2 phƣơng trình nhƣng thiếu sự tạo ra nhiệt lƣợng Q.
Hoặc phƣơng trình tạo khí acetylene: CaC2 + 2H2O →C2H2 + Ca(OH)2 + Hoặc không trả lời hoặc trả lời sai. Câu 3: - Mức đầy đủ: Câu trả lời là không, vì:
+ Trong đèn xì acetylene, oxygen nguyên chất có nồng độ cao hơn oxygen trong không khí. Nồng độ cao thì phản ứng xảy ra nhanh và mạnh, khi đó nhiệt lƣợng tạo ra cao và đủ tiêu chuẩn để thực hiện các công dụng của nó.
+ Còn đèn xì acetylene thì lúc này sử dụng oxygen không khí, nhƣ vậy nồng độ oxygen thấp hơn, phản ứng xảy ra không mạnh nhƣ đèn xì oxygen – acetylene dùng oxygen nguyên chất nên nhiệt lƣợng tạo ra không cao và không đủ tiêu chuẩn để thực hiện các công dụng của nó.
- Mức chưa đầy đủ: HS trả lời không và nêu đƣợc một trong hai ý trên.
- Không đạt: Chỉ nêu câu trả lời không mà không có giải thích hay giải thích sai hoặc không nêu hoặc nêu có.

Bài tập PISA 5:
NHIÊN LIỆU ĐUN NẤU.
OFFICIAL
Than Củi
Từ xƣa củi và than thƣờng đƣợc dùng làm nhiên liệu trong đun nấu và ngày nay vẫn còn sử dụng khá phổ biến.
Câu 1: Tại sao than lại thường được dùng làm nhiên liệu trong các gia đình?
Câu 2: Khi sử dụng than để sưởi ấm đã gây ra một số trường hợp bị chết ngạt. Hãy giải thích nguyên nhân và cách phòng tránh?
Câu 3: Vì sao khi đun nấu thường ở những nơi thoáng khí?
Câu 4: Vì sao thường chẻ nhỏ củi khi nấu?
Câu 5: Vì sao than không đập quá nhỏ nhưng cũng không để quá lớn khi đun nấu? Hƣớng dẫn đánh giá bài tập PISA 5. Câu 1:
HS nêu đƣợc ít nhất 2 ý trong các ý sau:
Ngọn lửa phát ra từ than rất mạnh.
Than phổ biến và rẻ, mỗi gia đình đều có khả năng mua và sử dụng than.
Than cháy với ngọn lửa vừa đều và vừa, không to nhƣ khi đun củi nên rất thích hợp với các món hầm, kho.
+ Than cũng là nguyên liệu rất tốt dùng để sƣởi ấm vào mùa lạnh, đặc biệt ở những vùng cao,...
- Mức chưa đầy đủ: Nêu đƣợc 1 ý.
- Không đạt: Không trả lời hoặc trả lời sai.
DẠYKÈMQUYNHƠN
21
-
Mức đầy đủ:
+
+
+
Câu 2: - Mức đầy đủ:
+ HS nêu đƣợc nguyên nhân: Khi đốt than trong phòng, than cháy sẽ đốt hết khí oxygen (O2), sinh ra khí carbon (IV) oxide (CO2) gây ngạt, ngộ độc cho ngƣời trong phòng. Than củi cháy trong điều kiện thiếu không khí sẽ tạo ra một loại khí cực độc là carbon (II) oxide (CO). Nạn nhân khi hít phải khí này nặng thì bị tử vong, nhẹ hơn thì để lại di chứng thần kinh – tâm thần. Để phòng kín khi sƣởi ấm, không có chỗ thông khí. + Cách phòng tránh: Trong quá trình sƣởi ấm không đƣợc để phòng kín. Có thể chọn những lò sƣởi, máy sƣởi có tính an toàn hơn.
OFFICIAL
- Mức chưa đầy đủ: HS nêu đƣợc ít nhất 1 nguyên nhân và 1 cách phòng tránh.
- Không đạt: Chỉ nêu nguyên nhân hoặc chỉ nêu cách phòng tránh hoặc không trả lời hoặc trả lời sai.
Câu 3:
- Mức đầy đủ: Cần nấu ở những nơi thoáng khí vì lúc đó lƣợng oxygen (O2) cung cấp đủ hoặc dƣ để củi, than cháy hoàn toàn. Tức là nồng độ oxygen (O2) lớn phản ứng sẽ xảy ra nhanh và hoàn toàn; Tránh sự tạo khí carbon (II) oxide (CO) gây độc; Tránh sự thiếu oxygen (O2) trong khi đun nấu.
- Mức chưa đầy đủ: Nói đƣợc ở những nơi thoáng khí thì nồng độ oxygen (O2) cao hơn và giúp củi, than cháy hoàn toàn.
- Không đạt: Không trả lời hoặc trả lời sai.
Câu 4:
- Mức đầy đủ: Giải thích đƣợc chẻ nhỏ củi sẽ làm tăng diện tích tiếp xúc của củi với oxygen (O2). Khi đó phản ứng sẽ xảy ra nhanh và hoàn toàn hơn. Tránh đƣợc hiện tƣợng sản sinh ra khí carbon (II) oxide (CO) gây độc.
- Mức chưa đầy đủ: Giải thích đƣợc chẻ nhỏ củi sẽ làm tăng diện tích tiếp xúc của củi với oxygen (O2).
- Không đạt: Không trả lời hoặc trả lời sai.
Câu 5:
- Mức đầy đủ: HS trả lời đầy đủ các ý sau:
+ Khi than đập quá nhỏ sẽ tạo ra vụn than. Do vậy diện tích tiếp xúc của oxygen (O2) với than chỉ là trên bề mặt bên trên. Oxygen (O2) khó len lỏi vào bên trong để phản ứng.
DẠYKÈMQUYNHƠN
22
+ Khi để quá lớn thì diện tích tiếp xúc với oxygen (O2) cũng kém do đó sự cháy của than sẽ chậm và không hoàn toàn. Dễ gây trƣờng hợp sản sinh ra carbon (II) oxide (CO) gây độc.
+ Khi kích thƣớc than vừa phải thì diện tích tiếp xúc với oxygen (O2) đủ lớn nên tốc độ cháy của than sẽ nhanh và hoàn toàn.

- Mức chưa đầy đủ: HS nêu đƣợc 2 trong 3 ý trên.
- Không đạt: Chỉ nêu đƣợc 1 ý hoặc không trả lời hoặc trả lời sai.
Bài tập PISA 6: NỒI ÁP SUẤT
Trƣớc đây, để có một nồi hầm xƣơng, giò heo hay gà luộc nguyên con thật ngon thì tốn rất nhiều thời gian, tốn kém về mặt nhiên liệu (củi, than, gas) và không phải lúc nào nồi hầm cũng chín tới và luôn ngon nhƣ mong muốn. Ngày nay, chuyện đó đã trở nên đơn giản hơn với nồi áp suất. Món ăn đƣợc chế biến với nồi áp suất sẽ rất nhanh và tiện lợi.
OFFICIAL

Nồi áp suất điện đa năng Sunhouse Sh1555
Khi sử dụng nồi áp suất cần đặc biệt lƣu ý van giảm áp. Khi van tắc, không thấy xì hơi, ngƣời sử dụng dễ lầm tƣởng áp suất trong nồi đã giảm, nếu vặn ra có thể gây nổ. Có thể kiểm tra van giảm áp bằng cách nhấp lên nhấp xuống, nếu thấy không đảm bảo thì phải thay mới. Lƣợng thức ăn cho vào nồi chỉ khoảng 2/3 dung tích nồi;với thức ăn có độ nở cao và sinh bọt nhƣ cháo, các loại đậu hoặc những thứ có nhiều nƣớc, lƣợng thực phẩm giới hạn là 1/3 dung tích. Đối với các thức ăn khác (thịt, cá) lƣợng thực phẩm không quá 3/4 dung tích nồi.
DẠYKÈMQUYNHƠN
23
1: Nồ
áp su
Câu 2: Hãy giải
ằ
ế
ứ
ọ
1.Tại sao khi đun nấu, lửa bật to thì thực phẩm nhanh chín? 2.Tại sao khi nấu các món củ mà muốn nhanh chín thì xắt nhỏ hoặc thái mỏng? 3.Tại sao cần nấu ăn ở nơi thông
Câu
i
ất hoạt động dựa trên cơ sở hóa học nào?
thích các mẹo vặt trong nấu nướng b
ng ki
n th
c hóa h
c?
thoáng?
Hƣớng dẫn đánh giá bài tập PISA 6.
Câu 1:
- Mức đầy đủ: Dựa trên yếu tố áp suất ảnh hƣởng tới tốc độ phản ứng. Với áp suất cao thì tốc độ phản ứng tăng nhanh, làm cho thực phẩm nhanh chín hơn.
- Mức chưa đầy đủ: Nói đƣợc dựa trên yếu tố áp suất.
- Không đạt: Không trả lời hoặc trả lời sai.
Câu 2: - Mức đầy đủ: HS trả lời đƣợc tất cả các ý trên nhƣ sau:
1.Cung cấp nhiệt độ cao, tăng nhiệt độ thì phản ứng xảy ra nhanh nên thực phẩm nhanh chín.


OFFICIAL
2.Tăng diện tích tiếp xúc sẽ tăng tốc độ phản ứng và thực phẩm nhanh chín. Nấu ăn ở nơi thông thoáng giúp cung cấp đủ lƣợng oxygen cho quá trình nấu, hay tăng nồng độ oxygen, khi đó phản ứng xảy ra nhanh và thực phẩm nhanh chín. Ngoài ra, nấu ăn ở nơi thông thoáng giúp cho một số khí sinh ra trong quá trình nấu đƣợc thoát tốt hơn, không gây độc và ô nhiễm tới con ngƣời.
- Mức chưa đầy đủ: Trả lời đƣợc ít nhất 1 trong 3 ý trên.
- Không đạt: Không trả lời hoặc trả lời sai.


2.3.2. Bài tập tiếp cận PISA nội dung halogen và hợp chất.
Bài tập PISA 7: VŨ KHÍ HÓA HỌC.
Tháng 4 năm 1915, vào một ngày trời râm mát, binh sĩ liên quân Anh- Pháp đang đồn trú dƣới chiến hào, chiến trƣờng hoàn toàn yên tĩnh. Đột nhiên từ phía quân Đức, một vùng chất khí màu vàng lục nhƣ một màng yêu khí tràn tới theo gió bay về phía quân Anh- Pháp. Trong chiến hào vang lên tiếng ho, tiếng gào thét của các binh sĩ. Đó là lần đầu tiên khí độc đƣợc sử dụng trong chiến tranh đại chiến, từ đó mở màn cho cuộc chiến tranh hóa học. Thời gian gần đây từ tháng 4 năm 2014 đến tháng 1 năm 2015 nhóm cực đoan Nhà nƣớc Hồi giáo (IS) đã 3 lần sử dụng bom có chứa khí này trong các lần giao tranh tại Iraq.
DẠYKÈMQUYNHƠN
24
Bom của phiến quân IS
Lính NATO đeo mặt nạ phòng độc
Để đối phó với các loại vũ khí hóa học, các nhà khoa học phải tiến hành nghiên cứu trong thời gian dài và tìm ra đƣợc dụng cụ có khả năng phòng độc làm từ than hoạt tính.
Câu 1: Chất khí màu vàng lục đã tràn tới phía quân Anh - Pháp trong đoạn trích trên là khí gì?
A. Khí Hydrogen sulfide (H2S).
B. Khí của chất độc màu da cam mà sau này Mỹ đã dùng nó để thả xuống rừng của Việt Nam.
C. Khí Chlorine (Cl2).
D. Khí Nitrogen(IV)oxide (NO2).
Câu 2: Trên cơ sở nắm đƣợc nội dung đoạn trích, hãy lựa chọn Đúng/ Sai cho các ý sau:
Vũ khí hóa học
1. Thƣờng đƣợc dùng là các chất độc có thể đe dọa tính mạng của con ngƣời.
OFFICIAL
2. Đƣợc liên hợp quốc cho phép các nƣớc trên thế giới sử dụng để bảo vệ độc lập tự do cho tổ quốc.
3. Than hoạt tính dùng làm mặt nạ chống độc có tính oxi hóa mạnh dễ phản ứng với tất cả các khí làm vũ khí hóa học.
Đúng/ sai
Câu 3: Hãy giải thích tác dụng của than hoạt tính trong khả năng chống độc.
Hƣớng đẫn đánh giá bài tập PISA 7.
Câu 1: Câu hỏi trắc nghiệm khách quan kiểu đơn giản, mức độ 1.
- Mức đầy đủ: Đáp án C.
- Mức không đạt: Câu trả lời sai ; không trả lời.
Câu 2: Câu hỏi Đúng/sai phức hợp, mức độ 2. - Mức đầy đủ: (1)Đ, (2)S, (3)S. - Mức chưa đầy đủ: Trả lời đúng 2 ý. - Mức không đạt: Câu trả lời 1 ý hoặc sai; không trả lời.
Câu 3: Câu hỏi mở trả lời ngắn, mức độ 3.
- Mức đầy đủ: HS trả lời đúng tác dụng của than hoạt tính: Than hoạt tính đƣợc làm từ các vật liệu chứa nhiều các bon nhƣ gỗ vỏ dừa…đem đốt ở nhiệt độ cao trong điều kiện thiếu oxygen để tạo thành than gỗ, qua quá trình xử lý than gỗ tạo thành than hoạt tính.
Than hoạt tính thƣờng có dạng hạt nhỏ hoặc chất bột màu đen, có diện tích bề mặt rất lớn. Khi than hoạt tính tiếp xúc với các các chất, do diện tích bề mặt lớn nên
DẠYKÈMQUYNHƠN
25
than hoạt tính có thể hấp thụ trên bề mặt nhiều loại phân tử, hoặc có thể tác dụng với chất độc (thƣờng là các chất oxi hóa mạnh) để giảmthiểu hàm lƣợng chất độc.
- Mức chưa đầy đủ: Trả lời đúng một số ý nhƣng chƣa đầy đủ nhƣ ý trên.
Mức không đạt: Câu trả sai hoặc có cách hiểu lệch lạc; không trả lời.
Bài

tập PISA 8: THÍ NGHIỆM ĐIỀU
OFFICIAL
CHẾ KHÍ CHLORINE
Dƣới đây là một sơ đồ điều chế chlorine trong phòng thí nghiệm : Sơ đồ điều chế Chlorine trong phòng thí nghiệm

Câu 1: Viết phƣơng trình phản ứng xảy ra khi tiến hành điều chế chlorine theo sơ đồ trên.
Câu 2: Trên cơ sở hiểu đƣợc sơ đồ thí nghiệm, hãy lựa chọn Đúng/ Sai cho các ý sau: Phát biểu Đúng/ sai
DẠYKÈMQUYNHƠN
26
1. Có
2 ở
2. Bình
ng
ị
Cl2 3. Bình
4.
tại bình tam giác để dùng thu khí Cl2 còn thiếu cái gì? Đặt ở đâu? Câu 4: Nếu dùng KMnO4 để thay cho MnO2 ở thí nghiệm trên thì Cl2 thu đƣợc thƣờng có lẫn thêm khí gì? Giải thích và viết phƣơng trình phản ứng. Hƣớng dẫn đánh giá bài tập PISA 8. Câu 1: Câu hỏi mở trả lời ngắn. - Mức đầy đủ: Viết đúng phƣơng trình phản ứng
thể thay MnO
thí nghiệm trên bằng KMnO4.
đự
dung d
ch NaCl có tác dụng sinh thêm khí
đựng H2SO4 đặc có tác dụng hấp thụ hơi nƣớc.
Khí Cl2 sinh ra có thể thu bằng phƣơng pháp đẩy nƣớc. Câu 3: Để thật sự an toàn trong thí nghiệm thì
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O.
- Mức không đạt: Câu trả lời sai ; không trả lời.
Câu 2: Câu hỏi Đúng/sai phức hợp.
- Mức đầy đủ: (1)Đ, (2)S, (3)Đ, (4)S.


- Mức chưa đầy đủ: Trả lời đúng 2 ý.
- Mức không đạt: Câu trả lời 1 ý hoặc sai; không trả lời.
Câu 3: Câu hỏi mở trả lời ngắn.
- Mức đầy đủ: HS trả lời đƣợc tại bình tam giác dùng thu khí Cl2 còn thiếu bông tẩm NaOH để ngăn chặn Cl2 tràn ra.
- Mức chưa đầy đủ: Trả lời thiếu dụng cụ thu khí Cl2 thừa, hoặc trả lời thiếu nắp đậy bằng cao su.
- Mức không đạt: Câu trả lời sai ; không trả lời.
OFFICIAL
Câu 4: Câu hỏi mở trả lời ngắn.
- Mức đầy đủ: HS trả lời đƣợc nguyên nhân do trong quá trình điều chế có dùng đèn cồn nên cung cấp nhiệt độ vì thế xảy ra thêm phản ứng nhiệt phân KMnO4. 2KMnO4 → K2MnO4 + MnO2 + O2.
Phản ứng trên sinh ra O2 nên trong sản phẩm thu đƣợc có thể lẫn khí O2
- Mức chưa đầy đủ: Trả lời sản phẩm thu đƣợc có lẫn khí O2 nhƣng không giải thích đƣợc đầy đủ. - Mức không đạt: Câu trả lời sai ; không trả lời. Bài tập PISA 9: KHẮC CHỮ VẼ HÌNH TRÊN THỦY TINH. Thủy tinh là loại chất liệu dùng để làm rất nhiều đồ dùng trong cuộc sống con ngƣời, thủy tinh có bề mặt rất nhẵn, việc vẽ hình khắc chữ trên thủy tinh là rất khó nếu chúng ta dùng tay, vẽ bằng bút hay phun sơn. Tuy nhiên trên thực tế có rất nhiều vật dụng bằng thủy tinh đƣợc khắc chữ và vẽ hình rất công phu, việc làm này thành công là nhờ trợ giúp của một chất hóa học. Câu hỏi: Chất nào dùng để khắc chữ và hình trên vật liệu thủy tinh? Hƣớng dẫn đánh giá bài tập PISA 9. - Mức đầy đủ: Giải thích đúng và đầy đủ : Acid hydrofluoric (HF) hòa tan dễ dàng Silicon dioxide (SiO2) theo phƣơng trình: SiO2 + 4HF → SiF4↑ + 2H2O.
DẠYKÈMQUYNHƠN
27
Nhờ tính chất này nên Acid hydrofluoric (HF) đƣợc dùng để khắc chữ hoặc các họa tiết trên thủy tinh. Do đó ta có thể trang trí trên thủy tinh nhƣ ý muốn .
- Mức chưa đầy đủ: chỉ nêu đƣợc chất dùng để khắc chữ là Acid hydrofluoric (HF) chứ không giải thích đƣợc vì sao.
- Mức không đạt: Trả lời sai không có câu trả lời.
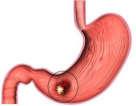
Bài tập PISA 10: VAI TRÕ CỦA HYDROCHLORIC ACID VỚI CƠ THỂ.
Hydrochloric acid (HCl) có vai trò rất quan trọng đối với quá trình trao đổi chất của cơ thể. Trong dung dịch dạ dày của ngƣời có Hydrochloric acid (HCl) với nồng độ khoảng từ 0,0001 đến 0,001 mol/l (có độ pH tƣơng ứng là 4 và 3).
OFFICIAL
Mô hình dạ dày người
Ngoài việc hòa tan các muối khó tan, hydrochloric acid còn là chất xúc tác cho các phản ứng thủy phân các chất gluxit (chất đƣờng, bột) và chất protein (chất đạm) thành các chất đơn giản hơn để cơ thể có thể hấp thụ đƣợc.
Lƣợng Hydrochloric acid (HCl) trong dịch vị dạ dày ngƣời nhỏ hơn hoặc lớn hơn mức bình thƣờng đều gây bệnh cho ngƣời. Khi trong dịch vị dạ dày có nồng độ Hydrochloric acid (HCl) nhỏ hơn 0,0001 mol/l , ngƣời ta mắc bệnh khó tiêu, ngƣợc lại nồng độ lớn hơn 0,001 mol/l , ngƣời ta mắc bệnh ợ chua.
Câu 1: Để làm giảm lƣợng Hydrochloric acid (HCl) trong dạ dày ngƣời ta dùng loại thuốc có thành phần chính là chất nào sau đây:
A. NaHCO3 B. NaOH C. Ca(OH)2 D. NaCl

Câu 2: Trên cơ sở nắm đƣợc nội dung đoạn trích, hãy lựa chọn Đúng/ Sai cho các ý sau:
Ý kiến Đúng/ sai
1. Thỉnh thoảng con ngƣời ta có ợ chua là do trong dạ dày ngƣời có nhiều Acetic acid. 2. Một ngƣời có nồng độ acid trong dạ dày là 0,002M, đây là mức acid cao hơn bình thƣờng, cần nhanh chữa trị để tránh hiện tƣợng loét dạ dày. 3. Khi ợ chua có nên ăn nhiều muối ăn để trung hòa acid dƣ trong cơ thể.
DẠYKÈMQUYNHƠN
28
Hƣớng dẫn đánh giá bài tập PISA 10.
Câu 1: Câu hỏi trắc nghiệm khách quan kiểu đơn giản.
- Mức đầy đủ: Đáp án A.
- Mức không đạt: Câu trả lời sai ; không trả lời.
Câu hỏi 2: Câu hỏi Đúng/sai phức hợp.
- Mức đầy đủ: (1)S, (2)Đ, (3)S.
- Mức chưa đầy đủ: Trả lời đúng 2 ý.
- Mức không đạt: Câu trả lời 1 ý hoặc sai; không trả lời.
Bài tập PISA 11: MUỐI IODINE VÀ BỆNH BƢỚU CỔ.
OFFICIAL
Để cơ thể khỏe mạnh, con ngƣời cần phải đƣợc cung cấp đầy đủ các nguyên tố hóa học cần thiết. Có những nguyên tố cần đƣợc cung cấp với khối lƣợng lớn và có những nguyên tố cần đƣợc cung cấp với khối lƣợng nhỏ (đƣợc gọi là nguyên tố vi lƣợng). Iodine là một nguyên tố vi lƣợng hết sức cần thiết đối với con ngƣời. Theo các nhà khoa học mỗi ngày cơ thể con ngƣời cần đƣợc cung cấp từ 1.10-4 đến 2.10-4 gam nguyên tố iodine. Cơ thể tiếp nhận đƣợc phần iodine cần thiết dƣới dạng hợp chất của iodine có sẵn trong muối ăn và một số loại thực phẩm. Nhƣng việc thiếu hụt iodine vẫn thƣờng xảy ra. Hiện nay, tính trên toàn thế giới một phần ba dân số bị thiếu iodine trong cơ thể. Ở Việt Nam, theo điều tra mới nhất, 94% số dân thiếu hụt iodine ở những mức độ khác nhau.Thiếu hụt iodine trong cơ thể dẫn đến hậu quả rất tai hại. Thiếu iodine làm não bị hƣ hại nên ngƣời thiếu iodine trở nên đần độn, chậm chạp, có thể điếc, câm, liệt chi, lùn. Thiếu iodine còn gây ra bệnh bƣớu cổ và hàng loạt rối loạn khác, đặc biệt nguy hiểm đối với bà mẹ và trẻ em.

Câu 1: Muối Iodine là muối ăn có trộn chất nào sau đây:
Bệnh nhân bị bướu cổ
A. AgI. B. I2 (đơn chất iodine). C.HI. D. KI hoặc KIO3.
Câu 2: Trên cơ sở nắm đƣợc nội dung đoạn trích, hãy lựa chọn Đúng/ Sai cho các ý sau: Đúng/ sai 1. Để phân biệt muối ăn thƣờng và muối ăn Iodine ngƣời ta dùng hồ tinh bột vì nếu muối có chứa iodine sẽ làm hồ tinh bột chuyên thành màu xanh. 2. Nên bỏ muối iodine sau khi thức ăn đã chín vì hợp chất iodine có thể bị phân hủy ở nhiệt độ cao.

DẠYKÈMQUYNHƠN
29
Câu 3: Nêu cách phòng tránh bệnh bƣớu cổ.

Hƣớng dẫn đánh giá bài tập PISA 11.
Câu 1: Câu hỏi trắc nghiệm khách quan kiểu đơn giản.
- Mức đầy đủ: Đáp án D.
- Mức không đạt: Câu trả lời sai ; không trả lời.
Câu 2: Câu hỏi Đúng/sai phức hợp.
- Mức đầy đủ: (1)S, (2)Đ.
- Mức chưa đầy đủ: Trả lời đúng 1 ý.
- Mức không đạt: Câu trả lời 1 ý hoặc sai; không trả lời.
Câu 3: Câu hỏi mở trả lời ngắn.
- Mức đầy đủ: HS trả lời cách phòng tránh bệnh bƣớu cổ:
+ Phòng bệnh bƣớu giáp chủ yếu là bổ sung Iodine trong khẩu phần ăn hàng ngày nhƣ dùng muối iodine thay cho muối thƣờng. Những biện pháp bổ sung iodine trong nƣớc mắm, dầu, bánh mì… cũng rất tốt .
+ Cần tiếp tục truyền thông cho các bà nội trợ, trong trƣờng học và cộng đồng những ích lợi của việc dùng muối iodine và cách dùng, nhƣ: muối iodine an toàn cho tất cả mọi ngƣời, không làm thay đổi mùi vị thức ăn, nêm vào thức ăn hoặc dùng trong muối dƣa, cà, trộn gỏi. Mua muối ở nơi có uy tín, xem kỹ nơi sản xuất, bao bì nguyên vẹn để phòng muối iodine giả. Cho muối vào lọ khô có nắp đậy hoặc buột chặt miệng túi sau khi dùng xong, tránh để muối iodine nơi quá nóng, nhiều ánh sáng.
+ Ăn thức ăn hải sản tùy khả năng: cá biển, sò ốc, mực; rong biển (rong sụn, rau câu, tảo…), các loại rau xanh, rau xà lách, trứng, phủ tạng động vật, sữa hoặc dùng thêm viên tảo có bán không đơn tại các nhà thuốc tây.
- Mức chưa đầy đủ: Trả lời đúng một số ý nhƣng chƣa đầy đủ nhƣ ý trên.
- Mức không đạt: Câu trả sai hoặc có cách hiểu lệch
DẠYKÈMQUYNHƠN
30
OFFICIAL
lạc; không trả lời Bài tập PISA 12: THÍ NGHIỆM SO SÁNH HOẠT ĐỘNG GIỮA CHLORINE – BROMINE – IODINE. Ngƣời ta bố trí các dụng cụ thí nghiệm nhƣ hình vẽ dƣới đây. Bóp mạnh quả bóp cao su của ống nghiệm chứa dung dịch Hydrochloric acid (HCl) đặc vào dung dịch Potassium permanganate (KMnO4). Hơ nhẹ ngọn lửa đèn cồn chỗ có miếng bông tẩm dung dịch
Potassium iodide (KI).
Câu 1: Nêu hiện tƣợng xảy ra trong ống hình trụ và trong ống nghiệm chứa dung dịch hồ tinh bột, nhận xét và rút ra kết luận .
Câu 2: Cho biết vai trò của dung dịch Sodium hydroxide (NaOH) đặc. Hƣớng dẫn đánh giá bài tập PISA 12.
Câu 1: Câu hỏi mở .
- Mức đầy đủ: Sau một thời gian ngắn, ở đoạn thứ nhất của ống hình trụ xuất hiện màu vàng lục của khí chlorine, đoạn thứ hai có màu nâu của bromine, đoạn thứ ba có màu tím của iodine. Dung dịch trong ống nghiệm 2 xuất hiện màu xanh do iodine đã làm xanh hồ tinh bột.
Cl2 + KBr → KCl + Br2 Br2 + KI → KBr + I2
OFFICIAL
- Mức chưa đầy đủ: Viết đƣợc phƣơng trình phản ứng, nêu đƣợc đoạn thứ nhất có chứa bromine, đoạn thứ 2 có chứa iodine nhƣng không mô tả đƣợc hiện tƣợng. Hoặc trả lời chƣa đƣợc đầy đủ
- Mức không đạt: Câu trả lời chỉ đƣợc 1 ý hoặc trả lời sai. Không trả lời. Câu 2: Câu hỏi mở .
- Mức đầy đủ: Dung dịch Sodium hydroxide (NaOH) đặc chứa trong cốc thủy tinh dùng hoà tan lƣợng halogen còn dƣ để tránh độc hại cho GV và HS.
- Mức không đạt: Câu trả lời sai; Không trả lời.
Bài tập PISA 13: DÙNG OZONE (O3) THAY CHLORINE (Cl2) TRONG XỬ LÝ NƢỚC.
Trên thực tế hiện nay, có rất nhiều nhà máy xử lý nƣớc tại các thành phố sử dụng hệ thống xử lý Ozone (O3) để sản xuất nƣớc sạch cho ngƣời dùng là các hộ dân cƣ và khu công nghiệp. Trong khi tất cả các loại hệ thống xử lý nƣớc đều có những lợi thế và bất lợi của họ, hệ thống ozone (O3) đƣợc biết đến nhƣ một hệ thống rất ƣu việt với việc cung cấp hệ thống khử trùng hữu hiệu và tránh một số vấn đề về sản phẩm phụ hóa học khi sử dụng chất chlorine. Rất nhiều hệ thống nƣớc sinh hoạt công cộng sử dụng ozone để khử vi khuẩn thay vì sử dụng chlorine. Ozone không tạo thành các hợp chất hữu cơ chứa chlorine, nhƣng chúng cũng không tồn tại trong nƣớc sau khi xử lý, vì thế một số hệ thống cho thêm một chút chlorine vào để ngăn cản sự phát triển của vi khuẩn trong đƣờng ống. Câu hỏi : Biết rằng cả Cl2 và O3 đều là có tính tẩy trùng. Nhƣng để tiệt trùng nƣớc dùng trong sản xuất các nhà máy này chỉ sử dụng O3 mà không dùng Cl2. Vì sao Cl2 và O3 có tinh tẩy trùng? Nguyên nhân các nhà máy chỉ sử dụng O3 là do đâu?
DẠYKÈMQUYNHƠN
31
Hƣớng dẫn đánh giá bài tập PISA 13.
Câu hỏi mở trả lời ngắn.
* Mức đầy đủ:
- Do Cl2 và O3 đều có tính oxi hóa mạnh nên có tính sát trùng. O3 khi phân rã nó tạo thành các gốc tự do của oxygen, là những chất có hoạt tính cao và gây nguy hiểm hay tiêu diệt phần lớn các phân tử hữu cơ.
- Các nguyên nhân là do:
+ Nƣớc khử trùng bằng Cl2 có mùi khó chịu do lƣợng Cl2 dƣ gây nên.
+ Nƣớc khử trùng bằng O3 không có mùi do chỉ cần lƣợng nhỏ O3 có thể khử trùng nhiều m3 nƣớc, O3 không bền, luôn tự phân giải và cuối cùng chỉ còn oxygen vô hại và không có các sản phẩm phụ gây ô nhiễm nƣớc.
+ Nƣớc khử trùng bằng O3 có thể diệt đƣợc cả vi khuẩn cỡ lớn nhƣ: vi khuẩn Kock gây bệnh lao, amip…
- Mức chưa đầy đủ: Trả lời đƣợc một trong các ý trên.
- Mức không đạt: Các đáp án khác ; không trả lời.
Bài tập PISA 14: CHLOROFLUOROCARBON (CFC) SỨC KHỎE VÀ MÔI TRƢỜNG.
Các khí Chlorofluorocarbon (CFC) đƣợc xem là tác nhân nguy hiểm tới môi trƣờng. Vào năm 1987, một nghị định đã đƣợc ban hành và cấm sử dụng CFC trên toàn cầu. Đƣợc biết, kể từ khi các nhà khoa học phát hiện ra chất CFC gây ra sự suy giảm của tầng ozone, CFC đã bị loại bỏ, nhƣng tủ lạnh cũ và các thiết bị khác sử dụng CFC vẫn đƣợc sử dụng rất nhiều. Tuy nhiên, ít ngƣời biết rằng qua đƣờng hô hấp, tiêu hóa hoặc tiếp xúc vật lý khác cũng nhƣ tiếp xúc với mức độ gây hại của tia cực tím, CFC có thể có tác động tiêu cực đến sức khỏe con ngƣời.
Câu 1: CFC gồm những nguyên tố hóa học nào sau đây?
A. Cl2 – F2.
C. C – Ca – F2.
B. Cl2 – C – F2.
D. C – F2.
Câu 2: Hãy cho biết CFC đƣợc sinh ra chủ yếu ở đâu? Chúng tác động tới môi trƣờng nhƣ thế nào? Nêu cơ chế tác động?
Hƣớng dẫn đánh giá bài tập PISA 14.
Câu 1: Câu hỏi trắc nghiệm khách quan kiểu đơn giản.
- Mức đầy đủ: Đáp án B
- Mức không đạt: Câu trả lời sai ; không trả lời.
Câu 2: Câu hỏi mở trả lời ngắn. - Mức đầy đủ:
DẠYKÈMQUYNHƠN
32
OFFICIAL
+ CFC là chất sinh hàn, đƣợc dùng trong tủ lạnh, điều hòa, …
+ Các khí Chlorofluorocarbon (CFC) gây hiện tƣợng suy giảm tầng ozone Bức xạ cực tím của vũ trụ qua những lỗ thủng này tới mặt đất gây ra bệnh ung thƣ da, hủy hoại mắt…
+ Cơ chế phân hủy ozone bởi feron đƣợc viết nhƣ sau: Các chất CFC gây ra hiện tƣợng "lỗ thủng ozone". Cơ chế phân hủy ozone bởi Chlorofluorocarbon (ví dụ CF2Cl2) đƣợc viết nhƣ sau.
CF2 Cl2 → Cl* + CF2 Cl.
O3 + Cl* → O2 + ClO* . O3 + ClO* → 2O2 + Cl*
Gốc tự do Cl* sinh ra lại tiếp tục thực hiện phản ứng dây chuyền với O3 . Mỗi gốc Cl* phá hủy hàng nghìn, hàng chục nghìn phân tử O3 gây ra hiện tƣợng thủng tầng ozone. - Mức chưa đầy đủ: chỉ trả lời đƣợc 1 trong các ý trên.
- Mức không đạt: đáp án khác, không có câu trả lời.
Bài tập PISA 15: POTASSIUM CHLORATE (KClO3) VÀ PHÁO HOA. Thời kỳ đầu, pháo hoa đƣợc làm từ hỗn hợp nhiên liệu và Potassium chlorate (KClO3), KClO3 vừa có tác dụng nhƣ chất oxy hóa, vừa là chất cung cấp oxygen. Nhƣng không may là khi tiếp xúc với sulfur, bột kim loại, muối Ammonium (NH4 +) hoặc khi bị ẩm thì KClO3 có xu hƣớng tạo thành các hợp chất nhạy cảm với tác động ma sát, vì vậy có thể gây ra những vụ nổ chết ngƣời. Do đó, về sau ít khi ngƣời ta sử dụng KClO3 làm pháo hoa. Ngày nay, thành phần chính tạo ra các điểm lóe sáng nhiều màu sắc của pháo hoa là potassium perchlorate (KClO4), một chất khó bốc cháy hơn. Ngoài KClO3 là một chất rất nguy hiểm, các nhà sản xuất pháo hoa còn sử dụng một số chất có độc tính rất cao để làm pháo hoa. Việc tạo ra màu xanh nƣớc biển luôn là một thách thức đặc biệt đối với các nhà sản xuất pháo hoa, vì chất tạo ra màu này là copper (II) chloride (CuCl2) chỉ tồn tại rất ngắn trong ngọn lửa nóng. Nhƣng trong thời gian qua, công nghệ sản xuất pháo hoa đã tiến một bƣớc lớn nhờ sử dụng hợp kim Mg –Al. Với hợp kim này, ngƣời ta có thể sản xuất pháo hoa với các màu xanh lá cây, đỏ, vàng và cả những màu tím, xanh nƣớc biển khá đẹp. Bản thân hợp kim Mg – Al tạo cho pháo hoa có màu bạc và lấp lánh, đồng thời chúng có tác dụng nhƣ nhiên liệu đốt pháo. Nói chung các hạt kim loại khi cháy thƣờng lóe sáng rất mạnh, làm át đi màu của pháo hoa, riêng hợp kim Mg – Al làm cho ngọn lửa pháo hoa cháy nóng mà không át đi màu của pháo hoa. Nguyên nhân có thể là do hợp kim này tạo ra một dạng hơi trong pha khí, vì vậy nó không lóe sáng quá mạnh.
DẠYKÈMQUYNHƠN
33
OFFICIAL
Câu hỏi: Vì sao KClO3 hay KClO4 đƣợc dùng làm pháo hoa? Hƣớng dẫn đánh giá bài tập PISA 15.
Câu hỏi mở trả lời ngắn.
- Mức đầy đủ: Trả lời đúng theo nguyên nhân sau: Các muối KClO3 hay KClO4 đều là những chất oxi hóa mạnh, giàu oxygen và dễ bị phân hủy do nhiệt. Khi phân hủy giải phóng ra oxygen: 2KClO3 →2 KCl +3O2 KClO4 → KCl + 2O2
Oxygen giải phóng ra đốt cháy các muối của các kim loại trong hỗn hợp tạo nên các màu sắc đặc trƣng cho muối đó.
- Mức chưa đầy đủ: Trả lời đúng một ý là 2 muối trên có tính oxi hóa và viết đƣợc phƣơng trình phản ứng.
- Mức không đạt: Câu trả sai; không trả lời.
OFFICIAL
2.4. Các biện pháp sử dụng bài tập theo hƣớng tiếp cận PISA để phát triển năng lực cho học sinh.
2.4.1. Biện pháp 1: Giúp học sinh thấy được ý nghĩa của bài tập theo hướng tiếp cận PISA.
a. Nội dung và tác dụng của biện pháp.
Bài tập theo hƣớng tiếp cận PISA chƣa đƣợc phổ biến rộng rãi trong quá trình giảng dạy ở trƣờng phổ thông. Ngƣời GV cần giúp HS của mình thấy đƣợc ý nghĩa của bài tập theo hƣớng tiếp cận PISA đối với việc nâng cao kết quả học tập môn Hóa học; hình thành và phát triển năng lực; kết nối kiến thức hóa học đƣợc học trong nhà trƣờng với thực tiễn. Từ đó, HS sẽ hứng thú và tích cực trong quá trình học tập với các bài tập theo hƣớng tiếp cận PISA.
b. Ý nghĩa của bài tập theo hướng tiếp cận PISA.
- Giúp kết nối kiến thức hóa học với thực tiễn.
- Phát triển năng lực cho HS.
- Nâng cao kết quả học tập môn Hóa học.
- Giúp HS hứng thú, say mê học tập.
c. Cách thực hiện.
- Bƣớc 1: Tìm hiểu, nghiên cứu về chƣơng trình đánh giá HS quốc tế PISA và bài tập theo hƣớng tiếp cận PISA.
- Bƣớc 2: Tổ chức giới thiệu về ý nghĩa của bài tập theo hƣớng tiếp cận PISA đối với việc nâng cao kết quả học tập và phát triển năng lực cho HS.
- Bƣớc 3: Giải đáp các thắc mắc của HS về việc sử dụng bài tập theo hƣớng tiếpcận PISA trong quá trình dạy học môn Hóa học.
DẠYKÈMQUYNHƠN
34
- Bƣớc 4: Khảo sát ý kiến của HS sau khi đƣợc học tập với các bài tập theo hƣớng tiếp cận PISA.
2.4.2. Biện pháp 2: Lựa chọn bài tập phù hợp với nội dung bài học và mục tiêu dạy học.
a. Nội dung và tác dụng của biện pháp.
Trong quá trình dạy học, nếu GV lựa chọn bài tập phù hợp với nội dung bài học và mục tiêu dạy học thì sẽ góp phần quan trọng vào việc tăng cƣờng hiệu quả của việc sử dụng bài tập theo hƣớng tiếp cận PISA để phát triển cũng nhƣ đánh giá năng lực học tập của HS.
Khi sử dụng bài tập theo hƣớng tiếp cận PISA cần chú ý đến chất lƣợng và số lƣợng bài tập nhằm để đạt đƣợc mục đích dạy học theo hƣớng phát triển năng lực HS.
b. Cách thực hiện.
OFFICIAL
- Bƣớc 1: Xác định nội dung và mục tiêu dạy học đáp ứng yêu cầu phát triển năng lực.
- Bƣớc 2: Lựa chọn bài tập phù hợp với nội dung và mục tiêu dạy học đã xác định.
- Bƣớc 3: Sử dụng bài tập trong các khâu đa dạng của quá trình dạy học.
- Bƣớc 4: Đánh giá hiệu quả của sử dụng bài tập để dạy học nhằm nâng cao kết quả học tập và phát triển năng lực của HS.
c.Ví dụ minh họa.
- Để củng cố và khắc sâu kiến thức về tốc độ phản ứng, GV có thể sử dụng bài tập PISA 3.
- Để mở đầu bài acid HCl, GV có thể sử dụng bài tập PISA 10 để dẫn dắt HS vào nội dung bài học mới một cách thú vị và hấp dẫn. 2.4.3. Biện pháp 3: Kết hợp sử dụng bài tập theo hướng tiếp cận PISA với các phương pháp dạy học tích cực. a. Nội dung và tác dụng của biện pháp. GV cần đôi mơi hınh thƣc tô chƣc tiêt giai bai tâp; kêt hợp sử dụng bài tập với các phƣơng pháp, kỹ thuâ day học tích cực để nâng cao hiệu quả sử dụng bài tập theo hƣớng tiếp cận PISA. Ngƣợc lại, bài tập theo hƣớng tiếp cận PISA là một lựa chọn phù hợp, khả thi để các phƣơng pháp dạy học này phát huy vai trò tích cực hoạt động hóa ngƣời học và phát triển năng lực của HS. b. Cách thực hiện. Đối với kỷ thuật dạy học theo trạm, GV có thể sử dụng bài tập theo hƣớng tiếp cận PISA để hoàn thiện, củng cố kiến thức.
DẠYKÈMQUYNHƠN
35
c. Ví dụ minh họa. Kết hợp sử dụng bài tập theo hƣớng tiếp cận PISA với kỷ thuật dạy học theo trạm (Giáo án bài “tốc độ phản ứng”).
2.4.4. Biện pháp 4: Giao nhiệm vụ, tổ chức hoạt động nhóm và cho HS trình bày trước lớp.
OFFICIAL
a. Nội dung và tác dụng của biện pháp. GV có thể tổ chức cho HS sƣu tầm và giới thiệu các bài tập theo hƣớng tiếp cận PISA hoặc các tình huống thực tế hay có thể sử dụng để thiết kế bài tập. GV cần cung cấp kiến thức, phƣơng pháp giải và những hƣớng dẫn cần thiết để HS có thể hoàn thành bài tập về nhà theo nhóm. Sau khi giải bài tập, HS sẽ đƣợc GV nhận xét, góp ý để hoàn thiện bài làm. Bƣớc tiếp theo, GV tổ chức cho HS trình bày bài giải và cách giải trƣớc lớp để tất cả các thành viên trong lớp theo dõi và nhận xét. GV sẽ tổng kết và đánh giá, cho điểm. Để tăng cƣờng hiệu quả của việc sử dụng bài tập theo hƣớng tiếp cận PISA, GV cần đa dạng hóa các hoạt động học tập gắn liền với việc sử dụng bài tập theo hƣớngtiếp cận PISA nhƣ: tổ chức trò chơi, tổ chức cho HS hoạt động nhóm, seminar… Cách làm này sẽ giúp tăng hứng thú học tập, khơi dậy niềm đam mê, say sƣa học tập của HS và góp phần làm tăng hiệu quả của việc sử dụng bài tập.
b. Cách thực hiện.
- Bƣớc 1: GV giao nhiệm vụ và cung cấp những hƣớng dẫn cần thiết cho HS.
- Bƣớc 2: HS làm việc theo nhóm để hoàn thành các nhiệm vụ đƣợc giao.
- Bƣớc 3: GV tổ chức cho các nhóm báo cáo kết quả thực hiện nhiệm vụ đƣợc giao.
- Bƣớc 4: HS các nhóm nhận xét, góp ý lẫn nhau.
- Bƣớc 5: GV nhận xét, rút kinh nghiệm, đánh giá, cho điểm. c. Ví dụ minh họa. (Biện pháp này đƣợc sử dụng để thiết kế giáo án bài “tốc độ phản ứng”)
Biện pháp 5: Hướng dẫn học sinh khai thác và sử dụng thông tin từ nội dung câu hỏi của bài tập, sách giáo khoa, tài liệu học tập, internet để giải bài tập. a. Nội dung và tác dụng của biện pháp. Đặc điểm của bài tập theo hƣớng tiếp cận PISA là sử dụng kiến thức thực tiễn phong phú và đa dạng để thiết kế. Bài tập theo hƣớng tiếp cận PISA bao gồm nhiều dạng câu hỏi nên việc khai thác thông tin từ nhiều nguồn khác nhau nhƣ: nội dung câu hỏi của bài tập, SGK, tài liệu học tập, internet…để trả lời các câu hỏi đó là rất cần thiết. GV cần hƣớng dẫn để HS thu thập và xử lý thông tin một cách có hiệu quả, không chỉ để giải quyết yêu cầu của bài tập mà còn giúp mở rộng kiến thức cho HS.
DẠYKÈMQUYNHƠN
36
2.4.5.
b. Cách thực hiện.
- Bƣớc 1: Đọc kĩ đề bài (xem bài tập đề cập đến lĩnh vực nào trong thực tiễn).
- Bƣớc 2: Xác định nguồn thông tin có thể sử dụng để trả lời câu hỏi.
- Bƣớc 3: Tìm hiểu kĩ lời văn của đề bài, tóm tắt ý chính để trả lời các câu hỏi mà nội dung trả lời là phần dẫn của bài tập.
- Bƣớc 4: Lựa chọn những kiến thức hoá học có liên quan để tìm ra mối liên hệ logic giữa dữ kiện và yêu cầu để trả lời câu hỏi kiểm tra kiến thức hóa học.
- Bƣớc 5: HS vận dụng sự hiểu biết về kiến thức hóa học, kiến thức thực tiễn, kinh nghiệm sống hoặc có thể tra cứu thông tin từ SGK, các tài liệu học tập hoặc tìm kiếm thông tin mới từ internet để trả lời câu hỏi vận dụng kiến thức khoa học.
OFFICIAL
- Bƣớc 6: Trình bày bài giải. c.Ví dụ minh họa. Để giải bài tập PISA 14, GV cần hƣớng dẫn cho HS thực hiện theo các bƣớc sau:
- Bƣớc 1: Đọc kĩ đề bài, xác định bài tập đề cập đến vấn đề môi trƣờng (cụ thể là lỗ thủng tầng ozone).
- Bƣớc 2: Xác định nguồn thông tin cần thiết để trả lời các câu hỏi 1, 2.
- Bƣớc 3: Tìm hiểu kĩ lời văn của đề bài để xác định các thông tin cần thiết để trả lời câu hỏi số 1.
- Bƣớc 4: Sử dụng kiến thức đã học về cách viết công thức cấu tạo các đồng phân của dẫn xuất halogen để trả lời câu hỏi số 2.
- Bƣớc 5: Kết hợp hiểu biết của bản thân và kết quả tìm kiếm, xử lý thông tin vềvấn đề lỗ thủng tầng ozone để trả lời câu hỏi số 2. - Bƣớc 6: Trình bày bài giải. 2.4.6. Biện pháp 6: Lồng ghép bài tập theo hướng tiếp cận PISA với các hoạt động ngoại khóa. a. Nội dung và tác dụng của biện pháp. Hoạt động ngoại khóa có thể coi nhƣ một hình thức để đánh giá HS theo quan điểm phát triển toàn diện và càng có ý nghĩa hơn nếu các hoạt động ngoại khoá có tác động trở lại, giúp HS có thêm hứng thú, niềm vui trong học tập, rèn luyện đạo đức. Hình thức tổ chức hoạt động ngoại khóa rất phong phú và đa dạng.
b. Cách thực hiện.
- Bƣớc 1: Lựa chọn hoạt động ngoại khóa phù hợp với thực tiễn dạy học.
- Bƣớc 2: Xây dựng kế hoạch thực hiện hoạt động ngoại khóa.
DẠYKÈMQUYNHƠN
37
- Bƣớc 3: Thực hiện hoạt động ngoại khóa.
- Bƣớc 4: Đánh giá, rút kinh nghiệm.
c.Ví dụ minh họa Bài tập theo hƣớng tiếp cận PISA có thể đƣợc lồng ghép vào các hoạt động ngoại khóanhƣ: tổ chức trò chơi, tổ chức thi đố vui,bảng tin Hóa học, bồi dƣỡng HS giỏi.
2.4.7. Biện pháp 7: Sử dụng đánh giá quá trình.
a. Nội dung và tác dụng của biện pháp.
Đánh giá quá trình không phải là một hoạt động độc lập với quá trình dạy học,nó có thể đƣợc xem là một phƣơng pháp đánh giá mang lại hiệu quả cao cho việc giảng dạy của GV và việc học tập của HS.
OFFICIAL
Đánh giá quá trình cung cấp thông tin về việc học của HS nhằm giúp HS kiểm soát và cải thiện việc học của mình. Kết quả của đánh giá quá trình sẽ gợi ý cho những bƣớc tiếp theo của việc dạy (điều chỉnh phƣơng pháp dạy) của GV và việc học (thay đổi phong cách học) của HS. Việc đánh giá mang tính hình thành khi phản hồi từ hoạt động học đƣợc sử dụng để điều chỉnh việc dạy cho phù hợp với nhu cầu của ngƣời học. Loại đánh giá này có thể kịp thời nhận đƣợc các tin tức phản hồi, kịp thời điều tiết, kiểm soát nhằm thu gọn khoảng cách giữa quá trình dạy học và mục tiêu đặt ra.
Bên cạnh việc đánh giá để điều chỉnh phƣơng pháp dạy học phù hợp, GV cần kịp thời động viên, khích lệ tinh thần học tập của HS. Ở lứa tuổi THPT, các em luôn có nhu cầu muốn đƣợc thể hiện và cần đƣợc ngƣời khác đánh giá đúng khả năng, năng lực của mình. Do đó, khi các em có những tiến bộ, có những biểu hiện tích cực thì việc khuyến khích, khen thƣởng kịp thời là vô cùng quan trọng. Đó chính là liều thuốc tinh thần kích thích hứng thú học tập của các em. Điều này sẽ có ảnh hƣởng mang tính quyết định đến sự tiến bộ, sự phát triển năng lực cũng nhƣ phát triển toàn diện của các em.
b. Một số phương pháp sử dụng khi đánh giá quá trình.
* Phƣơng pháp làm việc theo nhóm.
- GV chia nhóm, luân phiên mỗi nhóm sẽ chuẩn bị nội dung một chủ đề. Đến buổi học, đại diện một ngƣời trong nhóm sẽ lên đóng vai là GV có nhiệm vụ truyềnđạt các thông tin của bài học (ngƣời trình bày do giáo viên chỉ ngẫu nhiên trong nhóm). Các bạn HS khác trong lớp phải có nhiệm vụ xem ngƣời thuyết trình đó nhƣ là một GV, phải làm theo những yêu cầu của họ và phải tham gia phát biểu ý kiến, đóng góp cho buổi học sinh động. Sau mỗi tiết học, phải tham gia ý kiến để đánh giá ngƣời thuyết trình và chất lƣợng của bài giảng của nhóm chịu trách nhiệm soạn ra, ai có ý kiến đánh giá sẽ có điểm. GV có nhiệm vụ chỉnh sửa nội dụng cho HS trƣớc khi thuyết trình. Khi HS thuyết trình, GV phải quan sát tất cả HS trong lớp về thái độ học tập,qua đó sẽ đánh giá, ghi lại, cuối tiết học sẽ đƣa ra ý kiến về những trƣờng hợp có thái độ học tập không tốt, để lần sau HS hoàn thiện hơn.
DẠYKÈMQUYNHƠN
38
* Phƣơng pháp đặt câu hỏi và thảo luận lớp học.
- Mời các HS trao đổi những suy nghĩ của mình về một câu hỏi hay một chủ đề theo nhóm 2 ngƣời hay theo các nhóm nhỏ, sau đó yêu cầu đại diện nhóm chia sẻ suy nghĩ với nhóm lớn hơn.
- Trình bày nhiều câu trả lời cho một câu hỏi và sau đó yêu cầu HS bầu chọn.
- Yêu cầu tất cả HS viết ra câu trả lời và sau đó đọc to các câu trả lời đƣợc chọn.
* Phƣơng pháp cho bài kiểm tra và bài tập về nhà.
- GV có thể đƣợc sử dụng thƣờng xuyên phƣơng pháp cho bài kiểm tra và bài tập về nhà nếu GV phân tích đƣợc HS đang đứng ở đâu trong việc học tập và cung cấp các phản hồi cụ thể liên quan đến khả năng và cách thức để nâng cao thành tích học tập.
- GV thƣờng xuyên cho các bài kiểm tra ngắn sau mỗi chủ đề học, qua đó có thể kiểm tra đƣợc mức độ tiếp thu kiến thức của HS nhƣ thế nào.
OFFICIAL
- Các bài vừa mới học sẽ đƣợc kiểm tra trong vòng 1 tuần kể từ ngày GV giảng bài đó đầu tiên.
* Các phƣơng pháp khác
- Yêu cầu HS tóm tắt các ý chính vừa thu đƣợc từ bài giảng, cuộc thảo luận hay bài tập đƣợc giao.
- Cho HS làm một số bài tập hay trả lời các câu hỏi sau khi GV hƣớng dẫn bài xong và kiểm tra lại câu trả lời.
- Hỏi HS (từng cá nhân hoặc theo nhóm) về những suy nghĩ khi giải quyết cácvấn đề đặt ra trong bài học.
- Yêu cầu HS viết tóm tắt trong lớp.
Trong quá trình giảng dạy, GV sẽ áp dụng nhiều cách đánh giá khác nhau, phù hợp với chủ đề dạy và học, cuối học kỳ, GV sẽ cộng điểm trung bình chung từ các lần kiểm tra đánh giá và lấy điểm đó làm điểm kiểm tra cho quá trình học. Nhƣ thế GV sẽ có đƣợc kết quả chính xác nhất về ngƣời học; HS sẽ vì thế mà chăm chỉ học tập hơn, sáng tạo hơn và phát huy tinh thần học theo nhóm hơn.
2.5. Giáo án thực nghiệm (phụ lục).
DẠYKÈMQUYNHƠN
39
CHƢƠNG 3
THỰC NGHIỆM SƢ PHẠM.
3.1. Mục đích và nhiệm vụ thực nghiệm.
3.1.1. Mục đích thực nghiệm.
Mục đích của thực nghiệm sƣ phạm nhằm giải quyết các vấn đề sau:
- Khẳng định hƣớng đi đúng đắn và cần thiết của đề tài trên cơ sở lý luận và thực tiễn.
- Thu thập các thông tin định tính, định lƣợng, xử lý kết quả thực nghiệm bằng thông kê xác suất.
- Kiểm chứng tính hiệu quả của đề tài khi áp dụng vào quá trình giảng dạy ở trƣờng THPT Nghi Lộc 5 và THPT trên địa bàn.
3.1.2. Nhiệm vụ thực nghiệm
- Xây dựng các phiếu điều tra GV, phiếu điều tra HS trƣớc và sau khi tiến hành thực nghiệm.
- Kiểm tra đánh giá hiệu quả của tài liệu và cách sử dụng nó trong dạy học và kiểm tra đánh giá.
- Xử lý các kết quả thực nghiệm, phân tích, nhận xét và đánh giá hiệu quả đề tài.
3.2. Đối tƣợng và địa bàn thực nghiệm.
* Tại Trƣờng THPT X tại nơi chúng tôi đang công tác. Đề tài này chúng tôi tiến hành thực nghiệm tại Trƣờng THPT X.
Chúng tôi tiến hành xây dựng và sử dụng hệ thống bài tập theo hƣớng tiếp cận PISA nội dung “tốc độ phản ứng hóa học và nhóm halogen” trong chƣơng trình giáo dục phổ thông mới nhằm phát triển năng lực và phẩm chất cho HS, trải nghiệm ở các lớp 1
DẠYKÈMQUYNHƠN
40
OFFICIAL
Lớp thực nghiệm: + Lớp 10A1 (Lớp
–
+ Lớp 10A3 (Lớp
Lớp đối chứng: + Lớp 10A2 (Lớp định
+ Lớp 10A4 (Lớp
–
* Tại các
Thông
0 chúng tôi trực tiếp giảng dạy:
định hƣớng A
Ban cơ bản - sĩ số 41 em).
đại trà – Ban cơ bản - sĩ số 40 em).
hƣớng A – Ban cơ bản - sĩ số 40 em).
đại trà
Ban cơ bản – sĩ số 40 em).
trƣờng THPT khác.
qua Ban GiámHiệu nhà trƣờng, chúng tôiđã trao đổiphƣơng pháp và kĩ thuật dạy học, thiết kế và sử dụng hệ thống bài tập theo hƣớng tiếp cận PISA trong
dạy học hóa học 10 nội dung “tốc độ phản ứng và nhóm halogen” chƣơng trình giáo dục phổ thông 2018 nhằm phát triển năng lực cho HS. Đồng nghiệp đã tiến hành thực nghiệm tại một số lớp ở một số trƣờng bạn.
3.3. Thực hiện chƣơng trình thực nghiệm.
Tổ chức các buổi giới thiệu về kỳ thi PISA, cách ra đề, chấm điểm… tại các lớpTN với sự tham gia của GV dạy TN.
Tổ chức biên soạn giáo án có sử dụng bài tập theo hƣớng tiếp cận PISA.
Trao đổi ý kiến với GV dạy TN về ý đồ sƣ phạm của đợt TN để có sự thống nhất về nội dung và phƣơng pháp dạy học.
Ở các lớp ĐC, GV dạy theo phƣơng pháp thông thƣờng cùng với các bài tập có sẵn trong SGK và sách bài tập hiện hành. Ở các lớp TN, GV dạy theo giáo án đƣợc thiết kế có sử dụng bài tập theo hƣớng tiếp cận PISA. Các tiết dạy theo đúng tiến độ quy định chƣơng trình của Bộ đã ban hành.
OFFICIAL
Sau khi đã dạy các bài TN, chúng tôi tiến hành kiểm tra đồng thời các lớp ĐC và các lớp TN để xác định hiệu quả, tính khả thi của phƣơng án TN.
3.4. Kết quả thực nghiệm và xử lí kết quả thực nghiệm.
3.4.1. Kết quả kiểm tra trước thực nghiệm.
Trƣớc khi tiến hành TNSP, chúng tôi sử dụng bài thi khảo sát đầu năm lớp 10 của nhóm HS (LTN và LĐC). Kết quả thể hiện ở bảng sau: Bảng 3.1. Số học sinh đạt điểm Xi trước khi thực nghiệm.
đạt điểm
DẠYKÈMQUYNHƠN
41
đƣơng nhau về khả năng học tập. 3.4.2. Kết quả kiểm tra sau thực nghiệm. Kết quả kiểm tra sau thực nghiệm đƣợc trình bày lần lƣợt nhƣ sau: Bảng 3.2. Số lượng HS đạt điểm Xi của trường THPT X Nhóm Tổng số Số HS đạt từng loại điểm xi 0 1 2 3 4 5 6 7 8 9 10 TN 81 0 0 0 0 1 4 14 28 22 11 1 ĐC 80 0 0 0 0 6 12 23 25 11 3 0
Nhóm Số học sinh
Xi Trung Bình Tổng số 1 2 3 4 5 6 7 8 9 10 Thực nghiệm 81 0 0 0 5 17 17 20 13 9 0 6.58 Đối chứng 80 0 0 0 5 17 16 19 18 5 0 6.56 Nhƣ vậy, 2 nhóm HS đƣợc chọn (LTN và LĐC) là tƣơng
Bảng 3.3. Số lượng HS đạt điểm Xi của trường THPT Y
Nhóm Tổng số Số HS đạt từng loại điểm xi 0 1 2 3 4 5 6 7 8 9 10
TN 81 0 0 0 0 0 3 12 27 25 13 1 ĐC 82 0 0 0 0 7 12 24 23 11 3 0
3.4.3. Kết quả tham khảo ý kiến học sinh, giáo viên. 3.4.3.1. Kết quả tham khảo ý kiến HS.
Để khảo sát ý kiến của HS về việc sử dụng bài tập theo hƣớng tiếp cận PISA trong quá trình dạy học hóa học ở trƣờng THPT, chúng tôi đã gửi phiếu tham khảo ý kiến đến HS thuộc các trƣờng tham gia TN (phụ lục 3). Số phiếu phát ra: 163, số phiếu thu vào hợp lê: 163. Bảng 3.4. Đánh giá của HS về việc sử dụng bài tập theo hướng tiếp cận PISA. (Mức 1: Hoàn toàn không đồng ý; 2: Không đồng ý; 3: Không đồng ý, không bác bỏ;4: Đồng ý; 5: Hoàn toàn đồng ý).
STT Nội
dung
% Mức độ đồng ý Trung Bình 1 2 3 4 5
Vừa với lực học của em. 2.47 3.09 34.57 36.42 23.46 3.75 2 Giúp rèn luyện toàn diện các năng lực cần thiết. 1.23 1.85 32.10 43.83 20.99 3.81 3
1
Có những thông tin gần gũi với cuộc sống giúp em tăng thêm hứng thú học tập. 0.00 2.47 21.60 34.57 41.36 4.15 4
Giúp rèn khả năng phân tích, giải thích, giải quyết vấn đề. 1.23 1.23 20.99 42.59 33.95 4.07 5 Giúp rèn khả năng tổng hợp các
DẠYKÈMQUYNHƠN OFFICIAL 42
6
kiến thức liên môn. 0.62 3.70 31.48 30.86 33.33 3.93
Giúp dễ nhớ kiến thức và nhớ kiến thức lâu hơn. 1.23 1.85 24.07 33.95 38.89 4.07 7 Giúp thấy tự tin hơn khi vận dụng kiến thức để giải quyết một tình huống thực tế. 0.62 4.32 27.16 38.89 29.01 3.91
STT Nội dung
8 Những kiến thức tiếp thu đƣợc là cần thiết trong cuộc sống.
9
10
3.09 4.32 30.25 32.72 29.63 3.81
% Mức độ đồng ý Trung Bình
Nên sử dụng thƣờng xuyên bài tập theo hƣớng tiếp cận PISA khi học Hóa học. 0.00 1.85 25.31 50.00 22.84 3.94
Em muốn đƣợc trả lời nhiều bài tập theo hƣớng tiếp cậnPISA hơn khi học Hóa học. 0.00 1.85 24.69 49.38 24.07 3.96
Tổng hợp 3.94
OFFICIAL
Kết quả thể hiện ở bảng 3.4 cho thấy số HS đƣợc hỏi ý kiến về việc thích và muốn học các tiết học, làm các BTHH theo hƣớng tiếp cận PISA chiếm tỉ lệ cao. Tỉ lệ HS đồng ý về tác dụng của bài tập theo hƣớng tiếp cận PISA trong việc giúp các em nắm vững và nhớ lâu kiến thức, giải quyết tình huống thực tế, tổng hợp kiến thức liên môn, phát triển năng lực, tăng sự yêu thích môn Hóa học ở các mức cao (4,5) chiếm ƣu thế (trung bình mức độ đồng ý đạt 3.94/5).
3.4.3.2. Kết quả tham khảo ý kiến GV. Để khảo sát tác dụng của bài tập theo hƣớng tiếp cận PISA và hiệu quả của các biện pháp sử dụng loại bài tập này trong quá trình dạy học hóa học, chúng tôi đã gửi phiếu tham khảo ý kiến (phụ lục 3) đến các GV, cán bộ quản lý thuộc các trƣờng TN; các GV thuộc các trƣờng THPT ở huyện Nghi Lộc. Số phiếu phát ra: 30, số phiếu thu vào hợp lê: 28. a) Đánh giá của GV về tác dụng của bài tập theo hƣớng tiếp cận PISA. Bảng 3.5. Mức
DẠYKÈMQUYNHƠN
43
bài tập theo hướng tiếp cận PISA đối với một số yêu cầu sư phạm. (Mức 1: Không cần thiết; 2: Bình thường; 3: Cần thiết; 4: Rất cần thiết) STT Nội dung % Mức độ cần thiết Trung Bình 1 2 3 4 1 Gắn kết nội dung bài học với thực tiễn. 0.00 1.61 46.77 51.61 3.50 2 Phát triển năng lực cho HS. 0.00 1.61 43.55 54.84 3.53 3 Gây hứng thú học tập cho HS. 0.00 1.61 53.23 45.16 3.44 4 Nâng cao kết quả dạy và học môn Hóa học. 0.00 6.45 61.29 32.26 3.26 Tổng hợp 3.43
độ cần thiết của việc sử dụng
Kết quả thể hiện ở bảng 3.5 cho thấy các GV tham gia khảo sát đều đánh giácao mức độ cần thiết của bài tập theo hƣớng tiếp cận PISA trong việc gắn kết nội dung bài học với thực tiễn, phát triển năng lực học tập cho HS, gây hứng thú học tập cho HS, nâng cao kết quả của quá trình dạy và học môn Hóa học (trung bình mức độ đồng ý đạt 3.43/4).
b) Đánh giá của GV về các biện pháp sử dụng bài tập theo hƣớng tiếp cận PISA để phát triển năng lực cho HS
Bảng 3.6. Mức độ cần thiết của những biện pháp sử dụng bài tập theo hướng tiếpcận PISA để phát triển năng lực học tập cho HS phổ thông. (Mức 1: Không cần thiết; 2: Bình thường; 3: Cần thiết; 4: Rất cần thiết)
STT
Nội dung % Mức độ cần thiết Trung Bình 1 2 3 4 1 Giúp HS thấy đƣợc ý nghĩa của bài tập theo hƣớng tiếp cận PISA. 3.23 14.52 41.94 40.32 3.19
OFFICIAL
2 Lựa chọn bài tập phù hợp với nội dung bài học và mục tiêu dạy học. 0.00 12.70 34.92 52.38 3.40
3
4
Kết hợp sử dụng bài tập theo hƣớng tiếp cận PISA với các phƣơng pháp dạy học tích cực. 8.06 16.13 51.61 24.19 2.92
Giao nhiệm vụ, tổ chức hoạt động nhóm, HS trình bày trƣớc lớp. 6.45 12.90 46.77 33.87 3.08
Hƣớng dẫn HS khai thác và sử dụng thông tin từ nội dung câu hỏi của bài tập, SGK, tài liệu học tập, internet để giải bài tập. 3.23 6.45 32.26 58.06 3.45 6
5
Lồng ghép bài tập theo hƣớng tiếp cận PISA với các hoạt động ngoại khóa. 11.29 22.58 40.32 25.81 2.81
7 Sử dụng đánh giá quá trình. 4.84 9.68 43.55 41.94 3.23 Tổng hợp 3.15
Kết quả thể hiện ở bảng 3.6 cho thấy các GV tham gia khảo sát đánh giá tốt về các biện pháp sử dụng bài tập theo hƣớng tiếp cận PISA mà chúng tôi đề ra (trung bình mức độ đồng ý đạt 3.15/4), đặc biệt là biện pháp số 2 và số 5.
DẠYKÈMQUYNHƠN
44
1. Kết luận.
Đổi mới phƣơng pháp dạy học nói chung, đổi mới công tác kiểm tra đánh giá nói riêng luôn là yêu cầu hàng đầu của thực tiễn giáo dục và là việc làm cấp thiết đối với tất cả các cấp học. Trong quá trình nghiên cứu và thực hiện đề tài này, chúng tôi đã thực hiện đƣợc các vấn đề sau:
- Xác định đƣợc cơ sở lý luận và thực tiễn của việc xây dựng và sử dụng hệ thống bài tập đánh giá kiến thức, phát triển năng lực cho HS ở trƣờng THPT theo hƣớng tiếp cận PISA.
- Đề xuất đƣợc quy trình và xây dựng, sử dụng đƣợc hệ thống bài tập theo định hƣớng PISA để phát triển năng lực cho HS.
- Kết quả thu đƣợc qua việc tổ chức kiểm nghiệm, đánh giá của đề tài bằng phƣơng pháp chuyên gia đã khẳng định tính khả thi của đề tài và giá trị của hệ thống bài tập đã xây dựng.
Kết quả nghiên cứu của đề tài đã góp phần quan trọng trong việc đổi mới PPDH, góp phần nâng cao hiệu quả dạy học đối với hoạt động giáo dục, thúc đẩy sự hình thành và phát triển các phẩm chất, các năng lực khác cũng nhƣ kỹ năng sống cho HS.
Xây dựng và sử dụng hệ thống bài tập theo hƣớng tiếp cận PISA trong dạy học nội dung “tốc độ phản ứng hóa học và nhóm halogen” trong chƣơng trình GDPT 2018 nhằm phát triển năng lực cho HS, góp phần tạo tƣ duy logic cho HS, giúp cho kiến thức của HS mang tính hệ thống và luôn có mối liên hệ chặt chẽ với nhau, giúp GV tăng sự linh hoạt trong bài giảng. Điều quan trọng nhất sẽ giúp HS nắm đƣợc kiến thức hóa học thực tiễn, giải thích đƣợc các hiện tƣợng hóa học xảy ra trong tự nhiên, của vạn vật xung quanh, trong cuộc sống hằng ngày. Hƣớng dẫn HS phát huy những kiến thức đã học, rèn luyện các kĩ năng học tập, phát huy tính tích cực và gây hứng thú học tập cho các em.
PISA đạt hiệu quả cao nhất, Bộ Giáo dục và Đào tạo cần trang bị đầy đủ, đúng chuẩn về cơ sở vật chất, thiết bị, dụng cụ – đồ dùng dạy học cho nhà trƣờng. 2.2. Với các trường THPT. Tổ chứccácbuổi sinh hoạt chuyên môn về chƣơng trình đánh giá HSquốctếPISA, vềviệcthiếtkếvàsửdụngbàitậptheohƣớngtiếpcậnPISAtrongquátrìnhdạyhọc.
DẠYKÈMQUYNHƠN
45 C.
OFFICIAL
KẾT LUẬN VÀ KIẾN NGHỊ.
2. Kiến nghị. Từ kết quả nghiên
2.1. Với Bộ Giáo dục và Đào tạo. Thƣờng xuyên tổ chức tập huấn, bồi dƣỡng về chƣơng trình đánh giá HS quốc tế PISA, về việc thiết kế và sử dụng bài tập theo hƣớng tiếp cận PISA ở bậc THPT. Nhằm tạo điều kiện tốt nhất cho việc
i mớ
ục
ể
năng lực cho HS thông qua việc sử dụng
ậ
ng
ận
cứu của đề tài, chúng tôi xin có một số kiến nghị sau:
đổ
i giáo d
theo hƣớng phát tri
n
bài t
p theo hƣớ
tiếp c
Phát triển sâu rộng các cuộc thi GV giỏi cấp trƣờng, cấp cụm qua những tiết dạy áp dụng các PPDH hiện đại kết hợp với các kỹ thuật dạy học tích cực cũng nhƣ bài tập theo hƣớng tiếp cận PISA nhằm phát triển các năng lực học tập cho HS.
2.3. Với giáo viên.
Tham gia các buổi tập huấn đổi mới PPDH, đổi mới kiểm tra đánh giá; tập huấn về chƣơng trình đánh giá HS quốc tế PISA, thiết kế và sử dụng bài tập theo hƣớng tiếp cận PISA trong dạy học hóa học.
Tìm hiểu, nghiên cứu về chƣơng trình đánh giá HS quốc tế PISA, thiết kế và sử dụng bài tập theo hƣớng tiếp cận PISA để áp dụng thành công trong quá trình dạyhọc của bản thân. Chia sẻ với đồng nghiệp về những điều hay cũng nhƣ kinh nghiệm khi thiết kế và sử dụng bài tập theo hƣớng tiếp cận PISA.
OFFICIAL
DẠYKÈMQUYNHƠN
46
TÀI LIỆU THAM KHẢO
1. Bộ Giáo dục và Đào tạo (2012), PISA và các dạng câu hỏi, Nxb Giáo dục Việt Nam.
2. Bộ Giáo dục và Đào tạo (2014), Tài liệu tập huấn PISA 2015 và các dạng câu hỏido OECD phát hành lĩnh vực Khoa học.
3. Đỗ Tiến Đạt (2011), “Chƣơng trình đánh giá học sinh quốc tế PISA”, Kỷ yếu Hội thảo Quốc gia về giáo dục Toán học phổ thông.
4. Cao Cự Giác (2009), Thiết kế và sử dụng bài tập thực nghiệm trong dạy và họcHóa học, Nxb Giáo dục.
5. Nguyễn Cƣơng (1995), Một số biện pháp phát triển ở HS năng lực giải quyết vấn đề trong dạy học hóa học ở trường phổ thông ,Nxb Đại học sƣ phạm Hà Nội.
6. Bộ Giáo dục và Đào tạo (2010), Dạy và học tích cực, một số phương pháp và kỷ thuật dạy học, Nxb Đại học Sƣ phạm, Hà Nội.
OFFICIAL
7. Lê Thị Mỹ Hà (2011), “Chƣơng trình đánh giá quốc tế PISA tại Việt Nam – Cơ hội và thách thức”, Tạp chí khoa học Giáo dục.
8. Chƣơng trình tổng thể giáo dục phổ thông 2018. Bộ Giáo dục và đào tạo.
9. PISA và các dạng câu hỏi, Bộ Giáo dục và Đào tạo (2012), Nxb Giáo dục Việt Nam, Hà Nội.
10. Nguồn tƣ liệu từ internet.
DẠYKÈMQUYNHƠN
47
PHỤ LỤC Phụ lục 1
GIÁO ÁN THỰC NGHIỆM TỐC ĐỘ PHẢN ỨNG HÓA HỌC.
Môn: Hoá học. Lớp: 10 Thời gian thực hiện: 2 tiết
I. MỤC TIÊU BÀI HỌC
Năng lực hoá học
1. - Trình bày đƣợc khái niệm tốc độ phản ứng hoá học và cách tính tốc độ trung bình của phản ứng.
Nhận thức hoá học
- Viết đƣợc biểu thức tốc độ phản ứng theo hằng số tốc độ phản ứng và nồng độ (còn gọi là định luật tác dụng khối lƣợng (M. Guldberg và P. Waage, 1864) chỉ đúng cho phản ứng đơn giản nên không tùy ý áp dụng cho mọi phản ứng).
OFFICIAL
2. - Giải thích đƣợc các yếu tố ảnh hƣởng tới tốc độ phản ứng nhƣ: nồng độ, nhiệt độ, áp suất, diện tích bề mặt, chất xúc tác.
- Nêu đƣợc ý nghĩa của hệ số nhiệt độ Van’t Hoff (γ).
Tìm hiểu thế giới tự nhiên dƣới góc độ hoá học
3. Thảo luận, quan sát thí nghiệm (thí nghiệm về các phản ứng hoá học xảy ra nhanh, chậm khác nhau; Ảnh hƣởng của nồng độ, nhiệt độ, diện tích bề mặt, xúc tác tới tốc độ phản ứng).
Vận dụng kiến thức, kĩ năng đã học
4. - Vận dụng các kiến thức, kĩ năng hoá học đã học để phát hiện, giải thích một số vấn đề trong học tập và trong thực tiễn đời sống liên quan đến nội dung bài học - Vận dụng đƣợc hiểu biết về các yếu tố ảnh hƣởng đến tốc độ phản ứng vào cuộc sống thƣờng ngày.
Phẩm chất chủ
yếu
Trung thực
5. Trình bày các kết quả thí nghiệm trong báo cáo phù hợp với các kết quả thí nghiệm trong quá trình thực hiện.
Năng lực chung
Năng lực giải quyết vấn đề và sáng tạo
6. Thông qua các hoạt động HS: Xác định vấn đề cần giải quyết; nghiên cứu đề xuất phƣơng án giải quyết (có ứng dụng CNTT) ; Thực hiện giải quyết vấn đề; Đánh giá và rút kinh nghiệm khi tìm hiểu về tốc độ phản ứng hoá học.
DẠYKÈMQUYNHƠN
Năng lực tự chủ và tự học
Năng lực tin học
7. Thông qua các hoạt động cá nhân và hoạt động nhóm (có ứng dụng CNTT) để thu thập và xử lí thông tin giải quyết các vấn đề đặt ra trong nhiệm vụ học tập gồm:.).
8. Thông qua hƣớng dẫn HS sử dụng phần các mềm Power Point, Producshow/Camtasia, Yenka, Crocodile Chemistry... để thiết kế bài báo cáo, hoàn thành sản phẩm; Tổ chức một số hoạt động nhóm, báo cáo, thuyết trình thông qua các ứng dụng: Zalo, Teams, Zoom,… Sử dụng tìm kiếm trên các trang Web google.com, youtube.com.....
Giao tiếp và hợp tác
9. Thông qua hoạt động thảo luận nhóm, báo cáo sản phẩm,...(có ứng dụng CNTT).
OFFICIAL
10. Sử dụng ngôn ngữ phối hợp với đồ thị, dữ liệu, hình ảnh để trình bày thông tin và ý tƣởng có liên quan đến tốc độ phản ứng.
II. THIẾT BỊ VÀ HỌC LIỆU.
1. Giáo viên.
- Kế hoạch bài dạy, file cài đặt và hƣớng dẫn sử dụng một số phần mềm: Powerpoint; Word; Producshow/Camtasia,...(Cắt nối video).
- Hình ảnh, các nguồn tƣ liệu nhƣ: tranh ảnh, tƣ liệu các môn học liên quan đến bài học, phiếu học tập, bút dạ,giấy A0. Filethí nghiệmảo (bằng phần mềmYenka).
- Phiếu học tập, dụng cụ và hóa chất để làm thí nghiệm. Cụ thể dụng cụ, hóa chất gồm: + Dụng cụ: Cốc thủy tinh 250 ml, ống đong 100 ml, ống nghiệm, đồng hồ bấm giây, bếp điện nhỏ.
Hóa chất: Dung dịch: H2SO4 0,1M; H2SO4 1M; Na2S2O3 0,1M; BaCl2 0,1M; H2O2 10%; nƣớc cất; Zn bột; Zn hạt; MnO2 bột.
Thiết bị số và phần mềm được sử dụng trong bài học: Máy chiếu, máy tính/điện thoại có kết nối internet; phần mềm Powerpoint; Word; Producshow/Camtasia,... (Ghép hình ảnh, cắt nối video), phần mềm Yenka, Phim mô phỏng, phần mềm Crocodile Chemistry, các trang Web google.com, youtube.com.....
2. Học sinh.
- Sử dụng phần mềm Crocodile Chemistry/Yenka để nghiên cứu về các yếu tố ảnh hƣởng tới tốc độ phản ứng.
- Tìm kiếm và khai thác một số mô phỏng thí nghiệm về các yếu tố ảnh hƣởng tới tốc độ phản ứng trên mạng Internet.
DẠYKÈMQUYNHƠN
+
-
- Nghiên cứu cách sử dụng một số phần mềm nhƣ: Powerpoint; Word; Producshow/Camtasia,... (Ghép hình ảnh, cắt nối video).
III. TIẾN TRÌNH DẠY HỌC.
1. Hoạt động 1: Xác định vấn đề/nhiệm vụ học tập/Mở đầu.
a) Mục tiêu: HS huy động đƣợc một số kiến thức, kĩ năng, kinh nghiệm đã có của bản thân về tốc độ phản ứng và các yếu tố ảnh hƣởng đến tốc độ phản ứng của các phản ứng xảy ra trong đời sống thực tiễn để kích thích sự tò mò, mong muốn tìm hiểu bài học mới.
b) Nội dung:
PHIẾU
HỌC TẬP
- Vận dụng kiến thức đã được học và kiến thức thực tiễn trả lời các câu hỏi sau đây:
OFFICIAL
(1): Kể tên một số phản ứng hoá học xảy ra nhanh và phản ứng hoá học xảy ra chậm mà em quan sát đƣợc trong quá trình học tập và trong cuộc sống? (Học sinh có thể tìm kiếm các phản ứng này trên Internet).
(2): Lựa chọn một phản ứng hoá học đã nêu ở trên và cho biết các yếu tố: nồng độ, nhiệt độ, áp suất, diện tích bề mặt và xúc tác ảnh hƣởng nhƣ thế nào đến khả năng xảy ra nhanh hay chậm của phản ứng? ..............................................................................................................................
- Ghi kết quả hoạt động cá nhân, kết quả hoạt động nhóm cặp đôi và những điều muốn chia sẻ trước lớp vào bảng dưới đây:
Think (Hoạt động cá nhân) Pair (Hoạt động nhóm cặp đôi) Share (Chia sẻ với các bạn trong lớp)
c) Sản phẩm. HS có thể nêu đƣợc một số phản ứng xảy ra nhanh, một số phản ứng xảy ra chậm trong đời sống nhƣ: Đốt cháy than, củi; Phản ứng oxi hoá Fe,... và một số yếu
hƣởng đến tốc độ phản ứng nhƣ nhiệt độ càng cao thì phản ứng xảy ra càng nhanh,... Tuy nhiên, chƣa đầy đủ. Đặc biệt, HS chƣa giải thích đƣợc bản chất của các yếu tố ảnh hƣởng tới tốc độ phản ứng. Để giải quyết vấn đề này HS cần nghiên cứu kiến thức trong bài mới.
d) Tổ chức thực hiện:
DẠYKÈMQUYNHƠN
................................. ........................................ ..........................................
tố ảnh
GV tổ chức cho HS học tập theo kĩ thuật Think - Pair - Share, thực hiện các hoạt động sau và hoàn thành phiếu học tập:
- Think (Suy nghĩ cá nhân - 4 phút): HS thực hiện nhiệm vụ cá nhân, trả lời các câu hỏi dƣới đây:

(1): Kể tên một số phản ứng hoá học xảy ra nhanh và phản ứng hoá học xảy ra chậm mà em quan sát đƣợc trong quá trình học tập và trong cuộc sống?
(2): Lựa chọn một phản ứng hoá học đã nêu ở trên và cho biết các yếu tố: nồng độ, nhiệt độ, diện tích bề mặt, xúc tác và áp suất ảnh hƣởng nhƣ thế nào đến khả năng xảy ra nhanh hay chậm của phản ứng.
- Pair (Trao đổi cặp đôi - 3 phút): Hai HS ngồi cạnh nhau chia sẻ suy nghĩ của mình theo câu hỏi ở hoạt động trên với nhau.

OFFICIAL
- Share (chia sẻ ý kiến với cả lớp - 3 phút): GV mời một số cặp HS đại diện ở mỗi nhóm chia sẻ câu trả lời với cả lớp.

GV nhận xét, tổng kết các kết quả đạt đƣợc của các nhóm HS và nêu câu hỏi bài học: Làm thế nào để điều khiển tốc độ của phản ứng theo mục đích của con người?
- Phương án đánh giá. Thông qua kết quả hoạt động nhóm của HS (Phiếu ghi kết quả hoạt động), GV đánh giá những kiến thức ban đầu HS đã có về tốc độ phản ứng, trên cơ sở đó khai thác, vận dụng trong quá trình tổ chức các hoạt động học tiếp theo. Thiết bị số/phần mềm đƣợc sử dụng: Máy tính/điện thoại có kết nối internet; HS các nhóm sử dụng công cụ tìm kiếm trên Google search, youtube để thu thập thông tin; Google Meet, Zalo để trao đổi thảo luận; Phần mềm Word/Powerpoint để trình bày báo cáo.
DẠYKÈMQUYNHƠN
Hoạt động
ến thức mới/giải quyết vấn đề/thực thi nhiệm vụ đặt ra từ Hoạt động 1. Hoạt động 2.1. TÌM HIỂU KHÁI NIỆM VỀ TỐC ĐỘ PHẢN ỨNG . a) Mục tiêu: Trình bày đƣợc khái niệm tốc độ phản ứng hoá học và cách tính tốc
của phản ứng. b) Nội dung: HS hoàn thiện phiếu học tập.
2.
2: Hình thành ki
độ trung bình
PHIẾU HỌC TẬP
Hoàn thành các nhiệm vụ học tập sau đây:
1. Tiến hành 02 thí nghiệm (a) và (b), quan sát và rút ra nhận xét về mức độ xảy ra nhanh hay chậm của hai phải ứng này. (a). Đổ 5 ml dung dịch H2SO4 0,1M vào cốc 1 đựng 5 ml dung dịch BaCl2 0,1M. (b). Đổ 5 ml dung dịch H2SO4 0,1M vào cốc 2 đựng 5 ml dung dịch Na2S2O3 0,1M. (Nếu không có hoá chất thí nghiệm, GV có thể cho học sinh dùng phần mềm mô phỏng phòng thí nghiệm Hoá học – hƣớng dẫn học sinh cài đặt trên máy tính của mình – Crocodile Chemistry hoặc File thí nghiệm ảo (bằng phần mềm Yenka) để tiến hành phản ứng). 2. Xét phản ứng: A + B → C + D Quan sát bảng số liệu ghi lại nồng độ của chất A và B theo thời gian dƣới đây: Thời gian t (s) CA (M) CB (M) ∆CA (M) ∆CB (M) 0 0,5638 0,3114 393 0,4866 0,2342 669 0,4467 0,1943 1004 0,4113 0,1589 1265 0,3879 0,1355 Hoàn thành bảng trên bằng cách tính độ biến thiên
OFFICIAL
luận: Nói chung, các phản ứng hóa học khác nhau xảy ra nhanh, chậm khác nhau. Để đánh giá mức độ xảy ra nhanh hay chậm của các phản ứng hóa học, ngƣời ta đƣa ra khái niệmtốc độ phản ứng hóa học, gọi tắt là tốc độ phản ứng.
Câu 2:
DẠYKÈMQUYNHƠN
nồng
của chất A biết ∆CA = CA, ban đầu – CA,t và chất B biết ∆CB = CB, ban đầu – CB,t và nhận xét sự biến thiên nồng độ các chất theo thời gian. c) Sản phẩm: Câu 1: a. Ta thấy xuất hiện ngay kết tủa trắng của BaSO4. PTHH: H2SO4 + BaCl2 → BaSO4 ↓ + 2HCl (1) b. Sau một thời gian mới thấy màu trắng đục của S xuất hiện. PTHH: H2SO4 + Na2S2O3 → Na2SO4 + H2O + SO2 ↑ + S ↓ (2) Từ 2 thí nghiệm này cho thấy, phản ứng (1) xảy ra nhanh hơn phản ứng
Kết
độ
(2).
Thời gian t (s) CA (M) CB (M) ∆CA (M) ∆CB (M) 0 0,5638 0,3114 393 0,4866 0,2342 0,0772 0,0772 669 0,4467 0,1943 0,1171 0,1171 1004 0,4113 0,1589 0,1525 0,1525 1265 0,3879 0,1355 0,1759 0,1759
Trong quá trình diễn biến của phản ứng, nồng độ các chất phản ứng (chất A, B) giảm dần, đồng thời nồng độ các sản phẩm tăng dần. Phản ứng xảy ra càng nhanh thì trong một đơn vị thời gian nồng độ các chất phản ứng giảm càng nhiều và nồng độ các sản phẩm tăng càng nhiều.
Nhận xét, sự biến thiên nồng độ của chất A và chất B ở từng thời điểm là giống nhau.
Nhƣ vậy, có thể dùng độ biến thiên nồng độ theo thời gian của một chất bất kì trong phản ứng làm thƣớc đo tốc độ phản ứng.
d) Tổ chức thực hiện:
- Chuyển giao nhiệm vụ:
HS hoạt động theo nhóm (mỗi nhóm từ 5 - 7 HS), thực hiện nhiệm vụ trong phiếu học tập.
- Thực hiện nhiệm vụ học tập: Hoạt động nhóm thực hiện nhiệm vụ đƣợc giao trong thời gian 10 phút. HS sử dụng các dụng cụ, hoá chất hoặc sử dụng phần mềm thí nghiệm ảo Crocodile Chemistry và tiến hành thí nghiệm theo các bƣớc hƣớng dẫn, ghi nhận các dữ liệu thí nghiệm. HS sử dụng Google Meet, Zalo để trao đổi thảo luận.
- Báo cáo kết quả: HS báo cáo kết quả thông qua Word hoặc Power point. Tìm kiếm đƣợc các video, thông tin theo yêu cầu.
- GV: Yêu cầu đại diện một nhóm báo cáo kết quả, các nhóm còn lại lắng nghe, trao đổi, nhận xét, góp ý.
- GV: Nhận xét kết quả hoạt động nhóm và kết luận: Tốc độ phản ứng là độ biến thiên nồng độ của một trong các chất phản ứng hoặc sản phẩm trong một đơn vị thời gian. Tốc độ phản ứng được xác định bằng thực nghiệm. Trong thực tiễn ngƣời ta không xác định đƣợc tốc độ tức thời của phản ứng mà chỉ xác định đƣợc tốc độ trung bình của phản ứng. Xét phản ứng: A → C - Tốc độ phản ứng tính theo chất A (chất phản ứng) trong khoảng thời gian từ
DẠYKÈMQUYNHƠN
OFFICIAL
t1 đến t2 đƣợc xác định: (Tại thời điểm t1 chất A có nồng độ C1 mol/l; tại thời điểm t2 nồng độ chất A là C2 mol/l).
- Tốc độ phản ứng tính theo chất C (chất sản phẩm của phản ứng) trong khoảng thời gian từ t1 đến t2 đƣợc xác định: (Tại thời điểm t1 chất C có nồng độ C1' mol/l; tại thời điểm t2 nồng độ chất B là C2' mol/l).
là tốc độ trung bình của phản ứng trong khoảng thời gian từ t1 đến t2. - Phương án đánh giá. Đánh giá sản phẩmcủa HS (thông qua câu trảlời của HS so với đáp án trên).
Mức 1. Trả lời đầy đủ nhƣ đáp án ở trên. Mức 2. Trả lời chƣa đầy đủ Mức 3. Chƣa trả lời đƣợc.
OFFICIAL
Hoạt động 2.2. TÌM HIỂU VỀ PHƢƠNG TRÌNH TỐC ĐỘ PHẢN ỨNG VÀ HẰNG SỐ TỐC ĐỘ CỦA PHẢN ỨNG.
a) Mục tiêu: - Viết đƣợc biểu thức tốc độ phản ứng theo hằng số tốc độ phản ứng và nồng độ (còn gọi là định luật tác dụng khối lƣợng (M. Guldberg và P. Waage, 1864) chỉ đúng cho phản ứng đơn giản nên không tùy ý áp dụng cho mọi phản ứng). Từ đó nêu đƣợc ý nghĩa hằng số tốc độ phản ứng. - Nêu đƣợc ý nghĩa hằng số tốc độ phản ứng. b) Nội dung: HS hoàn thiện phiếu học tập PHIẾU HỌC TẬP. Hoàn thành các bài tập dƣới đây: Câu 1. Cho phản ứng: Br2 + HCOOH → 2HBr + CO2. Nồng độ ban đầu của Br2 là a mol/lít, sau 50 giây nồng độ Br2 còn lại là 0,01 mol/lít. Tốc độ trung bình của phản ứng tính theo Br2 là 4.10-5 mol/(l.s). Giá trị của a là A. 0,012. B. 0,016. C. 0,014. D. 0,018. Câu 2. Trong công nghiệp, ngƣời ta tổng hợp NH3 theo phƣơng trình hoá học sau: N2(k) + 3H2(k) 2NH3(k) Khi tăng nồng độ H2 lên 2 lần (giữ nguyên nồng độ của khí N2 và nhiệt độ của phản ứng) thì tốc độ phản ứng tăng lên bao nhiêu lần? c) Sản phẩm: Phiếu học tập số 03: Câu 1. Đáp án A.
DẠYKÈMQUYNHƠN
1221 2121 v = + CCCCC ttttt '' 21
ΔC v
Δt CC
21
=
tt v
Câu 2. v=k.[N2].[H2]3.Khinồngđộ H2 tănglên2lầnthìtốcđộtănglên8lần.
d) Tổ chức thực hiện: - GV: Giới thiệu nội dung định luật tác dụng khối lƣợng và công thức tính tốc độ phản ứng theo hằng số tốc độ và nồng độ. Giả sử có phản ứng tổng quát: aA + bB → cC + dD - Nội dung định luật tác dụng khối lƣợng: “Ở nhiệt độ không đổi, tốc độ
ủa ph
n
ng t
l
với tích số nồng độ của các chất phản ứng được lũy thừa lên với
mũ bằng hệ số tỉ lượng tương ứng” Với phản ứng tổng quát trên, định luật tác dụng khối lƣợng đƣợc biểu diễn bằng biểu thức: v = k. - Ý nghĩa của hằng số tốc độ phản ứng: Hệ số tỉ lệ k là hằng số tốc độ của phản ứng hóa học, cũng đƣợc gọi là “tốc độ riêng” của phản ứng vì k = v khi nồng độ của mỗi chất ban đầu bằng đơn vị. Hằng số tốc độ phụ thuộc vào bản chất của các chất phản ứng và nhiệt độ Ví dụ: Thực nghiệm cho thấy tốc độ phản ứng hoá học: A(k) + 2B(k) → C(k) + D(k) Đƣợc tính theo biểu thức: v = k.[A].[B]2. Nếu nồng độ chất B tăng 3 lần và nồng độ chất A không thay đổi thì tốc độ của phản ứng trên tăng lên bao nhiêu lần? A. 3 lần B. 6 lần C. 9 lần D. 12 lần
- Chuyển giao nhiệm vụ học tập: Yêu cầu HS hoạt động theo nhóm hoàn thành nhiệm vụ trong phiếu học tập. - Thực hiện nhiệm vụ: - Phương án đánh giá.
DẠYKÈMQUYNHƠN
OFFICIAL
c
ả
ứ
ỉ
ệ
số
Mức 1: Trả lời đầy đủ
Mức 2: Trả lời chƣa đầy đủ. Ví dụ
đáp án tốc
Mức 3: Chƣa trả lời
Hoạt động 2.3: NGHIÊN CỨU CÁC YẾU TỐ ẢNH HƢỞNG TỚI TỐC ĐỘ PHẢN ỨNG. a) Mục tiêu: - Thực hiện đƣợc một số thí nghiệm (hoặc qua quan sát video, hoặc qua mô tả) nghiên cứu các yếu tố ảnh hƣởng tới tốc độ phản ứng (nồng độ, nhiệt độ, áp suất, diện tích bề mặt, chất xúc tác). - Giải thích đƣợc các yếu tố ảnh hƣởng tới tốc độ phản ứng nhƣ: nồng độ, nhiệt độ, áp suất, diện tích bề mặt, chất xúc tác. ab ABCC
nhƣ đáp án ở trên.
: Câu 2 chỉ viết đƣợc biểu thức v mà chƣa đƣa ra đƣợc
độ tăng 8 lần.
đƣợc.
b) Nội dung. Tổ chức dạy họctheo trạm(5 trạm) với nội dung ởcác trạmnhƣ sau:
TRẠM 1
- Tiến hành thí nghiệm: Lấy 02 ống nghiệm thƣờng và đánh số thứ tự (a), (b). Cho vào ống nghiệm (a) 5 ml dd Na2S2O3 0,1M; ống nghiệm (b) 2 ml dd Na2S2O3 0,1M và 3 ml nƣớc cất. Đổ lần lƣợt vào mỗi ống nghiệm 5 ml dd H2SO4 0,1M và sử dụng đồng hồ bấm giây xác định thời gian xuất hiện kết tủa ở mỗi ống nghiệm.
1. Nêu hiện tƣợng thí nghiệm và viết PTHH xảy ra.
............................................................................................................................... ...............................................................................................................................
2. So sánh thời gian xuất hiện màu trắng đục của S trong 2 ống nghiệm và giải thích nguyên nhân của sự khác nhau về tốc độ xuất hiện kết tủa ở hai cốc. ...............................................................................................................................
OFFICIAL
3. Kết luận về ảnh hƣởng của nồng độ chất phản ứng đến tốc độ phản ứng: Khi tăng nồng độ chất phản ứng, tốc độ phản ứng...............................................
TRẠM 2
- Tiến hành thí nghiệm:
(TN1): Lấy vào ống nghiệm 5 ml dung dịch Na2S2O3 0,1M và đổ vào đó 5 ml dung dịch H2SO4 0,1M. Dùng đồng hồ bấm giây xác định thời gian từ khi đổ dung dịch H2SO4 vào dung dịch Na2S2O3 đến khi bắt đầu xuất hiện kết tủa.
(TN2): Cũng lấy lƣợng 2 dung dịch nhƣ trên, đun nóng cả hai dung dịch rồi đổ vào nhau. Dùng đồng hồ bấm giây xác định thời gian bắt đầu xuất hiện kết tủa.
DẠYKÈMQUYNHƠN
...............................................................................................................................
............................................................................................................................... ...............................................................................................................................
............................................................................................................................... ...............................................................................................................................
......................................................................
1. So sánh thời gian xuất hiện kết tủa ở thí nghiệm 1 và thí nghiệm 2.
2. Giải thích sự khác nhau về tốc độ xuất hiện kết tủa trong 02 thí nghiệm trên
3. Kết luận về ảnh hƣởng của nhiệt độ đến tốc độ phản ứng Khi tăng nhiệt độ, tốc độ phản ứng
TRẠM 3
1. Đối với các phản ứng có chất khí, khi áp suất tăng, nồng độ của các chất khí trong phản ứng thay đổi nhƣ thế nào?
2. Sự thay đổi nồng độ chất khí ảnh hƣởng nhƣ thế nào tới tốc độ của phản ứng và giải thích?
TRẠM 4
- Tiến hành thí nghiệm: Lấy 02 cốc thủy tinh (thể tích 100 ml) và đánh số thứ tự (a), (b). Cân khối lƣợng 1 viên Zn hạt và lấy lƣợng Zn bột tƣơng ứng. Cho vào cốc (a) 30 ml dd H2SO4 1M và lƣợng Zn bột đã xác định ở trên; Cốc (b) 30 ml dd H2SO4 1M và 1 viên Zn hạt. Dùng đồng hồ bấm giây xác định thời gian Zn bị hoà tan hết ở 2 cốc.
OFFICIAL
1. So sánh thời gian Zn bị hòa tan hết ở 2 cốc: ............................................................................................................................... ...............................................................................................................................
2. Giải thích sự khác nhau về tốc độ hoà tan Zn trong hai cốc trên
3. Kết luận về ảnh hƣởng của diện tích tiếp bề mặt tới tốc độ phản ứng: Khi tăng diện tích bề mặt chất phản ứng, tốc độ phản ứng ...............................................................................................................................
TRẠM 5
- Tiến hành thí nghiệm: Lấy 02 cốc thủy tinh loại có thể tích 250 ml và đánh số thứ tự (a), (b). Cho 25 ml dd H2O2 vào mỗi cốc: - Cốc (a) để yên ở nhiệt độ phòng. - Cốc (b) cho thêm một ít bột MnO2 và để ở nhiệt độ phòng. Quan sát hiện tƣợng phản ứng xảy ra. 1. Nêu hiện tƣợng thí nghiệm:
2. So sánh lƣợng khí O2 thoát ra ở hai cốc:
3. Kết luận về ảnh hƣởng của chất xúc tác tới tốc độ phản ứng:
DẠYKÈMQUYNHƠN
............................................................................................................................... ...............................................................................................................................
...............................................................................................................................
...............................................................................................................................
...............................................................................................................................
...............................................................................................................................
..........................................................
.........................
c) Sản phẩm: Mô tả đƣợc hiện tƣợng các thí nghiệm và giải thích, kết luận về các yếu tố ảnh hƣởng đến tốc độ phản ứng.
* Ảnh hưởng của nồng độ: S xuất hiện trong cốc (a) nhanh hơn, nghĩa là tốc độ phản ứng trong cốc (a) lớn hơn.
PTHH: Na2S2O3 + H2SO4 → Na2SO4 + S↓ + H2O + SO2↑ (1). Giải thích: Để các chất phản ứng đƣợc với nhau (VD: Na2S2O3 và H2SO4) thì giữa các phân tử tham gia phản ứng phải va chạm “hiệu quả” với nhau, số va chạm “hiệu quả” càng lớn, tốc độ phản ứng càng lớn. Khi nồng độ các chất phản ứng tăng, số vachạmtăng,số va chạm“hiệu quả” tăng nên tốcđộ phản ứng tăng.
Kết luận: Khi tăng nồng độ chất phản ứng, tốc độ phản ứng tăng.
* Ảnh hưởng của nhiệt độ: Kết tủa (sulfur) xuất hiện trong TN2 nhanh hơn, nghĩa là ở nhiệt độ cao tốc độ phản ứng lớn hơn ở nhiệt độ thấp.
OFFICIAL
Giải thích: Khi nhiệt độ phản ứng tăng dẫn tới hai hệ quả sau:
- Tốc độ chuyển động của các phân tử tăng, dẫn đến tần số va chạm giữa các phân tử chất phản ứng tăng.
- Tần số va chạm có hiệu quả giữa các phân tử chất phản ứng tăng nhanh. Đây là yếu tố chính làm cho tốc độ phản ứng tăng nhanh khi tăng nhiệt độ.
Kết luận: Khi tăng nhiệt độ, tốc độ phản ứng tăng.
* Ảnh hưởng của áp suất:
1. Khi áp suất tăng, nồng độ của chất khí tăng theo.
2. Nồng độ chất khí tăng làm cho tốc độ phản ứng tăng, tƣơng tự nhƣ ảnh hƣởng của nồng độ đến tốc độ phản ứng.
Kết luận: Đối với phản ứng có chất khí,khi tăng áp suất, tốcđộ phản ứng tăng.
DẠYKÈMQUYNHƠN
Zn phản ứng hết trong cốc (a) ít hơn trong cốc (b). PTHH: Zn + H2SO4 → ZnSO4 + H2↑ Giải thích: Chất rắn với kích thƣớc nhỏ (Zn bột) có tổng diện tích bề mặt tiếp xúc với chất phản ứng (H2SO4) lớn hơn so với chất rắn có kích thƣớc hạt lớn hơn (Zn hạt) cùng khối lƣợng, nên có tốc độ phản ứng lớn
Kết luận: Khi tăng diện tích bề mặt các chất phản ứng,tốc độ phản ứng
* Ảnh hưởng của chất xúc tác: + Ống nghiệm (a):
2
2
ủy chậm trong
ịch ở nhiệt
ng (mắt thƣờng không quan sát đƣợc bọt
ả
ứ
2H2
2
2H
↑
* Ảnh hưởng của diện tích bề mặt: Ta thấy thời gian để
hơn.
tăng.
H
O
phân h
dung d
độ thƣờ
khí O2 thoát ra) theo ph
n
ng sau:
O
→
2O + O2
+ Ống nghiệm (b): Cho thêm vào dung dịch H2O2 một ít bột MnO2, bọt O2
thoát ra rất mạnh (mắt thƣờng quan sát rõ). Khi phản ứng kết thúc, MnO2 vẫn còn nguyên. Vậy MnO2 là chất xúc tác cho phản ứng phân hủy H2O2. Kết luận: Chất xúc tác là chất làm tăng tốc độ phản ứng, nhƣng còn lại sau khi phản ứng kết thúc.
d) Tổ chức thực hiện.
- GV tổ chức cho HS hoạt động theo nhóm theo trạm. - Tổ chức cho các nhóm tổng kết các kết quả nghiên cứu đã đạt đƣợc về các yếu tố ảnh hƣởng tới tốc độ phản ứng theo bảng dƣới đây.
STT Các yếu tố Ảnh hƣởng của yếu tố tới tốc độ phản ứng
OFFICIAL
Ghi chú 1. Nồng độ 2. Nhiệt độ
Áp suất
Diện tích bề mặt 5. Chất xúc tác
- HS hoạt động theo nhóm và hoàn thành nhiệm vụ học tập
- GV: Yêu cầu đại diện một nhóm báo cáo kết quả. Các nhóm còn lại lắng nghe, trao đổi nhận xét, bổ sung.
- HS: Đại diện một nhóm HS báo cáo: HS báo cáo kết quả thông qua Word hoặc Power point. Tìm kiếm đƣợc các video, thông tin theo yêu cầu. - Phƣơng án đánh giá:
DẠYKÈMQUYNHƠN
sẽ
3.
4.
đƣợc từ 2 - 3 nhiệm vụ học
ập. Mức 3. HS hoàn thành
c 1 nhiệm vụ
ọc tậ
ệm vụ học tậ
Thiết bị
Ho
Mức 1. HS hoàn thành đƣợc ít nhất 4 nhiệm vụ học tập. Mức 2. HS hoàn thành
t
đƣợ
h
p hoặc không hoàn thành đƣợc nhi
p nào.
số/phần mềm đƣợc sử dụng: Máy tính/điện thoại có kết nối internet; HS các nhóm sử dụng phần mềm Crocodile Chemistry/ Yenka; Google Meet, Zalo để trao đổi thảo luận; Phần mềm Word/Powerpoint để trình bày báo cáo.
ạt động 2.4: Tìm hiểu ý nghĩa của tốc độ phản ứng và cân bằng hóa học trong sản xuất hóa học
a) Mục tiêu: ý nghĩa thực tiễn của tốc độ phản ứng
b) Nội dung:
- Tại sao trời nắng nóng thức ăn dễ thiu hơn so với khi nhiệt độ mát mẻ? Vậy cách bảo quản thực phẩm là nhƣ thế nào?
- Tại sao khi ủ rƣợu ngƣời ta phải cho men?
- Tại sao viên than tổ ong lại có nhiều lỗ?
- Tại sao khí nhóm bếp than ban đầu ngƣời ta phải quạt?
c) Sản phẩm.
- Nhiệt độ cao làm tăng khả năng phân hủy thức ăn. Ta nên bảo quản nơi thoáng mát hoặc tủ lạnh.
-Men là chất xúc tác sinh họcgiúp quá trình lên men rƣợu xảy ranhanh hơn.
- Tăng khả năng tiếp xúc với oxygen không khí.
OFFICIAL
- Tăng nồng độ oxygen để than cháy nhanh hơn
d) Tổ chức thực hiện.
GV: Phân công học sinh tìm hiểu trƣớc ở nhà và thuyết trình – thảo luận trên lớp giữa các nhóm với nhau. (Học sinh có thể thuyết trình trên Powerpoint hoặc chuẩn bị các video về ý nghĩa thực tiễn của tốc độ phản ứng).
Tổ chức cho HS thảo luận nhóm và cho biết ngƣời ta đã sử dụng yếu tố nào để tăng tốc độ phản ứng.
-Phƣơngánđánhgiá:Thôngquamứcđộhoànthànhvàtraođổi,gópýcủaHS.
Thiết bị số/phần mềm đƣợc sử dụng: Máy tính/điện thoại có kết nối internet; HS các nhóm sử dụng công cụ tìm kiếm trên Google search để thu thập thông tin; Google Meet, Zalo để trao đổi thảo luận; Phần mềm Word/Powerpoint để trình bày báo cáo hoặc video.
DẠYKÈMQUYNHƠN
3.
a)
b) Nội dung HĐ: GVtổ chức cho HS củng cố kiến thức bằng cácbài tập PISA1; 2; 3; 4; 5; 6. 4. Hoạt động 4: Vận dụng. a) Mục tiêu: HS vận dụng đƣợc kiến thức tốc độ phản ứng hoá học vào việc giải thích một số vấn đề thƣờng gặp trong cuộc sống và sản xuất. b) Nội dung: - HS tìm 2 tình huống, một tình huống trong cuộc sống và một tình huống trong sản xuất có vận dụng kiến thức ảnh hƣởng của các yếu tố ảnh hƣởng tới tốc độ phản ứng hoá học;
Hoạt động 3: Luyện tập.
Mục tiêu: Củng cố, khắc sâu kiến thứcđã họctrong bài về tốcđộ phản ứng
- HS viết báo cáo về yếu tố ảnh hƣởng trong hai tình huống và giải thích sự ảnh hƣởng của yếu tố đến tốc độ phản ứng. Nội dung bài báo cáo bao gồm:
+ Giới thiệu tình huống và phản ứng hoá học xảy ra trong tình huống;
+ Nêu đƣợc sự vận dụng yếu tố ảnh hƣởng đến tốc độ phản ứng;
+ Nêu yếu tố ảnh hƣởng đến tốc độ phản ứng hoá học trong tình huống;
+Giảithíchđƣợcsựảnhhƣởngcủayếutốđóđếntốcđộphản ứnghoáhọc.
c) Sản phẩm:
Bài báo cáo tìm hiểu sự vận dụng đƣợc kiến thức tốc độ phản ứng hoá học vào việc giải thích một số vấn đề thƣờng gặp trong cuộc sống và sản xuất.
d) Tổ chức thực hiện:
- GV thông báo HS thực hiện nhiệm vụ học tập này ở nhà. GV thông báo yêu cầu về nội dung bài báo cáo, hình thức nộp bài, thời hạn và công cụ nộp bài và tiêu chí đánh giá.
OFFICIAL
+ Hình thức nộp: Biên soạn trên file word, nộp bài trên trang cá nhân trong Onenote.
+ Thời gian nộp bài: Trong vòng 1 tuần sau buổi học.
- HS tìm tình huống, thực hiện bài báo cáo và chia sẻ trong Onenote ở trang cá nhân.
- Sau thời hạn nộp bài, GV công bố các sản phẩm của HS. HS dựa trên bảng tiêu chí đánh giá để nhận xét và đánh giá lẫn nhau.
- GV tổng kết các nội dung quan trọng về yếu tố ảnh hƣởng đến tốc độ phản ứng và sự vận dụng vào các tình huống trong đời sống và sản xuất.
DẠYKÈMQUYNHƠN
DẠYKÈMQUYNHƠN OFFICIAL
Phụ lục 2 Hình ảnh thực nghiệm


DẠYKÈMQUYNHƠN OFFICIAL


DẠYKÈMQUYNHƠN OFFICIAL


DẠYKÈMQUYNHƠN OFFICIAL


DẠYKÈMQUYNHƠN OFFICIAL


Đề Kiểm tra năng lực
Phần I: Trắc nghiệm.
Câu 1: Có hai mẫu đá vôi:
Mẫu 1: đá vôi có dạng khối.
Mẫu 2: đá vôi có dạng hạt nhỏ. Hòa tan cả hai mẫu đá vôi bằng cùng một thể tích dung dịch acid HCl dƣ có cùng nồng độ. Ta thấy thời gian để mẫu 1 phản ứng hết nhiều hơn mẫu 2. Thí nghiệm trên chứng minh điều gì?
A. Tốc độ phản ứng phụ thuộc vào nhiệt độ tiến hành phản ứng.
B. Tốc độ phản ứng phụ thuộc vào diện tích tiếp xúc giữa các chất phản ứng.
C. Tốc độ phản ứng phụ thuộc vào thời gian xảy ra phản ứng.
D. Tốc độ phản ứng không phụ thuộcvào nồng độ cácchất thamgiaphản ứng. Câu 2: Nồi áp suất dùng để ninh, hầm thức ăn có thể làm nóng nƣớc tới nhiệt độ 1200C so với 1000C khi dùng nồi thƣờng. Trong quá trình hầm xƣơng thƣờng diễn ra nhiều phản ứng hóa học, ví dụ quá trình biến đổi protein, chẳng hạn nhƣ thủy phân một phần collagen thành gelatin. Hãy cho biết tốc độ quá trình thủy phân collagen thành gelatin thay đổi nhƣ thế nào khi sử dụng nồi áp suất thay cho nồi thƣờng.
A. Không thay đổi.
B. Giảm đi 4 lần.
D. Ít nhất giảm 16 lần. Câu 3: Trong nguồn nƣớc ngầm thƣờng chứa ion Fe2+ tồn tại dƣới dạng muối Fe(HCO3)2 và Fe(OH)2. Nếu nguồn nƣớc sinh hoạt chứa nhiều Fe2+ thì gây ảnh hƣởng đến sức khỏe con ngƣời. Để loại bỏ Fe2+ có một phƣơng pháp đơn giản, rẻ tiền đó là dùng oxygen trong không khí để oxi hóa Fe2+ thành hợp chất Fe2+ (có độ tan nhỏ trong nƣớc) rồi lọc để thu đƣợc nƣớc sạch. Để tăng tốc độ của phản ứng oxi hóa Fe2+ thành Fe3+ ngƣời ta đã thiết kế hệ thống giàn phun sƣơng. Nguồn nƣớc ngầm đƣợc dẫn vào hệ thống dàn phun sƣơng, bên dƣới dàn phun có hệ th
C. Ít nhất tăng 4 lần.
DẠYKÈMQUYNHƠN
OFFICIAL
Phụ lục 3
ể lắ
của phản ứng oxi
A. Tăng diện tích tiếp
của Fe
với oxygen. B. Thay đổi tốc độ của
c. C. Thay đổi áp suất
ủa
c. D. Thay đổi nhiệt độ của
c.
ống b
ng và lọc nƣớc. Ngƣời ta đã vận dụng nguyên tắc nào để làm tăng tốc độ
hóa?
xúc
2+
nƣớ
c
nƣớ
nƣớ
Câu 4: Tốc độ của phản ứng tăng lên khi:
A. giảm nhiệt độ.
B. tăng diện tích tiếp xúc giữa các chất phản ứng.
C. tăng lƣợng chất xúc tác.
D. giảm lƣợng chất tham gia phản ứng.
Câu 5: Trong các phản ứng sau đây, nếu lƣợng Fe và thể tích dung dịch acid HCl trong các phản ứng đều đƣợc lấy bằng nhau thì cặp chất nào có tốc độ phản ứng lớn nhất?
A. Fe + dd HCl 0,1M.
B. Fe + dd HCl 0,2M. C. Fe + dd HCl 0,3M. D. Fe + dd HCl 10%, (d = 1 g/ml).
OFFICIAL
Câu 6: Để hòa tan một tấm Zn trong dung dịch acid HCl ở 20oC thì cần 27 phút, cũng tấm Zn đó tan hết trong dung dịch acid HCl nói trên ở 40oC trong 3 phút. Vậy để hòa tan hết tấm Zn đó trong dung dịch HCl trên ở 60oC cần bao nhiêu thời gian?
A. 60 s. B. 34,64 s. C. 40 s. D. 20 s. Câu 7: Khi ninh (hầm) thịt, cá, để chúng nhanh chín ngƣời ta thƣờng: A. Dùng nồi áp suất để nấu. B. Thái thành nhiều miếng nhỏ. C. Đun lửa lớn đều, vừa. D. Cả ba phƣơng án trên đều đúng.
Câu 8: Tăng nhiệt độ của một hệ phản ứng sẽ dẫn đến sự va chạm có hiệu quả giữa các phân tử chất phản ứng. Tính chất của sự va chạm đó là:
A. Thoạt đầu tăng, sau đó giảm dần. B. Chỉ có giảm dần.
C. Thoạt đầu giảm, sau đó tăng dần. D. Chỉ có tăng dần.
Câu 9: Cho 5 gam Zn viên vào cốc đựng 5 ml dung dịch acid H2SO4 4M ở nhiệt độ phòng. Trƣờng hợp nào sau đây tốc độ phản ứng không đổi? A. Thực hiện phản ứng ở 50oC. B. Thay dung dịch acid H2SO4 4M bằng dung dịch acid H2SO4 2M. C. Dùng dung dịch acid H2SO4 gấp đôi
DẠYKÈMQUYNHƠN
ban đầu. D. Thay 5 gam Zn viên bằng 5 gam
bột. Câu 10: Cho ba mẫu đá vôi
3) có
khối
ng: mẫu 1 dạng khối, mẫu 2 dạng viên nhỏ, mẫu 3 dạng bột mịn vào 3 cốc đựng cùng thể tích dung dịch acid HCl (dƣ, cùng nồng độ, ở điều kiện thƣờng). Thời gian để đá vôi tan hết trong ba cốc tƣơng ứng là t1, t2, t3 giây. So
nào sau đây đúng ? A. t1 = t2 = t3. B. t1 < t2 < t3. C. t2 < t1 < t3. D. t3 < t2 < t1.
Zn
(100% CaCO
cùng
lƣợ
sánh
Phần II: Tự luận. Câu 11: Hãy cho biết ngƣời ta lợi dụng yếu tố nào để tăng tốc độ phản ứng các trƣờng hợp sau và giải thích:
1. Chẻ nhỏ củi khi nấu bếp củi.
2. Bật lửa lớn khi đun nấu để thức ăn chín nhanh hơn.
3. Que đóm đang cháy trong không khí khi đƣa vào trong bình chứa oxygen thì cháy to và mạnh hơn. Câu 12: Khảo sát các yếu tố ảnh hƣởng tới tốc độ phản ứng. Để tìm hiểu về các yếu tố ảnh hƣởng đến tốc độ phản ứng, ngƣời ta thực hiện thí nghiệm giữa Zinc và dung dịch sulfuric acid loãng. Bảng dƣới đây cho biết kết quả của 6 thí nghiệm xảy ra. Trong mỗi thí nghiệm, ngƣời ta dùng 0,3 gam Zinc tácdụng với thể tích bằng nhau của acid, nhƣng có nồng độ khác nhau.
OFFICIAL
DẠYKÈMQUYNHƠN
Nồng
Dạng
1 1M 25
2 1M 25
3 2M 25
4 2M 50
5 2M 50
6 3M 50
1.
2. Từ các phản ứng trên,
giải
sự ảnh
phản ứng? 3. Nếu song song với thí nghiệm 3, ta
3*
thí nghiệm 3 nhƣng
3*
3.
và giải thích?
Thí nghiệm
độ acid Nhiệt độ (oC)
của Zn Thời gian phản ứng (s)
Viên 220
Bột 105
Bột 92
Viên 55
Bột 30
Bột 11
Những thí nghiệm nào nói lên đƣợc sự ảnh hƣởng của các yếu tố đến tốc độ phản ứng?
hãy
thích
hƣởng của nhiệt độ tới tốc độ
thực hiện một thí nghiệm
giống với
chỉ thay đổi lƣợng acid dùng trong thí nghiệm
gấp đôi lƣợng acid dùng trong thí nghiệm
Nhận xét về tốc độ của 2 thí nghiệm
Phụ
ục 4
DẠYKÈMQUYNHƠN OFFICIAL
l
PHIẾU KHẢO SÁT
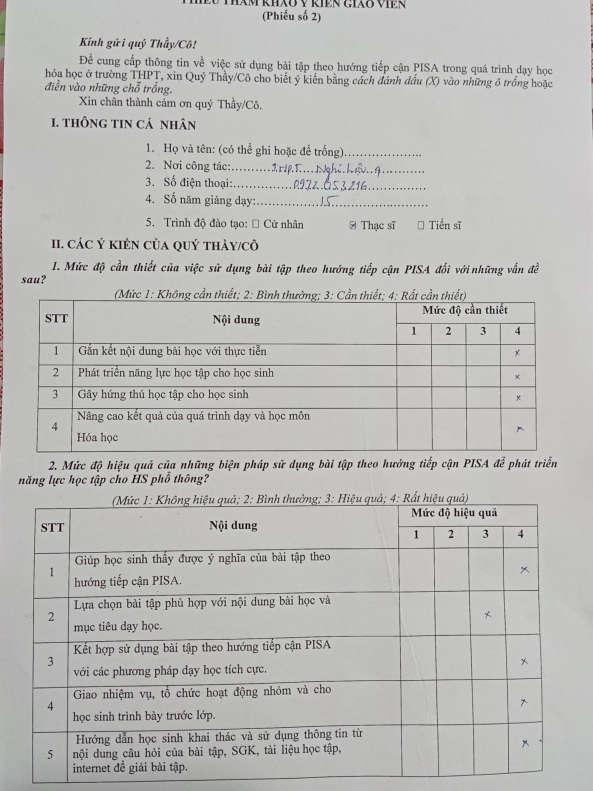
DẠYKÈMQUYNHƠN OFFICIAL
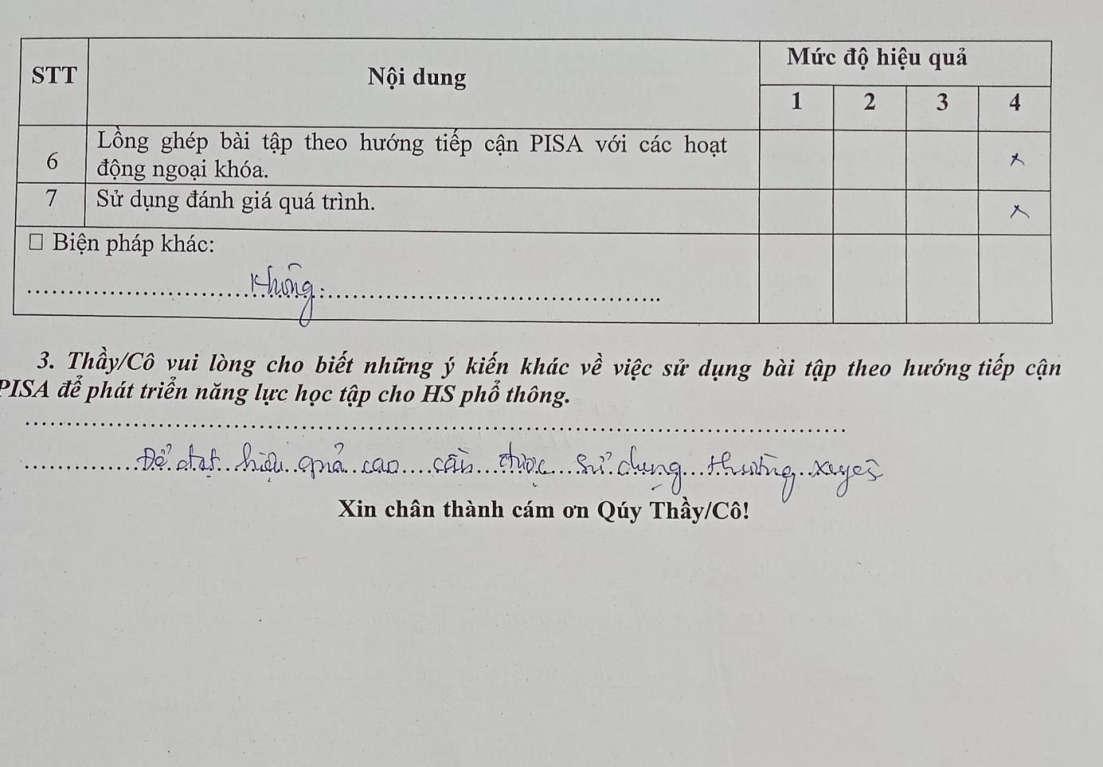
DẠYKÈMQUYNHƠN OFFICIAL
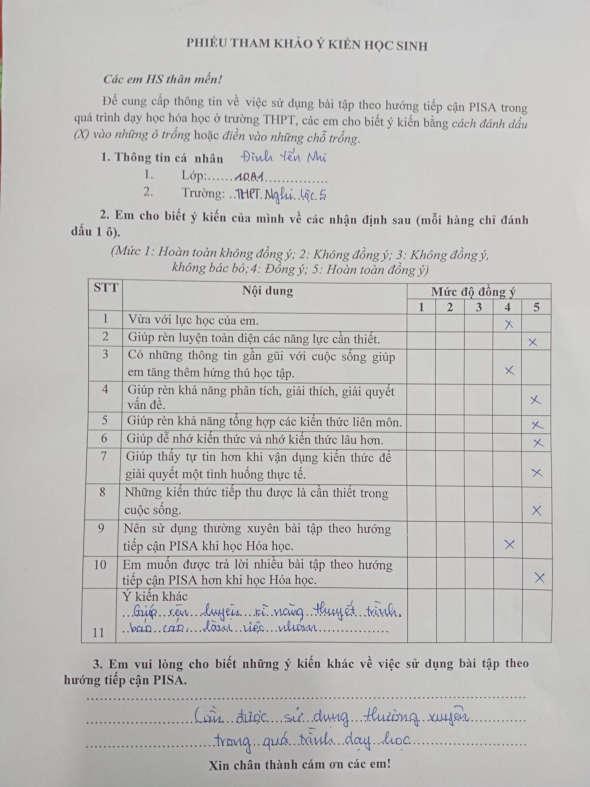
DẠYKÈMQUYNHƠN OFFICIAL























































