5 minute read
Psoriasis artrit-patienter, TNF-hæmmere og hæmatologiske cancere
En nylig nordisk registerundersøgelse har vist, at personer med psoriasis artrit (PsA) har en let til moderat øget risiko for at udvikle hæmatologiske cancere sammenlignet med alders- og kønsmatchede individer fra den almindelige befolkning. Undersøgelsen har dog også afsløret, at patienter med PsA, der er blevet behandlet med TNF-hæmmere, ikke har en øget risiko for hæmatologiske cancere sammenlignet med PsA-patienter, der ikke er blevet behandlet med TNF-hæmmere.
RENÉ CORDTZ er uddannet læge fra Københavns Universitet og har en ph.d. inden for reumatologisk epidemiologi. Han arbejder som post.doc. ved Center of Rheumatic Research Aalborg ved Aalborg Universitetshospital. LENE DREYER er klinisk lærestolsprofessor og specialeansvarlig overlæge i reumatologi ved Aalborg Universitet og Aalborg Universitetshospital. Hun er leder af Center of Rheumatic Research Aalborg (CERRA) og medlem af Dansk Reumatologisk Database (DANBIO)’s styregruppe.
Patienter med psoriasis artrit (PsA) har en øget forekomst af adskillige komorbiditeter.1 Der findes dog ikke et entydigt klart billede af, om hæmatologiske cancere hører til i denne byrde af komorbiditeter, hvilket ellers er tilfældet ved andre reumatologiske sygdomme med inflammation, herunder reumatoid artrit og systemisk lupus erythematosus.2,3 Det er heller ikke velundersøgt, om incidensen er forhøjet for undertyper som lymfoide og myeloide maligniteter sammenlignet med generelbefolkningen.4,5
I den moderne behandling af PsA indgår TNF-hæmmere som et vigtigt element i det samlede behandlingsrepertoire. Selvom det for reumatoid artrit er velbelyst, at behandling med TNF-hæmmere ikke er associeret med en øget incidens af hæmatologiske cancere, så er det forholdsvis mindre klart, hvorvidt det også er tilfældet for PsA-patienter behandlet med TNF-hæmmere.
Idet hæmatologiske cancere er forholdsvis sjældne cancertyper, søgte vi i et nordisk forskningssamarbejde at undersøge incidensen af denne cancertype hos PsA-patienter identificeret igennem de nordiske kliniske kvalitetsregistre for artritsygdomme.6 Studiets primære formål var at undersøge incidensen af hæmatologiske cancere hos patienter behandlet med TNF-hæmmere sammenlignet med PsA-patienter, der ikke fik behandling med TNF-hæmmere eller andre biologiske lægemidler. Som et sekundært formål blev incidensen af hæmatologiske cancere hos samtlige PsA-patienter sammenlignet med generelbefolkningen.
Identifikation af PsA-patienter og kontrolgrupper
Alle patienter med PsA blev identificeret i de kliniske, reumatologiske, forsknings- og kvalitetsregistre i Danmark (DANBIO), Finland (ROB-FIN), Island (ICEBIO), Norge (NOR-DMARD) og Sverige (SRQ). Denne kohorte af
PsA-patienter blev grupperet efter, om de var behandlet med TNF-hæmmere eller ej. For Danmark og Sverige blev der fra de to landes hospitalsregistre ligeledes identificeret endnu en gruppe af PsA-patienter, der ikke fik TNF-hæmmerbehandling. Danske og svenske patienter, der havde fået behandling med TNF-hæmmere, blev hver matchet med op til ti individer fra generelbefolkningen af samme alder og køn (og for svenske patienter, bopælsregion).
Med udgangspunkt i de danske og svenske data blev der dannet en overordnet PsA-kohorte bestående af alle PsA-patienter fra DANBIO, SRQ og de to førnævnte grupper af PsA-patienter fra hospitalsregistrene. Hver PsA-patient blev også her matchet på alder og køn med 10 individer fra generelbefolkningen.
Identifikation af hæmatologiske
cancere
Ved kobling med de respektive landes cancerregistre blev tilfælde af hæmatologiske cancere identificeret. Disse blev i sekundære analyser analyseret separat, alt efter om de var lymfoide eller myeloide maligniteter.
Opfølgning af behandling med TNF-hæmmere
TNF-hæmmer-behandlede patienter blev fulgt fra datoen for deres første TNF-hæmmer-behandling, mens TNF-hæmmer-naive patienter blev fulgt fra datoen for deres første registrerede ambulante besøg i det kliniske kvalitetsregister eller anden diagnosedato for PsA registreret i hospitalsregisteret. Alle patienter blev fulgt indtil datoen for deres første hæmatologiske cancer, emigration, død eller ved datoen for data-cut (forskellig for de involverede lande), alt efter hvad der kom først. Derudover blev TNF-hæmmer-naive PsA-patienter censureret, hvis de startede i behandling med et biologisk lægemiddel.
Statistisk analyse
Med brug af data fra alle fem lande beregnede vi i en modificeret Poisson-regressionsanalyse en poolet incidensrateratio (IRR) med 95% konfidensinterval for hæmatologiske cancere hos PsA-patienter behandlet med TNF-hæmmere sammenlignet med de PsApatienter, der ikke fik TNF-hæmmere.
Med danske og svenske data blev der også beregnet en justeret IRR for hæmatologiske cancere hos TNFhæmmer-behandlede patienter sammenlignet med TNF-hæmmer-naive PsA-patienter fra hospitalsregistrene. Ydermere beregnede vi den justerede IRR for TNF-hæmmer-behandlede patienter sammenlignet med matchede kontroller fra generelbefolkningen.
For at vurdere risikoen for hæmatologisk cancer i den overordnede danske og svenske PsA-kohorte (med alle PsA-patienter fra DANBIO, SRQ samt de danske og svenske hospitalsregistre) blev der beregnet en justeret IRR sammenlignet med matchede kontroller.
I sekundære analyser undersøgte vi for hver af ovenstående sammenligninger den separate IRR for hhv. lymfoide og myeloide maligniteter.
TNF-hæmmer, hæmatologiske cancere og PsA
I alt blev 10.621 TNF-hæmmer-behandlede patienter sammenlignet med 18.387 TNF-hæmmer-naive patienter.
Størstedelen af patienterne kom fra svenske SRQ (55%) og danske DANBIO (32%). Ved behandlingens start var patienter behandlet med TNF-hæmmere i alle lande yngre end tilsvarende TNF-hæmmer-naive patienter fra samme land og havde desuden højere DAS28-CRP, mens kønsratioen var nogenlunde ens.
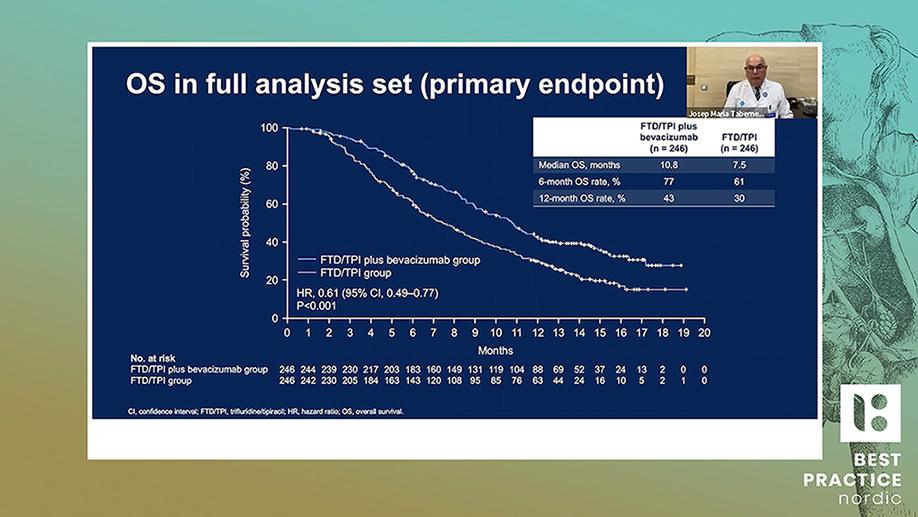
Sammenlignet med TNF-hæmmer-naive patienter var der ikke en øget incidens af hæmatologiske cancere hos patienter behandlet med TNF-hæmmere ; dette baseret på hhv. 63 og 40 tilfælde : IRR 1,0 (0,7 til 1,4).
Sammenlignet med de TNF-hæmmer-naive PsApatienter fra Danmarks og Sveriges hospitalsregistre var der heller ikke en øget incidens baseret på hhv. 172 og 35 tilfælde : IRR 0,8 (0,6 til 1,1).
Derimod sås en øget incidens, når TNF-hæmmerbehandlede blev sammenlignet med deres matchede kontroller fra generelbefolkningen, her baseret på 35 mod 125 tilfælde : IRR 1,4 (1,0 til 1,9).
Den øgede incidens var dog generel for hele PsAkohorten, idet den havde en IRR på 1,4 (1,2 til 1,6) sammenlignet med de matchede kontroller, her baseret på 236 mod 908 tilfælde.
Disse IRR-estimater var stort set identiske for både lymfoide og myeloide maligniteter. Derudover viste resultaterne sig særdeles robuste i adskillige sensitivitetsanalyser.
Figur 1 – Incidensrateratioer for hæmatologiske cancere hos patienter med psoriasis artrit
Figur 1 – Incidensrateratioer for hæmatologiske cancere hos patienter med psoriasis artrit
Hæmatologisk cancer
TNF-hæmmer behandlede vs bionaive (kvalitetsregistre)
TNF-hæmmer behandlede vs bionaive (hospitalsregistre)
TNF-hæmmer behandlede vs matchede kontrolindivider
PsA kohorte vs matchede kontrolindivider
Figuren viser justerede incidensrateratioer for hhv. hæmatologiske cancere, lymfoide og myeloide maligniteter. Figuren er opdelt efter, hvilke grupper der sammenlignes, hvilket konkret udfald der undersøges, samt hvilke lande der bidrog med data til den pågældende analyse. DK : Danmark, NO : Norge, SE : Sverige, FI : Finland. Figur tilpasset fra : Cordtz RL et al. Haematological malignancies in patients with psoriatic arthritis overall and treated with TNF inhibitors : a Nordic cohort study. RMD Open. 2022 Dec ;8(2).
Figuren viser justerede incidensrateratioer for hhv. hæmatologiske cancere, lymfoide og myeloide maligniteter. Figuren er opdelt efter, hvilke grupper der sammenlignes, hvilket konkret udfald der undersøges, samt hvilke lande der bidrog med data til den pågældende analyse. DK: Danmark, NO: Norge, SE: Sverige, FI: Finland. Figur tilpasset fra: Cordtz RL et al. Haematological malignancies in patients with psoriatic arthritis overall and treated with TNF inhibitors: a Nordic cohort study. RMD Open. 2022 Dec;8(2).
Referencer :
1. Shah K, Paris M, Mellars L, Changolkar A, Mease PJ. Real-world burden of comorbidities in US patients with psoriatic arthritis. RMD Open. 2017 ;3(2) : e000588. DOI :10.1136/rmdopen-2017-000588
2. Baecklund E, Smedby KE, Sutton LA, Askling J, Rosenquist R. Lymphoma development in patients with autoimmune and inflammatory disorders – what are the driving forces ? Semin Cancer Biol. Feb 2014 ;24 : 61-70. DOI :10.1016/j.semcancer.2013.12.001
4. Vaengebjerg S, Skov L, Egeberg
3. Gross RL, Schwartzman-Morris JS, Krathen M, et al. A comparison of the malignancy incidence among patients with psoriatic arthritis and patients with rheumatoid arthritis in a large US cohort. Arthritis Rheumatol. Jun 2014 ;66(6) : 1472-1481. DOI :10.1002/art.38385
A, Loft ND. Prevalence, Incidence, and Risk of Cancer in Patients With Psoriasis and Psoriatic Arthritis : A Systematic Review and Meta-analysis. JAMA Dermatol. Apr 1 2020 ;156(4) : 421-429. DOI :10.1001/jamadermatol.2020.0024
5. Polachek A, Muntyanu A, Lee KA, et al. Malignancy in psoriatic disease : Results from prospective longitudinal cohorts. Semin Arthritis Rheum. Feb 2021 ;51(1) : 144-149. DOI :10.1016/j.semarthrit.2020.12.008
6. Cordtz RL, Askling J, Delcoigne B, et al. Haematological malignancies in patients with psoriatic arthritis overall and treated with TNF inhibitors : a Nordic cohort study. RMD Open. Dec 2022 ; 8(2). DOI :10.1136/rmdopen-2022-002776.
INTERESSEKONFLIKTER : René Cordtz er ansat ved IQVIA uden for dette arbejde. Lene Dreyer har modtaget honorarer for oplæg/ betalt kongresrejse fra Abbvie, Eli Lilly, Galderma, og Janssen og projekt-forskningsbevilling fra BMS uden for dette projekt.