2 minute read
COMPOSIZIONE QUALITATIVA E QUANTITATIVA
Grazie ad un’efficace randomizzazione i due gruppi di pazienti, quelli trattati con il farmaco (n=261) e quelli trattati con placebo (n=131) erano assolutamente simili in termini di età media, sesso, aree geografiche di provenienza, istotipo di carcinoma tiroideo e distribuzione delle metastasi a distanza.
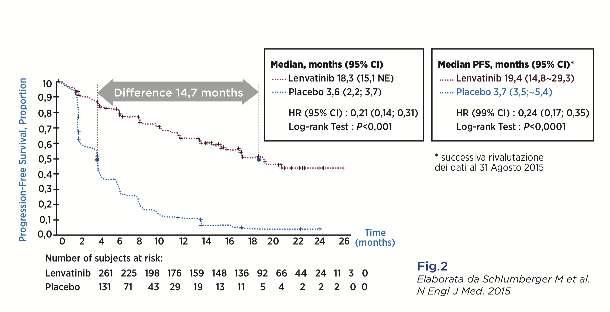
Al momento della prima analisi lo studio ha mostrato un prolungamento statisticamente significativo della PFS mediana con una differenza tra i due gruppi di 14,7 mesi (Fig. 2). Una successiva rivalutazione dei dati al 31 Agosto 2015, mostrava un ulteriore incremento della differenza della PFS (15,7 mesi) tra i pazienti trattati con il farmaco o con il placebo. La durata di risposta media risultava inoltre di 30 mesi (18,4-35,2 mesi) (Fig. 2).
Advertisement
Tra gli obiettivi secondari i pazienti trattati con lenvatinib mostravano una OOR nel 65% dei casi rispetto ad un 2% di quelli trattati con placebo. La riduzione maggiore delle lesioni si osservava nei primi due mesi di trattamento e continuava fino a due anni dall’inizio della terapia, sebbene più lentamente. Da segnalare che 4 pazienti trattati con lenvatinib (2%) hanno mostrato una risposta completa al farmaco con scomparsa delle lesioni target. La OS non ha mostrato alcun miglioramento nei pazienti trattati con il farmaco ma occorre conside- rare che lo studio prevedeva la possibilità che i pazienti trattati con placebo, una volta in progres- sione, potessero iniziare la terapia farmacologica con lenvatinib (cross-over). Questa possibilità, certamente utile per i pazienti, ha avuto un impatto sul calcolo della OS tanto è vero che, dopo un aggiustamento statistico secondo un metodo in grado di tenere conto del cross-over (rank-preserving structural failure time [RPSFT]), la OS risultava significativamente aumentata nei pazienti trattati con lenvatinib. Per quanto riguarda gli effetti collaterali quelli che si sono dimostrati di gran lunga più frequenti sono l’incremento della pressione arteriosa (68%), seguito dalla diarrea (60%), dalla astenia/fatigue (59%), perdita di appetito (50%). Altri effetti collaterali da ricordare sono la nausea, la perdita di peso, la mucosite, la sindrome mano-piede e la proteinuria. La gestione degli effetti collaterali all’interno dello studio SELECT ha portato alla riduzione del dosaggio giornaliero di lenvatinib nel 67,8% dei casi con un dosaggio medio per giorno di 17,2 mg. La prima riduzione di dose si verificava media- mente dopo 3 mesi dall’inizio della terapia. Riteniamo che l’aumento della conoscenza di lenvatinib da parte dei clinici, derivata dalla sua diffusione sul territorio e dell’informazione sugli effetti collaterali (ad esempio, con brochure informative), possa migliorare la gestione degli effetti collaterali nella pratica clinica, consenten- do addirittura di prevenirli laddove possibile. Tale conoscenza consentirà di mantenere i pazienti in terapia più a lungo, cercando di evitare il più possibile le interruzioni del trattamento e le riduzioni di dose, massimizzando l’efficacia di lenvatinib in assenza di altre valide alternative terapeutiche.
Distinguendo i soggetti trattati in sottogruppi si sono potuti osservare alcuni dati importanti: a- soggetti di età superiore ai 65 anni presentavano una risposta alla terapia simile a quella dei soggetti più giovani in termini di PFS ma, al contrario di questi, presentavano un significativo incremento della OS (p=0,02). b- il sottogruppo di pazienti con istotipo follicolare presentava un significativo incremento della OS quando trattati con il lenvatinib rispetto al placebo (p<0,035). In entrambi i casi tale differenza statistica era ottenuta senza alcun aggiustamento per il cross-over.
segue a pagina 3



