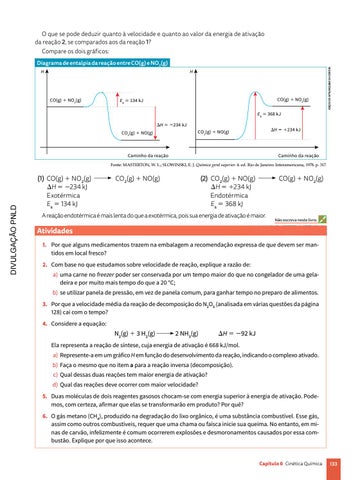
O que se pode deduzir quanto à velocidade e quanto ao valor da energia de ativação da reação 2, se comparados aos da reação 1? Diagrama de entalpia da reação entre CO(g) e NO2(g) H
H
CO(g) 1 NO2(g)
CO(g) 1 NO2(g)
Ea 5 134 kJ
EDIÇÃO DE ARTE/ARQUIVO DA EDITORA
Compare os dois gráficos:
Ea 5 368 kJ DH 5 2234 kJ CO2(g) 1 NO(g)
DH 5 1234 kJ
CO2(g) 1 NO(g)
Caminho da reação
Caminho da reação
DIVULGAÇÃO PNLD
Fonte: MASTERTON, W. L.; SLOWINSKI, E. J. Química geral superior. 4. ed. Rio de Janeiro: Interamericana, 1978. p. 317.
(1) CO(g) 1 NO2(g) DH 5 2234 kJ Exotérmica Ea 5 134 kJ
(2) CO2(g) 1 NO(g) DH 5 1234 kJ Endotérmica Ea 5 368 kJ
CO2(g) 1 NO(g)
CO(g) 1 NO2(g)
A reação endotérmica é mais lenta do que a exotérmica, pois sua energia de ativação é maior.
Não escreva neste livro.
Atividades 1. Por que alguns medicamentos trazem na embalagem a recomendação expressa de que devem ser mantidos em local fresco? 2. Com base no que estudamos sobre velocidade de reação, explique a razão de: a) uma carne no freezer poder ser conservada por um tempo maior do que no congelador de uma geladeira e por muito mais tempo do que a 20 °C; b) se utilizar panela de pressão, em vez de panela comum, para ganhar tempo no preparo de alimentos. 3. Por que a velocidade média da reação de decomposição do N2O5 (analisada em várias questões da página 128) cai com o tempo? 4. Considere a equação:
N2(g) 1 3 H2(g)
2 NH3(g) DH 5 292 kJ
Ela representa a reação de síntese, cuja energia de ativação é 668 kJ/mol. a) Represente-a em um gráfico H em função do desenvolvimento da reação, indicando o complexo ativado. b) Faça o mesmo que no item a para a reação inversa (decomposição). c) Qual dessas duas reações tem maior energia de ativação? d) Qual das reações deve ocorrer com maior velocidade? 5. Duas moléculas de dois reagentes gasosos chocam-se com energia superior à energia de ativação. Podemos, com certeza, afirmar que elas se transformarão em produto? Por quê? 6. O gás metano (CH4), produzido na degradação do lixo orgânico, é uma substância combustível. Esse gás, assim como outros combustíveis, requer que uma chama ou faísca inicie sua queima. No entanto, em minas de carvão, infelizmente é comum ocorrerem explosões e desmoronamentos causados por essa combustão. Explique por que isso acontece.
Capítulo 6 Cinética Química
EME18_VIVA_QU2_U3C6_120A153.indd 133
133
10/06/16 19:06