Comprobando el descenso del punto de congelación del naftaleno
Laboratorio 6 Antecedentes
El naftaleno (C10H8), conocido comúnmente como naftalina, es un sólido blanco que se produce por la combustión de combustibles fósiles. Esta sustancia se emplea como materia prima para la síntesis de una variedad de productos químicos, como los antipolillas y los conservantes de madera, entre otros. Reactivos · naftaleno (C10H8) · p-diclorobenceno (C6H4Cl2) · agua destilada Materiales · vaso de precipitado de 250 mL • dos tubos de ensayo • vidrio de reloj · mechero, trípode y rejilla · soporte universal, pinza y nuez · termómetro · balanza · espátula
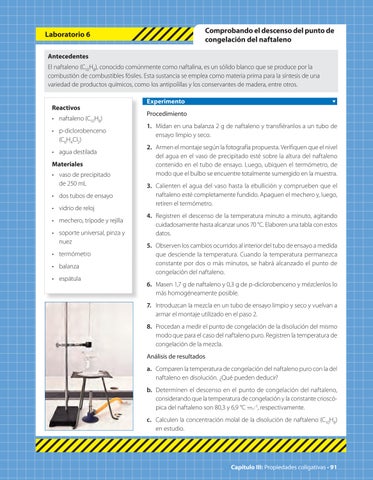
Experimento Procedimiento 1. Midan en una balanza 2 g de naftaleno y transfiéranlos a un tubo de ensayo limpio y seco. 2. Armen el montaje según la fotografía propuesta. Verifiquen que el nivel del agua en el vaso de precipitado esté sobre la altura del naftaleno contenido en el tubo de ensayo. Luego, ubiquen el termómetro, de modo que el bulbo se encuentre totalmente sumergido en la muestra. 3. Calienten el agua del vaso hasta la ebullición y comprueben que el naftaleno esté completamente fundido. Apaguen el mechero y, luego, retiren el termómetro. 4. Registren el descenso de la temperatura minuto a minuto, agitando cuidadosamente hasta alcanzar unos 70 °C. Elaboren una tabla con estos datos. 5. Observen los cambios ocurridos al interior del tubo de ensayo a medida que desciende la temperatura. Cuando la temperatura permanezca constante por dos o más minutos, se habrá alcanzado el punto de congelación del naftaleno. 6. Masen 1,7 g de naftaleno y 0,3 g de p-diclorobenceno y mézclenlos lo más homogéneamente posible. 7. Introduzcan la mezcla en un tubo de ensayo limpio y seco y vuelvan a armar el montaje utilizado en el paso 2. 8. Procedan a medir el punto de congelación de la disolución del mismo modo que para el caso del naftaleno puro. Registren la temperatura de congelación de la mezcla. Análisis de resultados a. Comparen la temperatura de congelación del naftaleno puro con la del naftaleno en disolución. ¿Qué pueden deducir? b. Determinen el descenso en el punto de congelación del naftaleno, considerando que la temperatura de congelación y la constante crioscópica del naftaleno son 80,3 y 6,9 °C -1, respectivamente.
m
c. Calculen la concentración molal de la disolución de naftaleno (C10H8) en estudio.
Capítulo III: Propiedades coligativas • 91