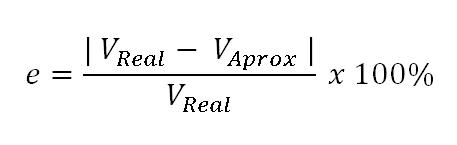
7 minute read
CALOR ESPECIFICO
- La dilatación o contracción térmica existe en cualquier tipo de material, pero no en todos los materiales se puede apreciar a simple vista.
- No todos los objetos y/o materiales se van a dilatar a la misma proporción.
Advertisement
- Del experimento 3, se puede deducir que no todos los materiales vuelven a su forma original después de exponerlos a un aumento de temperatura.
RESUMEN: CALOR ESPECIFICO
Se evidencio la transferencia de calor en algunos metales como el hierro, cobre, grafito, oro, entre otros con ayuda del simulador propuesto por la docente, se determinó su capacidad calorífica y su calor especifico gracias a las fórmulas para su óptimo despeje de la guía número 6.
INTRODUCCIÓN:
En este informe se adquirieron conocimientos de calor específico, la importancia de este en escenarios de la vida cotidiana y además el cómo podemos calcular tanto el calor específico como su capacidad calorífica de algunos metales. Pero ¿Qué es el calor especifico?
En resumen, el calor específico es la cantidad de calor que por kilogramo necesita un cuerpo para que su temperatura se eleve en un grado centígrado. Lo podemos encontrar como una constante para diferentes tipos de materiales, el calor específico se solicita a la hora de calcular la capacidad calorífica y la cantidad de calor.
Para el desarrollo del laboratorio utilizamos las siguientes ecuaciones:
La capacidad calorífica de un cuerpo es el cociente entre la cantidad de energía calorífica transferida a un cuerpo o sistema en un proceso cualquiera y el cambio de temperatura que experimenta. Cuanto mayor sea la capacidad calorífica de una sustancia, mayor será la cantidad de calor entregada a ella para subir su temperatura. Esta dada por esta ecuación:
Como se puede observar en la ilustración 1. Algunos valores de calor específico para diferentes materiales
Ilustración 1. Calor específico.
Ecuación 1. Capacidad calorífica Como se puede observar en la ecuación 1, está conformada por “m” que es la masa y “c” que es la constante de calor especifico.
La Cantidad de calor se define como la energía cedida o absorbida por un cuerpo de masa cuando su temperatura varía en un número determinado de grados. Esta dada por la siguiente ecuación.
Ecuación 2. Cantidad de calor Como se puede observar en la ecuación 2, donde ���� es la temperatura inicial y ���� es la final, las demás variables se explicaron anteriormente.
Ecuación 4. Despeje del calor específico del material que pierde energía.
El porcentaje de error es una operación que permite determinar de forma clara el margen de error entre las diferencias existentes entre el valor estimado y el valor real, por lo que, si se quiere obtener dicha respuesta, se hace indispensable tener ambos valores para realizar la operación matemática
Nuestro objetivo fue experimentar, analizar y pensar en cómo resolver el despeje del calor especifico con los datos obtenidos gracias al simulador y a las ecuaciones dadas.
MÉTODO EXPERIMENTAL:
Para el experimento usamos el simulador de la imagen 1. Calentamos los diferentes materiales (6 materiales) hasta que alcanzaran los 100°C y luego se introducían en un recipiente con agua a 20°C y el material permanecía dentro del recipiente hasta que se alcanzara el equilibrio térmico. Después tomamos datos y calculamos el calor específico de cada material (Ecuación 4), la capacidad calorífica del material (Ecuación 1) y el porcentaje de error (Ecuación 5).

Imagen 1. Simulador.
RESULTADOS Y ANALISIS:
Mediante la Ecuación 4 se calculó el calor específico de cada sistema respectivamente (Tabla 1- Hierro, Tabla 2- Cobre, Tabla 3 – Grafito, Tabla 4 – Oro, Tabla 5- Berilio, Tabla 6 –Aluminio).
T0 agua Tf agua m (kg) T0 (°C) Tf(°C) c(J/kg °C) m agua (kg) (°C) (°C) c agua (J/g°C) C(J/°C) 0,02 100 20,9 476,28 0,2 20 20,9 4186 9,53 0,025 100 21,1 466,88 0,2 20 21,1 4186 11,67 0,03 100 21,3 460,97 0,2 20 21,3 4186 13,83 0,035 100 21,5 457,07 0,2 20 21,5 4186 16,00 0,04 100 21,7 454,42 0,2 20 21,7 4186 18,18 0,045 100 21,9 452,60 0,2 20 21,9 4186 20,37 0,05 100 22,1 451,38 0,2 20 22,1 4186 22,57 0,055 100 22,3 450,58 0,2 20 22,3 4186 24,78 0,06 100 22,5 450,11 0,2 20 22,5 4186 27,01 0,065 100 22,7 449,88 0,2 20 22,7 4186 29,24
Promedio c (J/kg°C) 457,02
Tabla 1. Sistema Hierro-Agua.
T0 agua Tf agua m (kg) T0 (°C) Tf(°C) c(J/kg °C) m agua (kg) (°C) (°C) c agua (J/g°C) C(J/°C) 0,02 100 20,7 369,51 0,2 20 20,7 4186 7,39
0,025 100 20,9 381,03 0,2 20 20,9 4186 9,53 0,03 100 21,1 389,07 0,2 20 21,1 4186 11,67 0,035 100 21,3 395,12 0,2 20 21,3 4186 13,83 0,04 100 21,4 372,80 0,2 20 21,4 4186 14,91 0,045 100 21,6 379,68 0,2 20 21,6 4186 17,09 0,05 100 21,8 385,41 0,2 20 21,8 4186 19,27 0,055 100 22 390,30 0,2 20 22 4186 21,47 0,06 100 22,1 376,15 0,2 20 22,1 4186 22,57 0,065 100 22,3 381,26 0,2 20 22,3 4186 24,78
Promedio c (J/kg°C) 382,03
Tabla 2. Sistema Cobre-Agua.
T0 agua Tf agua m (kg) T0 (°C) Tf(°C) c(J/kg °C) m agua (kg) (°C) (°C) c agua (J/g°C) C(J/°C) 0,02 100 21,3 691,46 0,2 20 21,3 4186 13,83 0,025 100 21,7 727,07 0,2 20 21,7 4186 18,18 0,03 100 22 715,56 0,2 20 22 4186 21,47 0,035 100 22,3 708,06 0,2 20 22,3 4186 24,78 0,04 100 22,6 703,07 0,2 20 22,6 4186 28,12 0,045 100 22,9 699,78 0,2 20 22,9 4186 31,49 0,05 100 23,3 720,41 0,2 20 23,3 4186 36,02 0,055 100 23,6 717,26 0,2 20 23,6 4186 39,45 0,06 100 23,9 715,09 0,2 20 23,9 4186 42,91 0,065 100 24,2 713,67 0,2 20 24,2 4186 46,39
Promedio c (J/kg°C) 711,14
Tabla 3. Sistema Grafito-Agua.

Gráfica 1. Capacidad calorífica hierro, cobre, grafito vs Masa.
- La capacidad calórica aumenta a mayor masa como se puede observar en la Gráfica 1.
T0 agua Tf agua m (kg) T0 (°C) Tf(°C) c(J/kg °C) m agua (kg) (°C) (°C) c agua (J/g°C) C(J/°C) 0,075 100 20,9 127,01 0,2 20 20,9 4186 9,53 0,07 100 20,9 136,08 0,2 20 20,9 4186 9,53 0,065 100 20,8 130,10 0,2 20 20,8 4186 8,46 0,06 100 20,7 123,17 0,2 20 20,7 4186 7,39 0,055 100 20,7 134,37 0,2 20 20,7 4186 7,39 0,05 100 20,6 126,53 0,2 20 20,6 4186 6,33 0,045 100 20,6 140,59 0,2 20 20,6 4186 6,33 0,04 100 20,5 131,64 0,2 20 20,5 4186 5,27 0,035 100 20,4 120,20 0,2 20 20,4 4186 4,21 0,03 100 20,4 140,23 0,2 20 20,4 4186 4,21
Promedio c (J/kg°C) 130,99
Tabla 4. Sistema Oro-Agua.
T0 agua Tf agua m (kg) T0 (°C) Tf(°C) c(J/kg °C) m agua (kg) (°C) (°C) c agua (J/g°C) C(J/°C) 0,075 100 31,2 1817,18 0,2 20 31,2 4186 136,29 0,07 100 30,6 1826,74 0,2 20 30,6 4186 127,87 0,065 100 29,9 1819,00 0,2 20 29,9 4186 118,24 0,06 100 29,2 1813,15 0,2 20 29,2 4186 108,79 0,055 100 28,5 1809,59 0,2 20 28,5 4186 99,53 0,05 100 27,8 1808,91 0,2 20 27,8 4186 90,45 0,045 100 27,1 1811,96 0,2 20 27,1 4186 81,54 0,04 100 26,4 1820,00 0,2 20 26,4 4186 72,80 0,035 100 25,7 1835,05 0,2 20 25,7 4186 64,23 0,03 100 24,9 1820,81 0,2 20 24,9 4186 54,62
Promedio c (J/kg°C) 1818,24
Tabla 5. Sistema Berilio-Agua.
T0 agua Tf agua m (kg) T0 (°C) Tf(°C) c(J/kg °C) m agua (kg) (°C) (°C) c agua (J/g°C) C(J/°C) 0,075 100 26 905,08 0,2 20 26 4186 67,88 0,07 100 25,6 900,22 0,2 20 25,6 4186 63,02 0,065 100 25,2 895,40 0,2 20 25,2 4186 58,20 0,06 100 24,8 890,64 0,2 20 24,8 4186 53,44 0,055 100 24,5 907,26 0,2 20 24,5 4186 49,90
0,05 100 24,1 904,48 0,2 20 24,1 4186 45,22 0,045 100 23,7 902,18 0,2 20 23,7 4186 40,60 0,04 100 23,3 900,51 0,2 20 23,3 4186 36,02 0,035 100 22,9 899,71 0,2 20 22,9 4186 31,49 0,03 100 22,5 900,22 0,2 20 22,5 4186 27,01
Promedio c (J/kg°C) 900,57
Tabla 6. Sistema Aluminio-Agua.
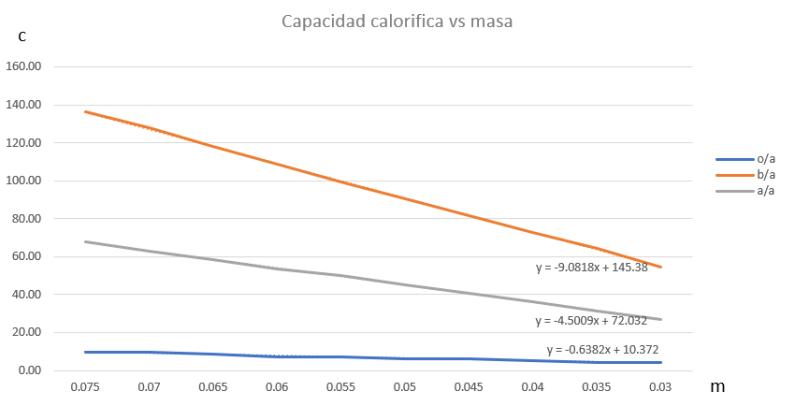
Gráfica 2. Capacidad calorífica vs Masa.
- Cuando el sistema se encuentra en equilibrio térmico la temperatura final del material y del agua son iguales (Tablas 1 a 6). - La capacidad calórica disminuye a menor masa como se puede observar en la Gráfica 2.
Teniendo en cuenta la información recopilada de las Tablas 1 a la 6 la temperatura final depende de la masa del material, a medida que hay mayor masa su temperatura final aumenta.
Teniendo en cuenta el cálculo del promedio de cada material de las Tablas 1 a 6 y consultando el valor teórico del calor específico de cada material se calculó el porcentaje de error mediante la Ecuación 5.
Material Promedio c(J/kg°C) Valor teórico c(J/kg°C) %Error
Hierro 457,02 450 1,56
Cobre 382,03 390 2,04 Grafito 711,14 710 0,16
Oro 130,99 130 0,76
Berilio 1818,24 1825 0,37 Aluminio 900,57 900 0,06 Tabla 7. %Error.




