




Cuidado Integral do Recém-nascido: Prevenção e Condutas Terapêuticas, 2a Ed.
Leandro Meirelles Nunes
Silvana Salgado Nader
Paulo de Jesus Hartmann Nader
Doenças Exantemáticas em Pediatria, 2a Ed.
Carlos Eduardo Schettino
Manual de Terapêutica em Gastrenterologia e Hepatologia
Pediátrica
Ana Daniela Izoton de Sadovsky
Vera Lúcia Ângelo Andrade
Neuropediatria no Dia a Dia
Flávia Nardes dos Santos
Giuseppe Pastura
Neuropsiquiatria Infantil
Giuseppe Pastura
Flávia Nardes dos Santos
Pediatria no Dia a Dia, 2a Ed.
Giuseppe Pastura
Flávia Nardes dos Santos
Puericultura no Dia a Dia
Giuseppe Pastura
Flávia Nardes dos Santos
Semiologia Pediátrica, 3a Ed.
Adauto Dutra
Urgências e Emergências Pediátricas no Dia a Dia
Adriana Rodrigues Fonseca
Mariana Tschoepke Aires
Rafaela Baroni Aurilio
Saiba mais sobre estes e outros títulos em nosso site: www.rubio.com.br

A editora e os autores deste livro não mediram esforços para assegurar dados corretos e informações precisas. Entretanto, por ser a medicina uma ciência em permanente evolução, recomendamos aos nossos leitores recorrer à bula dos medicamentos e a outras fontes fidedignas, bem como avaliar, cuidadosamente, as recomendações contidas no livro em relação às condições clínicas de cada paciente.

Mestre em Medicina – Pediatria pela Universidade Federal do Rio de Janeiro (UFRJ).
Doutor em Medicina – Pediatria pela Escola Paulista de Medicina (EPM) da Universidade Federal de São Paulo (Unifesp).
Pós-doutorado em Neonatologia (Conselho Nacional de Desenvolvimento Científico e Tecnológico [CNPq]) pela University of Miami, EUA.
Professor Titular de Pediatria da Faculdade de Medicina da Universidade Federal Fluminense (UFF).
Mestre e Doutor em Ciências – Saúde da Mulher e da Criança pelo Instituto Fernandes Figueira (IFF) da Fundação Oswaldo Cruz (Fiocruz).
Professor Titular de Pediatria da Faculdade de Medicina da Universidade Federal Fluminense (UFF).
Doutor em Ciências – Saúde da Mulher e da Criança pelo Instituto Fernandes Figueira (IFF) da Fundação Oswaldo Cruz (Fiocruz).
Professor Associado de Pediatria da Faculdade de Medicina da Universidade Federal Fluminense (UFF).
Instrutor do Programa de Reanimação Neonatal da Sociedade Brasileira de Pediatria (SBP).
Consultor Nacional do Método Canguru pelo Ministério da Saúde.
Perinatologia no Dia a Dia
Copyright © 2026 Editora Rubio Ltda.
ISBN 978-85-8411-145-9
Todos os direitos reservados.
É expressamente proibida a reprodução desta obra, no todo ou em parte, sem autorização por escrito da Editora.
Produção
Equipe Rubio
Diagramação
Paulo Teixeira
Imagens de Capa e Capa
Bruno Sales
B195p
Perinatologia no dia a dia/organização Adauto Dutra Moraes Barbosa, Alan Araújo Vieira, Arnaldo Costa Bueno. – 1. ed. – Rio de Janeiro: Rubio, 2025.
288 p. : il.; 23 cm.
Inclui bibliografia
ISBN 978-85-8411-145-9
1. Neonatologia. 2. Perinatologia. I. Barbosa, Adauto Dutra Moraes. II. Vieira, Alan Araújo. III. Bueno, Arnaldo Costa.
25-101289.0
CDD: 618.32
CDU: 618.2
Gabriela Faray Ferreira Lopes – Bibliotecária – CRB-7/6643
Editora Rubio Ltda.
Av. Franklin Roosevelt, 194 s/l. 204 – Castelo
20021-120 – Rio de Janeiro – RJ
Tel: 55(21) 2262-3779
E-mail: rubio@rubio.com.br www.rubio.com.br
Impresso no Brasil
Printed in Brazil
Alexandre Ribeiro Fernandes
Mestre em Ciências – Saúde da Mulher e da Criança pelo Instituto Fernandes Figueira (IFF) da Fundação Oswaldo Cruz (Fiocruz).
Doutor em Neurologia pela Faculdade de Medicina da Universidade Federal Fluminense (UFF).
Professor Associado de Pediatria da Faculdade de Medicina da UFF.
Neurologista Pediátrico pelo IFF/Fiocruz.
Ana Flávia Malheiros Torbey
Mestre em Saúde da Criança e do Adolescente pela Faculdade de Medicina da Universidade Federal Fluminense (UFF).
Doutora em Ciências Cardiovasculares pela UFF.
Professora Adjunta de Pediatria da Faculdade de Medicina da UFF.
Anna Esther Araujo e Silva
Mestre em Saúde da Criança e do Adolescente pela Universidade Federal Fluminense (UFF).
Especialista em Cardiologia Pediátrica e Fetal pelo The Hospital for Sick Children – University of Toronto, ON, Canada.
Especialista em Segurança do Paciente pela Fundação Oswaldo Cruz (Fiocruz).
Médica do Hospital Getúlio Vargas Filho, RJ.
Camila Barros Melgaço da Silva
Mestre em Saúde Materno-Infantil pela Universidade Federal Fluminense (UFF).
Médica Neonatologista do Hospital Universitário Antônio Pedro (Huap) da UFF.
Carlos Alberto Bhering
Doutor em Ciências – Saúde da Mulher e da Criança pelo Instituto Fernandes Figueira (IFF) da Fundação Oswaldo Cruz (Fiocruz).
Professor Titular de Saúde da Criança e do Adolescente da Universidade de Vassouras.
Danielle Rodrigues Lopes
Pós-graduada em Cuidados Paliativos e Terapia da Dor pela Pontifícia Universidade Católica de Minas Gerais (PUC-MG).
Médica Neonatologista da Maternidade Escola da Universidade Federal do Rio de Janeiro (UFRJ).
Fernanda Catta-Preta Pereira Pontes
Especialista em Pediatra pelo Hospital Universitário Antônio Pedro (Huap) da Universidade Federal Fluminense (UFF).
Hematologista Pediátrica pelo Instituto de Puericultura e Pediatria Martagão Gesteira (IPPMG) da Universidade Federal do Rio de Janeiro (UFRJ).
Hematologista Pediátrica do Instituto Estadual de Hematologia Arthur de Siqueira Cavalcanti (Hemorio).
Hematologista Pediátrica do Hospital Municipal Getúlio Vargas Filho, RJ.
Heron Werner Júnior
Mestre em Medicina (Clínica Obstétrica) pela Universidade Federal do Rio de Janeiro (UFRJ).
Doutor em Medicina (Radiologia) pela UFRJ. Médico da Clínica de Diagnóstico por Imagem (CDPI) e da Alta Excelência Diagnóstica.
Professor do Programa de Pós-graduação em Radiologia da UFRJ.
Isabela Vieira de Sousa Residência Médica em Oftalmologia pela Universidade Federal Fluminense (UFF).
Mestre em Saúde Materno-Infantil pela UFF. Médica do Ministério da Defesa – Comando da Marinha.
Oftalmologista pelo Conselho Brasileiro de Oftalmologia (CBO).
Jaqueline Serra Brand
Mestre em Saúde da Criança e Adolescente pela Universidade Federal Fluminense (UFF).
Médica Neonatologista do Hospital Universitário Antônio Pedro (Huap) da UFF.
José Eduardo da Silva
Oftalmologista da Secretaria Municipal de Saúde do Rio de Janeiro.
José Roberto de Moraes Ramos
Doutor em Ciências – Saúde da Mulher e da Criança pelo Instituto Fernandes Figueiras (IFF) da Fundação Oswaldo Cruz (Fiocruz).
Lilian Kuhnert Campos
Mestre em Saúde da Criança e do Adolescente pela Universidade Federal Fluminense (UFF).
Doutora em Ciências – Saúde da Mulher e da Criança pelo Instituto Fernandes Figueira (IFF) da Fundação Oswaldo Cruz (Fiocruz).
Professora Adjunta de Pediatria da Faculdade de Medicina da UFF.
Lisieux Eyer de Jesus
Doutora em Cirurgia pela Universidade Federal do Rio de Janeiro (UFRJ).
Especialista em Urologia Pediátrica e Educação
Médica pelo The Hospital for Sick Children – University of Toronto, ON, Canadá.
Cirurgiã Pediátrica do Hospital Federal dos Servidores do Estado do Rio de Janeiro.
Lucia De La Candelaria Arenas Viera
Mestre em Medicina pela Universidade do Estado do Rio de Janeiro (Uerj).
Doutoranda em Ciências Médicas pela Uerj.
Neonatologista pela Uerj, com título de Neonatologista pela Associação Médica Brasileira (AMB) e pela Sociedade Brasileira de Pediatria (SBP).
Pediatra pela Pontifícia Universidade Católica do Rio de Janeiro (PUC-Rio), com título de Pediatra pela AMB e pela SBP.
Márcia Gonçalves Ribeiro
Professora Titular de Genética Clínica do Departamento de Pediatria da Faculdade de Medicina da Universidade Federal do Rio de Janeiro (UFRJ).
Marcio Moacyr Vasconcelos
Fellowship em Neurologia Pediátrica pela George Washington University, Washington DC, EUA.
Doutor em Neurologia pela Universidade Federal Fluminense (UFF).
Professor Associado de Pediatria da UFF.
Maria Dolores Salgado Quintans
Mestre em Saúde da Criança e do Adolescente pela Universidade Federal Fluminense (UFF).
Doutora em Ciências Médicas pela UFF.
Professora Adjunta de Pediatria da UFF.
Maria Elisabeth Lopes Moreira
Doutora em Saúde da Criança e do Adolescente pela Universidade de São Paulo (USP-RP).
Professora da Pós-graduação em Saúde da Mulher e da Criança da Fiocruz.
Maura Calixto Cecherelli de Rodrigues
Médica Pediatra e Neonatologista.
Doutora em Ciências – Saúde da Mulher e da Criança pelo Instituto Fernandes Figueira (IFF) da Fundação Oswaldo Cruz (Fiocruz).
Professora Associada da Faculdade de Ciências Médicas do Departamento de Pediatria da Universidade do Estado do Rio de Janeiro (Uerj).
Pedro Teixeira Castro
Mestre e Doutor em Medicina pela Universidade Federal do Rio de Janeiro (UFRJ).
Raphael de Faria Schumann
Mestre em Saúde da Criança e do Adolescente pela Universidade Federal Fluminense (UFF).
Doutorando de Oftalmologia da Universidade Federal de São Paulo (Unifesp).
Master of Business Administration (MBA) Executivo em Saúde pela Fundação Getúlio Vargas (FGV-Rio).
Especialista em Oftalmologia pela UFF.
Título de Especialista em Oftalmologia pelo Conselho Brasileiro de Oftalmologia (CBO).
Raquel Germer Toja Couto
Pós-graduação em Aconselhamento Genético em Predisposição Hereditária ao Câncer pelo Hospital Israelita Albert Einstein.
Título de Especialista em Genética Médica pela Sociedade Brasileira de Genética Médica (SBGM). Médica Geneticista do Hospital Universitário Antônio Pedro (Huap) da Universidade Federal Fluminense (UFF).
Raquel Monteiro Nobre Machado
Mestre em Saúde Materno-Infantil pela Universidade Federal Fluminense (UFF).
Professora Assistente de Otorrinolaringologia da Faculdade de Medicina da UFF.
Rinaldo Fábio Souza Tavares
Mestre em Pediatria pela Universidade Federal do Rio de Janeiro (UFRJ).
Médico Pediatra/Neonatologista do Hospital
Universitário Antônio Pedro (Huap) da Universidade Federal Fluminense (UFF).
Professor Adjunto de Toxicologia Clínica da Faculdade de Medicina da UFF.
Roberta Furtado Stivanin Rachid Novais
Mestre em Saúde Materno-infantil pela Universidade Federal Fluminense (UFF).
Professora Assistente de Obstetrícia da UFF.
Sandra Trindade de Almeida Leal
Pós-graduada em Qualidade e Segurança no Cuidado ao Paciente pela Sociedade Beneficente de Senhoras Hospital Sírio-Libanês, SP.
Pós-graduada em Cuidados Paliativos pela Faculdade Israelita de Ciências da Saúde Albert Einstein, SP.
Médica Neonatologista e Gestão da Qualidade da Maternidade Escola pela Universidade Federal do Rio de Janeiro (UFRJ).
Sully Diderot Melo Turon
Pós-graduada em Gestão da Qualidade em Saúde da Faculdade Israelita de Ciências da Saúde Alber Einstein, SP.
Mestre em Saúde Perinatal pela Maternidade Escola pela Universidade Federal do Rio de Janeiro (UFRJ).
Título de Especialista em Anestesiologia pela Sociedade Brasileira de Anestesiologia (SBA)/ Associação Médica Brasileira (AMB).
Médico Anestesiologista e da Gestão da Qualidade da Maternidade Escola pela UFRJ.
Tatiana Mendonça Fazecas e Costa
Mestre em Saúde Materno-Infantil pela Universidade Federal Fluminense (UFF).
Especialista em Radiologia pelo Hospital da Lagoa, RJ.
Especialista em Radiologia pelo Colégio Brasileiro de Radiologia.
Radiologista do Hospital Municipal Jesus – Secretaria Municipal de Saúde Rio de Janeiro.
Radiologista Pediátrica da Clínica de Diagnóstico por Imagem (CDPI) e do Alta Excelência Diagnóstica, RJ.
Thaís Bomfim Teixeira
Residência de Genética Médica pela Universidade Federal de Minas Gerais (UFMG).
Pós-graduação em Oncogenética pela Faculdade de Ciências da Saúde de Barretos Dr. Paulo Prata (Facisb).
Médica Responsável do Serviço de Referência em Doenças Raras da Associação de Pais e Amigos dos Excepcionais (Apae), Anápolis – GO.
Viviane Lanzelotte
Residência em Pediatria no Hospital dos Servidores do Estado do Rio de Janeiro.
Mestre em Saúde Materno-Infantil pela Universidade Federal Fluminense (UFF).
Especialista em Oftalmologia pela Pontifícia Universidade Católica do Rio de Janeiro (PUC-Rio).
Médica da Secretaria Municipal de Saúde do Rio de Janeiro.
Agradecemos a Deus pela oportunidade de termos um grupo de médicos e professores tão coesos, dedicados a transmitir seus conhecimentos aos estudantes e aos profissionais que desejam informações rápidas e precisas em Perinatologia e que se dispuseram a participar da elaboração deste pequeno manual.
Nominalmente, agradecemos aos ilustres professores Alexandre Ribeiro Fernandes, Ana Flavia Malheiros Torbey, Anna Esther Araujo e Silva, Camila Barros Melgaço da Silva, Carlos Alberto Bhering, Danielle Rodrigues Lopes, Fernanda Catta-Preta Pereira Pontes, Heron Werner Júnior, Isabela Vieira de Sousa, Jaqueline Serra Brand, José Eduardo da Silva, José Roberto de Moraes Ramos, Lilian Kuhnert Campos, Lisieux Eyer de Jesus, Lucia De La Candelaria Arenas Viera, Márcia Gonçalves Ribeiro, Marcio Moacyr Vasconcelos, Maria Dolores Salgado Quintans, Maria Elisabeth Lopes Moreira, Maura Calixto Cecherelli de Rodrigues, Pedro Teixeira Castro, Raphael de Faria Schumann, Raquel Germer Toja Couto, Raquel Monteiro Nobre Machado, Rinaldo Fábio Souza Tavares, Roberta Furtado Stivanin Rachid Novais, Sandra Trindade de Almeida Leal, Sully Diderot Melo Turon, Tatiana Mendonça Fazecas e Costa, Thaís Bomfim Teixeira, Viviane Lanzelotte.
Finalmente, agradecemos à Editora Rubio e à sua equipe pela aquiescência a esta publicação.
Nosso muito obrigado!
Dedicamos a todos os colegas pediatras, obstetras e interessados no estudo da Perinatologia.
Os Organizadores
Perinatologia é a área conjunta da Medicina na qual se encontram, sobretudo, duas grandes especialidades: a Neonatologia e a Obstetrícia. Envolve também um expressivo número de outras áreas do conhecimento, tais como a Pneumologia, a Cardiologia, a Radiologia, a Hematologia, a Otorrinolaringologia, a Gastrenterologia, a Cirurgia Pediátrica e a Patologia. Além disso, recebe o apoio de áreas muito importantes, como Enfermagem, Psicologia, Assistência Social, Nutrição e Fonoaudiologia, entre outras. Em trabalho conjunto, com ações concatenadas e atitudes homogêneas, a Perinatologia tem se destacado como área de atuação, sendo capaz de conduzir satisfatoriamente a saúde da gestante e do seu feto, minimizando ao máximo, particularmente no recém-nascido pré-termo, suas comorbidades, a fim de se obter uma gravidez saudável e um recém-nascido com pleno crescimento e desenvolvimento.
Os Organizadores
A Perinatologia é uma das áreas mais dinâmicas da Medicina e demanda a necessidade de atualização constante. Contudo, em meio a correria e às múltiplas responsabilidades da rotina assistencial, nem sempre é fácil dedicar tempo às longas e densas leituras.
Foi com essa realidade em mente que os organizadores Adauto Dutra Moraes Barbosa, Alan Araújo Vieira e Arnaldo Costa Bueno, doutores e professores da Universidade Federal Fluminense (UFF), idealizaram esta obra.
Longe de pretender ser mais um livro exaustivo, seu propósito é distinto: ser uma fonte de consulta rápida e confiável que condense informações essenciais, objetivas e embasadas nas melhores evidências científicas, apresentadas de maneira prática e acessível.
Os colaboradores, reconhecidos especialistas em suas áreas, compartilham seus conhecimentos com rigor científico e clareza didática, enfatizando condutas diagnósticas e terapêuticas atualizadas.
Composta por 42 capítulos, a obra percorre, de forma estruturada, os principais eixos da atenção perinatal. Inicia-se com assistência pré-natal e aborda temas relevantes, como os cuidados ao recém-nascido na sala de parto, asfixia perinatal, protocolos diferenciados de reanimação para recém-nascido pré-termo, uso de hipotermia terapêutica na síndrome hipóxico-isquêmica e infecções neonatais, entre outros. Assim, Perinatologia no Dia a Dia se consolida como contribuição valiosa para obstetras, neonatologistas, pediatras e residentes, oferecendo um conteúdo sustentado por conhecimento atualizado e compromisso com a qualidade do cuidado perinatal.
Manoel de Carvalho Doutor em Saúde da Mulher e da Criança pelo Instituto Fernandes Figueira (IFF) da Fundação Oswaldo Cruz (Fiocruz).
1 Assistência Pré-natal e Vias de Parto Baseadas em Evidências, 3
2 Rotina do Recém-nascido no Alojamento Conjunto, 9
3 Atenção Humanizada ao Recém-nascido de Baixo Peso –Método Canguru, 13
4 Triagem Neonatal Biológica, 16
5 Imunização no Recém-nascido Pré-termo, 18
6 Seguimento do Prematuro: uma Abordagem Sumarizada, 23
Maura Calixto Cecherelli de Rodrigues Lucia De La Candelaria Arenas Viera
Introdução
A prematuridade é um relevante problema de saúde pública e figura entre as principais causas de mortalidade neonatal no mundo. No Brasil, a prevalência de nascimentos prematuros atingiu 11,9% em 2023, semelhante à prevalência observada no estado do Rio de Janeiro.1
Segundo a Organização Mundial da Saúde (OMS), definem-se como recém-nascidos prétermo (RNPT) os nascidos antes de 37 semanas de gestação, que são classificados como:
Prematuros extremos : menos de 28 semanas.
Muito prematuros: 28 a 32 semanas.
Moderadamente prematuros: 32 a 34 semanas.
Prematuros tardios: 35 a 36 semanas.
Os recém-nascidos (RN) são também categorizados pelo peso para a idade gestacional (IG):2,3
Pequenos para a idade gestacional (PIG): percentil inferior ao 10.
Adequados para a IG: percentil entre 10 e 90.
Grandes para a idade gestacional (GIG): percentil superior ao 90.
Os RNPT com peso inferior a 1.500g têm risco aumentado para alterações no neurodesenvolvimento e doenças crônicas, tais como:
Broncodisplasia pulmonar (BDP) ou doença pulmonar crônica da prematuridade (DPCP).
Retinopatia da prematuridade (ROP; do inglês, retinopathy of prematurity).
Doença metabólica óssea (DMO).
Anemia.
Falha de crescimento.
O seguimento pós-alta é essencial para vigilância clínica, promoção do desenvolvimento e redução de reinternações, especialmente no primeiro ano de vida. A abordagem deve ser multiprofissional, centrada na família, com intervenções oportunas e individualizadas, promovendo impactos positivos na saúde da criança e dos cuidadores, e na geração de evidências para a prática neonatal.4
Ambulatório de Seguimento de Recém-nascidos Prematuros de Alto Risco
Importância da Interprofissionalidade e da Inter(Trans)Disciplinaridade
O seguimento ambulatorial do RN de alto risco deve ser interprofissional e transdisciplinar, com diálogo contínuo entre profissionais de saúde e de educação e os cuidadores. Esse modelo permite cuidado integral, centrado na família, e favorece inclusão social e suporte à saúde mental. A equipe pode incluir:
Pediatra neonatologista.
Enfermeira(o).
Nutricionista.
Fonoaudióloga(o).
Fisioterapeuta.
Terapeuta ocupacional.
Psicóloga(o).
Assistente social.
Odontólogo(a).
Pareceres especializados (de profissionais de neurologia, oftalmologia, psiquiatria, otorrinolaringologia e cirurgia) e articulação com a educação são frequentemente necessários. O objetivo consiste em monitorar o crescimento e o neurodesenvolvimento, identificar precocemente alterações e intervir oportunamente, valorizando o contexto psicossocial da família.5
Em termos de logística, há que se ter um recorte da heterogênea população de prematuros, e um recorte mais adequado seria o da gravidade, e de maior comprometimento na morbidade e na mortalidade. A Figura 6.1 apresenta critérios, sugeridos a partir da literatura e também da observação do contexto nacional e da experiência das autoras, do que é praticado em termos de acompanhamento ambulatorial desses RN de alto risco no mundo.4
Critérios para inclusão no seguimento ambulatorial de RN de alto risco
Peso ao nascer <1.500g e/ou idade gestacional 32 semanas ≤
PIG <2 desvios-padrão ou abaixo do10 p
Encefalopatia hipóxico-isquêmica
RN (35 semanas) submetidos à hipotermia ≥ terapêutica
Hemorragia intracraniana ou leucomalacia
Hiperbilirrubinemia e/ou com teste de Coombs direto positivo
Sepse neonatal e enterocolite
Figura 6.1 Critérios para inclusão de recém-nascidos (RN) no ambulatório de seguimento
PIG: pequenos para a idade gestacional.
Fonte: elaborada pelas autoras.
Sugestão de Periodicidade dos Atendimentos
A primeira consulta deve ocorrer 7 a 10 dias após o RN ter alta da unidade neonatal (UNN). Nessa ocasião, deve-se revisar e registrar o resumo de alta (prontuário e cópia para os responsáveis), incluindo:
Diagnósticos.
Condutas.
Exames relevantes (ultrassonografia transfontanelar [UST], fundoscopia óptica, ecocardiograma [ECO], hemograma, cálcio, fósforo, fosfatase alcalina, triagens neonatais).
Dados antropométricos da alta e imunização.
Com base na avaliação multiprofissional, define-se um plano individualizado de seguimento. A periodicidade das consultas está descrita na Tabela 6.1, e pode ser ajustada conforme as necessidades integrais do paciente.
A avaliação do crescimento e do neurodesenvolvimento e as orientações nutricionais para o RNPT devem ser baseadas na idade gestacional corrigida (IGC), até pelo menos os 2 anos de idade, e permite que se estabeleçam expectativas adequadas
e intervenções oportunas. A Tabela 6.2 apresenta orientações práticas para o cálculo da IGC.
Tabela 6.1 Sugestão de periodicidade dos atendimentos ambulatoriais por faixa etária para seguimento de crianças de alto risco
Periodicidade dos atendimentos ambulatoriais para crianças de alto risco
Primeira consulta: 7 a 14 dias
Mensais: até 6 meses de idade corrigida
Bimestrais: 6 a 12 meses de idade corrigida
Trimestrais: 13 a 24 meses
Semestrais: 2 a 4 amos de idade cronológica
Anuais: de 4 a 12 anos incompletos
Fonte: adaptada de SBP, 2024.6
Tabela 6.2 Cálculo da idade gestacional corrigida (IGC) com base na idade cronológica e na idade gestacional ao nascimento
Cálculo da IGC para crianças nascidas prematuras: IGC = idade cronológica – (40 semanas – idade gestacional em semanas)
Exemplo: lactente de 6 meses de vida nascido com 32 semanas de IG
Cálculo:
40 semanas – 32 semanas = 8 semanas
IGC = 6 meses – 8 semanas (2 meses) = 4 meses de IGC
IG: idade gestacional.
Fonte: elaborada pelas autoras.
7 Aleitamento Materno, 37
8 Nutrição Enteral em Recém-nascidos Pré-termo, 45
9 Nutrição Parenteral Total, 52
10 Enterocolite Necrosante Neonatal, 56
Introdução
Maria Elisabeth Lopes Moreira
Nutrir adequadamente, com o objetivo de proporcionar ao prematuro um crescimento semelhante ao crescimento intrauterino, é um dos grandes desafios no campo da neonatologia. A importância de uma nutrição adequada, para assegurar sobrevida, crescimento e desenvolvimento dos recém-nascidos (RN), tem sido reconhecida como uma emergência neonatal. O objetivo da nutrição do RN prematuro consiste em fornecer nutrientes para atender à taxa de crescimento e à composição corporal do feto saudável normal da mesma idade gestacional (IG) em termos de peso, comprimento e perímetro cefálico, tamanho dos órgãos, componentes dos tecidos, incluindo número e estrutura das células, concentrações de nutrientes no sangue e nos tecidos e resultados do desenvolvimento.1,2
Diminuir a perda de proteína endógena nos primeiros dias de vida.
Proporcionar uma perda de peso mínima nos primeiros dias de vida.
Proporcionar um ganho de peso de 14 a 16g/kg/dia após a recuperação do peso de nascimento.
Evitar que o RN atinja o termo com peso abaixo do percentil 5.
Proporcionar um crescimento em peso, comprimento e perímetro cefálico o mais aproximado possível do crescimento intrauterino.
Desafios para a Nutrição Enteral no Recém-nascido Pré-termo
As necessidades nutricionais não estão bem estabelecidas e se modificam de acordo com a IG e o quadro clínico do RN.
Tem sido recomendado que se forneçam nutrientes suficientes aos recém-nascido pré-termo (RNPT), para que alcancem fora do útero a velocidade de crescimento fetal.1 O problema é que,
ainda nos dias de hoje, existe pouco conhecimento sobre a qualidade e a quantidade de nutrientes que os fetos humanos recebem em cada IG. Várias estratégias já foram adotadas para determinação das necessidades nutricionais dos RNPT, incluindo balanços nutricionais, dosagem de nutrientes no sangue do cordão, infusão de isótopos estáveis, entre outras. Além disso, as necessidades nutricionais também irão variar com o tipo de doença e estresse metabólico apresentados pelo bebê.2
Atenção
O recomendado é acompanhamento da evolução do peso do RNPT, objetivando um ganho de 14 a 16g/kg/dia após a recuperação do peso de nascimento.3
Ajustes na qualidade e na quantidade de leite oferecido devem levar em conta essa variável.
O Objetivo de Atingir uma Velocidade de Crescimento Semelhante ao Intrauterino é Difícil de ser Alcançado
A meta de atingir o ganho de peso fetal não decorre do simples ganho de peso, mas principalmente do fato de que um ganho de peso insuficiente é um bom marcador de nutrição inadequada, o que, por sua vez, tem grande impacto no desenvolvimento cognitivo.2-5
Existem evidências suficientes para demonstrar que uma nutrição inadequada em períodos precoces da vida tem forte impacto no desenvolvimento a longo prazo.2,4,6
Má nutrição em um período vulnerável do desenvolvimento do cérebro resulta em diminuição do número de células cerebrais, com prejuízos importantes no comportamento, na capacidade de aprendizagem e na memória. Entretanto, o oposto
não está tão claro. Existem dúvidas sobre se o aumento ou a melhora da oferta de nutrição precocemente teriam impacto positivo no desempenho a longo prazo.2
Clínicas e Peculiaridades dos Prematuros que Contribuem para uma Nutrição
A restrição de volume que às vezes é necessária para os prematuros pode limitar a oferta de nutrição. A intolerância à glicose que os bebês de peso extremamente baixo podem apresentar nas primeiras semanas de vida também contribui para redução da ingestão de caloria. Eventos patológicos diminuem as possibilidades de oferta, além de aumentarem a demanda, e a preocupação com a enterocolite necrosante (ECN) impede manuseios nutricionais agressivos por via enteral.2 O trato gastrintestinal (TGI) apresenta funções digestiva e motora imaturas, e a tolerância à alimentação por via enteral está frequentemente alterada.
Atenção
A alimentação do bebê pré-termo deve ser adequada à sua situação clínica e às limitações relacionadas ao desenvolvimento de cada IG.5
O intestino é a interface entre a dieta e o metabolismo, por meio do qual todos os nutrientes devem passar. A eficiência da nutrição enteral está relacionada à competência do TGI em coordenar sucção e deglutição, propiciar um esvaziamento gástrico completo e motilidade intestinal adequada (Tabela 8.1). Além disso, é também regulada pela secreção salivar, gástrica, pancreática e hepatobiliar, e pela capacidade do enterócito de sintetizar e secretar enzimas apropriadas, promovendo uma absorção efetiva, proteção da mucosa e eliminação de produtos não digeridos ou produtos de degradação.7
Dois fatores são importantes no processo de adaptação à nutrição enteral:
1. Maturação do TGI.
2. Composição do alimento oferecido.
A competência do esfíncter esofagiano é relacionada à IG, e RN prematuros estão sob maior risco de refluxo gastresofágico. O estômago é anatomicamente maduro por volta da 7a semana de gestação. Contudo, as contrações rítmicas não ocorrem até cerca de 4 dias de vida do RN a termo.
Tabela 8.1 Estágios de desenvolvimento do trato gastrintestinal
Função
IG (semanas) Deglutição de líquido amniótico18
Sucção não nutritiva 18 a 24
Coordenação de sucção, deglutição e respiração
Motilidade intestinal:
Ondas peristálticas desorganizadas
34 a 36
Peristalse organizada <31
Enzimas detectáveis:
Lactase
Glicoamilase
Tempo de trânsito intestinal até o ceco:
9h
4h
IG: idade gestacional.
Fonte: adaptada de Romero, 1993.7
31 a 34
35 a 40 <20
32 >37
O esvaziamento do estômago nos prematuros é lento, provavelmente refletindo a imaturidade da função motora do duodeno e a ausência de uma atividade coordenada entre o antro e o duodeno.8,9 O esvaziamento gástrico pode ser influenciado pelo conteúdo da dieta. Assim, um aumento da densidade calórica do alimento oferecido pode retardar o esvaziamento. Polímeros de glicose propiciam um esvaziamento mais rápido que as soluções que contenham lactose ou glicose; o mesmo ocorre com os triglicerídios de cadeia média (TCM) em relação aos de cadeia longa.
Vários aspectos da digestão e da absorção no RN têm sido estudados há longo tempo, mas ainda faltam informações, sobretudo no que se relaciona ao papel das enzimas no processo de digestão. Os estudos indicam que, apesar da imaturidade de muitos mecanismos da digestão utilizados por adultos, o RN dispõe de uma série de mecanismos compensatórios para uma adequada digestão. Por exemplo, apesar de a proteólise gástrica ser muito limitada no bebê, a digestão da proteína intestinal é adequada.
Os eletrólitos e a água são absorvidos no prematuro a partir do intestino delgado. O sódio é transportado por gradiente de concentração até o enterócito e pela bomba de sódio-potássio até o espaço interepitelial basolateral. Glicose e sódio são cotransportados por difusão facilitada, e a água segue um gradiente osmótico.
11 Abordagem Diferenciada para Recém-nascidos com 34 Semanas ou Mais e com Menos de 34 Semanas, 67
Arnaldo Costa Bueno
Introdução
A transição da vida intrauterina para a extrauterina requer atenção especial e é um dos eventos fisiológicos mais complexos e dramáticos do ciclo da vida. A maioria dos recém-nascidos (RN) realiza essa transição sem dificuldades e sem necessidade de intervenções, mas uma pequena parcela necessita de algum tipo de manobra para iniciar e manter a respiração. A reanimação neonatal consiste em uma série de procedimentos padronizados e sequenciais que visam garantir uma ventilação pulmonar eficaz e, em consequência, circulação e perfusão tecidual adequadas. Todos estes procedimentos têm por objetivo reduzir a morbidade e a mortalidade neonatal associadas à asfixia perinatal.
É importante mencionar que, no Brasil, asfixia perinatal é a terceira causa básica de óbito de crianças abaixo de 5 anos de idade, atrás apenas de prematuridade e anomalias congênitas.
A necessidade de reanimação é inversamente proporcional à idade gestacional (IG) e ao peso ao nascimento.
Ao nascimento, somente cerca de 2 recémnascidos a termo (RNT) – considerados, neste texto, aqueles com 34 semanas ou mais de gestação –, em cada 10, não choram ou não respiram; 1 RNT em cada 10 precisará de ventilação com pressão positiva (VPP); 1 a 2 em cada 100 requerem intubação traqueal; e 1 a 3 RNT em cada 1.000 necessitam de reanimação avançada. Entende-se por reanimação avançada a necessidade de ventilação acompanhada de massagem cardíaca e/ou medicações, desde que a ventilação seja aplicada adequadamente. Enquanto cerca de 10% dos RNT a termo necessitam de alguma ajuda para iniciar a respiração, esse número aumenta drasticamente entre os recém-nascidos pré-termo (RNPT) – considerados, neste texto, aqueles com
menos de 34 semanas. A imaturidade de vários sistemas, especialmente o pulmonar, o cardiovascular e o neurológico, torna os RNPT mais vulneráveis à asfixia perinatal e às lesões decorrentes dos próprios procedimentos de reanimação.
As diretrizes de 2022 da Sociedade Brasileira de Pediatria (SBP), alinhadas com as recomendações do International Liaison Committee on Resuscitation (ILCOR), estabelecem protocolos distintos para RN com IG ≥34 semanas e para aqueles com <34 semanas, reconhecendo as particularidades anatômicas e fisiológicas de cada grupo.
O sucesso da reanimação neonatal deve, obrigatoriamente, começar antes do nascimento. Uma preparação adequada, que compreende a previsão de fatores de risco, montagem do material e um briefing da equipe, que inclui anamnese materna, preparo do ambiente e do material para uso imediato na sala de parto e divisão das funções de cada membro da equipe, deixando claro a quem caberá o papel de liderança nos procedimentos de reanimação. O briefing pode ser entendido como uma rápida reunião entre os membros da equipe para planejar, antes do nascimento, o atendimento ao neonato, tornando-se fator importante para um atendimento de qualidade.
A identificação de fatores de risco antenatais e intraparto é essencial para se prever a necessidade de reanimação. Condições como prematuridade, gestação múltipla, pré-eclâmpsia, diabetes materno, líquido amniótico meconial e padrões anormais de frequência cardíaca fetal são sinais de alerta para uma possível necessidade de procedimentos de reanimação (Tabela 11.1). Entretanto, a ausência destes fatores de risco não torna desnecessário o preparo já citado.
Tabela 11.1 Fatores de risco para necessidade de reanimação neonatal
Fatores antenataisFatores relacionados ao parto
Idade materna <16 ou >35 anos
Diabetes ou hipertensão materna
Gestação múltipla
Ausência de acompanhamento pré-natal
Infecção ou sangramento materno
Malformação fetal
Trabalho de parto prematuro
Parto cesáreo
Líquido amniótico meconial
Padrão anormal de frequência cardíaca fetal
Uso de opioides 4h antes do parto
Descolamento prematuro de placenta
Fonte: adaptada de Almeida & Guinsburg, 2022.1
Mínima para um parto de risco habitual e gestação ≥34 semanas. Considerando-se a frequência de RNT que precisam de algum procedimento de reanimação e a rapidez com que tais manobras devem ser iniciadas, é fundamental que pelo menos um profissional de saúde, capaz de realizar os passos iniciais e a VPP por meio de máscara facial, esteja presente em todos os partos.
Para um parto que apresente fatores de risco ou de feto com IG <34 semanas, é fundamental a presença de pelo menos dois profissionais de saúde, de preferência pediatras, treinados em reanimação neonatal, aptos a realizar todos os procedimentos, inclusive a intubação traqueal.
Todo o material necessário para a reanimação deve ser preparado, testado e estar disponível em local de fácil acesso antes do nascimento. Isso inclui fontes de calor, material para aspiração, ventilação, intubação e medicações, entre outros itens.
A avaliação da vitalidade ao nascimento é a base para todas as decisões subsequentes. Imediatamente após o nascimento, três perguntas devem ser respondidas:
1. É uma gestação a termo?
2. O RN está respirando ou chorando?
3. O RN tem bom tônus muscular?
Se todas as respostas forem “sim”, o RN é considerado vigoroso, e na sala de parto deve ser colocado em contato pele a pele com a mãe para os cuidados de rotina. Se qualquer resposta for “não”,
o RN deve ser levado à mesa de reanimação para realização dos passos iniciais.
Prover calor: manter a normotermia (36,5ºC a 37,5ºC); recomenda-se que a temperatura da sala esteja em torno de 23ºC a 25ºC, e recepcionar os RN em campos previamente aquecidos ou em saco plástico e touca dupla, em caso de RNPT. Os RN devem ser recebidos sob uma fonte de calor radiante e com compressas aquecidas.
Posicionar : leve extensão do pescoço para abrir as vias aéreas.
Aspirar (somente se necessário): aspirar na boca e depois narinas apenas se houver obstrução por secreções.
Secar: secar o corpo e a cabeça para evitar perda de calor e estimular a respiração.
Avaliação: as decisões quanto à estabilização ou reanimação e necessidade de outras modalidades de reanimação dependem da avaliação simultânea da frequência cardíaca (FC) e da respiração. É necessário monitorar a saturação de oxigênio (SatO2) no RN >34 semanas que necessita de VPP.
≥34 semanas
Particularidades
Clampeamento do cordão umbilical: para RNT vigorosos, recomenda-se o clampeamento tardio ou oportuno do cordão, aguardando-se, no mínimo, 60s após o nascimento. Este procedimento está associado aos níveis mais altos de hemoglobina e de reservas de ferro. Se o RNT não for vigoroso, o clampeamento deve ser imediato, para que sejam iniciados a reanimação e os passos iniciais.
Líquido amniótico meconial: na presença de líquido amniótico meconial, independentemente de sua viscosidade, se o RNT, logo após o nascimento, estiver respirando ou chorando e apresentar tônus muscular em flexão, entendese que ele apresenta boa vitalidade e deve continuar junto da parturiente.
Se houver líquido meconial e o RN não estiver vigoroso, não é mais recomendada a aspiração de rotina na traqueia antes de se iniciar a ventilação. Em RNT com líquido amniótico meconial de qualquer viscosidade que, após os passos ini-
12 Cardiopatias Congênitas com Repercussão no Período Neonatal, 75
13 Apneia da Prematuridade: Fisiopatologia, Diagnóstico e Manejo Clínico, 87
14 Hipotensão e Choque no Recém-nascido, 93
15 Distúrbios Respiratórios, 100
16 Modalidades Ventilatórias, 104
Introdução
Anna Esther Araujo e Silva Ana Flávia Malheiros Torbey
As cardiopatias congênitas consistem em defeitos na formação do coração presentes desde a vida intrauterina. Sua etiologia multifatorial pode estar relacionada a infecções congênitas, exposição às substâncias teratogênicas e condições maternas, tais como diabetes e algumas colagenoses.
Muitas cardiopatias congênitas também ocorrem na presença de síndromes genéticas. A síndrome de Down é a mais frequente, além de outras cromossomopatias, como as trissomias do 15 e do 18 e a síndrome de Turner. Outras condições genéticas, como as síndromes de Noonan e de Williams, também podem ser citadas.
As cardiopatias congênitas podem ter apresentações clínicas variadas no período neonatal, desde quadros sem repercussão clínica e pacientes assintomáticos até situações em que a cardiopatia pode evoluir para choque cardiogênico ou hipoxemia grave nos primeiros dias de vida.
É fundamental que o pediatra e o neonatologista estejam aptos para identificar e realizar a abordagem adequada das cardiopatias consideradas críticas no período neonatal.
Neste capítulo serão abordadas as principais cardiopatias críticas dependentes de canal e as cardiopatias de hiperfluxo que se apresentam mais tardiamente no período neonatal. Para fins didáticos, as cardiopatias serão divididas de acordo com a fisiopatologia subjacente.
Epidemiologia
As cardiopatias congênitas são as malformações congênitas mais frequentes, e representam cerca de um terço de todas as anomalias congênitas de maior vulto.
Ao longo do último século, há relatos de aumento na prevalência de cardiopatias congênitas. Esse aumento ao longo do tempo pode ter sido secundário à melhor acurácia dos métodos diagnósticos e de rastreio, com mais facilidade na de
tecção de defeitos simples (p. ex., comunicações interventriculares [CIV] pequenas), e também pode representar um aumento real em consequência da sobrevivência de neonatos prematuros e mudanças na exposição aos fatores ambientais, entre outros fatores.
Nos dias atuais, considerase uma prevalência global de cardiopatias congênitas de 8 a 12 por 1.000 nascidos vivos (0,8% a 1,2%), com alguma variação regional (China e Europa apresentam taxas de prevalência mais altas).1
Entre as cardiopatias congênitas, 25% são consideradas cardiopatias congênitas críticas (CCC). As CCC são aquelas que se manifestam no período neonatal com hipoxemia ou baixo débito sistêmico e requerem intervenção cirúrgica ou outros procedimentos ainda no primeiro ano de vida, sendo responsáveis por significativas mortalidade e morbidade.2,3 A Tabela 12.1 descreve as principais CCC.
Com a realização de diagnóstico prénatal e avanços no tratamento, tais como o avanço das técnicas cirúrgicas e o desenvolvimento de técnicas percutâneas terapêuticas no período neonatal, a história natural das CCC se modificou. Assim, atualmente muitos indivíduos com cardiopatia congênita, inclusive aqueles com CCC, alcançam a idade adulta com adequada qualidade de vida. Este aspecto contribui para aumento da prevalência de cardiopatia congênita entre crianças de mais idade e adultos.
É necessário que o sistema de saúde, tanto público quanto privado, esteja atento a essa crescente população, para que a prestação de serviços de saúde adequados seja direcionada para esses indivíduos.4
A apresentação clínica de algumas CCC depende diretamente das modificações que ocorrem na transição da circulação fetal para a neonatal. Devido
Artéria pulmonar
Aorta
Canal arterial
Figura 12.3 Desenho esquemático de cardiopatia com fluxo pulmonar dependente do canal arterial AD: átrio direito, AE: átrio esquerdo, VD: ventrículo direito, VE: ventrículo esquerdo.
as mamadas, evoluindo para cianose em repouso; pode haver taquipneia, porém na maioria dos casos não há sinais de esforço respiratório ou de baixo débito sistêmico associados.
Além do fluxo pulmonar comprometido, a presença de shunt direitaesquerda no nível do forame oval patente ou, se houver, presença de CIV contribui para queda da saturação da circulação sistêmica.
O exame cardiovascular pode não evidenciar sopro, como se observa em caso de atresia pulmonar com septo íntegro, mas na estenose pulmonar crítica e na tetralogia de Fallot há sopro sistólico ejetivo.
O teste de hiperoxia, que consiste em ofertar ao RN O2 a 100% sob máscara ou capuz (HOOD) por um período de 10min, é muito útil no diagnóstico diferencial com doenças pulmonares. O objetivo do teste é observar se há melhora da saturação com a utilização de oxigênio suplementar. Este é um teste de fácil realização.2,5
Para a realização do teste, devese coletar gasometria arterial em ar ambiente e, após, ao final da oxigenoterapia. A ocorrência de elevação da pressão parcial de oxigênio (PaO2) a valores superiores a 100mmHg é sugestiva de doença de origem pulmonar. Por outro lado, se a causa for uma cardiopatia cianótica, a PaO2 não irá se elevar em mais de 30mmHg.
A radiografia de tórax irá mostrar uma pobreza de vasos pulmonares, e a área cardíaca pode apresentar silhueta característica, como o aspecto de “tamanco holandês”, que ocorre na tetralogia de Fallot e na atresia pulmonar com CIV.
Cardiopatias com Obstrução ao Fluxo Sistêmico
Nessas cardiopatias há uma alteração anatômica que acarreta diminuição importante ou mesmo interrupção do fluxo sanguíneo anterógrado do VE para a AO, tornando o canal arterial a principal via para que o sangue alcance a circulação sistêmica, especialmente a parte inferior do corpo (Figura 12.4).
O fechamento fisiológico do canal arterial, que normalmente ocorre nas primeiras horas ou dias de vida, pode causar rapidamente hipoperfusão sistêmica, congestão venosa pulmonar, acidose metabólica, choque e risco de morte se não houver intervenção.
As principais cardiopatias desse grupo são:
Síndrome de hipoplasia do coração esquerdo (SHCE).
Atresia ou estenose aórtica crítica (EAC).
Interrupção do arco aórtico (IAA).
Coarctação da aorta (CoA) crítica.
Achados Clínicos e Laboratoriais
Os sintomas podem surgir poucas horas após o nascimento e frequentemente se iniciam entre o 2o e o 7o dias de vida, coincidindo com o fechamento fisiológico do canal arterial. Variam desde sinais de insuficiência cardíaca aguda até o quadro completo de baixo débito e choque cardiogênico (má perfusão periférica, taquicardia, palidez cutânea, redução da amplitude dos pulsos arteriais, hipotensão, acidose metabólica). No entanto, taquipneia é o sintoma mais precoce e, portanto, o principal.
Artéria pulmonar
Aorta
Canal arterial
Figura 12.4 Desenho esquemático de cardiopatia com fluxo sistêmico dependente do canal arterial
AD: átrio direito, AE: átrio esquerdo, VD: ventrículo direito, VE: ventrículo esquerdo. AD AE VDVE
17 Hiperbilirrubinemia Indireta no Período Neonatal, 113
18 Doença Hemorrágica do Recém-nascido por Deficiência de Vitamina K, 119
19 Anemia da Prematuridade, 122
20 Policitemia Neonatal, 126
Jaqueline Serra Brand
Introdução
A policitemia neonatal se caracteriza por um hematócrito venoso que excede os valores normais para a idade gestacional (IG) e pós-natal. Os recém-nascidos a termo (RNT) têm um aumento dos glóbulos vermelhos devido à resposta fetal de aumento da produção de hemoglobina (Hb) pelo ambiente intrauterino hipoxêmico. Embora muitos dos bebês afetados sejam assintomáticos, acredita-se que os aspectos clínicos característicos surjam da hiperviscosidade.1
A policitemia é definida como valores de hematócrito ou Hb acima de 2 desvios-padrão dos valores normais para IG e pós-natal, ou seja: condição em que, em uma amostra venosa periférica, o hematócrito se encontra >65% e/ou a Hb está >22g/dL.2
A hiperviscosidade ocorre quando o valor da viscosidade sanguínea for >2 desvios-padrão da normalidade, aferido com microviscosímetro.3
A viscosidade sanguínea e o hematócrito têm uma relação linear quando hematócrito é <60%.
Quando a viscosidade está superior a 65%, essa relação passa a ser exponencial, de tal modo que um pequeno aumento no hematócrito está associado a um grande aumento na viscosidade.4
A policitemia afeta aproximadamente 1% a 5% dos RN.1
A hiperviscosidade, aferida em amostras venosas, ocorre somente em 3% a 5% dos RN policitêmicos. Em amostras de sangue do cordão, a hiperviscosidade ocorre em cerca de 50% dos bebês com policitemia.5
É importante ressaltar que vários fatores interferem na aferição do hematócrito no primeiro dia de vida, interferindo, portanto, no diagnóstico de policitemia. Entre esses fatores, destacamos:
Local de coleta da amostra de sangue: o valor do hematócrito varia de acordo com o local da amostra de sangue obtida – alto em amos-
tra capilar, intermediário em amostra venosa periférica e baixo em sangue da veia umbilical.4
Tempo para clampeamento do cordão: quanto mais longo o tempo, maior a transfusão placentária e maior o hematócrito.6
Tempo de vida no momento da coleta de sangue: o hematócrito aumenta após o nascimento, atinge um valor máximo com 2h de vida e diminui somente a partir de 18h de vida.7
A policitemia tem etiologia multifatorial, mas as causas devem-se principalmente a dois mecanismos:8
1. Passivo (transfusão de hemácias).
2. Ativo (aumento da eritropoiese intrauterina).
A transfusão de hemácias é a causa mais comum de policitemia nos RN a termo e a demora para clampeamento do cordão umbilical (>3min), o que leva a um aumento da passagem do sangue da placenta para o bebê (aumento de 30% do volume sanguíneo).9 Outras associações incluem transfusão feto-fetal (ocorre em 10% a 15% dos gemelares monocoriônicos) e asfixia perinatal com consequente desvio do sangue da placenta para o compartimento fetal e que é também promovido pela vasodilatação fetal consequente à hipoxia.8 O aumento da eritropoiese intrauterina geralmente ocorre devido à insuficiência placentária e da hipoxia intrauterina crônica. Observa-se em RN pequenos para a idade gestacional (PIG), cujas mães apresentam pré-eclâmpsia ou outras vasculopatias. Também pode ocorrer em gestações complicadas por hipoxemia materna crônica em função de doenças cardíacas e pulmonares, uso de fármacos (propranolol), tabagismo, alta altitude e parto pós-termo; RN filhos de mães diabéticas (insulinodependentes ou com diabetes gestacional); RN grandes para a idade gestacional (GIG), como na síndrome de Beckwith-Wiedemann; hiperplasia adrenal congênita e anomalias cromossomiais (trissomias dos cromossomas 13, 18 e 21).10
y Hematócrito >70%: aumentar a taxa diária de ingesta de líquidos em 20mL/kg, por via enteral ou parenteral, para provocar uma hemodiluição e, consequentemente, diminuição da viscosidade. Atenção especial ao aumento de volume administrado em RN prematuros; portanto, tal conduta deve ser direcionada aos bebês hemodinamicamente estáveis.11,15
y Hematócrito >75%: exsanguineotransfusão parcial.11,15
RN sintomáticos:
y Hematócrito >65%: exsanguineotransfusão parcial.15
Procedimento que reduz o hematócrito sem causar hipovolemia, reduz a resistência vascular nos pulmões e aumenta a velocidade do fluxo sanguíneo no cérebro, normalizando a hemodinâmica cerebral e melhorando o estado clínico.16 O objetivo do procedimento é reduzir o hematócrito para 55%.16 O líquido que deve ser utilizado é solução fisiológica a 0,9%. O acesso vascular pode ser por via periférica ou central.17
A técnica para exsanguineotransfusão parcial ou soroferese é a seguinte: o sangue é retirado da via arterial periférica e substituído simultaneamente por líquido na via venosa. No caso de utilização de via central, o cateter venoso umbilical pode ser utilizado para retirada de sangue, enquanto a mesma quantidade de solução salina é infundida em veia periférica ou pelo próprio cateter.16
O cálculo do volume a ser trocado é realizado por meio da Fórmula 1. A volemia é estimada em 80mL/kg em RN a termo e 90mL/kg em RN prematuros.16
Fórmula 1 – cálculo do volume de sangue a ser retirado na exsanguineotransfusão parcial: Volume da EXT =
HtobservadoHtdesejado
Htdesejado
Em que: EXT: exsanguineotransfusão. Ht: hematócrito.
Prognóstico
Segundo os últimos estudos, pacientes com hiperviscosidade sanguínea no período neonatal apresentaram três vezes mais dificuldades neurológicas do que pacientes sem hiperviscosidade; o fator
que mais tem influência na função neurológica é a viscosidade, não a policitemia.16 Observa-se, adicionalmente, aumento no risco de ECN após realização da exsanguineotransfusão parcial via cateter umbilical. Ainda não se sabe se essas complicações são atribuídas à policitemia ou aos seus fatores determinantes, como insuficiência placentária ou diabetes materno.18 Ambos os fatores podem determinar morbidades independentemente da presença de policitemia. Não há evidências quanto aos benefícios da exsanguineotransfusão parcial em RN com policitemia, sobretudo em desfechos em longo prazo. Todavia, na prevenção de sintomas neurológicos graves, a exsanguineotransfusão tem se mostrado benéfica.19
Nos RN com sinais e sintomas de policitemia, deve sempre ser realizada a dosagem do hematócrito. Não se deve realizar de rotina o hematócrito em bebês aparentemente bem, mesmo com histórico de crescimento intrauterino restrito, já que RN policitêmicos assintomáticos não apresentam benefícios com o tratamento. Em todos os RN policitêmicos deve-se manter controle rigoroso de hidratação e monitoração das complicações mais comuns, como hipoglicemia e hiperbilirrubinemia. O manejo desses bebês varia de acordo com a presença, ou não, de sinais e sintomas, incluindo desde cuidados de suporte até exsanguineotransfusão parcial, geralmente limitada a pacientes com sintomas graves e que não apresentaram melhora após aumento da taxa de ingesta de líquidos. Ainda há necessidade de mais estudos comparando o efeito da exsanguineotransfusão com o manejo expectante nos desfechos a curto e longo prazo em RN policitêmicos sintomáticos e assintomáticos.
1. Gallagher PG. The neonatal erythrocyte and its disorders. In: Orkin SH, Fisher DE, Look T, Lux SE, Ginsburg D, Nathan DG (eds.). Nathan and Oski’s hematology and oncology of infancy and childhood. 8. ed. Philadelphia: WB Saunders, 2015. p. 52.
2. Luchtman-Jones L, Wilson DB. Hematologic problems in the fetus and neonate. In: Martin RJ, Fanaroff AA, Walsh MC (eds.). Neonatal-perinatal medicine. 9. ed. St. Louis: Elsevier Mosby, 2011. p. 1303.
3. Bashir BA, Othman SA. Neonatal polycythaemia. Sudan J Paediatr. 2019; 19(2):81-3.
4. Sarkar S, Rosenkrantz TS. Neonatal polycythemia and hyperviscosity. Semin Fetal Neonatal Med. 2008; 13(4): 248-55.
21 Infecções Congênitas: Diagnóstico e Conduta para Gestante e Recém-nascido, 133
22 Infecção Relacionada à Assistência à Saúde, 144
Introdução
Maria Dolores Salgado Quintans
As infecções congênitas do grupo STORCH constituem um conjunto de doenças infecciosas capazes de acometer o feto durante a gestação. O termo corresponde a um acrônimo que reúne as principais etiologias:
Sífilis.
Toxoplasma gondii.
Outras infecções (como sífilis, vírus varicela-zóster, parvovírus B19 e vírus Zika).
Rubéola.
Citomegalovírus.
Virus do herpes simples (HSV; do inglês, herpes simplex virus).
Essas infecções podem ser transmitidas verticalmente da mãe para o feto, geralmente por via transplacentária, e estão associadas a um amplo espectro de manifestações clínicas, que variam desde infecções assintomáticas até graves malformações congênitas, restrição de crescimento intrauterino, parto prematuro ou óbito fetal.
Toxoplasmose Congênita
Trata-se de uma zoonose causada pelo protozoário intracelular Toxoplasma gondii, transmitida por via transplacentária quando a infecção ocorre durante a gestação. Tem alta prevalência no Brasil.1
Etiologia
O protozoário tem como hospedeiros definitivos os felinos (gatos) e, como hospedeiros intermediários humanos e animais de sangue quente. A transmissão congênita ocorre por infecção aguda primária, reativação em gestantes imunocomprometidas e por reinfecção por cepas virulentas.2,3
Fisiopatologia
A forma ativa (taquizoíto) atravessa a placenta com infecção fetal. A transmissão é mais comum no final da gestação, porém mais grave no 1o trimestre.3
A presença de coriorretinite, calcificações intracranianas e hidrocefalia compõe a tríade clássica da toxoplasmose congênita. As características de gravidade são:
Febre.
Hidrocefalia ou microcefalia.
Hepatosplenomegalia.
Icterícia.
Convulsões.
Coriorretinite (frequentemente bilateral).
Calcificações cerebrais.
Líquido cefalorraquidiano (LCR) anormal.
Ocasionalmente, ocorrem:4-6
Erupção cutânea (maculopapular, petequial ou ambas).
Miocardite.
Pneumonite e desconforto respiratório (DR).
Defeitos auditivos.
Quadro semelhante ao da eritroblastose, trombocitopenia, linfocitose, monocitose e síndrome nefrótica.
Diagnóstico
Para a definição de toxoplasmose em gestantes, é necessário avaliar o resultado dos exames conforme pode ser visto na Tabela 21.1.
Em caso de suspeita de infecção materna por toxoplasmose antes das 16 semanas de gestação, indica-se espiramicina até a amniocentese. Após 16 semanas, se houver infecção fetal confirmada, troca-se para sulfadiazina, pirimetamina e ácido folínico. Caso o exame do líquido amniótico seja negativo e a ultrassonografia (USG) fetal esteja normal, mantém-se apenas a espiramicina. A investigação do feto inclui:
USG.
Cordocentese.
Amniocentese.
Biópsia de vilosidades coriônicas.
Tabela 21.1 Definição de infecção em gestantes
Comprovada
Soroconversão gestacional
Detecção do DNA do toxoplasma em líquido amniótico pela PCR
Provável
IgG+, IgM+, baixo índice de avidez (amostra coletada em qualquer IG)
Aumento progressivo nos títulos de IgG, IgM
IgM+ e histórico clínico sugestivo de toxoplasmose aguda gestacional
Possível
IgG+, IgM+, índice de avidez alto (amostra coletada após 12 semanas de gestação) ou indeterminado
IgG+, IgM+, em amostra única coletada em qualquer IG, sem realização de índice de avidez
Improvável
IgG+, IgM+ ou –, índice de avidez alto (amostra coletado antes de 12 semanas de gestação)
Ausente
IgG– e IgM– durante toda a gestação
IgG+ antes da concepção
IgM+, sem aparecimento de IgG
DNA: ácido desoxirribonucleico; PCR: reação em cadeia de polimerase; IgG: imunoglobulina G; IgM: imunoglobulina M, IG: idade gestacional; +: positiva; –: negativa.
Fonte: adaptada de SBP, 2020.5
A abordagem do recém-nascido (RN) está sintetizada na Figura 21.1.
Tratamento
O tratamento do RN com toxoplasmose congênita pode ser visto na Tabela 21.2. Sua duração total é de 12 meses. Nos primeiros 6 meses o esquema completo, posteriormente haverá redução das doses e monitoração mensal.5,6
Prevenção
Consiste em fazer higiene alimentar, lavar frutas e verduras, evitar consumo de carnes cruas, consumir água filtrada ou fervida, evitar manipulação de fezes ou caixas de areia de gatos e adequação do pré-natal com testagem e orientações contínuas.7,8
Sífilis Congênita
A sífilis congênita (SC) consiste em infecção fetal causada por transmissão vertical do Treponema pallidum durante a gestação, em gestantes com sífilis não tratada ou tratada de maneira inadequada.1,9,10
Etiologia e Epidemiologia
O Treponema pallidum (espiroqueta, Gram-negativo) tem alta prevalência de tratamento inadequado no Brasil (>80% entre 2019 e 2022).11
Fisiopatologia
É transmitida pela via transplacentária, com maior risco nos estágios iniciais da infecção materna (primária e secundária). A transmissão pode ocorrer em qualquer fase da gestação, sendo mais grave quanto mais precoce for a infecção do feto.12,13
RN assintomático
Realizar exames: anatomopatológico da placenta, ELISA, IgM por captura, IgG do binômio, UST, fundoscopia, hemograma
Exames alterados: estudo do LCR, função hepática e renal, audiometria, TC de crânio
Resultados normais
Criança infectada: tratamento por um ano Criança não infectada: queda progressiva dos títulos de IgG
Em RN sintomáticos deve-se solicitar o estudo anatomopatológico da placenta, ELISA, IgM por captura, IgG do binômio, fundoscopia ocular, hemograma, estudo do LCR, audiometria, funções hepática e renal, bem como TC de crânio.
Figura 21.1 Fluxograma de recém-nascido (RN) assintomático, de mãe com infecção pelo Toxoplasma gondii
ELISA: ensaio de imunoadsorção enzimática; IgM: imunoglobulina M; IgG: imunoglobulina G; UST: ultrassonografia transfontanela; TC: tomografia computadorizada.
Fonte: adaptada de SBP, 2020.5
23 Hipoglicemia no Recém-nascido, 153
24 Hiperglicemia no Recém-nascido, 161
25 Hipocalcemia no Recém-nascido, 164
26 Doença Metabólica Óssea da Prematuridade, 167
27 Erros Inatos do Metabolismo, 172
28 Síndromes Genéticas no Período Neonatal: Diagnóstico e Manejo, 181
Introdução
Adauto Dutra Moraes Barbosa
O valor exato de glicose no sangue abaixo do qual um recém-nascido (RN) corre o risco de apresentar neurodesenvolvimento adverso é desconhecido, mas dosagem de glicose no plasma ≤47mg/dL (≤2,6mmol/l) tem sido considerada o nível de investigação e intervenção terapêutica.1,2
Um valor de glicemia capilar inferior a 60mg/dL, obtido por glicosímetro à beira do leito, deverá ser confirmado por dosagem de glicose no plasma.3
Incidência
Hipoglicemia ocorre em 1,3 a 4,4 casos por 1.000 recém-nascido a termo (RNT) e em 15 a 55 casos por 1.000 recém-nascido pré-termo (RNPT).
A incidência descrita é de cerca de 15% em todos os neonatos assintomáticos4 e de 50% em bebês nascidos com fatores de risco, incluindo RN filhos de gestantes diabéticas, RN grandes ou pequenos para a idade gestacional (IG), e RN nascidos de partos prematuros ou de partos com estresse perinatal.3
A hipoglicemia incide em cerca de 8% nos RN grandes para a idade gestacional (GIG) e 15% nos pequenos para a idade gestacional (PIG).5
Etiopatogenia
De maneira geral, a hipoglicemia do RN ocorre por três mecanismos principais:
1. Situações que cursam com hiperinsulinemia.6
2. Situações que cursam com baixo estoque de glicogênio.7
3. Situações que cursam com excessivo consumo de glicose.8
Situações que Cursam com Hiperinsulinemia
Entre as situações que cursam com hiperinsulinemia podem ser citadas:
RN filho de gestante diabética.
RN GIG.
Casos que cursam com hiperinsulinismo.
Recém-nascido Filho de Gestante Diabética
O filho de uma gestante diabética pode ser anormalmente grande ao nascimento (RN grande para a IG), mesmo quando a gestante consegue manter normal ou praticamente normal sua concentração de glicose no sangue durante toda a gestação.
A ação da alta concentração de insulina circulante no feto, secundária à alta taxa de glicose ofertada pela gestante diabética, promove o crescimento dos órgãos, exceto do fígado e do cérebro, resultando em macrossomia.9
O risco de defeitos congênitos9 é duas a quatro vezes maior nos fetos de gestantes diabéticas, sobretudo quando sua glicemia é mal controlada durante o período de formação dos órgãos do feto, particularmente entre a 6a e a 7a semanas de gestação.
A taxa de mortalidade neonatal é superior a cinco vezes à taxa dos neonatos de gestantes não diabéticas.10
Hiperglicemia materna intermitente causa hiperglicemia no feto, estimulando a hiperprodução de insulina pelo pâncreas do feto (Figura 23.1). Por um lado, esse incremento de insulina no feto estimula o crescimento excessivo dos órgãos, exceto o cérebro e possivelmente o fígado, pois estes não dependem do aporte de insulina para o seu crescimento, levando à macrossomia fetal. Por outro lado, eleva a incidência de hipoglicemia neonatal e lipólise acentuada durante as primeiras horas após o nascimento. O hiperinsulinismo e a hiperglicemia podem, também, provocar acidose no feto, que resulta em maior taxa de partos de natimortos. Embora o hiperinsulinismo seja provavelmente a principal causa da hipoglicemia, as respostas reduzidas de epinefrina e glucagon também podem ser fatores contribuintes. Os níveis de cortisol e de hormônio do crescimento são normais.
Estimula crescimento dos órgãos (exceto cérebro e fígado)
Macrossomia
Hiperglicemia gestacional intermitente
Hiperglicemia fetal
Superprodução de insulina pelo pâncreas fetal
Promove acidose fetal
Nas primeiras horas após o nascimento
Maior taxa de natimortos Hipoglicemia Lipólise acentuada
Figura 23.1 Recém-nascido filho de gestante diabética
SNC: sistema nervoso central.
Fonte: elaborada pelo autor.
Recém-nascido Grande para a Idade
Gestacional
O RN GIG também pode apresentar hipoglicemia pelo mesmo mecanismo do filho de diabética; entretanto, a normalização da glicemia ocorre logo nas primeiras horas de vida.
A hipoglicemia associada à hipoglicemia hiperinsulinêmica persistente da infância (HHPI) resulta de secreção inapropriada de insulina ou de hiperinsulinismo.11 Nos portadores dessa doença, a hipoglicemia desencadeada pelo jejum é sempre acompanhada de aumento da concentração de insulina no plasma, em geral inapropriadamente alta em relação à baixa concentração de glicose no sangue concomitante. A doença parece estar relacionada mais a um aumento global da atividade endócrina funcional do pâncreas do que a um aumento do número de células beta do pâncreas. Os pacientes com HHPI são, em sua maioria, RN GIG, como consequência do hiperinsulinismo, mas sem hepatomegalia importante. Apresentam sintomas persistentes de hipoglicemia, incluindo hipotonia, cianose, apneia e convulsões de difícil controle, já no período neonatal. Morte súbita em RN também é vista em pacientes com HHPI. Apesar de rara, a grande frequência de dano cerebral e retardamento mental, em consequência de hipoglicemias graves, justifica a necessidade de diagnóstico etiológico precoce e tratamento imediato das crianças com hipoglicemia de difícil controle.
Lesão de SNC
O diagnóstico de HHPI é cogitado quando a hipoglicemia surge logo após o nascimento e requer altas taxas de infusão de glicose, geralmente excedendo a 10mg/kg/min, podendo chegar a valores de 15 a 20mg/kg/min. Tipicamente, esses neonatos apresentam altos níveis de insulina no sangue, e, com frequência, são acima de 10µU/mL e a relação entre insulina (µU/mL) e glicose (mg/dL) apresenta valores superiores a 1:4 ou mais.
Os adenomas de células beta caracterizam-se por um hiperinsulinismo acentuado e de início precoce. Requerem remoção cirúrgica12 ou pancreatectomia parcial e são pouco comuns no período neonatal.
O diagnóstico definitivo pode ser feito somente com exame anatomopatológico e pode requerer estudo imuno-histoquímico.
O prognóstico dessa doença depende essencialmente de detecção precoce, diagnóstico correto e imediata instalação de terapêutica para correção da hipoglicemia. Quando necessário, o tratamento cirúrgico impõe-se precocemente.
A síndrome de Beckwith-Weidemann 13 é uma das mais comuns síndromes de supercrescimento em que se pode identificar mais de 75% dos RN acima do percentil 90 para o peso e para o comprimento. Estima-se que ocorra em 1 a cada 13.700 nascimentos, mas a existência de casos leves pode subestimar a verdadeira frequência desta síndrome. Não há predomínio em nenhum dos sexos. Caracteriza-se por gigantismo, onfalocele, e
29 Cirurgia Neonatal: o Básico para não Especialistas, 193
30 Procedimentos em Neonatologia, 203
Lisieux Eyer de Jesus
Introdução
A melhora dos resultados do tratamento de crianças de alto risco em unidade de terapia intensiva neonatal (UTIN) e a evolução da medicina fetal, com melhores protocolos e nascimentos de crianças portadoras de doenças graves em hospitais de referência, modificaram o tratamento das doenças cirúrgicas neonatais e trouxeram novos desafios técnicos e tecnológicos. Cirurgia não é a arte de operar; é a arte de tratar da melhor maneira possível pacientes com indicação de procedimentos cirúrgicos, e não é trabalho de uma pessoa: é da harmonia entre os vários experts na equipe multiprofissional, do uso razoável de recursos e da predominância de planejamento baseado em evidências, levando-se em conta as circunstâncias individuais, que nascem bons resultados (Figura 29.1).
Outra questão é o aumento na incidência de nascimentos de crianças de peso extremamente baixo, de partos múltiplos e de prematuros extremos e de doenças típicas desses pacientes (obstrução intestinal funcional por íleo por mecônio do prematuro extremo e perfuração espontânea do trato digestivo, que atualmente competem com as enterocolites necrosantes [ECN]), trazendo questões ligadas a expertise, protocolos em evolução e miniaturização de materiais necessários para a assistência.
Optamos, neste capítulo, pela abordagem preferencial de alguns temas, de maior urgência, maior frequência ou que exigem a participação imediata do neonatologista como mediador da conduta clínica até a chegada do cirurgião, já que frequentemente estes profissionais trabalham em regime de consultoria alcançável e que a transferência
Diagnóstico gestacional de feto com malformação congênita
Discussão equipe multiprofissional
Planejamento do parto, planejamento da conduta perinatal
Preparo dos pais para a situação
Planejamento de pessoal/logística/ materiais para atendimento
Inserção de monitoração invasiv/cateteres a centrais
Estabilização clínica e preparo doRN para cirurgia
Investigação e avaliação anestésica
Cirurgia
Figura 29.1 Fluxograma da conduta ideal para tratamento de crianças com diagnóstico de malformação fetal RN: recém-nascido.
para serviços terciários é muitas vezes necessária para bebês nascidos com doenças cirúrgicas não previstas. Em muitos casos, a conduta até o momento da entrega do paciente ao serviço especializado será determinante dos resultados.
As principais anomalias são:
Gastrósquise: tipicamente, um orifício periumbilical na parede abdominal direita, através do qual vísceras (mais frequentemente, intestino delgado e estômago) se exteriorizam livremente, sem nenhuma cobertura por membrana amniótica ou peritoneal. O cordão umbilical é independente do defeito, embora se situe em sua vizinhança (Figura 29.2).
Onfalocele: trata-se de uma formação incompleta da parede abdominal. O conteúdo visceral
Vísceras sem cobertura
presente no abdome é visível por transparência, contido por uma cobertura de membrana amniótica ou peritônio parietal: as vísceras não se encontram “livres”. O cordão umbilical situa-se dentro do defeito (ver Figura 29.2).
Se ocorrer ruptura da membrana de cobertura (onfalocele rota), pode haver dificuldade em diferenciar onfalocele de gastrósquise, e, nesses casos (incomuns), o examinador vê que o cordão e os vasos umbilicais estão dentro do defeito, passando sobre as vísceras exteriorizadas. A grande maioria das onfaloceles é central com relação ao cordão umbilical, mas é possível a ocorrência de onfaloceles cefálicas (associadas à pêntade de Cantrell, tipicamente apresentando exposição do coração coberto por pericárdio, com batimentos visíveis) e caudais (estas relacionadas às anomalias genitais e à diástase púbica, nas extrofias vesicais e de cloaca) (Figura 29.3).
Orifício da gastroquise
Cordão umbilical
Linha média
Linha média Gastrquise Onfalocele ó
Figura 29.2 Diferenças entre gastrósquise e onfalocele
Batimento cardíaco visível
Vísceras com cobertura (membrana)
Contorno da onfalocele
Cordão umbilical
Linha média
Linha média
Vísceras com cobertura (membrana)
Contorno da onfalocele (parede abdominal)
Cordão umbilical
Vísceras com cobertura (membrana)
Conto no da r onfalocele
Cordão umbilical Onfalocele cefálica
Placa vesical (extrofia)
Onfalocele caudal
CAPÍTULOS
31 Síndrome Hipóxico-isquêmica e Hipotermia Terapêutica, 209
32 Convulsões Neonatais, 218
33 Hemorragia Intracraniana Neonatal, 224
34 Abordagem da Dor em Neonatologia, 229
Introdução
Arnaldo Costa Bueno Lucia De La Candelaria Arenas Viera
O termo asfixia, do grego asphyxia, significa sufocamento e é utilizado no contexto neonatal para descrever a interrupção do fluxo de oxigênio através da placenta ou do cordão umbilical para o feto.1 Trata-se de uma das principais causas de morbilidade e mortalidade em crianças e está presente em 20% dos óbitos neonatais precoces, segundo os dados do Programa de Reanimação Neonatal da Sociedade Brasileira de Pediatria (SBP). No Brasil, a asfixia perinatal é a terceira causa básica de óbito, atrás apenas de prematuridade e anomalias congênitas.2 Em 2023, foram registrados 2.537.576 nascidos vivos. Estima-se que cerca de 3.600 recém-nascidos (RN) tenham evoluído para óbito precoce relacionado à asfixia perinatal, à hipoxia ao nascimento e/ou à síndrome de aspiração de mecônio. A mortalidade neonatal precoce associada à asfixia perinatal é elevada mesmo em RN de baixo risco, ou seja, aqueles com peso ao nascimento superior ou igual a 2.500g e sem malformações congênitas.3
A lesão cerebral que resulta da asfixia é conhecida como encefalopatia hipóxico-isquêmica (EHI) e ocorre em aproximadamente 1 a 3 a cada 1.000 nascidos vivos em países desenvolvidos.4,5 Ensaios clínicos mostraram que o tratamento com hipotermia terapêutica (HT) durante três dias consecutivos (72h) é protetor para o cérebro do RN que sofreu um evento agudo de asfixia com EHI moderada a grave.6
A EHI resulta de um insulto agudo ou prolongado de hipoxia e/ou isquemia, que desencadeia um processo em fases, afetando especialmente o cérebro imaturo. A fase inicial (primária) envolve falência da microcirculação, depleção de trifosfato de adenosina (ATP), acúmulo de íons intracelulares e edema citotóxico, acarretando necrose celular. A fase secundária ocorre horas após a reperfusão
e caracteriza-se por disfunção mitocondrial, produção de radicais livres, excitotoxicidade mediada por glutamato e influxo de cálcio, ativação de caspases e morte celular por apoptose. A resposta inflamatória local, com liberação de citocinas e ativação microglial, contribui para agravamento do dano. Fatores, como idade gestacional (IG), vascularização do cérebro e tipo e duração do insulto, influem no padrão de lesão, com predomínio de lesões nos núcleos da base e no tálamo nas formas agudas, e em regiões corticais ou de watershed nas formas mais prolongadas. A compreensão dessas fases fundamenta a janela terapêutica de até 6h para intervenções neuroprotetoras, como a hipotermia.7
A HT é indicada para RN com EHI moderada a grave manifestada nas primeiras 6h de vida. Inicialmente, devem-se excluir contraindicações absolutas (IG <35 semanas, peso <1.800g, idade >6h ou malformações maiores incompatíveis com a vida). Na sequência, recomenda-se a verificação dos critérios mostrados adiante (Tabela 31.1).
Confirmado o insulto, avalia-se o critério categoria B: presença de encefalopatia moderada ou grave, com base na avaliação clínica (Sarnat em estágio II ou III, ou escore de Thompson ≥8). Quando o exame neurológico é inconclusivo, o eletroencefalograma de amplitude integrada (aEEG) pode auxiliar na decisão terapêutica. O algoritmo mostrado na Figura 31.1 ilustra os critérios clínicos, laboratoriais
Tabela 31.1 Critérios de categoria A para confirmação de insulto
Evidência de insulto hipóxico-isquêmico por gasometria (pH <7 ou excesso de base ≤–16mEq/L)
Achados clínicos compatíveis (Apgar ≤5 aos 10min, necessidade de VPP prolongada)
VPP : ventilação com pressão positiva.
Critérios de elegibilidade
Avaliação clínica e bioquímica
Critérios de exame neurológico
Gasometria da primeira hora <7,0 ou BD 16mE/L
IG >35 semanas PN >1.800g
Gasometria da primeira hora <7,0 a 7,15 ou BD 10 a 15mE/L
Gasometria da primeira hora não disponível
Evento agudo perinatal
Apgar no 10min de vida≤5 pontos ou VPP >10min
EHI moderada (Sarnat II) ou grave (Sarnat III), Thompson >8 Iniciar hipotermia
Atividade convulsiva confirmada Iniciar hipotermia
Figura 31.1 Fluxograma de elegibilidade para hipotermia terapêutica em recém-nascidos ≥35 semanas
IG: idade gestacional; PN: peso ao nascimento; BD: déficit de base (excesso de base); VPP: ventilação com pressão positiva; EHI: encefalopatia hipóxico-isquêmica; Sarnat: classificação clínica da encefalopatia neonatal.
e neurológicos para indicação de HT nos casos de EHI moderada ou grave. A abordagem baseia-se na identificação precoce de insulto hipóxico-isquêmico, seguida de avaliação neurológica estruturada.
Terapêutica Neonatal
Manejo Ventilatório
O suporte ventilatório durante a HT deve ser instituído de acordo com a necessidade clínica do
RN, e pode incluir ventilação não invasiva (VNI), pressão positiva contínua nas vias aéreas (CPAP; do inglês, continuous positive airway pressure) ou ventilação mecânica invasiva (VMI) (Figura 31.2).
Manejo de Fluidos e Eletrólitos
No manejo de fluidos e eletrólitos durante a HT, devem-se considerar as alterações fisiológicas relacionadas à redistribuição de líquidos, ao metabolismo reduzido e às mudanças na função renal e eletrolítica induzidas por hipotermia e processo de
Manejo ventilatório conforme necessidade clínica (CPAP/VNI/VMI)
Surfactante considerar em casos de alteração da oxigenação: Síndrome de aspiração meconial hemorragia pulmonar lesão inflamatória pós-asfixia dose: 200mg/kg
VMI VG: Volume corrente alvo: 4 a 6mL/kg Parâmetros mínimos eficazes
pCOalvo: 2 40 a 50mmHg corrigir para 33,5°C (a 0,83) pO: 60 a 80mmHg 2 SatO: 90% a 95% 2
Evitar: Hipocapnia/ Hiperoxia Gases umidificados e aquecidos a 37°C. Evitar contato entre: Circuitos respiratórios, dispositivos de arrefecimentorisco → de condensação
Figura 31.2 Manejo ventilatório do recém-nascido em hipotermia terapêutica conforme a necessidade clínica
CPAP: pressão positiva contínua nas vias aéreas; VNI: ventilação não invasiva; VMI: ventilação mecânica invasiva; VG: volume-alvo; pCO2₂: pressão parcial de dióxido de carbono; pO2₂: pressão parcial de oxigênio; SatO2₂: saturação periférica de oxigênio.
35 Cuidados Paliativos, 237
36 Triagem Auditiva Neonatal, 247
37 Oftalmoscopia e Triagem Ocular Neonatal, 250
38 Retinopatia da Prematuridade: a Interface entre Oftalmologia e Neonatologia, 253
39 Hidratação Venosa: Guia Prático para Neonatologistas, 260
40 Efeitos Fetais e Neonatais das Drogas de Abuso, 267
41 Transporte Neonatal, 278
42 Exames de Imagem em Perinatologia, 283
Heron Werner Júnior Pedro Teixeira Castro Tatiana Mendonça Fazecas e Costa
Introdução
A perinatologia, também conhecida como medicina materno-fetal, é uma subespecialidade dedicada ao estudo, ao diagnóstico e ao acompanhamento de gestações de alto risco, com atenção tanto à saúde da gestante quanto ao desenvolvimento do feto. Nesse campo, os métodos de imagem desempenham papel essencial na avaliação da anatomia e da fisiologia do feto, na identificação precoce de malformações, no planejamento terapêutico e no aconselhamento à família.1,2
O exame por imagem em perinatologia evoluiu significativamente nas últimas décadas, acompanhando os avanços tecnológicos que permitiram melhor resolução, maior rapidez e mais segurança. Atualmente, a ultrassonografia (USG) e a ressonância magnética (RM) são as principais modalidades, complementadas em casos específicos por radiografia, tomografia computadorizada (TC) (de uso restrito, devido à radiação ionizante) e, mais recentemente, técnicas emergentes de inteligência artificial (IA) aplicadas à análise de imagens.3,4
Ultrassonografia: Método de Primeira Escolha
A USG é universalmente reconhecida como a primeira linha de investigaçãoem perinatologia. Entre suas principais vantagens estão:2,4,5
Baixo custo.
Portabilidade.
Ausência de radiação ionizante.
Boa aceitação pela gestante.
Grande disponibilidade de profissionais capacitados.
O exame ultrassonográfico permite:
Rastreamento de malformações congênitas.
Avaliação do crescimento e do bem-estar do feto.
Estudo hemodinâmico por Doppler colorido.
Guia em procedimentos invasivos (como biópsia de vilo corial, amniocentese, transfusões intrauterinas).
Entretanto, a USG apresenta limitações. Fatores, como obesidade da gestante, oligo-hidrâmnio e posição desfavorável do feto, podem reduzir a qualidade das imagens. Além disso, algumas anomalias complexas, especialmente do sistema nervoso central (SNC), podem não ser caracterizadas de maneira adequada apenas por meio da USG.
Nas últimas duas décadas, a RM fetal consolidouse como método complementar indispensável. A RM oferece excelente contraste entre tecidos moles, maior campo de visão e independência em relação aos fatores que limitam a USG (Figuras 42.1e 42.2).1,3
Vantagens da RM:
y Detalhamento da anatomia, superior, sobretudo no SNC.
y Avaliação precisa em situações de oligohidrâmnio e obesidade da gestante.
y Imagens multiplanares de alta resolução.
y Ausência de radiação ionizante.
Limitações da RM:
y Menor disponibilidade em relação à USG.
y Maior custo.
y Movimentação do feto pode gerar artefatos.
y Necessidade de profissionais altamente especializados.
De acordo com as diretrizes da Sociedade Internacional de Ultrassom em Obstetrícia e Ginecologia (ISUOG), a RM deve ser utilizada em casos selecionados, preferencialmente após a 22a semana de gestação, para complementar achados ultrassonográficos e oferecer informações adicionais para o aconselhamento perinatal.
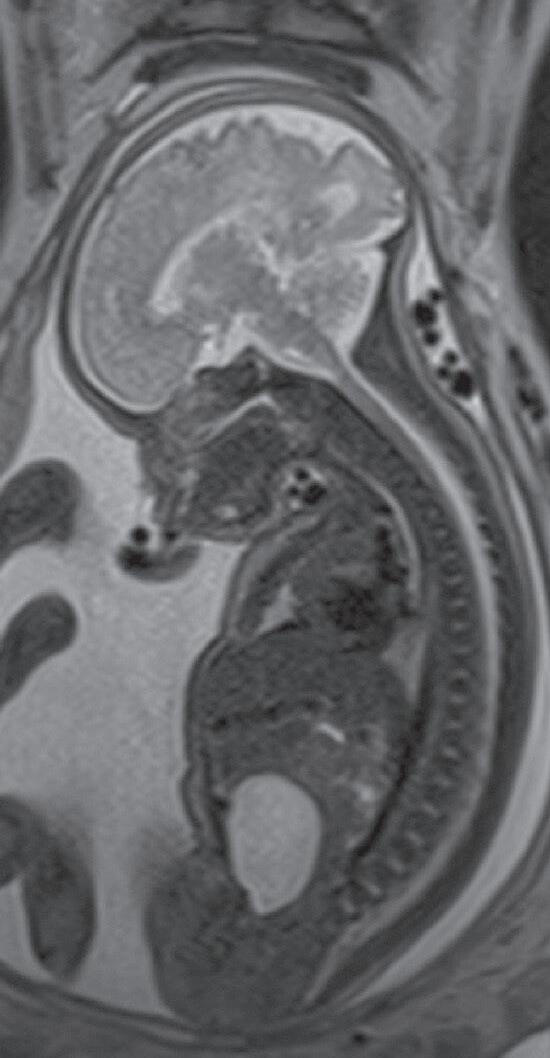
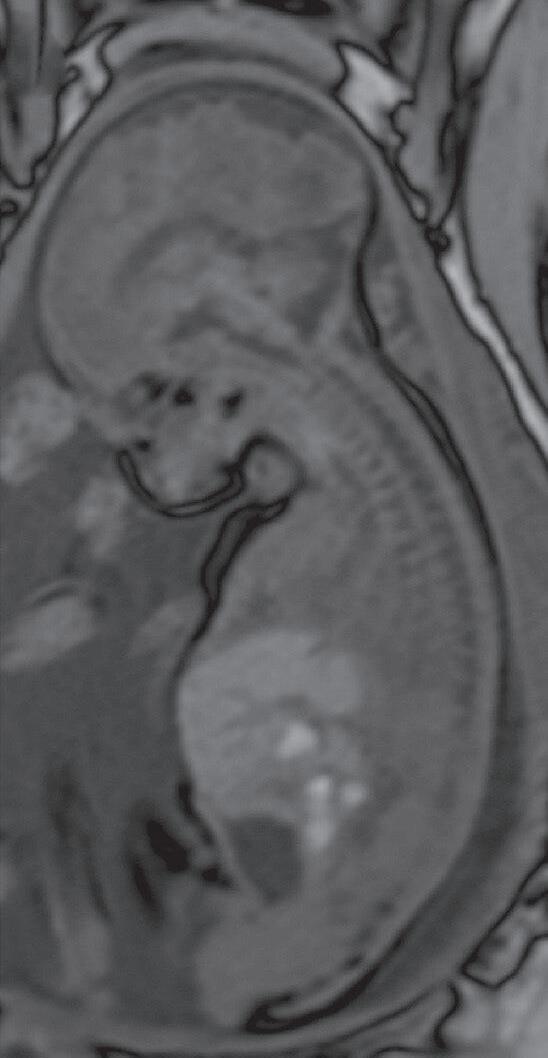
Figura 42.1 (A e B) Vantagens da ressonância magnética do feto: o grande campo de visão permite a visualização da anatomia do feto em grande escala, mesmo em gestações cronologicamente mais avançadas. A visualização das relações entre órgãos e o bom contraste entre eles permite um estudo anatômico detalhado do feto. A imagem sagital em sequência pesada em T2 de um feto na 32a semana de gestação permite a visualização de todo o seu sistema nervoso central, do sacro ao encéfalo (A ). A imagem do feto em sequência pesada em T1 mostra alguns órgãos com contraste diferente em comparação às sequências T2, principalmente fígado e cólon (B)
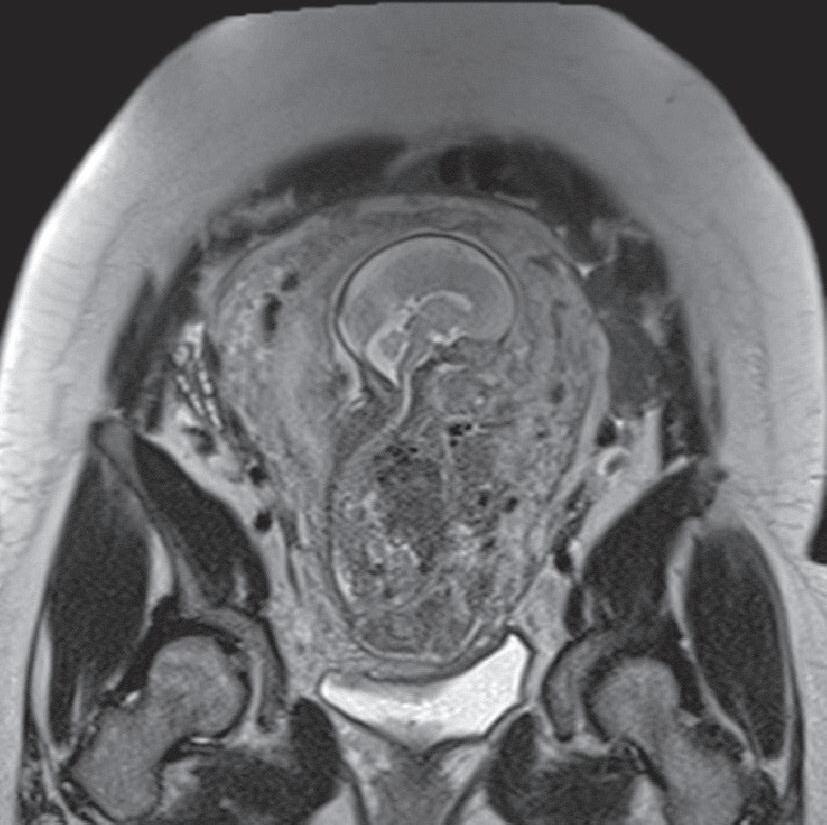
Figura 42.2 Imagem coronal da gestante de um feto com 24 semanas, adramnia e obesidade materna. A ressonância magnética (RM) pode auxiliar na avaliação do feto em casos com pouco líquido amniótico e em casos de obesidade materna, obtendo bom contraste entre tecidos fetais. No caso aqui ilustrado, a RM possibilitou o diagnóstico de agenesia renal bilateral
da Ressonância Magnética
Estudos internacionais mostram que a RM fetal, quando realizada sem contraste e em campos de 1,5 Tesla, não está associada aos efeitos adversos para o feto nem para a gestante. O uso de campos de 3 Tesla ainda é mais restrito, mas crescente, em razão do maior detalhamento anatômico que proporciona. As contraindicações absolutas seguem as mesmas da RM em adultos, como marca-passos não compatíveis e implantes ferromagnéticos.3
Aplicações Clínicas da Imagem em Perinatologia
Sistema Nervoso Central
A RM é particularmente útil na avaliação de ventriculomegalias, agenesia do corpo caloso, malformações de fossa posterior e alterações relacionadas às infecções congênitas (como vírus Zika [ZIKV], citomegalovirus [CMV] e toxoplasmose) (Figuras 42.3 a 42.6).6-11
