
Fibrosis Sí, inflamación ¿Sí o no?. ¿Es importante una correcta estratificación del paciente?
Javier Crespo Hospital Universitario Marqués de Valdecilla@DrJavierCrespo
Javier.crespo@scsalud.es


Fibrosis Sí, inflamación ¿Sí o no?. ¿Es importante una correcta estratificación del paciente?
Javier Crespo Hospital Universitario Marqués de Valdecilla@DrJavierCrespo
Javier.crespo@scsalud.es

• MAFLD: A Consensus-Driven Proposed Nomenclature for MAFLD. Gastroenterology 2020 https://doi.org/10.1053/j.gastro.2019.11.312
• A new definition for metabolic dysfunction-associated fatty liver disease: An international expert consensus statement. J Hepatol 2020.
• Romero-Gómez M, Ampuero J. Looking for a new name for non-alcoholic fatty liver disease in Spanish: esteatosis hepática metabólica (EHmet). Rev Esp Enferm Dig. 2021 Mar;113(3):161-163. doi: 10.17235/reed.2021.7862/2021. PMID: 33573385.



Prevalencia del 25% en la población general
La fibrosis hepática es el marcador pronóstico clave de mortalidad general en pacientes con NAFLD



Mortalidad global del 44,98%; HR 1,97

El grado de fibrosis es determinante del pronóstico
Fibrosis is the only independent predictor of clinical outcomes1

Greatest unmet medical need in NASH is in the F3/F4 population


Prevalencia MAFLD con fibrosis significativa en España.

Calleja JL, Rivera-Esteban J, Aller R, Hernández-Conde M, Abad J, Pericàs JM, Benito HG, Serra MA, Escudero A, Ampuero J, Lucena A, Sánchez Y, Arias-Loste MT, Iruzubieta P, Romero-Gómez M, Augustin S, Crespo J. Prevalence estimation of significant fibrosis because of NASH in Spain combining transient elastography and histology. Liver Int. 2022 May 28. doi: 10.1111/liv.15323. Epub ahead of print. PMID: 35643936.

Calleja JL, Rivera Esteban J, Aller R, Hernández Conde M, Abad J, Pericàs JM, Benito HG, Serra MA, Escudero A, Ampuero J, Lucena A, Sánchez Y, Arias-Loste MT, Iruzubieta P, Romero-Gómez M, Augustin S, Crespo J. Prevalence estimation of significant fibrosis because of NASH in Spain combining transient elastography and histology. Liver Int. 2022 May 28. doi: 10.1111/liv.15323. Epub ahead of print. PMID: 35643936.

Prevalencia MAFLD con fibrosis significativa en España.
Consenso en MAFLD. AEEH 2022.
Pregunta 5.- ¿Es clínicamente suficiente detectar fibrosis hepática avanzada mediante métodos no invasivos bioquímicos en las enfermedades hepáticas prevalentes ocultas como EHmet y EHAlc?
Respuesta 5: Sí, para el cribado, la detección de datos de sospecha de fibrosis avanzada en las enfermedades hepáticas prevalentes puede ser el criterio más adecuado para la toma de decisiones en EHmet y EHAlc. En las hepatitis virales se investigará además la serología y carga viral.

Nivel de evidencia: A; Grado de recomendación: 1. En el caso de las enfermedades no virales (EHmet y EHAlc), la evaluación de la fibrosis mediante métodos bioquímicos se considera la opción más adecuada de cribado debido a que la fibrosis es el principal factor pronóstico y la diana terapéutica.
Además, en pacientes con sospecha de fibrosis avanzada se debe indicar la derivación al hepatólogo para confirmar el diagnóstico, plantear el seguimiento y la propuesta terapéutica.
2022
13:S0210-5705(22)00137-6.
Romero-Gómez M, Aller R, Ampuero J, Fernández Rodríguez C, Augustín S, Latorre R, Rivera-Esteban J, Martínez Urroz B, Gutiérrez García ML, López SA, Albillos A, Hernández M, Graupera I, Benlloch S, Olveira A, Crespo J, Calleja JL. AEEH «Consensus about detection and referral of hidden prevalent liver diseases». Gastroenterol Hepatol. May English, Spanish. doi: 10.1016/j.gastrohep.2022.04.001. Epub ahead of print. PMID: 35569541.Consenso en MAFLD. AEEH 2022.

Pregunta 15. Desde un punto de vista práctico, ¿se puede asumir la ausencia de fibrosis avanzada o cirrosis en individuos adultos de población general con elastografía transitoria < 8 kPa?
Respuesta 15: Sí. El dintel de 8 kPa ha demostrado un alto valor predictivo negativo para excluir cirrosis en estudios diagnósticos y un bajo riesgo de eventos hepáticos en estudios longitudinales
Nivel de evidencia: B; Grado de recomendación: 1. La ET (medida con FibroScan®) ha demostrado una gran utilidad diagnóstica para la predicción de fibrosis avanzada/cirrosis hepática. Los puntos de corte de ET recomendados para descartar fibrosis avanzada y cirrosis hepática varían entre 8 y 13 kPa, en función de la etiología subyacente. En este sentido, cabe destacar que el riesgo a medio plazo de eventos hepáticos en pacientes con ET por debajo de estos dinteles es muy bajo (para el ejemplo de EHmet, el riesgo de evento hepático a 5 años con FibroScan® < 12 kPa es 0.3%).
En función de lo anterior, parece prudente adoptar, de forma generalizada, el valor de ET < 8 kPa para descartar fibrosis avanzada y cirrosis hepática, dada su transferibilidad entre etiologías, la baja tasa de falsos negativos y la prácticamente nula incidencia de eventos hepáticos a medio plazo.
Romero-Gómez M, Aller R, Ampuero J, Fernández Rodríguez C, Augustín S, Latorre R, Rivera-Esteban J, Martínez Urroz B, Gutiérrez García ML, López SA, Albillos A, Hernández M, Graupera I, Benlloch S, Olveira A, Crespo J, Calleja JL. AEEH «Consensus about detection and referral of hidden prevalent liver diseases». Gastroenterol Hepatol. 2022 May 13:S0210-5705(22)00137-6. English, Spanish. doi: 10.1016/j.gastrohep.2022.04.001. Epub ahead of print. PMID: 35569541.




Nuevo paradigma: Inflamación


1. Las IMIDs (al menos algunas IMID) se asocian a un alto riesgo de MAFLD.

2. Este riesgo es, en ocasiones, independiente de los factores de riesgo clásicos (Obesidad, DM2)
3. Además del incremento del riesgo de MAFLD, existe un claro incremento del riesgo de fibrosis significativa.
4. ¿EXISTE UN MAFLD DE FENOTIPO INFLAMATORIO?
Sujetos > 50 años + DM2 + IMC > 25
N = 224
NASH registry.
N = 223
No hay datos de analítica completos (falta AST), n=1
Nos disponen de fibroscan (n= 9)
N = 214
Fibroscan válido
N = 214
Biopsia hepática
N = 141
Analítica completa, fibroscan + FIB-4
N = 140
Biopsia y analítica difieren menos de 1 año
N = 124
Nos disponen de evaluación fibra (n= 1)
Biopsia y analítica más de año (n= 16) Iruzubieta
NASH registry. Descripción de la cohorte.
Analítica completa, fibroscan + FIB-4 (biopsia y analítica < 1 año)


N = 124
N = 23 (18,6%)
N = 35 (28,2%)
N = 66 (53,2%)
Iruzubieta et al. NASH registry 2022; submitted. NAFL NASH (F0-F1) NASH (F2-F4)FIBROSIS
0: 12 (52%), 1: 11 (48%), 2: 0 (0%), 3: 0 (0%), 4: 0 (0%)
0: 8 (23%), 1: 27 (77%),
2: 0 (0%), 3: 0 (0%), 4: 0 (0%)
0 (0%)
0: 0 (0%), 1: 0 (0%),
2: 23 (35%), 3: 25 (38%), 4: 18 (27%) 2.26e-25
0: 21 (17%), 1: 72 (58%), 2: 31 (25%), 3: 0 (0%)
0: 20 (16%), 1: 38 (31%), 2: 23 (19%), 3: 25 (20%), 4: 18 (15%)
Tabla: Clinical and biochemical characteristics of the patients included in the study. Statistical significance was determined by Chi-square test for categorical variables and Kruskal-Wallis Htest for continuous variables.
NASH registry. Descripción de la cohorte.
NASH registry. Sistemática de estudio.
1. Test no invasivos de fibrosis hepática:
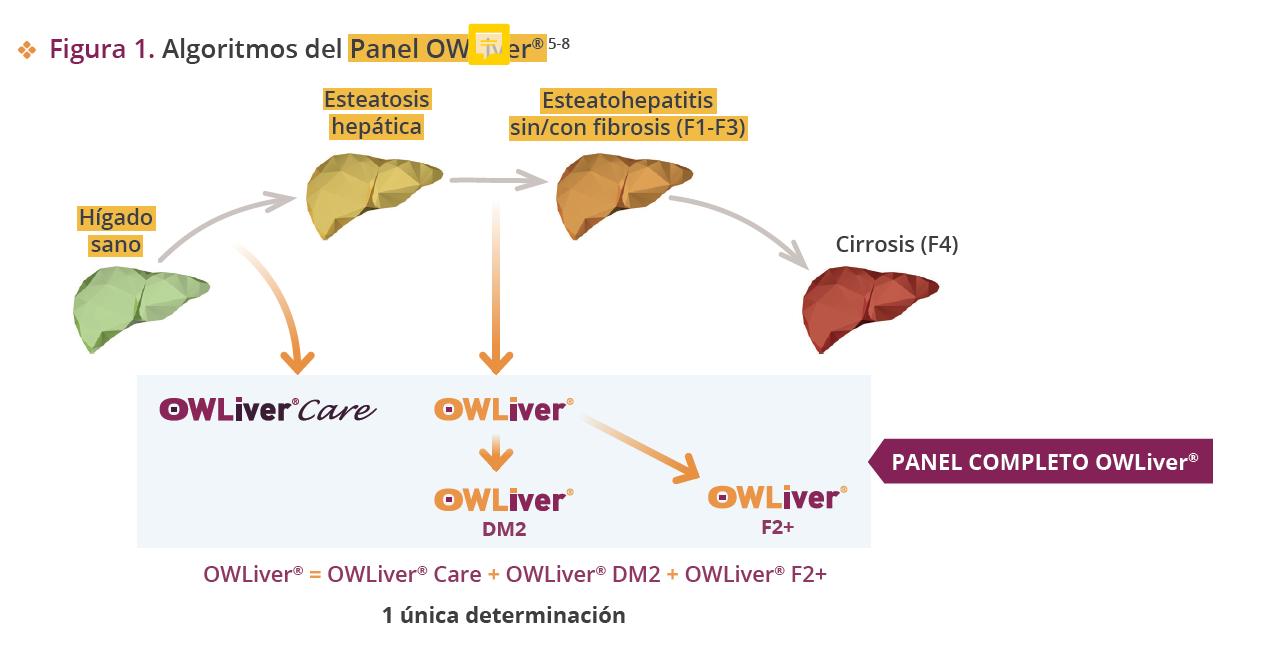
a. FIB4
b. Fibroscan
2. OWliver
NASH registry. Resultados FIB4.
Sujetos >50 años + DM2 + IMC>25 N = 124
16 + 11 + 21 = 48
El punto de corte inferior de FIB-4 tiene un VPN pobre en esta población de riesgo
NASH registry. Resultados.
Positivo
De los 48 pacientes, se rescatan 32
Sujetos >50 años + DM2 + IMC>25
El Fibroscan sobre-estima la fibrosis en esta población de riesgo
Dx inadecuado: 45
De los 45 casos con diagnóstico inadecuado, se rescatan 31
NASH registry. Conclusiones.
• El perfil metabolómico OWLiver®DM2 presenta una excelente capacidad para diagnosticar NASH en pacientes con diabetes mellitus.
• El punto de corte inferior de FIB-4 tiene un VPN pobre en esta población de riesgo, por lo tanto, el rendimiento diagnóstico de este índice no invasivo en pacientes con alto riesgo de NASH es bajo.
• La aplicación secuencial de FIB-4 y OWLiver®F2+ puede ser una herramienta de cribado precisa, no invasiva, y fácil de usar para la detección de esteatosis hepática metabólica progresiva entre los sujetos con un riesgo elevado.
Consenso en MAFLD. AEEH 2022.

Romero-Gómez M, Aller R, Ampuero J, Fernández Rodríguez C, Augustín S, Latorre R, Rivera-Esteban J, Martínez Urroz B, Gutiérrez García ML, López SA, Albillos A, Hernández M, Graupera I, Benlloch S, Olveira A, Crespo J, Calleja JL. AEEH «Consensus about detection and referral of hidden prevalent liver diseases». Gastroenterol Hepatol. 2022 May 13:S0210-5705(22)00137-6. English, Spanish. doi: 10.1016/j.gastrohep.2022.04.001. Epub ahead of print. PMID: 35569541.
