
Especial Diabetes
Agonistas del receptor GLP-1 y su relación con la retinopatía diabética
p. 6
Tomografía de coherencia óptica en el tratamiento de la retinopatía diabética p. 12






Agonistas del receptor GLP-1 y su relación con la retinopatía diabética
p. 6
Tomografía de coherencia óptica en el tratamiento de la retinopatía diabética p. 12



EDITOR CLÍNICO EN JEFE REVIEW OF OPHTHALMOLOGY MÉXICO
Dr. Raúl Suárez Sánchez Asesor del Departamento de Córnea y Cirugía Refractiva Instituto de Oftalmología Conde de Valenciana
COMITÉ EDITORIAL REVIEW OF OPHTHALMOLOGY MÉXICO 2025
Dr. Arturo Ramírez Miranda, del Conde de Valenciana.
Profesor adjunto de oftalmología, médico adscrito del Departamento de Córnea y Cirugía Refractiva del Conde de Valenciana
Dr. Charles Van Lansingh, Director médico Help Me See, director de Investigación del Instituto Mexicano de Oftalmología, presidente del Centro Mexicano de Salud Visual Preventiva y Profesor Asociado del Departamento de Salud Pública, de la Universidad de Miami
Dr. Juan Carlos Serna Ojeda, Presidente de la Asociación Mexicana de Bancos de Tejidos Oculares y presidente del Instituto Visión Láser.
Dra. María Ana Martínez-Castellanos, Cirujano de retina pediátrica
Dra. Silvia Moguel Ancheita, Expresidente Sociedad Mexicana de Oftalmología (SMO)
Dr. Jorge E. Valdez-García MD, PhD, Decano de la Escuela de Medicina y Ciencias de la Salud del Tecnológico de Monterrey

Apreciados colegas:
Dr. Raúl Suárez Sánchez
Asesor del Departamento de Córnea y Cirugía Refractiva Instituto de Oftalmología
Conde de Valenciana
Cerramos un año intenso, lleno de eventos que han puesto a prueba nuestro sistema límbico, especialmente nuestra amígdala. Los invito a tomar una pausa: busquen su sillón favorito, una buena taza de café y disfruten la lectura de los artículos que compartimos en este volumen.
El Dr. Arturo Ramírez M. y colaboradores presentan el artículo “Neurotización corneal indirecta como tratamiento de queratopatía neurotrófica”, donde describen una técnica innovadora para reinervar córneas con úlcera trófica resistente al tratamiento convencional, un desafío clínico frecuente que suele derivar en leucomas vascularizados o perforaciones corneales.
En el artículo “Agonistas del receptor GLP-1 y su relación con la retinopatía diabética: hallazgos recientes”, la Dra. Denis Anaya destaca la relevancia del tratamiento sistémico de la diabetes para prevenir el empeoramiento temprano de la retinopatía diabética y resalta la necesidad de que oftalmólogos y endocrinólogos trabajen en conjunto para evitar complicaciones retinianas.
El artículo “La diabetes podría reducir el efecto de la terapia anti-VEGF en la DMAE” concluye que los pacientes con degeneración macular asociada a la edad, que además tienen diagnóstico de diabetes mellitus, pueden presentar una evolución más tórpida frente al tratamiento anti-VEGF, en comparación con quienes no padecen enfermedad metabólica.
El consejo editorial de Review Of Ophthalmology México en Español invita a nuestros lectores a escribir al correo lmalkinstuart@clatinmedia.com y eolguin@clatinmedia.com sus casos clínicos o experiencias científicas que consideren de interés para compartir con nosotros. Por favor indicarnos, lugar de contacto, número telefónico y correo electrónico.
Finalmente, el artículo “Tomografía de coherencia óptica en el tratamiento de la retinopatía diabética”, de los doctores Landon J. Rohowetz y Harry W. Flynn Jr., destaca el papel esencial del OCT no solo en el diagnóstico, sino también en el seguimiento del tratamiento. La alteración de las capas internas de la retina, visible únicamente mediante esta técnica, se reconoce como un marcador del potencial visual y predictor de progresión. Estos hallazgos orientan las decisiones terapéuticas iniciales y facilitan la evaluación de la evolución de la enfermedad a lo largo del tiempo.
Quiero felicitar al Dr. José Antonio Paczka Zapata y a su mesa directiva por el valioso trabajo realizado durante estos dos años, enfrentando con dedicación y liderazgo un periodo lleno de desafíos. Asimismo, doy la bienvenida al Dr. David Lozano Rechy, quien asumirá la presidencia de la Sociedad Mexicana de Oftalmología Colegio Nacional para el periodo 2026–2028, deseándole el mayor de los éxitos en esta nueva gestión.
A todos ustedes, apreciados colegas, les deseo lo mejor en esta próxima Navidad y Año Nuevo. ¡Felicidades!
Con mis mejores deseos.
Edición n°6. Volumen 132

Elizabeth Olguín
Editora en jefe Review of Ophthalmology México eolguin@clatinmedia.com
Con esta edición, Review of Ophthalmology México cierra su ciclo editorial 2025. Durante estos doce meses, compartimos seis ediciones especiales: Glaucoma, Córnea, Catarata, Miopía, Retina y Diabetes, en las que la evidencia científica y la experiencia clínica se unieron para ofrecer una visión integral, precisa y actual del presente y futuro de la oftalmología.
A quienes depositaron su confianza en nuestras páginas, autores comprometidos y verdaderos arquitectos de este diálogo científico, les extendemos nuestro más sincero agradecimiento. Su generosidad al compartir el fruto de su trabajo no solo enriqueció cada edición, sino que reafirmó que el progreso de la ciencia médica se sustenta en el conocimiento compartido.
Nuestro reconocimiento también para la industria, aliada esencial en la innovación, que cada año acerca a los profesionales de la salud visual a lo más recientes avances en tecnología y productos que transforman la práctica clínica. Gracias por confiar en nuestros medios para compartir sus productos.
Cabe destacar que, más allá de su función informativa, las seis portadas que dieron identidad a cada edición se convirtieron en verdaderos emblemas visuales. Cada una fue concebida con una intención artística cuidadosamente planeada, logrando capturar la esencia única de cada especial y reflejando, al mismo tiempo, un año en el que la inteligencia artificial se consolidó como una herramienta clave en la oftalmología.
Cerramos el 2025 con una comunidad que supera los 42,800 profesionales, fortalociendo a Oftalmólogo al Día como el medio líder en comunicación. Nuestras plataformas digitales continúan siendo un espacio de actualización constante, donde los especialistas encuentran noticias, innovaciones tecnológicas y casos clínicos de alto nivel.
A este crecimiento se suma el desempeño de nuestra Web App de Review of Ophthalmology, que en sus ediciones México y en Español ha alcanzado, de manera combinada, 67,140 sesiones y 28,473 usuarios únicos a lo largo del año.
Más allá de las cifras, estos resultados confirman que Oftalmólogo al Día se ha establecido como un referente en la difusión del conocimiento oftalmológico. Con este respaldo, reafirmamos nuestro compromiso de seguir siendo el punto de encuentro esencial entre la ciencia, la práctica clínica y la comunidad médica.
Les deseamos unas felices fiestas decembrinas y un 2026 lleno de salud, prosperidad y avances significativos en su práctica profesional. Que cada nuevo desafío se transforme en una oportunidad de crecimiento, y que el conocimiento siga siendo el motor que impulse su vocación y su compromiso con la excelencia en la oftalmología.

Editora en Jefe: Laura Malkin-Stuart
Editor Clínico en Jefe (Español): Dr. Eduardo Viteri
Editor Clínico en Jefe (México): Dr. Raúl Suárez
Editor en Español: Juan Pablo Chajín
Editora en Jefe México: Elizabeth Olguín
Editoras México: Anaís Barrera Cecimar Kerch
Editor Europa: Nicolas Plotnicoff
Diseño Gráfico: Nathalia López
Diseñador Gráfico de Medios Digitales: Cristian Puentes
Producción y Preprensa: Alejandro Bernal
Profesional Logística: Ximena Ortega Bernal
Ilustración basada en el artículo: Tomografía de coherencia óptica en el tratamiento de la retinopatía diabética
Producida / Editada / Diseñada / Distribuida por: 3 Touch Media S.A.S.
Director General (CEO): Sergio Plotnicoff Presidente Honorario: Juan Carlos Plotnicoff
Directora de Comunicaciones: Laura Malkin-Stuart Directora Administrativa y Financiera: Luisa Fernanda Vargas A. Dirección de Distribución: José Antonio Ferrarotto
Creative Latin Media LLC 2901 Clint Moore Rd, P.M.B 117 Boca Raton, FL 33496
USA
Tel: +57 310 304-8820
e-mail: suscripciones@clatinmedia.com
Las traducciones y el contenido editorial de Review of Ophthalmology En Español, no pueden ser reproducidos sin el permiso de Creative Latin Media™.
USA, Europa y Brasil, Héctor Serna: Director Comercial Cel: +1 561 4437192, ventas1@clatinmedia.com
México Carlos Cerezo: Cel: +52 5513523306 ccerezo@clatinmedia.com
Latinoamérica Kelly Triana: Cel: +57 (320) 945-4400, ktriana@clatinmedia.com
Proyectos Especiales Ángela Peralta: pespeciales@clatinmedia.com, Cel: +57 (320) 945-4382
USA: 2901 Clint Moore Rd, P.M.B 117 Boca Raton, FL 33496, Tel: +1 (561) 716-2711
Colombia: Carrera 7 No. 106 - 73 Of. 301
Bogotá, Colombia, Tel: +57 (310) 304-8820
México: Río Mississippi 49, piso 14, int. 1402. Colonia Cuauhtémoc, Alcaldía Cuauhtémoc, Ciudad de México, CP. 06500, Tel: (55) 2803-8170
Review of Ophthalmology (ISSN 1088-9507) es una revista publicada por Creative Latin Media, LLC bajo licencia de Jobson Publishing LLC. Su distribución es gratuita a todos los profesionales de la Salud Visual que cumplan con los requisitos requeridos para recibir la revista en América Latina. Tarifas de suscripción anual, seis ediciones. Colombia US$60, México US$60, Latinoamérica (paises de habla hispana) US$120, Brasil US$180, USA y Canada US$220, Europa y Asia US$260. Para suscripciones comuniquese a suscripciones@clatinmedia.com Otros productos de Creative Latin Media son: 20/20 En Español y 20/20 México

Agonistas del receptor GLP-1 y su relación con la retinopatía diabética: hallazgos recientes 06
La diabetes podría reducir el efecto de la terapia anti-VEGF en la DMAE 10
Tomografía de coherencia óptica en el tratamiento de la retinopatía diabética 12
Inteligencia artificial para la detección de la retinopatía diabética 18
Neurotización Corneal Indirecta como tratamiento de queratopatía neurotrófica 22
Cirugía refractiva y superficie ocular: manejo del ojo seco post-LASIK, SMILE y PRK 24
Controversias en los Tratamientos Láser Modernos para la Retina y Vítreo 26
PRODUCTOS
El láser Nd:YAG MR Q Supine: innovación en tratamientos oftálmicos en posición supina 28
Difluprednato: una nueva alternativa terapéutica en México para el control de la inflamación ocular 30
Pictor Plus, tu aliada móvi para una atención visual de primer nivel 31



Dra. Denis Anaya
La diabetes mellitus (DM) constituye un grupo heterogéneo de trastornos caracterizados por una alteración en el metabolismo de los carbohidratos, que se manifiesta por una utilización ineficiente de la glucosa como fuente de energía y un incremento en su producción endógena, debido a una gluconeogénesis y glucogenólisis inapropiadamente aumentadas. Estas alteraciones conllevan a un estado de hiperglucemia crónica, eje fisiopatológico de la enfermedad y principal determinante de sus complicaciones microvasculares y macrovasculares (1).
En la actualidad, el manejo terapéutico de la diabetes mellitus se basa en un enfoque integral que combina intervenciones no farmacológicas y farmacológicas. Entre las primeras destacan las modificaciones del estilo de vida, como la reducción del peso corporal y la práctica regular de actividad física. En cuanto al tratamiento farmacológico, se dispone de diversas clases de agentes hipoglucemiantes, entre ellos: metformina, inhibidores del cotransportador sodio-glucosa tipo 2 (SGLT2, sodium–glucose cotransporter 2 inhibitors), agonistas del receptor del péptido similar al glucagón tipo 1 (GLP-1, glucagon-like peptide-1 receptor agonists), agonistas del péptido insulinotrópico dependiente de glucosa (GIP, glucose-dependent insulinotropic polypeptide), inhibidores de la dipeptidil peptidasa tipo 4 (DPP-4, dipeptidyl peptidase-4 inhibitors), pioglitazona, sulfonilureas, así como insulinas y análogos de insulina (2).
La selección del tratamiento farmacológico debe individualizarse, considerando las características clínicas de cada paciente, sus comorbilidades, el perfil de seguridad y los posibles efectos adversos de los fármacos, así como la carga terapéutica, los objetivos metabólicos y las preferencias del paciente (2).
Los agonistas del receptor del péptido similar al glucagón-1 (GLP-1 AR) como la liraglutida, semaglutida, dulaglutida, entre otros; han revolucionado el manejo de la diabetes tipo 2 y la obesidad, pues además de mejoría sostenida de HbA1c y peso corporal, han mostrado beneficios cardiovasculares y antiinflamatorios (3).
La relación de los GLP-1 AR con la retinopatía diabética (RD) ha sido controversial desde la publicación del estudio SUSTAIN-6 en el 2016, que reportó mayor frecuencia de complicaciones relacionadas con retinopatía diabética (hemorragia vítrea, ceguera, o necesidad de tratamiento con láser o inyecciones de antiangiogénico) (HR 1,76; IC95% 1,11–2,78) en los pacientes tratados con semaglutida versus placebo. Este aumento en el número de complicaciones se dio principalmente en pacientes con RD previa, HbA1c basal elevada, uso previo de insulina y descensos rápidos y severos de HbA1c tras iniciar la semaglutida (3). Sin embargo, análisis posteriores y la evidencia acumulada sugieren que dicho empeoramiento es a corto plazo, transitorio y está ligado a la magnitud y velocidad de la reducción de HbA1c, consistente con el fenómeno clásico de “empeoramiento temprano” y no a un efecto tóxico directo (4). Este fenómeno, generado tras mejoras rápidas del control glucémico, está descrito desde la era de la insulina intensiva. Y apunta a que la causa del empeoramiento de la retinopatía no depende del tipo específico de fármaco, sino del cambio abrupto en la glucemia y su efecto en el flujo retiniano y estrés vascular transitorio. Sin embargo, en 2023, Simó y colaboradores demostraron que el descenso de HbA1c no se asocia a progresión de la retinopatía en casos de retinopatía no proliferativa leve o moderada, sino en casos de retinopatía diabética no proliferativa severa o ya proliferativa. Es decir con mayor daño endotelial previo (5).
Por otro lado, aunque los Ensayos Clínicos de Seguridad Cardiovascular (CardioVascular Outcome Trials o CVOTs) con GLP-1 RA no fueron diseñados específicamente para evaluar desenlaces de retinopatía diabética, sus hallazgos no son consistentes con el SUSTAIN-6. El estudio LEADER, mostró un aumento no significativo de progresión de RD en pacientes tratados con liraglutida (6) y; REWIND reportó más complicaciones de RD en pacientes tratados con dilaglutida que ya tenían RD al previamente, pero sin incremento global claro frente a placebo (7)
Más allá del corto plazo, la suma de beneficios cardiometabólicos de los GLP-1 RA: mejoría sostenida de HbA1c y peso, mayor estabilidad glucémica, reducción de inflamación sistémica y protección renal, podría traducirse en menor daño microvascular a lo largo del tiempo. Incluso estudios preclínicos y revisiones proponen efectos neuroprotectores y antiinflamatorios retinianos mediados por estos fármacos. Recientemente, Talebi y colaboradores en un estudio con seguimiento de hasta 10 años, encontraron que comparado con los no usuarios, los usuarios de GLP-1 RA mostraron menor riesgo de desarrollar retinopatía diabética (HR 0,31 - IC 95%: 0,26-0,37) y menor riesgo también de edema macular diabético (HR 0,40 - IC 95%: 0,27-0,59) (5).
En la práctica, el oftalmólogo debe tener claras las implicaciones y consideraciones para disminuir el riesgo de progresión de retinopatía diabética en estos pacientes. En primera instancia identificar pacientes de alto riesgo de “empeoramiento temprano”: retinopatía diabética preexistente (no proliferativa moderada o severa o proliferativa previa), HbA1c basal elevada, uso de insulina y larga duración de la DM. En segundo lugar, trabajar en conjunto con endocrinología para tratar de evitar reducciones >1–2% de HbA1c en pocas semanas, sobre todo en aquellos pacientes con retinopatía avanzada de base. Instaurar un programa de seguimiento estandarizado para los pacientes usuarios de GLP-1 RA, que incluya una valoración previa al inicio del tratamiento, para definir el grado de retinopatía inicial. Posteriormente revaloraciones cada 3 o 6 meses y si se da el empeoramiento tratar ya sea con láser o antiangiogénico según sea necesario. No suspender el GLP-1 RA en la medida de lo posible, la mayoría de casos se estabiliza tras la fase de ajuste metabólico y de hecho mantener el fármaco dentro de un plan integral
probablemente beneficia la microvasculatura sistémica. Y por último, asegurarse de que el control de otros factores (presión arterial, lípidos, nefropatía) se maneje de manera óptima simultánea y enfatizar en la educación del paciente: explicar el fenómeno de empeoramiento pasajero, reforzar adherencia, automonitoreo y asistencia a controles (5).
En conclusión, la hipótesis inicial de que los GLP-1 RA “empeoran la retinopatía diabética” se origina en la teoría de un fenómeno ya conocido con terapias hipoglucemiantes eficaces por disminución rápida y marcada de HbA1c. Sin embargo, la evidencia integradora de ensayos y metaanálisis indica que, a largo plazo, los GLP-1 RA no incrementan globalmente la progresión de RD y, dentro de un abordaje cardiometabólico integral y un titulado prudente, pueden contribuir a mejores desenlaces microvasculares. Para el oftalmólogo, la clave es anticipar el “empeoramiento temprano” con seguimiento estrecho inicial, el trabajo coordinado y multidisciplinario para evitar caídas abruptas de HbA1c, y sostener la terapia cuando el balance beneficio-riesgo lo permita.
Declaro que no tengo conflicto de interés relacionado con esta publicación.
La Dra. Denis Anaya es médica egresada de la Universidad El Bosque y especialista en Oftalmología por la Fundación Universitaria de Ciencias de la Salud - Hospital de San José (FUCS-HSJ), con subespecialidad en Cirugía de Retina y Vítreo de la Universidad Javeriana de Cali. Se desempeña como oftalmóloga socia y adscrita en la Clínica de Oftalmología de Cali, además de ser docente de pregrado, posgrado y fellow en la Universidad Javeriana de Cali. Es miembro de la junta directiva de la Asociación Colombiana de Retina y Vítreo (ACOREV) y miembro activo de sociedades como SOCOFTAL, PAAO y Euretina.
Para más información sobre la clínica y el XVII Congreso Internacional de Oftalmología, puedes escribir a xviicongresointernacionaldeoftalmologia@clinicaofta.com o visitar su página web www.clinicaofta.com.
Sigue sus redes sociales para conocer más sobre sus novedades y actividades científicas:
• Instagram: @clinicaoftalmologiadecali o https://www.instagram.com/clinicaoftacongresointer/
• Facebook: Clínica de Oftalmología de Cali
• LinkedIn: Clínica de Oftalmología de Cali
Descubre el cubrimiento completo del XVII Congreso Internacional de Oftalmología en nuestro newsletter, en oftalmologoaldia.com, y en las redes sociales de @oftalmologoaldia.
1. American Diabetes Association Professional Practice Committee. 2. Diagnosis and Classification of Diabetes: Standards of Care in Diabetes-2025. Diabetes Care. 2025 Jan 1;48(1 Suppl 1):S27-S49. doi: 10.2337/ dc25-S002. PMID: 39651986; PMCID: PMC11635041.
2. American Diabetes Association Professional Practice Committee. 9. Pharmacologic Approaches to Glycemic Treatment: Standards of Care in Diabetes-2025. Diabetes Care. 2025 Jan 1;48(1 Suppl 1):S181-S206. doi: 10.2337/dc25-S009. PMID: 39651989; PMCID: PMC11635045.
3. Marso SP, Bain SC, Consoli A, Eliaschewitz FG, Jódar E, Leiter LA, Lingvay I, Rosenstock J, Seufert J, Warren ML, Woo V, Hansen O, Holst AG, Pettersson J, Vilsbøll T; SUSTAIN-6 Investigators. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med. 2016 Nov 10;375(19):1834-1844. doi: 10.1056/NEJMoa1607141. Epub 2016 Sep 15. PMID: 27633186.
4. Vilsbøll T, Bain SC, Leiter LA, Lingvay I, Matthews D, Simó R, Helmark IC, Wijayasinghe N, Larsen M. Semaglutide, reduction in glycated haemoglobin and the risk of diabetic retinopathy. Diabetes Obes Metab. 2018 Apr;20(4):889-897. doi: 10.1111/dom.13172. Epub 2018 Jan 8. PMID: 29178519; PMCID: PMC5888154..
5. Simó R, Franch-Nadal J, Vlacho B, Real J, Amado E, Flores J, Mata-Cases M, Ortega E, Rigla M, Vallés JA, Hernández C, Mauricio D. Rapid Reduction of HbA1c and Early Worsening of Diabetic Retinopathy: A Real-world Population-Based Study in Subjects With Type 2 Diabetes. Diabetes Care. 2023 Sep 1;46(9):1633-1639. doi: 10.2337/dc22-2521. PMID: 37428631.
6. Marso SP, Daniels GH, Brown-Frandsen K, Kristensen P, Mann JF, Nauck MA, Nissen SE, Pocock S, Poulter NR, Ravn LS, Steinberg WM, Stockner M, Zinman B, Bergenstal RM, Buse JB; LEADER Steering Committee; LEADER Trial Investigators. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med. 2016 Jul 28;375(4):311-22. doi: 10.1056/NEJMoa1603827. Epub 2016 Jun 13. PMID: 27295427; PMCID: PMC4985288
7. Gerstein HC, Colhoun HM, Dagenais GR, Diaz R, Lakshmanan M, Pais P, Probstfield J, Riddle MC, Rydén L, Xavier D, Atisso CM, Avezum A, Basile J, Chung N, Conget I, Cushman WC, Franek E, Hancu N, Hanefeld M, Holt S, Jansky P, Keltai M, Lanas F, Leiter LA, Lopez-Jaramillo P, Cardona-Munoz EG, Pirags V, Pogosova N, Raubenheimer PJ, Shaw J, Sheu WH, Temelkova-Kurktschiev T; REWIND Trial Investigators. Design and baseline characteristics of participants in the Researching cardiovascular Events with a Weekly INcretin in Diabetes (REWIND) trial on the cardiovascular effects of dulaglutide. Diabetes Obes Metab. 2018 Jan;20(1):42-49. doi: 10.1111/dom.13028. Epub 2017 Jul 14. PMID: 28573765.

Este artículo fue publicado y traducido bajo los términos de nuestra licencia con Jobson Healthcare Information. Queda estrictamente prohibida su reproducción total o parcial.
Varios factores ambientales y genéticos contribuyen a la patogénesis de la degeneración macular relacionada con la edad (DMAE). Sin embargo, dentro de la comunidad científica persiste el debate sobre el papel de la diabetes mellitus en la forma neovascular avanzada de la enfermedad (DMAE-n), cuestionándose si esta condición contribuye a la progresión o, por el contrario, ejerce un efecto protector. Mediante el uso de OCT-A para observar los cambios morfológicos en la neovascularización macular exudativa tipo 1 (MNV) tras un año de tratamiento con anti-VEGF, los investigadores encontraron que los pacientes con retinopatía diabética leve mostraron una respuesta divergente en el área de la lesión MNV tipo 1.
Según sus hallazgos, publicados recientemente en la revista Investigative Ophthalmology & Visual Science,1 aunque se observó una reducción significativa del tamaño de la lesión entre la visita inicial y la fase posterior a la carga, no se observó una reducción adicional notable del área de la lesión en la visita de seguimiento a los 12 meses. Por el contrario, los pacientes con DMAE neovascular sin antecedentes de DM presentaron una reducción continua del tamaño de la MNV. Los investigadores afirman que esto pone de relieve la importancia de la RD como posible modificador de los resultados del tratamiento en el manejo de la DMAE neovascular, ya que la DM se considera un factor de riesgo durante el tratamiento antiangiogénico.
El estudio retrospectivo incluyó 45 ojos con DMAE exudativa con MNV tipo 1, todos ellos inscritos en el Servicio de Retina Médica de la Universidad de Bari Aldo Moro en Italia. Los pacientes se dividieron en el grupo diabético, que incluía 21 ojos de 21 pacientes con RD leve, y el grupo no diabético, que consistía en 24 ojos de 24 pacientes sin antecedentes de DM. Las medidas de resultado incluyeron los cambios en la mejor agudeza visual corregida, el grosor macular central, el área de la lesión MNV y el área de flujo MNV. Según el estudio, todos estos parámetros mostraron una mejora significativa después de la fase de carga.
“El hallazgo más relevante se relacionó con el comportamiento de la lesión neovascular un año después del inicio del tratamiento”, señalaron los autores del estudio. “En concreto, el grupo con diabetes no mostró una reducción significativa del área de neovascularización macular (MNV) tras 12 meses, mientras que el grupo no diabético presentó una disminución continua en su tamaño. Este último resultado parece especialmente importante, dado que el tamaño de la MNV, evaluado mediante OCT-A, constituye un valioso biomarcador para determinar la respuesta o la falta de respuesta al tratamiento”.
Los investigadores especularon sobre los posibles mecanismos que podrían explicar estos resultados, entre ellos la posibilidad de que la presencia de retinopatía diabética (RD) modifique las vías angiogénicas implicadas en la neovascularización macular (MNV). “La RD se asocia con una desregulación de la señalización del VEGF y con un aumento en los niveles de citocinas inflamatorias, lo que podría generar una respuesta distinta al tratamiento anti-VEGF”, señalaron.
“Estas alteraciones podrían derivar en una menor eficacia terapéutica, ocasionando una reducción menos pronunciada de la neovascularización con el tiempo. Otra hipótesis es que los cambios microvasculares característicos de la RD, como la pérdida capilar y el engrosamiento de la membrana basal, crean un entorno menos favorable para la resolución de los complejos neovasculares. La estructura y función vasculares comprometidas en los ojos diabéticos podrían limitar la capacidad del tratamiento anti-VEGF para inducir una regresión significativa de la MNV, lo que se traduce en una disminución menos marcada en comparación con los ojos no diabéticos.”
Los autores señalaron que el tamaño de la muestra era relativamente pequeño, lo que podría haber limitado la generalización de sus resultados. La falta de un grupo de control también significa que las diferencias observadas durante el periodo de seguimiento podrían haberse producido incluso sin la terapia antiangiogénica. “Además, el uso de OCT-A de dominio espectral, que utiliza luz de longitud de onda más corta en comparación con la OCTA de fuente barrida, puede dar lugar a una reducción de la penetración de la señal a través del EPR, lo que podría afectar a la precisión de nuestros datos de imagen”, añadieron.
A pesar de estos factores, los autores afirman que confían en la solidez de su estudio y señalan que se trata de la primera investigación exhaustiva sobre el impacto de la RD en los cambios morfológicos y funcionales longitudinales en la MNV tipo 1 asociada a la DMAE en pacientes sometidos a terapia anti-VEGF durante un año. La respuesta divergente que descubrieron en este estudio destaca el papel que desempeña la RD en los resultados del tratamiento, y concluyeron diciendo: “Son necesarios estudios futuros más amplios que utilicen OCT-A de fuente barrida y duraciones de seguimiento más largas para validar nuestros hallazgos preliminares”.
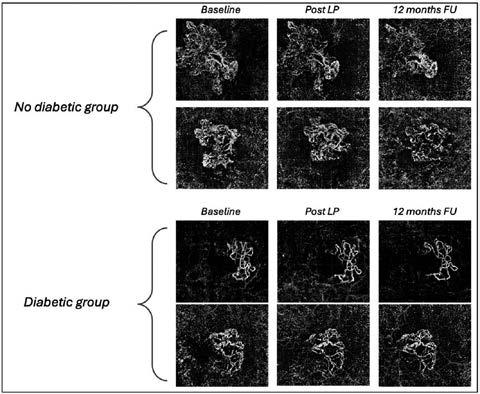
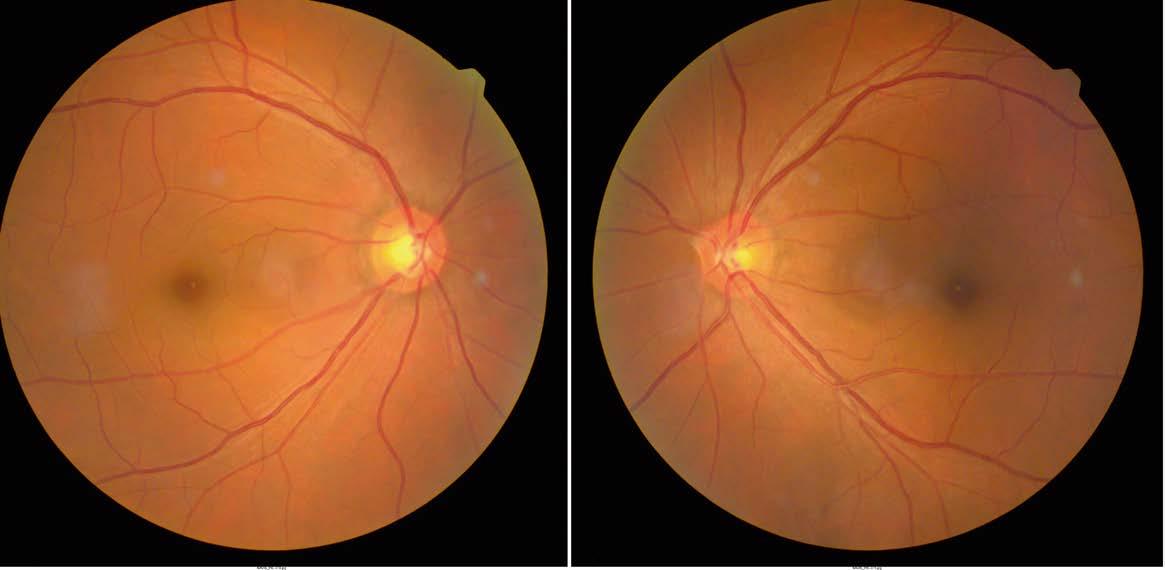
Los investigadores informaron que, durante la terapia anti-VEGF, el tamaño de la lesión de neovascularización macular continuó disminuyendo en el grupo no diabético a lo largo de 12 meses, pero presentó una reducción menor en el grupo diabético, lo que sugiere que la diabetes podría ser un factor de riesgo a considerar durante el tratamiento antiangiogénico
Foto: Boscia G, et al. Invest Ophthalmol Vis Sci. 2 de agosto de 2024.
1. Boscia G, Bacherini D, Vujosevic S, Grassi M.O., Borrelli E., Giancipoli E., Landini L., Pignataro M., Alessio G., Boscia F., Viggiano P. Impacto a largo plazo de la retinopatía diabética en la respuesta al tratamiento anti-VEGF en la DMAE neovascular. Investigative Ophthalmology & Visual Science. 2 de agosto de 2024.
2. Review of Ophthalmology. (2024, agosto). Diabetes may lessen the effect of anti-VEGF therapy in AMD. Review of Ophthalmology. https:// www.reviewofophthalmology.com/article/diabetes-may-lessen-theeffect-of-antivegf-therapy-in-amd
Autores: Dr Landon J. Rohowetz y Dr. Harry W. Flynn Jr.

Dr Landon J. Rohowetz

Dr. Harry W. Flynn Jr.
Este artículo fue publicado y traducido bajo los términos de nuestra licencia con Jobson Healthcare Information. Queda estrictamente prohibida su reproducción total o parcial.
El Dr. Rohowetz es Fellow de cirugía vitreorretiniana en el Bascom Palmer Eye Institute del Miller School of Medicine (University of Miami).
El Dr. Flynn es el titular de la cátedra distinguida J. Donald M. Gass de Oftalmología en la University of Miami Miller School of Medicine y profesor de oftalmología en el Bascom Palmer Eye Institute.
Recomendaciones clave para optimizar el uso de esta tecnología en la evaluación y seguimiento de pacientes con retinopatía diabética (RD).
• La OCT proporciona una evaluación precisa y objetiva del edema macular diabético, lo que orienta las decisiones terapéuticas y mejora la participación del paciente.
• La OCT permite a los médicos evaluar la respuesta al tratamiento en pacientes con retinopatía diabética, tanto en el ámbito clínico como en el de la investigación.
• Los biomarcadores de la OCT, como el DRIL y la alteración de la zona elipsoidal, respaldan la terapia individualizada y ayudan a predecir la respuesta al tratamiento en la retinopatía diabética.
• Las tecnologías emergentes, como la OCT de fuente barrida y la angiografía OCT, amplían las capacidades de diagnóstico al mejorar el campo de visión e identificar de forma no invasiva las anomalías microvasculares.
La retinopatía diabética continúa siendo una de las principales causas de discapacidad visual y ceguera en adultos en edad laboral a nivel mundial. 1 Con el aumento de la prevalencia de la diabetes, los especialistas en retina enfrentan el desafío no solo de tratar las complicaciones que amenazan la visión, sino también de detectar y controlar la enfermedad de manera más temprana y eficaz. La tomografía de coherencia óptica (OCT), gracias a su capacidad para ofrecer imágenes transversales de alta resolución de la retina, se ha consolidado como una herramienta esencial en la evaluación y el manejo de la retinopatía diabética. Desde la detección de cambios subclínicos hasta la personalización de los regímenes terapéuticos, la OCT desempeña un papel clave en la optimización de los resultados clínicos. A continuación, revisaremos las capacidades de la OCT en este ámbito y analizaremos las ventajas que pueden aportar las nuevas tecnologías.
Los sistemas tradicionales de estadificación de la retinopatía diabética, como la clasificación del Estudio de Tratamiento Temprano de la Retinopatía Diabética, se basan en gran medida en la fotografía del fondo de ojo y el examen clínico. Si bien estas herramientas siguen siendo fundamentales, a menudo pasan por alto los cambios estructurales tempranos, en particular los que afectan a la mácula. La tomografía de coherencia óptica permite detectar alteraciones sutiles, como el engrosamiento de la retina, los quistes intrarretinianos tempranos o los signos de disfunción neurorretiniana, antes de que sean visibles clínicamente. De hecho, la OCT ha sido una herramienta importante en los ensayos de la Red de Investigación Clínica de la Retinopatía Diabética.2,3
Los cambios patológicos más específicos, como la desorganización de las capas internas de la retina (DRIL; Figura 1), solo pueden apreciarse mediante OCT y se han identificado como marcadores del potencial visual y predictores de la progresión de la RD.4 Del mismo modo, la alteración de la retina externa (Figura 2) y el daño temprano de los fotorreceptores pueden indicar una enfermedad más avanzada con un pronóstico visual desfavorable.5
Al incorporar los hallazgos de la OCT y estas tecnologías en evolución al flujo de trabajo clínico, los especialistas en retina pueden identificar a los pacientes con mayor riesgo de progresión, lo que permite una intervención más temprana e intervalos de seguimiento más personalizados. Esto resulta especialmente útil en pacientes con diabetes que aún no cumplen los criterios para recibir tratamiento, pero que requieren una vigilancia más estrecha.
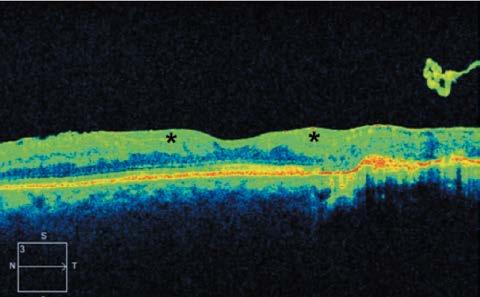
Figura 1. Tomografía de coherencia óptica de un varón de 41 años con antecedentes de retinopatía diabética proliferativa que muestra una desorganización de las capas internas de la retina (asteriscos).
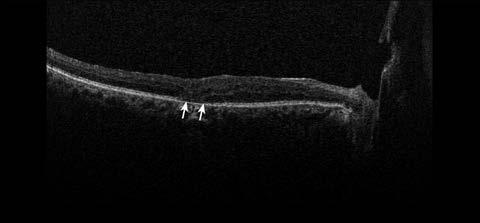
Figura 2. Tomografía de coherencia óptica de un paciente de 59 años con antecedentes de retinopatía diabética proliferativa que muestra una alteración de la retina externa (flechas).
Una de las contribuciones más impactantes de la OCT al cuidado ocular de los pacientes diabéticos ha sido el tratamiento del edema macular diabético, la principal causa de pérdida de visión en la RD.6 Mientras que la oftalmoscopia puede detectar un edema macular clínicamente significativo, la OCT proporciona una evaluación mucho más sensible y cuantitativa del engrosamiento de la retina y de la presencia de líquido intrarretiniano o subretiniano.7
La tomografía de coherencia óptica permite medir con precisión el grosor del subcampo central, que a menudo se utiliza como criterio de valoración sustitutivo en ensayos clínicos y protocolos de tratamiento. También permite caracterizar los patrones de líquido e identificar características estructurales como focos hiperreflectantes o exudados duros.
Estas características no solo orientan las decisiones terapéuticas iniciales, sino que también ayudan a los especialistas en retina a evaluar la actividad de la enfermedad a lo largo del
tiempo. Por ejemplo, la persistencia de líquido intrarretiniano a pesar de múltiples inyecciones anti-VEGF puede motivar el cambio a un agente alternativo, mientras que la resolución del líquido puede justificar la prolongación de los intervalos de tratamiento.8
La interpretación de la OCT asistida por inteligencia artificial también está surgiendo como una herramienta para la detección más temprana y estandarizada del EMD. Los algoritmos de IA entrenados con grandes conjuntos de datos de imágenes pueden identificar patrones de actividad de la enfermedad, señalar cambios anatómicos sutiles y, potencialmente, apoyar un manejo más consistente y proactivo.9 Paralelamente, se están desarrollando plataformas de OCT para el hogar que permiten la monitorización remota de pacientes con enfermedades maculares como el EMD. Estos dispositivos pueden permitir evaluaciones más frecuentes, la detección temprana de la recurrencia del líquido y ajustes oportunos del tratamiento, lo que resulta especialmente beneficioso para los pacientes que tienen dificultades para acudir con frecuencia a la clínica.10
Además, las imágenes obtenidas mediante OCT favorecen la toma de decisiones compartida con los pacientes, al permitirles visualizar el efecto de su tratamiento y comprender mejor la importancia de mantener la adherencia terapéutica. La posibilidad de monitorear de forma objetiva las mejoras en la arquitectura retiniana contribuye a aumentar su compromiso y satisfacción con el proceso de atención (Figura 3).
al tratamiento
El manejo de la retinopatía diabética está evolucionando del enfoque “único para todos” hacia una atención más personalizada, con la tomografía de coherencia óptica (OCT) como herramienta central en esta transformación. La respuesta a la terapia intravítrea es altamente variable, y los hallazgos estructurales en la OCT no siempre se correlacionan de manera directa con los cambios en la agudeza visual. No obstante, ciertos biomarcadores —como la desorganización de las capas internas de la retina (DRIL), la alteración de la zona elipsoidal o la persistencia de espacios cistoides— ofrecen información pronóstica valiosa para guiar el manejo a largo plazo 4, 11
Por ejemplo, en pacientes sometidos a terapia anti-VEGF, la OCT es muy valiosa para determinar los intervalos de retratamiento en regímenes de tratamiento y extensión o PRN. Las pruebas sugieren que los pacientes con líquido persistente o recalcitrante responden mejor a intervalos más cortos, mientras que los pacientes estables a menudo pueden tolerar la extensión.12 Asimismo, los corticosteroides intravítreos, como los implantes de dexametasona o fluocinolona y el acetónido de triamcinolona, representan alternativas terapéuticas para
el edema macular diabético crónico, y la monitorización con OCT permite evaluar su eficacia y determinar los intervalos de aplicación óptimos. 13
En contextos quirúrgicos, la OCT también puede ayudar en la planificación al identificar elementos de tracción o adherencias vitreomaculares que pueden requerir una vitrectomía. Después de la operación, las exploraciones OCT en serie pueden documentar la resolución del edema y la reimplantación de la retina, lo que permite una evaluación más objetiva de los resultados quirúrgicos.
Recientemente, la angiografía por OCT se ha consolidado como una herramienta poderosa para evaluar la retinopatía diabética. Esta técnica de imagen no invasiva detecta el movimiento del flujo sanguíneo, ofreciendo una visualización detallada de la microvasculatura retiniana y coroidea sin requerir el uso de colorantes con fluoresceína. 14
La angiografía por tomografía de coherencia óptica (OCTA) permite identificar áreas de no perfusión capilar, microaneurismas y agrandamiento de la zona avascular foveal, signos característicos de isquemia asociados a la gravedad de la retinopatía diabética. A diferencia de la angiografía con fluoresceína, la OCTA puede repetirse con frecuencia y sin invasión, lo que la hace ideal para el seguimiento longitudinal.
En ojos con retinopatía diabética no proliferativa, la OCTA permite detectar cambios microvasculares progresivos incluso antes de que sean clínicamente visibles, facilitando una vigilancia más estrecha o una intervención temprana. 16 En la retinopatía diabética proliferativa, la OCTA complementa la oftalmoscopia y las imágenes de campo amplio al delinear con precisión las redes neovasculares y evaluar su respuesta a tratamientos como la fotocoagulación panretiniana o la terapia anti-VEGF (Figura 4). 17
Aunque la OCTA tradicional presenta limitaciones, como un campo de visión más reducido frente a la angiografía de fluoresceína de campo ultra amplio y la susceptibilidad a artefactos por movimiento, constituye un avance prometedor hacia una visualización vascular retiniana más completa y no invasiva.
Aunque muchos pacientes con retinopatía diabética son tratados médicamente, la intervención quirúrgica sigue siendo una opción para complicaciones como la hemorragia vítrea que no se resuelve, el desprendimiento de retina por tracción y las membranas epirretinianas densas. La tomografía de co-
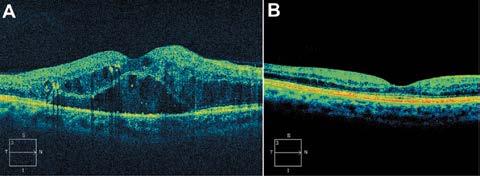
Figura 3. (A) Tomografía de coherencia óptica de un varón de 47 años con antecedentes de retinopatía diabética no proliferativa que muestra la presencia de líquido subretiniano, líquido intrarretiniano y depósitos intrarretinianos. (B) Tomografía de coherencia óptica seis años después del inicio del tratamiento intravítreo regular con anti-VEGF que muestra la resolución del líquido intrarretiniano y subretiniano.
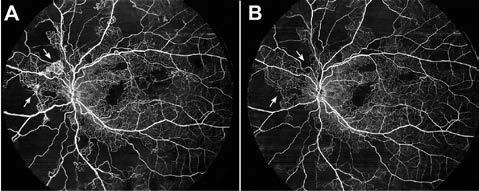
Figura 4. (A) Angiografía por tomografía de coherencia óptica de una mujer de 40 años con antecedentes de retinopatía diabética proliferativa que muestra la falta de perfusión capilar y neovascularización peripapilar en otras zonas (flechas). (B) Angiografía por tomografía de coherencia óptica un año después del tratamiento con bevacizumab intravítreo que muestra la regresión de la neovascularización (flechas).
herencia óptica proporciona información preoperatoria esencial en estos casos, especialmente para identificar signos de progresión o afectación foveal.18
Después de la cirugía, la OCT permite monitorear la arquitectura retiniana, detectar edema residual o recurrente y evaluar la integridad de la zona elipsoidal y las capas de fotorreceptores. Esta información resulta clave para orientar el pronóstico visual y planificar tratamientos complementarios cuando sea necesario.
A pesar de sus numerosas ventajas, la OCT no está exenta de limitaciones. Las opacidades de los medios, los movimientos del paciente o los errores de segmentación pueden dar lugar a artefactos en las imágenes, lo que puede conducir a interpretaciones erróneas. Además, la OCT tradicional suele proporcionar solo una visión limitada de la retina periférica, donde pueden producirse cambios proliferativos e isquemia fuera de la mácula.19 Sin embargo, se están desarrollando nuevas tecnologías de campo amplio para mejorar la calidad de la imagen y ampliar el campo de visión.
Es fundamental recordar que la OCT complementa, pero no sustituye, el examen clínico ni las pruebas funcionales. En ciertos casos, las variaciones en la agudeza visual pueden preceder a los cambios estructurales observados en la OCT, lo que resalta la importancia de una evaluación integral.
El costo, la disponibilidad y el reembolso también son factores clave, especialmente en clínicas que atienden poblaciones vulnerables o trabajan en contextos con recursos limitados.
Dado que la OCT y la OCTA se incluyen en algunos códigos de evaluación o servicios de imagen, no siempre se reembolsan por separado, lo que puede influir en los patrones de uso en la práctica clínica.
La tomografía de coherencia óptica (OCT) ha revolucionado el diagnóstico, seguimiento y tratamiento de la retinopatía diabética. Su capacidad para detectar cambios estructurales sutiles, cuantificar la actividad de la enfermedad y guiar terapias personalizadas ha elevado la calidad de la atención y mejorado los resultados visuales de millones de pacientes. Con innovaciones como la OCT de fuente barrida, la interpretación asistida por inteligencia artificial y los sistemas de monitoreo domiciliario, el futuro del manejo de la enfermedad diabética ocular será cada vez más preciso, individualizado y preventivo. Integrar la OCT dentro de una estrategia de manejo integral permite a los especialistas en retina anticiparse a la progresión de la enfermedad y proteger la visión de una población en riesgo creciente.
1. Yau JW, Rogers SL, Kawasaki R, et al. Prevalencia global y principales factores de riesgo de la retinopatía diabética. Diabetes Care. 2012;35:3:556-564
2. Wells JA, Glassman AR, Ayala AR, et al. Aflibercept, bevacizumab o ranibizumab para el edema macular diabético: resultados de dos años de un ensayo clínico aleatorizado de eficacia comparativa. Ophthalmology. 2016;123:6:1351-1359
3. Baker CW, Glassman AR, Beaulieu WT, et al. Efecto del tratamiento inicial con aflibercept frente a la fotocoagulación con láser frente a la observación sobre la pérdida de visión en pacientes con edema macular diabético que afecta al centro de la mácula y buena agudeza visual: ensayo clínico aleatorizado. JAMA. 2019;321:19:1880-1894
4. Sun JK, Lin MM, Lammer J, et al. Desorganización de las capas internas de la retina como predictor de la agudeza visual en ojos con edema macular diabético que afecta al centro. JAMA Ophthalmol. 2014;132:11:1309-1316
5. Otani T, Kishi S, Maruyama Y. Patrones de edema macular diabético con tomografía de coherencia óptica. Am J Ophthalmol. 1999;127:6:688-693
6. Red de Investigación Clínica sobre Retinopatía Diabética, Wells JA, Glassman AR, et al. Aflibercept, bevacizumab o ranibizumab para el edema macular diabético. N Engl J Med. 2015;372:13:1193-1203
7. Browning DJ, McOwen MD, Bowen RM Jr, O’Marah TL. Comparación del diagnóstico clínico del edema macular diabético con el diagnóstico mediante tomografía de coherencia óptica. Ophthalmology. 2004;111:4:712-715
8. Gillies MC, Sutter FK, Simpson JM, Larsson J, Ali H, Zhu M. Triamcinolona intravítrea para el edema macular diabético refractario: resultados a dos años de un ensayo clínico aleatorizado, doble ciego y controlado con placebo. Oftalmología. 2006;113:9:1533-1538.
9. Li L, Zhang W, Tu X, et al. Aplicación de la inteligencia artificial en la medicina de precisión para el edema macular diabético. Asia Pac J Ophthalmol (Phila). 2023;12:5:486-494.
10. Blinder KJ, Calhoun C, Maguire MG, et al. Imágenes OCT domiciliarias para la degeneración macular neovascular relacionada con la edad recién diagnosticada: un estudio de viabilidad. Ophthalmol Retina. 2024;8:4:376-387.
11. Borrelli E, Grosso D, Barresi C, et al. Resultados visuales a largo plazo y biomarcadores morfológicos de la pérdida de visión en ojos con edema macular diabético tratados con terapia anti-VEGF. Am J Ophthalmol. 2022;235:80-89
12. Lim SY, Wong WM, Seah I, et al. Régimen de tratamiento y prolongación para el edema macular diabético: revisión sistemática y metaanálisis. Graefes Arch Clin Exp Ophthalmol. 2023;261:2:303-315
13. Boyer DS, Yoon YH, Belfort R Jr, et al. Ensayo aleatorio de tres años, controlado con placebo, del implante intravítreo de dexametasona en pacientes con edema macular diabético. Ophthalmology. 2014;121:10:1904-1914
14. Spaide RF, Klancnik JM Jr, Cooney MJ. Capas vasculares de la retina obtenidas mediante angiografía con fluoresceína y angiografía por tomografía de coherencia óptica. JAMA Ophthalmol. 2015;133:1:45-50
15. Waheed NK, Rosen RB, Jia Y, et al. Angiografía por tomografía de coherencia óptica en la retinopatía diabética. Prog Retin Eye Res. 2023;97:101206
16. Durbin MK, An L, Shemonski ND, et al. Cuantificación de la densidad microvascular retiniana en imágenes de angiografía por tomografía de coherencia óptica en la retinopatía diabética. JAMA. Ophthalmol 2017;135:4:370-376
17. Ishibazawa A, Nagaoka T, Takahashi A, et al. Angiografía por tomografía de coherencia óptica en la retinopatía diabética: un estudio piloto prospectivo. Am J Ophthalmol. 2015;160:1:35-44 e31
18. Oellers P, Mahmoud TH. Cirugía para la retinopatía diabética proliferativa: nuevos consejos y trucos. J Ophthalmic Vis Res. 2016;11:1:93-99
19. Blodi BA, Domalpally A, Tjaden AH, et al. Comparación de la imagen digital ETDRS de 7 campos con la de 4 campos amplios en la evaluación de la gravedad de la retinopatía diabética. Transl Vis Sci Technol. 2022;11:1:13
20. Rohowetz, L. J., & Flynn, H. W., Jr. (2025, June 24). Optical coherence tomography in the management of diabetic retinopathy: Tips on what to look for when using this technology to assess and follow patients with DR. Retina Specialist. https://www.retina-specialist.com/article/optical-coherence-tomography-in-the-management-of-diabetic-retinopathy


Autores: Anand E. Rajesh, MD; Aaron y Lee, MD, MSCI

Anand E. Rajesh, MD

Aaron Y. Lee, MD, MSCI
Este artículo fue publicado y traducido bajo los términos de nuestra licencia con Jobson Healthcare Information. Queda estrictamente prohibida su reproducción total o parcial.
Un análisis del rendimiento de los algoritmos y las formas en que podrían mejorarse.
Biografías
El Dr. Anand E. Rajesh es residente de oftalmología en la Oregon Health & Science University.
El Dr. Aaron Y. Lee es profesor de oftalmología y titular de la cátedra C. Dan e Irene Hunter en la Universidad de Washington. Declaraciones financieras: El Dr. Rajesh no reporta conflictos de interés.
El Dr. Lee ha declarado vínculos con la FDA, Amazon, Carl Zeiss Meditec, iCareWorld, Meta, Microsoft, Novartis, Nvidia, Regeneron, Santen Pharmaceutical, Topcon, Alcon, Boehringer Ingelheim, Genentech/Roche, Gyroscope, Janssen, Johnson & Johnson, Verana Health y Microsoft.
Puntos clave
• Actualmente existen tres algoritmos de inteligencia artificial aprobados por la FDA en Estados Unidos para la detección de retinopatía diabética, con sensibilidades y especificidades de al menos 87 % y 89 %, respectivamente.
• Desde 2022, se han registrado más de 15 000 reclamaciones a Medicare por el uso de algoritmos de IA para detección de RD, principalmente en zonas urbanas con centros académicos.
• La responsabilidad por diagnósticos omitidos de RD probablemente recae en los fabricantes, aunque no está claro quién responde si el modelo no identifica otras patologías oculares graves.
• Se requieren más estudios comparativos en poblaciones diversas para garantizar un rendimiento equitativo y libre de sesgos en los modelos de IA.
La inteligencia artificial ya forma parte del panorama oftalmológico. Desde 2018, cuando la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó el primer algoritmo para la detección autónoma de la retinopatía diabética, su papel en la práctica clínica no ha dejado de crecer. Hoy existen tres algoritmos aprobados en Estados Unidos y múltiples soluciones adicionales en la Unión Europea, el Reino Unido, China, India y otros países. En este artículo se analizan estas tecnologías, las barreras regulatorias y de reembolso que limitan su adopción, así como los principales retos para su integración efectiva en la atención oftalmológica.
En términos generales, la inteligencia artificial (IA) consiste en la capacidad de una computadora para analizar datos, aprender y ejecutar una tarea. El aprendizaje automático es un subconjunto de la IA, y el aprendizaje profundo es un subconjunto del aprendizaje automático que emplea una arquitectura de red neuronal. Todos los algoritmos de IA aprobados actualmente por la FDA para la detección de la retinopatía diabética utilizan modelos basados en aprendizaje profundo.
Un modelo es una función matemática capaz de reconocer patrones en los datos y generar predicciones. Su entrenamiento se realiza mediante la introducción de datos etiquetados. Por ejemplo, en un modelo para la detección de retinopatía diabética, un equipo de ingenieros desarrolla una estructura matemática que se alimenta de manera iterativa con fotografías del fondo de ojo, clasificadas según el grado de severidad de la enfermedad. A partir de estas imágenes, el modelo aprende a predecir la gravedad de la retinopatía diabética y mejora progresivamente su precisión a través del proceso de entrenamiento.
Por último, una vez entrenado, el modelo debe validarse utilizando distintos conjuntos de datos que incluyan variaciones geográficas, étnicas y clínicas, entre otras, con el fin de garantizar su capacidad de generalización a una población más amplia. Los ingenieros realizan pruebas para verificar que la sensibilidad, la especificidad y otras métricas de desempeño se mantengan dentro de los parámetros establecidos en todos esos conjuntos. Es fundamental recordar que un buen rendimiento en un conjunto de datos no asegura resultados equivalentes en otro con características diferentes o más diversas.
En Estados Unidos existen tres dispositivos de inteligencia artificial autorizados por la FDA para la detección autónoma de la retinopatía diabética: IDx-DR de Digital Diagnostics, EyeArt de Eyenuk y AEYE Health. Es probable que otros algoritmos se encuentren actualmente en desarrollo para ampliar las opciones de detección automatizada de esta enfermedad.
Entre estos tres algoritmos, las cámaras aprobadas por la FDA para su uso varían ligeramente. IDx-DR emplea la Topcon NW400 1; EyeArt, las Canon CR-2 AF, Canon CR-2 Plus AF y Topcon NW400 2; mientras que AEYE Health es compatible con la Topcon NW400 y una cámara portátil de fondo de ojo de Optomed 3. También existen pequeñas diferencias en el número de imágenes requeridas por ojo: algunos sistemas necesitan fotografías centradas en la mácula y el disco óptico, mientras que otros solo en la mácula. Todos estos algoritmos operan con ojos no dilatados y son capaces de analizar de forma autónoma las fotografías retinianas obtenidas en la clínica para determinar si el paciente presenta una retinopatía diabética más que leve y requiere evaluación presencial por un oftalmólogo.
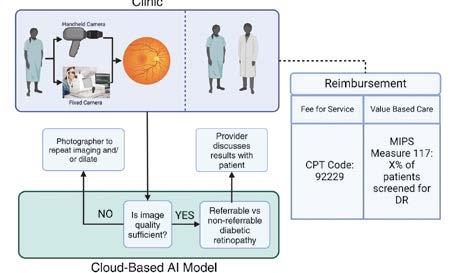
Aunque estos dispositivos de inteligencia artificial cuentan con la aprobación de la FDA, su uso aún no es universal. El Centro de Servicios de Medicare y Medicaid (CMS) publica informes anuales sobre las reclamaciones de los beneficiarios, los cuales permiten evaluar la frecuencia con que se emplean determinados procedimientos médicos. Si bien el primer algoritmo fue aprobado en 2018, en ese momento aún no existía un código de facturación que permitiera su reembolso por parte de los seguros.
En 2021 se aprobó el uso del código 92229 de la Terminología Procedimental Actual (CPT) —imágenes de retina para detección o seguimiento de enfermedades; análisis autónomo y reporte en el punto de atención—, lo que permitió a los proveedores solicitar reembolsos a Medicare y Medicaid.
Aunque diversos estudios han demostrado la eficacia de estos algoritmos, aún existe un largo camino por recorrer antes de que obtengan una aprobación amplia por parte de los organismos reguladores. El primer dispositivo avalado por la FDA para el cribado de retinopatía diabética mediante inteligencia artificial fue IDx-DR, el cual alcanzó los siguientes resultados en la detección de casos derivables de retinopatía diabética:
• Sensibilidad: 87,4 % (IC del 95 %, 81,9 % a 92,9 %);
• Especificidad: 89,5 % (IC del 95 %, 86,9 % a 93,1 %);
• Capacidad de visualización: 96 %;
• Valor predictivo positivo (VPP): 73 %; y
• Valor predictivo negativo (VPN): 96 %.5,6
La FDA requiere que todos los algoritmos posteriores demuestren un rendimiento equivalente al de IDx-DR como condición para su aprobación. Esta equivalencia debe comprobarse mediante un estudio prospectivo que incluya una cohorte diversa. Una vez aprobado un algoritmo, los fabricantes no pueden modificar sus parámetros ni actualizar el modelo sin una nueva revisión y autorización por parte de la FDA. Otra área regulatoria aún en desarrollo es la responsabilidad médico-legal ante posibles casos de negligencia relacionados con sistemas autónomos de inteligencia artificial. Actualmente existen pocos precedentes judiciales, dado el reducido número de demandas por daños personales atribuibles a la IA que hayan derivado en fallos legales.
Tanto la Asociación Médica Americana7 como diversos expertos coinciden en que, en el caso de sistemas de IA autónoma, la responsabilidad ante un diagnóstico inexacto recae principalmente en el fabricante del dispositivo que desarrolló el algoritmo. Cuando un médico decide no seguir las recomendaciones de la IA que representan el estándar de atención —o, por el contrario, ignora una sugerencia que no cumple dicho estándar 8, 9— la responsabilidad puede variar según el contexto clínico y legal. En general, el fabricante tiende a asumir la mayor carga de responsabilidad frente al personal médico.
Surge además una interrogante ética y legal relevante: ¿quién responde si un modelo de IA no detecta otra patología grave visible en la imagen, como un desprendimiento de retina o un melanoma coroideo potencialmente mortal? La omisión de una alerta podría causar un daño significativo al paciente. En contraste, los evaluadores humanos que realizan telerretinografía sí pueden reconocer estas lesiones y comunicarlas directamente. Sin embargo, los algoritmos actuales no están entrenados para identificar otras enfermedades oculares fuera de la retinopatía diabética.
Para que el cribado con IA DR tenga el efecto generalizado en la población que muchos esperan, debe ser económicamente viable para las clínicas adoptarlo.
En el modelo de pago por servicio, los proveedores presentan reclamaciones al seguro cada vez que prestan el servicio de detección de RD por IA a un paciente. En 2023, el reembolso base, independiente de la ubicación, para el código CPT 92229 (imágenes remotas - análisis automatizado) era de 40,28 dólares, en comparación con el código CPT 92227 (Imágenes remotas: revisión por parte del personal) de 17,35 dólares y el código CPT 92228 (Imágenes remotas: interpretación por parte de un médico) de 29,14 dólares.10
Actualmente, la IA reembolsa más que los evaluadores humanos, lo que probablemente sea necesario para fomentar la adopción de esta tecnología y permitir un mayor acceso a la atención para la detección de la retinopatía diabética.11 Las tasas de reembolso de los seguros comerciales son más difíciles de evaluar porque son muy variables y no suelen hacerse públicas. Sin embargo, una fuente reveló que la tarifa media negociada de forma privada para la detección mediante IA de Anthem Healthcare en California y Nueva York era de 127,81 dólares en 2021.4
Otra forma en que el cribado con IA puede generar ingresos es a través del modelo de reembolso de la atención basada en el valor. En este sistema de pago, se paga a la clínica, el grupo o el proveedor por la salud general de la población a la que atiende, y se incentiva a los grupos para que presten la mejor atención a la población basándose en métricas basadas en procesos. En Estados Unidos, el Sistema de Pago por Méritos ofrece pagos a los grupos o proveedores que cumplen determinadas métricas de calidad. En el caso de las pruebas de detección de diabetes ocular, que se clasifican en la medida 117 del MIPS, se registra el porcentaje de pacientes con diabetes atendidos que se someten a pruebas periódicas de detección de diabetes ocular. Si se cumple la medida, Medicare ofrece incentivos económicos a los grupos o proveedores.12 Por lo tanto, los grupos o proveedores que no se acogen al modelo de pago por servicio prestado pueden seguir recibiendo reembolsos por realizar pruebas de detección de diabetes ocular con IA.
A medida que el cribado con IA se vuelve más común en la práctica clínica, es esencial garantizar que funcione de manera equitativa en poblaciones diversas en términos raciales, socioeconómicos, geográficos, de género y de otro tipo. Aunque estos modelos pueden funcionar bien en una población, eso no significa que vayan a funcionar bien en otra diferente.
EyeART e IDx-DR no han mostrado ninguna disminución sustancial en su rendimiento en los diferentes subgrupos; sin embargo, hay pocos estudios que analicen el rendimiento de estos algoritmos de forma comparativa 13,16. AEYE no ha publicado sus resultados en ninguna revista científica revisada por pares. Aunque estos algoritmos han funcionado bien hasta ahora, se necesitan más estudios para evaluar su rendimiento en diferentes conjuntos de datos diversos y garantizar así un funcionamiento equitativo.
En conclusión, la IA para la detección de la RD está llamada a tener un impacto significativo en la atención al paciente en los próximos años. Sin embargo, aún existen importantes interrogantes en cuanto a la elección de los algoritmos, la regulación
1. LumineticsCoreTM. Diagnóstico digital. Publicado el 28 de marzo de 2023. https://www.digitaldiagnostics.com/products/eye-disease/lumineticscore/. Consultado el 24 de junio de 2024.
2. EyeArt - Eyenuk, Inc. ~ Examen ocular con inteligencia artificial. Eyenuk, Inc. ~ Examen ocular con inteligencia artificial. Publicado el 14 de abril de 2020. https://www.eyenuk.com/us-en/products/eyeart/. Consultado el 24 de junio de 2024.
3. Examen diagnóstico AEYE. AEYE Health. https://www.aeyehealth.com/ aeye-diagnostic-screening. Consultado el 30 de junio de 2024.
4. Wu Kevin, Wu Eric, Theodorou Brandon, Liang Weixin, Mack Christina, Glass Lucas, et al. Caracterización de la adopción clínica de dispositivos médicos de inteligencia artificial a través de reclamaciones de seguros en EE. UU. NEJM AI. 2023;1(1):AIoa2300030.
5. K221183.pdf. https://www.accessdata.fda.gov/cdrh_docs/pdf22/ K221183.pdf
6. K223357.pdf. https://www.accessdata.fda.gov/cdrh_docs/pdf22/ K223357.pdf
7. ai-2018-board-policy-summary.pdf. https://www.ama-assn.org/system/ files/2019-08/ai-2018-board-policy-summary.pdf
8. Saenz AD, Harned Z, Banerjee O, Abràmoff MD, Rajpurkar P. Sistemas autónomos de IA frente a la responsabilidad, las regulaciones y los costos. NPJ Digit Med. 2023;6(1):185.
9. Mello MM, Guha N. Comprensión del riesgo de responsabilidad derivado del uso de herramientas de inteligencia artificial en la atención médica. N Engl J Med. 2024;390(3):271-278.
y las estructuras de reembolso. A medida que se siga adoptando esta nueva tecnología, esperamos que se utilice para prestar atención a las personas con acceso limitado, con el fin de ayudar a prevenir la progresión de la retinopatía diabética.
10. Facturación y codificación: Imágenes remotas de la retina para detectar enfermedades retinianas. https://www.cms.gov/medicare-coverage-database/view/article.aspx?articleid=58914. Consultado el 5 de abril de 2023
11. AAO a CMS 2024 MPFS PR Comentario 09.08.23 1 (1).pdf.
12. Abramoff Michael D., Dai Tinglong, Zou James. Ampliación de la adopción de la IA médica: reembolso desde la perspectiva de la atención basada en el valor y la tarifa por servicio. NEJM AI. 2024;1(5): AIpc2400083.
13. Tufail A, Rudisill C, Egan C, Kapetanakis VV, Salas-Vega S, Owen CG, et al. Software automatizado de evaluación de imágenes de retinopatía diabética: precisión diagnóstica y rentabilidad en comparación con los evaluadores humanos. Oftalmología. 2017;124(3): 343-351.
14. Ipp E, Liljenquist D, Bode B, Shah VN, Silverstein S, Regillo CD, et al. Evaluación fundamental de un sistema de inteligencia artificial para la detección autónoma de la retinopatía diabética que requiere derivación y pone en peligro la visión. JAMA Netw Open. 2021;4(11):e2134254.
15. Lee AY, Yanagihara RT, Lee CS, Blazes M, Jung HC, Chee YE, et al. Estudio multicéntrico, comparativo y de validación en el mundo real de siete sistemas automatizados de detección de la retinopatía diabética basados en inteligencia artificial. Diabetes Care. 2021;44(5):1168-1175.
16. Rajesh AE, Davidson OQ, Lee CS, Lee AY. Inteligencia artificial y retinopatía diabética: marco de IA, estudios prospectivos, validación comparativa y rentabilidad. Diabetes Care. 2023;46(10):1728-1739.



Autores: Arturo Ramírez Miranda, María José González Guerra, Alejandro Navas, Enrique Graue Hernández
Departamento de Córnea y Cirugía Refractiva, Instituto de Oftalmología “Conde de Valenciana”, Ciudad de México.
La queratopatía neurotrófica (NK) es una enfermedad ocular grave caracterizada por la pérdida de la inervación sensorial de la córnea, lo que conduce a alteraciones en la cicatrización epitelial, reducción en la producción lagrimal y riesgo de úlceras recurrentes. Entre las causas más frecuentes se encuentran la cirugía de base de cráneo, tumores intracraneales, traumatismos y procesos inflamatorios o infecciosos. Las terapias médicas tradicionales (lágrimas artificiales, antibióticos, factores de crecimiento o tarsorrafia) suelen ser insuficientes en estos casos.
La neurotización corneal (CN) se ha desarrollado como una técnica quirúrgica innovadora para restaurar la sensibilidad corneal. Consiste en transferir nervios sanos hacia la córnea, utilizando técnicas directas (transferencia de nervios vecinos) o indirectas (uso de injertos nerviosos como puente). El presente estudio multicéntrico reporta los resultados a largo plazo de la CN indirecta utilizando injerto de nervio sural en pacientes con parálisis facial y NK secundaria a neurocirugía.
Se realizó un estudio prospectivo, intervencional, multicéntrico y no controlado, entre julio de 2018 y junio de 2022, en tres instituciones de referencia de la Ciudad de México: Instituto de Oftalmología Fundación Conde de Valenciana IAP, Instituto Nacional de
Neurología y Neurocirugía y el Hospital General Dr. Gea González. Se incluyeron 14 ojos de 14 pacientes (5 hombres y 9 mujeres) con edad promedio de 36.7 años (rango 18–63), todos con NK severa (Mackie estadio III). El tiempo medio entre el inicio de síntomas y la cirugía fue de 21.4 meses.
La técnica quirúrgica consistió en la obtención de injertos nerviosos autólogos (10 nervios surales y 4 peroneos superficiales), que fueron coaptados al nervio supratroclear contralateral. Los fascículos del injerto se distribuyeron de manera perilímbica para permitir la reinervación corneal. Todos los procedimientos se realizaron bajo anestesia general y formaron parte de un abordaje reconstructivo integral, que incluyó en la mayoría de los pacientes, técnicas de reanimación facial y procedimientos palpebrales (tarsorrafia, implante de peso de oro) (Figura 1).
Se evaluaron parámetros clínicos durante un seguimiento promedio de 51.6 meses: sensibilidad corneal (estesiometría de Cochet-Bonnet), agudeza visual mejor corregida (BCVA), estabilidad de la película lagrimal (tiempo de ruptura), integridad epitelial y complicaciones postoperatorias.
Previo a la cirugía, todos los pacientes tenían pérdida completa de la sensibilidad corneal y compromiso severo de la
superficie ocular (13 casos con leucoma central y 1 con colgajo conjuntival). Tras la intervención, se observó una recuperación progresiva de la sensibilidad corneal, iniciando alrededor del tercer mes y estabilizándose hacia los 36 meses, con una mediana final de 3.5 mm en la estesiometría. Para el sexto mes, el 85.7% de los pacientes ya mostraba mejoría significativa.
El tiempo de ruptura lagrimal mejoró de manera estadísticamente significativa, pasando de 2.85 segundos en la evaluación basal a 5.15 segundos a los 24 meses (p < 0.001), lo que refleja una mejoría en la estabilidad de la película lagrimal.
La agudeza visual mostró una ligera mejoría sin alcanzar significancia estadística: la mediana de BCVA fue de 0.06 LogMAR al inicio frente a 0.05 LogMAR a los 36 meses. Aun así, clínicamente se observó resolución de defectos epiteliales, reducción de la neovascularización y disminución del leucoma en varios pacientes.
Las complicaciones reportadas fueron limitadas: dos granulomas relacionados con el injerto, dos casos de queratitis bacteriana (uno requirió queratoplastia penetrante) y defectos epiteliales transitorios en dos pacientes, resueltos con tratamiento tópico. En ningún caso hubo falla completa del procedimiento o complicaciones graves derivadas del injerto (Figura 2).
Discusión:
La CN indirecta mediante injerto de nervio sural se mostró como una opción quirúrgica segura y eficaz para restaurar sensibilidad corneal y mejorar la salud de la superficie ocular en pacientes con NK avanzada y parálisis facial. La mejoría sostenida hasta los 36 meses respalda la viabilidad de la técnica.
Estos hallazgos coinciden con estudios previos que demuestran la capacidad del nervio sural de servir como puente efectivo para la regeneración axonal y la reinervación corneal. Aunque las complicaciones aparecieron en un número reducido de pacientes, fueron manejables con medidas convencionales.
Conclusiones:
La neurotización corneal indirecta con injerto de nervio sural representa una alternativa quirúrgica prometedora para pacientes con NK severa refractaria a terapias convencionales, particularmente en aquellos con parálisis facial secundaria a procedimientos neurológicos. Este abordaje permite la recuperación sostenida de la sensibilidad corneal, mejora la estabilidad de la superficie ocular y reduce el riesgo de complicaciones visuales graves. Se requieren estudios multicéntricos con mayor número de pacientes, seguimientos prolongados y métodos diagnósticos avanzados para validar y optimizar esta técnica en la práctica clínica.
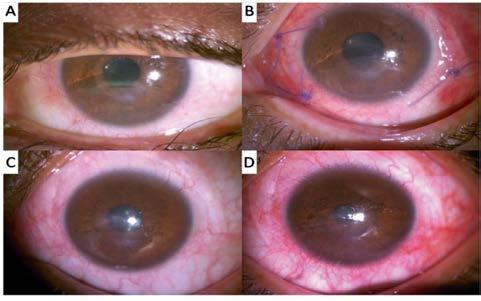
Figura 1. Fotografías con lámpara de hendidura de un paciente con antecedente de resección de craneofaringioma que ocasionó lesión iatrogénica de los nervios craneales V y VII, además de comorbilidades como diabetes mellitus tipo 1 y obesidad. (A)Imagen preoperatoria que muestra cicatriz central corneal con neovascularización inferior secundaria a queratopatía neurotrófica progresiva. (B)Fotografía inmediata tras la neurotización corneal. (C) Un año después de la cirugía, se observa mejoría en la cicatrización y en la neovascularización, con fascículos del nervio sural subconjuntivales próximos al limbo nasal y temporal. (D) Imagen a los tres años postoperatorios, tras un episodio de úlcera epitelial corneal resuelta, en la que se aprecia superficie ocular estable con cicatriz corneal central y sin defectos epiteliales activos.
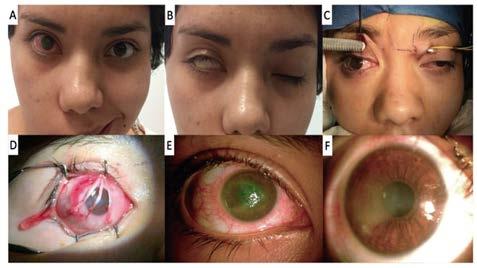
2. (A, B) Paciente con parálisis facial. (C) Creación de un túnel subcutáneo sobre el dorso nasal para el injerto de nervio sural invertido.(D) Vista microscópica de tres fascículos del nervio donador distribuidos sobre la córnea afectada. (E, F) Fotografías con lámpara de hendidura de la córnea antes y tres meses después de la neurotización corneal indirecta, respectivamente.
1. Albavera-Giles, T., Vera-Duarte, G. R., Ortiz-Morales, G., Serrano-Robles, G., Gomez-Villegas, T., Navas, A., Graue-Hernandez, E., Ramirez-Miranda, A. (2025). Indirect corneal neurotization: Long-term outcomes using a sural nerve graft in patients with facial palsy and neurotrophic keratopathy. Cornea, 00(00), 1–8. https://doi.org/10.1097/ICO.0000000000003922

Dr. Alejandro J. Aguilar MD, pHD Argentina aguilar.alejandrojavier@usal.edu.ar
Este artículo salió en el Noticiero #71 septiembreoctubre y se publicó con el permiso de ALACCSA - R. Su reproducción está prohibida. Para más información sobre el noticiero visite la página web www.alaccsa.com
El avance de las diferentes técnicas quirúrgicas refractivas, así como también de la bioingeniería aplicada a los dispositivos tecnológicos e instrumental para realizarlas, han permitido en la actualidad, disminuir el impacto que sobre la superficie ocular estos procedimientos pueden ocasionar. Para minimizar esta posibilidad y preservar aún más la salud de la superficie ocular se hace imperioso establecer distintas estrategias pre y post operatorias.
El camino entre la promesa del resultado refractivo y la posibilidad de la insatisfacción del paciente así como también de la frustración del cirujano dependerá, en buena medida, de la salud de la superficie ocular y muy especialmente de la homeostasis del film lagrimal. Una superficie ocular sana en el preoperatorio, que se expresa inestable en el post o una superficie ocular inestable en el pre (el peor escenario), que se agrava en el post quirúrgico pueden ser causa de insatisfacción del paciente (1) y frustración del cirujano.
La función refractiva del film es indispensable para mantener la correcta agudeza visual y más importante aún su calidad.
Es muy frecuente encontrarnos frente a pacientes que cuantitativamente presentan 10/10 en el post y sin embargo están insatisfechos. Su “cantidad” visual es buena, pero su “calidad” visual es mala. Fluctuaciones visuales, visión de halos, enturbiamiento visual con el parpadeo, alteraciones de la acomodación y astenopia son algunas de las típicas manifestaciones de pacientes con mala calidad visual provocada por la sequedad ocular. (2). En este sentido el ojo seco es el principal responsable de la mencionada ecuación: insatisfacción / frustración
De la misma manera que el cirujano selecciona al candidato realizando los test inherentes a sus características refractivas y determina el procedimiento quirúrgico a realizar, resulta indispensable que incluya un exhaustivo examen de la superficie ocular y del film lagrimal.
Si bien en la actualidad contamos con modernos y sofisticados equipos de diagnóstico: interferómetros, escáneres del film y de la superficie ocular y meibógrafos; el examen biomicroscópico de la superficie ocular y sus anexos palpebrales, así como también del film y del menisco lagrimal junto a test como el tiempo de ruptura de la película lagrimal (BUT) -en relación al parpadeo- y las tinciones de córnea y conjuntiva siguen siendo valiosos e indiscutidos aliados del cirujano.
Las estrategias terapéuticas para mejorar la calidad de la lágrima son similares para el pre y post quirúrgico; sin embargo la decisión de incluir o no a un paciente con sospecha de ojo seco previo a la cirugía es la clave y el punto crítico a definir. Ante la duda: no incluir.
El manejo del ojo seco posterior a cirugía de córnea y refractiva comienza en el prequirúrgico, en la correcta elección del candidato.
Teniendo en cuenta lo que conocemos hoy en día del ojo seco, su manejo debería incluir, la estabilidad film (3) , el bajar su hiperosmolaridad para evitar el daño tisular y la cascada inflamatoria (4), controlar la inflamación de la superficie ocular y evitar o mejorar el daño celular epitelial (5). Debemos considerar al paciente post quirúrgico como portador de ojo seco hasta que no se demuestre lo contrario.
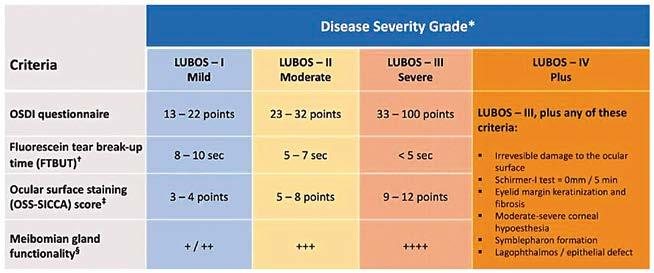
Se debe tener en cuenta además el grado de ojo seco: leve, moderado o grave y el tipo: lacrimo-deficiente, evaporativo o mixto para adecuar las medidas terapéuticas a cada forma en particular. Tabla 1
Los lubricantes artificiales (gotas, geles, ungüentos) y las nanoemulsiones lipídicas para los casos evaporativos permiten estabilizar el film lagrimal, brindar efecto mucomimético y proteger la salud de la superficie ocular epitelial. El manejo antiinflamatorio local incluye a los esteroides para el momento agudo y a la ciclosporina para el proceso crónico. Nuevas moléculas como el lifitegrast pueden ser empleadas para el manejo crónico
Se deben elegir, en lo posible, libres de conservantes (6).
Suero autólogo, secretagogos y suplementos dietarios como el ácido omega 3 deben ser tenidos en cuenta.
El control de las condiciones ambientales así como también la exposición a pantallas son factores que el cirujano debe considerar.
Lentes de protección o las denominadas cámaras húmedas pueden ser de utilidad.
Métodos no farmacológicos como la oclusión de los puntos lagrimales con implantes intracanaliculares forman parte de la batería terapéutica. En mi experiencia personal, evito el uso de los llamados tapones lagrimales y prefiero los de aplicación intracanalicular profunda.
Un capítulo aparte lo merecen aquellos pacientes que han sido correcta y satisfactoriamente tratados, donde la superficie ocular se encuentra estable y sin embargo siguen presentando sintomatología e insatisfacción. Estos casos son los más complejos de revertir. La génesis de una superficie ocular neurológica debe ser considerada y adecuar el mejor esquema terapéutico para controlarla.
1. Woodward MA, Randleman JB, Stulting RD. Dissatisfaction after multifocal intraocular lens implantation. J Cataract Refract Surg 2009; 35:992-997
2. Aguilar AJ. Síndrome del ojo seco. En: Bregliano G, Fernández Mendy J, Nicoli M. Guia para el manejo de la presbicia y la multifocalidad. Sociedad Argentina de Oftalmologia. Ediciones Científicas Argentinas . Buenos Aires 2024 p. 47-51
3. Pereira Gomes J.A.; Ruiz Alves, M. Editores. Ferreira Pires, R.T. Co Editores. Superficie Ocular: cornea, limbo, conjunctiva, filme lacrimal. Cultura Medica. Rio de Janeiro 2006.
4. Aguilar AJ, Berra A. Hyperosmolarity of the tear film in the dry eye. En The Ocular Surface. Intech Open Edit. United Kingdom 2020. P 1-7
5. Rodriguez-Garcia A, Nuñez MX, Pereira-Gomes JA, Henriquez MA, Garza-Leon M. Aguilar AJ and the LUBOS expert panelists. Latin American Consensus on ocular lubricants an dry eye didease (LUBOS): a report onclassification, diagnosis and therapy. Severity. Corneajml. 2025.
6. Baudouin C, Labbé A, Liang H, et al. Preservatives in eyedrops: the good, the bad and the ugly. Prog Retin Eye Res. 2010;29:312–334.
Por Juan Pablo Chajin, editor

Resumen
Durante el simposio “Controversias sobre los tratamientos láser modernos para la retina y el vítreo”, el Dr. Lihteh Wu moderó a los doctores Dr José Antonio Roca Dr. Juan Gonzalo Sánchez y la Dra María Berrocal mientras debatían la eficacia, riesgos y el futuro del láser en los siguientes escenarios:
• Tratamiento de las miodesopsias sintomáticas (vitreolisis láser) con láser YAG Reflex.
• Tratamiento de la retinopatía diabética proliferativa (RDP) con la fotocoagulación panretiniana multispot.
• Tratamiento del edema macular diabético (EMD) utilizando el láser 577 subumbral.
Este artículo resume sus posturas y reflexiones, citando directamente a los expertos y contextualizando sus argumentos en la evidencia científica disponible.
Vitreolisis con Láser YAG:
¿Observar o intervenir?
Postura conservadora:
“Yo abogo por la observación”
– Dr. José Antonio Roca
El Dr. José Antonio Roca abrió el simposio planteando una visión cautelosa frente a la vitreolisis con láser YAG. “Las moscas volan-
tes son inofensivas, se desvanecen con el tiempo. Yo abogo por la observación de esta patología”, afirmó.
Basado en su experiencia, destacó que la mayoría de los pacientes con desprendimiento del vítreo posterior (DVP) logran neuroadaptación. “Yo tengo miodesopsias. Me neuroadapté y no tengo ningún inconveniente”, comentó. Citó que el 40% de los pacientes con DVP experimentan remisión espontánea de los síntomas, por lo que recomendó evitar cualquier intervención antes de los 6 a 12 meses posteriores al evento.
Respecto a la eficacia del procedimiento, mencionó un estudio con seguimiento de 14 meses en el que solo el 2.5% de los pacientes reportaron mejoría significativa, mientras que más del 50% no tuvo ningún cambio. “La vitreolisis puede tener riesgos reales: agujeros maculares, hemorragias subretinianas, cataratas traumáticas, e incluso desprendimiento de retina años después del procedimiento”, advirtió.
Postura intervencionista:
“Es hora de evolucionar”
– Dr. Juan Gonzalo Sánchez
A continuación, el Dr. Juan Gonzalo Sánchez, ofreció una visión opuesta: “Los flotadores sintomáticos son una discapacidad visual real. Es hora de evolucionar de la observación pasiva a la medicina restaurativa”.
Presentó múltiples estudios que demuestran una mejoría objetiva entre el 56% y el 94% de los pacientes tratados con vitreolisis, incluyendo mejoría en la calidad de vida y sensibilidad al contraste. “El número necesario a tratar (NNT) es de 2.3. Es decir, por cada tres pacientes tratados, dos mejoran significativamente”, enfatizó.
También recalcó el impacto emocional y funcional de los flotadores en pacientes de alto desempeño: “En un estudio, los pacientes llegaron a decir que preferían perder un año de vida por cada 10 con tal de eliminar sus miodesopsias. ¡Esto muy significativo!”
En cuanto a seguridad, destacó que 7 de 10 estudios no reportaron complicaciones. “Sí, hubo un artículo en 2017 que reportó 16 eventos adversos, pero sus propios autores reconocieron que no había evidencia concluyente. Lo cierto es que bien indicada, la vitreolisis es segura”.
Finalmente, diferenció casos de candidatos ideales para láser y de aquellos que deben tratarse con vitrectomía : “La vitreolisis no es la panacea, pero tenemos hoy las herramientas para devolver la calidad de vida a nuestros pacientes. ¿Seguiremos negándoles el alivio que merecen por paradigmas obsoletos?”.
La Dra. María Berrocal defendió firmemente el uso del láser panretiniano como tratamiento de primera línea para la RDP. “Desde 1972 sabemos que reduce el riesgo de pérdida visual severa en más del 50%. Es costo-eficiente, tiene pocas complicaciones y estabiliza el ojo a largo plazo”.
Criticó el uso exclusivo de antiangiogénicos en esta patología, especialmente en poblaciones con baja adherencia a tratamiento. “Más del 25% de los pacientes no vienen a controles anuales. De ellos, el 33% termina con desprendimiento traccional si solamente se utilizaron antiangiogénicos”.
Respaldó su argumento con datos del Protocolo S, donde los pacientes tratados con anti-VEGF necesitaron el doble de visitas, y muchos igualmente requirieron láser. “Incluso en ensayos clínicos con seguimiento estricto, hubo más eventos cardíacos, fibrosis, e incluso el doble de muertes en el grupo con antiangiogénicos. Y no olvidemos que el láser no produce endoftalmitis. Ningún paciente ha tenido una por láser”, afirmó de forma contundente.
Para Berrocal, la monoterapia con antiangiogénicos para el tratamiento de la RDP es “la forma más eficaz de causar ceguera irreversible”.
El Dr. Lihteh Wu abordó el uso del láser subumbral en la zona macular para el tratamiento de EMD con un enfoque pragmático. “Yo uso antiangiogénicos como primera línea. Pero hay escenarios donde el láser es útil: edemas no centrales, pacientes con buena visión central, o aquellos que no responden tras 6 inyecciones”.
Mostró un caso tratado con láser subumbral (micropulsado) en un paciente que vivía a ocho horas del centro médico. “Decidimos usar láser por su imposibilidad de seguimiento. A los 4 meses, el edema había desaparecido”.
El Protocolo V del DRCR.net fue citado como evidencia de que observación, láser y antiangiogénicos pueden ofrecer resultados similares en pacientes con buena visión. “Pero veamos los costos: tratar con aflibercept cuesta más de 17 mil dólares por ojo en 10 años, mientras que el láser cuesta 5 mil. Ningún sistema de salud puede sostener el uso masivo de antiangiogénicos”.
Finalmente, explicó el mecanismo del láser subumbral. “No quema la retina. Activa células gliales y reduce citoquinas inflamatorias. Estudios han evidenciado que cuando el láser se combina con antiangiogénicos un número menor de inyecciones son requeridas”.
El simposio dejó claro que no hay respuestas absolutas. Como resumió el Dr. Sánchez: “La pregunta ya no es si podemos intervenir de forma segura. Es si estamos dispuestos a seguir negando alivio a nuestros pacientes por paradigmas del pasado”.
El juicio clínico, la individualización y la evidencia deben guiar el uso del láser en retina y vítreo. Mientras algunos abogan por la prudencia, otros impulsan una visión restauradora y proactiva. Lo cierto es que el debate continúa.

En los últimos años, la tecnología láser aplicada a la oftalmología ha evolucionado hacia soluciones más versátiles y adaptadas a las necesidades específicas de los pacientes.1 Entre estas innovaciones se encuentra el láser Nd:YAG
MR Q Supine, un equipo desarrollado por Meridian Medical que ha sido concebido para realizar procedimientos con el paciente en posición supina.2 Este diseño, permite el uso del equipo en entornos quirúrgicos, en pacientes bajo sedación o en aquellos que presentan limitaciones para posicionarlos frente a una lámpara de hendidura convencional.3
Standby/Ready Indications Symbols
Standby/Ready Button
El MR Q Supine incorpora un sistema Nd:YAG Qswitched en estado sólido que opera a una longitud de onda de 1064 nm, con una duración de pulso de aproximadamente 4 nanosegundos. La tecnología permite generar impactos de energía concentrada, con un tamaño de punto de tratamiento de alrededor de 10 micras y una divergencia de haz de 16 grados.4 La calibración entre el ocular y el haz guía se ajusta de forma que ambos sean cofocales, y el control se realiza mediante un joystick que permite desplazar el cabezal y la torre de iluminación en los tres ejes.
El operador cuenta, además, con un binocular inclinable y un sistema de enfoque fino, lo que podría contribuir a que mantenga una postura ergonómica durante el procedimiento.5
El equipo cuenta con un sistema de control digital del “offset” anterior y posterior, que facilita la configuración rápida de la distancia de enfoque en función del tipo de tejido a tratar. Tras cada procedimiento, el sistema restablece automáticamente los valores predeterminados, lo que contribuye a minimizar el riesgo de errores en la práctica clínica. Lo que le permite al equipo realizar procedimientos como capsulotomías posteriores, iridotomías y membranectomías pupilares con mayor precisión. 5

La disposición supina del paciente ofrece mayor estabilidad de la cabeza y el ojo del paciente durante el procedimiento, lo que favorece la exactitud del disparo y reduce el riesgo de movimientos bruscos. Asimismo, esta posición facilita el acceso a pacientes con movilidad reducida, niños, personas con problemas de columna o pacientes hospitalizados que no pueden mantenerse sentados. En entornos quirúrgicos, la integración de la posición supina permite un flujo de trabajo más ágil, ya que evita traslados innecesarios y puede combinarse con otros procedimientos bajo anestesia, optimizando el tiempo de quirófano y la comodidad del paciente. 6
El MR Q Supine combina un diseño robusto con una mesa eléctrica de altura regulable mediante columnas telescópicas sincronizadas. El conjunto integra un sistema de bloqueo automático de ruedas que se activa durante la operación, y cuenta con un acceso controlado por código PIN para limitar su uso a personal autorizado. 7

1. Meridian Medical (n.d.). Meridian MRQ Supine Brochure (1st ed.).Pag.6 [PDF]. https://uk.haag-streit.com/2%20Products/Treatment/MR%20 Q%20&%20Mr%20Q%20Supine%20YAG%20laser/Brochures/English/ meridian_MRQ_supine_br_1026044_en.pdf
2. Meridian Medical. (n.d.). Meridian MRQ Supine Brochure (1st ed.).Pag.5 [PDF]. https://uk.haag-streit.com/2%20Products/Treatment/MR%20 Q%20&%20Mr%20Q%20Supine%20YAG%20laser/Brochures/English/ meridian_MRQ_supine_br_1026044_en.pdf
3. Meridian Medical. (n.d.). Meridian MRQ Supine Brochure (1st ed.).Pags. 5-6 [PDF]. https://uk.haag-streit.com/2%20Products/Treatment/ MR%20Q%20&%20Mr%20Q%20Supine%20YAG%20laser/Brochures/ English/meridian_MRQ_supine_br_1026044_en.pdf
4. Meridian Medical (n.d.). Meridian MRQ Supine Brochure (1st ed.).Pag. 11 [PDF]. https://uk.haag-streit.com/2%20Products/Treatment/MR%20 Q%20&%20Mr%20Q%20Supine%20YAG%20laser/Brochures/English/ meridian_MRQ_supine_br_1026044_en.pdf
5. Meridian Medical| Quick Reference Guide MRQ SUPINE. (n.d.). Meridian Medical Group. Pags. 1-2. https://uk.haag-streit.com/2%20Products/Treatment/MR%20Q%20&%20Mr%20Q%20Supine%20YAG%20 laser/Brochures/English/meridian_MRQ_supine_br_1026044_en_ quick-reference-guide.pdf
6. Promelle, V. (2020). Featuring the Nd:YAG laser capsulotomy in the operating room. International Journal of Ophthalmology, 13(3). Pag. 523 ijo-13-03-523.pdf
7. Meridian Medical (n.d.). Meridian MRQ Supine Brochure (1st ed.).Pag. 7[PDF]. https://uk.haag-streit.com/2%20Products/Treatment/ MR%20Q%20&%20Mr%20Q%20Supine%20YAG%20laser/Brochures/ English/meridian_MRQ_supine_br_1026044_en.pdf

La introducción de difluprednato en México representa un avance terapéutico significativo, al ampliar las opciones para el control del dolor y de la inflamación ocular. Laboratorios Sophia presenta Deslotan en su innovadora presentación en nanoemulsión, posicionándose como el laboratorio pionero en introducir esta sal en el país. Esta alternativa ha demostrado ser eficaz y segura, con respaldo clínico comprobado.
El control de la inflamación ocular es esencial para alcanzar resultados quirúrgicos óptimos y prevenir complicaciones como edema macular quístico, sinequias, glaucoma o pérdida visual irreversible. La manipulación intraocular durante la cirugía desencadena la liberación de ácido araquidónico y mediadores inflamatorios, responsables de la ruptura de la barrera hematoacuosa y de la respuesta inflamatoria posoperatoria [1] [2]. Aunque las técnicas quirúrgicas modernas han reducido este riesgo, un subgrupo de pacientes continúa presentando inflamación significativa que requiere manejo farmacológico intensivo [3] [4].

Difluprednato es un corticosteroide sintético derivado de la prednisolona, diseñado con modificaciones estructurales que potencian su actividad antiinflamatoria y mejoran su penetración corneal [5] [6]. La FDA aprobó en el año 2008 la emulsión oftálmica al 0.05% para inflamación y dolor asociados a cirugía ocular, y en 2018 fue autorizada en México por COFEPRIS para cirugía y
uveítis anterior endógena. Ensayos clínicos de fase 3 demostraron su superioridad frente a placebo en inflamación postquirúrgica y su no inferioridad frente a prednisolona 1% en uveítis, con menor frecuencia de dosificación y un perfil de seguridad aceptable [7].
1. C. Mithal, S. Singh, S. Gupta y S. Mithal, «Difluprednate: an overview,» Delhi Journal of Ophthalmology, vol. 23, nº 3, pp. 165-168, 2012.
2. B. Jain y M. Shrivastawa, «To compare the safety and efficacy of difluprednate 0.05% emulsion and prednisolone acetate 1% in the post operative inflammation following cataract extraction with iol implantation,» J of Evoluion of Med and Dent Sci, vol. 3, nº 53, pp. 12341-12343, 2014.
3. K. N. Jamal, «The role of difluprednate ophthalmic emulsion in clinical practice,» Clinical Ophthalmology, vol. 3, pp. 381-390, 2009.
4. U. Pleyer, Immune Modulation and Anti-Inflammatory Therapy in ocular Disorders, New York: Springer, 2014.
5. J. D.Bartlett, Clinical Ocular Pharmacology, 5 ed., St. Louis, Missouri: Butterworth-Heinemann, 2008, pp. 221,226-229,235,,236.
6. Center for Drug Evaluation and Research, «Application Number: 22-212 Pharmacology Review(s),» 26 Diciembre 2007. [En línea]. Available: https:// www.accessdata.fda.gov/drugsatfda_docs/ nda/2008/022212s000_PharmR.pdf. [Último acceso: 11 Julio 2022].
7. Novartis Pharmaceuticals Canada Inc., «Product Monograph Durezol,» Quebec, 2018.

Oftálmica Internacional tiene disponible
Pictor Plus, una cámara portátil que redefine la movilidad en la práctica oftalmológica. Desde la consulta hasta las revisiones en campo, o durante las visitas a residencias y centros de atención, Pictor Plus acompaña al especialista a donde sea necesario, ofreciendo la misma calidad diagnóstica en cualquier entorno.
Las imágenes de alta resolución son altamente eficaces durante las evaluaciones iniciales y los tratamientos de seguimiento. La información del paciente puede ingresarse directamente en el dispositivo para su historial clínico. Pictor Plus provee atención de salud visual de la más alta calidad, siendo especialmente efectiva en consultas iniciales y en el seguimiento de tratamientos. La información personal del paciente se registra directamente en la cámara, lo que permite una fácil adaptación a su práctica.
Dos módulos fácilmente intercambiables proveen imágenes retinales (no midriáticas) de alta resolución y videos. Dos módulos opcionales permiten la examinación del oído y piel.
Encuéntranos en Tijuana y CDMX. Más información en www.oftalmica.com
O en nuestras redes sociales @oftalmicainternacional
Para mayor información comunícate:
Vía telefónica:
��Tijuana (Matriz): (664) 684 8230
��CDMX (Equipos): (553) 341 3140
Correo electrónico:
Tijuana (Matriz): marcela@oftamica.com
CDMX (Sucursal): hugo@oftalmica.com
ASOCIACIÓN LATINOAMERICANA DE CIRUJANOS DE CATARATA, SEGMENTO ANTERIOR Y REFRACTIVA (ALACCSA-R) /Portada 3
© 2017 Alaccsa-R • 2446 W Whittier Blvd, Montebello, CA 90640-3041, USA https://alaccsa.com/contactenos/
ALCON /p. 5
MX
Tel. 5579021866
Email: michelle.betanzos@alcon.com
BAUSCH + LOMB / p. 1
MEX
Tel.: (55) 50-62-40-00 (55) 50-62-48-00 01-800-800-83-03 www.valeant.com.mx/bausch/
DEWIMED S.A. /p. 9
MEX
Tel.: (55) 56 06 07 77
Fax.: (55) 56 06 05 20 ventas@dewimed.com.mx www.dewimed.com.mx
HEIDELBERG ENGINEERING /p. 21
MEX
ARFAMEX
Tel.: +52 55 5135 6646 • 6648
E-mail: sales@arfamex.com
LABORATORIOS SOPHIA / Portada 4 COL
Tel.: +57 (1) 3778555
SOPHILINEA: 01800121293 www.sophia.com.mx
E-mail: contacto@sophia.com.mx
OFTÁLMICA INTERNACIONAL / p. 17
MEX Tijuana B.C (Matriz)
Tel.: (664) 684-8230
Wasap: (664) 279-3004 marcela@oftalmica.com
CDMX (Sucursal)
Tel.: (55) 5584 5594
Wasap: (553) 341 2224 bertha@oftalmica.com
CDMX (Equipos)
Tel.: (55) 5584 5594
Wasap: (553) 341 3140 hugo@oftalmica.com

