3 minute read
Cuantificación e identificación rápida de impurezas del producto (nitrosaminas)
CENEBA BIOPROCESS
La reciente crisis de las impurezas de los productos ha puesto el foco de atención en las impurezas genotóxicas (GTI). Las nitrosaminas, o más correctamente las N-nitrosaminas, se refieren a cualquier molécula que contenga el grupo funcional nitroso. Estas moléculas son preocupantes porque las impurezas de nitrosamina son probables carcinógenos humanos, lo que significa que la exposición a largo plazo por encima de ciertos niveles puede aumentar el riesgo de desarrollo de cáncer. Aunque también están presentes en algunos alimentos y en el suministro de agua potable, su presencia en los medicamentos se considera, sin embargo, inaceptable.
Advertisement

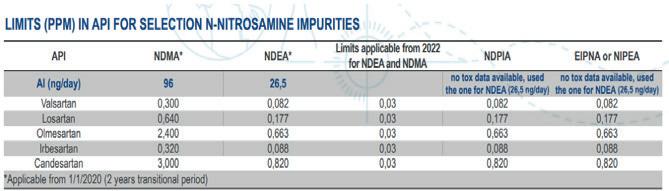
Las agencias reguladoras, entre ellas la FDA de EE.UU. y la Agencia Europea del Medicamento (EMA), han publicado directrices sobre los límites permitidos de impurezas genotóxicas en los productos farmacéuticos. Estos límites sirven para garantizar la seguridad de los productos, no solo para los que se destacan con frecuencia debido a las nitrosaminas, sino para todos los medicamentos y procesos potencialmente contaminados de la cartera de ingredientes farmacéuticos activos (API) de una empresa.
El CHMP y el CMDh ampliaron el plazo de presentación de solicitudes de modificación de medicamentos químicos del 26 de septiembre de 2022 al 1 de octubre de 2023 en julio de 2022.
Apenas pasa un día sin que se mencione un nuevo principio activo farmacéutico (API) nitrosamina, por ejemplo, la nitrosamina propranolol. Esto ha dado lugar a un gran intercambio de datos precompetitivos. Muchas empresas han puesto en marcha una base de datos de nitritos en excipientes para facilitar la evaluación de riesgos de los productos farmacéuticos. La base de datos clasifica los excipientes de la siguiente manera: 1) los excipientes muestran un contenido variable de nitritos con una pronunciada variación entre lotes, 2) el impacto de los nitritos depende de la cantidad de excipiente en un producto, 3) estos excipientes muestran niveles bajos de nitritos y una baja variabilidad, lo que da lugar a un valor medio de 1 μg/g de nitritos, y 4) los distintos proveedores de excipientes muestran diferencias pronunciadas en los niveles de nitritos.

Apenas pasa un día sin que se mencione un nuevo principio activo farmacéutico (API) nitrosamina, por ejemplo, la nitrosamina propranolol. Esto ha dado lugar a un gran intercambio de datos precompetitivos. Muchas empresas han puesto en marcha una base de datos de nitritos en excipientes para facilitar la evaluación de riesgos de los productos farmacéuticos. La base de datos clasifica los excipientes de la siguiente manera 1) los excipientes muestran un contenido variable de nitritos con una pronunciada variación entre lotes, 2) el impacto de los nitritos depende de la cantidad de excipiente en un producto, 3) estos excipientes muestran niveles bajos de nitritos y una baja variabilidad, lo que da lugar a un valor medio de 1 μg/g de nitritos, y 4) los distintos proveedores de excipientes muestran diferencias pronunciadas en los niveles de nitritos.
En CENEBA BIOPROCESS, laboratorio analítico mexicano ubicado en Jalisco, contamos con un método validado para la cuantificación altamente selectiva y sensible de nitrosaminas en productos farmacéuticos, en cumplimiento con los límites de la regulación FDA y EMA, y recientemente establecido por la FEUM 13va Ed. también en México.

Método rápido para la cuantificación de compuestos nitrosamínicos con confirmación al Análisis de nitrosaminas genotóxicas en principios activos farmacéuticos, por HPLC-MS/MS.